 Соли 1
Соли 1
 Классификация солей Средние соли – продукты полного замещения атомов водорода в кислоте химическим элементом металлом (состоят из катионов металла и анионов кислотного остатка) Na 2 SO 4, K 3 PO 4 Кислые соли - продукты неполного замещения атомов водорода в кислоте химическим элементом металлом (в анион кислотного остатка входит водород) Na. HSO 4, K 2 HPO 4 Основные соли - продукты неполного замещения гидроксогрупп в гидроксиде металла кислотными остатками (катион содержит гироксогруппы) 2 Cu. OHCl, Al. OH(NO 3)2
Классификация солей Средние соли – продукты полного замещения атомов водорода в кислоте химическим элементом металлом (состоят из катионов металла и анионов кислотного остатка) Na 2 SO 4, K 3 PO 4 Кислые соли - продукты неполного замещения атомов водорода в кислоте химическим элементом металлом (в анион кислотного остатка входит водород) Na. HSO 4, K 2 HPO 4 Основные соли - продукты неполного замещения гидроксогрупп в гидроксиде металла кислотными остатками (катион содержит гироксогруппы) 2 Cu. OHCl, Al. OH(NO 3)2
 Классификация солей Двойные соли – соли, содержащие два катиона KAl(SO 4)2 Смешанные соли – соли, содержащие два аниона Ca. OCl 2 Комплексные соли – соли, содержащие ион комплексообразователя, связанный с лигандами Na[Al(OH)4] 3
Классификация солей Двойные соли – соли, содержащие два катиона KAl(SO 4)2 Смешанные соли – соли, содержащие два аниона Ca. OCl 2 Комплексные соли – соли, содержащие ион комплексообразователя, связанный с лигандами Na[Al(OH)4] 3
 n 1. 2. 3. 4. К средним солям относится каждое из двух веществ Fe(OH)2 Cl и Fe(HSO 4)2 Mg. Cl 2 и Mg(OH)NO 3 KHCO 3 и Na. HSi. O 3 K 3 PO 4 и Ba. Si. O 3 4
n 1. 2. 3. 4. К средним солям относится каждое из двух веществ Fe(OH)2 Cl и Fe(HSO 4)2 Mg. Cl 2 и Mg(OH)NO 3 KHCO 3 и Na. HSi. O 3 K 3 PO 4 и Ba. Si. O 3 4
 Установите соответствие между формулой соли и её принадлежностью к определённой группе. А) Zn. SO 4 1) кислая Б) Cu 2(OH)2 CO 3 2) средняя В) KAl(SO 4)2 3)основная Г) Na. HSO 4 4) двойная 5)комплексная 5
Установите соответствие между формулой соли и её принадлежностью к определённой группе. А) Zn. SO 4 1) кислая Б) Cu 2(OH)2 CO 3 2) средняя В) KAl(SO 4)2 3)основная Г) Na. HSO 4 4) двойная 5)комплексная 5
 Установите соответствие между (группой) солей, к которому А) Сa(OCl)Cl Б) Na. H 2 PO 4 В) Al(OH)SO 4 Г) Fe(SCN)2 солью и классом она принадлежит. 1) основные 2) кислые 3) средние 4) двойные 5) смешанные 6
Установите соответствие между (группой) солей, к которому А) Сa(OCl)Cl Б) Na. H 2 PO 4 В) Al(OH)SO 4 Г) Fe(SCN)2 солью и классом она принадлежит. 1) основные 2) кислые 3) средние 4) двойные 5) смешанные 6
 Формулы только основных солей указаны в ряду, 1. KHCO 3, Na 2 Cr 2 O 7, (CUOH)2 SO 4 2. Cu. Cl 2, Na. HSO 3, (Al. OH)Cl 2 3. Ca(HCO 3)2, Zn. S, (Fe. OH)Cl 4. (Fe. OH)NO 3, (Cu. OH)2 CO 3, Mg. OHCl 7
Формулы только основных солей указаны в ряду, 1. KHCO 3, Na 2 Cr 2 O 7, (CUOH)2 SO 4 2. Cu. Cl 2, Na. HSO 3, (Al. OH)Cl 2 3. Ca(HCO 3)2, Zn. S, (Fe. OH)Cl 4. (Fe. OH)NO 3, (Cu. OH)2 CO 3, Mg. OHCl 7
 Способы получения средних солей n n Основания + кислота: 3 Na. OH + H 3 PO 4 = Na 3 PO 4 + 3 H 2 O Основный оксид + кислота: Mg. O + H 2 SO 4 = Mg. SO 4 + H 2 O n Кислотный оксид + щелочь: SO 3 + 2 Na. OH = Na 2 SO 4 + H 2 O n Кислотный оксид + основный оксид: SO 3 + Na 2 O = Na 2 SO 4 8
Способы получения средних солей n n Основания + кислота: 3 Na. OH + H 3 PO 4 = Na 3 PO 4 + 3 H 2 O Основный оксид + кислота: Mg. O + H 2 SO 4 = Mg. SO 4 + H 2 O n Кислотный оксид + щелочь: SO 3 + 2 Na. OH = Na 2 SO 4 + H 2 O n Кислотный оксид + основный оксид: SO 3 + Na 2 O = Na 2 SO 4 8
 Способы получения средних солей n n Соль + кислота: Ba. Cl 2 + H 2 SO 4 = Ba. SO 4↓ + 2 HCl Раствор соли + раствор соли: Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4↓ + 2 Na. Cl n Раствор соли + раствор щелочи: Mg. SO 4 + 2 Na. OH = Mg(OH)2 + Na 2 SO 4 9
Способы получения средних солей n n Соль + кислота: Ba. Cl 2 + H 2 SO 4 = Ba. SO 4↓ + 2 HCl Раствор соли + раствор соли: Ba. Cl 2 + Na 2 SO 4 = Ba. SO 4↓ + 2 Na. Cl n Раствор соли + раствор щелочи: Mg. SO 4 + 2 Na. OH = Mg(OH)2 + Na 2 SO 4 9
 Способы получения средних солей n Металл + неметалл: Mg + S = Mg. S n n Металл + раствор соли: Mg + Cu. SO 4 = Mg. SO 4 + Cu Металл + кислота: Mg + H 2 SO 4 = Mg. SO 4 + H 2 10
Способы получения средних солей n Металл + неметалл: Mg + S = Mg. S n n Металл + раствор соли: Mg + Cu. SO 4 = Mg. SO 4 + Cu Металл + кислота: Mg + H 2 SO 4 = Mg. SO 4 + H 2 10
 n 1. 2. 3. 4. Нерастворимая соль образуется при взаимодействии KOH(р-р) и H 3 PO 4(р-р) HCl(р-р) и Mg(NO 3)2(р-р) HNO 3(р-р) и Cu. O Ca(OH)2(р-р) и CO 2 11
n 1. 2. 3. 4. Нерастворимая соль образуется при взаимодействии KOH(р-р) и H 3 PO 4(р-р) HCl(р-р) и Mg(NO 3)2(р-р) HNO 3(р-р) и Cu. O Ca(OH)2(р-р) и CO 2 11
 Разложение средних солей n n n Разложение карбонатов 2 группы главной подгруппы: Ca. CO 3 = Ca. O + CO 2 Разложение нитратов: 2 Na. NO 3 = 2 Na. NO 2 +O 2 2 Cu(NO 3)2 = 2 Cu. O + 4 NO 2 +O 2 2 Ag. NO 3 = 2 Ag + 2 NO 2 + O 2 Разложение других солей: 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 2 KCl. O 3 = 2 KCl + 3 O 2 12
Разложение средних солей n n n Разложение карбонатов 2 группы главной подгруппы: Ca. CO 3 = Ca. O + CO 2 Разложение нитратов: 2 Na. NO 3 = 2 Na. NO 2 +O 2 2 Cu(NO 3)2 = 2 Cu. O + 4 NO 2 +O 2 2 Ag. NO 3 = 2 Ag + 2 NO 2 + O 2 Разложение других солей: 2 KMn. O 4 = K 2 Mn. O 4 + Mn. O 2 + O 2 2 KCl. O 3 = 2 KCl + 3 O 2 12
 Получение кислых солей n n Взаимодействие избытка кислоты с основанием: H 3 PO 4 + Na. OH = Na. H 2 PO 4 + H 2 O Взаимодействие избытка кислотного оксида с основанием: CO 2 + KOH = KHCO 3 13
Получение кислых солей n n Взаимодействие избытка кислоты с основанием: H 3 PO 4 + Na. OH = Na. H 2 PO 4 + H 2 O Взаимодействие избытка кислотного оксида с основанием: CO 2 + KOH = KHCO 3 13
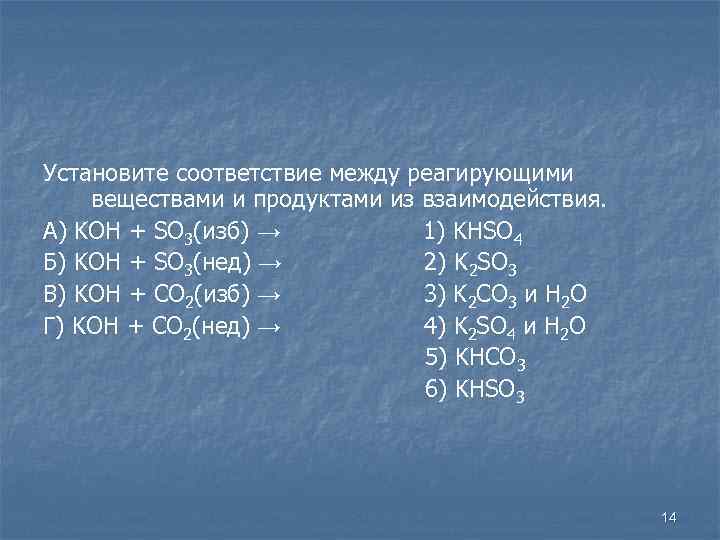 Установите соответствие между реагирующими веществами и продуктами из взаимодействия. А) KOH + SO 3(изб) → 1) KHSO 4 Б) KOH + SO 3(нед) → 2) K 2 SO 3 В) KOH + CO 2(изб) → 3) K 2 CO 3 и H 2 O Г) KOH + CO 2(нед) → 4) K 2 SO 4 и H 2 O 5) KHCO 3 6) KHSO 3 14
Установите соответствие между реагирующими веществами и продуктами из взаимодействия. А) KOH + SO 3(изб) → 1) KHSO 4 Б) KOH + SO 3(нед) → 2) K 2 SO 3 В) KOH + CO 2(изб) → 3) K 2 CO 3 и H 2 O Г) KOH + CO 2(нед) → 4) K 2 SO 4 и H 2 O 5) KHCO 3 6) KHSO 3 14
 Получение основных солей n n Взаимодействие кислоты с избытком основания: Fe(OH)3 + HCl = Fe(OH)2 Cl + H 2 O Взаимодействие избытка соли со щелочью: Cu(NO 3)2 +Na. OH = Cu. OHNO 3 + Na. NO 3 15
Получение основных солей n n Взаимодействие кислоты с избытком основания: Fe(OH)3 + HCl = Fe(OH)2 Cl + H 2 O Взаимодействие избытка соли со щелочью: Cu(NO 3)2 +Na. OH = Cu. OHNO 3 + Na. NO 3 15
 Переход одних солей в другие Средние → кислые: Na 3 PO 4 + 2 H 3 PO 4 = 3 Na. H 2 PO 4 Na 2 CO 3 + CO 2 + H 2 O = 2 Na. HCO 3 Кислые → средние: Na 2 HPO 4 + Na. OH = Na 3 PO 4 + H 2 O 16
Переход одних солей в другие Средние → кислые: Na 3 PO 4 + 2 H 3 PO 4 = 3 Na. H 2 PO 4 Na 2 CO 3 + CO 2 + H 2 O = 2 Na. HCO 3 Кислые → средние: Na 2 HPO 4 + Na. OH = Na 3 PO 4 + H 2 O 16
 Переход одних солей в другие Средние→ основные: Cu. Cl 2 + Na. OH = Cu. OHCl + Na. Cl Основные → средние: Cu. OHCl + HCl = Cu. Cl 2 + H 2 O 17
Переход одних солей в другие Средние→ основные: Cu. Cl 2 + Na. OH = Cu. OHCl + Na. Cl Основные → средние: Cu. OHCl + HCl = Cu. Cl 2 + H 2 O 17


