061bf07ebd8355bb0f846f7f298a411d.ppt
- Количество слайдов: 17

Соглашение о предоставлении субсидии 14. 576. 21. 0077 от 06 ноября 2014 г. Тема проекта: Клонирование, выделение и изучение свойств новых бактериальных ДНК-метилтрансфераз M. Ags. I, M. Alu. BI и M. Fat. I, узнающих и уникально модифицирующих последовательности ДНК TTSAA, AGCT и CATG, соответственно Получатель субсидии: Общество с ограниченной ответственностью «Сиб. Энзайм» , Новосибирск. Индустриальный партнер: не предусмотрен проектом. Объем средств субсидии 3 500 000 (Три миллиона пятьсот тысяч) рублей, в том числе: - в 2014 году 3 500 000 (Три миллиона пятьсот тысяч) рублей; – в 2015 году 0 (Ноль) рублей. Объем внебюджетных средств 5 300 000 (Пять миллионов триста тысяч) рублей, в том числе: - в 2014 году в размере 1 250 000 (Один миллион двести пятьдесят тысяч) рублей, - в 2015 году в размере 4 050 000 (Четыре миллиона пятьдесят тысяч) рублей. Докладчик: к. б. н. , Дедков Владимир Сергеевич, научный руководитель работ.

l l Цель проекта – расширение ферментной базы для биологии и медицины: Целью первого этапа является создание методами биоинженерии трех штаммов-суперпродуцентов новых бактериальных ДНК-метилтрансфераз, изучение их технологических характеристик и получение препаратов ферментов M. Ags. I, M. Alu. BI и M. Fat. I, не имеющих аналогов, и востребованных для создания метилированных ДНК-субстратов в молекулярно-биологических исследованиях и современных технологиях эпигенетики. На втором этапе предполагается исследование полученных генетических конструкций рекомбинантных штаммов и определение специфичности метилирования рекомбинантных ДНК –метилтрансфераз.
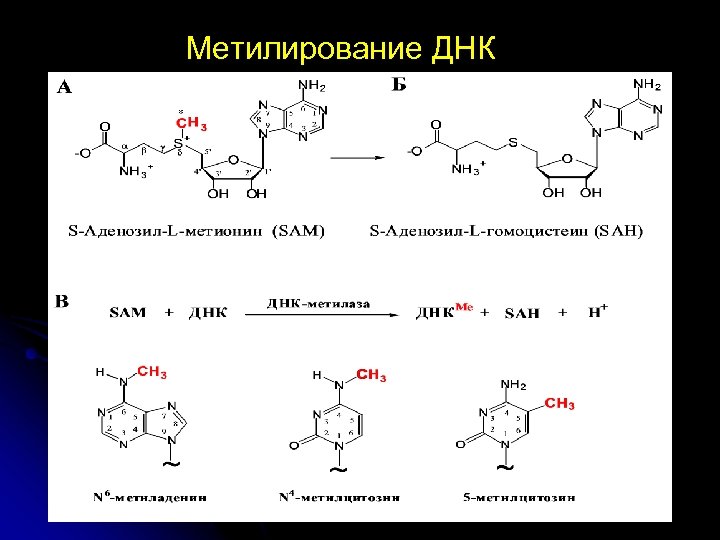
Метилирование ДНК

Процессы, связанные с метилированием ДНК l l l у животных: у бактерий: экспрессия генов, репликация, эмбриональное развитие, репарация, дифференцировка клеток, рекомбинация, защита от вирусов, защита от чужеродной канцерогенез, ДНК старение Для изучения метилирования ДНК используют эндонуклеаз рестрикции специфичность которых в отношении метилирования ДНК хорошо изучена. К ним относятся Hpa. II и Msp. I, узнающие CCGG. Hpa. II не расщепляет метилированную последовательность Cm 5 CGG, а Msp. I – расщепляет. Этот подход использован в ранней диагностике рака молочной железы и яичников [Логинов В. И. , Казубская Т. П. , Ходырев Д. С. , Пронина И. В. , Ермилова В. Д. , Паяниди Ю. Г. , Сельчук В. Ю. , Кашурников А. Ю. , Огай Д. С. , Брага Э. А. Роль метилирования генов–супрессоров в ранней диагностике первично– множественного и солитарного рака молочной железы и яичников. // Русский Медицинский Журнал. – 2012. – № 1 прил. – С. 20– 25. ]. Данный пример показывает связь между исследованиями метилирования ДНК бактерий и животных.

НАУЧНАЯ НОВИЗНА РАБОТЫ l ДНК-метилтрансфераза M. Ags. I бактерии Agrococcus species 25 будет прототипом, узнающим TTSAA, также как эндонуклеаза–прототип Ags. I. l M. Alu. BI Arthrobacter luteus B метилирует ДНК иначе, чем AGm 5 CT, поскольку Alu. BI расщепляет ДНК, метилированную таки образом M. Alu. I. l M. Fat. I Flavobacterium aquatile NL 3 метилирует ДНК иначе, чем Cm 6 ATG, поскольку Fat. I расщепляет ДНК, метилированную таки образом M. Nla. III.

ПЛАНИРУЕМЫЕ РЕЗУЛЬТАТЫ ПРОЕКТА Рекомбинантные плазмиды, содержащие гены ДНКметилтрансфераз Ags. I, Alu. BI и Fat. I – для хранения генов ДНК-метилтрансфераз Ags. I, Alu. BI и Fat. I в форме препаратов ДНК; – для проведения трансформации хотя бы одного из коммерчески доступных штаммов E. сoli с целью получения штамма-суперпродуцента соответствующего фермента. l Рекомбинантные штаммы Escherichia coli для высокоэффективной наработки новых ДНКметилтрансфераз М. Ags. I, М. Alu. BI и М. Fat. I. l Препараты ДНК-метилтрансфераз М. Ags. I, М. Alu. BI и М. Fat. I из рекомбинантных продуцентов E. сoli пригодные для исследовательских работ в биологии и медицине: - для ДНК при изучении эпигенома (метилома); - для изучения чувствительности к метилированию эндонуклеаз рестрикции, а также для других задач. l

КЛОНИРОВАНИЕ ГЕНОВ ДНК–МЕТИЛТРАНСФЕРАЗ Геномные библиотеки ДНК диких продуцентов в E. coli RRI получены в составе плазмиды p. UC 19. l Рекомбинантные продуценты ДНК– метилтрансфераз получены из библиотек ДНК, устойчивых к сопряжённым эндонуклеазам рестрикции: – E. coli N 106 (p. M. Ags. I) – продуцент M. Ags. I; – E. coli N 16 (p. M. Alu. BI) – продуцент M. Alu. BI; – E. coli N 3 (p. M. Fat. I) – продуцент M. Fat. I. l
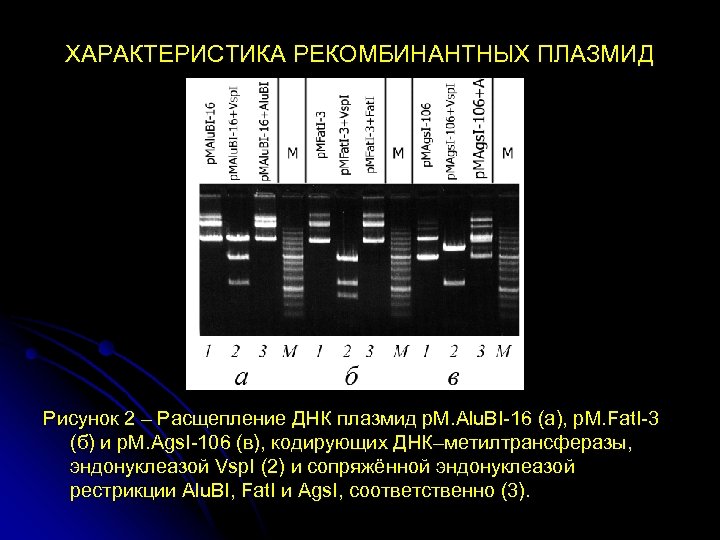
ХАРАКТЕРИСТИКА РЕКОМБИНАНТНЫХ ПЛАЗМИД Рисунок 2 – Расщепление ДНК плазмид p. M. Alu. BI-16 (а), p. M. Fat. I-3 (б) и p. M. Ags. I-106 (в), кодирующих ДНК–метилтрансферазы, эндонуклеазой Vsp. I (2) и сопряжённой эндонуклеазой рестрикции Alu. BI, Fat. I и Ags. I, соответственно (3).
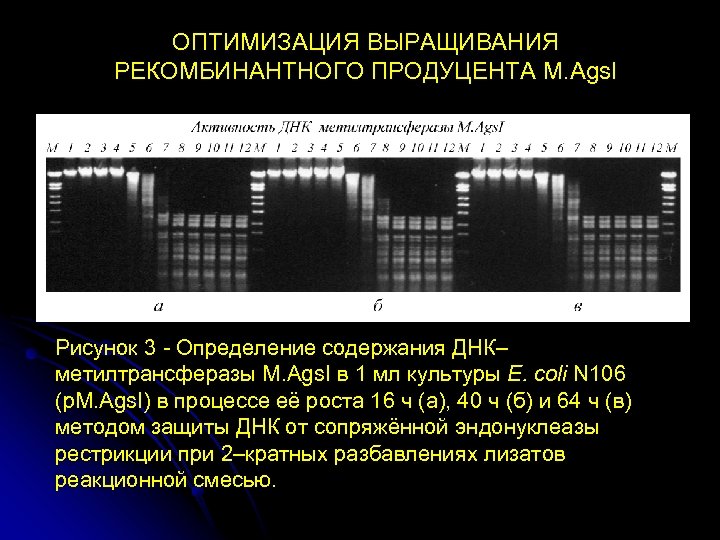
ОПТИМИЗАЦИЯ ВЫРАЩИВАНИЯ РЕКОМБИНАНТНОГО ПРОДУЦЕНТА M. Ags. I Рисунок 3 - Определение содержания ДНК– метилтрансферазы М. Ags. I в 1 мл культуры E. coli N 106 (p. M. Ags. I) в процессе её роста 16 ч (а), 40 ч (б) и 64 ч (в) методом защиты ДНК от сопряжённой эндонуклеазы рестрикции при 2–кратных разбавлениях лизатов реакционной смесью.

ОПТИМИЗАЦИЯ ВЫРАЩИВАНИЯ РЕКОМБИНАНТНОГО ПРОДУЦЕНТА M. Alu. BI l Рисунок 4 - Определение содержания ДНК– метилтрансферазы М. Alu. BI в 1 мл культуры E. coli N 16 (p. M. Alu. BI) в процессе её роста 16 ч (а), 40 ч (б) и 64 ч (в) методом защиты ДНК от сопряжённой эндонуклеазы рестрикции при 2–кратных разбавлениях лизатов реакционной смесью.

ОПТИМИЗАЦИЯ ВЫРАЩИВАНИЯ РЕКОМБИНАНТНОГО ПРОДУЦЕНТА M. Fat. I Рисунок 5 - Определение содержания ДНК– метилтрансферазы М. Fat. I в 1 мл культуры E. coli N 3 (p. M. Fat. I) в процессе её роста 16 ч (а), 40 ч (б) и 64 ч (в) методом защиты ДНК от сопряжённой эндонуклеазы рестрикции при 2–кратных разбавлениях лизатов реакционной смесью.

РЕЗУЛЬТАТЫ НАРАБОТКИ РЕКОМБИНАНТНЫХ БИОМАСС В ФЕРМЕНТЁРЕ l l l 124 г биомассы E. coli N 106 (p. M. Ags. I), содержащей 130 тысяч единиц активности ДНКметилтрансферазы M. Ags. I на 1 г клеток; 122 г E. coli N 16 (p. M. Alu. BI), содержащей M. Alu. BI 250 тысяч ед/г; 127 г E. coli N 3 (p. M. Fat. I), содержащей M. Fat. I 30 тысяч ед/г.

ВЫДЕЛЕНИЕ ПРЕПАРАТОВ ДНК-МЕТИЛТРАНСФЕРАЗ М. Ags. I, М. Alu. BI И М. Fat. I ИЗ БИОМАСС РЕКОМБИНАНТНЫХ ШТАММОВ l l l Стадии выделения I Получение экстракта путём разрушения 100 г клеток ультразвуком. II Хроматография на фосфоцеллюлозе Р 11. III Хроматография на гепарин–сефарозе. IV Гель-фильтрация на Сефакриле S-200. V Хроматография на гидроксилапатите. VI Концентрирование диализом против 50% глицерина.
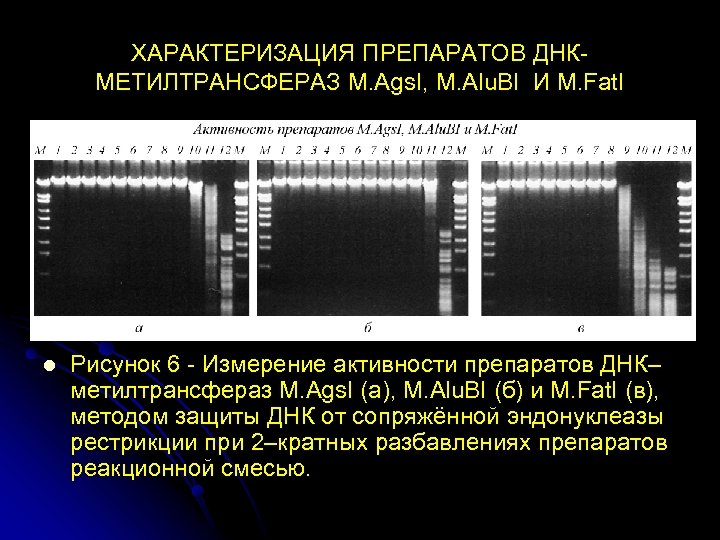
ХАРАКТЕРИЗАЦИЯ ПРЕПАРАТОВ ДНКМЕТИЛТРАНСФЕРАЗ М. Ags. I, М. Alu. BI И М. Fat. I l Рисунок 6 - Измерение активности препаратов ДНК– метилтрансфераз M. Ags. I (а), М. Alu. BI (б) и M. Fat. I (в), методом защиты ДНК от сопряжённой эндонуклеазы рестрикции при 2–кратных разбавлениях препаратов реакционной смесью.

Рисунок 7 – Определение наличия примесных фосфатаз и нуклеаз в препаратах ферментов ДНКметилтрансфераз Ags. I, Alu. BI и Fat. I на Р 32 -меченых одноцепочечном олигонуклеотиде (1) и двухцепоченом олигонуклеотидном дуплексе (2). Авторадиография электрофореграммы в 20% ПААГ с 7 М мочевиной.

ВЫВОДЫ 1. Получены рекомбинантные штаммы–продуценты ДНК–метилтрансфераз: – E. coli N 106 (p. M. Ags. I) – продуцент ДНКметилтрансферазы M. Ags. I, дающий 130 тысяч единиц активности M. Ags. I на 1 г клеток; – E. coli N 16 (p. M. Alu. BI) – продуцент ДНКметилтрансферазы M. Alu. BI, дающий M. Alu. BI 250 тысяч ед/г; – E. coli N 3 (p. M. Fat. I) – продуцент ДНКметилтрансферазы M. Fat. I, дающий M. Fat. I 30 тысяч ед/г. l

2. Разработана методика, по которой из 100 г клеток рекомбинантных штаммов получены препараты ДНК– метилтрансфераз: – М. Ags. I в 22 мл содержит 1, 1 млн ед. активности фермента при концентрации 50 тыс. ед/мл; – М. Alu. BI в 23 мл содержит 2, 3 млн ед. активности фермента при концентрации 100 тыс. ед/мл; – М. Fat. I в 22 мл содержит 0, 2 млн ед. активности фермента при концентрации 10 тыс. ед/мл. l 3. Полученные препараты ДНК–метилтрансфераз М. Ags. I, М. Alu. BI и М. Fat. I вполне пригодны для изучения специфичности этих ферментов. l
061bf07ebd8355bb0f846f7f298a411d.ppt