Соединительная ткань.pptx
- Количество слайдов: 42

Соединительная ткань Клетки: фибробласты, фиброкласты, макрофаги, меланоциты, тучные клетки, эндотелиоциты, мезенхимные клетки Внеклеточный матрикс (межклеточное вещество) 4 вида соединительной ткани: • волокнистая (связки) • твёрдая (кость) • жидкая (кровь, лимфа) • гелеобразная (стекловидное тело глаза, хрящ).

Соединительная ткань — это внеклеточный матрикс вместе с клетками различного типа (фибробласты, хондробласты, остеобласты, тучные клетки, макрофаги) и волокнистыми структурами. Межклеточный матрикс (ВКМ — внеклеточный матрикс) представлен белками — коллагеном и эластином, гликопротеидами и протеогликанами, гликозаминогликанами (ГАГ), а также неколлагеновыми структурными белками — фибронектином, ламинином и др. Соединительная ткань подразделяется на: • собственно соединительную ткань, • скелетную ткани — костную и хрящевую, • соединительную ткань со специфическими свойствами • жировую, слизистую, пигментную, ретикулярную.
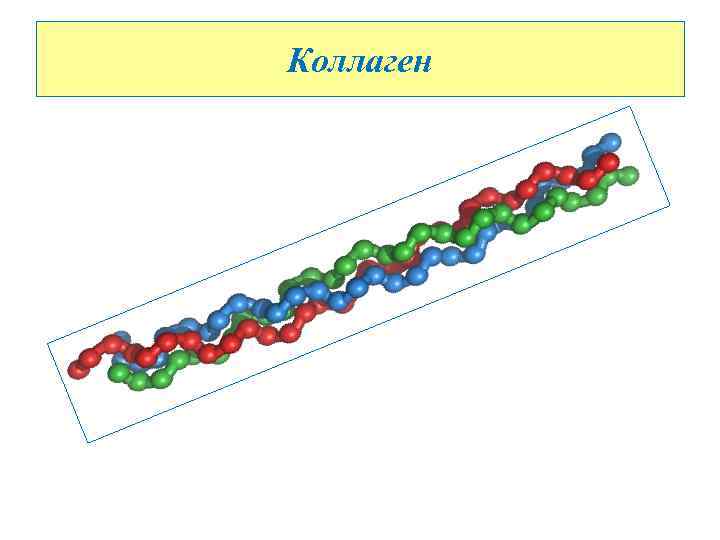
Коллаген

Молекула коллагена представляет собой правозакрученную спираль из трёх α-цепей. Такое образование известно под названием тропоколлаген. Один виток спирали α-цепи содержит три аминокислотных остатка. Молекулярная масса коллагена около 300 к. Да, длина 300 нм, толщина 1, 5 нм. Для первичной структуры белка характерно высокое содержание глицина, низкое содержание серосодержащих аминокислот и отсутствие триптофана. Коллаген относится к тем немногим белкам животного происхождения, которые содержат остатки нестандартных аминокислот: около 21 % от общего числа остатков приходится на 3 -гидроксипролин, 4 -гидроксипролин и 5 -гидроксилизин. Каждая из α-цепей состоит из триад аминокислот. В триадах третья аминокислота всегда глицин, вторая — пролин или лизин, первая — любая другая аминокислота, кроме трёх перечисленных.

Коллаген

Коллаген

Разновидности коллагена Типы Фибриллярные коллагены I, III, V, XI, XXIV, XXVII Фибрилл-ассоциированные коллагены (FACIT) IX, XII, XIV, XVI, XIX, XXI, XXII Коллагены, формирующие филаменты- бусины (beaded filament forming) VI Сетеобразующие коллагены IV, VIII, X Коллаген, формирующий якорные фибриллы VII Трансмембранные коллагены XIII, XVII, XXIII, XXV/CLAC-P Другие коллагены XXVIII, XVIII

Эластин состоит из глицина, валина, аланина и пролина. Эластин является специализированным белком с молекулярной массой от 64 до 66 к. Да. Эластин синтезируется клетками фибробластов через предшественник — растворимый тропоэластин, не содержащий поперечных связей. Из множества тропоэластина эластин получается в реакции, катализируемой лизилоксидазой. В эластине также присутствуют десмозин и изодесмозин, из-за чего эластин может растягиваться в двух направлениях.
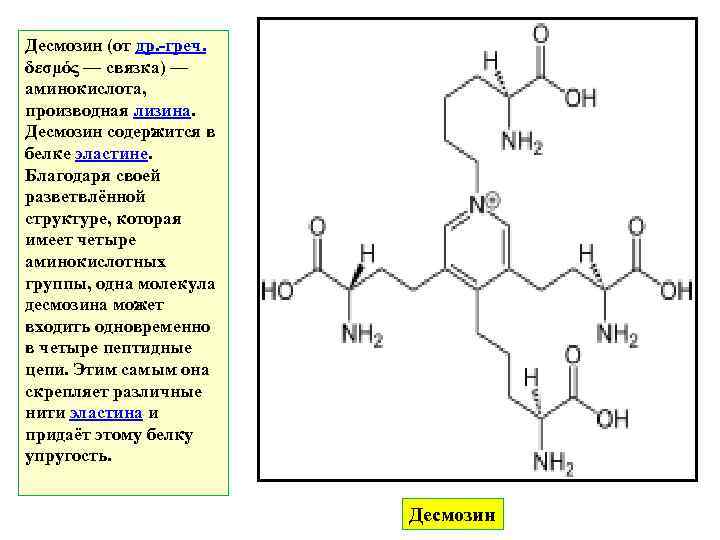
Десмозин (от др. -греч. δεσμός — связка) — аминокислота, производная лизина. Десмозин содержится в белке эластине. Благодаря своей разветвлённой структуре, которая имеет четыре аминокислотных группы, одна молекула десмозина может входить одновременно в четыре пептидные цепи. Этим самым она скрепляет различные нити эластина и придаёт этому белку упругость. Десмозин

Изодесмозин — аминокислота, изомер десмозина, отличающаяся от него лишь расположением боковых цепей на пиридиновом кольце. Вместе с десмозином скрепляет нити эластина.

Протеогликаны — сложные белки. Высокомолекулярные соединения, состоящие из белка (на белковую часть приходится 5 -10% от общей массы) с высокой степенью гликозилирования (на углеводную часть приходится 90 -95% от общей массы), углеводные остатки которых представляют собой длинные неразветвленные полисахаридные цепи — гликозаминогликаны, образованные чередующимися остатками гексозамина и уроновой кислоты (глюкуроновой, идуроновой или галактуроновой) либо галактозы. Гликозаминогликановые цепи часто сульфированы. Протеогликаны являются подклассом большого класса сложных белков, которые называются гликопротеинами. Гликопротеины тоже содержат полисахаридные цепи разной длины, ковалентно присоединённые к полипептидной основе, но углеводный компонент гликопротеинов гораздо меньше по массе, чем у протеогликанов, и составляет не более 40% от общей массы.
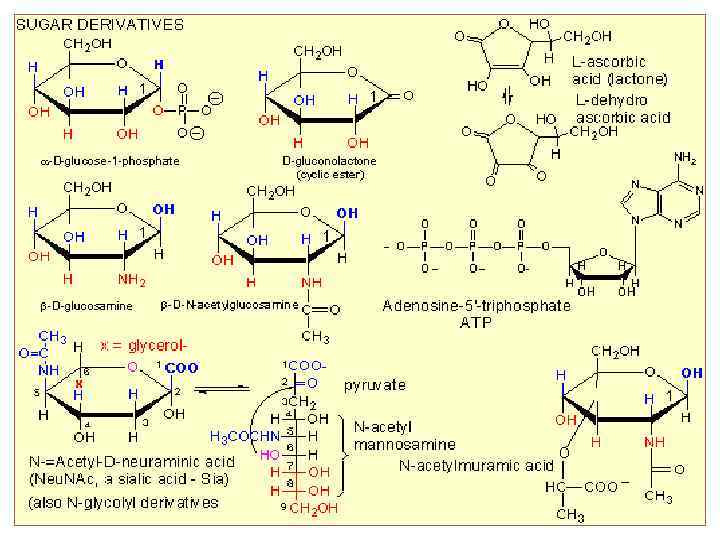


Протеогликаны являются одним из основных компонентов внеклеточного матрикса соединительной ткани. Протеогликаны состоят из сердцевинных белков (лат. core protein) с молекулярной массой от 10 до 600 к. Да, с которыми ковалентно связаны несколько гликозаминогликановых цепей (до 80 гликозидных звеньев массой до 50 — 60 к. Да). Число связанных с белком полисахаридных цепей варьирует от одной (декорин фибробластов) до 100 и выше (аггрекан хрящевой ткани). Такое строение обуславливает высокую молекулярную массу протеогликанов (у аггрекана до 5 МДа). Сердцевинные белки протеогликанов, как и другие белки, синтезируются рибосомами шероховатого эндоплазматического ретикулума и транспортируются в аппарат Гольджи, где происходит их гликозилирование. На первой стадии происходит «наращивание» на сериновом остатке сердцевинного белка «связующего тетрасахарида» (англ. proteoglycan linkage tetrasaccharide) «ксилоза-галактоза-глюкуроновая кислота» (ß 1 -4 Xyl ß 1 -3 Gal Glc. A), после чего соответствующими гликозилтрансферазами осуществяется наращивание специфичной для данного протеогликана гликозиламиногликановой цепи.
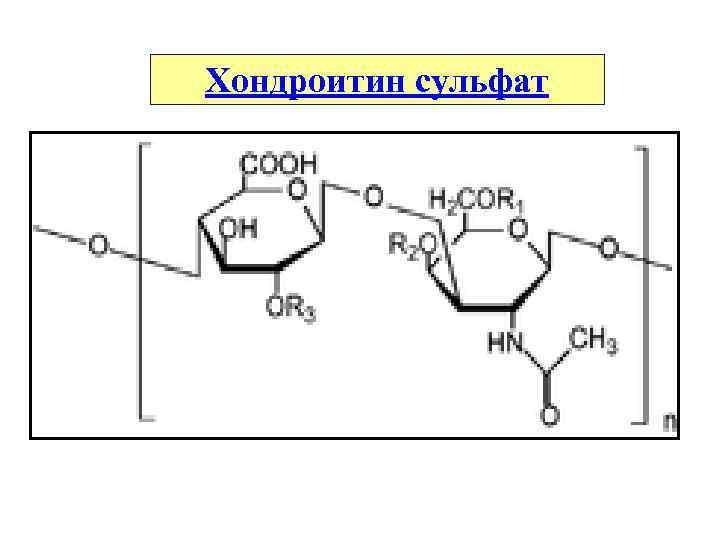
Хондроитин сульфат

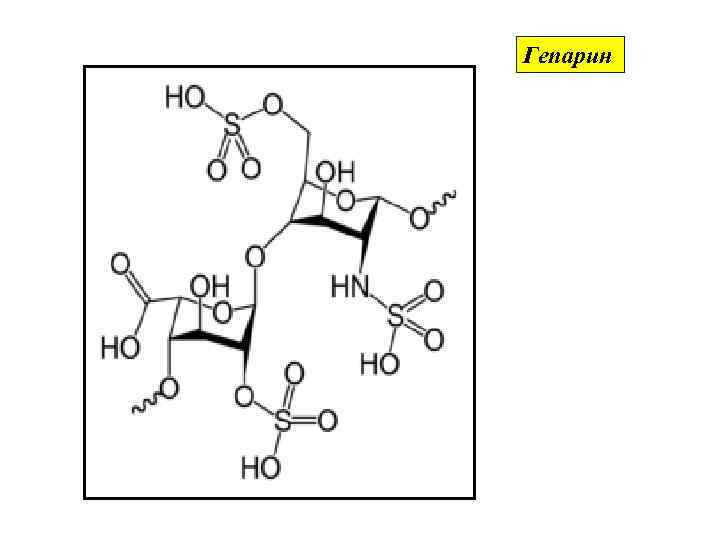
Гепарин
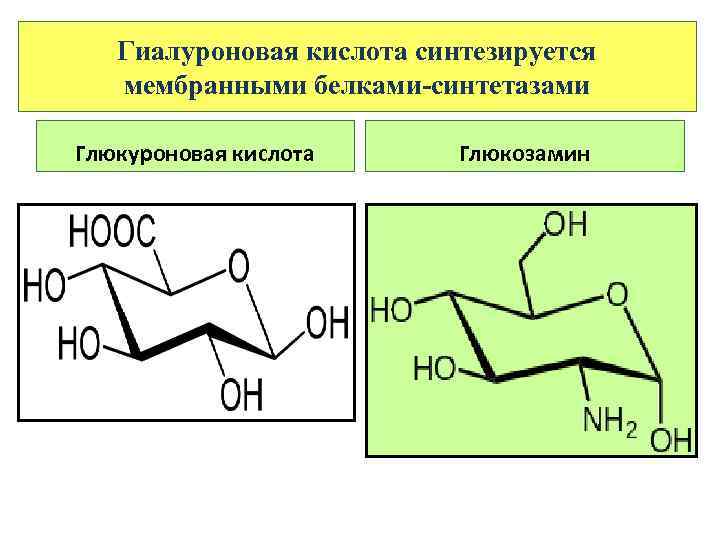
Гиалуроновая кислота синтезируется мембранными белками-синтетазами Глюкуроновая кислота Глюкозамин
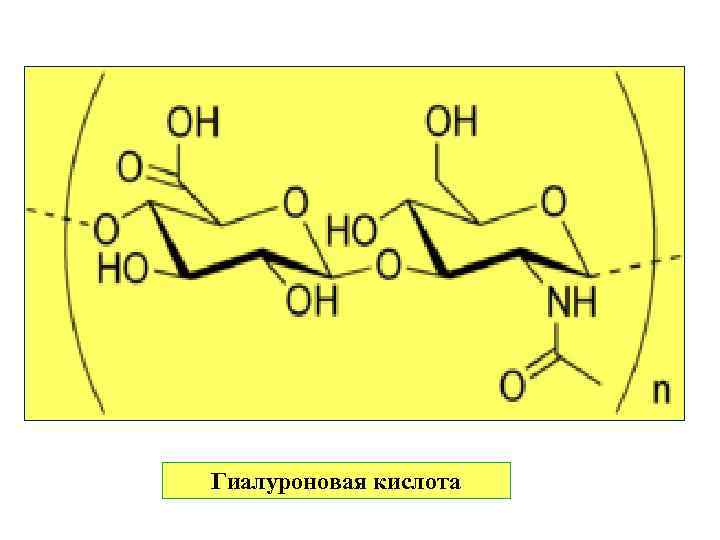
Гиалуроновая кислота

Синдром Марфана (Болезнь Марфана, Marfan syndrome) — аутосомно-доминантное заболевание из группы наследственных патологий соединительной ткани. Синдром вызван мутациями генов, кодирующих синтез гликопротеина фибриллина-1, и является плейотропным. Заболевание характеризуется различной пенетрантностью и экспрессивностью. В классических случаях лица с синдромом Марфана высоки (долихостеномелия), имеют удлиненные конечности, вытянутые пальцы (арахнодактилия) и недоразвитие жировой клетчатки. Помимо характерных изменений в органах опорно-двигательного аппарата (удлинённые трубчатые кости скелета, гипермобильность суставов), наблюдается патология в органах зрения и сердечно-сосудистой системы, что в классических вариантах составляет триаду Марфана.

Нарушения синтеза коллагена в организме лежат в основе таких наследственных заболеваний, как латиризм (характерна разболтанность суставов, привычные вывихи), синдром Элерса-Данлоса (14 типов проявлений), несовершенный остеогенез (osteogenesis imperfecta, болезнь «стеклянного человека» , врожденный рахит, врожденная ломкость костей), болезнь Марфана. Характерным проявлением этих заболеваний является повреждение связочного аппарата, хрящей, костной системы, наличие пороков сердечных клапанов. Болезни, вызванные дефектами при биосинтезе коллагена, в том числе так называемые коллагенозы, возникают из-за множества причин: Ø мутации в гене, кодирующем аминокислотную последовательность ферментов, продуцирующих коллаген, приводящей к изменению формы молекулы коллагена, или ошибки в посттрансляционной модификации коллагена; Ø пониженная активность ферментов, участвующих в биосинтезе коллагена — дефицит ферментов гидроксилирования (пролин-, лизингидроксилазы), гликозилтрансфераз, N-проколлагеновой и Спроколлагеновой пептидаз, лизилоксидаз с последующим нарушением поперечных сшивок, дефицит меди, витаминов В 6, C.

Синдром Э лерса — Данло са (синдром Э лерса — Данло , син. Ehlers-Danlos Syndrome, «гиперэластичность кожи» ( «Cutis hyperelastica» ), несовершенный десмогенез) — это группа наследственных системных заболеваний соединительной ткани, вызванных дефектом в синтезе коллагена. В зависимости от отдельной мутации, серьёзность синдрома может измениться от умеренного до опасного для жизни. Симптомы сильно варьируются в зависимости от типа болезни. Тем не менее, в каждом случае они вызваны повреждением или недостатком коллагена типа III. Болезнь как правило поражает суставы, кожу и кровеносные сосуды, с симптомами такими как свободные (плохо прикреплённые), сильно гнущиеся суставы; гладкая или эластичная, легко повреждающаяся кожа; неправильное заживление ран и формирование шрамов; маленькие и хрупкие кровеносные сосуды.

§Несоверше нный остеогене з (лат. osteogenesis imperfecta; иначе «несовершенное костеобразование» , болезнь «хрустального человека» ) — группа генетических нарушений. § Одно из заболеваний характеризующееся повышенной ломкостью костей. § Люди либо имеют недостаточное количество коллагена, либо его качество не соответствует норме. § Так коллаген — важный белок в структуре кости, это заболевание влечёт за собой слабые или ломкие кости. § Будучи генетическим нарушением, является аутосомно-доминантным дефектом. § Чаще передаётся по наследству от родителей, однако, возможна и индивидуальная спонтанная мутация.

ØПрактически любая генная мутация, ведет к утрате или изменению функций коллагена, что, в свою очередь, отражается на свойствах тканей и органов. Ø Генные мутации в коллагеновом домене могут привести к изменению формы тройной спирали, путём вставки/выпадения аминокислоты из полипептидной цепочки или замены Gly на другое основание. Ø Мутации в неколлагеновых доменах могут привести к неправильной пространственной сборке α-цепей в надмолекулярные структуры (фибриллы или сети), что также ведет к утрате функций. Ø Мутантные α-цепи способны образовывать трёхспиральный комплекс с нормальными α-цепями. В большинстве случаев, такие комплексы нестабильны и быстро разрушаются, однако, такая молекула может и нормально выполнять свою роль, если не затронуты функционально важные области. Ø Большинство болезней, вызванных мутациями в «коллагеновых» генах, являются доминантными.

Костная ткань В состав костей входят как органические, так и неорганические вещества; количество первых тем больше, чем моложе организм; в связи с этим кости молодых людей отличаются гибкостью и мягкостью, а кости взрослых — твёрдостью. У взрослого человека количество минеральных составных частей (гидроксиапатита) составляет около 60— 70 % веса кости, а органическое вещество (главным образом коллаген тип I) — 30— 40 %. По микроскопическому строению костное вещество представляет особый вид соединительной ткани, костную ткань, характерные признаки которой: твёрдое, пропитанное минеральными солями волокнистое межклеточное вещество и звездчатые, снабжённые многочисленными отростками, клетки.

Основу кости составляют коллагеновые волокна, окруженные кристаллами гидроксиапатита, которые слагаются в пластинки. Пластинки в костном веществе располагаются концентрическими слоями вокруг длинных разветвляющихся каналов (Гаверсовы каналы) или лежат между этими системами, частью обхватывают целые группы их или тянутся вдоль поверхности кости. Гаверсов канал в сочетании с окружающими его концентрическими костными пластинками считается структурной единицей компактного вещества кости — остеоном.
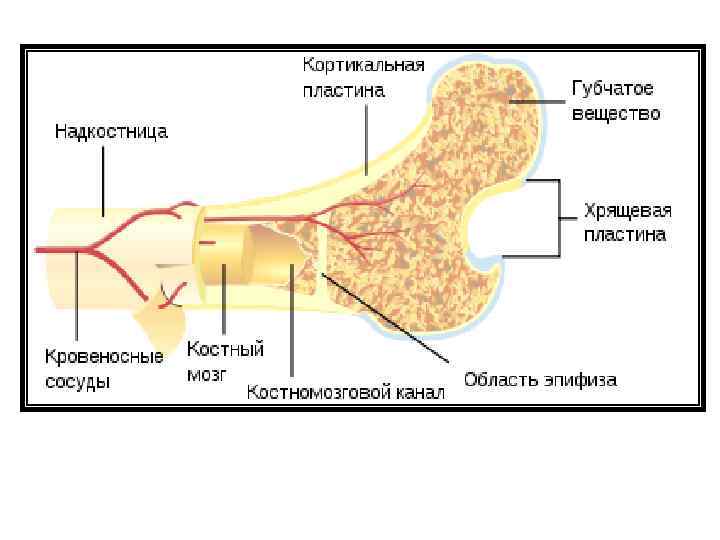
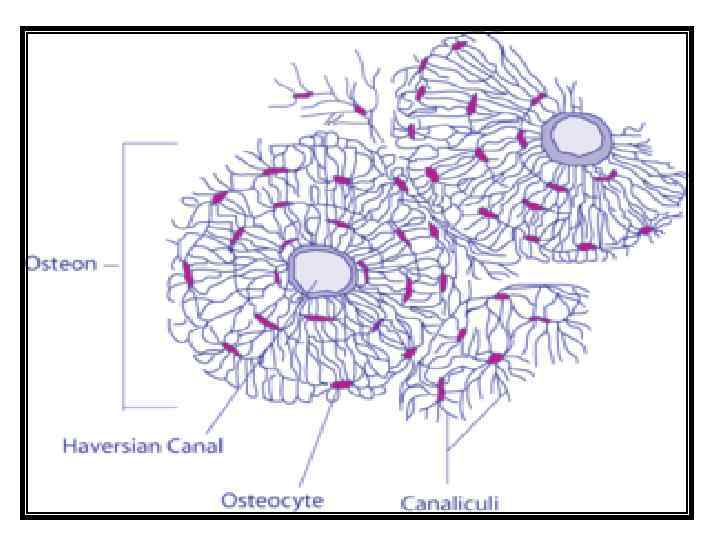

Остеобласты — молодые остеобразующие клетки костей (диаметр 15 -20 мкм), которые синтезируют межклеточное вещество — матрикс По мере накопления межклеточного вещества остеобласты замуровываются в нём и становятся остеоцитами. Родоначальником являются адвентициальные клетки. Остеоциты — клетки костной ткани позвоночных животных и человека, значительно или полностью утратившие способность синтезировать органический компонент матрикса. Они имеют отростчатую форму, округлое плотное ядро и слабобазофильную цитоплазму. утратили способность к делению. Они располагаются в костных полостях, или лакунах, повторяющих контуры остеоцита, и имеют длину 22 -25 мкм, а ширину 6 -14 мкм. Остеокласты Клетки гематогенного происхождения, образующиеся из моноцитов. Может содержать от 2 до 50 ядер. Организация остеокласта адаптирована к разрушению кости. В сочетании с остеобластами, остеокласты контролируют количество костной ткани (остеобласты создают новую костную ткань, а остеокласты разрушают старую.

Гидроксилапатит (гидроксиапатит), (англ. hydroxyapatite, hydroxylapatite, HA ) — минерал Ca 10(PO 4)6(OH)2 из группы апатита, гидроксильный аналог фторапатита и хлорапатита. Является основной минеральной составляющей костей (около 50 % от общего веса кости) и зубов (96 % в эмали). В состав костей входит 99% всего кальция (Ca) организма, 87% фосфора (P), ~ 60% магния (Mg) -25% натрия (Na). Кальций в костях находится в форме минерала гидроксиапатита. Гидроксиапатит образует кристаллы, имеющие обычно размер 20 × 5 × 1, 5 нм. В костной ткани содержится много микроэлементов, таких как медь, стронций, барий, цинк, фтор и др. , которые играют важную роль в обмене веществ в организме. Минеральная часть костей включает также карбонаты, гидроксиды и цитраты.

v Органические вещества костного матрикса представлены: белками, липидами и протеогликанами (небольшое количество). v Основной белок костной ткани - коллаген I типа (90 - 95%). v Кроме него, в матриксе костей присутствуют такие белки, как коллаген V типа, остеонектин, остеокальцин, так называемые морфогенетические белки кости (BMP) и v ферменты - щелочная фосфатаза (в остеобластах) и кислая фосфатаза (в остеокластах). Оба эти фермента служат маркёрами соответствующих клеток костной ткани. Углеводная часть протеогликанов костного матрикса представлена дерматан- и кератансульфатами.

Минерализация кости В минерализации кости важную роль играют все основные компоненты костной ткани, костеобразующие клетки (остеобласты) и клетки, разрушающие костную ткань (остеокласты). Определяющий фактор минерализации - взаимное расположение молекул тропоколлагена со смещением на 1/4 длины молекулы. Промежутки между молекулами тропоколлагена являются центрами минерализации кости, в которых начинается отложение фосфата кальция сначала в аморфном виде с последующим образованием кристаллов гидроксиапатита. Остеобласты контролируют минерализацию посредством регуляции транспорта ионов кальция и фосфата через свои мембраны. Присутствующая в них щелочная фосфатаза высвобождает неорганический фосфат из органических фосфорсодержащих соединений. Освобождающаяся фосфорная кислота реагирует с солями кальция с образованием Са 3(РО 4)2. Гликопротеин остеонектин имеет высокое сродство к коллагену I типа и к гидроксиапатиту. Он содержит Са 2+-связываюшие домены и способствует осаждению Са 2+ и РО 43 - в присутствии коллагена. Определённую роль в процессе минерализации играют также кислые фосфопротеины, специфичные для костной ткани. Они содержат последовательности поли-Асп и поли-Глу, к которым присоединяется кальций, и это может быть пусковым моментом в процессе минерализации.

Регуляция метаболизма костной ткани Формирование матрикса кости регулируется биомеханическими, гормональными и другими факторами. Остеобласты, которые являются клетками-мишенями для паратгормона, реагируют на повышение содержания этого гормона в крови снижением синтеза коллагена, а также повышением активности коллагеназ. Кальцитриол, как и паратгормон, вызывает резорбцию кости опосредованно через остеобласты, так как остеокласты не имеют к нему рецепторов. Повидимому, стимуляция остеокластов происходит при их контактном взаимодействии с остеобластами или в результате синтеза остеобластами активирующего остеокласты фактора. Простагландины (А, В, E 1, Е 2 и F) и некоторые цитокины (эпидермальный фактор роста, фактор некроза опухолей, ИЛ-1) стимулируют резобцию кости и перестройку костной ткани, воздействуя на остеобласты, которые выделяют фактор, активирующий остеокласты. Глюкокортикоиды тормозят пролиферацию остеобластов, подавляя в них синтез ДНК, РНК и белков.

Gla-белки Витамин K участвует в карбоксилировании остатков глутаминовой кислоты в полипептидных цепях некоторых белков. В результате такого ферментативного процесса происходит превращение остатков глутаминовой кислоты в остатки гамма-карбоксилглутаминовой кислоты (сокращенно Gla-радикалы). Остатки гамма-карбоксилглутаминовой кислоты (Gla-радикалы), благодаря двум свободным карбоксильным группам, участвуют в связывании кальция. Gla-радикалы играют важную роль в биологической активности всех известных Gla-белков. В настоящее время в организме человека обнаружены 14 Gla-белков, играющих ключевые роли в регулировании следующих физиологических процессов: § свёртывание крови (протромбин (фактор II), факторы VII, IX, X, белок C, белок S и белок Z). § метаболизм костей (остеокальцин, также названный Gla-белком кости, и матрицей gla белка (MGP)). § сосудистая биология.
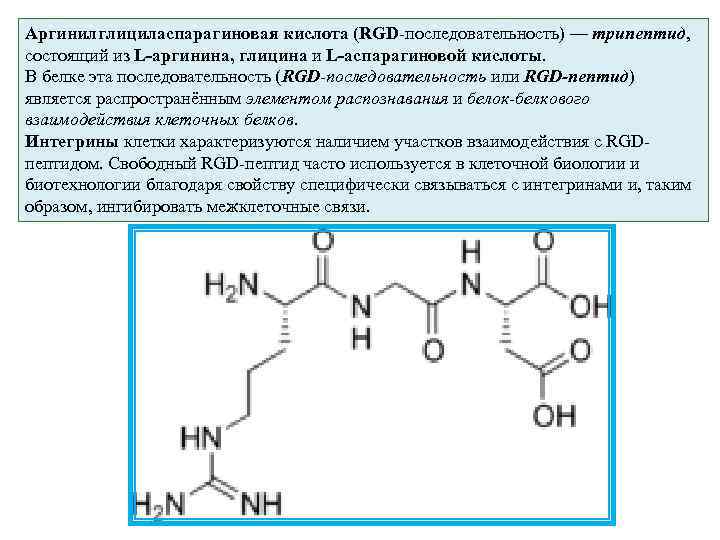
Аргинилглициласпарагиновая кислота (RGD-последовательность) — трипептид, состоящий из L-аргинина, глицина и L-аспарагиновой кислоты. В белке эта последовательность (RGD-последовательность или RGD-пептид) является распространённым элементом распознавания и белок-белкового взаимодействия клеточных белков. Интегрины клетки характеризуются наличием участков взаимодействия с RGDпептидом. Свободный RGD-пептид часто используется в клеточной биологии и биотехнологии благодаря свойству специфически связываться с интегринами и, таким образом, ингибировать межклеточные связи.

Остеокальцин — это наиболее информативный маркер формирования кости. Он высвобождается остеобластами в процессе остеосинтеза и частично поступает в кровоток. Для определения его уровня используют сыворотку или плазму крови, взятой натощак. Получена хорошая корреляция между уровнем остеокальцина в крови и данными инвазивных методов оценки состояния процесса формирования кости при различных метаболических поражениях скелета. Уровень остеокальцина в крови повышен при: § остеомаляции § болезни Педжета § гипертиреозе § первичном гиперпаратиреозе § почечной остеодистрофии § хронической почечной недостаточности § активных процессах формирования кости (в том числе и опухолевых) § активных процессах роста (подростковый возраст) § метастазировании опухолей различного происхождения в костную ткань Пониженные уровни остеокальцина отмечаются при: § гипопаратиреозе § беременности § дефиците соматотропина § продолжительной терапии кортикостероидами.
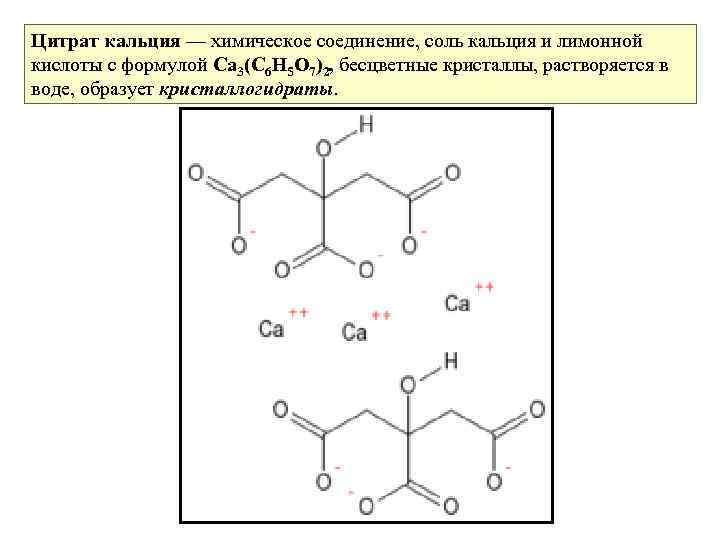
Цитрат кальция — химическое соединение, соль кальция и лимонной кислоты с формулой Ca 3(C 6 H 5 O 7)2, бесцветные кристаллы, растворяется в воде, образует кристаллогидраты.

Остеопоро з (лат. osteoporosis) — хронически прогрессирующее системное, обменное заболевание скелета или клинический синдром, проявляющийся при других заболеваниях, который характеризуется снижением плотности костей, нарушением их микроархитектоники и усилением хрупкости, по причине нарушения метаболизма костной ткани с преобладанием катаболизма над процессами костеобразования, снижением прочности кости и повышением риска переломов. При остеопорозе уровень остеокальцина может быть повышенным или нормальным, в зависимости от выраженности процессов остеосинтеза. Нужно иметь в виду, что уровень остеокальцина в крови подвержен большим суточным колебаниям.

Резорбция кости Группа остеокластов растворяет минеральный компонент кости, а также гидролизует органический матрикс. Разрушение кости начинается с прикрепления остеокласта к минерализованной костной поверхности «гофрированным краем» , через который выделяются гидролитические ферменты и протоны, а также различные интегрины (α₁, αᵥ, β₁, β₃), участвующие в растворении кости. Другие клетки, принимающие участие в резорбции костной ткани — это моноциты и макрофаги. Они взаимодействуют с костной тканью посредством фагоцитоза и хемотаксиса, в большинстве случаев действуя как «уборщики мусора» . Помимо фагоцитарной активности продуцируются цитокины (ИЛ-1, ИЛ-1α, ИЛ-1β, ФНО-α, tumor necrosis factor, TNF — внеклеточный белок, многофункциональный провоспалительный цитокин), влияющие на активизацию коллагеназ, разрушающих белковый матрикс. Кроме того, моноциты и макрофаги рассматриваются многими учёными как предшественники остеокластов. Имеются сведения о влиянии лимфоцитов на резорбцию костной ткани посредством секреции ФНО-β, а также через 1, 25 дигидроксихолекальциферол (витамин D) и ПТГ, к которым лимфоциты имеют рецепторы.

Биохимические методы выявления нарушений обмена костной ткани: • кальций-фосфорный метаболизм и кальций-регулирующие гормоны; • маркеры формирования и резорбции костной ткани. К первым относят: определение суточной экскреции фосфора и кальция (также кальция по отношению к креатинину), определение их уровня в крови, определение уровней кальцитонина, паратгормона, витамина D. Ко вторым: щелочную фосфатазу (остеокальцин), кислую фосфатазу, оксипролин и др. «Золотым стандартом» считают оценку уровней деоксипиридинолина и пиридинолина.

Преимуществом биохимических методов исследования является неинвазивность проведения, доступность, особенно параметров определяемых в моче, поскольку моча является одним из самых удобных объектов исследования. Маркёры костной резорбции являются высокоспецифичными, они быстрее реагируют на изменения в ремоделировании кости и появляются в исследуемых жидкостях, предоставляя информацию об активности процесса. В отличие от денситометрии, биохимические маркёры являются более ранними диагностическими критериями. Хотя денситометрия — весьма точный и нетравматичный метод исследования для оценки функциональноструктурного состояния костной ткани и диагностики остеопороза, однако, с момента начала изменения в костной ткани и до момента получения достоверной информации необходим более длительный промежуток времени. Хотя не существует какого-либо единственного и специфического костного маркёра и невозможно поставить диагноз только на основании исследования биохимических маркёров костного ремоделирования, тем не менее, они позволяют проводить дифференциальную диагностику метаболических заболеваний скелета (особенно с остеомаляцией) и наблюдение за динамикой костного метаболизма при лечении остеопороза.

Показатели костной резорбции: Продукты остеокластов: Ø кислая фосфатаза, Ø тартратрезистентная кислая фосфатаза (ТРКФ) — определяются биохимическим анализом крови. Продукты деградации коллагена: § гидроксипролин (определяется в моче), § пиридинолин и дезоксипиридинолин (могут определяться как в моче, так и в крови). Коллагеновые перекрёстные группы: § N-концевой телопептид, § С-концевой телопептид (Cross. Laps) — определяются в моче и крови. Продукты распада минерального комплекса: § уровень ионизированного кальция в крови, § концентрация кальция и фосфора в моче по отношению к креатинину (утром натощак).
Соединительная ткань.pptx