Соединения серы серная кислота.ppt
- Количество слайдов: 15

Соединения серы. Серная кислота.
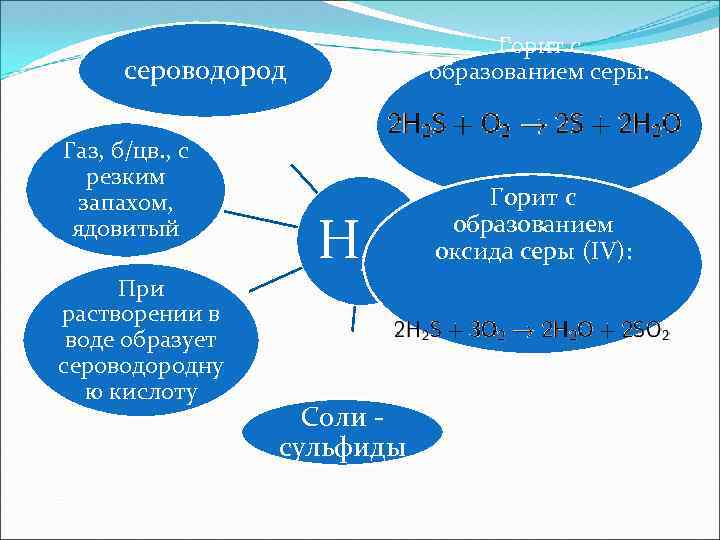
Горит с образованием серы: сероводород Газ, б/цв. , с резким запахом, ядовитый При растворении в воде образует сероводородну ю кислоту H 2 S Соли сульфиды Горит с При недостатке О 2 образованием оксида серы (IV):
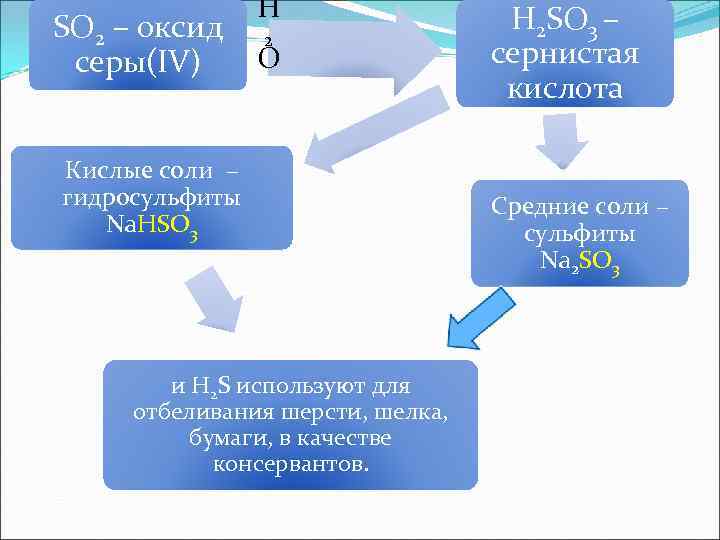
SO 2 – оксид серы(IV) Н 2 О Кислые соли – гидросульфиты Na. НSO 3 и H 2 S используют для отбеливания шерсти, шелка, бумаги, в качестве консервантов. H 2 SO 3 – сернистая кислота Средние соли – сульфиты Na 2 SO 3
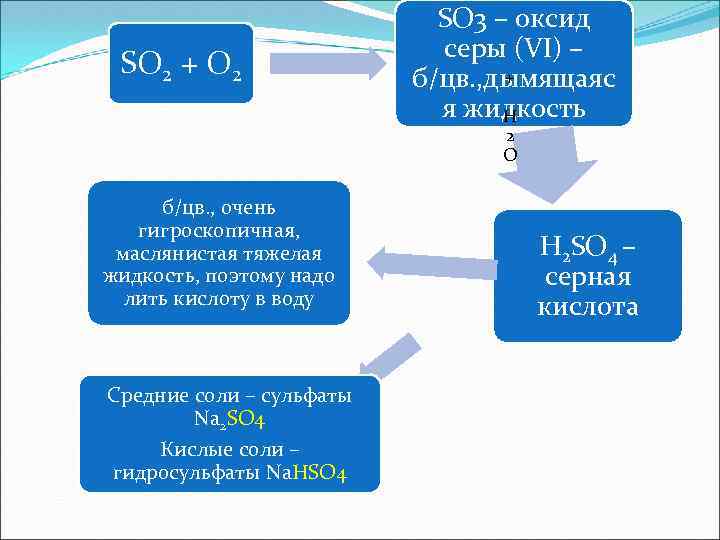
SO 2 + О 2 SO 3 – оксид серы (VI) – + б/цв. , дымящаяс я жидкость H 2 O б/цв. , очень гигроскопичная, маслянистая тяжелая жидкость, поэтому надо лить кислоту в воду Средние соли – сульфаты Na 2 SO 4 Кислые соли – гидросульфаты Na. НSO 4 H 2 SO 4 – серная кислота

Химические свойства концентрированной серной кислоты: Na. Cl + H 2 SO 4 → Na. HSO 4 + HCl↑

Химические свойства разбавленной серной кислоты:

Производство минеральных удобрений Простой Преципитат суперфосфат Двойной суперфосфат Сульфат аммония

Электролит в свинцовых аккумуляторах

Производство Синтетических моющих средств Красителей Пластмасс Лекарственных препаратов

Обогащение руд Очистка нефтепродуктов Керосин Парафин Осушение газов Смазочные масла

В отраслях промышленности Металлообрабатывающая Кожевенная Текстильная

В пищевой промышленности Пищевая добавка Е 513 регулятор кислотности

Органический синтез Сульфокислоты Этиловый спирт Уксусная кислота Водоотнимающее средство Нитробензол Нитроглицерин Пироксилин

Применение солей Медный купорос Железный купорос Горькая соль

Домашнее задание: § 23, № 3, с. 134, № 5 с. 142
Соединения серы серная кислота.ppt