соединения серы и углерода.pptx
- Количество слайдов: 11
 Соединения серы и углерода
Соединения серы и углерода
 Натрия тиосульфат Natrii thiosulfas Na 2 S 2 O 3 • 5 H 2 O Sodium thiosulfate (MHH) Натриевая соль тиосерной кислоты 1799 г Химические свойства. Реакция разложения Na 2 S 2 O 3 + CO 2 + H 2 O → Na 2 CO 3 + H 2 S 2 O 3 → S↓ + SO 2↑ + H 2 O желтый (муть) запах Подлинность 1. реакции на ион натрия (см. катины-анионы) 2. Реакции на тиосульфат-ион
Натрия тиосульфат Natrii thiosulfas Na 2 S 2 O 3 • 5 H 2 O Sodium thiosulfate (MHH) Натриевая соль тиосерной кислоты 1799 г Химические свойства. Реакция разложения Na 2 S 2 O 3 + CO 2 + H 2 O → Na 2 CO 3 + H 2 S 2 O 3 → S↓ + SO 2↑ + H 2 O желтый (муть) запах Подлинность 1. реакции на ион натрия (см. катины-анионы) 2. Реакции на тиосульфат-ион
 А. Реакция разложения с кислотой хлороводородной разведенной Na 2 S 2 O 3 + 2 НСl → 2 Na. Cl + SO 2↑ + S↓+ H 2 O S 2 - - 2ē = S↓ запах желтый(муть) S 6+ + 2ē = S 4+ Б. Реакция с раствором серебра нитрата. Na 2 S 2 O 3 + 2 Ag. N 03 → Ag 2 S 2 O 3 ↓ + 2 Na. N 03 белый Ag 2 S 2 O 3 → Ag 2 SO 3↓ + S↓желтый осадок Ag 2 SO 3 + S + H 2 O → Ag 2 S↓ + H 2 SO 4 черный белый → желтый → бурый → черный
А. Реакция разложения с кислотой хлороводородной разведенной Na 2 S 2 O 3 + 2 НСl → 2 Na. Cl + SO 2↑ + S↓+ H 2 O S 2 - - 2ē = S↓ запах желтый(муть) S 6+ + 2ē = S 4+ Б. Реакция с раствором серебра нитрата. Na 2 S 2 O 3 + 2 Ag. N 03 → Ag 2 S 2 O 3 ↓ + 2 Na. N 03 белый Ag 2 S 2 O 3 → Ag 2 SO 3↓ + S↓желтый осадок Ag 2 SO 3 + S + H 2 O → Ag 2 S↓ + H 2 SO 4 черный белый → желтый → бурый → черный
 Чистота -недопустимые примеси 1. Сульфиты и сульфаты SO 32 - + I 2 + H 2 O → SO 42 - + 2 HI SO 42 - + Ва(NO 3)2 → Ва. SO 4↓ + 2 NO 3 белый 2. Сульфиды – с натрия нитропруссидом Na 2 S + Na 2[Fe(CN)5 NO] → Na 4[Fe(CN)5 NOS] фиолетовое окрашивание Количественное определение 2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 IИндикатор – крахмал (до синего окрашивания)
Чистота -недопустимые примеси 1. Сульфиты и сульфаты SO 32 - + I 2 + H 2 O → SO 42 - + 2 HI SO 42 - + Ва(NO 3)2 → Ва. SO 4↓ + 2 NO 3 белый 2. Сульфиды – с натрия нитропруссидом Na 2 S + Na 2[Fe(CN)5 NO] → Na 4[Fe(CN)5 NOS] фиолетовое окрашивание Количественное определение 2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 IИндикатор – крахмал (до синего окрашивания)
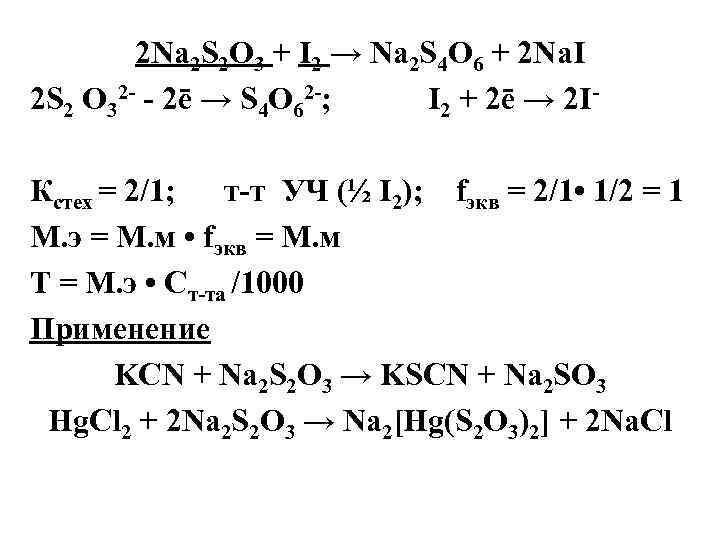 2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 I- Кстех = 2/1; т-т УЧ (½ I 2); fэкв = 2/1 • 1/2 = 1 М. э = М. м • fэкв = М. м Т = М. э • Ст-та /1000 Применение KCN + Na 2 S 2 O 3 → KSCN + Na 2 SO 3 Hg. Cl 2 + 2 Na 2 S 2 O 3 → Na 2[Hg(S 2 O 3)2] + 2 Na. Cl
2 Na 2 S 2 O 3 + I 2 → Na 2 S 4 O 6 + 2 Na. I 2 S 2 O 32 - - 2ē → S 4 O 62 -; I 2 + 2ē → 2 I- Кстех = 2/1; т-т УЧ (½ I 2); fэкв = 2/1 • 1/2 = 1 М. э = М. м • fэкв = М. м Т = М. э • Ст-та /1000 Применение KCN + Na 2 S 2 O 3 → KSCN + Na 2 SO 3 Hg. Cl 2 + 2 Na 2 S 2 O 3 → Na 2[Hg(S 2 O 3)2] + 2 Na. Cl
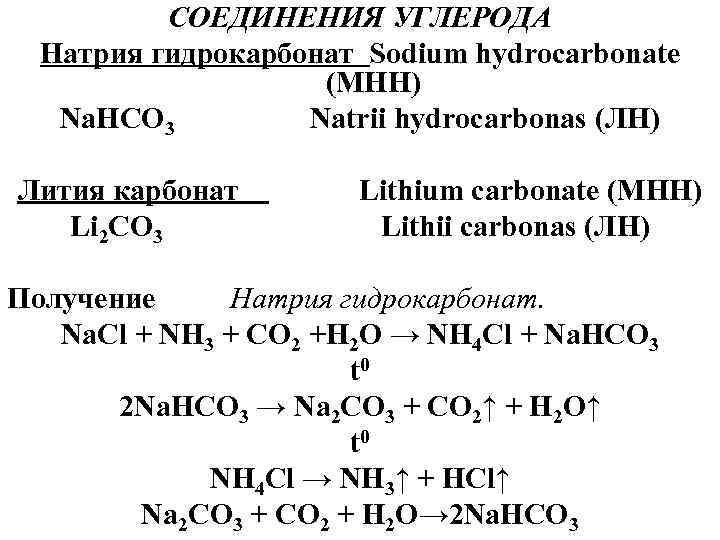 СОЕДИНЕНИЯ УГЛЕРОДА Натрия гидрокарбонат Sodium hydrocarbonate (MHH) Na. HCO 3 Natrii hydrocarbonas (ЛH) Лития карбонат Lithium carbonate (MHH) Li 2 CO 3 Lithii carbonas (ЛH) Получение Натрия гидрокарбонат. Na. Cl + NH 3 + CO 2 +H 2 O → NH 4 Cl + Na. HCO 3 t 0 2 Na. HCO 3 → Na 2 CO 3 + CO 2↑ + H 2 O↑ t 0 NH 4 Cl → NH 3↑ + HCl↑ Na 2 CO 3 + CO 2 + H 2 O→ 2 Na. HCO 3
СОЕДИНЕНИЯ УГЛЕРОДА Натрия гидрокарбонат Sodium hydrocarbonate (MHH) Na. HCO 3 Natrii hydrocarbonas (ЛH) Лития карбонат Lithium carbonate (MHH) Li 2 CO 3 Lithii carbonas (ЛH) Получение Натрия гидрокарбонат. Na. Cl + NH 3 + CO 2 +H 2 O → NH 4 Cl + Na. HCO 3 t 0 2 Na. HCO 3 → Na 2 CO 3 + CO 2↑ + H 2 O↑ t 0 NH 4 Cl → NH 3↑ + HCl↑ Na 2 CO 3 + CO 2 + H 2 O→ 2 Na. HCO 3
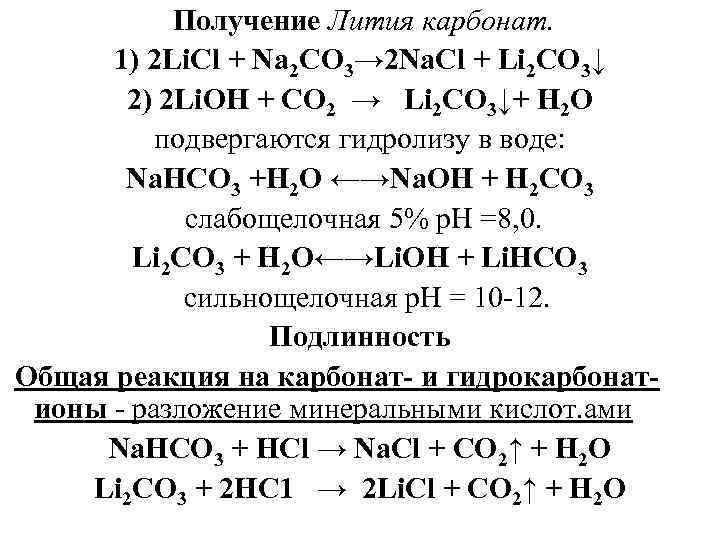 Получение Лития карбонат. 1) 2 Li. Cl + Na 2 CO 3→ 2 Na. Cl + Li 2 CO 3↓ 2) 2 Li. OH + CO 2 → Li 2 CO 3↓+ H 2 O подвергаются гидролизу в воде: Na. HCO 3 +H 2 O ←→Na. OH + H 2 CO 3 слабощелочная 5% р. Н =8, 0. Li 2 CO 3 + H 2 O←→Li. OH + Li. HCO 3 сильнощелочная р. Н = 10 -12. Подлинность Общая реакция на карбонат- и гидрокарбонатионы - разложение минеральными кислот. ами Na. HCO 3 + HCl → Na. Cl + CO 2↑ + H 2 O Li 2 CO 3 + 2 НС 1 → 2 Li. Cl + CO 2↑ + H 2 O
Получение Лития карбонат. 1) 2 Li. Cl + Na 2 CO 3→ 2 Na. Cl + Li 2 CO 3↓ 2) 2 Li. OH + CO 2 → Li 2 CO 3↓+ H 2 O подвергаются гидролизу в воде: Na. HCO 3 +H 2 O ←→Na. OH + H 2 CO 3 слабощелочная 5% р. Н =8, 0. Li 2 CO 3 + H 2 O←→Li. OH + Li. HCO 3 сильнощелочная р. Н = 10 -12. Подлинность Общая реакция на карбонат- и гидрокарбонатионы - разложение минеральными кислот. ами Na. HCO 3 + HCl → Na. Cl + CO 2↑ + H 2 O Li 2 CO 3 + 2 НС 1 → 2 Li. Cl + CO 2↑ + H 2 O
 Реакции отличия карбонат- и гидрокарбонат-ионов: 1. Реакция осаждения с насыщенным раствором магния сульфата. Карбонаты при обычной температуре. 4 Li 2 CO 3 + 4 Mg. SO 4 + 4 Н 2 O → 3 Mg. CO 3 ·Mg(OH)2· 3 H 2 O↓ + 4 Li 2 SO 4 + CO 2↑ Гидрокарбонаты образуют осадок только при нагревании 2 Na. HCO 3 + Mg. SO 4 → Mg(HCO 3)2 + Na 2 SO 4 растворим При кипячении раствора образуется белый осадок: t 0 4 Mg(HCO 3)2 → 3 Mg. C 03·Mg(OH)2· 3 H 2 O↓ + 5 CO 2↑
Реакции отличия карбонат- и гидрокарбонат-ионов: 1. Реакция осаждения с насыщенным раствором магния сульфата. Карбонаты при обычной температуре. 4 Li 2 CO 3 + 4 Mg. SO 4 + 4 Н 2 O → 3 Mg. CO 3 ·Mg(OH)2· 3 H 2 O↓ + 4 Li 2 SO 4 + CO 2↑ Гидрокарбонаты образуют осадок только при нагревании 2 Na. HCO 3 + Mg. SO 4 → Mg(HCO 3)2 + Na 2 SO 4 растворим При кипячении раствора образуется белый осадок: t 0 4 Mg(HCO 3)2 → 3 Mg. C 03·Mg(OH)2· 3 H 2 O↓ + 5 CO 2↑
 2. Проба с фенолфталеином. р. Н ф/ф 8, 2 -10, 0. Растворы гидрокарбонатов → в бледно-розовый цвет или бесцветный(слабощелочная). Растворы карбонатов → в красный цвет (сильнощелочная реакция среды). Специфические реакции. Натрия гидрокарбонат - на ион натрия 1. бесцветное пламя в желтый цвет. 2. Реакция осаждения цинкуранилацетатом. Лития карбонат - на ион лития: 1. бесцветное пламя в карминово-красный цвет. 2. Реакция осаждения натрия гидрофосфатом. 3 Li. Cl + Na 2 HPO 4 + NH 4 OH→ Li 3 PO 4↓ + 2 Na. Cl + NH 4 Cl + H 2 O 3. Реакция осаждения натрия фторидом. Li. Cl + Na. F → Li. F↓ + Na. Cl
2. Проба с фенолфталеином. р. Н ф/ф 8, 2 -10, 0. Растворы гидрокарбонатов → в бледно-розовый цвет или бесцветный(слабощелочная). Растворы карбонатов → в красный цвет (сильнощелочная реакция среды). Специфические реакции. Натрия гидрокарбонат - на ион натрия 1. бесцветное пламя в желтый цвет. 2. Реакция осаждения цинкуранилацетатом. Лития карбонат - на ион лития: 1. бесцветное пламя в карминово-красный цвет. 2. Реакция осаждения натрия гидрофосфатом. 3 Li. Cl + Na 2 HPO 4 + NH 4 OH→ Li 3 PO 4↓ + 2 Na. Cl + NH 4 Cl + H 2 O 3. Реакция осаждения натрия фторидом. Li. Cl + Na. F → Li. F↓ + Na. Cl
 Чистота предельное содержание общих примесей: хлоридов, сульфатов, железа, кальция, тяжелых металлов. В натрия гидрокарбонате определяют: 1. недопустимая примесь солей аммония – реакция с раствором натрия гидроксида. При t 0 не должен NH 3↑. 2. допустимаяпримесь карбонатов – определяют потерю в массе при прокаливании (должна быть не менее 36, 6%). t 0 2 Na. HCO 3 → Na 2 CO 3 + CO 2↑+ H 2 O↑ Теоретически прокаливании теряется 36, 9% от массы Na. HCO 3. В лития карбонате определяют: примеси солей других щелочных металлов, магния, бария.
Чистота предельное содержание общих примесей: хлоридов, сульфатов, железа, кальция, тяжелых металлов. В натрия гидрокарбонате определяют: 1. недопустимая примесь солей аммония – реакция с раствором натрия гидроксида. При t 0 не должен NH 3↑. 2. допустимаяпримесь карбонатов – определяют потерю в массе при прокаливании (должна быть не менее 36, 6%). t 0 2 Na. HCO 3 → Na 2 CO 3 + CO 2↑+ H 2 O↑ Теоретически прокаливании теряется 36, 9% от массы Na. HCO 3. В лития карбонате определяют: примеси солей других щелочных металлов, магния, бария.
 Количественное определение Ацидиметрический метод вытеснения натрия гидрокарбонат вариант прямого титрования, индикатор - метиловый оранжевый (от желтого к розовому) титрант HCl. Na. HCO 3 + HCl→Na. Cl + CO 2↑ + H 2 O fэкв=1 Лития карбонат вариант обратного титрования (трудно растворим в воде), индикатор - метиловый оранжевый (от розового к желтому) Li 2 CO 3 + 2 НСl → 2 Li. Cl + CO 2↑ + H 2 O избыток HCl + Na. OH → Na. Cl + H 2 O остаток fэкв =1/2
Количественное определение Ацидиметрический метод вытеснения натрия гидрокарбонат вариант прямого титрования, индикатор - метиловый оранжевый (от желтого к розовому) титрант HCl. Na. HCO 3 + HCl→Na. Cl + CO 2↑ + H 2 O fэкв=1 Лития карбонат вариант обратного титрования (трудно растворим в воде), индикатор - метиловый оранжевый (от розового к желтому) Li 2 CO 3 + 2 НСl → 2 Li. Cl + CO 2↑ + H 2 O избыток HCl + Na. OH → Na. Cl + H 2 O остаток fэкв =1/2


