 Соединения металлов 13 группы (13 M = Al, Ga, In, Tl) 1
Соединения металлов 13 группы (13 M = Al, Ga, In, Tl) 1
 Металлы 13 группы электронная конфигурация E: ns 2 np 1, E*: ns 1 np 2 Формальные степени окисления: 0, +1, +2, +3 M B Al Ga In Tl E 0(M 3+/M), В Ковалентный 0 3+ 1+ Электроотр. E (M /M ), В радиус, Å E 0(M 1+/M), В 2. 0 1. 6 1. 8 1. 6 Температура Плавления (0 C) 0. 84 0. 90 2075 1. 21 1. 70 660 1. 22 0. 56 29. 78 1. 42 0. 34 156. 6 1. 45 +1. 28 0. 34 304 2
Металлы 13 группы электронная конфигурация E: ns 2 np 1, E*: ns 1 np 2 Формальные степени окисления: 0, +1, +2, +3 M B Al Ga In Tl E 0(M 3+/M), В Ковалентный 0 3+ 1+ Электроотр. E (M /M ), В радиус, Å E 0(M 1+/M), В 2. 0 1. 6 1. 8 1. 6 Температура Плавления (0 C) 0. 84 0. 90 2075 1. 21 1. 70 660 1. 22 0. 56 29. 78 1. 42 0. 34 156. 6 1. 45 +1. 28 0. 34 304 2
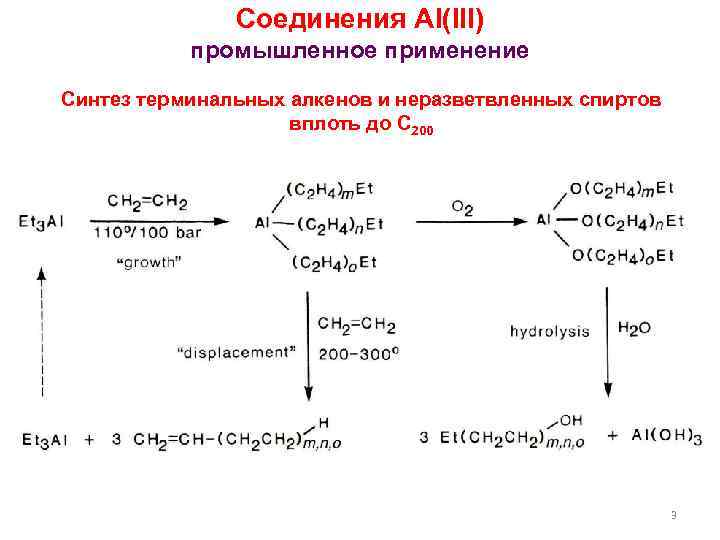 Соединения Al(III) промышленное применение Синтез терминальных алкенов и неразветвленных спиртов вплоть до C 200 3
Соединения Al(III) промышленное применение Синтез терминальных алкенов и неразветвленных спиртов вплоть до C 200 3
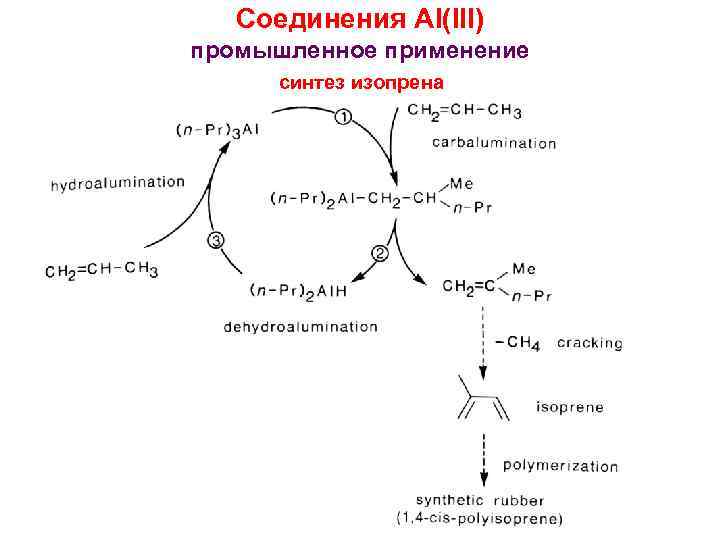 Соединения Al(III) промышленное применение синтез изопрена 4
Соединения Al(III) промышленное применение синтез изопрена 4
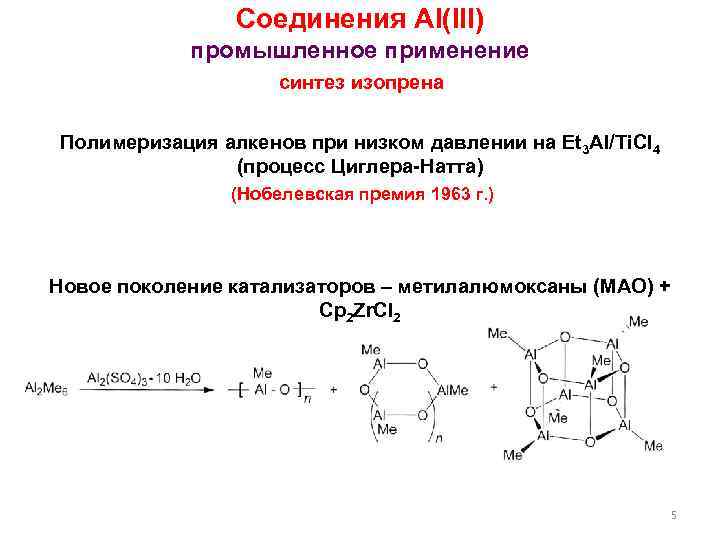 Соединения Al(III) промышленное применение синтез изопрена Полимеризация алкенов при низком давлении на Et 3 Al/Ti. Cl 4 (процесс Циглера-Натта) (Нобелевская премия 1963 г. ) Новое поколение катализаторов – метилалюмоксаны (МАО) + Cp 2 Zr. Cl 2 5
Соединения Al(III) промышленное применение синтез изопрена Полимеризация алкенов при низком давлении на Et 3 Al/Ti. Cl 4 (процесс Циглера-Натта) (Нобелевская премия 1963 г. ) Новое поколение катализаторов – метилалюмоксаны (МАО) + Cp 2 Zr. Cl 2 5
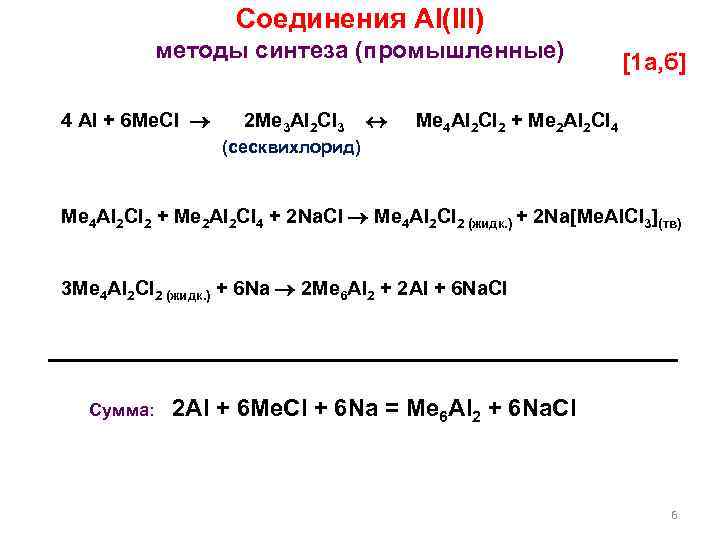 Соединения Al(III) методы синтеза (промышленные) 4 Al + 6 Me. Cl 2 Me 3 Al 2 Cl 3 [1 а, б] Me 4 Al 2 Cl 2 + Me 2 Al 2 Cl 4 (сесквихлорид) Me 4 Al 2 Cl 2 + Me 2 Al 2 Cl 4 + 2 Na. Cl Me 4 Al 2 Cl 2 (жидк. ) + 2 Na[Me. Al. Cl 3](тв) 3 Me 4 Al 2 Cl 2 (жидк. ) + 6 Na 2 Me 6 Al 2 + 2 Al + 6 Na. Cl Сумма: 2 Al + 6 Me. Cl + 6 Na = Me 6 Al 2 + 6 Na. Cl 6
Соединения Al(III) методы синтеза (промышленные) 4 Al + 6 Me. Cl 2 Me 3 Al 2 Cl 3 [1 а, б] Me 4 Al 2 Cl 2 + Me 2 Al 2 Cl 4 (сесквихлорид) Me 4 Al 2 Cl 2 + Me 2 Al 2 Cl 4 + 2 Na. Cl Me 4 Al 2 Cl 2 (жидк. ) + 2 Na[Me. Al. Cl 3](тв) 3 Me 4 Al 2 Cl 2 (жидк. ) + 6 Na 2 Me 6 Al 2 + 2 Al + 6 Na. Cl Сумма: 2 Al + 6 Me. Cl + 6 Na = Me 6 Al 2 + 6 Na. Cl 6
 Соединения Al(III) методы синтеза (промышленные) процесс Циглера Al + 1. 5 H 2 + 2 Et 3 Al 3 Et 2 Al. H (80– 160 o. C, 100– 200 атм) 3 Et 2 Al. H + 3 C 2 H 4 3 Et 3 Al (80– 110 o. C, 1– 10 атм) Сумма: Al + 3 C 2 H 4 + 3/2 H 2 = Et 3 Al 7
Соединения Al(III) методы синтеза (промышленные) процесс Циглера Al + 1. 5 H 2 + 2 Et 3 Al 3 Et 2 Al. H (80– 160 o. C, 100– 200 атм) 3 Et 2 Al. H + 3 C 2 H 4 3 Et 3 Al (80– 110 o. C, 1– 10 атм) Сумма: Al + 3 C 2 H 4 + 3/2 H 2 = Et 3 Al 7
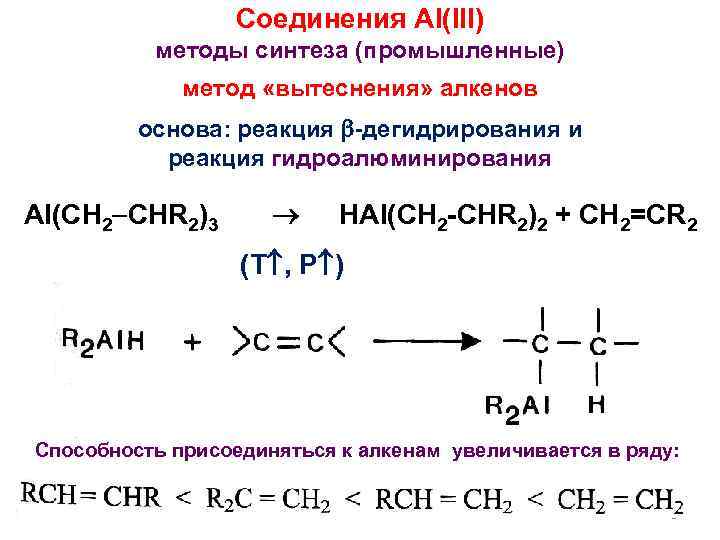 Соединения Al(III) методы синтеза (промышленные) метод «вытеснения» алкенов основа: реакция -дегидрирования и реакция гидроалюминирования Al(CH 2 CHR 2)3 HAl(CH 2 -CHR 2)2 + CH 2=CR 2 (T , P ) Способность присоединяться к алкенам увеличивается в ряду: 8
Соединения Al(III) методы синтеза (промышленные) метод «вытеснения» алкенов основа: реакция -дегидрирования и реакция гидроалюминирования Al(CH 2 CHR 2)3 HAl(CH 2 -CHR 2)2 + CH 2=CR 2 (T , P ) Способность присоединяться к алкенам увеличивается в ряду: 8
 Соединения Al(III) методы синтеза (промышленные) метод «вытеснения» алкенов Al + 3/2 H 2 + 3 CH 2=CMe 2 (i-Bu)3 Al Al(i-Bu)3 HAl(i-Bu)2 + CH 2=CMe 2 (T , P ) HAl(i-Bu)2 + CH 2=CHMe Al(i-Bu)2(n-Pr) HAl(i-Bu)(n-Pr) + CH 2=CMe 2 HAl(i-Bu)(n-Pr) + CH 2=CHMe Al(i-Bu)(n-Pr)2 HAl(n-Pr)2 + CH 2=CMe 2 HAl(n-Pr)2 + CH 2=CHMe Al(n-Pr)3 Al(i-Bu)3 + 3 CH 2=CHMe Al(n-Pr)3 + 3 CH 2=CMe 2 (T , P ) 10
Соединения Al(III) методы синтеза (промышленные) метод «вытеснения» алкенов Al + 3/2 H 2 + 3 CH 2=CMe 2 (i-Bu)3 Al Al(i-Bu)3 HAl(i-Bu)2 + CH 2=CMe 2 (T , P ) HAl(i-Bu)2 + CH 2=CHMe Al(i-Bu)2(n-Pr) HAl(i-Bu)(n-Pr) + CH 2=CMe 2 HAl(i-Bu)(n-Pr) + CH 2=CHMe Al(i-Bu)(n-Pr)2 HAl(n-Pr)2 + CH 2=CMe 2 HAl(n-Pr)2 + CH 2=CHMe Al(n-Pr)3 Al(i-Bu)3 + 3 CH 2=CHMe Al(n-Pr)3 + 3 CH 2=CMe 2 (T , P ) 10
![Соединения Al(III) методы синтеза (лабораторные) [2] [4] [9] 11 Соединения Al(III) методы синтеза (лабораторные) [2] [4] [9] 11](https://present5.com/presentation/5652994_164495112/image-10.jpg) Соединения Al(III) методы синтеза (лабораторные) [2] [4] [9] 11
Соединения Al(III) методы синтеза (лабораторные) [2] [4] [9] 11
 Соединения Al(III) Строение и свойства R 3 Al – бесцветные жидкости, энергично взаимодействующие с воздухом и взрывающиеся при контакте с водой. Соединения с небольшими R пирофорны! Реакции R 3 Al должны проводиться в алканах или ароматических углеводородах. С другими растворителями R 3 Al реагируют. Контакт R 3 Al с CHCl 3 и CCl 4 может привести к взрыву. Триалкильные соединения разлагаются на R 2 Al. H и соответствующий алкен: при 80 o. C – алкены с разветвлением в -положении и при 120 o. C – неразветвленные. Соединения Rn. Al. X 3–n (X = галоген, OR) существенно менее реакционноспособны. 12
Соединения Al(III) Строение и свойства R 3 Al – бесцветные жидкости, энергично взаимодействующие с воздухом и взрывающиеся при контакте с водой. Соединения с небольшими R пирофорны! Реакции R 3 Al должны проводиться в алканах или ароматических углеводородах. С другими растворителями R 3 Al реагируют. Контакт R 3 Al с CHCl 3 и CCl 4 может привести к взрыву. Триалкильные соединения разлагаются на R 2 Al. H и соответствующий алкен: при 80 o. C – алкены с разветвлением в -положении и при 120 o. C – неразветвленные. Соединения Rn. Al. X 3–n (X = галоген, OR) существенно менее реакционноспособны. 12
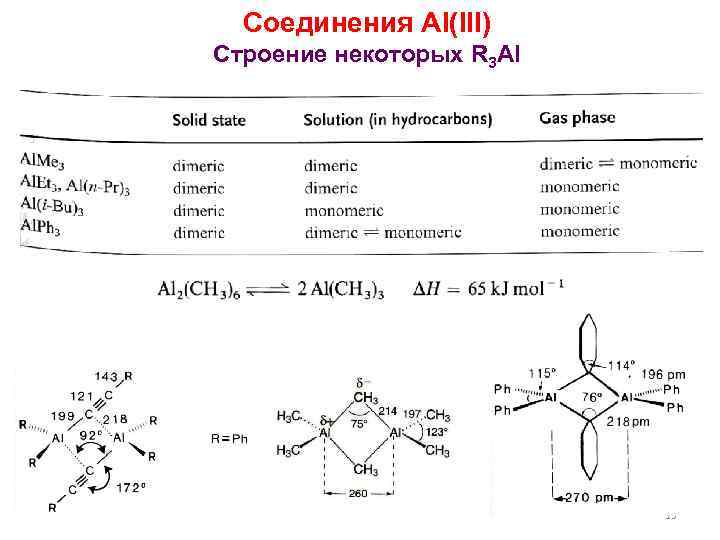 Соединения Al(III) Строение некоторых R 3 Al 13
Соединения Al(III) Строение некоторых R 3 Al 13
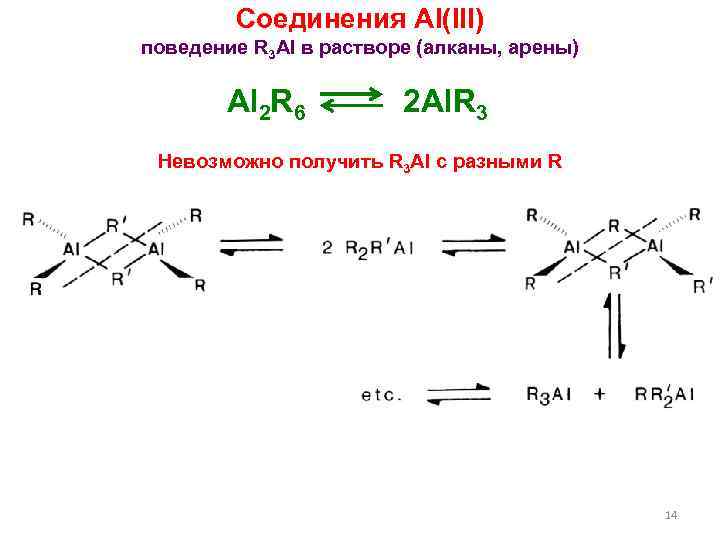 Соединения Al(III) поведение R 3 Al в растворе (алканы, арены) Al 2 R 6 2 Al. R 3 Невозможно получить R 3 Al c разными R 14
Соединения Al(III) поведение R 3 Al в растворе (алканы, арены) Al 2 R 6 2 Al. R 3 Невозможно получить R 3 Al c разными R 14
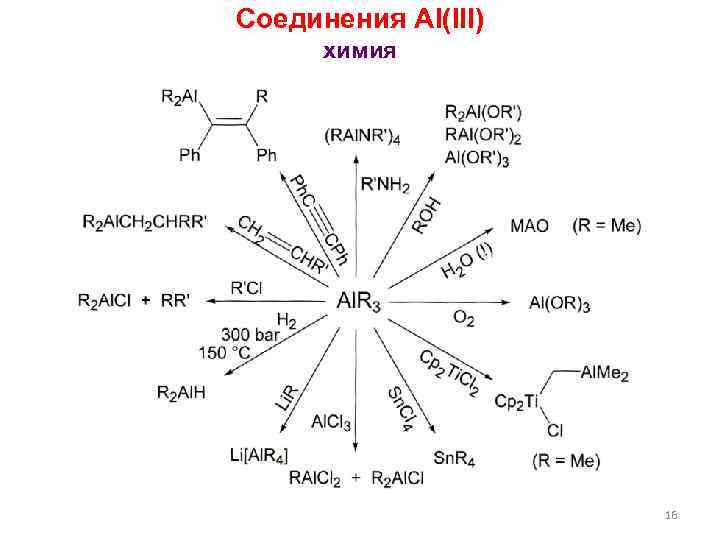 Соединения Al(III) химия 16
Соединения Al(III) химия 16
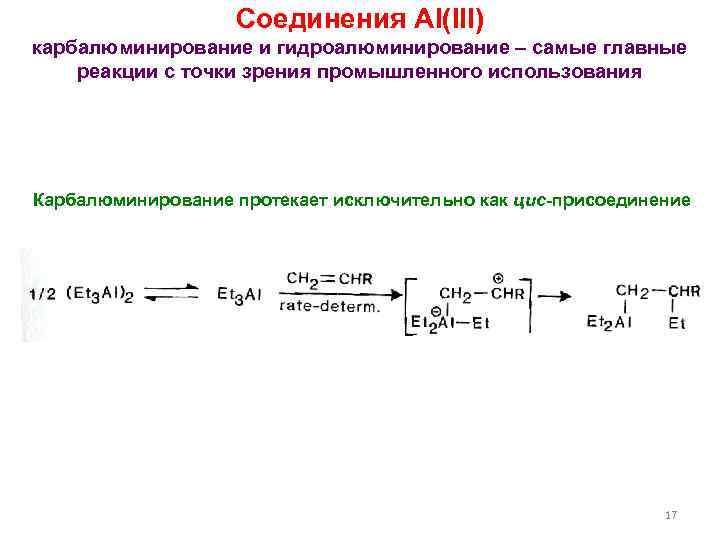 Соединения Al(III) карбалюминирование и гидроалюминирование – самые главные реакции с точки зрения промышленного использования Карбалюминирование протекает исключительно как цис-присоединение 17
Соединения Al(III) карбалюминирование и гидроалюминирование – самые главные реакции с точки зрения промышленного использования Карбалюминирование протекает исключительно как цис-присоединение 17
 Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al Устойчивость комплексов R 3 Al L изменяется в следующем ряду Жесткие основания Мягкие основания 18
Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al Устойчивость комплексов R 3 Al L изменяется в следующем ряду Жесткие основания Мягкие основания 18
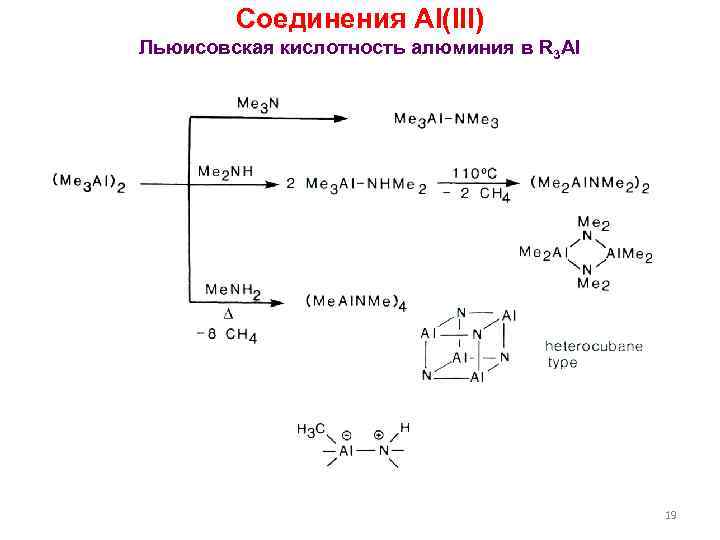 Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al 19
Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al 19
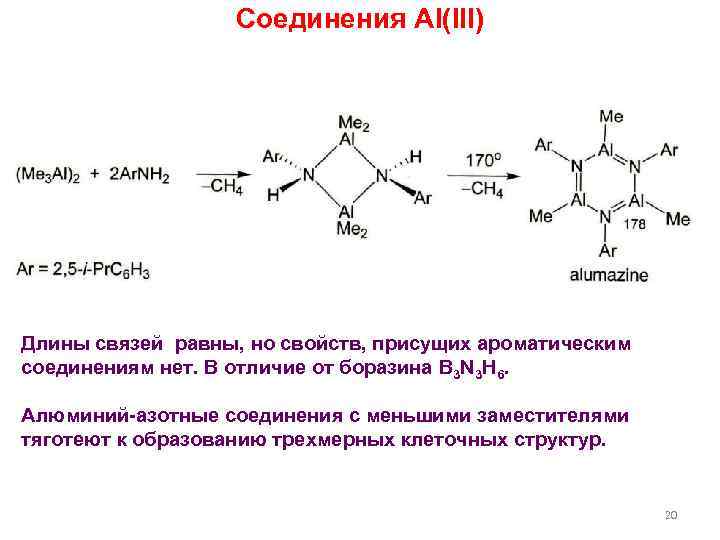 Соединения Al(III) Длины связей равны, но свойств, присущих ароматическим соединениям нет. В отличие от боразина B 3 N 3 H 6. Алюминий-азотные соединения с меньшими заместителями тяготеют к образованию трехмерных клеточных структур. 20
Соединения Al(III) Длины связей равны, но свойств, присущих ароматическим соединениям нет. В отличие от боразина B 3 N 3 H 6. Алюминий-азотные соединения с меньшими заместителями тяготеют к образованию трехмерных клеточных структур. 20
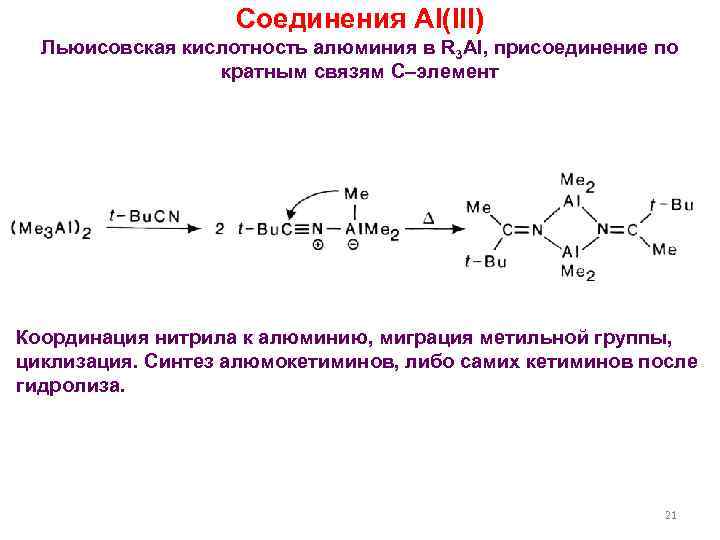 Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al, присоединение по кратным связям C–элемент Координация нитрила к алюминию, миграция метильной группы, циклизация. Синтез алюмокетиминов, либо самих кетиминов после гидролиза. 21
Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al, присоединение по кратным связям C–элемент Координация нитрила к алюминию, миграция метильной группы, циклизация. Синтез алюмокетиминов, либо самих кетиминов после гидролиза. 21
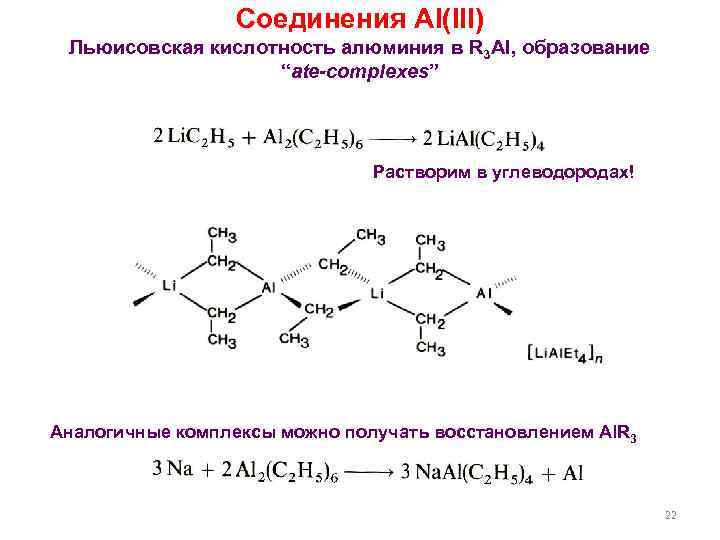 Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al, образование “ate-complexes” Растворим в углеводородах! Аналогичные комплексы можно получать восстановлением Al. R 3 22
Соединения Al(III) Льюисовская кислотность алюминия в R 3 Al, образование “ate-complexes” Растворим в углеводородах! Аналогичные комплексы можно получать восстановлением Al. R 3 22
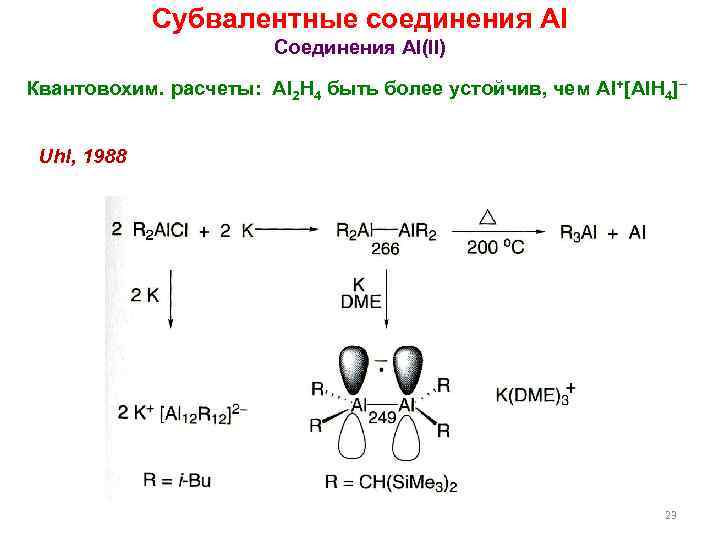 Субвалентные соединения Al Соединения Al(II) Квантовохим. расчеты: Al 2 H 4 быть более устойчив, чем Al+[Al. H 4] Uhl, 1988 l 23
Субвалентные соединения Al Соединения Al(II) Квантовохим. расчеты: Al 2 H 4 быть более устойчив, чем Al+[Al. H 4] Uhl, 1988 l 23
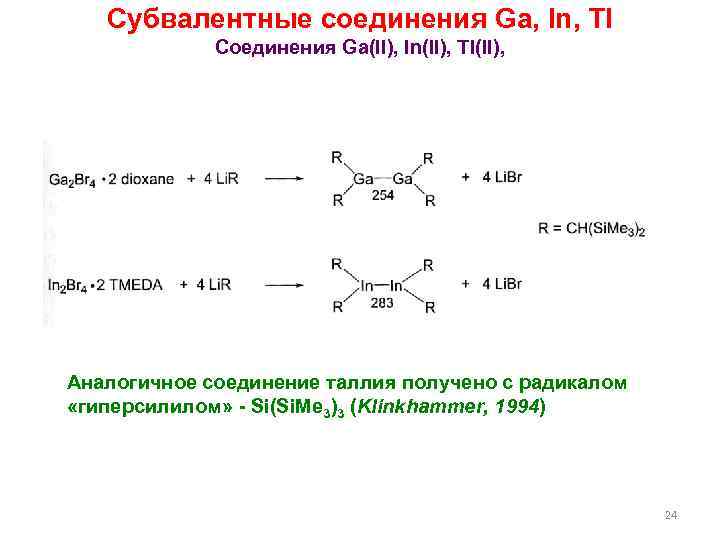 Субвалентные соединения Ga, In, Tl Соединения Ga(II), In(II), Tl(II), Аналогичное соединение таллия получено с радикалом «гиперсилилом» - Si(Si. Me 3)3 (Klinkhammer, 1994) 24
Субвалентные соединения Ga, In, Tl Соединения Ga(II), In(II), Tl(II), Аналогичное соединение таллия получено с радикалом «гиперсилилом» - Si(Si. Me 3)3 (Klinkhammer, 1994) 24
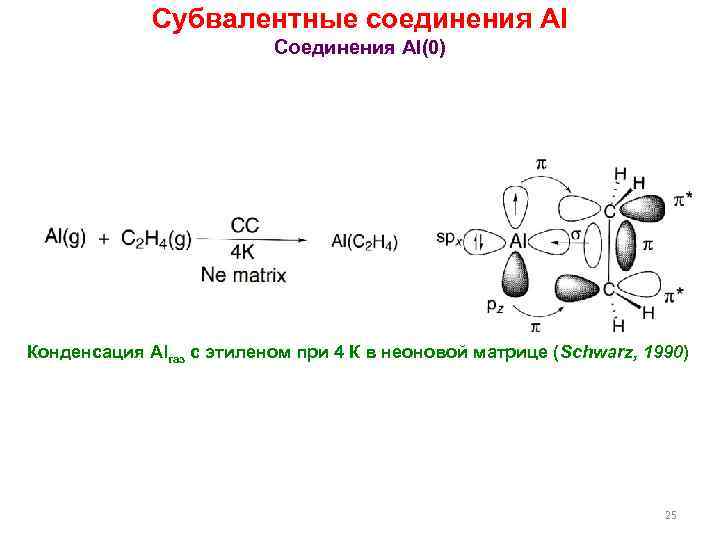 Субвалентные соединения Al Соединения Al(0) Конденсация Alгаз с этиленом при 4 К в неоновой матрице (Schwarz, 1990) 25
Субвалентные соединения Al Соединения Al(0) Конденсация Alгаз с этиленом при 4 К в неоновой матрице (Schwarz, 1990) 25
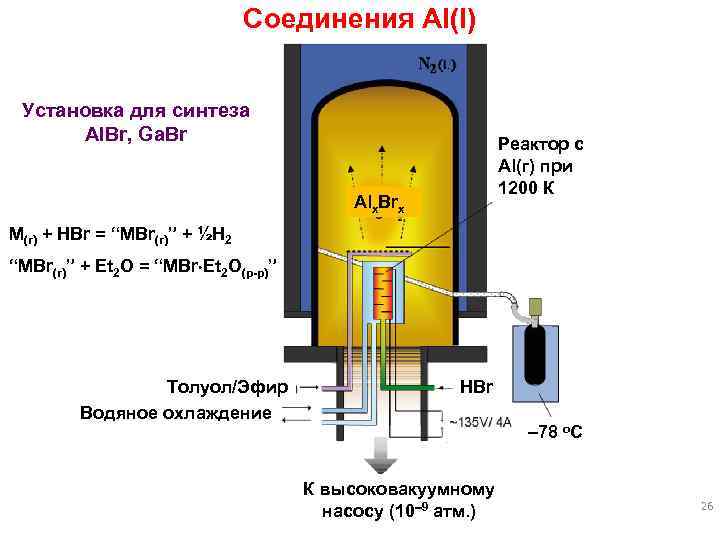 Cоединения Al(I) Установка для синтеза Al. Br, Ga. Br Реактор с Al(г) при 1200 К Alx. Brx M(г) + HBr = “MBr(г)” + ½H 2 “MBr(г)” + Et 2 O = “MBr Et 2 O(р-р)” Толуол/Эфир Водяное охлаждение HBr 78 o. C К высоковакуумному насосу (10 9 атм. ) 26
Cоединения Al(I) Установка для синтеза Al. Br, Ga. Br Реактор с Al(г) при 1200 К Alx. Brx M(г) + HBr = “MBr(г)” + ½H 2 “MBr(г)” + Et 2 O = “MBr Et 2 O(р-р)” Толуол/Эфир Водяное охлаждение HBr 78 o. C К высоковакуумному насосу (10 9 атм. ) 26
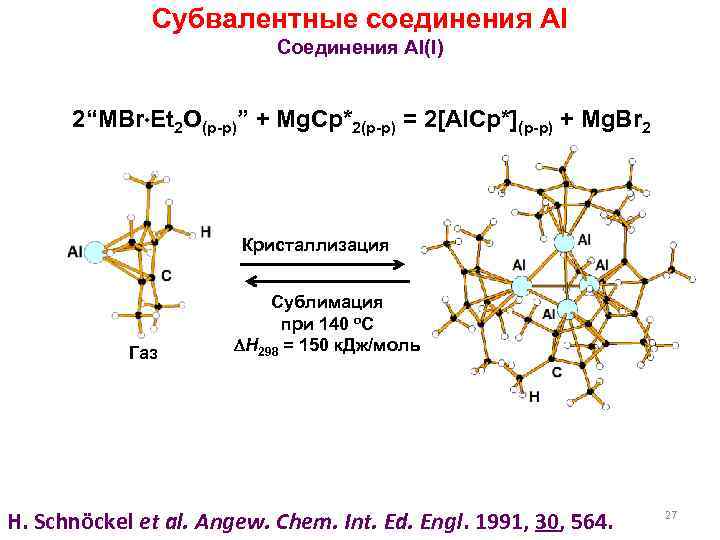 Субвалентные соединения Al Соединения Al(I) 2“MBr Et 2 O(р-р)” + Mg. Cp*2(р-р) = 2[Al. Cp*](р-р) + Mg. Br 2 Кристаллизация Газ Сублимация при 140 о. С H 298 = 150 к. Дж/моль H. Schnöckel et al. Angew. Chem. Int. Ed. Engl. 1991, 30, 564. 27
Субвалентные соединения Al Соединения Al(I) 2“MBr Et 2 O(р-р)” + Mg. Cp*2(р-р) = 2[Al. Cp*](р-р) + Mg. Br 2 Кристаллизация Газ Сублимация при 140 о. С H 298 = 150 к. Дж/моль H. Schnöckel et al. Angew. Chem. Int. Ed. Engl. 1991, 30, 564. 27
![Субвалентные соединения Al Соединения Al(I) 4 Cp*Al. Cl 2 + 8 K [Cp*Al]4 + Субвалентные соединения Al Соединения Al(I) 4 Cp*Al. Cl 2 + 8 K [Cp*Al]4 +](https://present5.com/presentation/5652994_164495112/image-26.jpg) Субвалентные соединения Al Соединения Al(I) 4 Cp*Al. Cl 2 + 8 K [Cp*Al]4 + 8 KCl H. W. Roesky et al. Angew. Chem. Int. Ed. Engl. 1993, 32, 1729. 28
Субвалентные соединения Al Соединения Al(I) 4 Cp*Al. Cl 2 + 8 K [Cp*Al]4 + 8 KCl H. W. Roesky et al. Angew. Chem. Int. Ed. Engl. 1993, 32, 1729. 28
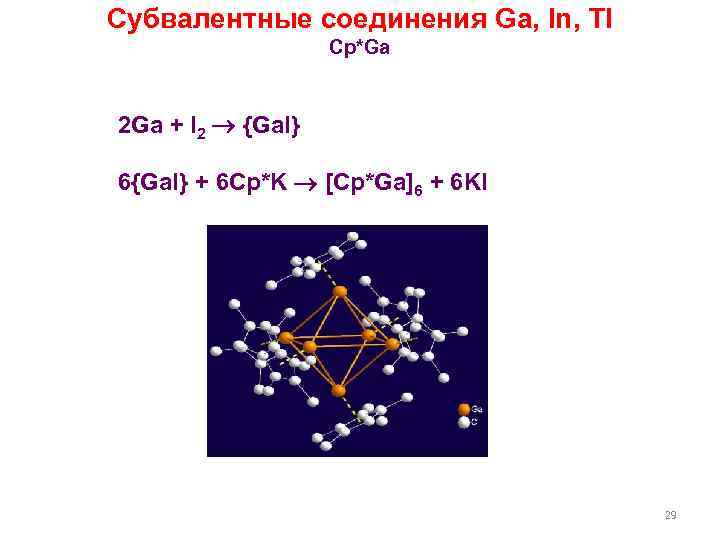 Субвалентные соединения Ga, In, Tl Cp*Ga 2 Ga + I 2 {Ga. I} 6{Ga. I} + 6 Cp*K [Cp*Ga]6 + 6 KI 29
Субвалентные соединения Ga, In, Tl Cp*Ga 2 Ga + I 2 {Ga. I} 6{Ga. I} + 6 Cp*K [Cp*Ga]6 + 6 KI 29
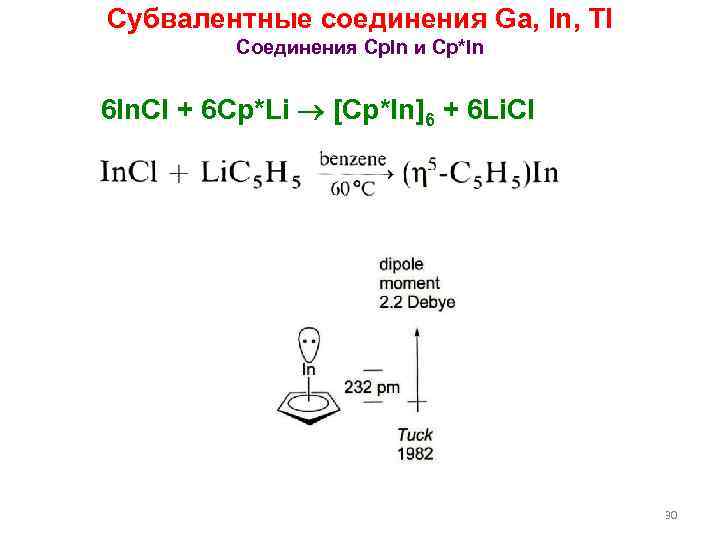 Субвалентные соединения Ga, In, Tl Соединения Cp. In и Cp*In 6 In. Cl + 6 Cp*Li [Cp*In]6 + 6 Li. Cl 30
Субвалентные соединения Ga, In, Tl Соединения Cp. In и Cp*In 6 In. Cl + 6 Cp*Li [Cp*In]6 + 6 Li. Cl 30
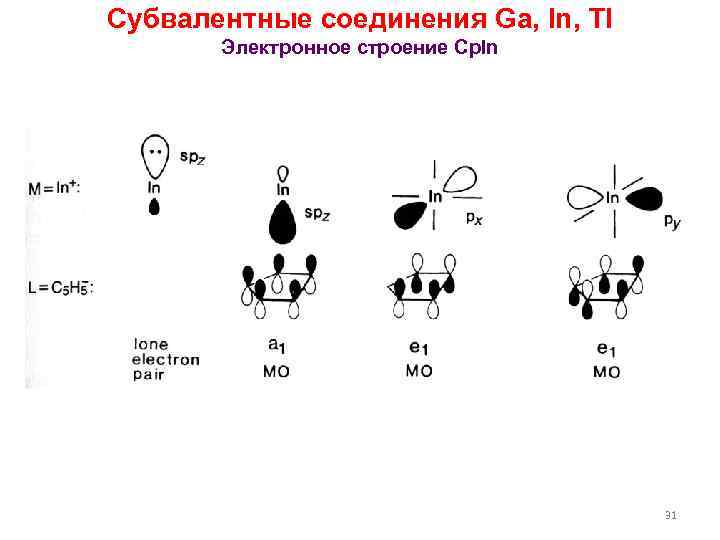 Субвалентные соединения Ga, In, Tl Электронное строение Cp. In 31
Субвалентные соединения Ga, In, Tl Электронное строение Cp. In 31
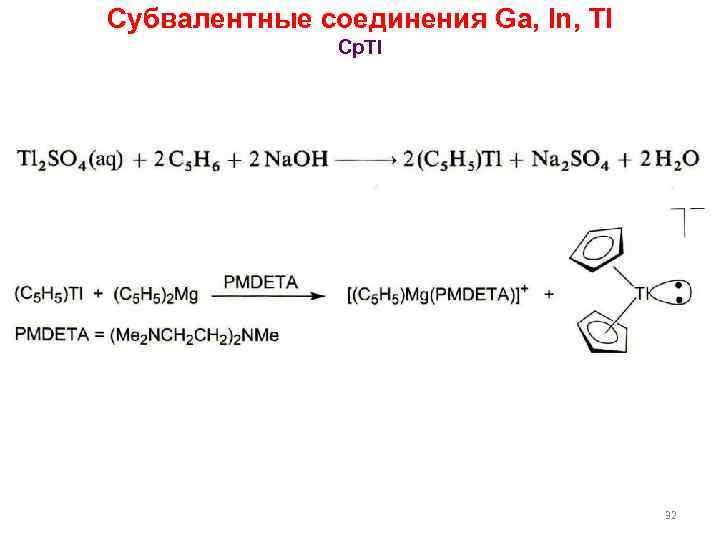 Субвалентные соединения Ga, In, Tl Cp. Tl 32
Субвалентные соединения Ga, In, Tl Cp. Tl 32
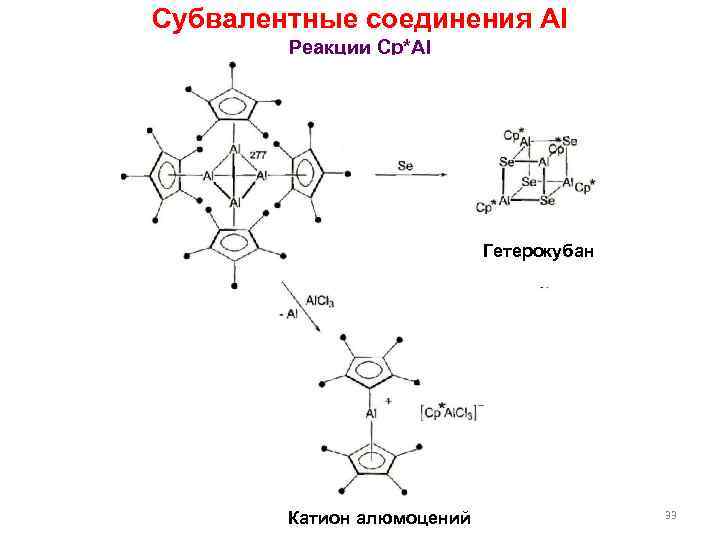 Субвалентные соединения Al Реакции Cp*Al Гетерокубан Катион алюмоцений 33
Субвалентные соединения Al Реакции Cp*Al Гетерокубан Катион алюмоцений 33
![Соединения Al(III) Катион [R 2 Al]+ Планировалось: Mg. Cp*2 + Cp*Al. Cl 2 толуол Соединения Al(III) Катион [R 2 Al]+ Планировалось: Mg. Cp*2 + Cp*Al. Cl 2 толуол](https://present5.com/presentation/5652994_164495112/image-32.jpg) Соединения Al(III) Катион [R 2 Al]+ Планировалось: Mg. Cp*2 + Cp*Al. Cl 2 толуол или гексан [Cp*Mg. Cl] + Cp*2 Al. Cl Получилось: осадок Mg. Cp*2 + Cp*Al. Cl 2 раствор 34
Соединения Al(III) Катион [R 2 Al]+ Планировалось: Mg. Cp*2 + Cp*Al. Cl 2 толуол или гексан [Cp*Mg. Cl] + Cp*2 Al. Cl Получилось: осадок Mg. Cp*2 + Cp*Al. Cl 2 раствор 34
![Соединения Al(III) Катион [R 2 Al]+ Осадок: [Cp*2 Al]+[Cp*3 Mg 3 Br 4] 35 Соединения Al(III) Катион [R 2 Al]+ Осадок: [Cp*2 Al]+[Cp*3 Mg 3 Br 4] 35](https://present5.com/presentation/5652994_164495112/image-33.jpg) Соединения Al(III) Катион [R 2 Al]+ Осадок: [Cp*2 Al]+[Cp*3 Mg 3 Br 4] 35
Соединения Al(III) Катион [R 2 Al]+ Осадок: [Cp*2 Al]+[Cp*3 Mg 3 Br 4] 35
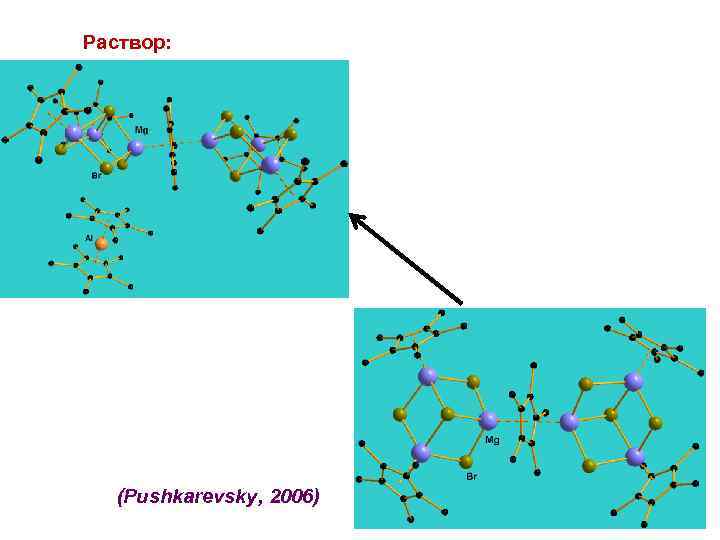 Раствор: (Pushkarevsky, 2006) 36
Раствор: (Pushkarevsky, 2006) 36
![Субвалентные соединения Al Соединения Al(I), [Cp*Al] как лиганд R. A. Fischer, G. Frenking et Субвалентные соединения Al Соединения Al(I), [Cp*Al] как лиганд R. A. Fischer, G. Frenking et](https://present5.com/presentation/5652994_164495112/image-35.jpg) Субвалентные соединения Al Соединения Al(I), [Cp*Al] как лиганд R. A. Fischer, G. Frenking et al. Angew. Chem. Int. Ed. Engl. 1997, 36, 70. A. H. Cowley et al. J. Am. Chem. Soc. 2000, 122, 950. M. T. Gamer, P. W. Roesky, S. N. Konchenko, P. Nava, R. Ahlrichs, Angew. Chem. , Int. Ed. 2006, 45, 4447 -4451.
Субвалентные соединения Al Соединения Al(I), [Cp*Al] как лиганд R. A. Fischer, G. Frenking et al. Angew. Chem. Int. Ed. Engl. 1997, 36, 70. A. H. Cowley et al. J. Am. Chem. Soc. 2000, 122, 950. M. T. Gamer, P. W. Roesky, S. N. Konchenko, P. Nava, R. Ahlrichs, Angew. Chem. , Int. Ed. 2006, 45, 4447 -4451.
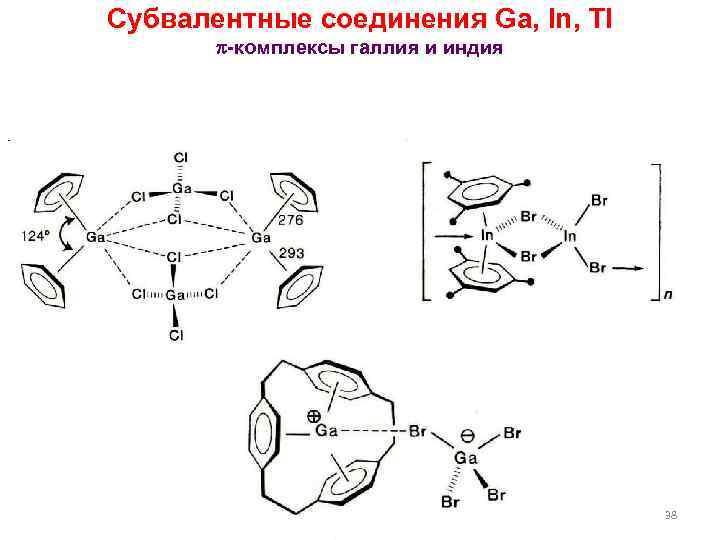 Субвалентные соединения Ga, In, Tl -комплексы галлия и индия 38
Субвалентные соединения Ga, In, Tl -комплексы галлия и индия 38
 Субвалентные соединения Ga, In, Tl Соединения Ga(I), In(I), Tl(I), 39
Субвалентные соединения Ga, In, Tl Соединения Ga(I), In(I), Tl(I), 39
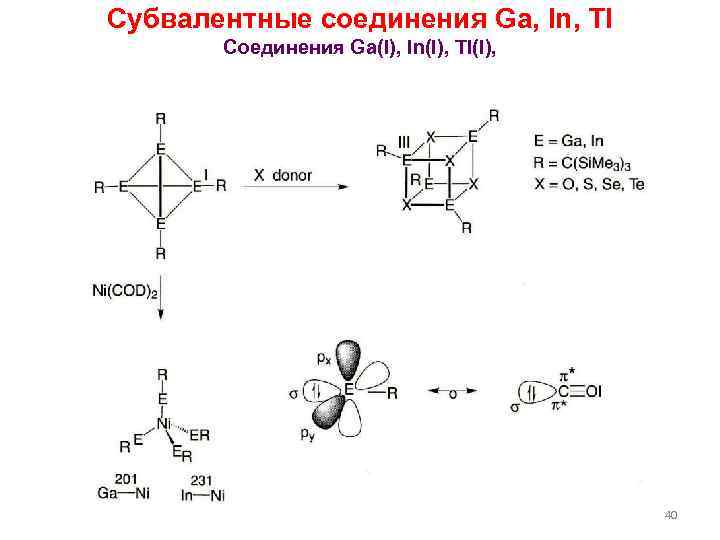 Субвалентные соединения Ga, In, Tl Соединения Ga(I), In(I), Tl(I), 40
Субвалентные соединения Ga, In, Tl Соединения Ga(I), In(I), Tl(I), 40
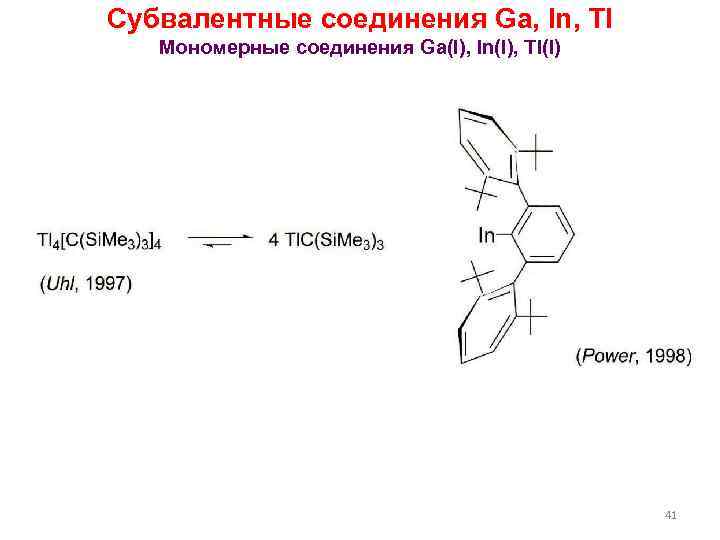 Субвалентные соединения Ga, In, Tl Мономерные соединения Ga(I), In(I), Tl(I) 41
Субвалентные соединения Ga, In, Tl Мономерные соединения Ga(I), In(I), Tl(I) 41
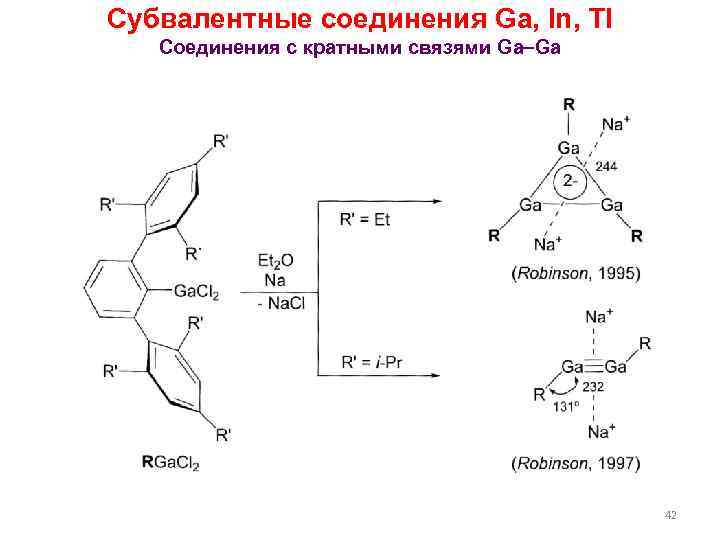 Субвалентные соединения Ga, In, Tl Соединения с кратными связями Ga Ga 42
Субвалентные соединения Ga, In, Tl Соединения с кратными связями Ga Ga 42
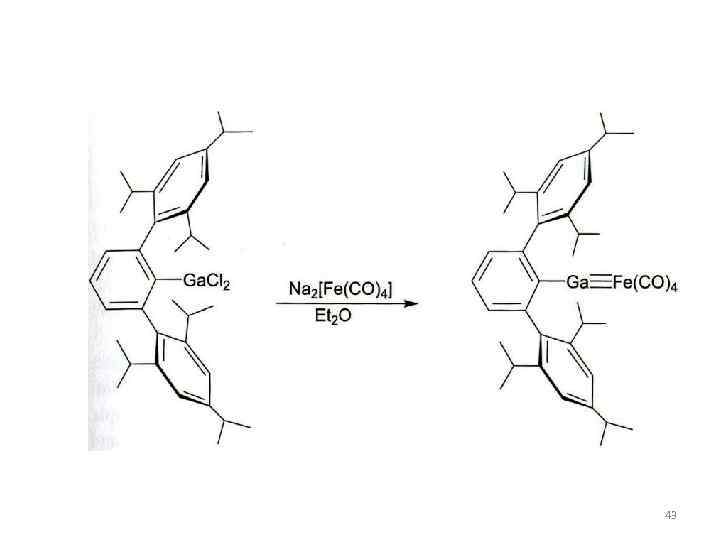 43
43
 Соединения Ga(III), In(III), Tl(III) методы синтеза 44
Соединения Ga(III), In(III), Tl(III) методы синтеза 44
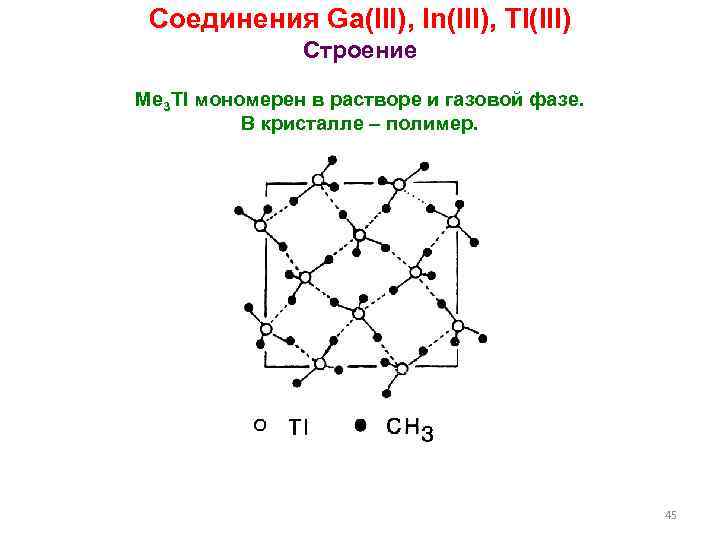 Соединения Ga(III), In(III), Tl(III) Строение Me 3 Tl мономерен в растворе и газовой фазе. В кристалле – полимер. 45
Соединения Ga(III), In(III), Tl(III) Строение Me 3 Tl мономерен в растворе и газовой фазе. В кристалле – полимер. 45
![Соединения Ga(III), In(III), Tl(III) Катион [R 2 Tl]+ - линейная частица сильное основание! 46 Соединения Ga(III), In(III), Tl(III) Катион [R 2 Tl]+ - линейная частица сильное основание! 46](https://present5.com/presentation/5652994_164495112/image-44.jpg) Соединения Ga(III), In(III), Tl(III) Катион [R 2 Tl]+ - линейная частица сильное основание! 46
Соединения Ga(III), In(III), Tl(III) Катион [R 2 Tl]+ - линейная частица сильное основание! 46
![Соединения Al(III) Катион [R 2 Al]+ В случае алюминия [R 2 M]+ возможен либо Соединения Al(III) Катион [R 2 Al]+ В случае алюминия [R 2 M]+ возможен либо](https://present5.com/presentation/5652994_164495112/image-45.jpg) Соединения Al(III) Катион [R 2 Al]+ В случае алюминия [R 2 M]+ возможен либо с краун-эфирами, либо в -комплексах 47
Соединения Al(III) Катион [R 2 Al]+ В случае алюминия [R 2 M]+ возможен либо с краун-эфирами, либо в -комплексах 47


