7 соединения меди, серебра, железа.pptx
- Количество слайдов: 23

Соединения меди, серебра, железа

Распространение в природе Медь – медный блеск – Cu 2 S, медный колчедан – Cu. Fe. S 2, малахит – Cu. CO 3 • Cu(OH)2 Серебро серебряный блеск или аргентит Ag 2 S Железо –магнитный железняк – Fe 3 O 4 мелантерит Fe. SO 4 • 7 Н 2 O Соединения меди Меди сульфат Cupri sulfas Cu. SO 4 · 5 Н 2 O Меди (II) сульфат

Получение 1. Из металлической меди действием кислоты серной в присутствии окислителей – кислорода воздуха или азотной кислоты 2 Cu+2 H 2 SO 4+O 2→ 2 Cu. SO 4+2 H 2 O 3 Cu+3 H 2 SO 4+2 HNO 3 → 3 Cu. SO 4+4 H 2 O+2 NO↑ 2. Растворением меди (II) оксида в кислоте серной Cu. O + H 2 SO 4 → Cu. SO 4 + H 2 O Гидролиз в водных растворах 2 Cu. SO 4 + 2 Н 2 O ←→ Cu 2(OH)2 SO 4 + H 2 SO 4 При нагреваниии до 1200 Cu. SO 4 • H 2 O – слегка голубоватого цвета порошок Безводный Cu. SO 4 – белый порошок

Подлинность 1. Реакция осаждения раствором аммиака 2 Cu. SO 4 + 2 NH 4 OH → Cu 2(OH)2 SO 4↓ + (NH 4)2 SO 4 эквив. голубой осадок Cu 2(OH)2 SO 4 + 6 NH 4 OH + (NH 4)2 SO 4→ избыток 2 [Cu(NH 3)4]SO 4 + 8 НO темно синий 2. Реакция восстановления меди (II) до металлической меди Cu. SO 4 + Fe → Cu↓ + Fe. SO 4 Cu 2++2 e→Cu 0 3. Реакция на SO 42 ион (ГФ катионы анионы).

3. Реакция осаждения раствором натрия гидроксида: Cu. SO 4 + 2 Na. OH → Cu(OH)2↓+ Na 2 SO 4 эквив. синий осадок Cu(OH)2 + 2 Na. OH→Na 2[Cu(OH)4] избыток синий раствор Cu(OH)2 + 2 НСl → Cu. Cl 2 + 2 Н 2 O 4. Реакция осаждения натрия сульфидом. Cu. SO 4 + Na 2 S → Cu. S↓+ Na 2 SO 4 черный осадок 5. Реакция осаждения калия гексацианоферратом (II) 2 Cu. SO 4 + K 4[Fe(CN)6] →Cu 2[Fe(CN)6]↓ + 2 K 2 SO 4 красно коричневый осадок
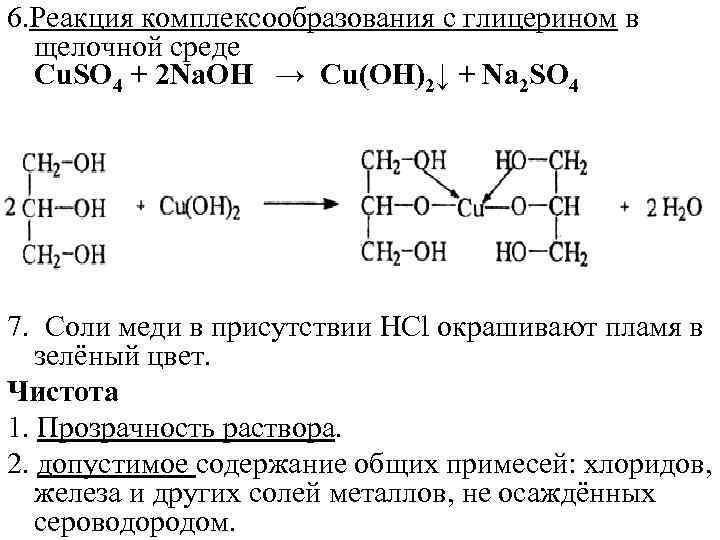
6. Реакция комплексообразования с глицерином в щелочной среде Cu. SO 4 + 2 Na. OH → Cu(OH)2↓ + Na 2 SO 4 7. Соли меди в присутствии HCl окрашивают пламя в зелёный цвет. Чистота 1. Прозрачность раствора. 2. допустимое содержание общих примесей: хлоридов, железа и других солей металлов, не осаждённых сероводородом.

Количественное определение 1. ФС йодометрический метод. Способ титрования – косвенный. . Йод оттитровывают Na 2 S 2 O 3, индикатор – крахмал. В кислой среде Н 2 SO 4 2 Cu. SO 4+4 KI → 2 Cu. I 2+2 K 2 SO 4 2 Cu. I 2 → 2 Cu. I↓+I 2 осадок белого цвета суммарно 2 Cu. SO 4 + 4 KI → I 2 + 2 Cul↓+ 2 K 2 SO 4 I 2+2 Na 2 S 2 O 3 → 2 Na. I+Na 2 S 4 O 6 2 Cu. SO 4→ 1 молекула I 2 → 2 молекулы. Na 2 S 2 O 3

fэкв. =1 ·1(РЧ); М. э=М. м. ; Допустимые пределы количественного содержания – 98% и 101% предел выветривания. 2. Комплексонометрический метод. Прямое титрование в среде ацетатного буфера, индикатор ксиленоловый оранжевый (см. висмут). f (меди (II) сульфата) =1 =1 ·1(РЧ); М. э=М. м. ; Формы выпуска «Олиговит» , «Компливит» и др.

СОЕДИНЕНИЯ СЕРЕБРА Серебра нитрат Silver Nitrate (MHH) Ag. NO 3 Argenti nitras (ЛH) Получение 3 Ag + 4 HNO 3 → 3 Ag. N 03 + NO↑+ 2 Н 2 O Ag • Cu+4 HNO 3→ Ag. NO 3+Cu(NO 3)2+NO↑+2 H 2 O Ag. NO 3+HСl→ Ag. Cl↓+HNO 3 2 Ag. Cl+Zn+H 2 SO 4→ 2 Ag↓+Zn. SO 4+2 HCl 3 Ag+4 HNO 3→ 3 Ag. NO 3+NO↑+2 H 2 O Подлинность Ион серебра 1. реакция «серебряного зеркала» Ag. NO 3 + 2 NH 4 OH →[Ag(NH 3)2]NO 3 + 2 Н 20

2. Реакция осаждения кислотой хлороводородной Ag. NO 3 + HCl → Ag. Cl↓+HNO 3 Ag. Cl + 2 NH 4 OH→[Ag(NH 3)]Cl + 2 Н 2 O 3. Реакция осаждения раствором натрия гидроксида или раствором аммиака: 2 Ag. N 03 + 2 NH 4 OH → Ag 2 O↓ + 2 NH 4 NO 3 Черный осадок Ag 2 O + 4 NH 4 OH → 2[Ag(NH 3)2]OH +ЗН 2 O 4. Реакция на нитрат ион с раствором дифениламина 5. с раствором Fe. SO 4 в среде концентрированной H 2 SO 4 образование бурого кольца
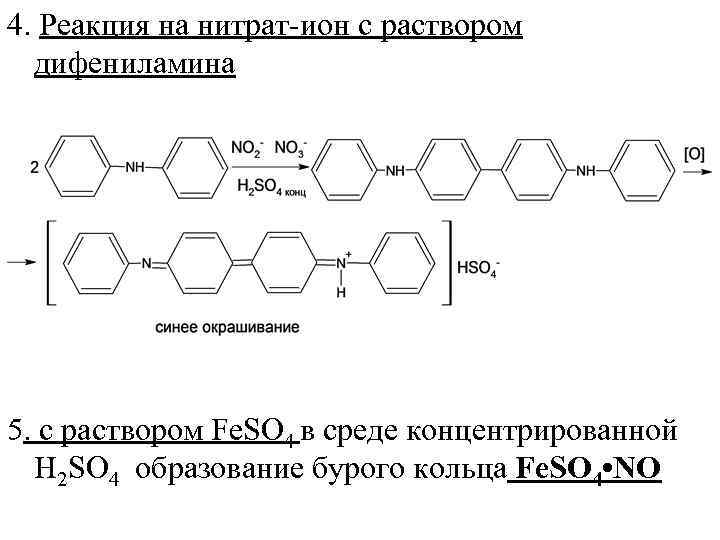
4. Реакция на нитрат ион с раствором дифениламина 5. с раствором Fe. SO 4 в среде концентрированной H 2 SO 4 образование бурого кольца Fe. SO 4 • NO

2 Ag. NO 3+H 2 SO 4→Ag 2 SO 4+2 HNO 3+3 H 2 SO 4+6 Fe. SO 4→ 3 Fe 2(SO 4)3+2 NO↑+4 H 2 O Fe. SO 4+NO→Fe. SO 4 • NO Чистота 1. Кислотность. По индикатору – м/ красному. 2. недопустимые примеси солей висмута, меди, свинца. При добавлении избытка NH 4 OH– раствор должен остаться бесцветным и прозрачным. Ag. NO 3 + 2 NH 4 OH→[Ag(NH 3)2]NO 3 + 2 Н 2 O Cu 2+ + 4 NH 4 OH → [Cu(NH 3)4]2+ + 4 Н 2 O cиний раствор Bi 3+ + 3 NH 4 OH→Bi(OH)3↓ + 3 NH 4+ белый Pb 2+ + 2 NH 4 OH → Pb(OH)2↓ + 2 NH 4+ белый

Количественное определение ФС Метод тиоцианометрии. прямое титрования. Индикатор железоаммонийные квасцы. Среда азотнокислая (для предотвращения гидролиза индикатора). Титрант – раствор роданида амммония Ag. NO 3 + NH 4 SCN→Ag. SCN↓ + NH 4 NO 3 белый осадок Fe(NH 4)(SO 4)2 + 3 NH 4 SCN → Fe(SCN)3 + 2(NH 4)2 SO 4 розовое окрашивание f(серебра нитрата) =1 Применение от 0, 05 до 0, 06% вяжущее, от 2 до 10% прижигающее, ВРД внутрь – 0, 03 г. ВСД – 0, 1 г. Все растворы Ag. NO 3 в условиях аптек подвергаются полному химическому контролю.

Коллоидные соединения серебра Колларгол - Col. Iargolum Содержит не менее 70% серебра Протаргол - Protargolum Содержит не менее 8% серебра ЛВ содержат неионизированное коллоидное серебро, связанное с белками (натриевые соли лизальбиновой и протальбиновой кислот) Получение из серебра нитрата и белков. Отличаются: протаргол содержит 7, 8 8, 3%; колларгол – не менее 70% серебра.
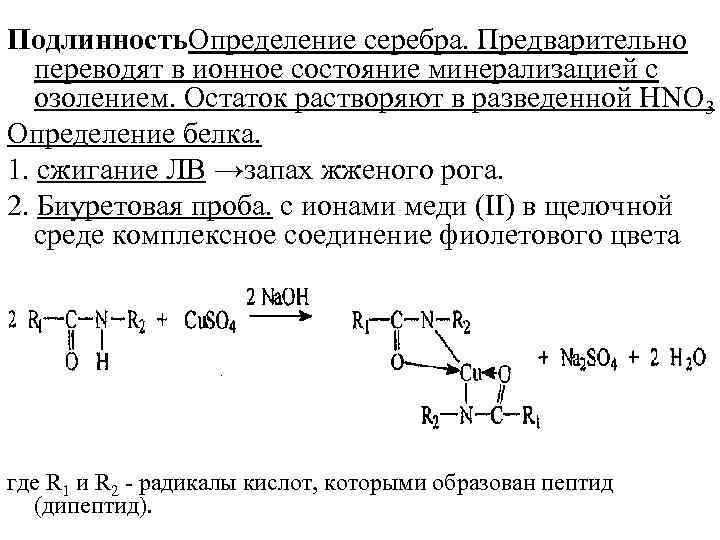
Подлинность. Определение серебра. Предварительно переводят в ионное состояние минерализацией с озолением. Остаток растворяют в разведенной НNO 3 Определение белка. 1. сжигание ЛB →запах жженого рога. 2. Биуретовая проба. с ионами меди (II) в щелочной среде комплексное соединение фиолетового цвета где R 1 и R 2 радикалы кислот, которыми образован пептид (дипептид).

Реакция отличия реакция образования серебролизальбиновой кислоты с НСI. У коралларгола тёмно-бурый осадок растворимый в Nа. ОН. У протаргола нет. Количественное определение мeтод тиоцианометрии предварительно минерализация в колбе Кельдаля кипячение в смеси HNO 3 конц+ H 2 SO 4 конц f(Ag) =1. Стандартизация ЛВ проводится по содержанию в них серебра.

СОЕДИНЕНИЯ ЖЕЛЕЗА (II) Соединения железа Железа (II) сульфат Ferri (II) sulfas (ЛH) Fe. SO 4 · 7 Н 2 O Ferrous sulfate (MHH) Получение Fe + H 2 SO 4 → Fe. SO 4 + H 2↑ Водные растворы слабо кислая реакция среды, гидролиз 2 Fe. SO 4 + H 2 O ←→ Fe 2(OH)2 SO 4 + H 2 SO 4 Химические свойства Fe. SO 4 + NH 4 OH→ Fe(OH)2↓ +(NH 4)2 SO 4 4 Fe (OH)2 + O 2 + 2 H 2 O → 4 Fe(OH)3↓

Подлинность 1. Реакция осаждения калия гексацианоферратом (III). 3 Fe. SО 4 + 2 K 3[Fe(CN)6] → Fe 3[Fe(CN)6]2↓ + 6 КСl синий осадок 2. Реакция осаждения аммония сульфидом. Fe. SO 4 + (NH 4)2 S → Fe. S↓ + (NH 4)2 SO 4 черный осадок 3. Реакция осаждения раствором натрия гидроксида или раствором аммиака: Fe. SO 4 + 2 Na. OH → Fe(OH)2↓ + Na 2 SO 4 белый осадок 4 Fe(OH) 2 + O 2 + 2 Н 2 О→ 4 Fe(OH)3↓ красно коричневый осадок

чистота 1. допустимые в пределах эталона общие примеси: хлориды, цинк, мышьяк. 2. недопустимые А) сульфиды Б) соли меди Количественное определение 1. ФС Перманганатометрический метод. Вариант прямого титрования. без индикатора до устойчивой (30 секунд) розовой окраски. 10 Fe. SO 4 + 2 КМn. O 4 + 8 H 2 SO 4 → 5 Fe 2(SO 4)3 + 2 Mn. SO 4 + K 2 SO 4 + 8 Н 2 O (Fe 2+ 1ē —> Fe 3+) Кст. =10/2=5 Титрант УЧ ⅕ КМn. О 4 fэкв. =Кст. • УЧ (титранта) fэкв. = 10/2 • 1/5 = 1 М. э=М. м.
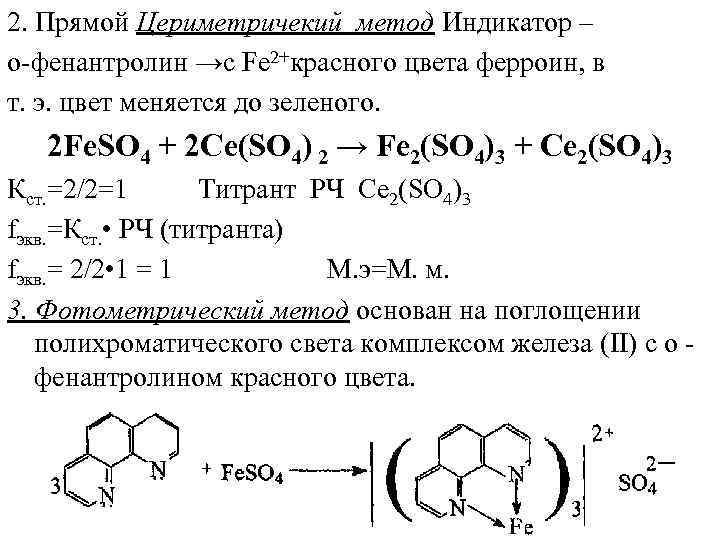
2. Прямой Цериметричекий метод Индикатор – о фенантролин →с Fe 2+красного цвета ферроин, в т. э. цвет меняется до зеленого. 2 Fe. SO 4 + 2 Ce(SO 4) 2 → Fe 2(SO 4)3 + Ce 2(SO 4)3 Кст. =2/2=1 Титрант РЧ Ce 2(SO 4)3 fэкв. =Кст. • РЧ (титранта) fэкв. = 2/2 • 1 = 1 М. э=М. м. 3. Фотометрический метод основан на поглощении полихроматического света комплексом железа (II) с о фенантролином красного цвета.
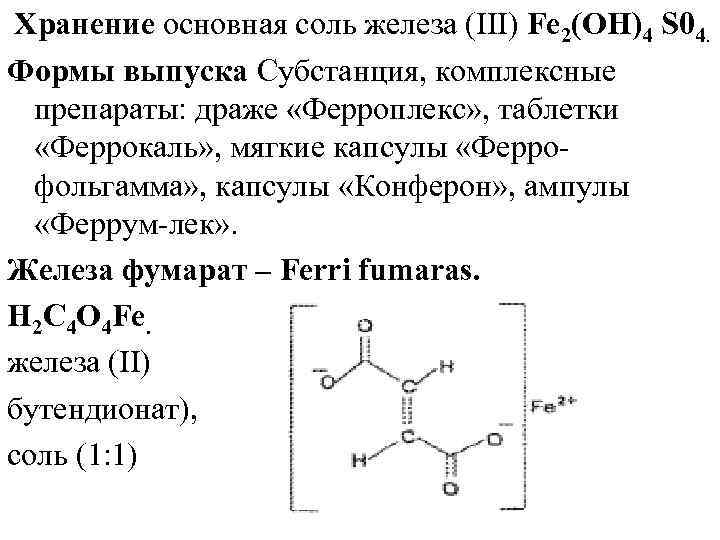
Хранение основная соль железа (III) Fe 2(OH)4 S 04. Формы выпуска Субстанция, комплексные препараты: драже «Ферроплекс» , таблетки «Феррокаль» , мягкие капсулы «Ферро фольгамма» , капсулы «Конферон» , ампулы «Феррум лек» . Железа фумарат – Ferri fumaras. H 2 C 4 O 4 Fe. железа (II) бутендионат), соль (1: 1)

Подлинность Ион железа (II) – см. железа сульфат Фумарат ион – ИК спектр Количественное определение Прямое цериметрическое титрование. Индикатор – о фенантролин. От красного до зеленого Fe 2++Ce(SO 4)2 →Fe 3++Ce 2(SO 4)3 Железа глюконат – Ferri gluconas. [H 11 C 6 O 7]2 Fe • 2 H 2 O. железа (II) D – глюконат (2: 1) дигидрат

Подлинность Ион железа (II) – см. железа сульфат. Глюконат – ион 1. Реакция солеобразования с железа (III) хлоридом – светло зеленое окрашивание 3(CH 2 OH – (CHOH)4 – COO)2 Fe + 2 Fe. Cl 3 → → 2(CH 2 OH – (CHOH)4) – COO)3 Fe + 3 Fe. Cl 2 2. ТСХ. Количественное определение Прямое цериметрическое титрование Индикатор – о фенантролин. От красного до зеленого
7 соединения меди, серебра, железа.pptx