Livshitz 6.ppt
- Количество слайдов: 20

СОДЕРЖАНИЕ РАБОТЫ 1 Исследование структуры и динамики супрамолекулярных комплексов на основе циклодекстринов (ЦД). 2 Изучение комплексов ЦД со спин-мечеными аналогами холестерина и влияния ЦД на структуру и динамику холестеринсодержащих мембран. 3 Исследование динамики комплексов ЦД, ковалентно связанных с микрочастицами силикагеля. Модель хемосенсорной системы.
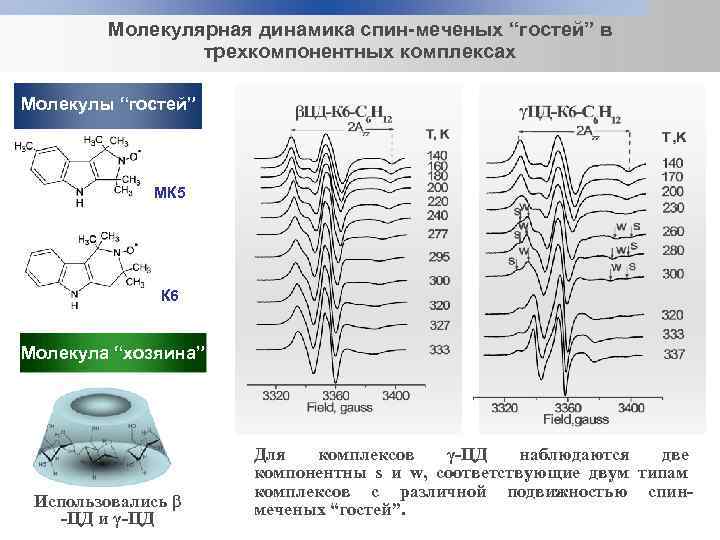
Молекулярная динамика спин-меченых “гостей” в трехкомпонентных комплексах Молекулы “гостей” МК 5 К 6 Молекула “хозяина” Использовались β -ЦД и γ-ЦД Для комплексов γ-ЦД наблюдаются две компонентны s и w, соответствующие двум типам комплексов с различной подвижностью спинмеченых “гостей”.
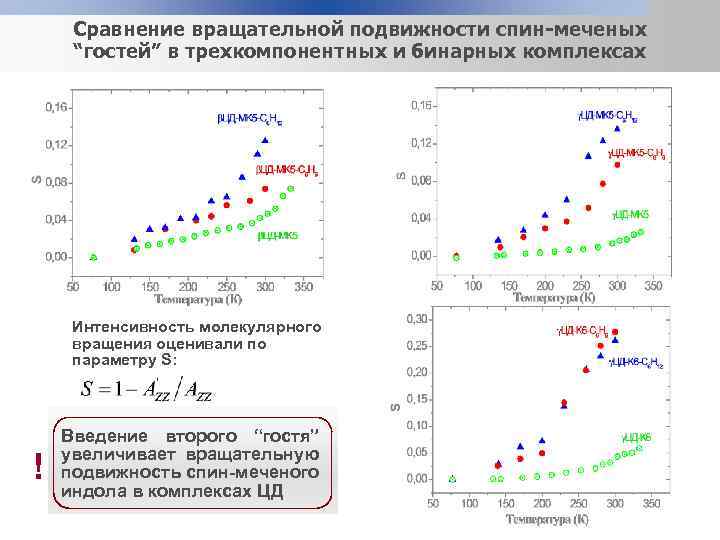
Сравнение вращательной подвижности спин-меченых “гостей” в трехкомпонентных и бинарных комплексах Интенсивность молекулярного вращения оценивали по параметру S: ! Введение второго “гостя” увеличивает вращательную подвижность спин-меченого индола в комплексах ЦД
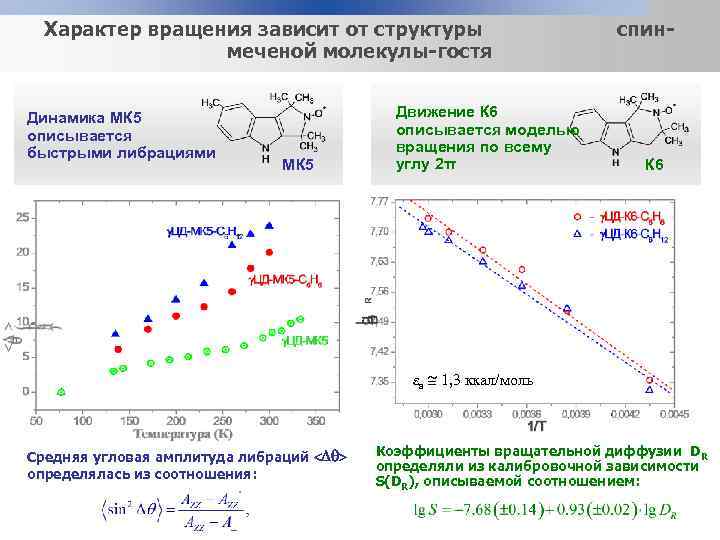
Характер вращения зависит от структуры меченой молекулы-гостя Динамика МК 5 описывается быстрыми либрациями МК 5 Движение К 6 описывается моделью вращения по всему углу 2π спин- К 6 εа 1, 3 ккал/моль Средняя угловая амплитуда либраций определялась из соотношения: Коэффициенты вращательной диффузии DR определяли из калибровочной зависимости S(DR), описываемой соотношением:
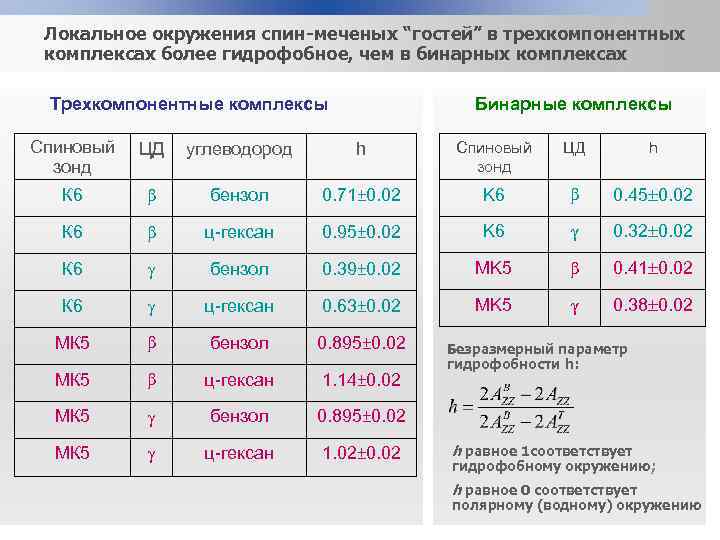
Локальное окружения спин-меченых “гостей” в трехкомпонентных комплексах более гидрофобное, чем в бинарных комплексах Трехкомпонентные комплексы Бинарные комплексы Спиновый зонд ЦД углеводород h Спиновый зонд ЦД h К 6 β бензол 0. 71± 0. 02 K 6 β 0. 45 0. 02 К 6 β ц-гексан 0. 95± 0. 02 K 6 γ 0. 32 0. 02 К 6 бензол 0. 39± 0. 02 MK 5 β 0. 41 0. 02 К 6 ц-гексан 0. 63± 0. 02 MK 5 γ 0. 38 0. 02 МК 5 β бензол 0. 895± 0. 02 МК 5 β ц-гексан 1. 14± 0. 02 МК 5 бензол 0. 895± 0. 02 МК 5 ц-гексан 1. 02± 0. 02 Безразмерный параметр гидрофобности h: h равное 1 соответствует гидрофобному окружению; h равное 0 соответствует полярному (водному) окружению
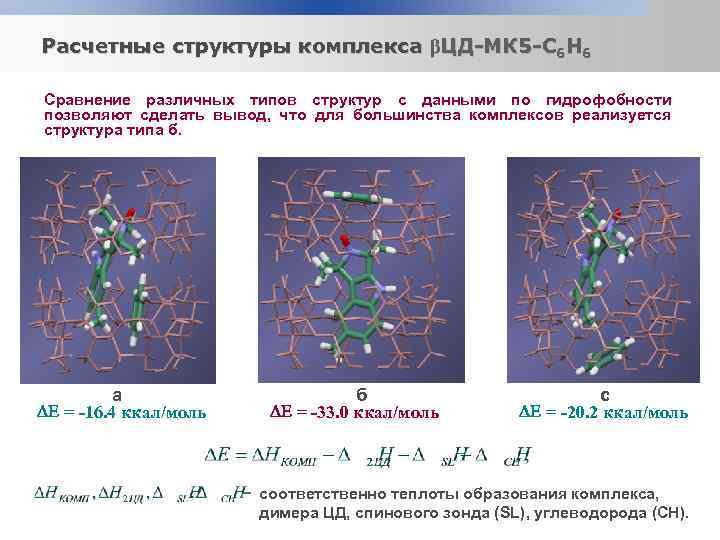
Расчетные структуры комплекса βЦД-МК 5 -С 6 Н 6 Сравнение различных типов структур с данными по гидрофобности позволяют сделать вывод, что для большинства комплексов реализуется структура типа б. а = -16. 4 ккал/моль б = -33. 0 ккал/моль с = -20. 2 ккал/моль соответственно теплоты образования комплекса, димера ЦД, спинового зонда (SL), углеводорода (СН).
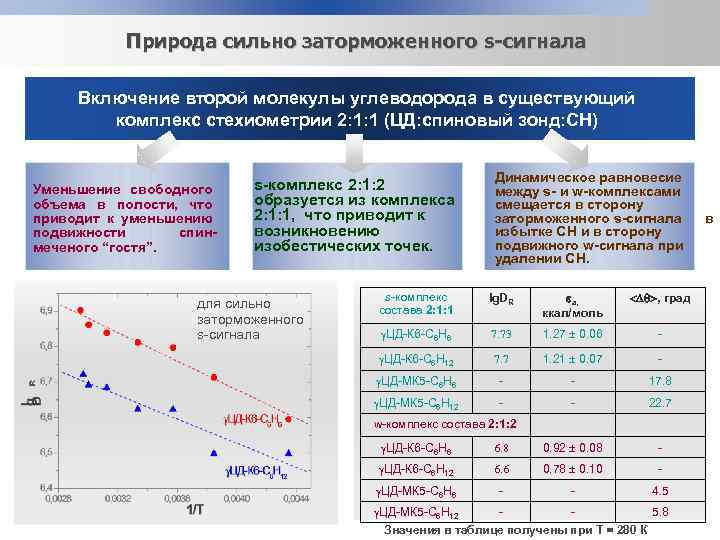
Природа сильно заторможенного s-сигнала Включение второй молекулы углеводорода в существующий комплекс стехиометрии 2: 1: 1 (ЦД: спиновый зонд: CH) Уменьшение свободного объема в полости, что приводит к уменьшению подвижности спинмеченого “гостя”. s-комплекс 2: 1: 2 образуется из комплекса 2: 1: 1, что приводит к возникновению изобестических точек. для сильно заторможенного s-сигнала Динамическое равновесие между s- и w-комплексами смещается в сторону заторможенного s-сигнала избытке CH и в сторону подвижного w-сигнала при удалении CH. s-комплекс состава 2: 1: 1 lg. DR a, ккал/моль , град ЦД-К 6 -С 6 Н 6 7. 73 1. 27 0. 06 - ЦД-К 6 -С 6 Н 12 7. 7 1. 21 0. 07 - ЦД-МК 5 -С 6 Н 6 - - 17. 8 ЦД-МК 5 -С 6 Н 12 - - 22. 7 w-комплекс состава 2: 1: 2 ЦД-К 6 -С 6 Н 6 6. 8 0. 92 0. 08 - ЦД-К 6 -С 6 Н 12 6. 6 0. 78 0. 10 - ЦД-МК 5 -С 6 Н 6 - - 4. 5 ЦД-МК 5 -С 6 Н 12 5. 8 Значения в таблице получены при Т = 280 К в
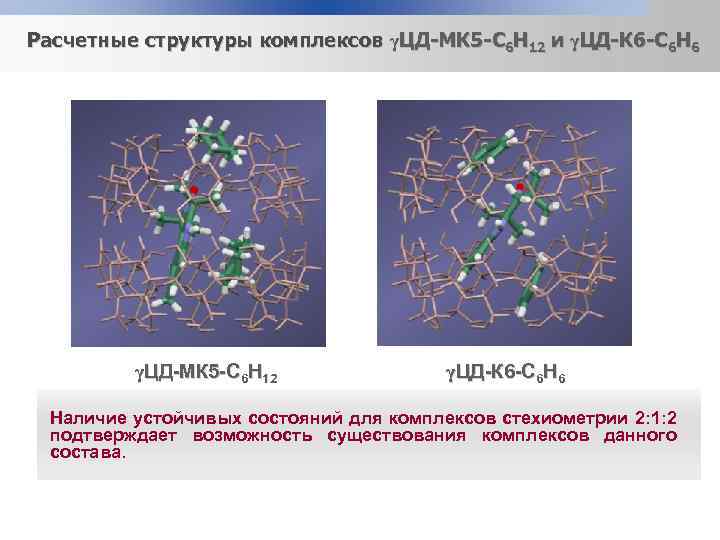
Расчетные структуры комплексов γЦД-МК 5 -С 6 Н 12 и γЦД-К 6 -С 6 Н 6 γЦД-МК 5 -С 6 Н 12 γЦД-К 6 -С 6 Н 6 Наличие устойчивых состояний для комплексов стехиометрии 2: 1: 2 подтверждает возможность существования комплексов данного состава.
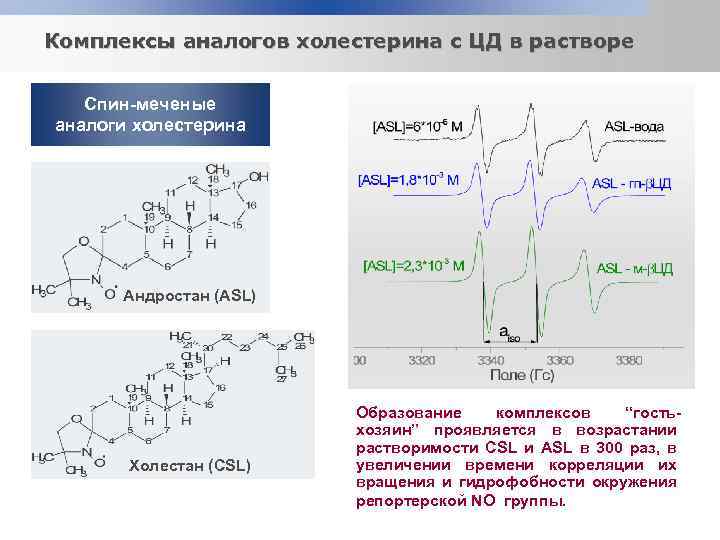
Комплексы аналогов холестерина с ЦД в растворе Спин-меченые аналоги холестерина Андростан (ASL) Холестан (СSL) Образование комплексов “гостьхозяин” проявляется в возрастании растворимости CSL и ASL в 300 раз, в увеличении времени корреляции их вращения и гидрофобности окружения репортерской NO группы.
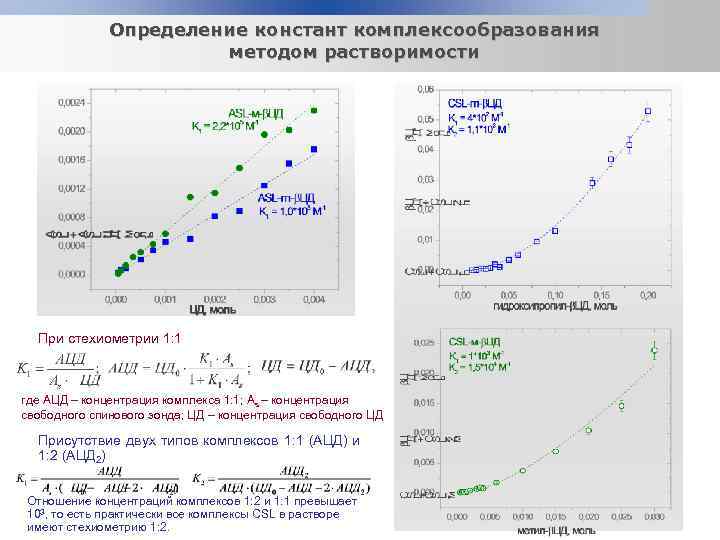
Определение констант комплексообразования методом растворимости При стехиометрии 1: 1 где AЦД – концентрация комплекса 1: 1; As – концентрация свободного спинового зонда; ЦД – концентрация свободного ЦД Присутствие двух типов комплексов 1: 1 (АЦД) и 1: 2 (АЦД 2) Отношение концентраций комплексов 1: 2 и 1: 1 превышает 103, то есть практически все комплексы CSL в растворе имеют стехиометрию 1: 2.

Спиновый обмен с парамагнитными ионами и гидрофобность окружения ASL и CSL в комплексах c ЦД Комплекс h eff(нс) kex (с-1 М-1) ASL-H 2 O 0 0. 42 5. 05·108 ASL–гп-βЦД 0. 3 0. 7 4. 2·107 ASL–м-βЦД 0. 38 0. 49 1. 8·107 СSL–гп-βЦД 0. 36 1. 62 7. 6·107 СSL–м-βЦД 0. 38 0. 88 2. 85·107 Изучение скорости спинового обмена с ионами Ni 2+ и гидрофобности окружения показывает, что NO группа спин-меченых молекул-гостей локализована внутри полости ЦД.
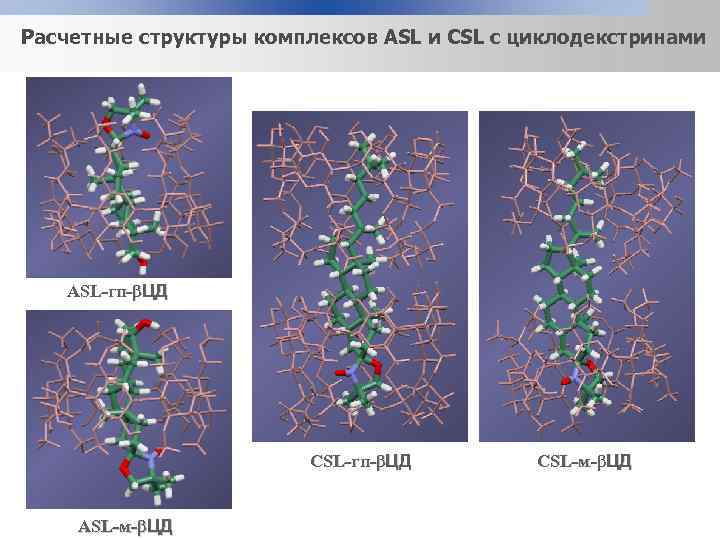
Расчетные структуры комплексов ASL и CSL с циклодекстринами ASL-гп-βЦД СSL-гп-βЦД ASL-м-βЦД СSL-м-βЦД
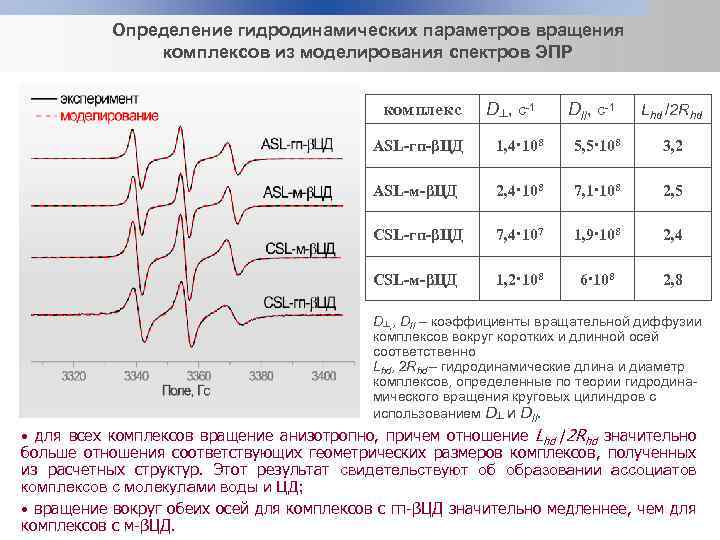
Определение гидродинамических параметров вращения комплексов из моделирования спектров ЭПР комплекс D┴, c-1 D//, c-1 Lhd /2 Rhd ASL-гп-βЦД 1, 4·108 5, 5·108 3, 2 ASL-м-βЦД 2, 4·108 7, 1·108 2, 5 CSL-гп-βЦД 7, 4·107 1, 9·108 2, 4 CSL-м-βЦД 1, 2·108 6·108 2, 8 D┴, , D// – коэффициенты вращательной диффузии комплексов вокруг коротких и длинной осей соответственно Lhd, 2 Rhd – гидродинамические длина и диаметр комплексов, определенные по теории гидродинамического вращения круговых цилиндров с использованием D┴ и D//. • для всех комплексов вращение анизотропно, причем отношение Lhd /2 Rhd значительно больше отношения соответствующих геометрических размеров комплексов, полученных из расчетных структур. Этот результат свидетельствуют об образовании ассоциатов комплексов с молекулами воды и ЦД; • вращение вокруг обеих осей для комплексов с гп-βЦД значительно медленнее, чем для комплексов с м-βЦД.
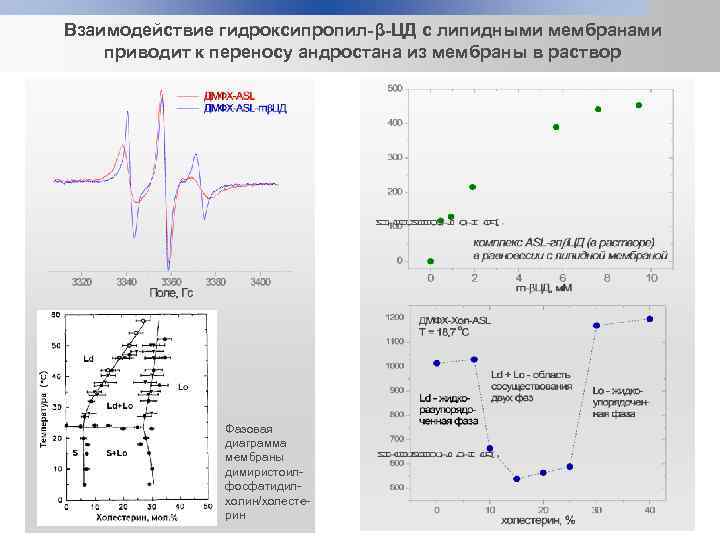
Взаимодействие гидроксипропил-β-ЦД с липидными мембранами приводит к переносу андростана из мембраны в раствор Фазовая диаграмма мембраны димиристоилфосфатидилхолин/холестерин
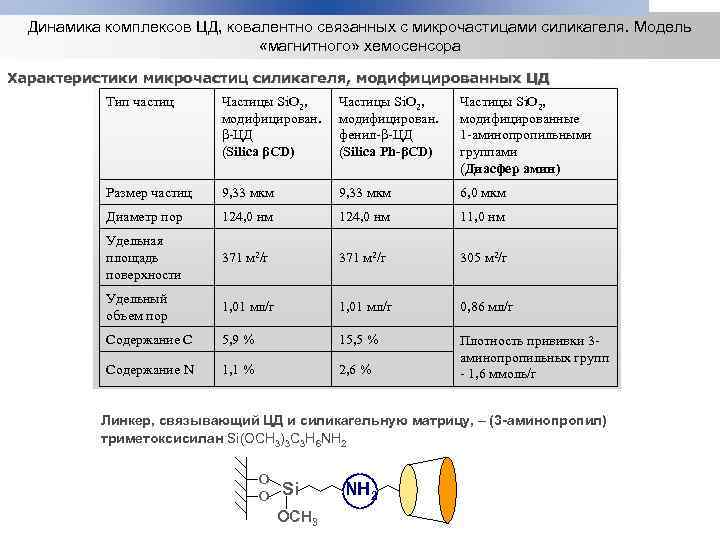
Динамика комплексов ЦД, ковалентно связанных с микрочастицами силикагеля. Модель «магнитного» хемосенсора Характеристики микрочастиц силикагеля, модифицированных ЦД Тип частиц Частицы Si. O 2, модифицирован. β-ЦД (Silica βCD) Частицы Si. O 2, модифицирован. фенил-β-ЦД (Silica Ph-βCD) Частицы Si. O 2, модифицированные 1 -аминопропильными группами (Диасфер амин) Размер частиц 9, 33 мкм 6, 0 мкм Диаметр пор 124, 0 нм 11, 0 нм Удельная площадь поверхности 371 м 2/г 305 м 2/г Удельный объем пор 1, 01 мл/г 0, 86 мл/г Содержание С 5, 9 % 15, 5 % Содержание N 1, 1 % 2, 6 % Плотность прививки 3 аминопропильных групп - 1, 6 ммоль/г Линкер, связывающий ЦД и силикагельную матрицу, – (3 -аминопропил) триметоксисилан Si(OСН 3)3 C 3 H 6 NH 2 о о Si OCH 3 NH 2
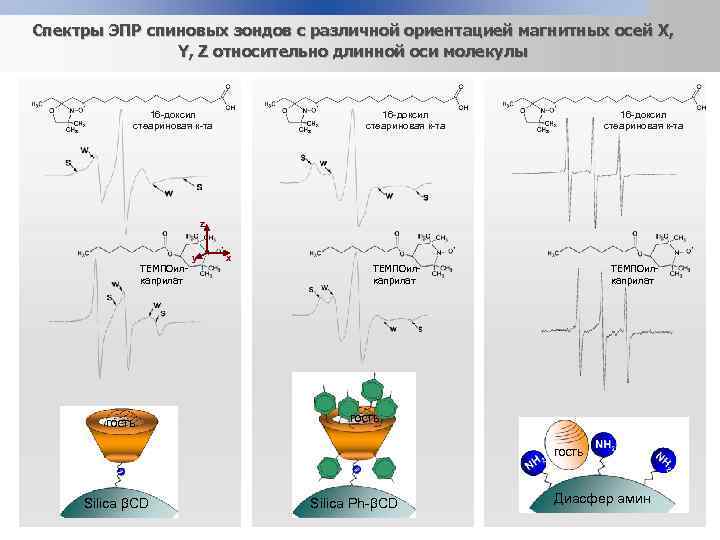
Спектры ЭПР спиновых зондов с различной ориентацией магнитных осей X, Y, Z относительно длинной оси молекулы 16 -доксил стеариновая к-та z ТЕМПОилкаприлат гость y x ТЕМПОилкаприлат гость Silica βCD Silica Ph-βCD Диасфер амин
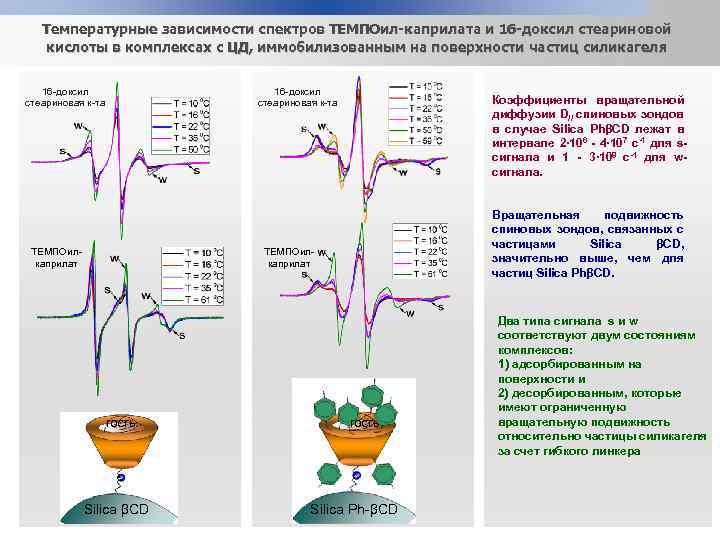
Температурные зависимости спектров ТЕМПОил-каприлата и 16 -доксил стеариновой кислоты в комплексах с ЦД, иммобилизованным на поверхности частиц силикагеля 16 -доксил стеариновая к-та ТЕМПОилкаприлат Коэффициенты вращательной диффузии D// спиновых зондов в случае Silica PhβСD лежат в интервале 2∙ 106 - 4∙ 107 с-1 для sсигнала и 1 - 3∙ 108 с-1 для wсигнала. Вращательная подвижность спиновых зондов, связанных с частицами Silica βСD, значительно выше, чем для частиц Silica PhβСD. ТЕМПОилкаприлат гость Silica βCD гость Silica Ph-βCD Два типа сигнала s и w соответствуют двум состояниям комплексов: 1) адсорбированным на поверхности и 2) десорбированным, которые имеют ограниченную вращательную подвижность относительно частицы силикагеля за счет гибкого линкера
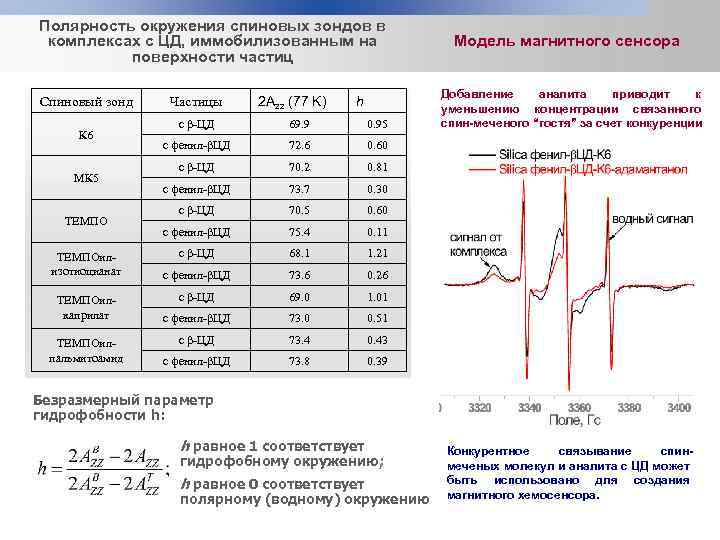
Полярность окружения спиновых зондов в комплексах с ЦД, иммобилизованным на поверхности частиц Спиновый зонд К 6 МК 5 ТЕМПОилизотиоцианат ТЕМПОилкаприлат ТЕМПОилпальмитоамид Частицы 2 Azz (77 K) h с β-ЦД 69. 9 0. 95 с фенил-βЦД 72. 6 70. 2 0. 81 с фенил-βЦД 73. 7 0. 30 с β-ЦД 70. 5 0. 60 с фенил-βЦД 75. 4 0. 11 с β-ЦД 68. 1 1. 21 с фенил-βЦД 73. 6 0. 26 с β-ЦД 69. 0 1. 01 с фенил-βЦД 73. 0 0. 51 с β-ЦД 73. 4 0. 43 с фенил-βЦД 73. 8 Добавление аналита приводит к уменьшению концентрации связанного спин-меченого “гостя” за счет конкуренции 0. 60 с β-ЦД Модель магнитного сенсора 0. 39 Безразмерный параметр гидрофобности h: h равное 1 соответствует гидрофобному окружению; h равное 0 соответствует полярному (водному) окружению Конкурентное связывание спинмеченых молекул и аналита с ЦД может быть использовано для создания магнитного хемосенсора.
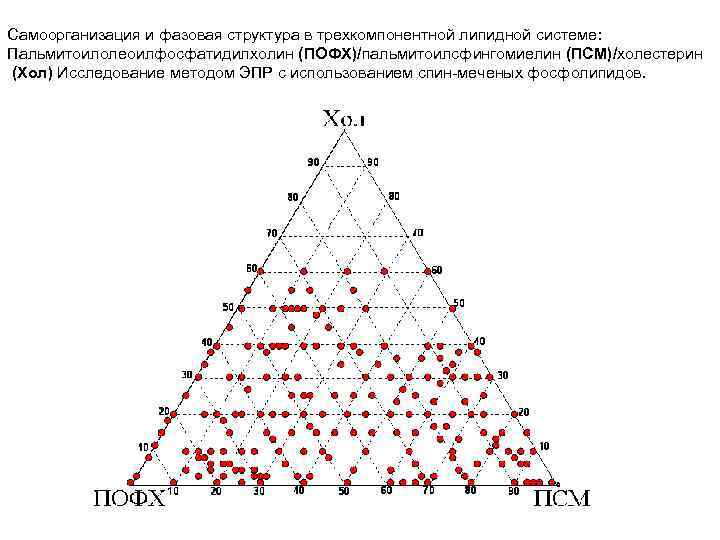
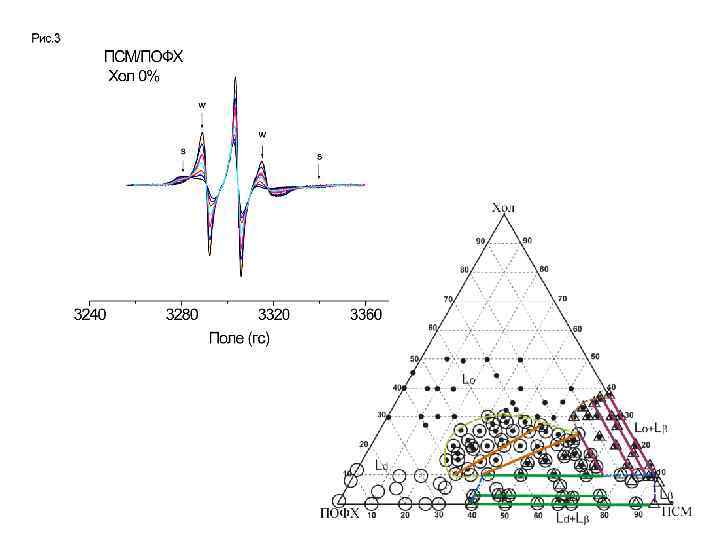
Самоорганизация и фазовая структура в трехкомпонентной липидной системе: Пальмитоилолеоилфосфатидилхолин (ПОФХ)/пальмитоилсфингомиелин (ПСМ)/холестерин (Хол) Исследование методом ЭПР с использованием спин-меченых фосфолипидов.
Livshitz 6.ppt