4.Каналы_насосы_потенциалы.ppt
- Количество слайдов: 110

Содержание Лекция № 6 Биофизика мембранных процессов мембранный транспорт ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 1

По форме молекулы мембранных липидов делятся на 2 вида: 1. Бислойные липиды – молекулы имеют форму цилиндра (объемы гидрофильной головки и гидрофобных хвостов приблизительно одинаковы). Например, фосфатидилхолин, сфингомиелин, фосфатидилинозитол. 2. Небислойные липиды 2. 1. Молекулы имеют форму опрокинутого конуса (объем гидрофильной головки превосходит объем гидрофобной части). Например, лизофосфолипиды. 2. 2. Молекулы имеют форму конуса (объем гидрофобных хвостов превосходит объем гидрофильной головки). Например, кардиолипин. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 2
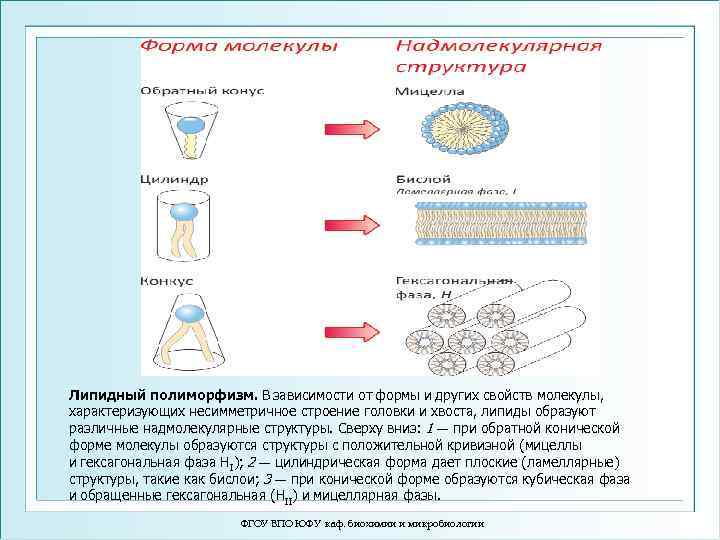
Липидный полиморфизм. В зависимости от формы и других свойств молекулы, характеризующих несимметричное строение головки и хвоста, липиды образуют различные надмолекулярные структуры. Сверху вниз: 1 — при обратной конической форме молекулы образуются структуры с положительной кривизной (мицеллы и гексагональная фаза HI); 2 — цилиндрическая форма дает плоские (ламеллярные) структуры, такие как бислои; 3 — при конической форме образуются кубическая фаза и обращенные гексагональная (HII) и мицеллярная фазы. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Основные типы структурной организации водно -липидных систем ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

3. Текучесть (микровязкость) липидной фазы биомембран регулирует мембранные процессы. В физиологических условиях липиды мембран имеют жидко-кристаллическую структуру, что необходимо для нормального функционирования. 2. Степень текучести мембран зависит от: - длины жирнокислотных цепей и степени их ненасыщенности; - соотношения фосфолипиды/стерины; - физических факторов (to , р, р. Н, потенциала) 1.

Взаимосвязь степени ненасыщенности липидных молекул и текучести мембран 1. При постоянной длине ацильной цепи и температуре, увеличение количества двойных связей повышает текучесть мембраны. 2. При постоянном количестве двойных связей и постоянной температуре, удлинение ацильной цепи уменьшает текучесть мембраны. 3. При любой комбинации длины цепей и двойных связей, увеличение температуры повышает текучесть мембраны

Гипотеза адаптационной роли мембранных липидов была выдвинута и обоснована акад. Е. М. Крепсом. В мембранных липидах быстро обнаруживаются изменения в наборе жирных кислот при смене температур и глубины обитания, а именно: понижение температуры и увеличение глубины синергично повышают содержание полиненасыщенных жирных кислот в составе мембранных липидов. Температура вдоль ноги полярного оленя от копыта до туловища зимой может меняться от − 20°С до +30°С. Клеточные мембраны у дистальной части ноги оленя содержат больше ненасыщенных фосфолипидов. Находясь на суше, императорские пингвины опираются на пятки своих лап. Это положение тела уменьшает площадь соприкосновения лап пингвинов с ледяной землей. Клеточные мембраны ноги пингвина содержат больше ненасыщенных фосфолипидов. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 7

Фазовое состояние мембранных липидов Выделяют два главных фазовых состояния мембранных липидов: 1. Твердо-кристаллическое (гель-состояние) - молекулы упорядочены, жирнокислотные ацилы в трансконформации 2. Жидко-кристаллическое – молекулы менее упорядочены, наблюдаются транс-гош-переходы. Различают: 2. 1. Жидко-кристаллическое неупорядоченное состояние (липиды свободного объема) 2. 2. Жидко-кристаллическое упорядоченное состояние (характерно для рафтов) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 8
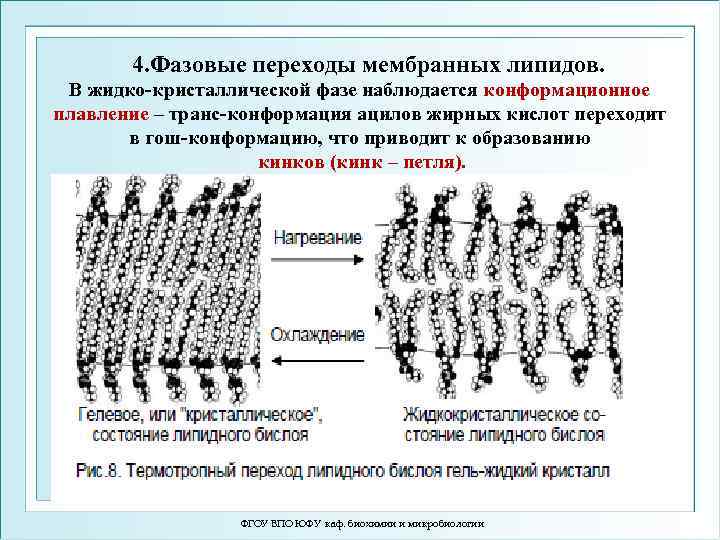
4. Фазовые переходы мембранных липидов. В жидко-кристаллической фазе наблюдается конформационное плавление – транс-конформация ацилов жирных кислот переходит в гош-конформацию, что приводит к образованию кинков (кинк – петля). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
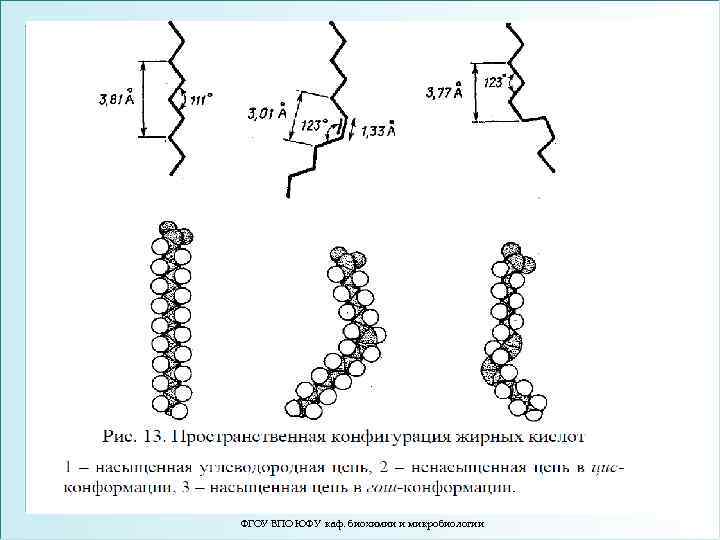
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
![[9] Гипотеза кинков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии [9] Гипотеза кинков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии](https://present5.com/presentation/19930286_335801633/image-11.jpg)
[9] Гипотеза кинков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
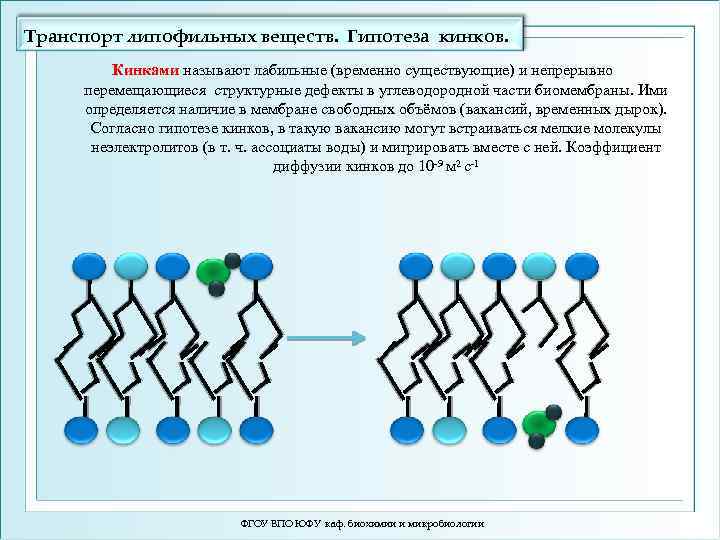
Транспорт липофильных веществ. Гипотеза кинков. Кинками называют лабильные (временно существующие) и непрерывно перемещающиеся структурные дефекты в углеводородной части биомембраны. Ими определяется наличие в мембране свободных объёмов (вакансий, временных дырок). Согласно гипотезе кинков, в такую вакансию могут встраиваться мелкие молекулы неэлектролитов (в т. ч. ассоциаты воды) и мигрировать вместе с ней. Коэффициент диффузии кинков до 10 -9 м 2 с-1 ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
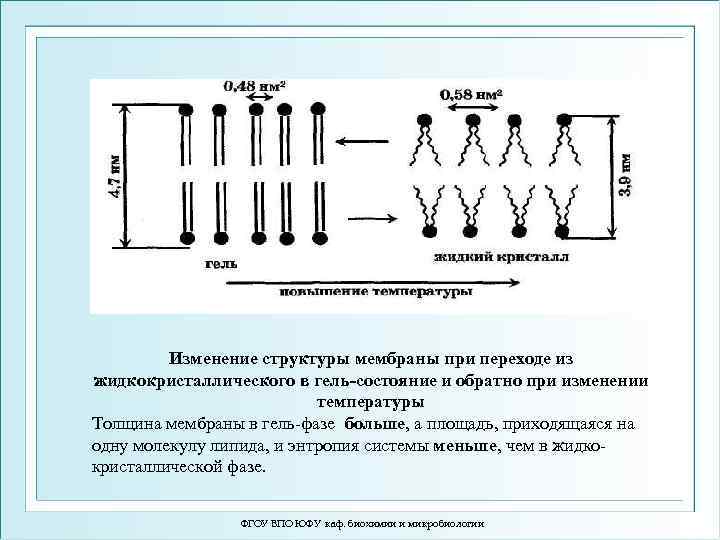
Изменение структуры мембраны при переходе из жидкокристаллического в гель-состояние и обратно при изменении температуры Толщина мембраны в гель-фазе больше, а площадь, приходящаяся на одну молекулу липида, и энтропия системы меньше, чем в жидкокристаллической фазе. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

5. Латеральная гетерогенность мембранных липидов. Латеральная гетерогенность мембраны – это свойство бислойной мембраны сложного липидного состава образовывать неоднородности (несмешиваемые микрофазы, микродомены или рафты). Мембранные рафты – это маленькие (10 -200 нм), гетерогенные и очень динамичные липидные домены, обогащенные холестеролом, сфинголипидами, специфическими белками, более структурированные и упорядоченные, чем окружающая «жидкая» фаза. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
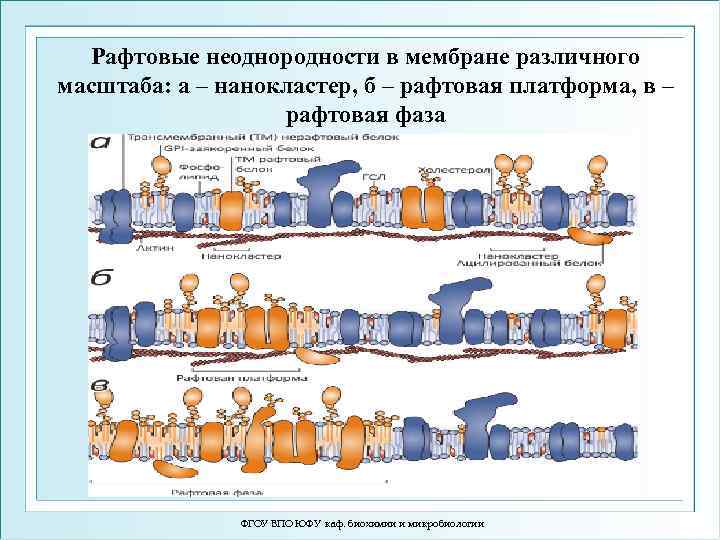
Рафтовые неоднородности в мембране различного масштаба: а – нанокластер, б – рафтовая платформа, в – рафтовая фаза ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Взаимодействие лейкоцитов с липидными рафтами ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

6. Трансбислойная асимметрия мембранных липидов – это различное распределение липидов между внутренним и наружным монослоями. 1. Во внешнем монослое локализуются холинсодержащие липиды – фосфатидилхолин, сфингомиелин, а также стероид холестерол. 2. Во внутреннем монослое локализуются аминосодержащие ФЛ – фосфатидилэтаноламин, фосфатидилсерин. 3. Во внешнем монослое – 1/3 двойных связей, во внутреннем – 2/3 двойных связей. 4. Известны 2 механизма, обеспечивающие асимметрию липидного бислоя: - различия конформационных размеров полярных «головок» липидов; - транслокация с помощью белков-переносчиков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
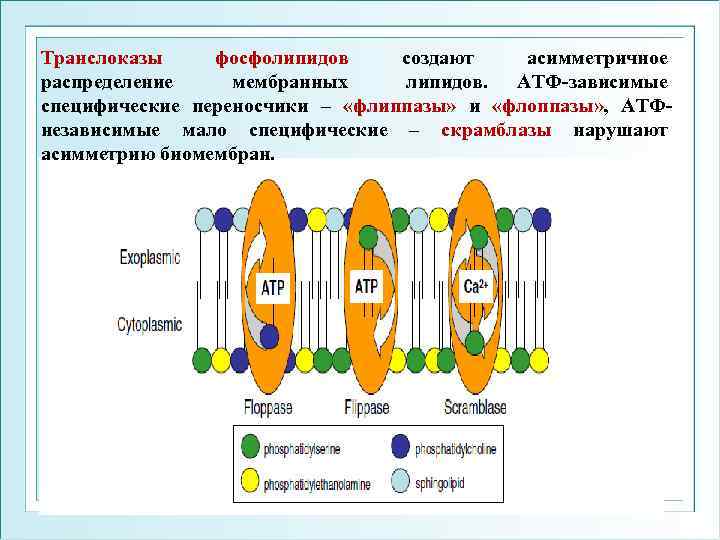
Транслоказы фосфолипидов создают асимметричное распределение мембранных липидов. АТФ-зависимые специфические переносчики – «флиппазы» и «флоппазы» , АТФнезависимые мало специфические – скрамблазы нарушают асимметрию биомембран.

Различные виды подвижности мембранных липидов 1. Изменение ориентации полярных голов. 2. Латеральная подвижность. 3. Сегментарная подвижность – колебания ацильный цепей. 4. Образование кинков и их миграция вдоль ацильных цепей. 5. Ротационная подвижность. 6. Флип-флоп переходы. 7. Выход из бислоя.

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
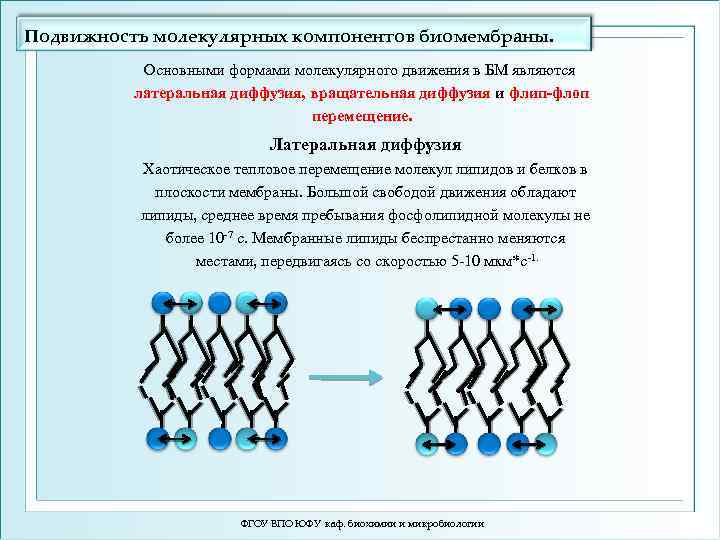
Подвижность молекулярных компонентов биомембраны. Основными формами молекулярного движения в БМ являются латеральная диффузия, вращательная диффузия и флип-флоп перемещение. Латеральная диффузия Хаотическое тепловое перемещение молекул липидов и белков в плоскости мембраны. Большой свободой движения обладают липиды, среднее время пребывания фосфолипидной молекулы не более 10 -7 с. Мембранные липиды беспрестанно меняются местами, передвигаясь со скоростью 5 -10 мкм*с-1. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
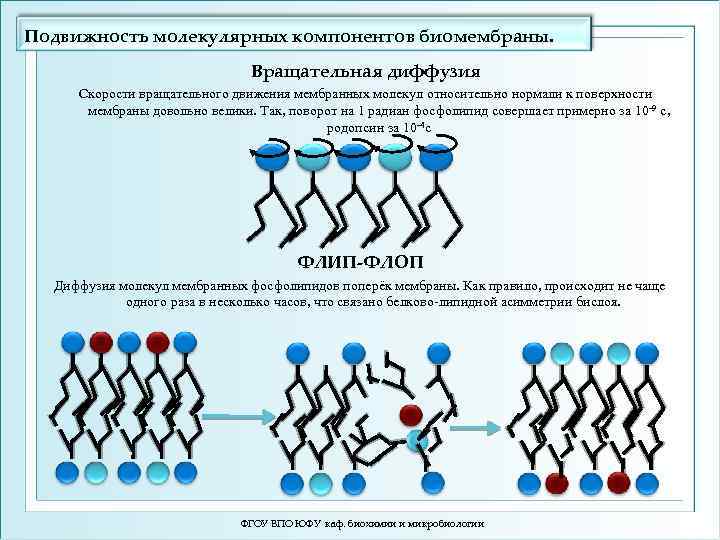
Подвижность молекулярных компонентов биомембраны. Вращательная диффузия Скорости вращательного движения мембранных молекул относительно нормали к поверхности мембраны довольно велики. Так, поворот на 1 радиан фосфолипид совершает примерно за 10 -9 с, родопсин за 10 -4 с ФЛИП-ФЛОП Диффузия молекул мембранных фосфолипидов поперёк мембраны. Как правило, происходит не чаще одного раза в несколько часов, что связано белково-липидной асимметрии бислоя. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Выделяют различные виды липидов по типу взаимодействия с белками: 1. Аннулярные или иммобилизованные липиды – создают микроокружение мембранных белков 2. Липиды общего липидного бислоя или свободного объема (часто находятся в жидко-неупорядоченном состоянии ) 3. Рафтовые липиды – локализованы в рафтах и находятся в жидко-упорядоченном состоянии

Мембранные белки

20 -30% всех белков – мембранные. По своему расположению относительно липидного бислоя мембранные белки разделяются на три типа: - Периферические - непрочно связаны с поверхностью мембраны и обычно находятся вне липидного бислоя. очень прочно связаны с -Интегральные мембраной и делятся на: собственно интегральные белки – полностью погружены в липидный бислой; полуинтегральные белки частично погружены в бислой. - Амфитропные - могут находиться в цитозоле и бислое.
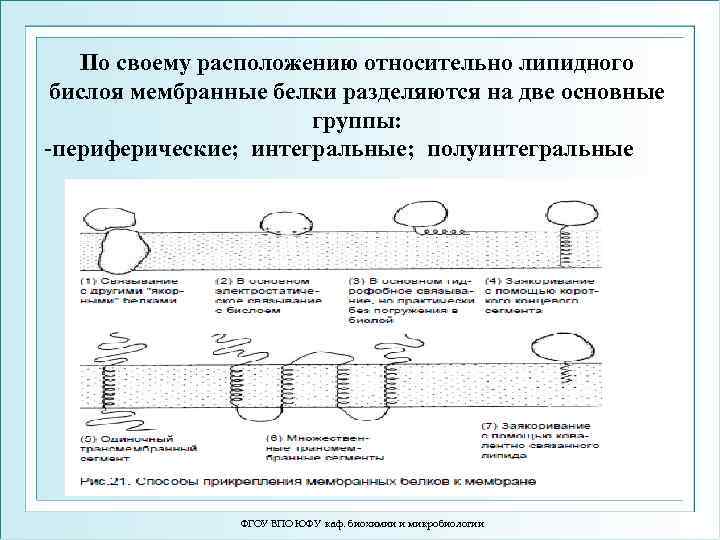
По своему расположению относительно липидного бислоя мембранные белки разделяются на две основные группы: -периферические; интегральные; полуинтегральные ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

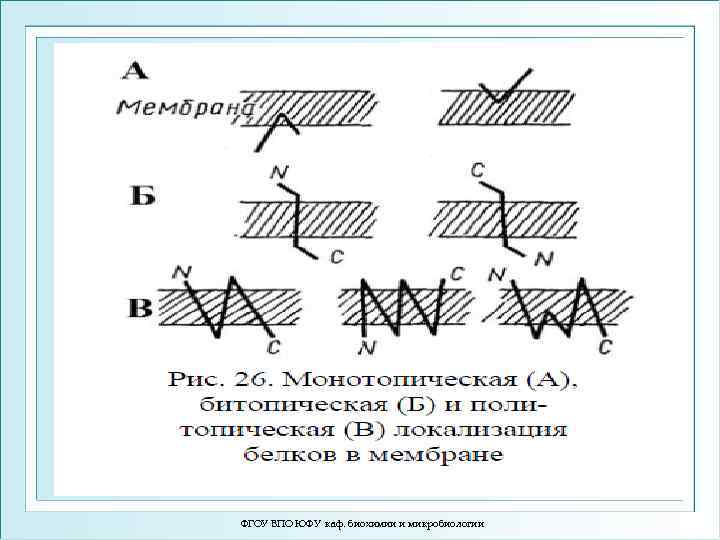
Топологическая классификация мембранных белков: 1. Монотопические – являются периферическими белками и не пронизывают мембрану (цит b 5) 2. Битопические – пронизывают мембрану один раз (гликофорин) 3. Политопические - пронизывают мембрану два и более раз (рецепторы, сопряженные с Gбелками; Na, K- АТФ-аза; АТФ-синтаза) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Основные типы мембранных α-спиральных белков I тип – один трансмембранный сегмент, N-конец снаружи II тип – одна трансмембранная спираль, N-конец внутри Ш тип – много трансмембранных спиралей IV тип – трансмембранные домены нескольких полипептидов соединяются с образованием канала через мембрану V тип – белки удерживаются бислоем с помощью ковалентно связанных липидов VI тип – содержат трансмембранные спирали и липидные ГФИ-якори (ГФИ- глицерофосфатидилинозитол)
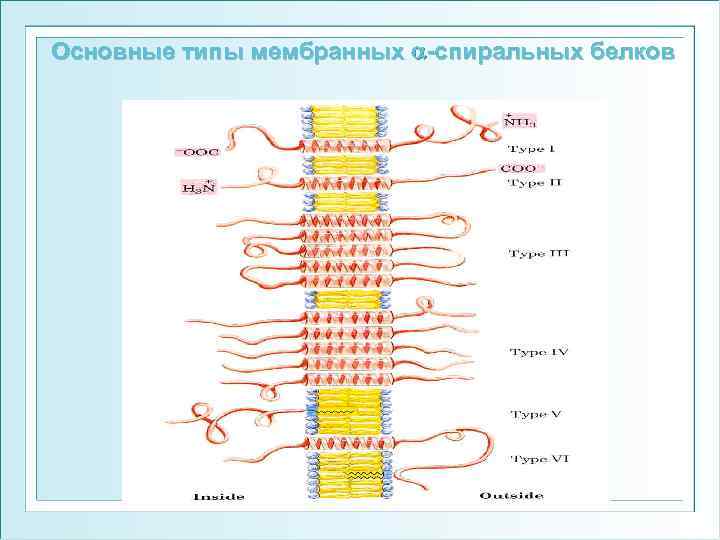
Основные типы мембранных -спиральных белков
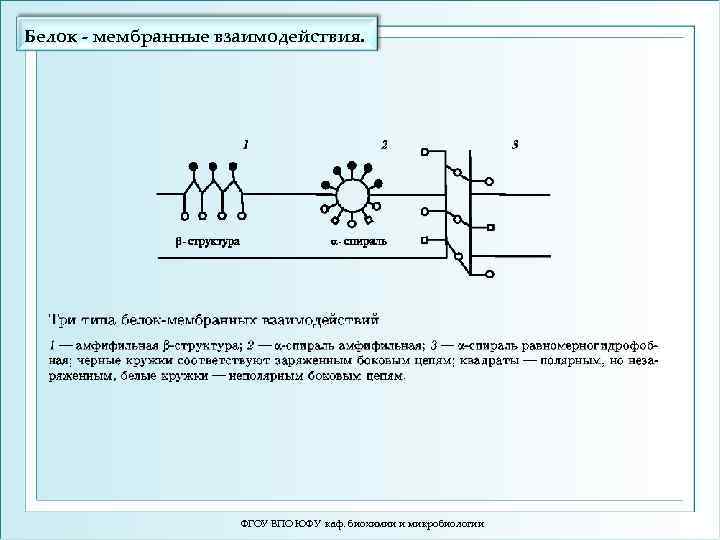
Белок - мембранные взаимодействия. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
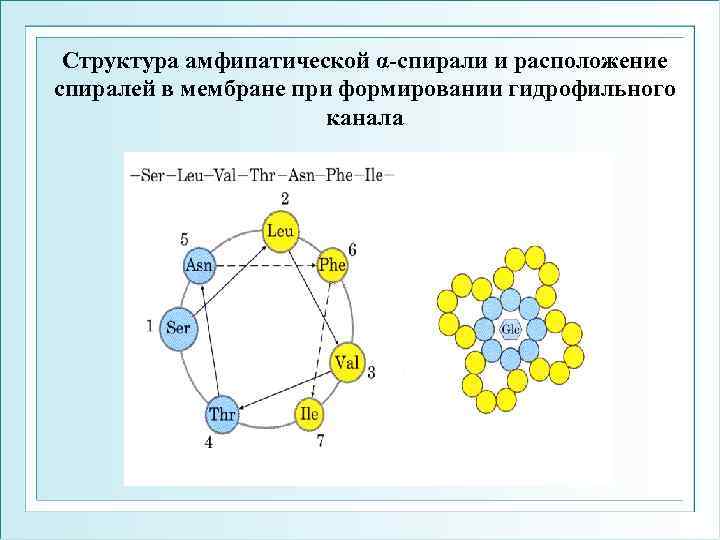
Структура амфипатической α-спирали и расположение спиралей в мембране при формировании гидрофильного канала

Функции мембранных белков • • • Мембранные белки по биологической роли делятся на 3 группы: 1)белки-ферменты, обладающие каталитической активностью 2)рецепторные белки, специфически связывающие лиганды 3) белки-ионные каналы 4)структурные белки
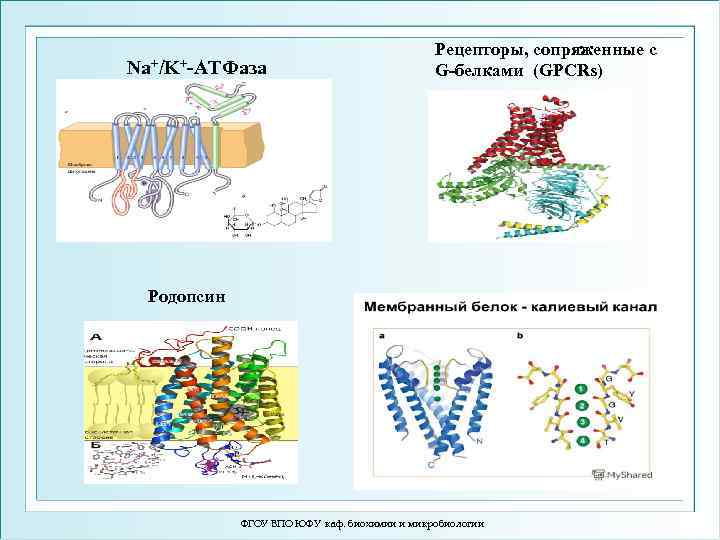
Na+/K+-ATФаза Рецепторы, сопряженные с G-белками (GPCRs) Родопсин ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
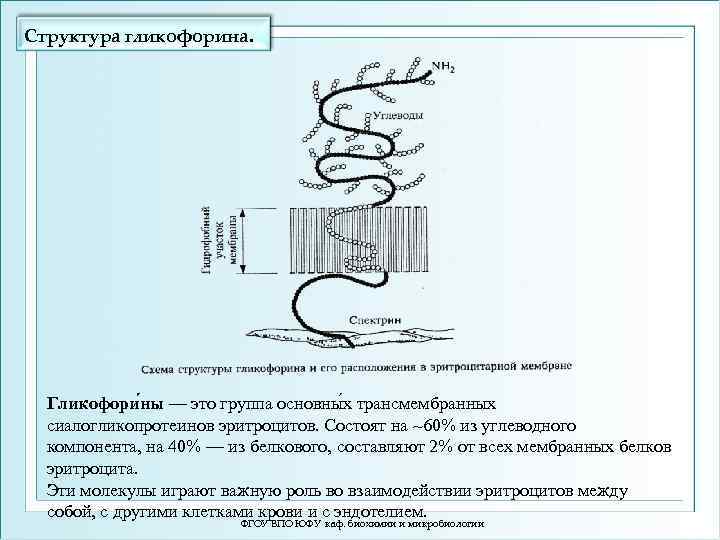
Структура гликофорина. Гликофори ны — это группа основны х трансмембранных сиалогликопротеинов эритроцитов. Состоят на ~60% из углеводного компонента, на 40% — из белкового, составляют 2% от всех мембранных белков эритроцита. Эти молекулы играют важную роль во взаимодействии эритроцитов между собой, с другими клетками крови и с эндотелием. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
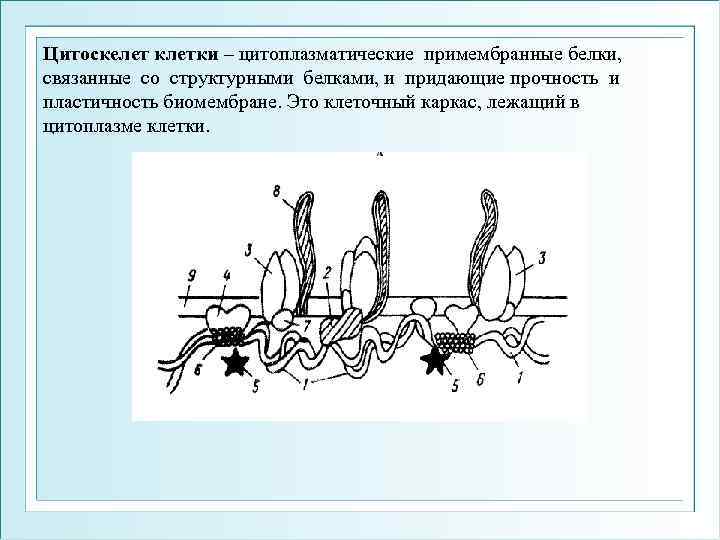
Цитоскелет клетки – цитоплазматические примембранные белки, связанные со структурными белками, и придающие прочность и пластичность биомембране. Это клеточный каркас, лежащий в цитоплазме клетки.

Липосомы. Образование и виды. Стремление фосфолипидов полностью исключить взаимодействие с водой приводит к замыканию плоского бислоя в сферические везикулы. Липосомы, или фосфолипидные везикулы (пузырьки), получают обычно при набухании сухих фосфолипидов в воде или при впрыскивании раствора липидов в воду. При этом происходит самосборка бимолекулярной липидной мембраны. Различные виды липосом: 1. мультиламеллярные везикулы (МЛВ). 2. большие моноламеллярные везикулы (БМВ). 3. олиголамеллярные везикулы (ОЛВ). 4. олиговезикулярные липосомы (ОВЛ). 5. малые моноламеллярные везикулы (ММВ). 6. дискомы - дискоообразные липосомы. 7. тубулярные трубчатые везикулы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
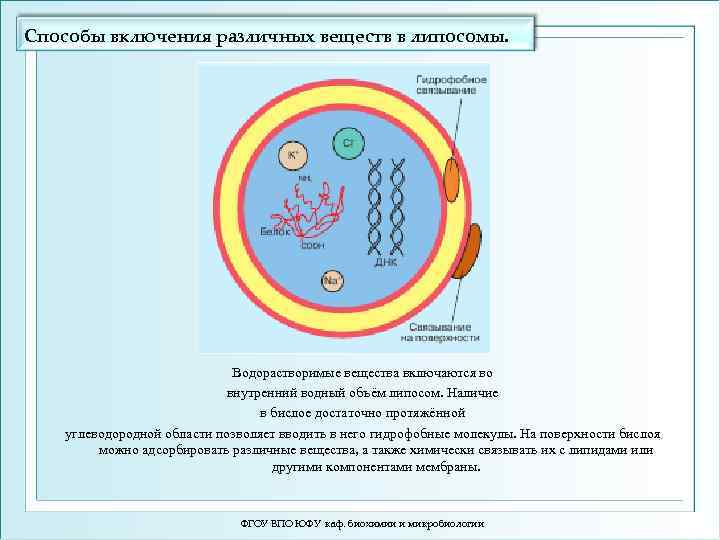
Способы включения различных веществ в липосомы. Водорастворимые вещества включаются во внутренний водный объём липосом. Наличие в бислое достаточно протяжённой углеводородной области позволяет вводить в него гидрофобные молекулы. На поверхности бислоя можно адсорбировать различные вещества, а также химически связывать их с липидами или другими компонентами мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Применение липосом. Применение липосом и везикул В фундаментальных научных исследованиях В фармакологии и медицине В косметологии ФГОУ ВПО ЮФУ каф. биохимии и микробиологии В пищевой индустрии
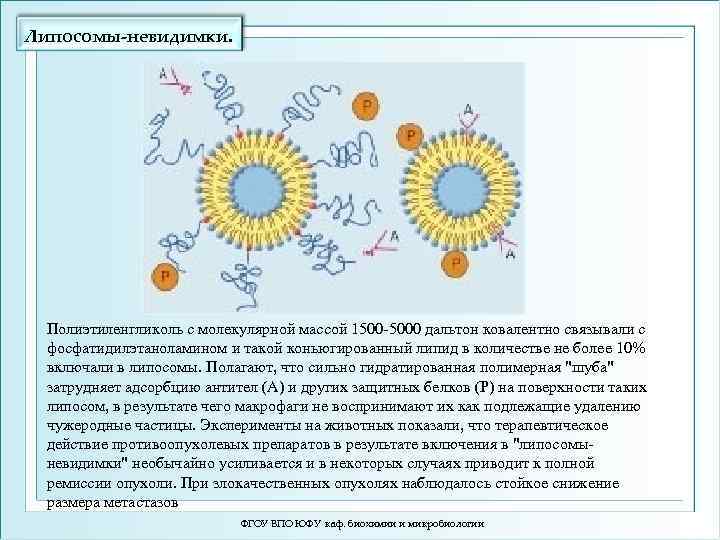
Липосомы-невидимки. Полиэтиленгликоль с молекулярной массой 1500 -5000 дальтон ковалентно связывали с фосфатидилэтаноламином и такой коньюгированный липид в количестве не более 10% включали в липосомы. Полагают, что сильно гидратированная полимерная "шуба" затрудняет адсорбцию антител (А) и других защитных белков (Р) на поверхности таких липосом, в результате чего макрофаги не воспринимают их как подлежащие удалению чужеродные частицы. Эксперименты на животных показали, что терапевтическое действие противоопухолевых препаратов в результате включения в "липосомыневидимки" необычайно усиливается и в некоторых случаях приводит к полной ремиссии опухоли. При злокачественных опухолях наблюдалось стойкое снижение размера метастазов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
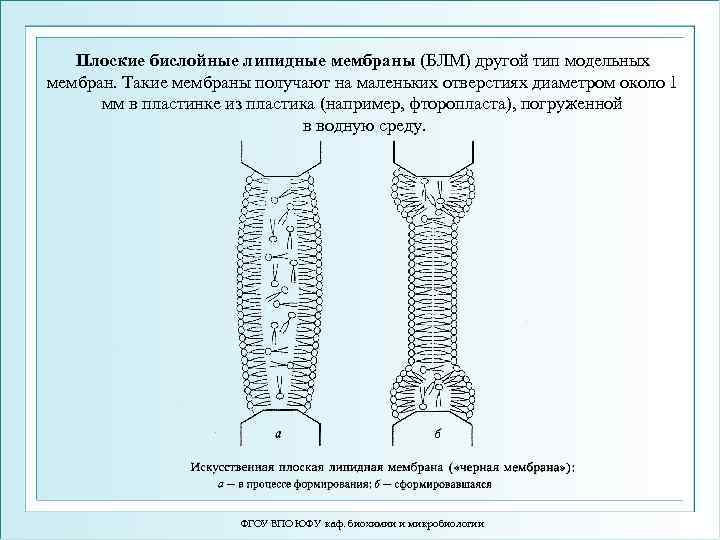
Плоские бислойные липидные мембраны (БЛМ) другой тип модельных мембран. Такие мембраны получают на маленьких отверстиях диаметром около 1 мм в пластинке из пластика (например, фторопласта), погруженной в водную среду. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
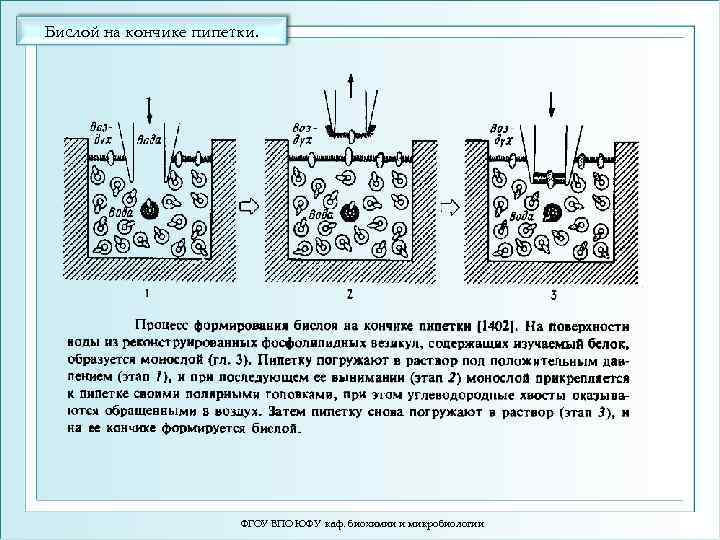
Бислой на кончике пипетки. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
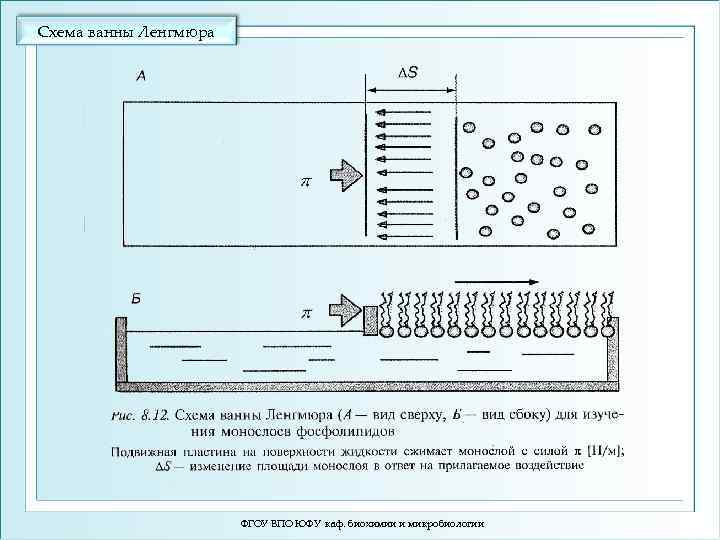
Схема ванны Ленгмюра ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
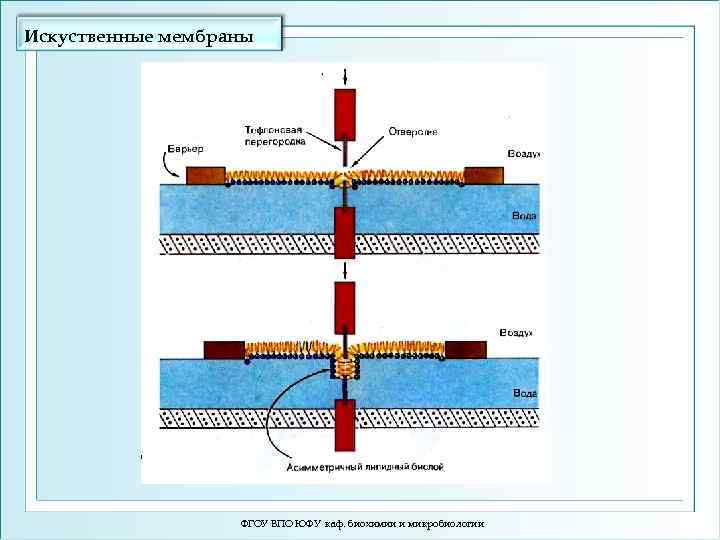
Искуственные мембраны ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Образование бислойной липидной мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Электрокинетические явления (ЭКЯ) • • • ЭКЯ – движение фаз гетерогенной среды под влиянием постоянного электрического поля, а также образование разности потенциалов в системе при механическом движении фаз. Электрофорез – движение частиц дисперсной фазы в постоянном электрическом поле к противоположно заряженному электроду. Электроосмос – движение дисперсионной среды в постоянном электрическом поле к противоположно заряженному электроду. Потенциалы течения - появление электрической разности потенциалов на концах капилляра или мембраны при протекании жидкости в результате градиента гидростатического давления. Потенциалы течения противоположны электроосмосу. Потенциалы оседания (седиментации) - появление электрической разности потенциалов в гетерогенной среде под влиянием сил гравитации между верхними и нижними слоями системы. Потенциалы оседания противоположны электрофорезу. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Схема опытов Ф. Рейсса (1808) по электроосмосу и электрофорезу В мокрую глину помещаются две заполненные водой стеклянные трубки, в которых расположены электроды, и прикладывается внешнее электрическое поле. В анодном пространстве появляется взвесь частиц, движущихся к аноду. Это указывает на то, что частицы глины заряжены отрицательно. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
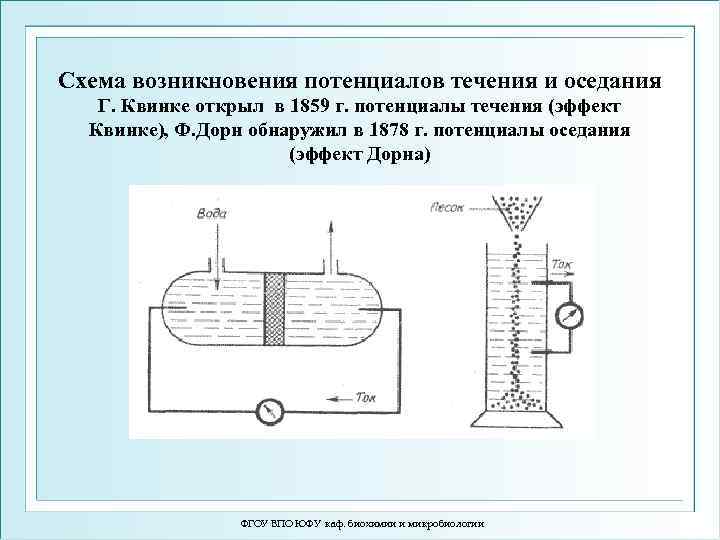
Схема возникновения потенциалов течения и оседания Г. Квинке открыл в 1859 г. потенциалы течения (эффект Квинке), Ф. Дорн обнаружил в 1878 г. потенциалы оседания (эффект Дорна) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

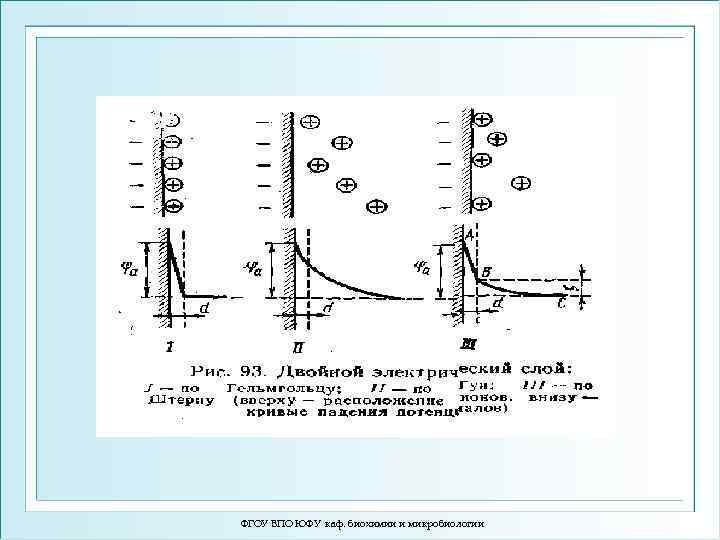
Причины возникновения ζ-потенциала и двойного электрического слоя (ДЭС) ЭКЯ связаны с образованием разности потенциалов (∆φ), возникающей между дисперсной фазой и дисперсионной средой. Это электрокинетический или ζ(дзета)-потенциал, который возникает вследствие движения фаз гетерогенной системы. Причина образования ζ-потенциала – возникновение поверхностного заряда на границе раздела двух фаз в результате асимметричного распределения ионов. Почему возникает поверхностный заряд? 1. За счет диссоциации ионогенных групп ( -NH 2, -COOH, -РО 43 -, OH) дисперсной фазы (клетки, мембраны, частицы), в результате образуется потенциалообразующий слой (ПС). 2. Вследствие адсорбции ионов на полярной поверхности мембраны, частицы, в результате образуется адсорбционный слой (АС). Такая система ионов, в целом электронейтральная, называется двойным электрическим слоем (ДЭС). ДЭС = ПС + АС ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 50

Между потенциалообразующим слоем и дисперсионной средой возникает полный электрохимический потенциал (φ) Между адсорбционным слоем и дисперсной средой возникает ζ-потенциал, он является частью полного электрохимического потенциала. Полный электрохимический потенциал (φ) уменьшается с расстоянием по экспоненциальному закону. Величина ζ-потенциала зависит от: 1. Толщины ДЭС: чем толще ДЭС, тем больше ζ-потенциал 2. Ионной силы раствора: чем больше ионная сила, тем меньше ζ-потенциал. Величина ζ-потенциала измеряется с помощью метода электрофореза по формуле Смолуховского: V = E • ε • ζ/ 4πη, где V – скорость движения частицы в электрическом поле E – напряженность электрического поля ε – диэлектрическая постоянная ζ – дзета-потенциал η – коэффициент вязкости среды ζ = 4πη • V/ E • ε ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 51
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
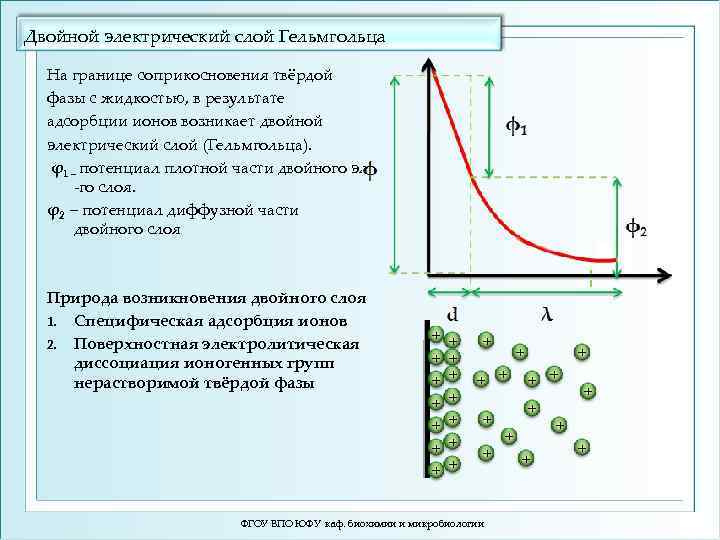
Двойной электрический слой Гельмгольца На границе соприкосновения твёрдой фазы с жидкостью, в результате адсорбции ионов возникает двойной электрический слой (Гельмгольца). φ1 – потенциал плотной части двойного эл -го слоя. φ2 – потенциал диффузной части двойного слоя Природа возникновения двойного слоя 1. Специфическая адсорбция ионов 2. Поверхностная электролитическая диссоциация ионогенных групп нерастворимой твёрдой фазы + + + + + ФГОУ ВПО ЮФУ каф. биохимии и микробиологии + + + + +
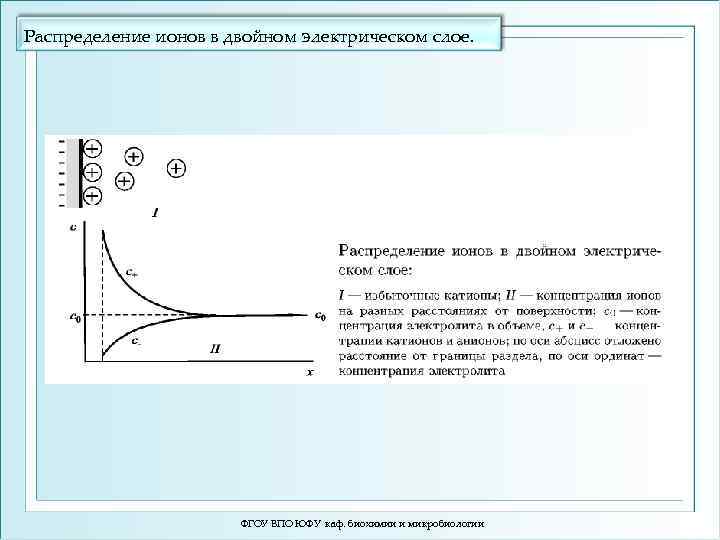
Распределение ионов в двойном электрическом слое. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
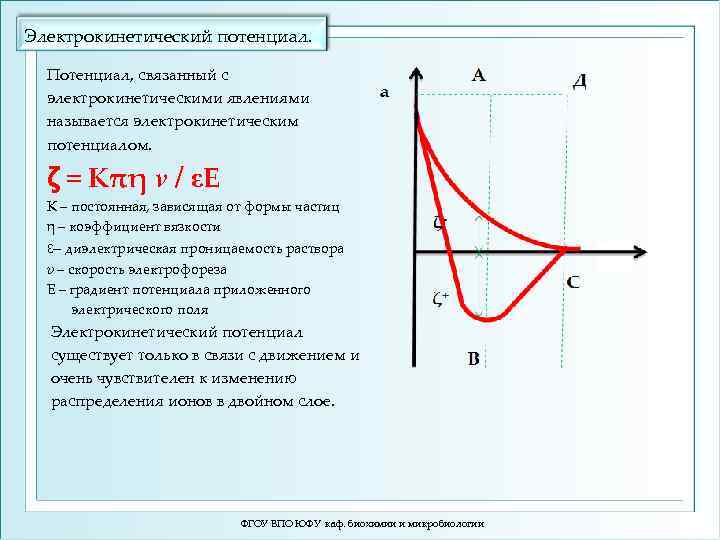
Электрокинетический потенциал. Потенциал, связанный с электрокинетическими явлениями называется электрокинетическим потенциалом. ζ = Кπη v / εЕ K – постоянная, зависящая от формы частиц η – коэффициент вязкости ε– диэлектрическая проницаемость раствора v – скорость электрофореза Е – градиент потенциала приложенного электрического поля Электрокинетический потенциал существует только в связи с движением и очень чувствителен к изменению распределения ионов в двойном слое. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Виды мембранного транспорта (МТ) 1. Пассивный транспорт 1. 1. Простая диффузия 1. 2. Облегченная диффузия 1. 3. Фильтрация 2. Активный транспорт 2. 1. Первичный активный транспорт 2. 2. Вторичный активный транспорт ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 56
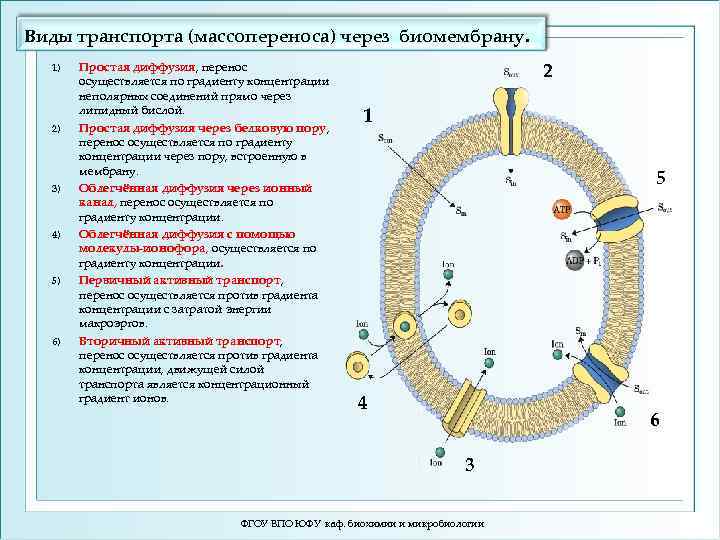
Виды транспорта (массопереноса) через биомембрану. 1) 2) 3) 4) 5) 6) Простая диффузия, перенос осуществляется по градиенту концентрации неполярных соединений прямо через липидный бислой. Простая диффузия через белковую пору, перенос осуществляется по градиенту концентрации через пору, встроенную в мембрану. Облегчённая диффузия через ионный канал, перенос осуществляется по градиенту концентрации. Облегчённая диффузия с помощью молекулы-ионофора, осуществляется по градиенту концентрации. Первичный активный транспорт, перенос осуществляется против градиента концентрации с затратой энергии макроэргов. Вторичный активный транспорт, перенос осуществляется против градиента концентрации, движущей силой транспорта является концентрационный градиент ионов. 2 1 5 4 6 3 ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
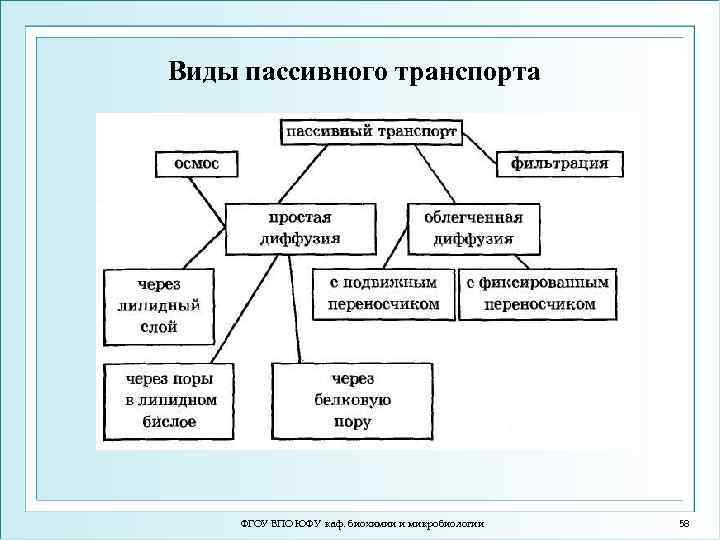
Виды пассивного транспорта ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 58
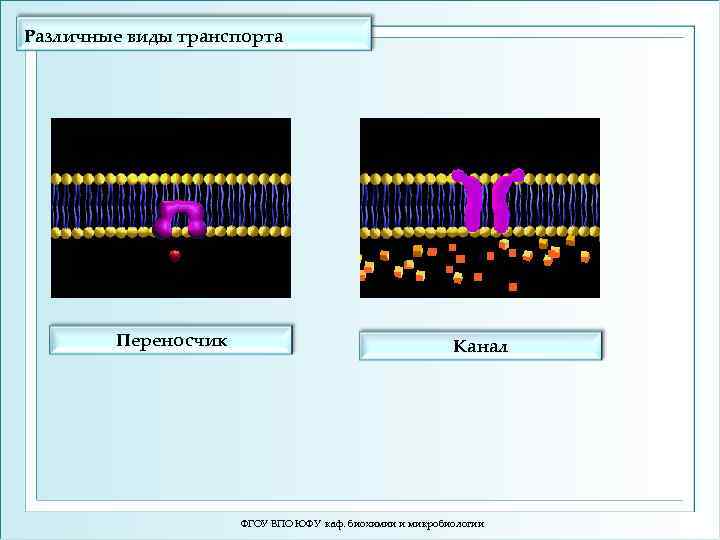
Различные виды транспорта Переносчик Канал ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
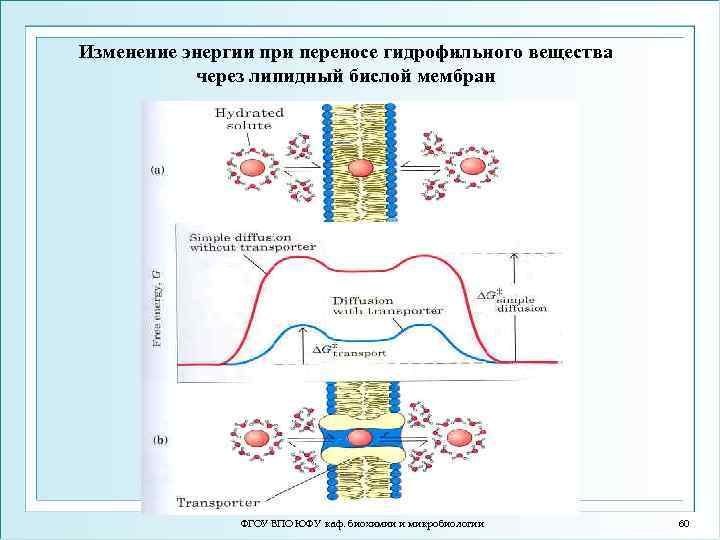
Изменение энергии при переносе гидрофильного вещества через липидный бислой мембран ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 60
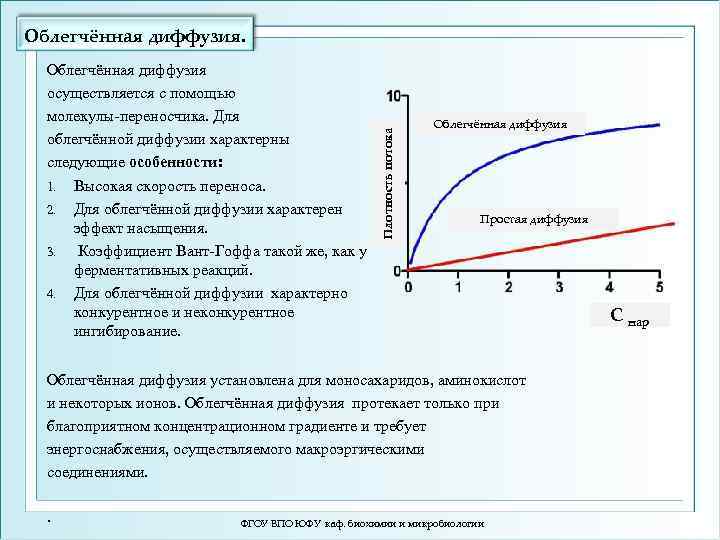
Облегчённая диффузия осуществляется с помощью молекулы-переносчика. Для облегчённой диффузии характерны следующие особенности: 1. Высокая скорость переноса. 2. Для облегчённой диффузии характерен эффект насыщения. 3. Коэффициент Вант-Гоффа такой же, как у ферментативных реакций. 4. Для облегчённой диффузии характерно конкурентное и неконкурентное ингибирование. Плотность потока Облегчённая диффузия Простая диффузия Облегчённая диффузия установлена для моносахаридов, аминокислот и некоторых ионов. Облегчённая диффузия протекает только при благоприятном концентрационном градиенте и требует энергоснабжения, осуществляемого макроэргическими соединениями. . ФГОУ ВПО ЮФУ каф. биохимии и микробиологии С нар
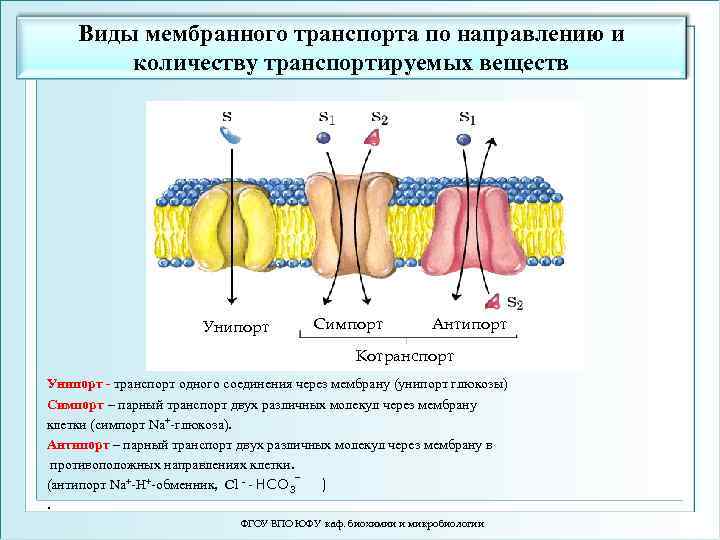
Виды мембранного транспорта по направлению и количеству транспортируемых веществ Унипорт Симпорт Антипорт Котранспорт Унипорт - транспорт одного соединения через мембрану (унипорт глюкозы) Симпорт – парный транспорт двух различных молекул через мембрану клетки (симпорт Na+-глюкоза). Антипорт – парный транспорт двух различных молекул через мембрану в противоположных направлениях клетки. (антипорт Na+-Н+-обменник, Сl - - НСО 3‾ ). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
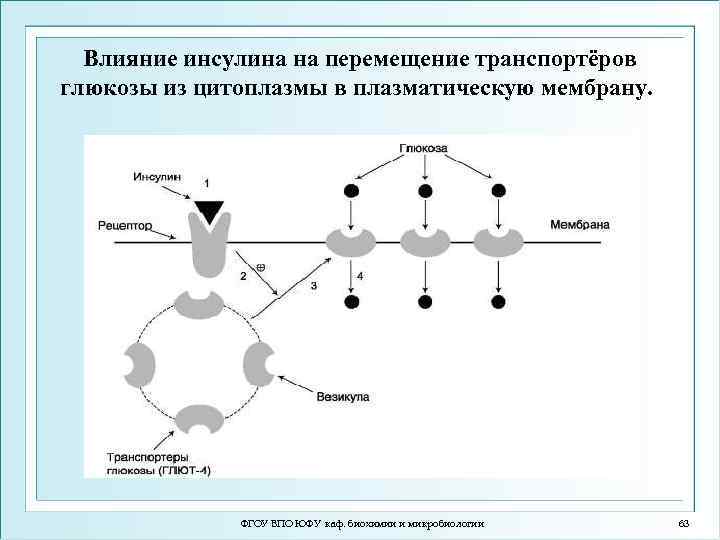
Влияние инсулина на перемещение транспортёров глюкозы из цитоплазмы в плазматическую мембрану. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 63
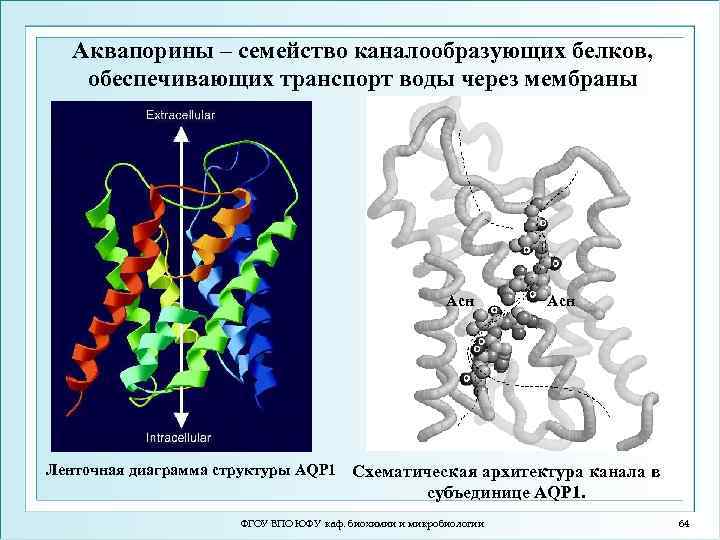
Аквапорины – семейство каналообразующих белков, обеспечивающих транспорт воды через мембраны Асн Ленточная диаграмма структуры АQP 1 Схематическая архитектура канала в субъединице АQP 1. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 64
Нобелевская премия по химии 2003 г. была вручена «за открытия, касающиеся каналов в клеточных мембранах» - Питеру Эгру «за открытие водных каналов» Выступление П. Эгра в МГУ в 2013 г. Открытие, сделанное профессором Эгром, — яркий пример роли счастливого случая в науке. Недаром сам нобелевский лауреат любит повторять на своих лекциях: «Всегда относитесь к научной деятельности как к приключению… Мы не знаем, что ждет нас за поворотом, и в этом смысле я, скорее, Гекльберри Финн, чем Альберт Эйнштейн» . ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 65
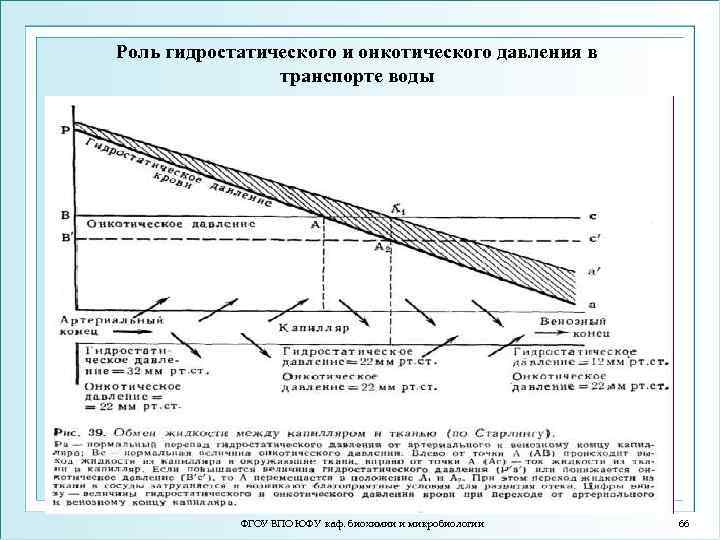
Роль гидростатического и онкотического давления в транспорте воды ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 66

Типы активного транспорта (АТ) 1. Первичный АТ – транспорт против ЭХГ за счет энергии АТФ. 1. 1. АТФ-азы Р-типа (фосфорилирование в процессе каталитического цикла) - Na+, K+- АТФ-аза - Са 2+ - АТФ-аза - флиппаза 1. 2. АТФ-азы F-типа (обратимое АТФ-зависимые протонные насосы) - Fo. F 1–АТФ–аза/ АТФ-синтаза 1. 3. АТФ-азы V- типа (протон-транспортные АТФ-азы отвечают за закисление среды внутриклеточных компартментов) 1. 4. ABC-транспортеры (АТФ-связывающие кассетные транспортеры) - Р-гликопротеин - флоппаза 2. Вторичный (АТ) – транспорт вещества против ЭХГ сопряжен с транспортом другого вещества по градиенту, которое было закачано с помощью первичного АТ. - переносчик лактозы E. coli (симпорт лактозы и Н+) - транспортер глюкозы в энтероцитах (симпорт глюкозы и Na+) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 67
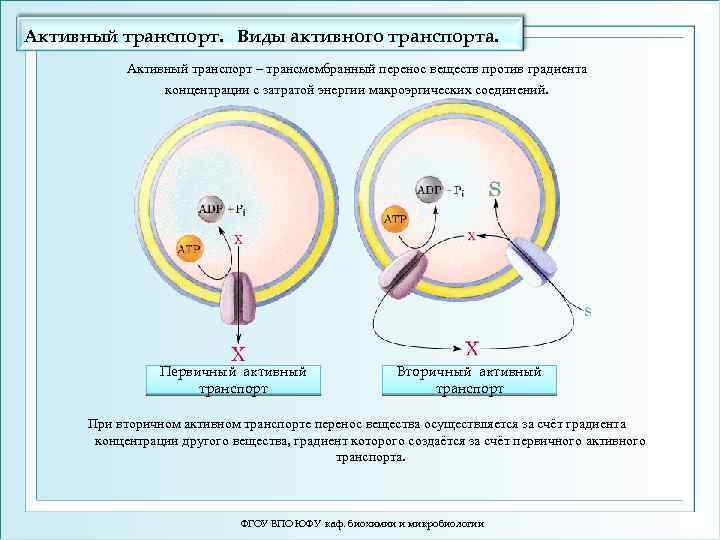
Активный транспорт. Виды активного транспорта. Активный транспорт – трансмембранный перенос веществ против градиента концентрации с затратой энергии макроэргических соединений. Первичный активный транспорт Вторичный активный транспорт При вторичном активном транспорте перенос вещества осуществляется за счёт градиента концентрации другого вещества, градиент которого создаётся за счёт первичного активного транспорта. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
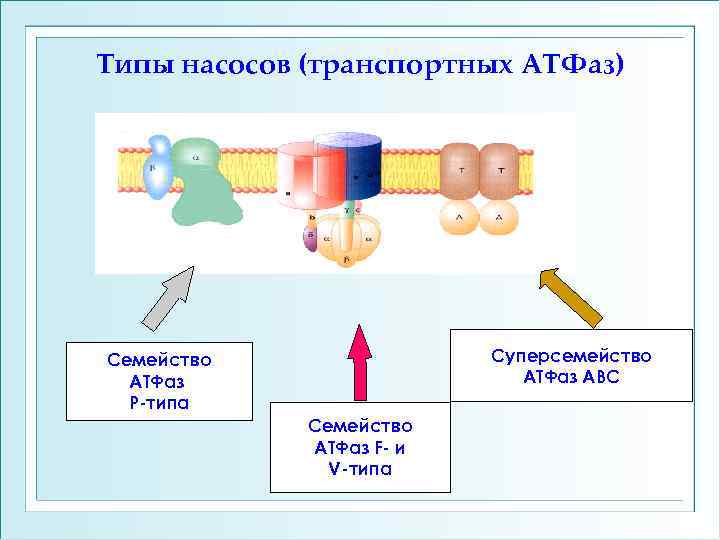
Типы насосов (транспортных АТФаз) Суперсемейство АТФаз АВС Семейство АТФаз Р-типа Семейство АТФаз F- и V-типа
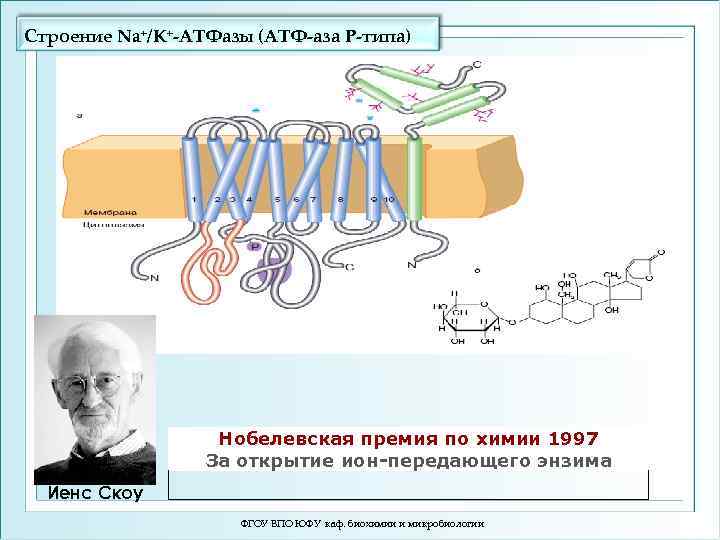
Строение Na+/K+-ATФазы (АТФ-аза Р-типа) а Нобелевская премия по химии 1997 За открытие ион-передающего энзима Йенс Скоу ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
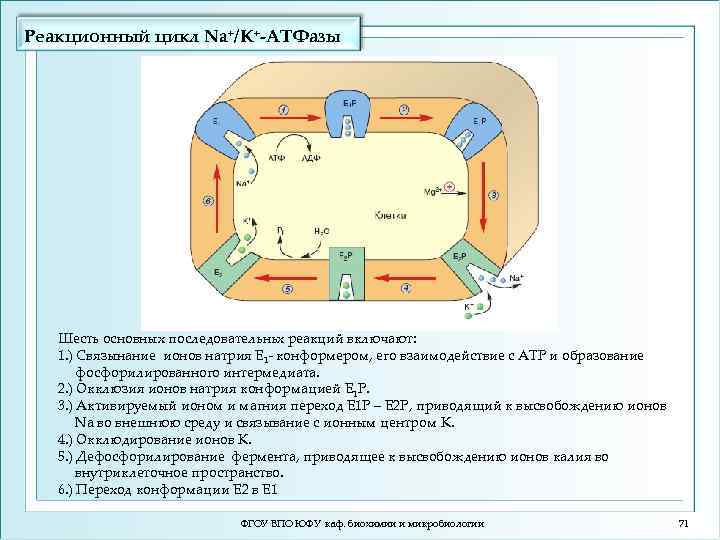
Реакционный цикл Na+/K+-ATФазы Шесть основных последовательньх реакций включают: 1. ) Связынание ионов натрия Е 1 - конформером, его взаимодействие с АТР и образование фосфорилированного интермедиата. 2. ) Окклюзия ионов натрия конформацией Е 1 Р. 3. ) Активируемый ионом и магния переход Е 1 Р – Е 2 Р, приводящий к высвобождению ионов Na во внешнюю среду и связывание с ионным центром K. 4. ) Окклюдирование ионов K. 5. ) Дефосфорилирование фермента, приводящее к высвобождению ионов калия во внутриклеточное пространство. 6. ) Переход конформации E 2 в E 1 ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 71

Рабочий цикл Na+/K+-ATФазы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 72
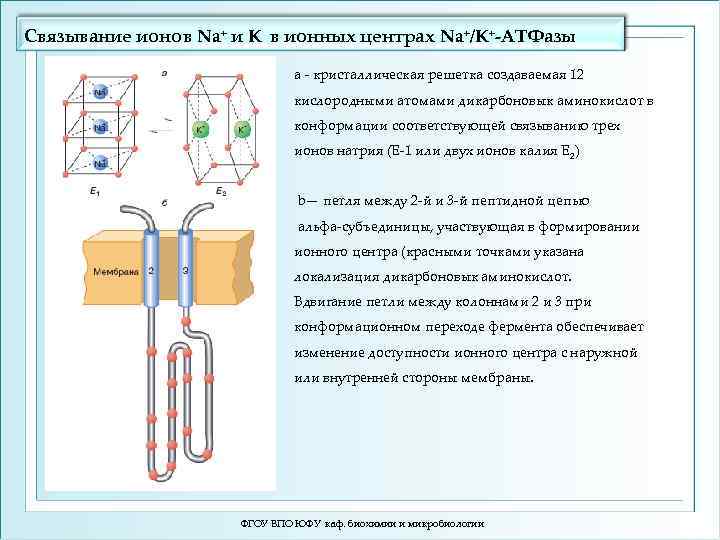
Связывание ионов Na+ и K в ионных центрах Na+/K+-ATФазы а - кристаллическая решетка создаваемая 12 кислородными атомами дикарбоновык аминокислот в конформации соответствующей связыванию трех ионов натрия (Е-1 или двух ионов калия Е 2) b— петля между 2 -й и 3 -й пептидной цепью альфа-субъединицы, участвующая в формировании ионного центра (красными точками указана локализация дикарбоновык аминокислот. Вдвигание петли между колоннами 2 и 3 при конформационном переходе фермента обеспечивает изменение доступности ионного центра с наружной или внутренней стороны мембраны. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
Все морские птицы (например, альбатрос) имеют ряд специальных приспособлений к круглогодичной жизни на морской воде - мощные солевые железы (содержат Na+/K+-ATФазу), через ноздри выводящие излишки соли из организма. При активном функционировании желез с клюва птиц регулярно стекают капли солевого секрета. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 74
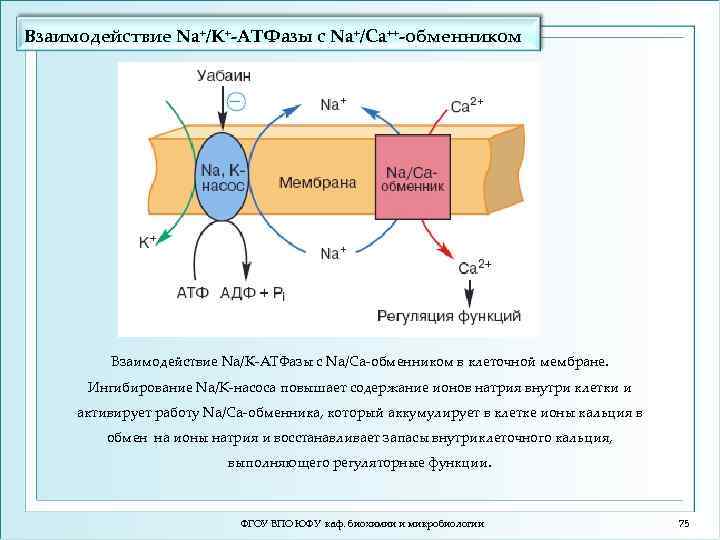
Взаимодействие Na+/K+-ATФазы с Na+/Ca++-обменником Взаимодействие Na/K-АТФазы с Na/Ca-обменником в клеточной мембране. Ингибирование Na/К-насоса повышает содержание ионов натрия внутри клетки и активирует работу Na/Ca-обменника, который аккумулирует в клетке ионы кальция в обмен на ионы натрия и восстанавливает запасы внутриклеточного кальция, выполняющего регуляторные функции. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 75
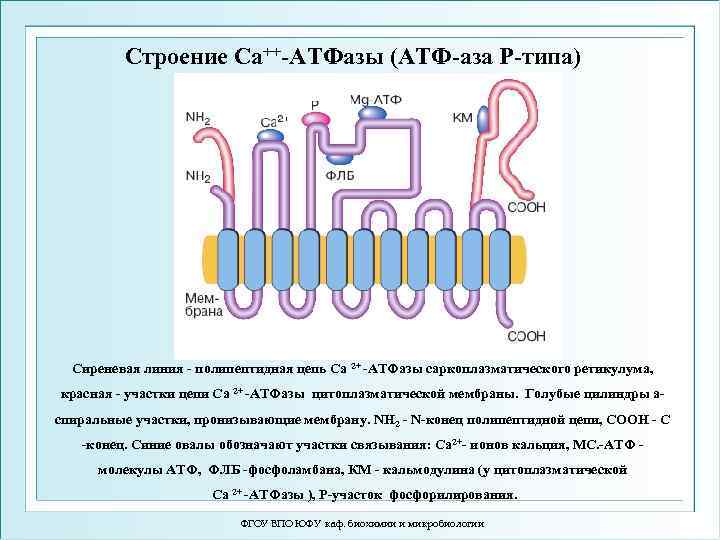
Строение Са++-ATФазы (АТФ-аза Р-типа) Сиреневая линия - полипептидная цепь Са 2+ -АТФазы саркоплазматического ретикулума, красная - участки цепи Са 2+ -АТФазы цитоплазматической мембраны. Голубые цилиндры аспиральные участки, пронизывающие мембрану. NH 2 - N-конец полипептидной цепи, СООН - С -конец. Синие овалы обозначают участки связывания: Са 2+- ионов кальция, МС. -АТФ молекулы АТФ, ФЛБ -фосфоламбана, КМ - кальмодулина (у цитоплазматической Са 2+ -АТФазы ), Р-участок фосфорилирования. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Работа Са++-ATФазы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 77
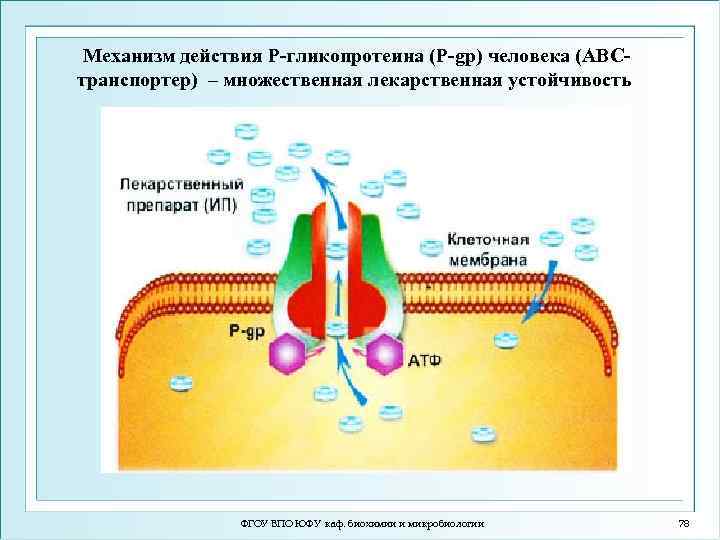
Механизм действия Р-гликопротеина (P-gp) человека (ABC- транспортер) – множественная лекарственная устойчивость ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 78
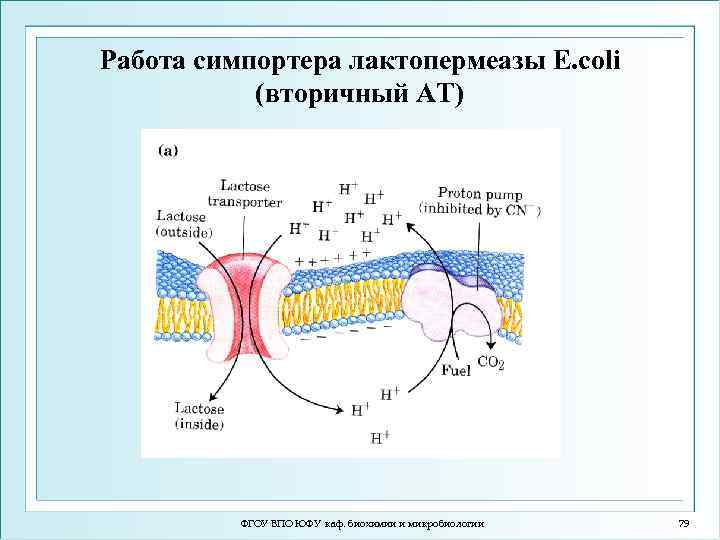
Работа симпортера лактопермеазы E. coli (вторичный АТ) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 79

Ионные каналы (ИК) - это интегральные трансмембранные белки, имеют субъединичное строение и образуют сквозную пору, содержат системы открытия, закрытия, избирательности и регуляции. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 80
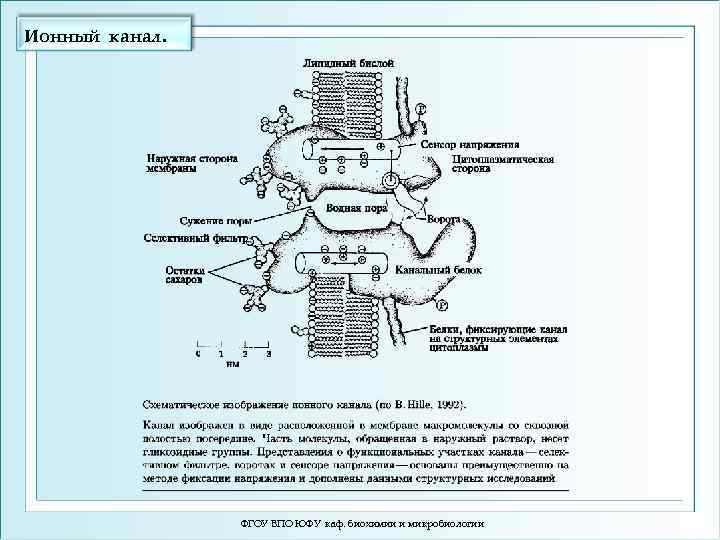
Ионный канал. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Свойства ионных каналов 1. Селективность – способность пропускать ионы одного типа. • ИК обладают абсолютной селективностью по отношению к катионам или анионам; • Через катион-селективные каналы проходят различные ионы, но проводимость для основного иона максимальна; • Способность ионного канала пропускать различные ионы называется относительной селективностью. • Ряд селективности - соотношение проводимости канала для различных ионов, взятых при одной крнцентрации. Для основного иона селективность принимается за 1 (для Na-канала ряд селективности: Na+ : K+ = 1 : 0, 05). 2. Независимость работы отдельных каналов. 3. Дискретный характер проводимости. 4. Управляемая проницаемость (потенциал-зависимые, лигандзависимые). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
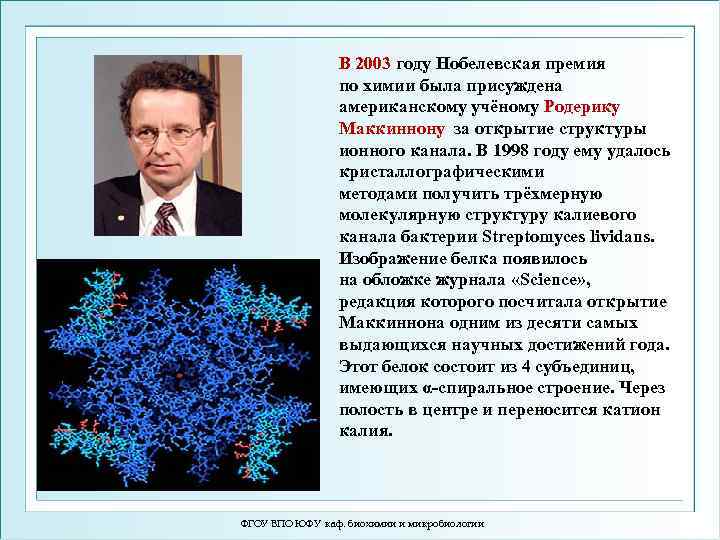
В 2003 году Нобелевская премия по химии была присуждена американскому учёному Родерику Маккиннону за открытие структуры ионного канала. В 1998 году ему удалось кристаллографическими методами получить трёхмерную молекулярную структуру калиевого канала бактерии Streptomyces lividans. Изображение белка появилось на обложке журнала «Science» , редакция которого посчитала открытие Маккиннона одним из десяти самых выдающихся научных достижений года. Этот белок состоит из 4 субъединиц, имеющих α-спиральное строение. Через полость в центре и переносится катион калия. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
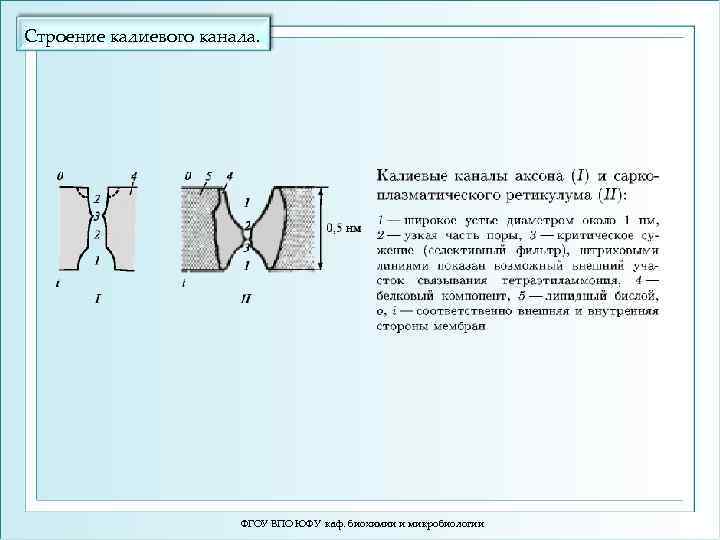
Строение калиевого канала. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
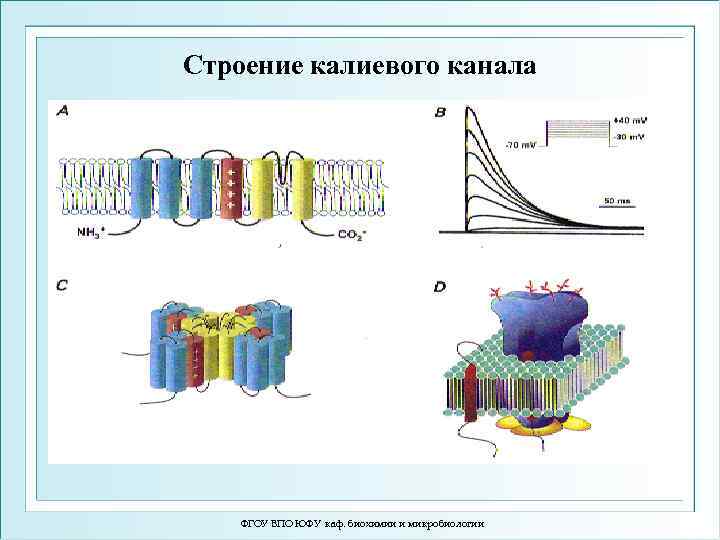
Строение калиевого канала ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Схема строения калиевого канала ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 86
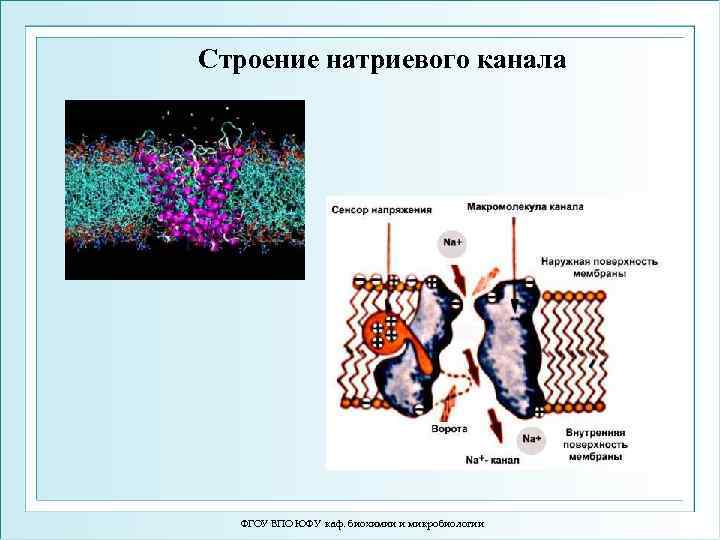
Строение натриевого канала ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
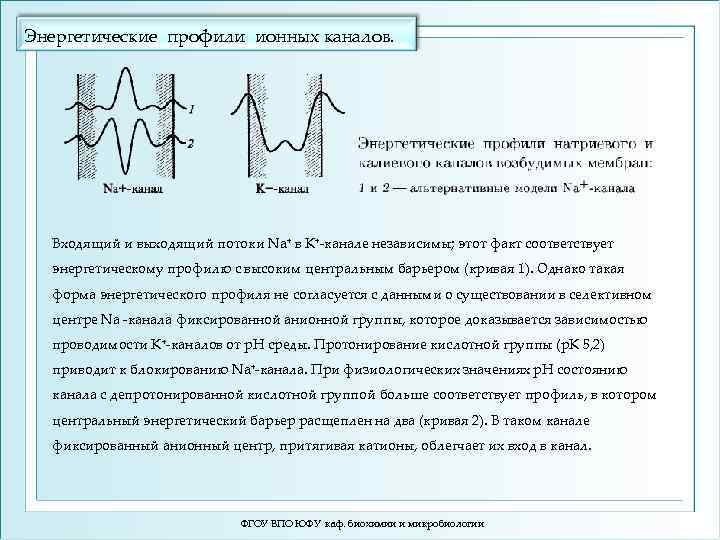
Энергетические профили ионных каналов. Входящий и выходящий потоки Na+ в К+-канале независимы; этот факт соответствует энергетическому профилю с высоким центральным барьером (кривая 1). Однако такая форма энергетического профиля не согласуется с данными о существовании в селективном центре Nа -канала фиксированной анионной группы, которое доказывается зависимостью проводимости К+-каналов от р. Н среды. Протонирование кислотной группы (р. К 5, 2) приводит к блокированию Na+-канала. При физиологических значениях р. Н состоянию канала с депротонированной кислотной группой больше соответствует профиль, в котором центральный энергетический барьер расщеплен на два (кривая 2). В таком канале фиксированный анионный центр, притягивая катионы, облегчает их вход в канал. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
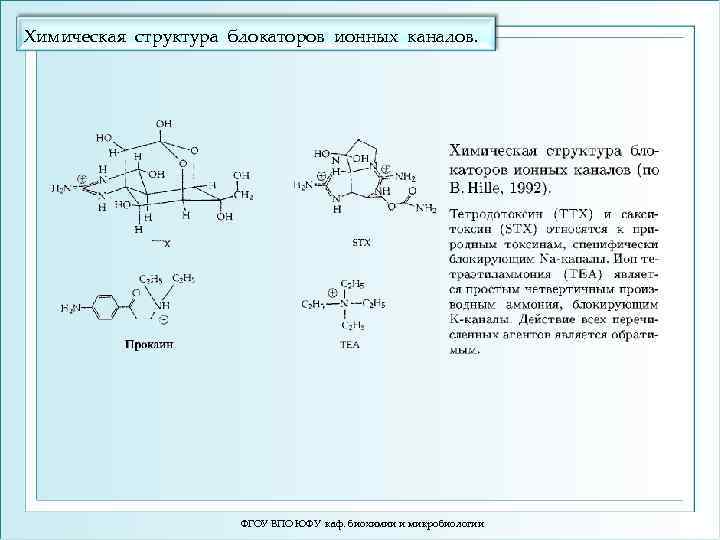
Химическая структура блокаторов ионных каналов. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Блокатор натриевых каналов тетродотоксин ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
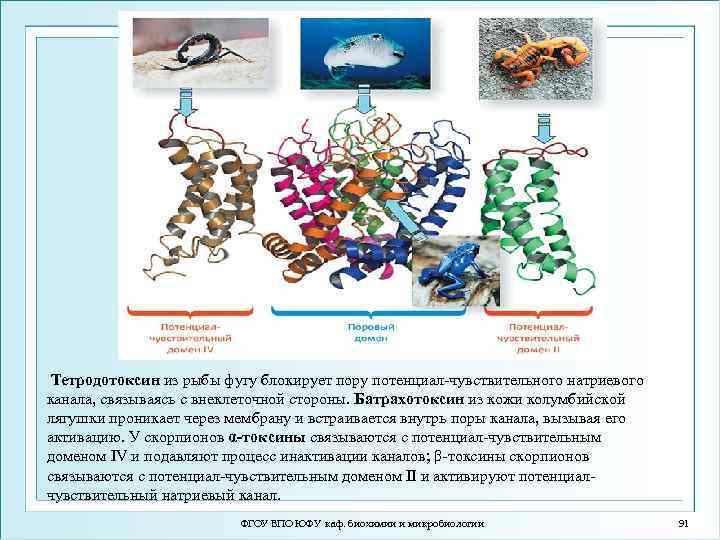
Тетродотоксин из рыбы фугу блокирует пору потенциал-чувствительного натриевого канала, связываясь с внеклеточной стороны. Батрахотоксин из кожи колумбийской лягушки проникает через мембрану и встраивается внутрь поры канала, вызывая его активацию. У скорпионов α-токсины связываются с потенциал-чувствительным доменом IV и подавляют процесс инактивации каналов; β-токсины скорпионов связываются с потенциал-чувствительным доменом II и активируют потенциалчувствительный натриевый канал. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 91
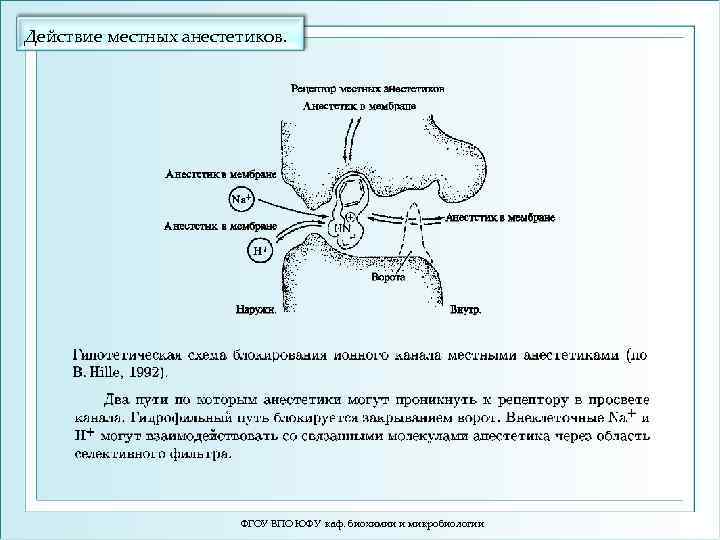
Действие местных анестетиков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Индуцированный транспорт осуществляется с помощью ионофоров, которые делятся на 2 вида: • Ионные переносчики образуют с ионом комплекс большого размера (валиномицин - переносит 104 ионов/c) • Каналоформеры формируют в мембране канал (пору, заполненную водой) (грамицидин А – переносит 107 – 108 ионов/c, аламетицин) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Антибиотик валиномицин впервые был выделен из экстракта штамма бактерий Streptomyces австрийским исследователем Г. Брокманом в 1954– 1955 годах. А в 1963 году в лаборатории акад. М. М. Шемякина установили химическую структуру этого соединения. Валиномицин - макроциклическое соединение, состоящее из шести α-аминокислот и шести αгидроксикислот, соединённых друг с другом попеременно амидными и сложноэфирными связями. В 1978 году акад. Ю. А. Овчинников и член-корр. АН СССР В. Т. Иванов были удостоены Ленинской премии за исследование ионофоров. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
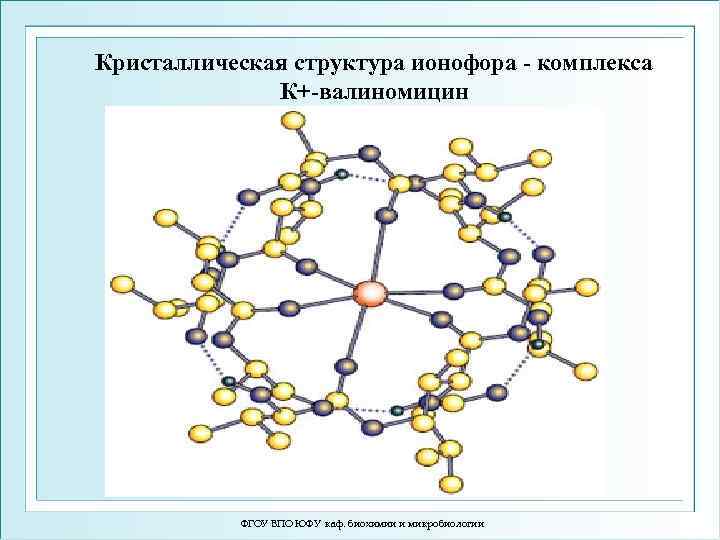
Кристаллическая структура ионофора - комплекса К+-валиномицин ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Облегчённая диффузия. Ионофоры. Валиномицин. Молекула валиномицина (а) напоминает своей конфигурацией браслет, является полярным соединением, причем отрицательные полюса образованных им диполей сосредоточены у карбонильных групп. Взаимодействуя между собой в слабо полярной среде, они отталкиваются друг от друга и потому повернуты наружу, что придает всей молекуле гидрофильность. В липидную мембрану она внедриться не может и находится в примембранном водном растворе (б). Если же в воде растворена калиевая соль, то К+ входит во внутреннюю полость браслета (в), о чем свидетельствуют данные рентгеноструктурного анализа молекулы антибиотика до и после взаимодействия с калием. Внедрение катиона в антибиотик вызывает разворот карбонильных групп валиномицина за счет ион-дипольного взаимодействия. Карбонильные группы смещаются во внутреннюю полость валиномицина, а снаружи его оказываются углеводородные цепочки, создающие гидрофобный чехол на молекулярноионном комплексе. Поэтому комплекс валиномицина с калием хорошо растворяется в липидах, легко внедряется в липидный бислой мембраны и диффундирует в нем как жирорастворимое вещество. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Скульптурная композиция комплекса К+-валиномицин перед входом в институт биоорганической химии им. М. М. Шемякина ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
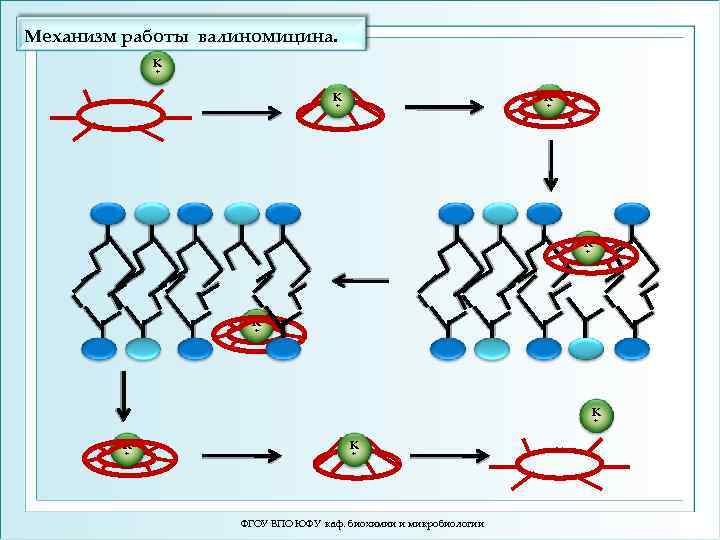
Механизм работы валиномицина. К + К К + + К + К + К + ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Грамицидиновый канал. 1. ) Грамицидиновый канал проводит преимущественно одновалентные катионы, причем проницаемость мембраны для них растет по мере уменьшения гидратного ионного радиуса в ряду: Li+ < Na+ < К+ < Rb+ < Cs+. 2. ) Почти не транспортируются анионы, так как внутрь поры «смотрят» отрицательно заряженные группы. 3. ) Канал образован димером — парой молекул грамицидина, расположенных «голова к голове» . Формильные концы соединяются межмолекулярными водородными связями. 4. ) Молекула грамицидина имеет форму спирали. Такая же форма присуща и димеру. Внутренность спирали гидрофильна и заполнена 5— 6 молекулами воды. Катион, движущийся по каналу, проталкивает их подобно поршню. 5. ) Скорость переноса 107 ионов калия за 1 с. 6. ) Грамицидиновый канал может пребывать либо в открытом, либо в закрытом состоянии, что обусловлено тепловым движением молекул грамицидина. За счет теплового движения концы димера то погружаются в липидную основу, то выходят на обе ее поверхности ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
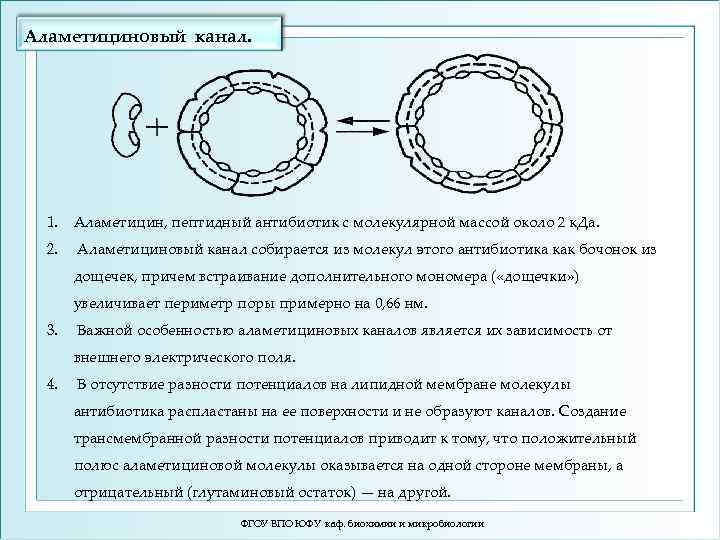
Аламетициновый канал. 1. Аламетицин, пептидный антибиотик с молекулярной массой около 2 к. Да. 2. Аламетициновый канал собирается из молекул этого антибиотика как бочонок из дощечек, причем встраивание дополнительного мономера ( «дощечки» ) увеличивает периметр поры примерно на 0, 66 нм. 3. Важной особенностью аламетициновых каналов является их зависимость от внешнего электрического поля. 4. В отсутствие разности потенциалов на липидной мембране молекулы антибиотика распластаны на ее поверхности и не образуют каналов. Создание трансмембранной разности потенциалов приводит к тому, что положительный полюс аламетициновой молекулы оказывается на одной стороне мембраны, а отрицательный (глутаминовый остаток) — на другой. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Потенциал покоя - это разность электрических потенциалов между внутренней и наружной сторонами мембраны, когда клетка находится в состоянии физиологического покоя. Его средняя величина составляет -70 м. В (милливольт). Мембранный потенциал покоя - это дефицит положительных зарядов внутри клетки, образовавшийся за счёт утечки из клетки положительных ионов калия. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
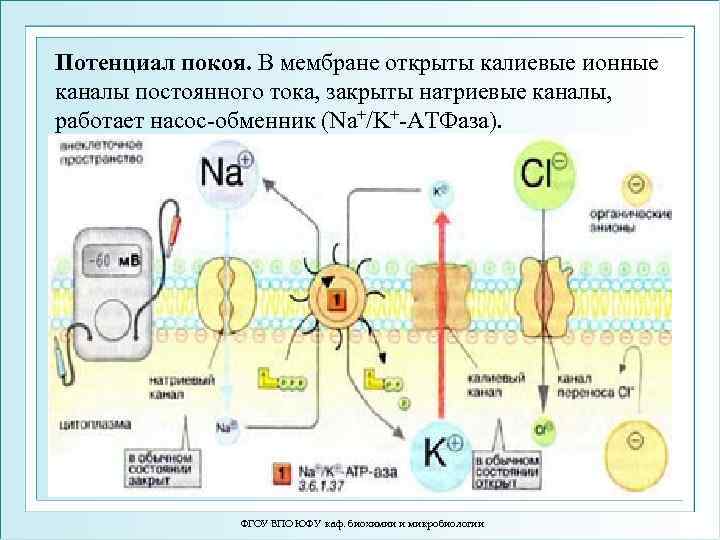
Потенциал покоя. В мембране открыты калиевые ионные каналы постоянного тока, закрыты натриевые каналы, работает насос-обменник (Na+/K+-АТФаза). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Причины отрицательности мембранного потенциала покоя: • Покоящаяся клеточная мембрана более проницаема для ионов К+, чем для других ионов. Поскольку концентрация К+ внутри клетки намного выше, чем снаружи, К+ через калиевые каналы выходит из клетки и создает избыток отрицательного заряда на цитоплазматической стороне клеточной мембраны. Это основной вклад: 60 м. В • Электорогенный Na/К- насос в мембране покоящейся клетки остается активен и также участвует в создании отрицательного заряда внутренней поверхности мембраны. Его вклад: -10 м. В. В сумме это дает -70 м. В. в мышечном волокне в состоянии покоя отношение коэффициентов проницаемости (P) ионов будет следующее: PK+ : PNa+ : PCl— = 1 : 0, 04 : 0, 45. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
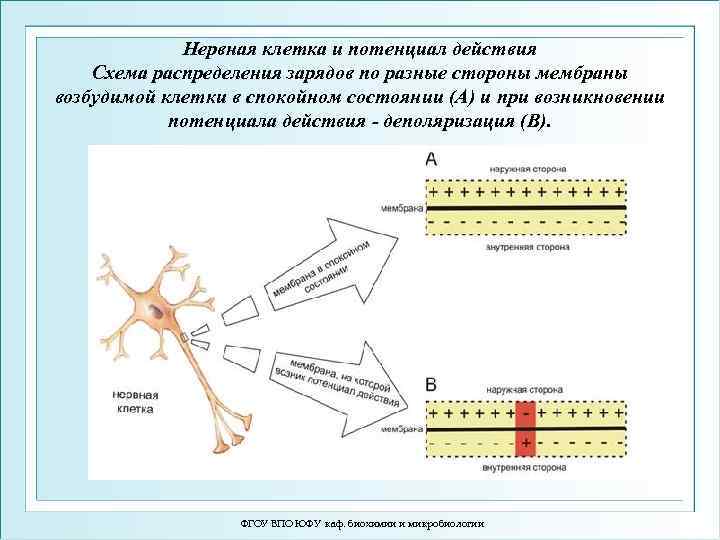
Нервная клетка и потенциал действия Схема распределения зарядов по разные стороны мембраны возбудимой клетки в спокойном состоянии (A) и при возникновении потенциала действия - деполяризация (B). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
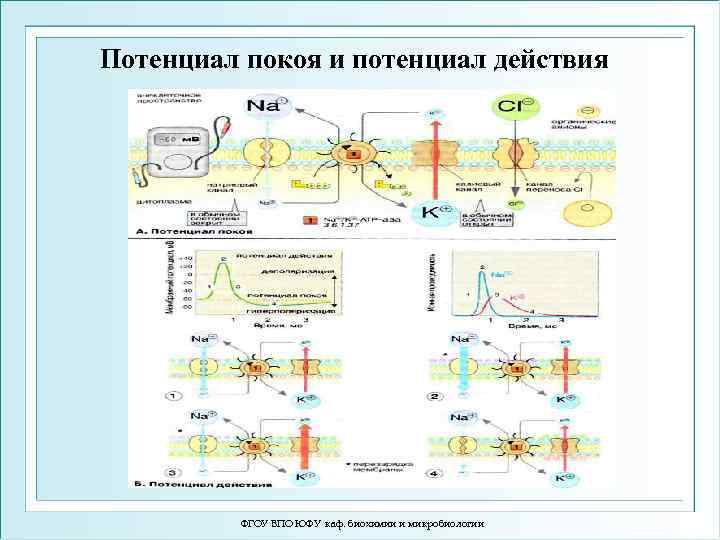
Потенциал покоя и потенциал действия ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
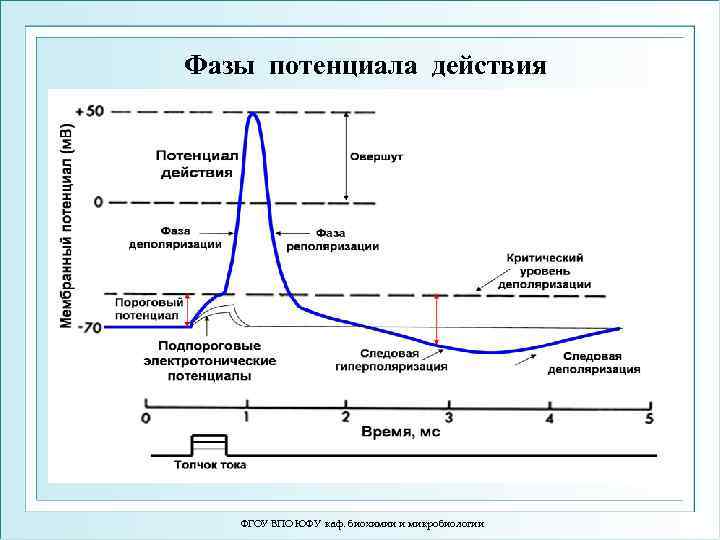
Фазы потенциала действия ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
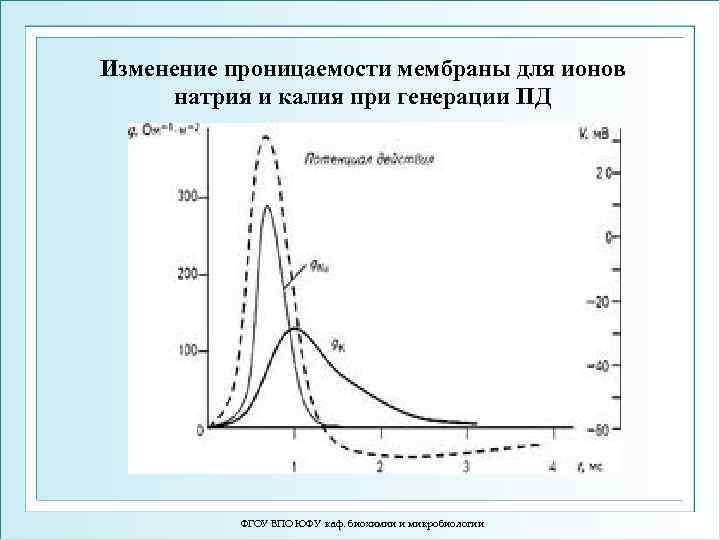
Изменение проницаемости мембраны для ионов натрия и калия при генерации ПД ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
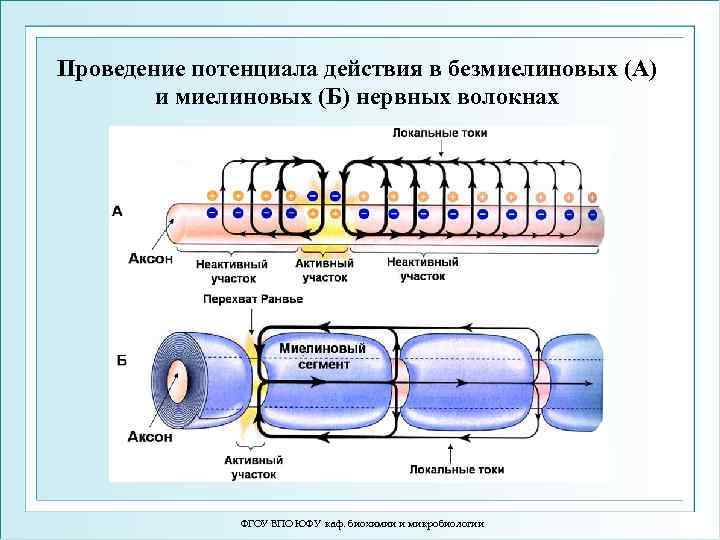
Проведение потенциала действия в безмиелиновых (А) и миелиновых (Б) нервных волокнах ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
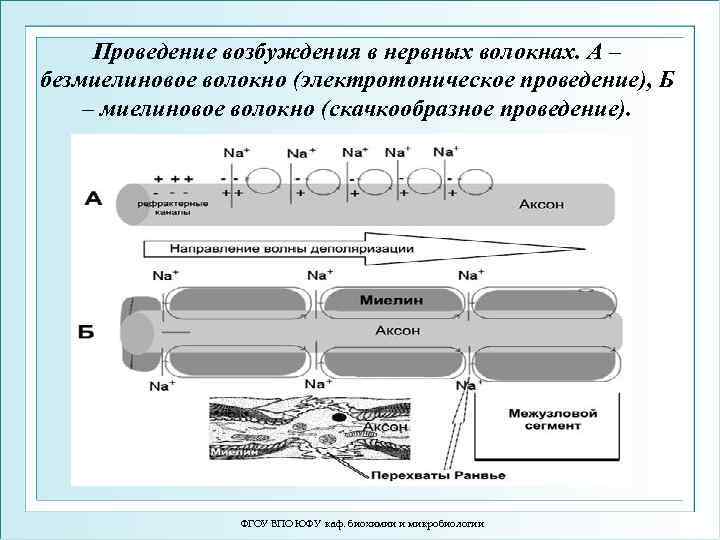
Проведение возбуждения в нервных волокнах. А – безмиелиновое волокно (электротоническое проведение), Б – миелиновое волокно (скачкообразное проведение). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
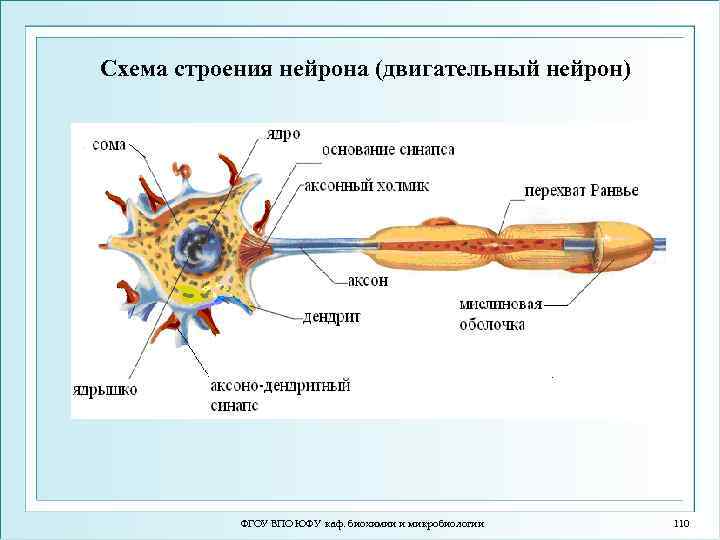
Схема строения нейрона (двигательный нейрон) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 110
4.Каналы_насосы_потенциалы.ppt