7.Биофизика мембран.ppt
- Количество слайдов: 89

Содержание Лекция № 6 Биофизика мембранных процессов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 1
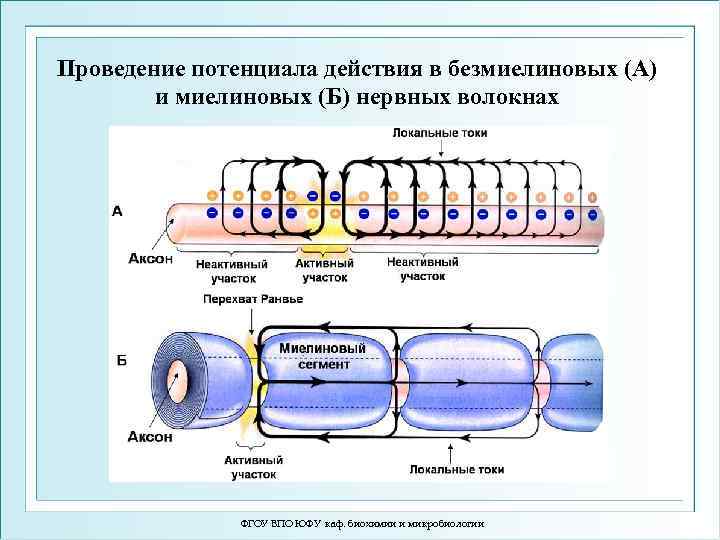
Проведение потенциала действия в безмиелиновых (А) и миелиновых (Б) нервных волокнах ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
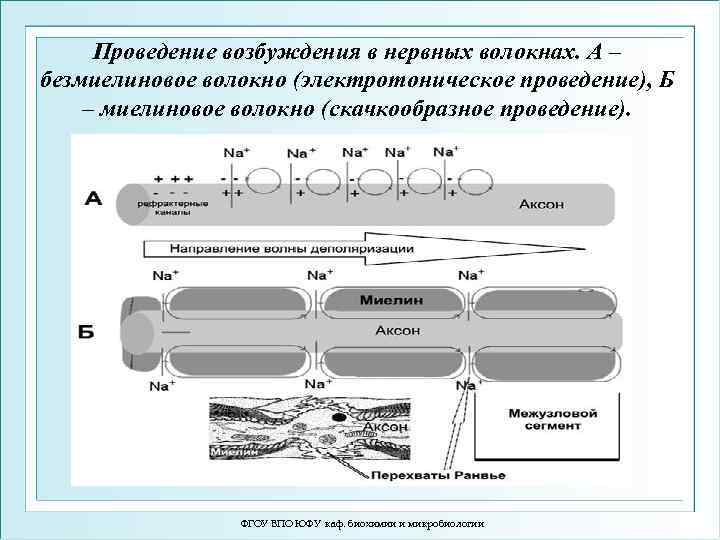
Проведение возбуждения в нервных волокнах. А – безмиелиновое волокно (электротоническое проведение), Б – миелиновое волокно (скачкообразное проведение). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Передача нервного импульса • • Выделяют 2 способа увеличения скорости передачи нервного импульса путем: 1. Увеличения диаметра нервных волокон (уменьшение сопротивления) 2. Уменьшения емкости аксолеммы за счет появления миелиновых волокон. Проведение идет скачками от одного перехвата Ранвье до другого и называется сальтаторным. Обеспечивает экономию энергии: - Скорость проведения больше (25 -140 м/c), чем при непрерывном проведении (0, 5 -0, 7 м/c) - Потребление кислорода в 200 раз меньше, чем при непрерывном проведении - Скорость проведения в миелиновом волокне прямо пропорциональна его диаметру, а в безмиелиновом - √ из величины диаметра. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 4

Окислительно-восстановительный потенциал • • • Реакции, при которых происходит перенос электронов от одних молекул к другим, называются окислительновосстановительными и образуют редокс-систему. Редокс-система характеризуется определенным соотношением окисленных(Ox) и восстановленных (Red) форм - Ox/ Red Способность донора в сопряженной окислительновосстановительной паре отдавать электроны сопряженному акцептору характеризуется окислительно-восстановительным потенциалом (ОВП) - Е 0 ׀ Чем выше ОВП системы, тем сильнее ее окислительные свойства; чем ниже ОВП, тем выше ее восстановительные свойства. Е 0 ׀ характеризует изменение свободной энергии системы при переносе электронов между компонентами ЭТЦ. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 5

• • Для измерения ОВП нужен стандартный электрод сравнения – водородный электрод (платиновая пластинка), погруженный в 1 М раствор Н+ , находящийся в равновесии с газообразным Н 2 при давлении 1 атм. Потенциал стандартного Н-электрода (Е 0 ) условно принимают равным 0 в растворе с активностью ионов Н+ = 1, Т = 298 К, [H] = 1 M Положительный ОВП – показатель более высокого, чем у Н 2 , сродства данного вещества к электронам. Отрицательный ОВП показывает, что вещество имеет меньшее сродство к электронам, чем Н 2. Уравнение редокс-потенциала: Е 0 =׀ Е 0 + RT/n. F • ln[Ox]/[Red] В ЭТЦ митохондрий Е 0 ׀ изменяется от -0, 32 В (в начале цепи) до +0, 82 В в конце цепи, ∆ Е 0 41, 1 = ׀ В Для синтеза 1 мол АТФ требуется ∆ Е 0 81, 0 = ׀ В (34, 5 к. Дж/моль) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 6

Каскад переноса π-электронов по дыхательной цепи. Каждый компонент дыхательной цепи обладает свойствами окислительновосстановительной пары. В окисленном состоянии такая молекула является акцептором электронов; приняв пару электронов, молекула становится донором. При переносе пары пи-электронов с НАД на О 2 разность ОВП составляет 1, 14 В (от -0, 32 В до +0, 82 В) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 7

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 8
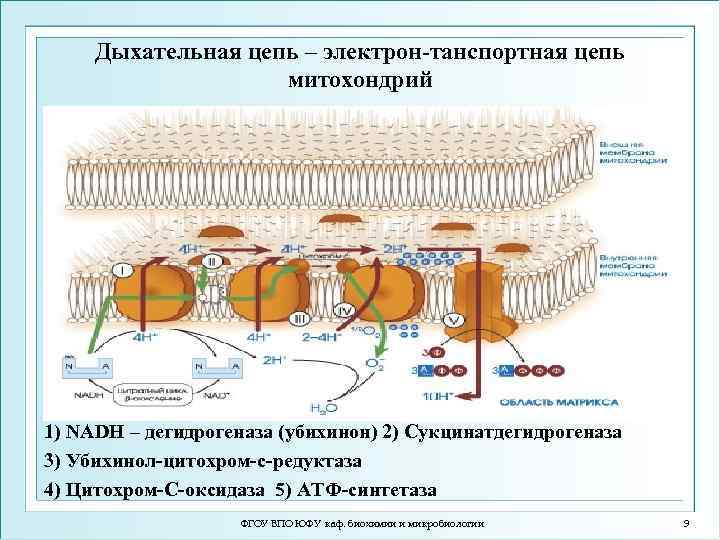
Дыхательная цепь – электрон-танспортная цепь митохондрий 1) NADH – дегидрогеназа (убихинон) 2) Сукцинатдегидрогеназа 3) Убихинол-цитохром-с-редуктаза 4) Цитохром-С-оксидаза 5) АТФ-синтетаза ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 9

Характеристика переносчиков дыхательной цепи. NAD*H – дегидрогеназа или Флавопротеид-1 (ФП-1) Содержит ФМН в качестве кофермента, который акцптирует водород, отщепляемый от NAD*H. Пересекает поперёк внутреннюю мембрану, находясь в окружении липидов. Активный центр обращён к матриксу. Кофермент Q или убихинон [2] Растворён в липидной части мембраны, может диффундировать как поперёк, так и вдоль мембраны. Цитохром b Имеет различные формы. b 562 и b 566, образуют комплекс, пересекающий липидную часть мембраны от внутренней к наружной. Цитохром с1 Расположен в липидном слое ближе к наружной поверхности внутренней мембраны. Цитохром с Относительно легко переходит в водный раствор. Находится на наружной поверхности внутренней мембраны и может выходить в межмембранное пространство. Цитохромы а и а 3 Образуют комплекс, называемый цитохромоксидазой. Комплекс пересекает мембрану поперек. Активный центр цитохрома а 3 обращён в матрикс. Содержит также ионы Cu 2+. Железосерные белки Участвуют в переносе электронов и протонов в дыхательной цепи на двух участках: Между ФП-1 и Q, а также между цитохромами b и c 1 ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 10

Нобелевская премия 1978 года «За вклад в понимание процесса переноса биологической энергии, благодаря созданию хемиосмотической теории» Питер Митчелл (1920 -1992) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 11

Хемиосмотическая теория Митчелла. Главный постулат – сопряжение окисления и фосфорилирования. Перенос электронов по ЭТЦ митохондрий создает, а АТР-синтаза использует трансмембранную разность электрохимических потенциалов протонов ∆μн+ для синтеза АТР. 1 этап – превращение химической энергии переноса электронов в энергию электрохимического градиента протонов - ∆μн+ в результате сопряжения транспорта электронов и переноса протонов через мембрану. Это приводит к возникновению химического градиента (∆р. Н) и электрического градиента (∆φ). Уравнение для электрохимического градиента протонов: ∆μн+ = 2, 3 RT∆р. Н + F ∆φ 2 этап – трансформация энергии ∆μн+ в энергию АТР за счет работы АТР-синтазы. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Положения хемиосмотической теории П. Митчелла (1961) 1. 2. 3. Разница в концентрациях протонов по обе стороны внутренней мембраны митохондрий, создаваемая реакциями окисления, играет роль резервуара энергии. Окисление связано с переносом электронов по ЭТЦ митохондрий. Высвобождение энергии при переносе электронов «вниз» (экзергонический процесс) сопряжен с транспортом протонов «вверх» через непроницаемую для протонов мембрану, что приводит к накоплению свободной энергии электронов в виде трансмембранного электрохимического потенциала протонов - ∆μн+ 4. Поток протонов из межмембранного пространства через протонные каналы по градиенту концентрации дает свободную энергию для синтеза АТР ферментом АТР-синтазой. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 13

Положения хемиосмотической теории П. Митчелла (1961) • Электрохимический градиент протонов включает две составляющих: осмотическую (∆р. Н) и электрическую (∆φ) ∆μн+ = 2, 3 RT∆р. Н + F ∆φ Результирующий эффект – возникновение протон- движущей силы (∆G) химический потенциал→синтез АТР под←электрический потенциал ∆р. Н действием ∆μн+ ∆φ ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 14
![Общая схема окислительного фосфорилирования. [2] Предполагают, что выход протонов из внутренней митохондриальной мембраны в Общая схема окислительного фосфорилирования. [2] Предполагают, что выход протонов из внутренней митохондриальной мембраны в](https://present5.com/presentation/20873161_337905697/image-15.jpg)
Общая схема окислительного фосфорилирования. [2] Предполагают, что выход протонов из внутренней митохондриальной мембраны в цитозоль происходит в трех участках дыхательной цепи: 1. ) Между НАДН и коэнзимом Q. 2. ) Между цитохромами b и c. 3. ) Между цитохромом с и цитохромоксидазой. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 15
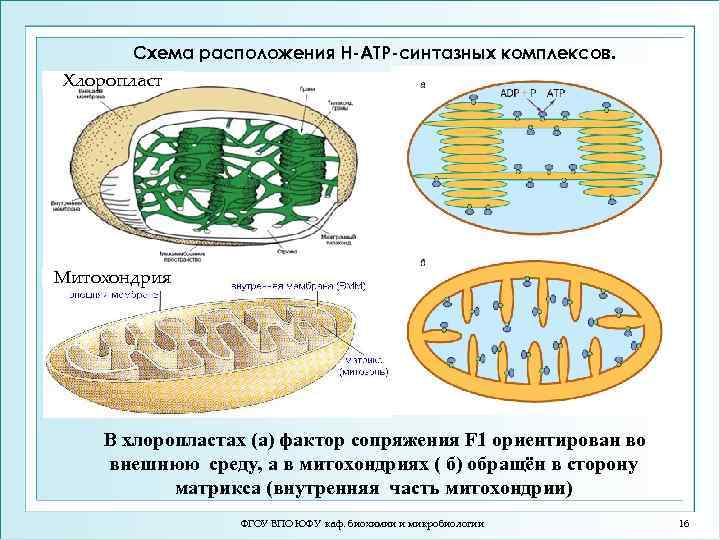
Схема расположения H-ATP-синтазных комплексов. Хлоропласт Митохондрия В хлоропластах (а) фактор сопряжения F 1 ориентирован во внешнюю среду, а в митохондриях ( б) обращён в сторону матрикса (внутренняя часть митохондрии) ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 16

Нобелевской премии 1997 года по химии «за установление ферментативного механизма, управляющего синтезом аденозинтрифосфата (АТФ)» . Пол Бойер. Джон Уокер. «Все ферменты красивы, но АТФ-синтаза является одним из самых красивых, а также самых необычных и важных» (П. Бойер, 1997). ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 17
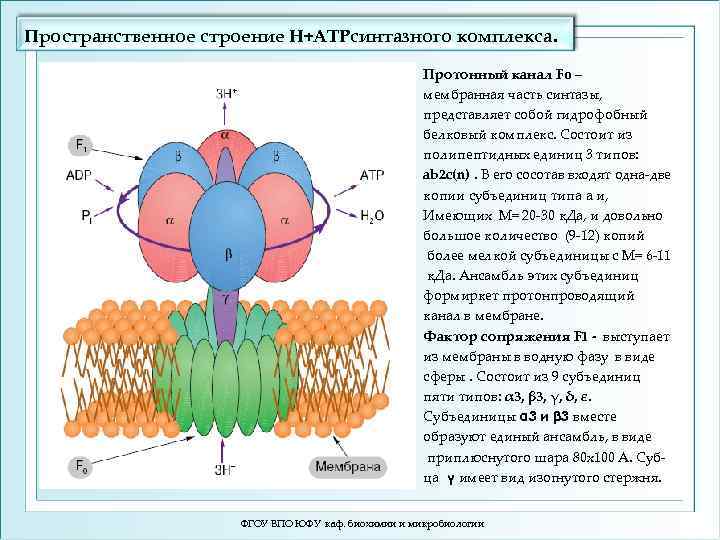
Пространственное строение H+ATPсинтазного комплекса. Протонный канал Fo – мембранная часть синтазы, представляет собой гидрофобный белковый комплекс. Состоит из полипептидных единиц 3 типов: ab 2 c(n). В его сосотав входят одна-две копии субъединиц типа a и, Имеющих М= 20 -30 к. Да, и довольно большое количество (9 -12) копий более мелкой субъединицы с М= 6 -11 к. Да. Ансамбль этих субъединиц формиркет протонпроводящий канал в мембране. Фактор сопряжения F 1 - выступает из мембраны в водную фазу в виде сферы. Состоит из 9 субъединиц пяти типов: α 3, β 3, γ, δ, ε. Субъединицы α 3 и β 3 вместе образуют единый ансамбль, в виде приплюснутого шара 80 х100 А. Субца γ имеет вид изогнутого стержня. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
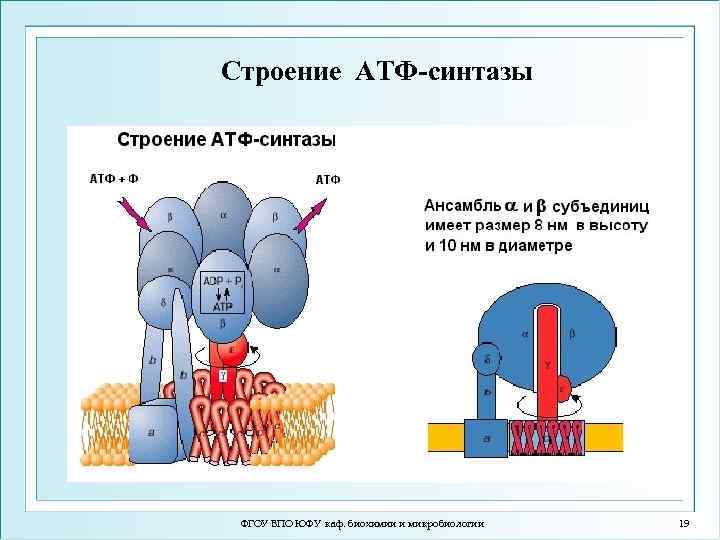
Строение АТФ-синтазы ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 19
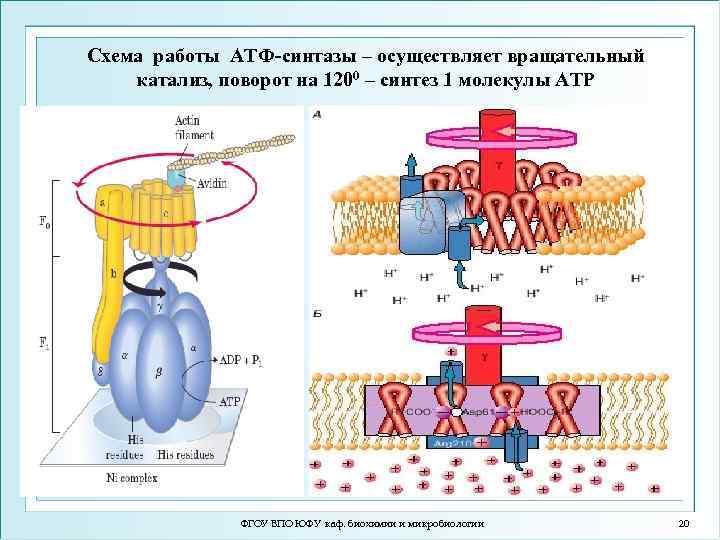
Схема работы АТФ-синтазы – осуществляет вращательный катализ, поворот на 1200 – синтез 1 молекулы АТР ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 20
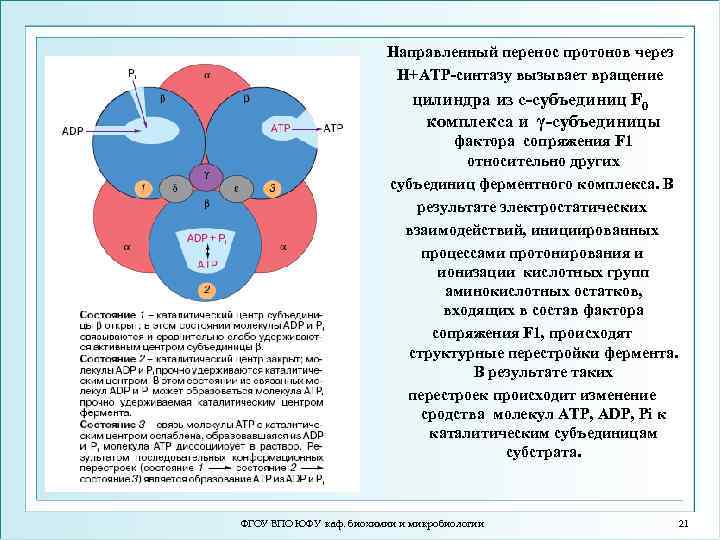
Направленный перенос протонов через H+ATP-синтазу вызывает вращение цилиндра из с-субъединиц F 0 комплекса и γ-субъединицы фактора сопряжения F 1 относительно других субъединиц ферментного комплекса. В результате электростатических взаимодействий, инициированных процессами протонирования и ионизации кислотных групп аминокислотных остатков, входящих в состав фактора сопряжения F 1, происходят структурные перестройки фермента. В результате таких перестроек происходит изменение сродства молекул ATP, ADP, Pi к каталитическим субъединицам субстрата. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 21
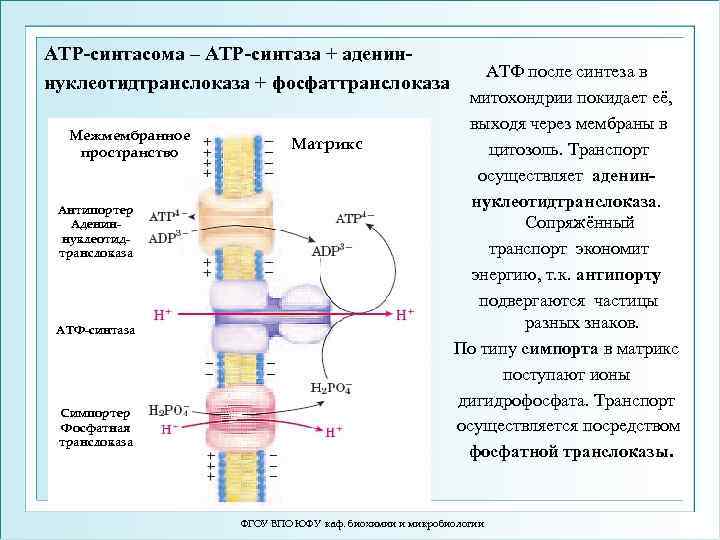
АТР-синтасома – АТР-синтаза + адениннуклеотидтранслоказа + фосфаттранслоказа Межмембранное пространство Антипортер Адениннуклеотидтранслоказа АТФ-синтаза Симпортер Фосфатная транслоказа Матрикс АТФ после синтеза в митохондрии покидает её, выходя через мембраны в цитозоль. Транспорт осуществляет адениннуклеотидтранслоказа. Сопряжённый транспорт экономит энергию, т. к. антипорту подвергаются частицы разных знаков. По типу симпорта в матрикс поступают ионы дигидрофосфата. Транспорт осуществляется посредством фосфатной транслоказы. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
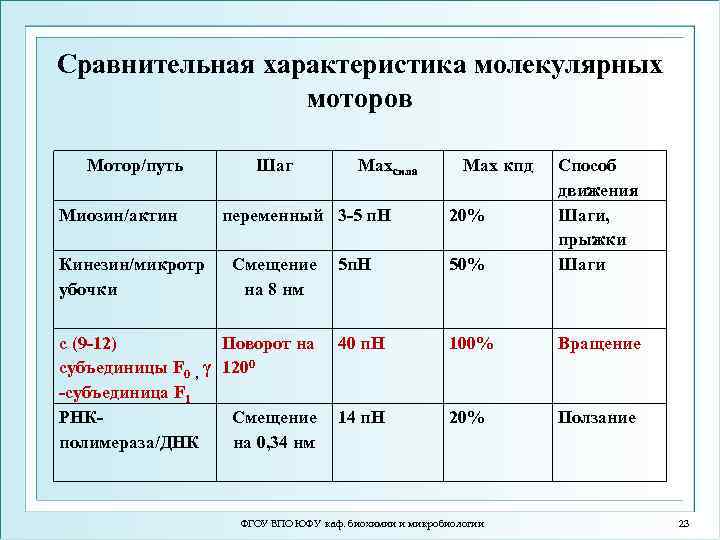
Сравнительная характеристика молекулярных моторов Мотор/путь Миозин/актин Кинезин/микротр убочки Шаг Maxсила переменный 3 -5 п. Н Смещение на 8 нм 5 п. Н с (9 -12) Поворот на 40 п. Н субъединицы F 0 , γ 1200 -субъединица F 1 РНКСмещение 14 п. Н полимераза/ДНК на 0, 34 нм Max кпд 50% Способ движения Шаги, прыжки Шаги 100% Вращение 20% Ползание 20% ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 23
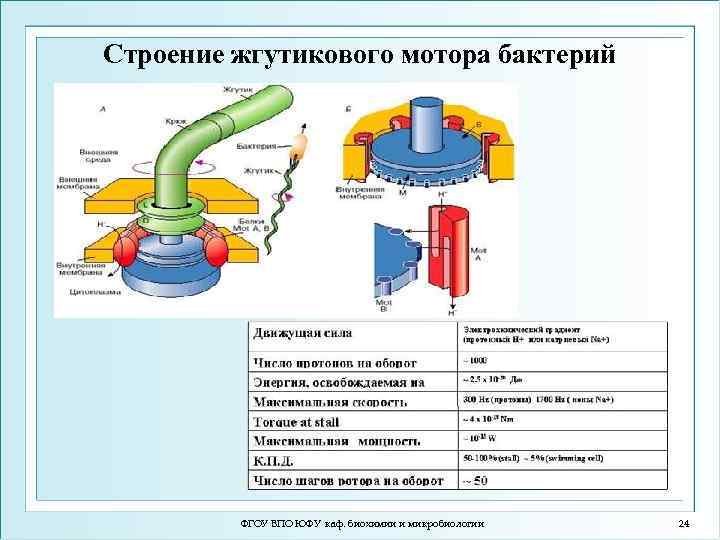
Строение жгутикового мотора бактерий ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 24
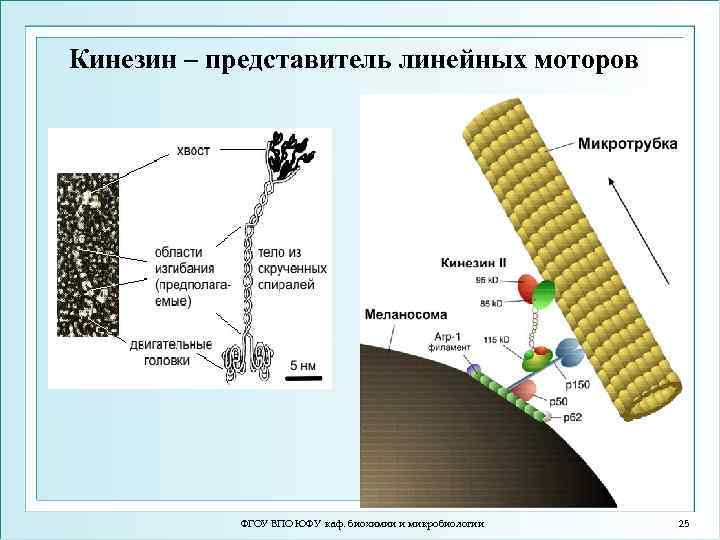
Кинезин – представитель линейных моторов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 25
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 26
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 27

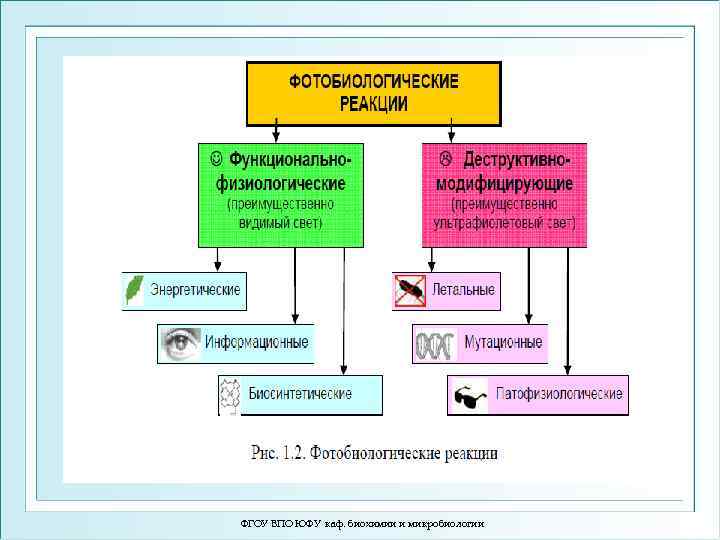
Фотобиология ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 28
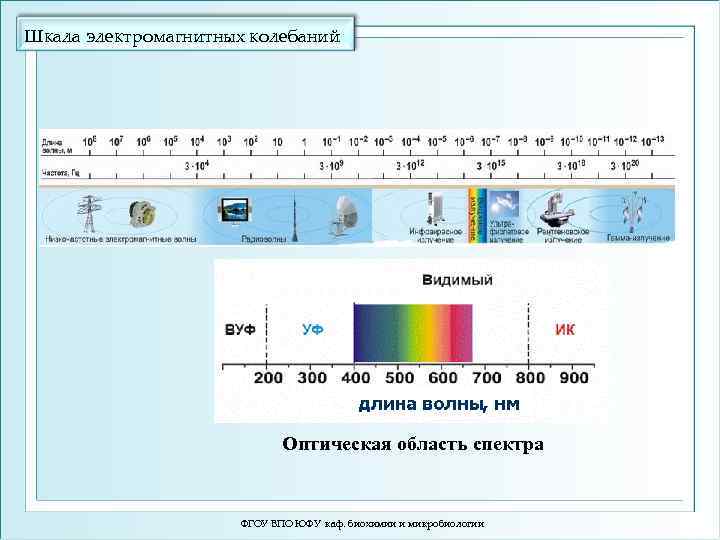
Шкала электромагнитных колебаний Оптическая область спектра ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Закон Бугера-Ламберта-Бера Зако н Буге ра — Ла мберта — Бе ра — физический закон, определяющий ослабление параллельного монохроматического пучка света при распространении его в поглощающей среде. Закон выражается следующей формулой: I (l) = I 0 e-Kλl или lg I 0I = ε c l D=εcl где I 0 — интенсивность входящего пучка, l — толщина слоя вещества, через которое проходит свет, kλ — показатель поглощения, D – оптическая плотность раствора 1. Оптическая плотность 1 М раствора называется молярной экстинкцией. 2. Свет различных длин волн поглощается неодинаково. 3. Показатель поглощения — коэффициент, характеризующий свойства вещества и зависящий от длины волны λ поглощаемого света. Эта зависимость называется спектром поглощения вещества. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
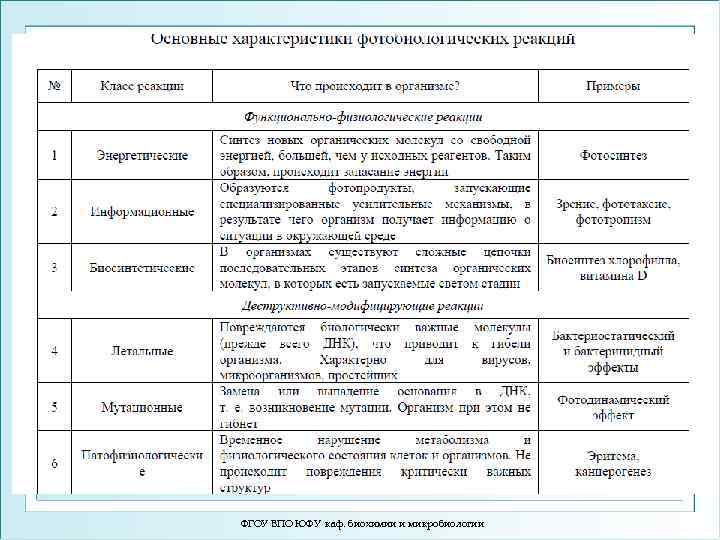
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
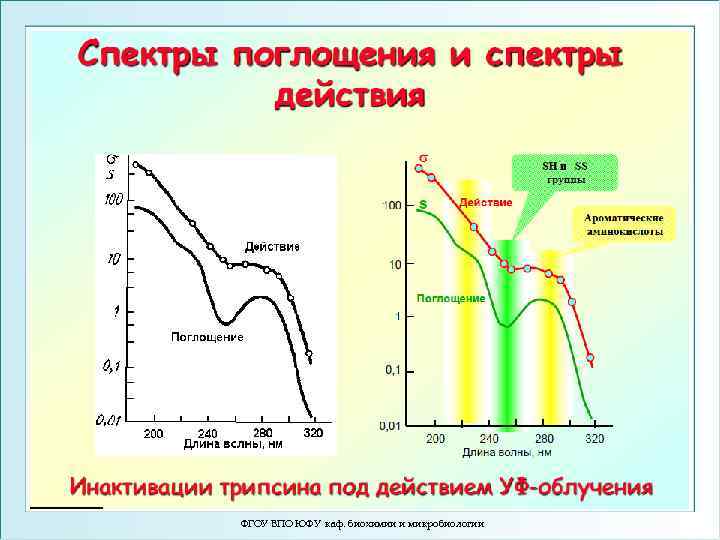
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
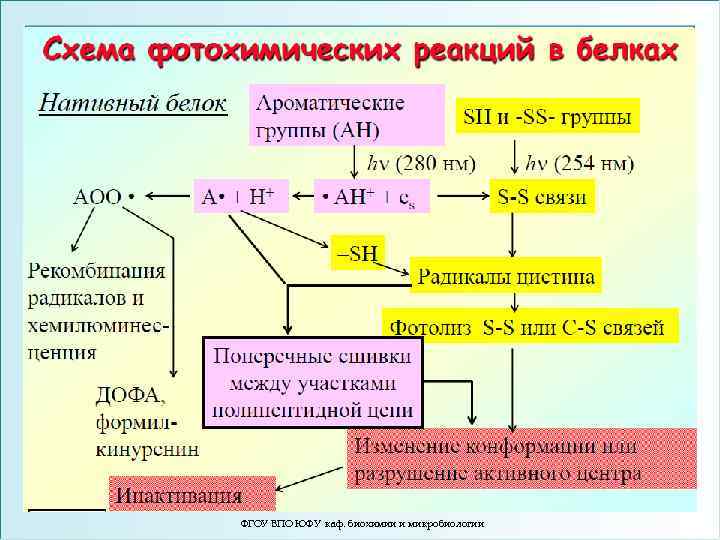
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 38
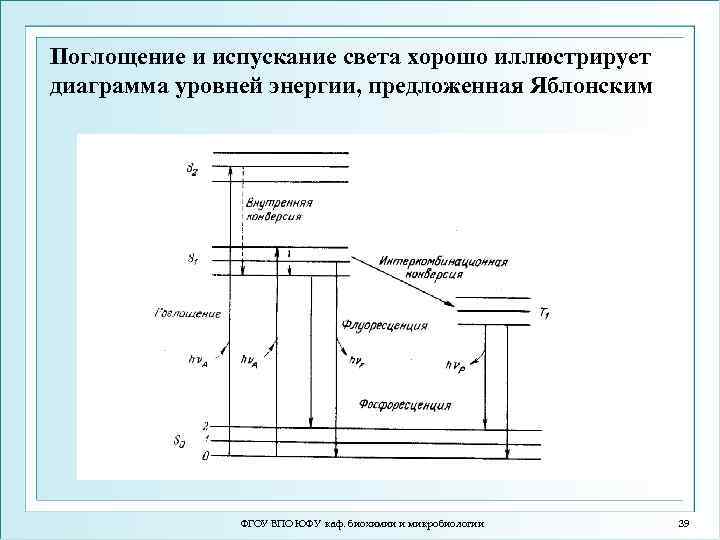
Поглощение и испускание света хорошо иллюстрирует диаграмма уровней энергии, предложенная Яблонским ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 39
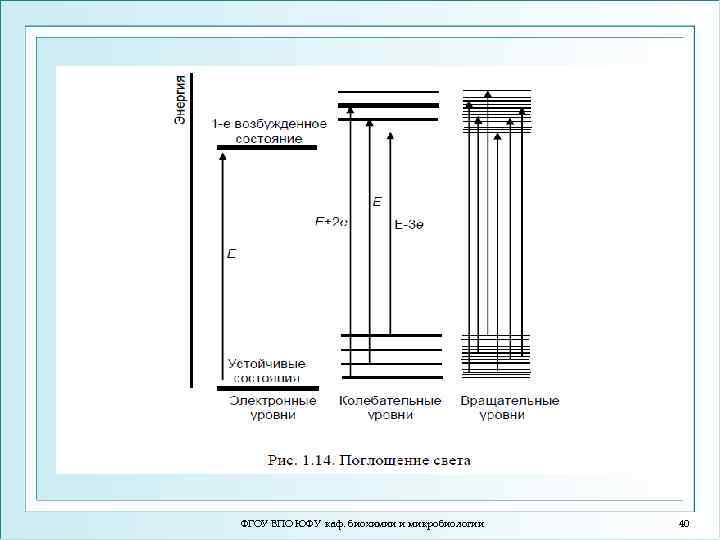
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 40
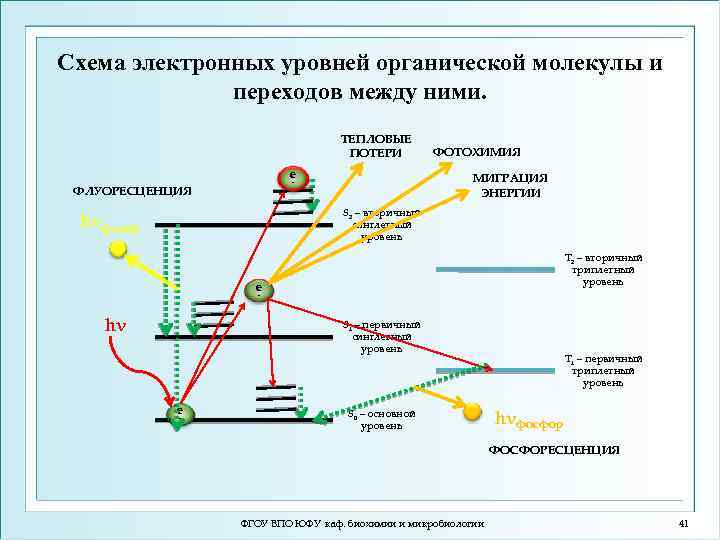
Схема электронных уровней органической молекулы и переходов между ними. ТЕПЛОВЫЕ ПОТЕРИ e МИГРАЦИЯ ЭНЕРГИИ - ФЛУОРЕСЦЕНЦИЯ ФОТОХИМИЯ S 2 – вторичный синглетный уровень hνфлуор Т 2 – вторичный триплетный уровень e - hν S 1 – первичный синглетный уровень e - S 0 – основной уровень Т 1 – первичный триплетный уровень hνфосфор ФОСФОРЕСЦЕНЦИЯ ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 41

Принцип Франка - Кондона. Время, в течение которого квант света поглощается и электрон перебрасывается на возбужденный уровень, составляет 10 -15 с. Период колебательных процессов молекулы (смещение ядер относительно положения равновесия) значительно больше 10 -13 с, поэтому за время электронного перехода положение ядер в пространстве практически не изменяется. В системе кривых потенциальной энергии основного и возбужденного поглощение изображается вертикальной стрелкой. «Невертикальные» переходы наименее вероятны. Это так называемый принцип Франка — Кондона. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 42

Индуктивно-резонансный механизм передачи энергии осуществляется при слабых энергиях взаимодействия между молекулами. Время миграции τ м >> 10 -12 с. Расстояния переноса энергии 2 -10 нм ~ 10 -13 c hν фл S 0 донор S 0 акцептор ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 43
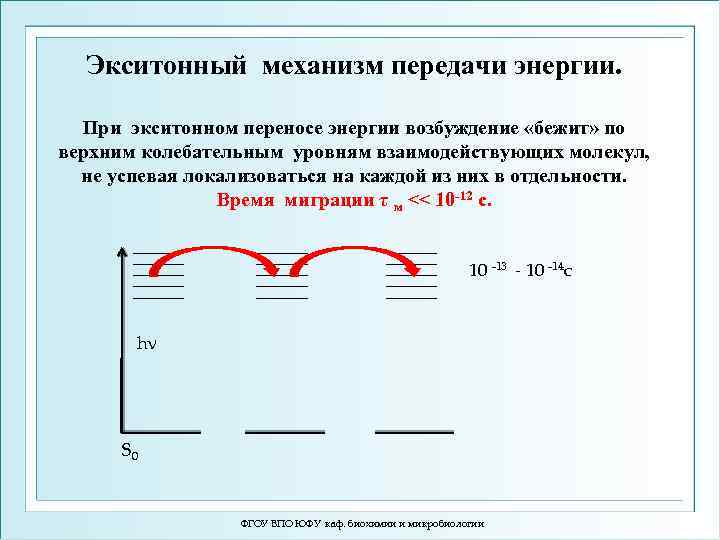
Экситонный механизм передачи энергии. При экситонном переносе энергии возбуждение «бежит» по верхним колебательным уровням взаимодействующих молекул, не успевая локализоваться на каждой из них в отдельности. Время миграции τ м << 10 -12 с. 10 -13 - 10 -14 c hν S 0 ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

1877 г. - Франц Болл открыл зрительный пурпур – родопсин сетчатки глаза, наблюдая выцветание сетчатки лягушки при освещении. 1967 г. – Джордж Уолд - Нобелевская премия по физиологии и медицине «за открытия, связанные с первичными физиологическими и химическими зрительными процессами» ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
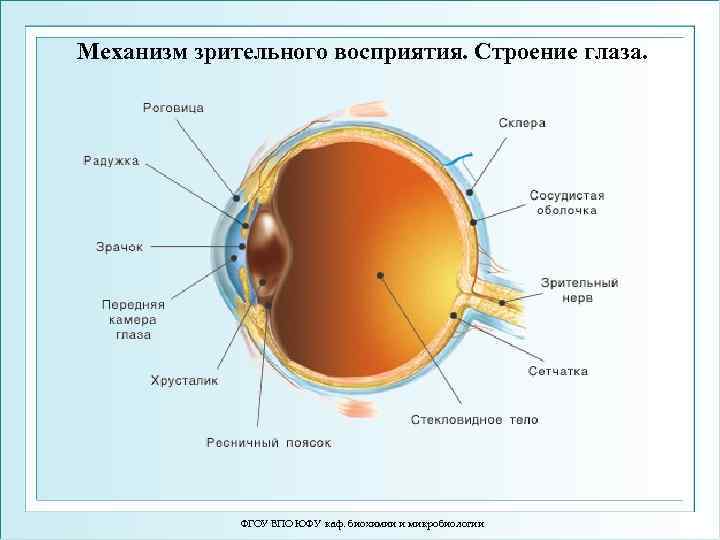
Механизм зрительного восприятия. Строение глаза. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
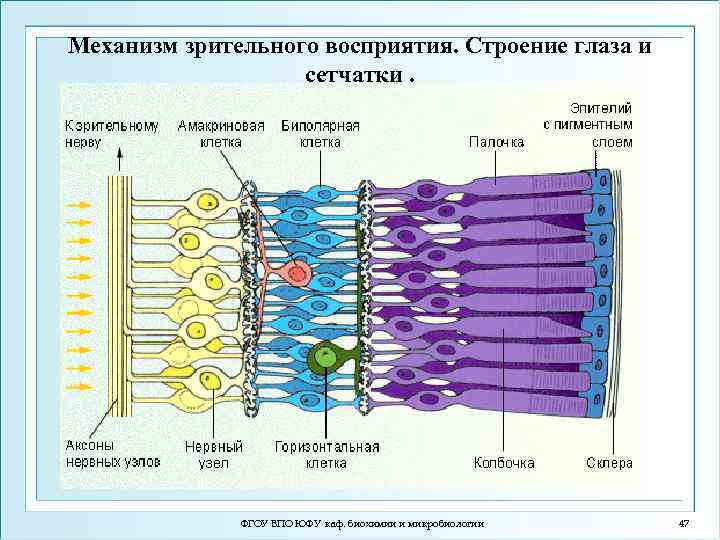
Механизм зрительного восприятия. Строение глаза и сетчатки. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 47
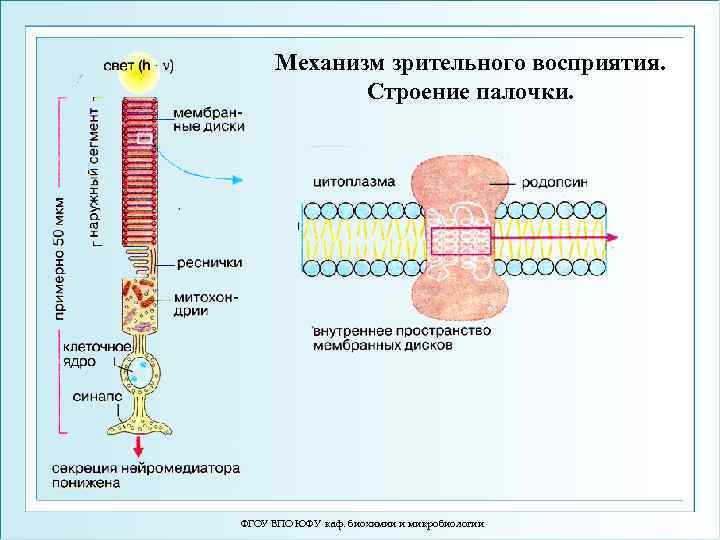
Механизм зрительного восприятия. Строение палочки. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
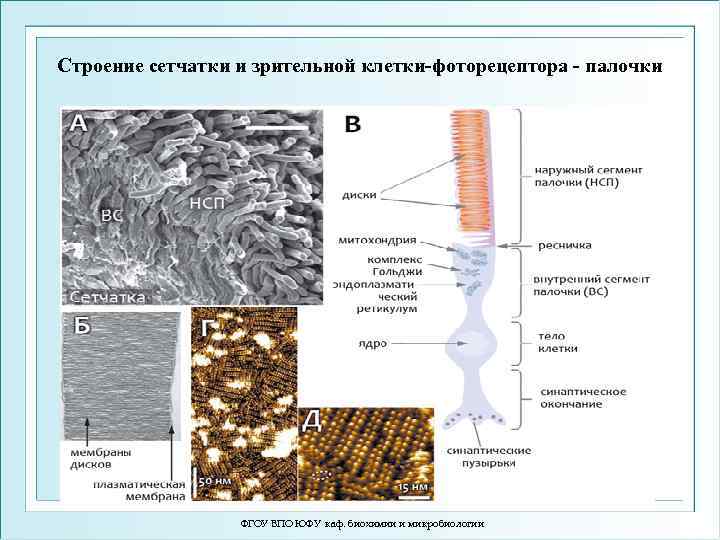
Строение сетчатки и зрительной клетки-фоторецептора - палочки ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
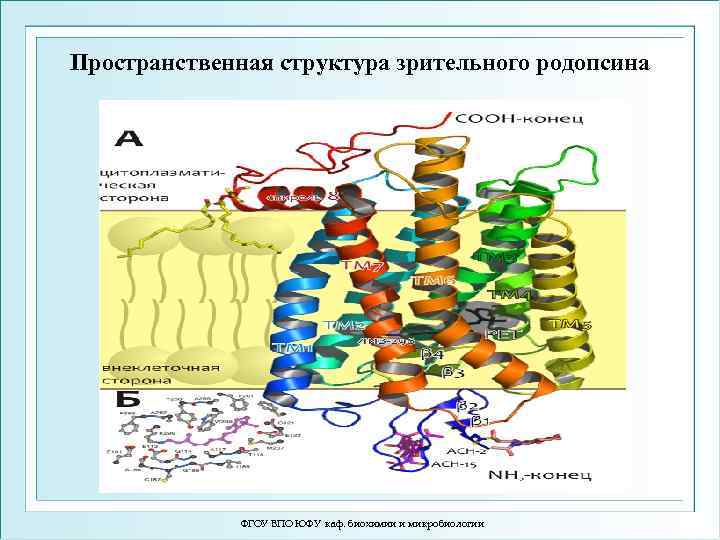
Пространственная структура зрительного родопсина ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
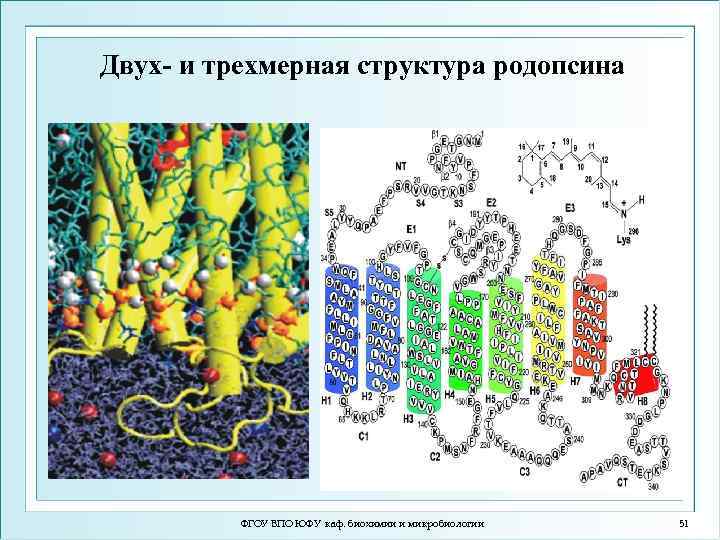
Двух- и трехмерная структура родопсина ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 51
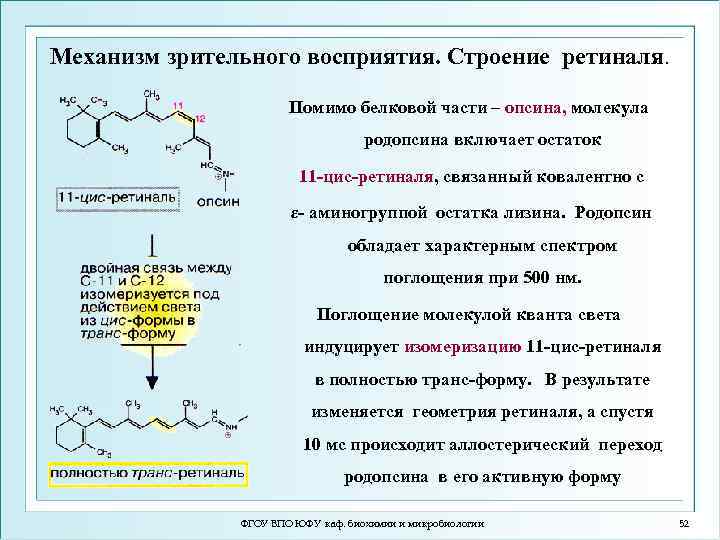
Механизм зрительного восприятия. Строение ретиналя. Помимо белковой части – опсина, молекула родопсина включает остаток 11 -цис-ретиналя, связанный ковалентно с ε- аминогруппой остатка лизина. Родопсин обладает характерным спектром поглощения при 500 нм. Поглощение молекулой кванта света индуцирует изомеризацию 11 -цис-ретиналя в полностью транс-форму. В результате изменяется геометрия ретиналя, а спустя 10 мс происходит аллостерический переход родопсина в его активную форму ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 52
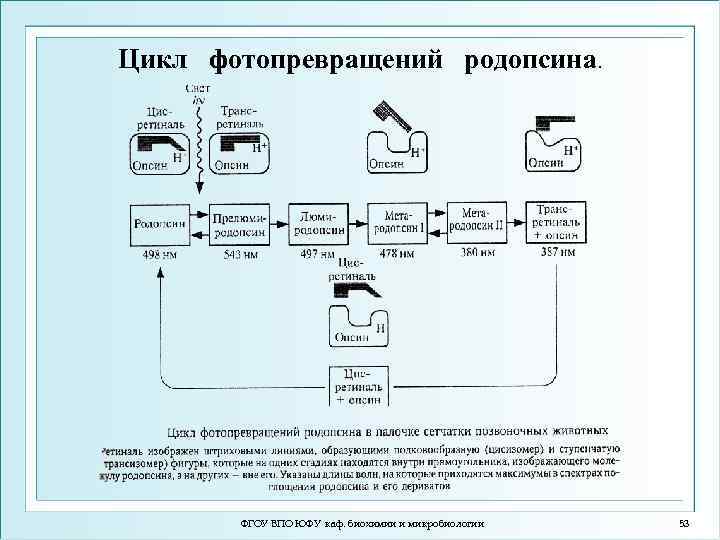
Цикл фотопревращений родопсина. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 53
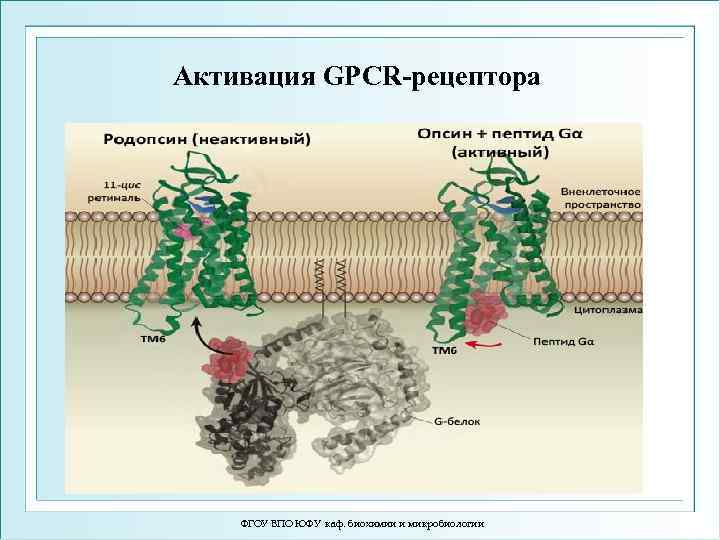
Активация GPCR-рецептора ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
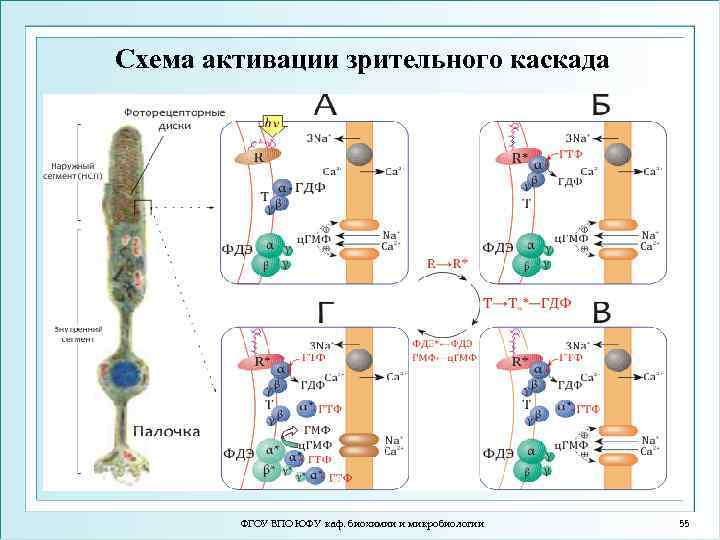
Схема активации зрительного каскада ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 55
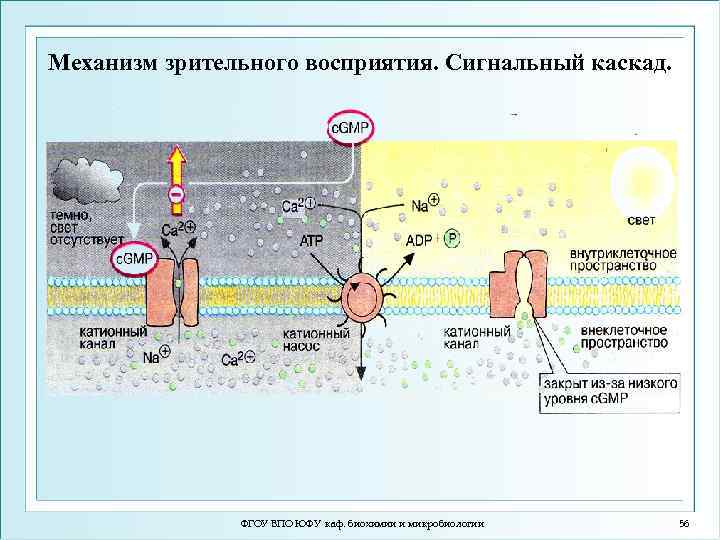
Механизм зрительного восприятия. Сигнальный каскад. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 56
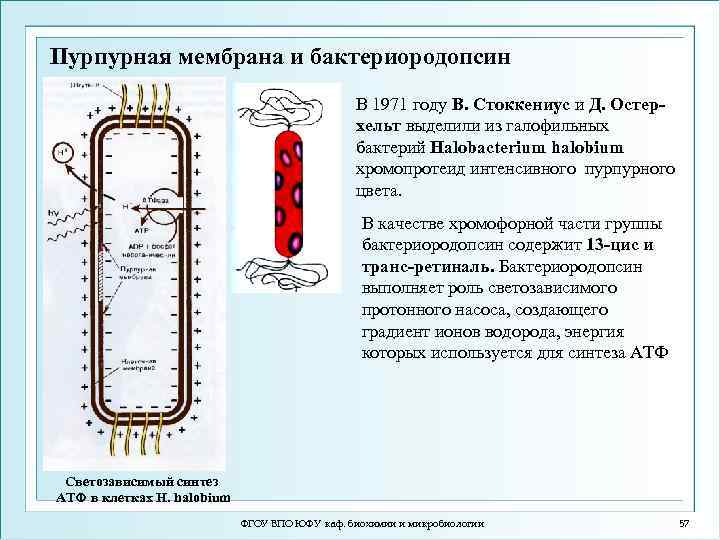
Пурпурная мембрана и бактериородопсин В 1971 году В. Стоккениус и Д. Остерхельт выделили из галофильных бактерий Halobacterium halobium хромопротеид интенсивного пурпурного цвета. В качестве хромофорной части группы бактериородопсин содержит 13 -цис и транс-ретиналь. Бактериородопсин выполняет роль светозависимого протонного насоса, создающего градиент ионов водорода, энергия которых используется для синтеза АТФ Светозависимый синтез АТФ в клетках H. halobium ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 57
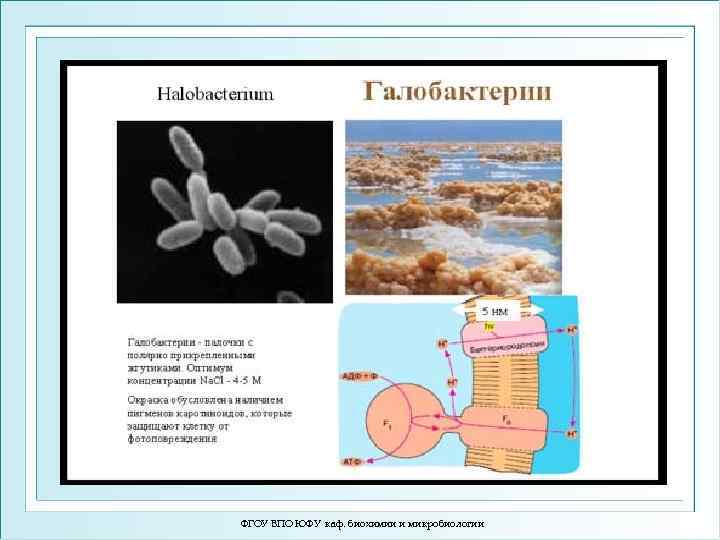
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Пруды на юге Мертвого моря с галобактериями ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
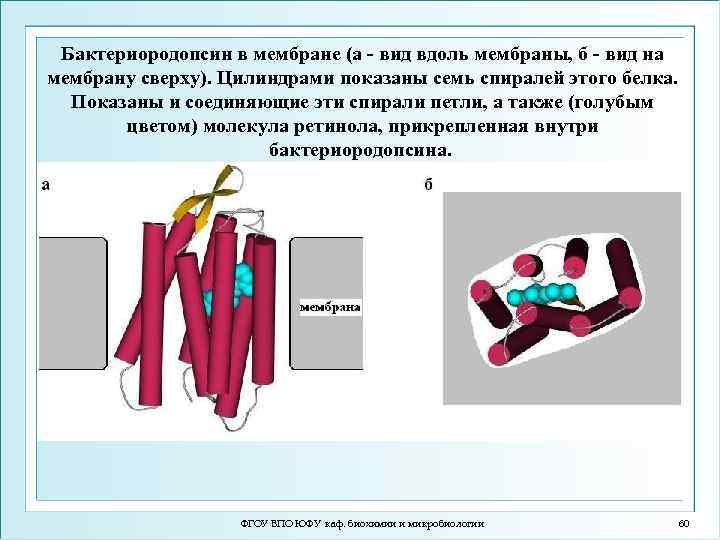
Бактериородопсин в мембране (а - вид вдоль мембраны, б - вид на мембрану сверху). Цилиндрами показаны семь спиралей этого белка. Показаны и соединяющие эти спирали петли, а также (голубым цветом) молекула ретинола, прикрепленная внутри бактериородопсина. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 60
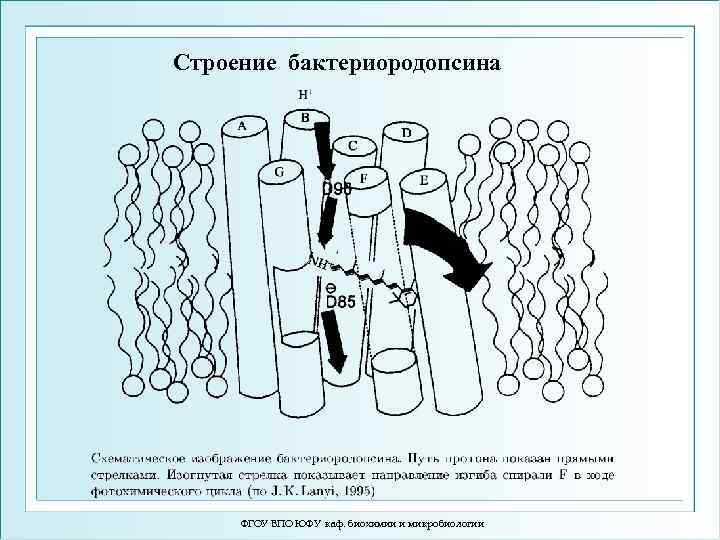
Строение бактериородопсина ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
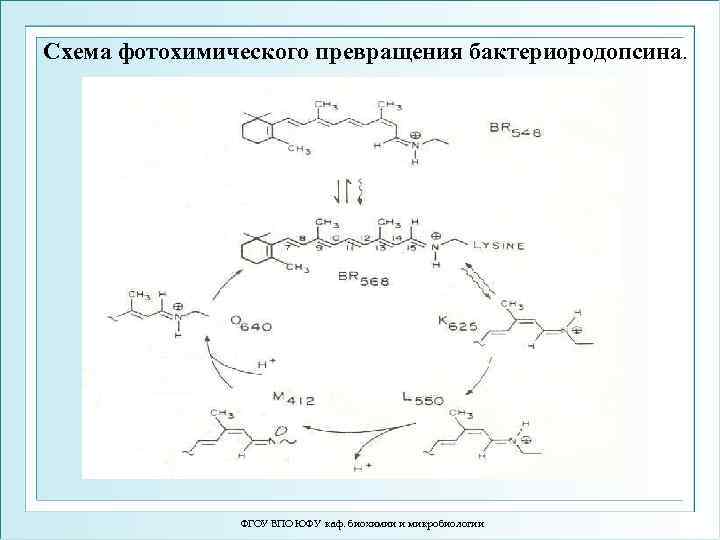
Схема фотохимического превращения бактериородопсина. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Технические приложения бактериородопсина (проекты): протонный транспорт: генерация АТФ в реакторах; опреснение морской воды; генерация электрической энергии из света; фотоэлектрические применения: ультрабыстрая световая детекция; искусственная сетчатка; детекция подвижности; фотохромные применения: хранение информации: 2 D-носители; 3 D-носители; голографические носители; различные применения: детекция радиации; биосенсорные приложения. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

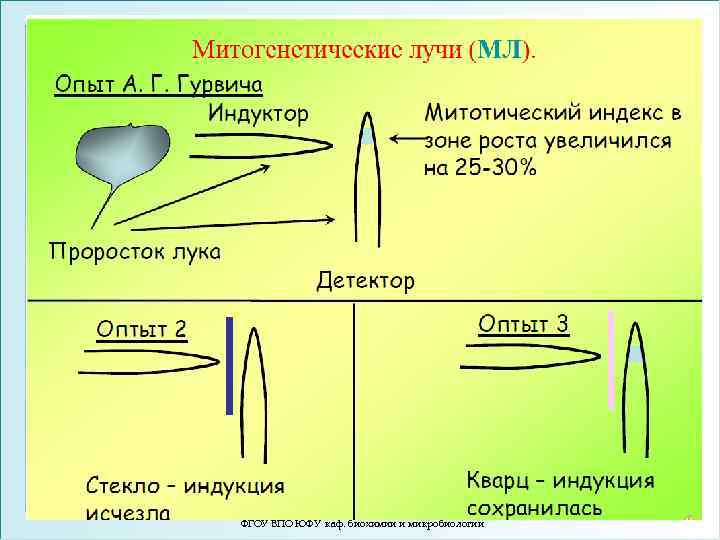
А. Г. Гурвич 1934 год Александр Гурвич предложил полевую модель развития живого от одноклеточной стадии к многоклеточной. В 1923 году Гурвич обнаружил митогенетическое излучение делящихся клеток и определил его диапазон (область ультрафиолетового излучения: λ = 180 -300 нм). Согласно его взглядам, поле клетки и организма создает и поддерживает в живых системах специфическую молекулярную упорядоченность. В многоклеточном организме электромагнитное поле, генерируемое одиночными клетками, выходит за их пределы. В результате полевого взаимодействия между различными клетками, формируется общее поле организма, которое играет важную роль в различных физиологических процессах. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
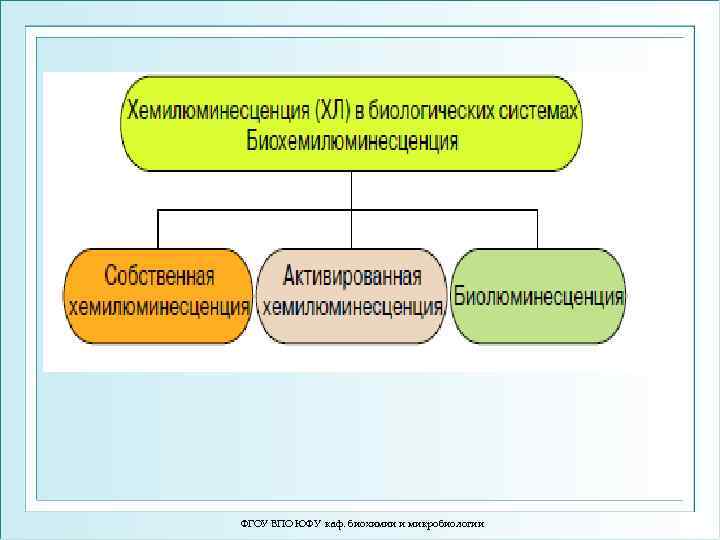
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Биолюминесце нция — способность живых организмов светиться, достигаемая самостоятельно или с помощью симбионтов. Это видимое глазом (т. е. весьма интенсивное свечение). Биолюминесценция связана со специфическими ферментативными реакциями, при которых освобождающаяся энергия выделяется в виде света. Специфический фермент называется люциферазой, а его субстрат – люциферином. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
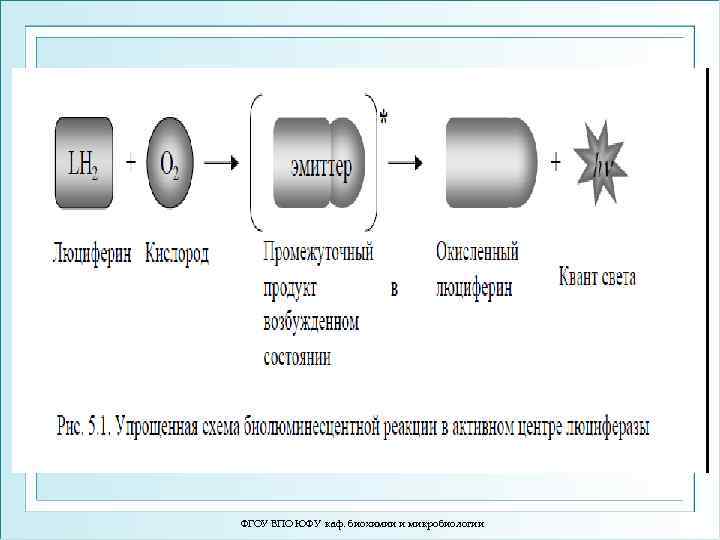
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
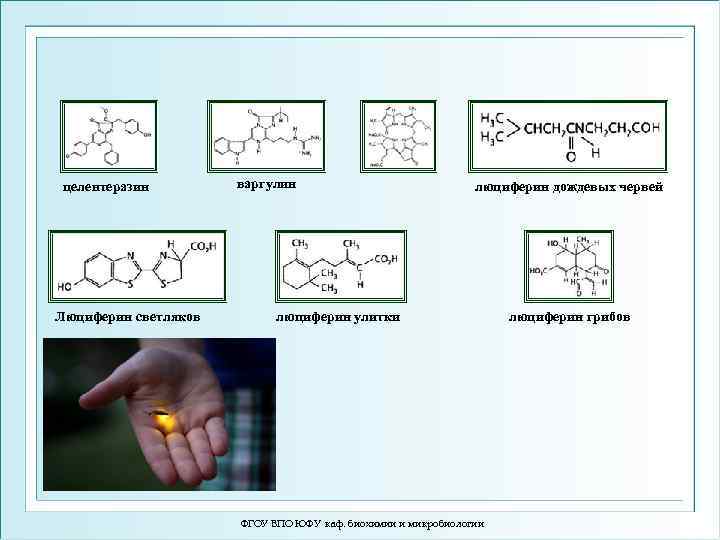
целентеразин Люциферин светляков варгулин люциферин дождевых червей люциферин улитки ФГОУ ВПО ЮФУ каф. биохимии и микробиологии люциферин грибов
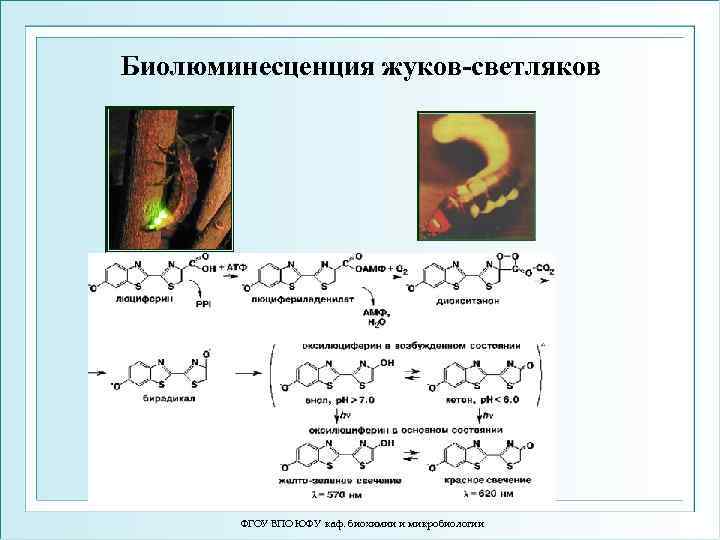
Биолюминесценция жуков-светляков ФГОУ ВПО ЮФУ каф. биохимии и микробиологии
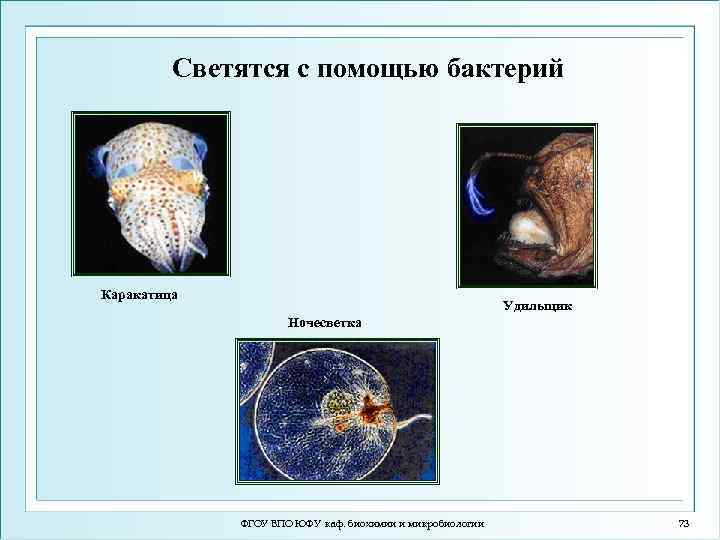
Светятся с помощью бактерий Каракатица Удильщик Ночесветка ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 73
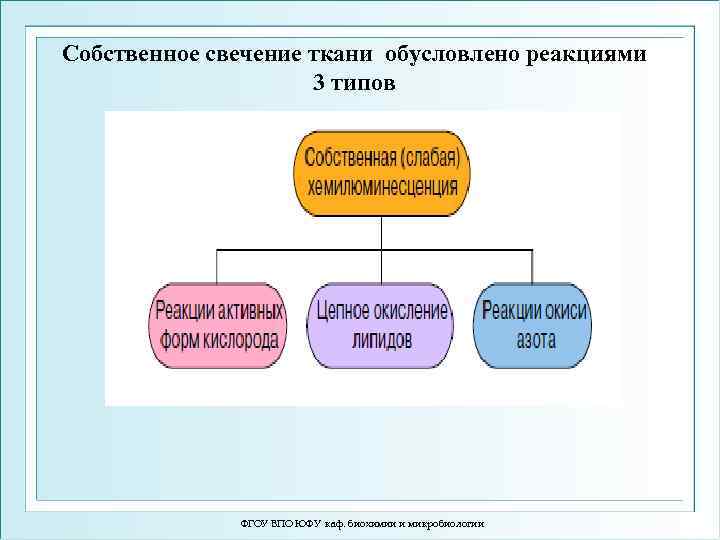
Собственное свечение ткани обусловлено реакциями 3 типов ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

ФГОУ ВПО ЮФУ каф. биохимии и микробиологии

Биолюминесценция медузы эквореи целентеразин Экворин — люминесцентный белок из медузы эквореи (Aequorea victoria) и некоторых других морских организмов. Впервые выделен в 1961— 1962 годах американскими учеными Джонсоном и Шимомурой. Состоит из белковой части (апопротеин) и простетической группы целентеразина Люминесцирует в присутствии ионов кальция. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 77

Исследование биолюминесцентной системы медузы Aequorea victoria Осама Шимомурой привели к открытию 2 белков – Са-регулируемого фотопротеина экворина и зеленого флуоресцирующего белка (GFP). Биолюминесценция экворина инициируется ионами Са и не зависит от кислорода. Фотопротеин образует стабильный комплекс белка и субстрата целентеразина. GFP излучает зеленый цвет, стал эффективным инструментом в био- и медицинских исследованиях как светящийся индикатор изучения живой клетки. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 78

Шимомура обнаружил, что выделенный из медузы и очищенный экворин in vitro излучает синий свет, в то время как живая медуза светится зелёным. Дальнейшие исследования показали, что за зелёное свечение ответственен другой белок — GFP (green fluorescent protein — зелёный флуоресцентный белок), флуоресцирующий зелёным светом под действием голубого излучния экворина. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 79
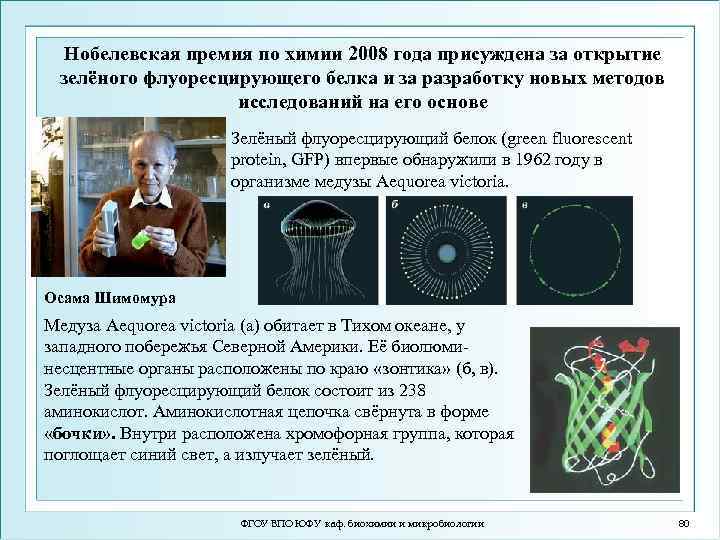
Нобелевская премия по химии 2008 года присуждена за открытие зелёного флуоресцирующего белка и за разработку новых методов исследований на его основе Зелёный флуоресцирующий белок (green fluorescent protein, GFP) впервые обнаружили в 1962 году в организме медузы Aequorea victoria. Осама Шимомура Медуза Aequorea victoria (а) обитает в Тихом океане, у западного побережья Северной Америки. Её биолюминесцентные органы расположены по краю «зонтика» (б, в). Зелёный флуоресцирующий белок состоит из 238 аминокислот. Аминокислотная цепочка свёрнута в форме «бочки» . Внутри расположена хромофорная группа, которая поглощает синий свет, а излучает зелёный. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 80
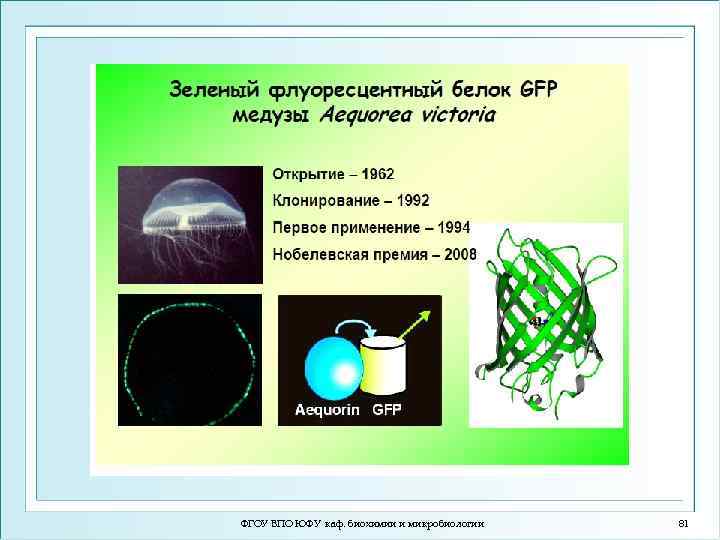
ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 81
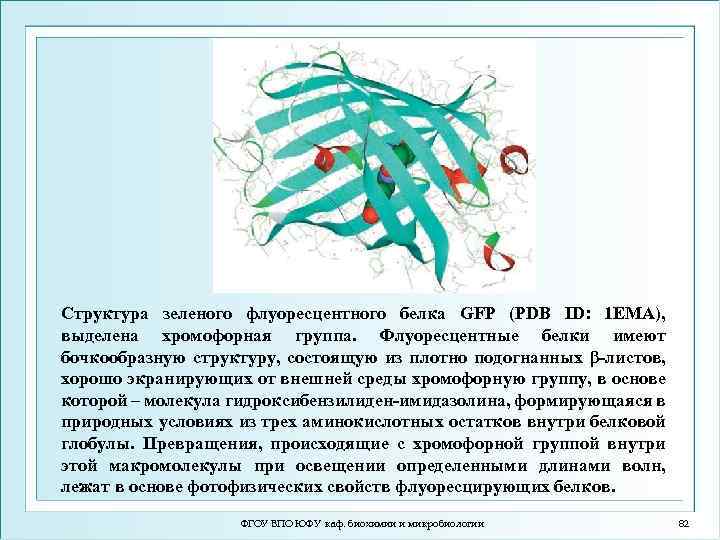
Структура зеленого флуоресцентного белка GFP (PDB ID: 1 EMA), выделена хромофорная группа. Флуоресцентные белки имеют бочкообразную структуру, состоящую из плотно подогнанных β-листов, хорошо экранирующих от внешней среды хромофорную группу, в основе которой – молекула гидроксибензилиден-имидазолина, формирующаяся в природных условиях из трех аминокислотных остатков внутри белковой глобулы. Превращения, происходящие с хромофорной группой внутри этой макромолекулы при освещении определенными длинами волн, лежат в основе фотофизических свойств флуоресцирующих белков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 82
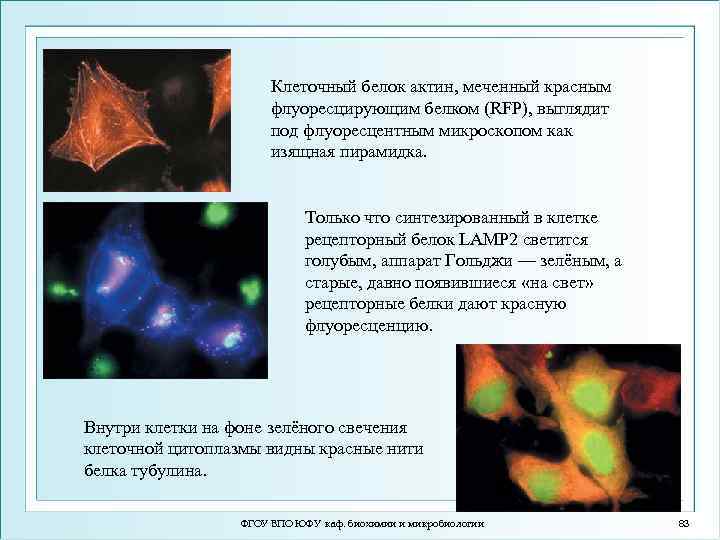
Клеточный белок актин, меченный красным флуоресцирующим белком (RFP), выглядит под флуоресцентным микроскопом как изящная пирамидка. Только что синтезированный в клетке рецепторный белок LAMP 2 светится голубым, аппарат Гольджи — зелёным, а старые, давно появившиеся «на свет» рецепторные белки дают красную флуоресценцию. Внутри клетки на фоне зелёного свечения клеточной цитоплазмы видны красные нити белка тубулина. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 83
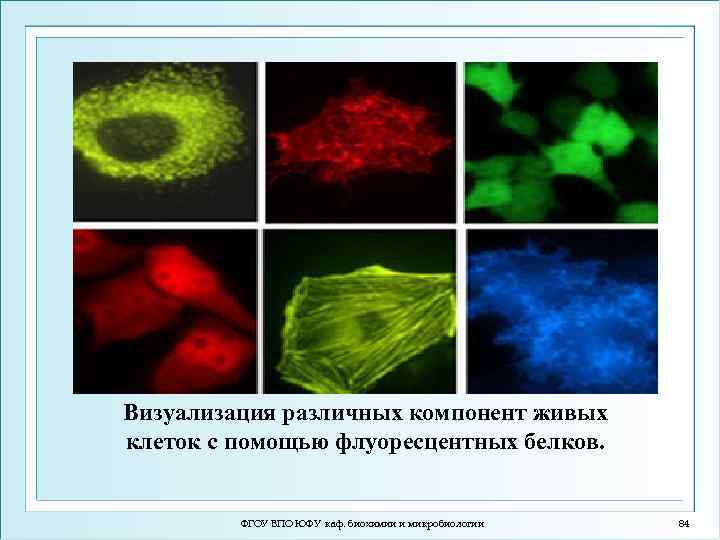
Визуализация различных компонент живых клеток с помощью флуоресцентных белков. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 84

Зеленые кошки не болеют СПИДом Американские ученые создали котов, невосприимчивых к кошачьему вирусу иммунодефицита (ВИК). Чтобы посмотреть, насколько обеспечивающий невосприимчивость ген активен в разных клетках животного, исследователи добавили к нему ген флуоресцирующего белка, благодаря которому генноинженерные коты в ультрафиолетовых лучах светятся зеленым светом. С помощью вирусного вектора внедрили в ДНК кошачьей яйцеклетки ген противовирусного фактора макаки TRIMCyp, снабжающего клетки устойчивостью к вирусу иммунодефицита. Чтобы проверить, не используя сложных инструментальных методик, насколько этот ген будет активен в различных тканях трансгенных животных, ученые добавили к нему ген зеленого флуоресцирующего белка медузы Aequorea victoria. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 85
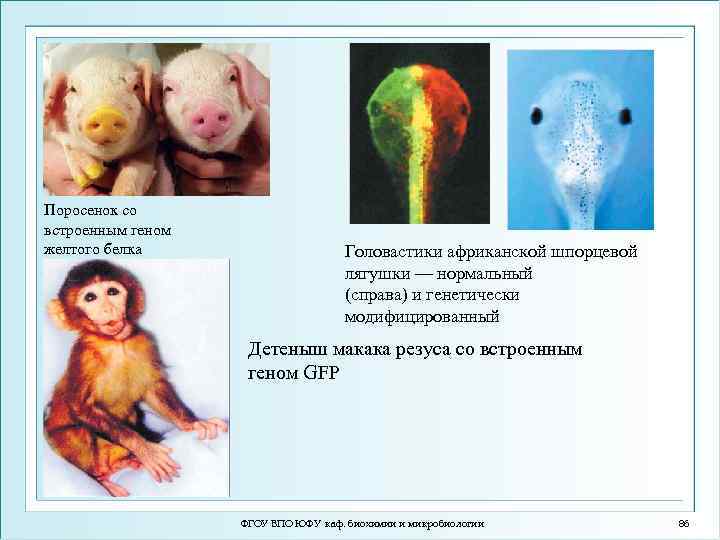
Поросенок со встроенным геном желтого белка Головастики африканской шпорцевой лягушки — нормальный (справа) и генетически модифицированный Детеныш макака резуса со встроенным геном GFP ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 86
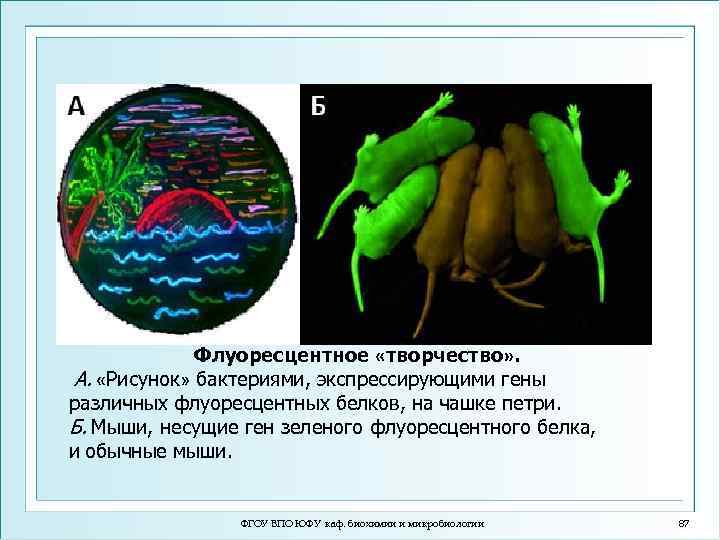
Флуоресцентное «творчество» . А. «Рисунок» бактериями, экспрессирующими гены различных флуоресцентных белков, на чашке петри. Б. Мыши, несущие ген зеленого флуоресцентного белка, и обычные мыши. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 87
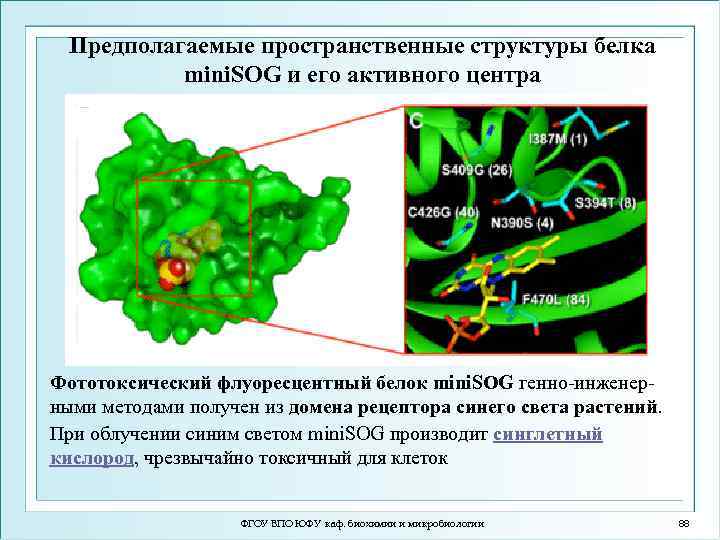
Предполагаемые пространственные структуры белка mini. SOG и его активного центра Фототоксический флуоресцентный белок mini. SOG генно-инженерными методами получен из домена рецептора синего света растений. При облучении синим светом mini. SOG производит синглетный кислород, чрезвычайно токсичный для клеток ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 88
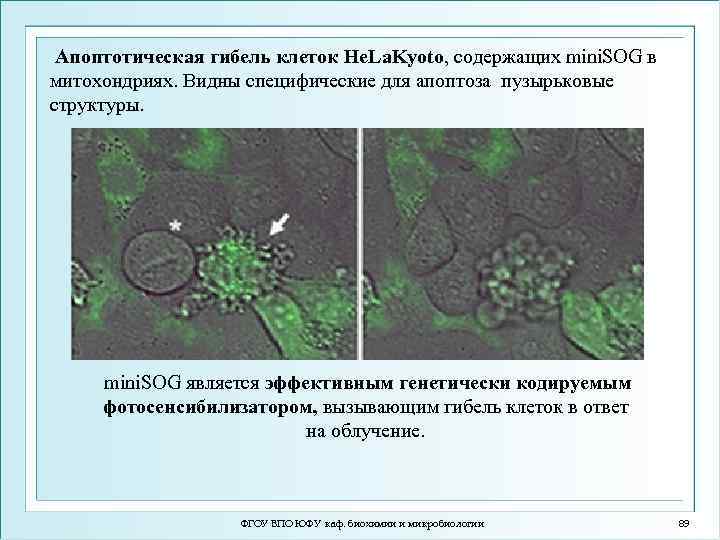
Апоптотическая гибель клеток He. La. Kyoto, содержащих mini. SOG в митохондриях. Видны специфические для апоптоза пузырьковые структуры. mini. SOG является эффективным генетически кодируемым фотосенсибилизатором, вызывающим гибель клеток в ответ на облучение. ФГОУ ВПО ЮФУ каф. биохимии и микробиологии 89
7.Биофизика мембран.ppt