През_ЛМконеч1111111.ppt
- Количество слайдов: 62
 Содержание курса лекций «Теоретические и экспериментальные методы исследования в химии. (Электрохимические методы исследования)» Базанов М. И. ФГБОУВПО «ИГХТУ» Кафедра аналитической химии 2012
Содержание курса лекций «Теоретические и экспериментальные методы исследования в химии. (Электрохимические методы исследования)» Базанов М. И. ФГБОУВПО «ИГХТУ» Кафедра аналитической химии 2012
 План лекции. 1. Введение (краткий экскурс из истории развития электрохимических методов исследования. Роль ученых России). 2. Классификация электрохимических методов исследования. 3. Современные электрохимические методы исследования (тип метода, вид установки или принципиальная схема, какие данные можно получить, где использовать, преимущества и недостатки. 4. Общий анализ и выводы.
План лекции. 1. Введение (краткий экскурс из истории развития электрохимических методов исследования. Роль ученых России). 2. Классификация электрохимических методов исследования. 3. Современные электрохимические методы исследования (тип метода, вид установки или принципиальная схема, какие данные можно получить, где использовать, преимущества и недостатки. 4. Общий анализ и выводы.
 В соответствии с рекомендациями ИЮПАК все электрохимические методы анализа подразделяются на две большие группы: - методы без протекания электрохимических реакций на электродах электрохимической ячейки (кондуктометрия с использованием токов низких 50 -10000 Гц и высоких частот более 1 МГЦ); - методы с протеканием электрохимических реакций на электродах электрохимической ячейки. К ним относятся потенциометрия, кулонометрия, вольтамперометрия (полярография) и другие методы анализа.
В соответствии с рекомендациями ИЮПАК все электрохимические методы анализа подразделяются на две большие группы: - методы без протекания электрохимических реакций на электродах электрохимической ячейки (кондуктометрия с использованием токов низких 50 -10000 Гц и высоких частот более 1 МГЦ); - методы с протеканием электрохимических реакций на электродах электрохимической ячейки. К ним относятся потенциометрия, кулонометрия, вольтамперометрия (полярография) и другие методы анализа.
 В электрохимических методах анализа аналитическим сигналом (измеряемой величиной) могут служить: Id - предельный диффузионный ток. Id =f(с) - метод амперометрии Е - потенциал электрода или эдс системы. Е =f(с) - метод потенциометрии Q - количество прошедшего электричества Q =f (с) - метод кулонометрии - Эквивалентная электрическая проводимость, æ - удельная электрическая проводимость. , æ = f(с) - метод кондуктометрии
В электрохимических методах анализа аналитическим сигналом (измеряемой величиной) могут служить: Id - предельный диффузионный ток. Id =f(с) - метод амперометрии Е - потенциал электрода или эдс системы. Е =f(с) - метод потенциометрии Q - количество прошедшего электричества Q =f (с) - метод кулонометрии - Эквивалентная электрическая проводимость, æ - удельная электрическая проводимость. , æ = f(с) - метод кондуктометрии
 ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА Вольтамперометрический метод анализа основан на расшифровке поляризационных кривых (вольтамперограмм), получаемых в электролитической ячейке с поляризующимся индикаторным электродом и неполяризующимся электродом сравнения. В зависимости от вида развертки потенциала и механизма массопереноса различают вольтамперометрию с линейной разверткой потенциала, вольтамперометрию со ступенчатым изменением потенциала, гидродинамические методы и инверсионную вольтамперометрию. Рис. Принципиальная схема полярографической установки. А-аккумулятор, Р-делитель напряжения, Ппотенциометр, Г-гальванометр, 1 -растущая ртутная капля, 2 -капилляр, 3 -система для регулирования высоты ртутного столба, 4 электрод сравнения, 5 - раствор электролита, 6 -вспомогательный ртутный электрод.
ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА Вольтамперометрический метод анализа основан на расшифровке поляризационных кривых (вольтамперограмм), получаемых в электролитической ячейке с поляризующимся индикаторным электродом и неполяризующимся электродом сравнения. В зависимости от вида развертки потенциала и механизма массопереноса различают вольтамперометрию с линейной разверткой потенциала, вольтамперометрию со ступенчатым изменением потенциала, гидродинамические методы и инверсионную вольтамперометрию. Рис. Принципиальная схема полярографической установки. А-аккумулятор, Р-делитель напряжения, Ппотенциометр, Г-гальванометр, 1 -растущая ртутная капля, 2 -капилляр, 3 -система для регулирования высоты ртутного столба, 4 электрод сравнения, 5 - раствор электролита, 6 -вспомогательный ртутный электрод.
 Рис. Полярограмма для растворов: 1 -1 М HCI + 5 10 -4 M Cd 2+ ; 2 - 1 М HCI (фоновый электролит). Без перемешивания раствора.
Рис. Полярограмма для растворов: 1 -1 М HCI + 5 10 -4 M Cd 2+ ; 2 - 1 М HCI (фоновый электролит). Без перемешивания раствора.
 Уравнением полярографической волны: Е = Е 1/2 + (R T / n F) ln ( Id – I ) / I, (1) где Е 1/2 – потенциал полуволны; Id – диффузионный ток. При I = Id / 2 уравнение (1) переходит в Е = Е 1/2. (2) Это соотношение показывает независимость потенциала полуволны от тока и, следовательно, от концентрации восстанавливающегося иона. Потенциал полуволны является качественной характеристикой иона в растворе данного фонового электролита, и определение потенциала полуволны составляет основу качественного полярографического анализа. Для обратимых электрохимических процессов можно показать, что Е 1/2 = Е 0 Однако, это следует делать с осторожностью. р. Н может влиять на величину Е 1/2. Так при электрохимическом восстановлении органических соединений с участием ионов водорода: Ox + ne- +2 H+ Red. H 2 выполняется уравнение Е 1/2 = Е 0 – р. Н. Для избежания влияния р. Н используют буферные растворы с высокой буферной емкостью.
Уравнением полярографической волны: Е = Е 1/2 + (R T / n F) ln ( Id – I ) / I, (1) где Е 1/2 – потенциал полуволны; Id – диффузионный ток. При I = Id / 2 уравнение (1) переходит в Е = Е 1/2. (2) Это соотношение показывает независимость потенциала полуволны от тока и, следовательно, от концентрации восстанавливающегося иона. Потенциал полуволны является качественной характеристикой иона в растворе данного фонового электролита, и определение потенциала полуволны составляет основу качественного полярографического анализа. Для обратимых электрохимических процессов можно показать, что Е 1/2 = Е 0 Однако, это следует делать с осторожностью. р. Н может влиять на величину Е 1/2. Так при электрохимическом восстановлении органических соединений с участием ионов водорода: Ox + ne- +2 H+ Red. H 2 выполняется уравнение Е 1/2 = Е 0 – р. Н. Для избежания влияния р. Н используют буферные растворы с высокой буферной емкостью.
 КОЛИЧЕСТВЕННЫЙ ПОЛЯРОГРАФИЧЕСКИЙ АНАЛИЗ Основан на уравнении Ильковича: Id=607 z. D 1/3 m 2/3 1/6 C (3) Z - заряд иона, m- скорость истечения ртути, мг/с - период капания, с D - коэффициент диффузии, см 2/c С - объемная концентрация анализируемого вещества, М При постоянных условиях полярографирования: z, m, , D – const Id = k. C Id (h)– количественная характеристика.
КОЛИЧЕСТВЕННЫЙ ПОЛЯРОГРАФИЧЕСКИЙ АНАЛИЗ Основан на уравнении Ильковича: Id=607 z. D 1/3 m 2/3 1/6 C (3) Z - заряд иона, m- скорость истечения ртути, мг/с - период капания, с D - коэффициент диффузии, см 2/c С - объемная концентрация анализируемого вещества, М При постоянных условиях полярографирования: z, m, , D – const Id = k. C Id (h)– количественная характеристика.
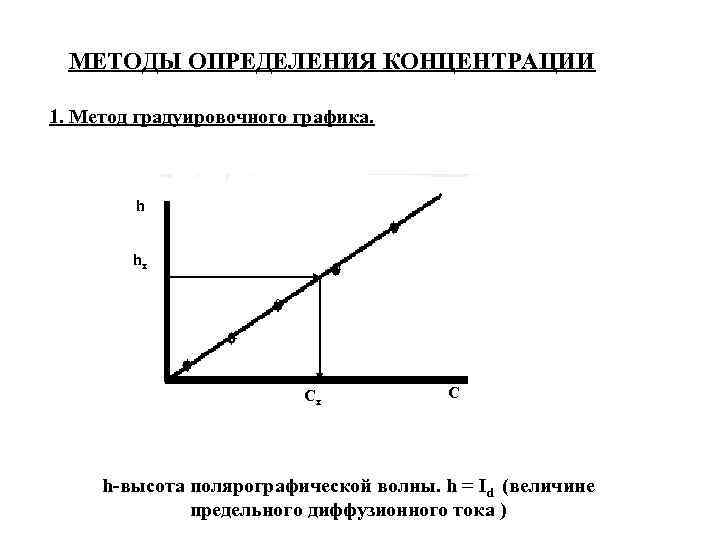 МЕТОДЫ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ 1. Метод градуировочного графика. h hx Cx C h-высота полярографической волны. h = Id (величине предельного диффузионного тока )
МЕТОДЫ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ 1. Метод градуировочного графика. h hx Cx C h-высота полярографической волны. h = Id (величине предельного диффузионного тока )
 2. В методе стандартных растворов в строго одинаковых условиях снимают полярограммы стандартного и анализируемого растворов и по уравнению 4. рассчитывают неизвестную концентрацию Сx : ( 4) где Сст - концентрация стандартного раствора; hx , hcт - высоты волн анализируемого и стандартного растворов(величины предельного диффузионного тока). 3. Метод добавок. Сначала регистрируется полярограмма исследуемого раствора, затем к раствору добавляется известное количество стандартного раствора Сст и снова регистрируется полярограмма. Концентрация исследуемого раствора Сx находится по уравнению 5. ( 5 ) где hx - высота волны исследуемого раствора; hx + ст - высота волны исследуемого раствора с добавкой стандартного вещества.
2. В методе стандартных растворов в строго одинаковых условиях снимают полярограммы стандартного и анализируемого растворов и по уравнению 4. рассчитывают неизвестную концентрацию Сx : ( 4) где Сст - концентрация стандартного раствора; hx , hcт - высоты волн анализируемого и стандартного растворов(величины предельного диффузионного тока). 3. Метод добавок. Сначала регистрируется полярограмма исследуемого раствора, затем к раствору добавляется известное количество стандартного раствора Сст и снова регистрируется полярограмма. Концентрация исследуемого раствора Сx находится по уравнению 5. ( 5 ) где hx - высота волны исследуемого раствора; hx + ст - высота волны исследуемого раствора с добавкой стандартного вещества.
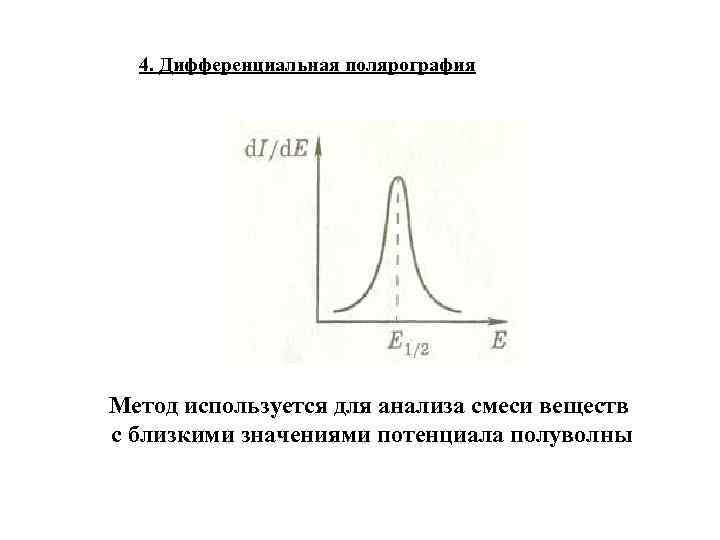 4. Дифференциальная полярография Метод используется для анализа смеси веществ с близкими значениями потенциала полуволны
4. Дифференциальная полярография Метод используется для анализа смеси веществ с близкими значениями потенциала полуволны
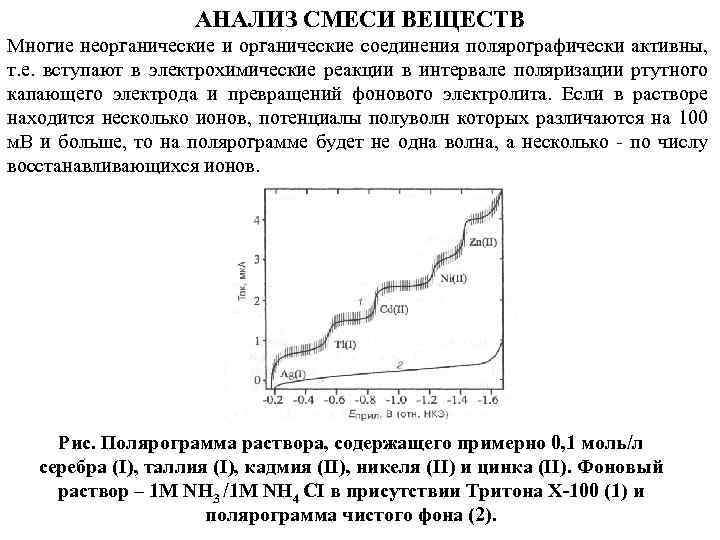 АНАЛИЗ СМЕСИ ВЕЩЕСТВ Многие неорганические и органические соединения полярографически активны, т. е. вступают в электрохимические реакции в интервале поляризации ртутного капающего электрода и превращений фонового электролита. Если в растворе находится несколько ионов, потенциалы полуволн которых различаются на 100 м. B и больше, то на полярограмме будет не одна волна, а несколько - по числу восстанавливающихся ионов. Рис. Полярограмма раствора, содержащего примерно 0, 1 моль/л серебра (I), таллия (I), кадмия (II), никеля (II) и цинка (II). Фоновый раствор – 1 М NH 3 /1 M NH 4 CI в присутствии Тритона Х-100 (1) и полярограмма чистого фона (2).
АНАЛИЗ СМЕСИ ВЕЩЕСТВ Многие неорганические и органические соединения полярографически активны, т. е. вступают в электрохимические реакции в интервале поляризации ртутного капающего электрода и превращений фонового электролита. Если в растворе находится несколько ионов, потенциалы полуволн которых различаются на 100 м. B и больше, то на полярограмме будет не одна волна, а несколько - по числу восстанавливающихся ионов. Рис. Полярограмма раствора, содержащего примерно 0, 1 моль/л серебра (I), таллия (I), кадмия (II), никеля (II) и цинка (II). Фоновый раствор – 1 М NH 3 /1 M NH 4 CI в присутствии Тритона Х-100 (1) и полярограмма чистого фона (2).
 Условия проведения полярографического анализа: 1. Раствор должен содержать полярографически неактивные фоновые электролиты (соли, кислоты, буферы). 2. В растворе должно содержаться некоторое количество ПАВ для подавления возможных нежелательных максимумов. 3. Предварительно нужно удалить растворенный кислород.
Условия проведения полярографического анализа: 1. Раствор должен содержать полярографически неактивные фоновые электролиты (соли, кислоты, буферы). 2. В растворе должно содержаться некоторое количество ПАВ для подавления возможных нежелательных максимумов. 3. Предварительно нужно удалить растворенный кислород.
 Рис. Максимум I рода на фоне 0, 05 М раствора KCI (1), исчезает после добавления ПАВ (желатина, Тритон Х-100) с концентрацией до 10 -4 % ) (2), полярограмма после удаления из раствора кислорода (3). Электролиты, контактирующие с воздухом, поглощают кислород, который электровосстанавливается по двум стадиям: О 2 + 2 H+ +2 e = H 2 O 2 Е 1/2 = - 0, 1 В (н. к. э. ) H 2 O 2 + 2 H+ +2 e = 2 H 2 O Е 1/2 = - 0, 9 В (н. к. э. ) При протекании этих процессов на полярограммах наблюдаются соответствующие 2 волны, которые лежат в той же области потенциалов, что и определяемые элементы. Это касается третьего условия – необходима оттдувка электролита инертным газом (аргон).
Рис. Максимум I рода на фоне 0, 05 М раствора KCI (1), исчезает после добавления ПАВ (желатина, Тритон Х-100) с концентрацией до 10 -4 % ) (2), полярограмма после удаления из раствора кислорода (3). Электролиты, контактирующие с воздухом, поглощают кислород, который электровосстанавливается по двум стадиям: О 2 + 2 H+ +2 e = H 2 O 2 Е 1/2 = - 0, 1 В (н. к. э. ) H 2 O 2 + 2 H+ +2 e = 2 H 2 O Е 1/2 = - 0, 9 В (н. к. э. ) При протекании этих процессов на полярограммах наблюдаются соответствующие 2 волны, которые лежат в той же области потенциалов, что и определяемые элементы. Это касается третьего условия – необходима оттдувка электролита инертным газом (аргон).
 АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ Установка для амперометрического титрования Она включает: полярографическую установку. Индикаторные электроды - ртутный капельный электрод, платиновый вращающийся и др. Электрод сравнения - насыщенный каломельный, хлоридсеребряный. Дополнительно в комплект установки входят микробюретка и магнитная мешалка. Вид кривой амперометрического титрования зависит от того, какой компонент реакции титрования вступает в электродную реакцию: определяемое вещество, титрант или продукт реакции. Типы кривых амперометрического титрования:
АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ Установка для амперометрического титрования Она включает: полярографическую установку. Индикаторные электроды - ртутный капельный электрод, платиновый вращающийся и др. Электрод сравнения - насыщенный каломельный, хлоридсеребряный. Дополнительно в комплект установки входят микробюретка и магнитная мешалка. Вид кривой амперометрического титрования зависит от того, какой компонент реакции титрования вступает в электродную реакцию: определяемое вещество, титрант или продукт реакции. Типы кривых амперометрического титрования:
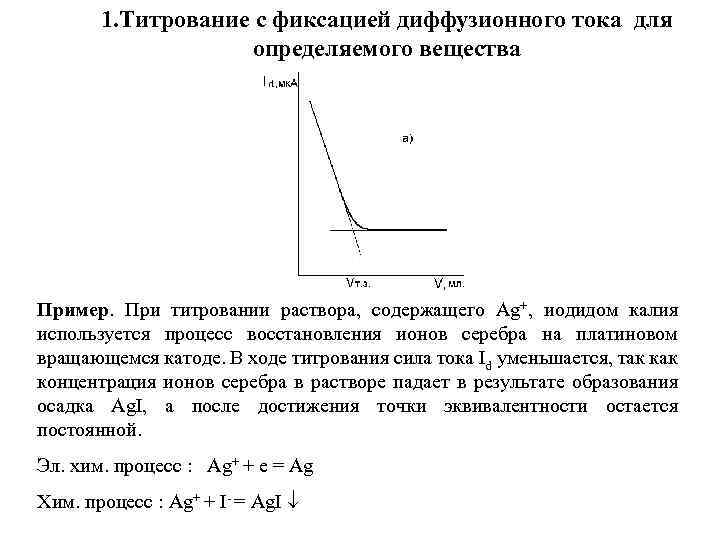 1. Титрование с фиксацией диффузионного тока для определяемого вещества Пример. При титровании раствора, содержащего Аg+, иодидом калия используется процесс восстановления ионов серебра на платиновом вращающемся катоде. В ходе титрования сила тока Id уменьшается, так концентрация ионов серебра в растворе падает в результате образования осадка Ag. I, а после достижения точки эквивалентности остается постоянной. Эл. хим. процесс : Аg+ + е = Аg Хим. процесс : Аg+ + I- = Аg. I
1. Титрование с фиксацией диффузионного тока для определяемого вещества Пример. При титровании раствора, содержащего Аg+, иодидом калия используется процесс восстановления ионов серебра на платиновом вращающемся катоде. В ходе титрования сила тока Id уменьшается, так концентрация ионов серебра в растворе падает в результате образования осадка Ag. I, а после достижения точки эквивалентности остается постоянной. Эл. хим. процесс : Аg+ + е = Аg Хим. процесс : Аg+ + I- = Аg. I
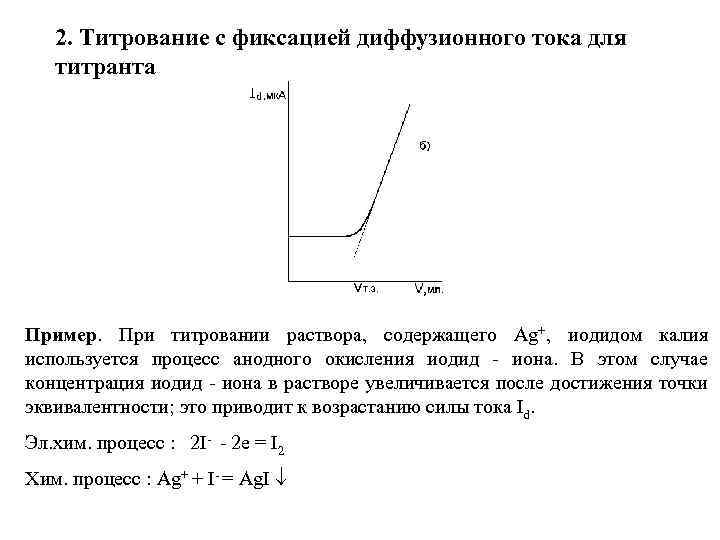 2. Титрование с фиксацией диффузионного тока для титранта Пример. При титровании раствора, содержащего Ag+, иодидом калия используется процесс анодного окисления иодид - иона. В этом случае концентрация иодид - иона в растворе увеличивается после достижения точки эквивалентности; это приводит к возрастанию силы тока Id. Эл. хим. процесс : 2 I- - 2 е = I 2 Хим. процесс : Аg+ + I- = Аg. I
2. Титрование с фиксацией диффузионного тока для титранта Пример. При титровании раствора, содержащего Ag+, иодидом калия используется процесс анодного окисления иодид - иона. В этом случае концентрация иодид - иона в растворе увеличивается после достижения точки эквивалентности; это приводит к возрастанию силы тока Id. Эл. хим. процесс : 2 I- - 2 е = I 2 Хим. процесс : Аg+ + I- = Аg. I
 3. Титрование с фиксацией диффузионного тока для определяемого вещества и титранта. До точки эквивалентности диффузионный ток уменьшается с уменьшением концентрации определяемого вещества. После точки эквивалентности диффузионный ток возрастает с увеличением концентрации титранта в растворе. Пример. Титрование Pb 2+ на ртутно - капающем электроде раствором бихромата калия. В растворе протекают: Электрохимические реакции при Е = -1, 0 В : Pb 2+ + 2 e = Pb ( Hg ); Cr 2 O 72 - + 14 H+ + 6 e = 2 Cr 3+ + 7 H 2 O. Хим. реакция: 2 Pb 2+ + Cr 2 O 72 - + H 2 O = 2 Pb. Cr. O 4 + 2 H+.
3. Титрование с фиксацией диффузионного тока для определяемого вещества и титранта. До точки эквивалентности диффузионный ток уменьшается с уменьшением концентрации определяемого вещества. После точки эквивалентности диффузионный ток возрастает с увеличением концентрации титранта в растворе. Пример. Титрование Pb 2+ на ртутно - капающем электроде раствором бихромата калия. В растворе протекают: Электрохимические реакции при Е = -1, 0 В : Pb 2+ + 2 e = Pb ( Hg ); Cr 2 O 72 - + 14 H+ + 6 e = 2 Cr 3+ + 7 H 2 O. Хим. реакция: 2 Pb 2+ + Cr 2 O 72 - + H 2 O = 2 Pb. Cr. O 4 + 2 H+.
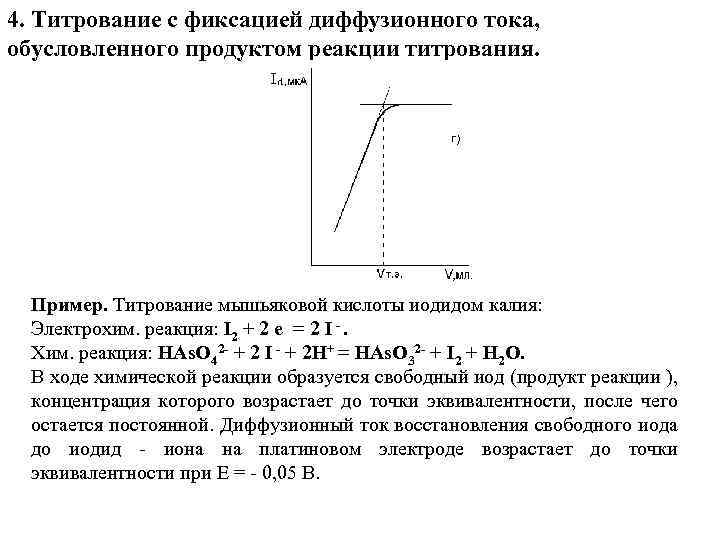 4. Титрование с фиксацией диффузионного тока, обусловленного продуктом реакции титрования. Пример. Титрование мышьяковой кислоты иодидом калия: Электрохим. реакция: I 2 + 2 e = 2 I -. Хим. реакция: HAs. O 42 - + 2 I - + 2 H+ = HAs. O 32 - + I 2 + H 2 O. В ходе химической реакции образуется свободный иод (продукт реакции ), концентрация которого возрастает до точки эквивалентности, после чего остается постоянной. Диффузионный ток восстановления свободного иода до иодид - иона на платиновом электроде возрастает до точки эквивалентности при Е = - 0, 05 В.
4. Титрование с фиксацией диффузионного тока, обусловленного продуктом реакции титрования. Пример. Титрование мышьяковой кислоты иодидом калия: Электрохим. реакция: I 2 + 2 e = 2 I -. Хим. реакция: HAs. O 42 - + 2 I - + 2 H+ = HAs. O 32 - + I 2 + H 2 O. В ходе химической реакции образуется свободный иод (продукт реакции ), концентрация которого возрастает до точки эквивалентности, после чего остается постоянной. Диффузионный ток восстановления свободного иода до иодид - иона на платиновом электроде возрастает до точки эквивалентности при Е = - 0, 05 В.
 В методах амперометрического титрования используют различные реакции: 1. -Осаждения. Многие анионы - Сl -, Br -, I -, SO 42 - и др. - титруются солью свинца при потенциале E = - 0, 4 B, при этом регистрируется ток восстановления Pb 2+ на ртутном капающем электроде. В реакциях осаждения часто применяется осаждение органическими реагентами: 8 - оксихинолином, купфероном, диметилглиоксимом и др. , причем титрование можно проводить как по току восстановления катиона, так и по току превращения органического реагента. 2 - Комплексообразования. Широко используется в амперометрическом титровании реакция образования комплексов с ЭДТА для различных катионов: Вi 3+, Fe 2+, Ni 2+, Pb 2+, Zn 2+, Cu 2+, Co 2+, Cd 2+. 3 - Окисления - восстановления. При амперометрическом титровании с использованием реакций окисления - восстановления в качестве титрантов используют К 2 Сr 2 O 7; Ce (SO 4)2; KBr. O 3 и I 2 для определения восстановителей; Fe. SO 4, Na 2 S 2 O 3 - для определения окислителей.
В методах амперометрического титрования используют различные реакции: 1. -Осаждения. Многие анионы - Сl -, Br -, I -, SO 42 - и др. - титруются солью свинца при потенциале E = - 0, 4 B, при этом регистрируется ток восстановления Pb 2+ на ртутном капающем электроде. В реакциях осаждения часто применяется осаждение органическими реагентами: 8 - оксихинолином, купфероном, диметилглиоксимом и др. , причем титрование можно проводить как по току восстановления катиона, так и по току превращения органического реагента. 2 - Комплексообразования. Широко используется в амперометрическом титровании реакция образования комплексов с ЭДТА для различных катионов: Вi 3+, Fe 2+, Ni 2+, Pb 2+, Zn 2+, Cu 2+, Co 2+, Cd 2+. 3 - Окисления - восстановления. При амперометрическом титровании с использованием реакций окисления - восстановления в качестве титрантов используют К 2 Сr 2 O 7; Ce (SO 4)2; KBr. O 3 и I 2 для определения восстановителей; Fe. SO 4, Na 2 S 2 O 3 - для определения окислителей.
 Общая характеристика метода: 1. Применим для анализа всех элементов периодической системы, если они окисляются или восстанавливаются. 2. Погрешность 2 -5 %, 3. Предел обнаружения 10 -8 – 10 -9 М 4. Быстрота анализа. Недостатки: Hg, калибровка.
Общая характеристика метода: 1. Применим для анализа всех элементов периодической системы, если они окисляются или восстанавливаются. 2. Погрешность 2 -5 %, 3. Предел обнаружения 10 -8 – 10 -9 М 4. Быстрота анализа. Недостатки: Hg, калибровка.
 МЕТОД ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ Сущность метода инверсионной вольтамперометрии заключается в выделении электролизом определяемого элемента из очень разбавленного раствора на стационарном индикаторном электроде (чаще всего на ртутной капле или тонкой пленке ртути) с последующим анодным растворением полученной амальгамы и регистрацией вольтамперной кривой. Процесс электролиза ( накопления ) проводят при постоянном потенциале (Еэ), соответствующем предельному току, в перемешиваемом растворе фонового электролита. Анодное окисление полученной амальгамы (переход анализируемых металлов в раствор) осуществляют при линейно - меняющемся потенциале.
МЕТОД ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ Сущность метода инверсионной вольтамперометрии заключается в выделении электролизом определяемого элемента из очень разбавленного раствора на стационарном индикаторном электроде (чаще всего на ртутной капле или тонкой пленке ртути) с последующим анодным растворением полученной амальгамы и регистрацией вольтамперной кривой. Процесс электролиза ( накопления ) проводят при постоянном потенциале (Еэ), соответствующем предельному току, в перемешиваемом растворе фонового электролита. Анодное окисление полученной амальгамы (переход анализируемых металлов в раствор) осуществляют при линейно - меняющемся потенциале.
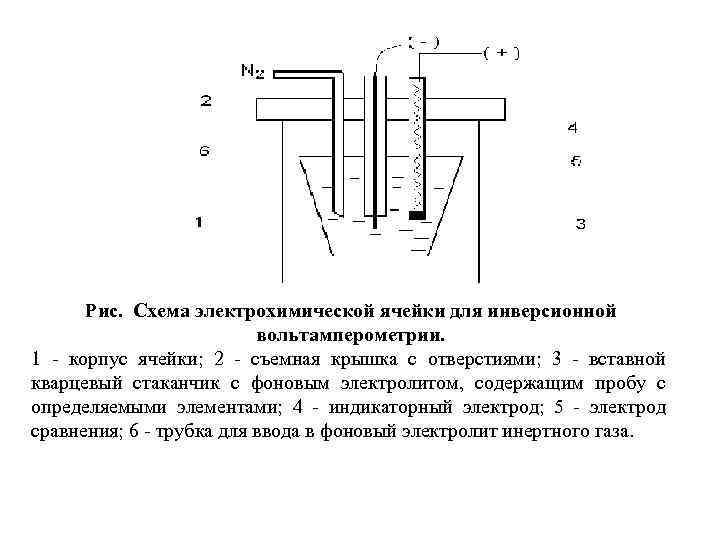 Рис. Схема электрохимической ячейки для инверсионной вольтамперометрии. 1 - корпус ячейки; 2 - съемная крышка с отверстиями; 3 - вставной кварцевый стаканчик с фоновым электролитом, содержащим пробу с определяемыми элементами; 4 - индикаторный электрод; 5 - электрод сравнения; 6 - трубка для ввода в фоновый электролит инертного газа.
Рис. Схема электрохимической ячейки для инверсионной вольтамперометрии. 1 - корпус ячейки; 2 - съемная крышка с отверстиями; 3 - вставной кварцевый стаканчик с фоновым электролитом, содержащим пробу с определяемыми элементами; 4 - индикаторный электрод; 5 - электрод сравнения; 6 - трубка для ввода в фоновый электролит инертного газа.
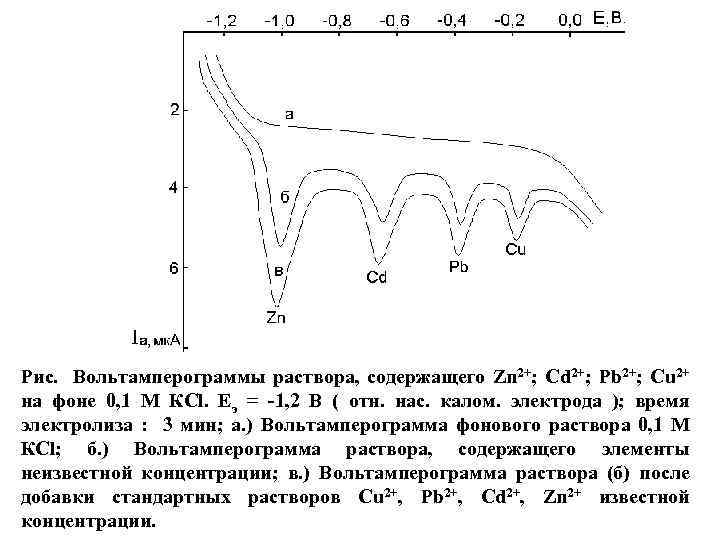 Рис. Вольтамперограммы раствора, содержащего Zn 2+; Cd 2+; Pb 2+; Cu 2+ на фоне 0, 1 М КСl. Еэ = -1, 2 В ( отн. нас. калом. электрода ); время электролиза : 3 мин; а. ) Вольтамперограмма фонового раствора 0, 1 М КСl; б. ) Вольтамперограмма раствора, содержащего элементы неизвестной концентрации; в. ) Вольтамперограмма раствора (б) после добавки стандартных растворов Cu 2+, Pb 2+, Cd 2+, Zn 2+ известной концентрации.
Рис. Вольтамперограммы раствора, содержащего Zn 2+; Cd 2+; Pb 2+; Cu 2+ на фоне 0, 1 М КСl. Еэ = -1, 2 В ( отн. нас. калом. электрода ); время электролиза : 3 мин; а. ) Вольтамперограмма фонового раствора 0, 1 М КСl; б. ) Вольтамперограмма раствора, содержащего элементы неизвестной концентрации; в. ) Вольтамперограмма раствора (б) после добавки стандартных растворов Cu 2+, Pb 2+, Cd 2+, Zn 2+ известной концентрации.
 ПРОЦЕССЫ: При электролизе происходит выделение ионов металла на ртути с образованием амальгамы металла по реакции: Меn+ + n e + Hg = Me (Hg). При использовании твердых электродов в стадии концентрирования происходит выделение определяемого элемента в виде металла: Men+ + n e = Me 0 или образование концентрата ( осадков оксидов, гидроксидов металла, химических и интерметаллических соединений с компонентами раствора или материала электрода ). Например: 2 VO 3 - + 3 H 2 O + 4 e = V 2 O 3 ( тв. ) + 6 ОН-. 3 Сu 2+ + 2 As 3+ + 12 e = Cu 3 As 2. В анодном процессе происходит окисление амальгамы металла, выделенного металла или полученного концентрата: Me ( Hg ) - n e =Men+ + Hg; Meo - n e = Men+.
ПРОЦЕССЫ: При электролизе происходит выделение ионов металла на ртути с образованием амальгамы металла по реакции: Меn+ + n e + Hg = Me (Hg). При использовании твердых электродов в стадии концентрирования происходит выделение определяемого элемента в виде металла: Men+ + n e = Me 0 или образование концентрата ( осадков оксидов, гидроксидов металла, химических и интерметаллических соединений с компонентами раствора или материала электрода ). Например: 2 VO 3 - + 3 H 2 O + 4 e = V 2 O 3 ( тв. ) + 6 ОН-. 3 Сu 2+ + 2 As 3+ + 12 e = Cu 3 As 2. В анодном процессе происходит окисление амальгамы металла, выделенного металла или полученного концентрата: Me ( Hg ) - n e =Men+ + Hg; Meo - n e = Men+.
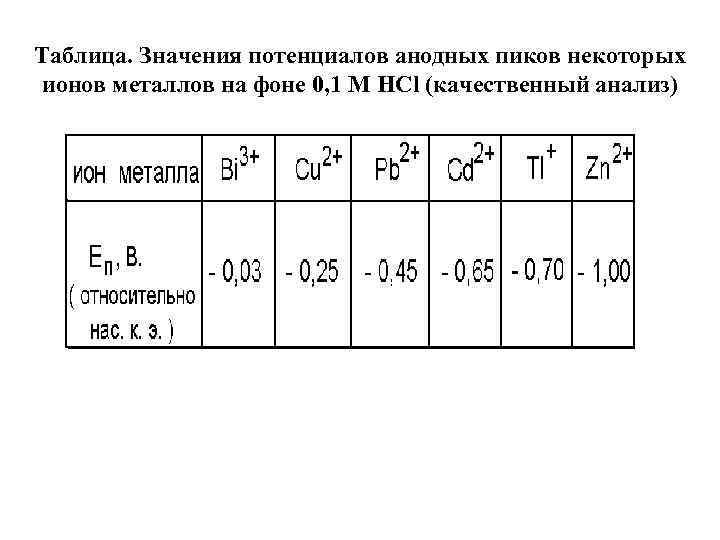 Таблица. Значения потенциалов анодных пиков некоторых ионов металлов на фоне 0, 1 М НСl (качественный анализ)
Таблица. Значения потенциалов анодных пиков некоторых ионов металлов на фоне 0, 1 М НСl (качественный анализ)
 ОСНОВА КОЛИЧЕСТВЕННОГО АНАЛИЗА где I - величина анодного тока, А; Со - концентрация ионов определяемого элемента, М; S - поверхность ртутного электрода, см 2; , V, - объемы раствора и ртутной капли, соответственно, см 3; КЭ, Kа - коэффициенты электролиза и анодного пика; - время электролиза, с; n - число электронов, принимающих участие в электродном процессе; F - число Фарадея : F = 96500 Кл / моль-экв.
ОСНОВА КОЛИЧЕСТВЕННОГО АНАЛИЗА где I - величина анодного тока, А; Со - концентрация ионов определяемого элемента, М; S - поверхность ртутного электрода, см 2; , V, - объемы раствора и ртутной капли, соответственно, см 3; КЭ, Kа - коэффициенты электролиза и анодного пика; - время электролиза, с; n - число электронов, принимающих участие в электродном процессе; F - число Фарадея : F = 96500 Кл / моль-экв.
 ВОЛЬТАМПЕРОМЕТРИЯ С ЛИНЕЙНОЙ РАЗВЕРТКОЙ ПОТЕНЦИАЛА НА СТАЦИОНАРНЫХ ЭЛЕКТРОДАХ (ЦИКЛИЧЕСКАЯ ВОЛЬТАМПЕРОМЕТРИЯ) Возрастающая популярность этого метода объясняется тем, что окисление многих органических соединений нельзя изучать на ртутном электроде из-за ограниченного диапазона анодных потенциалов. Поэтому, в данном случае применяются твердые микроэлектроды из благородных металлов (платина, золото), а также угольные (графитивые) электроды. Первые используются для неводных сред, последние – для водных растворов. На индикаторный электрод с постоянной площадью поверхности подают линейную развертку потенциала : Еt = Еi Vt, где Еt - начальный потенциал, V –скорость развертки потенциала (от 0, 001 до 0, 1 В/с, t – время электролиза.
ВОЛЬТАМПЕРОМЕТРИЯ С ЛИНЕЙНОЙ РАЗВЕРТКОЙ ПОТЕНЦИАЛА НА СТАЦИОНАРНЫХ ЭЛЕКТРОДАХ (ЦИКЛИЧЕСКАЯ ВОЛЬТАМПЕРОМЕТРИЯ) Возрастающая популярность этого метода объясняется тем, что окисление многих органических соединений нельзя изучать на ртутном электроде из-за ограниченного диапазона анодных потенциалов. Поэтому, в данном случае применяются твердые микроэлектроды из благородных металлов (платина, золото), а также угольные (графитивые) электроды. Первые используются для неводных сред, последние – для водных растворов. На индикаторный электрод с постоянной площадью поверхности подают линейную развертку потенциала : Еt = Еi Vt, где Еt - начальный потенциал, V –скорость развертки потенциала (от 0, 001 до 0, 1 В/с, t – время электролиза.
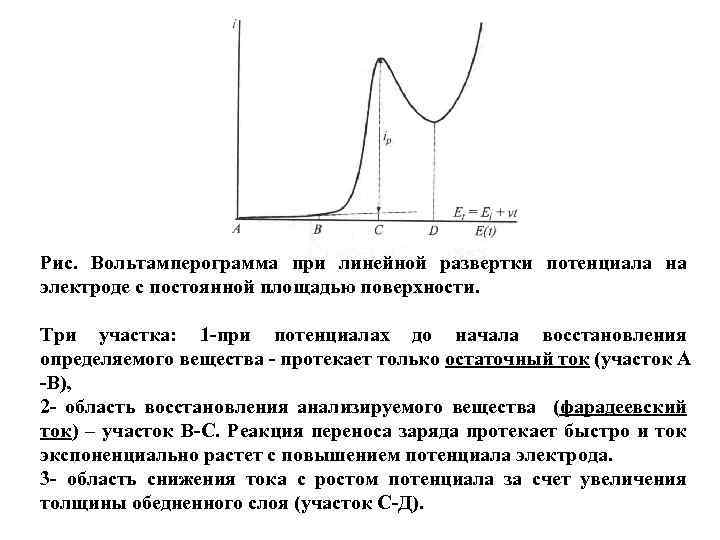 Рис. Вольтамперограмма при линейной развертки потенциала на электроде с постоянной площадью поверхности. Три участка: 1 -при потенциалах до начала восстановления определяемого вещества - протекает только остаточный ток (участок А -В), 2 - область восстановления анализируемого вещества (фарадеевский ток) – участок В-С. Реакция переноса заряда протекает быстро и ток экспоненциально растет с повышением потенциала электрода. 3 - область снижения тока с ростом потенциала за счет увеличения толщины обедненного слоя (участок С-Д).
Рис. Вольтамперограмма при линейной развертки потенциала на электроде с постоянной площадью поверхности. Три участка: 1 -при потенциалах до начала восстановления определяемого вещества - протекает только остаточный ток (участок А -В), 2 - область восстановления анализируемого вещества (фарадеевский ток) – участок В-С. Реакция переноса заряда протекает быстро и ток экспоненциально растет с повышением потенциала электрода. 3 - область снижения тока с ростом потенциала за счет увеличения толщины обедненного слоя (участок С-Д).
 МЕТОД ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ (ЦВАМ) Метод циклической вольтамперометрии отличается тем, что в нем осуществляется фиксация катодных и анодных токов при линейноизменяющемся потенциале со сменой его полярности при достижении определенного значения потенциала. I-E-кривые для электрода с ТФП Со. V=20 м. В/с. Диапазон от 0. 5 до -1. 4 В. 1 -полное насыщение электролита аргоном 2 - полное насыщение электролита дикислородом
МЕТОД ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ (ЦВАМ) Метод циклической вольтамперометрии отличается тем, что в нем осуществляется фиксация катодных и анодных токов при линейноизменяющемся потенциале со сменой его полярности при достижении определенного значения потенциала. I-E-кривые для электрода с ТФП Со. V=20 м. В/с. Диапазон от 0. 5 до -1. 4 В. 1 -полное насыщение электролита аргоном 2 - полное насыщение электролита дикислородом
 Форма I-E –кривых зависит от: 1. - Химического строения объекта исследования, наличия электрохимически-активных атомов(ионов), атомных групп, функциональных заместителей, сопряженных систем и др. - всего того, что участвует в электрохимическом процессе 2. - Обратимости электрохимических процессов. 3. - Чистоты используемых препаратов и техники выполнения эксперимента.
Форма I-E –кривых зависит от: 1. - Химического строения объекта исследования, наличия электрохимически-активных атомов(ионов), атомных групп, функциональных заместителей, сопряженных систем и др. - всего того, что участвует в электрохимическом процессе 2. - Обратимости электрохимических процессов. 3. - Чистоты используемых препаратов и техники выполнения эксперимента.
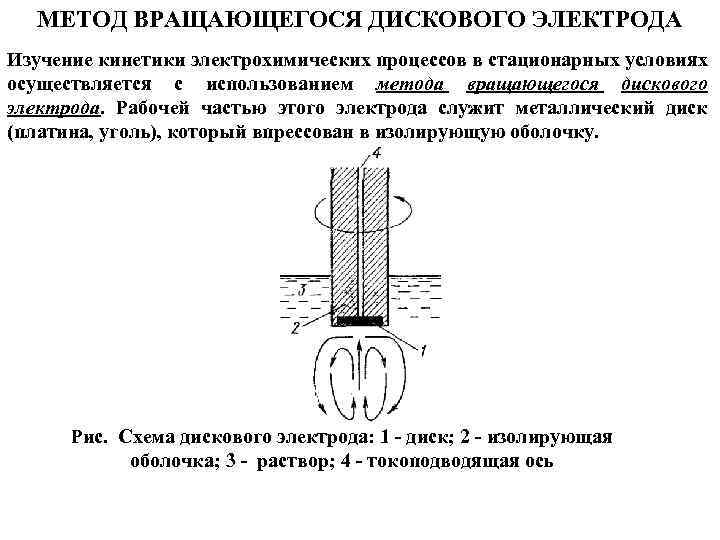 МЕТОД ВРАЩАЮЩЕГОСЯ ДИСКОВОГО ЭЛЕКТРОДА Изучение кинетики электрохимических процессов в стационарных условиях осуществляется с использованием метода вращающегося дискового электрода. Рабочей частью этого электрода служит металлический диск (платина, уголь), который впрессован в изолирующую оболочку. Рис. Схема дискового электрода: 1 - диск; 2 - изолирующая оболочка; 3 - раствор; 4 - токоподводящая ось
МЕТОД ВРАЩАЮЩЕГОСЯ ДИСКОВОГО ЭЛЕКТРОДА Изучение кинетики электрохимических процессов в стационарных условиях осуществляется с использованием метода вращающегося дискового электрода. Рабочей частью этого электрода служит металлический диск (платина, уголь), который впрессован в изолирующую оболочку. Рис. Схема дискового электрода: 1 - диск; 2 - изолирующая оболочка; 3 - раствор; 4 - токоподводящая ось
 Вращающийся дисковый электрод равнодоступен в диффузионном отношении (т. е. скорость диффузии одинакова в любой точке поверхности диска). Если скорость реакции на дисковом электроде лимитируется массопереносом, то плотность тока (в отсутствие миграции реагирующих ионов) одинакова по всей поверхности и равна: -угловая скорость вращения электрода, - кинематическая вязкость раствора, Коэффициент 0, 62 соответсвует размерностям : i – А/м 2, D и - м 2/с, сi – моль/м 3, - рад/с. При больших катодных поляризациях, когда 0, ток достигает своего предельного значения:
Вращающийся дисковый электрод равнодоступен в диффузионном отношении (т. е. скорость диффузии одинакова в любой точке поверхности диска). Если скорость реакции на дисковом электроде лимитируется массопереносом, то плотность тока (в отсутствие миграции реагирующих ионов) одинакова по всей поверхности и равна: -угловая скорость вращения электрода, - кинематическая вязкость раствора, Коэффициент 0, 62 соответсвует размерностям : i – А/м 2, D и - м 2/с, сi – моль/м 3, - рад/с. При больших катодных поляризациях, когда 0, ток достигает своего предельного значения:
 Достоинства метода ВДЭ 1. Значительно повышает измеряемые токи и резко сокращает время установления стационарного состояния (от часов до долей секунды). 2. Используется для определения эффективного числа электронов ( n ) электрохимического процесса и установления механизма электродных реакций, особенно с участием органических соединений. При определении n обычно сравнивают предельные диффузионные токи для исследуемого вещества и для другого вещества, близкого по строению, а следовательно и по величине Di, механизм электровосстановления которого известен. Некоторые различия в значениях D не играют роли, т. к. n имеет только целочисленные значения. 3. Используется для точного расчета коэффициента диффузии реагирующего вещества. 4. Используется для решения разнообразных теоретических и практических задач как модельная система.
Достоинства метода ВДЭ 1. Значительно повышает измеряемые токи и резко сокращает время установления стационарного состояния (от часов до долей секунды). 2. Используется для определения эффективного числа электронов ( n ) электрохимического процесса и установления механизма электродных реакций, особенно с участием органических соединений. При определении n обычно сравнивают предельные диффузионные токи для исследуемого вещества и для другого вещества, близкого по строению, а следовательно и по величине Di, механизм электровосстановления которого известен. Некоторые различия в значениях D не играют роли, т. к. n имеет только целочисленные значения. 3. Используется для точного расчета коэффициента диффузии реагирующего вещества. 4. Используется для решения разнообразных теоретических и практических задач как модельная система.
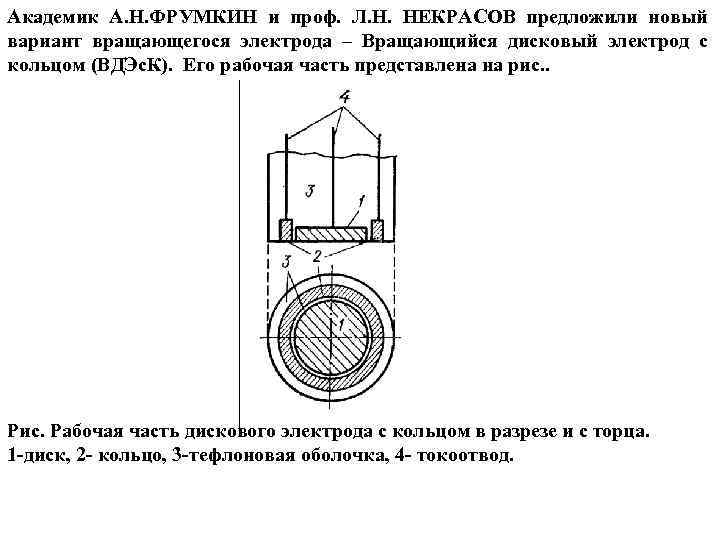 Академик А. Н. ФРУМКИН и проф. Л. Н. НЕКРАСОВ предложили новый вариант вращающегося электрода – Вращающийся дисковый электрод с кольцом (ВДЭс. К). Его рабочая часть представлена на рис. . Рис. Рабочая часть дискового электрода с кольцом в разрезе и с торца. 1 -диск, 2 - кольцо, 3 -тефлоновая оболочка, 4 - токоотвод.
Академик А. Н. ФРУМКИН и проф. Л. Н. НЕКРАСОВ предложили новый вариант вращающегося электрода – Вращающийся дисковый электрод с кольцом (ВДЭс. К). Его рабочая часть представлена на рис. . Рис. Рабочая часть дискового электрода с кольцом в разрезе и с торца. 1 -диск, 2 - кольцо, 3 -тефлоновая оболочка, 4 - токоотвод.
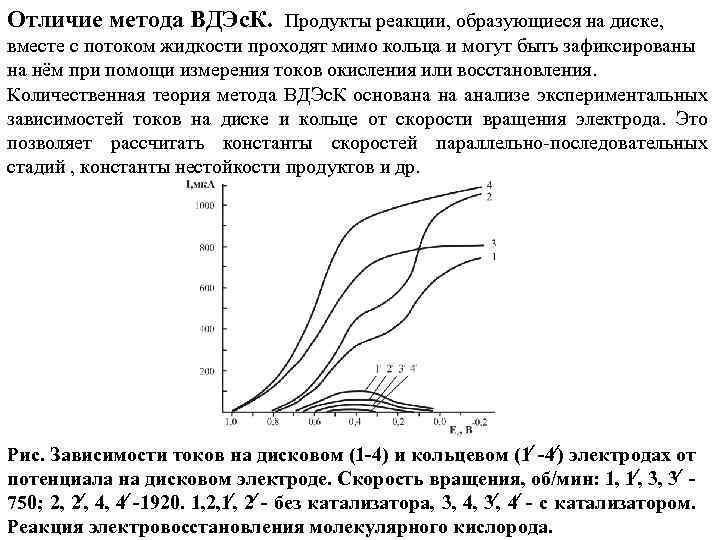 Отличие метода ВДЭс. К. Продукты реакции, образующиеся на диске, вместе с потоком жидкости проходят мимо кольца и могут быть зафиксированы на нём при помощи измерения токов окисления или восстановления. Количественная теория метода ВДЭс. К основана на анализе экспериментальных зависимостей токов на диске и кольце от скорости вращения электрода. Это позволяет рассчитать константы скоростей параллельно-последовательных стадий , константы нестойкости продуктов и др. Рис. Зависимости токов на дисковом (1 -4) и кольцевом (1 -4 ) электродах от потенциала на дисковом электроде. Скорость вращения, об/мин: 1, 1 , 3, 3 - 750; 2, 2 , 4, 4 -1920. 1, 2, 1 , 2 - без катализатора, 3, 4, 3 , 4 - с катализатором. Реакция электровосстановления молекулярного кислорода.
Отличие метода ВДЭс. К. Продукты реакции, образующиеся на диске, вместе с потоком жидкости проходят мимо кольца и могут быть зафиксированы на нём при помощи измерения токов окисления или восстановления. Количественная теория метода ВДЭс. К основана на анализе экспериментальных зависимостей токов на диске и кольце от скорости вращения электрода. Это позволяет рассчитать константы скоростей параллельно-последовательных стадий , константы нестойкости продуктов и др. Рис. Зависимости токов на дисковом (1 -4) и кольцевом (1 -4 ) электродах от потенциала на дисковом электроде. Скорость вращения, об/мин: 1, 1 , 3, 3 - 750; 2, 2 , 4, 4 -1920. 1, 2, 1 , 2 - без катализатора, 3, 4, 3 , 4 - с катализатором. Реакция электровосстановления молекулярного кислорода.
 ПОТЕНЦИОМЕТРИЯ Потенциометрический метод анализа основан на использовании зависимости электродвижущей силы (ЭДС) электрохимической цепи от активности (концентрации) анализируемого иона. Зависимость электродвижущей силы Е электрохимической цепи от активности анализируемого иона описывают уравнением Нернста для цепи: Е = Е 0 + (S / n) lg аан, гдe Е 0 - стандартная ЭДС цепи; п - заряд анализируемого иона с соответствующим знаком; S - крутизна электродной функции индикаторного электрода, селективного к однозарядному иону; аан - активность анализируемого иона.
ПОТЕНЦИОМЕТРИЯ Потенциометрический метод анализа основан на использовании зависимости электродвижущей силы (ЭДС) электрохимической цепи от активности (концентрации) анализируемого иона. Зависимость электродвижущей силы Е электрохимической цепи от активности анализируемого иона описывают уравнением Нернста для цепи: Е = Е 0 + (S / n) lg аан, гдe Е 0 - стандартная ЭДС цепи; п - заряд анализируемого иона с соответствующим знаком; S - крутизна электродной функции индикаторного электрода, селективного к однозарядному иону; аан - активность анализируемого иона.
 Для идеального индикаторного электрода: S = (RT) / F, где R - универсальная газовая постоянная, равная 8, 312 Дж/(моль · К); Т - абсолютная температура раствора, К; F - число Фарадея, равное 96500 Кл/моль; S= 0, 0591 В при 25°С. Для потенциометрических измерений применяют электрохимические цепи, содержащие два электрода: индикаторный и электрод сравнения Индикаторным называют электрод, потенциал которого определяет активность анализируемого иона в соответствии с уравнением Нернста. Электродом сравнения называют электрод, потенциал которого постоянен и не зависит от концентрации ионов в раствор. Если оба электрода погружены в анализируемый раствор, то такая цепь называется цепью без переноса. Если электрод сравнения соединяют с анализируемым раствором через жидкостный контакт (солевой мостик), то цепь называется цепью с переносом.
Для идеального индикаторного электрода: S = (RT) / F, где R - универсальная газовая постоянная, равная 8, 312 Дж/(моль · К); Т - абсолютная температура раствора, К; F - число Фарадея, равное 96500 Кл/моль; S= 0, 0591 В при 25°С. Для потенциометрических измерений применяют электрохимические цепи, содержащие два электрода: индикаторный и электрод сравнения Индикаторным называют электрод, потенциал которого определяет активность анализируемого иона в соответствии с уравнением Нернста. Электродом сравнения называют электрод, потенциал которого постоянен и не зависит от концентрации ионов в раствор. Если оба электрода погружены в анализируемый раствор, то такая цепь называется цепью без переноса. Если электрод сравнения соединяют с анализируемым раствором через жидкостный контакт (солевой мостик), то цепь называется цепью с переносом.
 Электродвижущую силу - Е электрохимической цепи, приведенной выше, определяют по уравнению: Е= Еср - Еин + Едиф, где Едиф - диффузионный (жидкостный) потенциал, В; Еср - потенциал электрода сравнения, В; Еив - потенциал индикаторного электрода, В. Подставим в это уравнение значение Еин выраженное через уравнение Нернста, с учетом соотношения аан = fан Сан, где fан и Сан - коэффициент активности и аналитическая концентрация анализируемого иона, соответственно. Получаем уравнение, лежащее в основе всех потенциометрических методов анализа: Е = Е 0 – ( S/n ) lg Сан – ( S/n ) lg faн + Едиф, где Е 0 = Еср – Е 0 ин - стандартная ЭДС цепи, В; E 0 ин - стандартный потенциал индикаторного электрода, В
Электродвижущую силу - Е электрохимической цепи, приведенной выше, определяют по уравнению: Е= Еср - Еин + Едиф, где Едиф - диффузионный (жидкостный) потенциал, В; Еср - потенциал электрода сравнения, В; Еив - потенциал индикаторного электрода, В. Подставим в это уравнение значение Еин выраженное через уравнение Нернста, с учетом соотношения аан = fан Сан, где fан и Сан - коэффициент активности и аналитическая концентрация анализируемого иона, соответственно. Получаем уравнение, лежащее в основе всех потенциометрических методов анализа: Е = Е 0 – ( S/n ) lg Сан – ( S/n ) lg faн + Едиф, где Е 0 = Еср – Е 0 ин - стандартная ЭДС цепи, В; E 0 ин - стандартный потенциал индикаторного электрода, В
 Электроды для потенциометрического анализа В качестве индикаторных в потенциометрическом анализе применяют: 1. Электроды, на поверхности которых протекают реакции с обменом электронов. Их называют электронообменными или окислительновосстановительными. В качестве таких электродов применяют электроды из химически инертных металлов - платины, золота и др. В аналитической практике находит применение выпускаемый промышленностью точечный платиновый электрод ЭПВ-1 -100 и изготовленный из специального стекла мембранный окислительновосстановительный электрод ЭО - 1. 2. Электроды, на поверхности которых протекают реакции обмена ионами. Их называют ионообменными или ионоселективными электродами. Основным элементом ионоселективных электродов является ионочувствительная мембрана. Поэтому их также иногда называют мембранными. Ионоселективные электроды изготавливают: - с твердыми мембранами; - со стеклянными мембранами; - с жидкостными мембранами.
Электроды для потенциометрического анализа В качестве индикаторных в потенциометрическом анализе применяют: 1. Электроды, на поверхности которых протекают реакции с обменом электронов. Их называют электронообменными или окислительновосстановительными. В качестве таких электродов применяют электроды из химически инертных металлов - платины, золота и др. В аналитической практике находит применение выпускаемый промышленностью точечный платиновый электрод ЭПВ-1 -100 и изготовленный из специального стекла мембранный окислительновосстановительный электрод ЭО - 1. 2. Электроды, на поверхности которых протекают реакции обмена ионами. Их называют ионообменными или ионоселективными электродами. Основным элементом ионоселективных электродов является ионочувствительная мембрана. Поэтому их также иногда называют мембранными. Ионоселективные электроды изготавливают: - с твердыми мембранами; - со стеклянными мембранами; - с жидкостными мембранами.
 ВИДЫ ПОТЕНЦИОМЕТРИЧЕСКОГО АНАЛИЗА Потенциометрические методы анализа подразделяются на два вида: - прямая потенциометрия, или ионометрия; -потенциометрическое титрование Прямая потенциометрия Метод прямой потенциометрии основан на определении концентрации иона непосредственно по измеренной ЭДС электрохимической цепи, содержащей соответствующий ионоселективный электрод. Расчет может быть выполнен по указанному выше уравнению Нернста, известны все параметры, входящие в это уравнение. Однако величины fан и Едиф заранее неизвестны, поэтому используют приемы, позволяющие обойти эти трудности (метод градуировочного графика и метод добавок).
ВИДЫ ПОТЕНЦИОМЕТРИЧЕСКОГО АНАЛИЗА Потенциометрические методы анализа подразделяются на два вида: - прямая потенциометрия, или ионометрия; -потенциометрическое титрование Прямая потенциометрия Метод прямой потенциометрии основан на определении концентрации иона непосредственно по измеренной ЭДС электрохимической цепи, содержащей соответствующий ионоселективный электрод. Расчет может быть выполнен по указанному выше уравнению Нернста, известны все параметры, входящие в это уравнение. Однако величины fан и Едиф заранее неизвестны, поэтому используют приемы, позволяющие обойти эти трудности (метод градуировочного графика и метод добавок).
 1. Метод градуировочного графика. . Е Ех lg. Cx Определяют ЭДС для ряда стандартных растворов. I=const 2. Метод добавок. Измеряют ЭДС цепи с анализируемым раствором и после добавления определённого объёма стандартного раствора. Решая систему двух уравнений, определяют Сх
1. Метод градуировочного графика. . Е Ех lg. Cx Определяют ЭДС для ряда стандартных растворов. I=const 2. Метод добавок. Измеряют ЭДС цепи с анализируемым раствором и после добавления определённого объёма стандартного раствора. Решая систему двух уравнений, определяют Сх
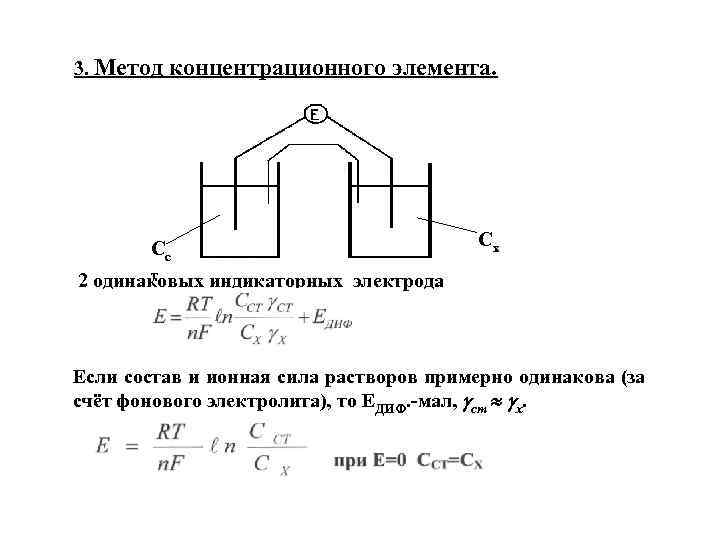 3. Метод концентрационного элемента. Cс Cх т 2 одинаковых индикаторных электрода Если состав и ионная сила растворов примерно одинакова (за счёт фонового электролита), то ЕДИФ. -мал, ст х.
3. Метод концентрационного элемента. Cс Cх т 2 одинаковых индикаторных электрода Если состав и ионная сила растворов примерно одинакова (за счёт фонового электролита), то ЕДИФ. -мал, ст х.
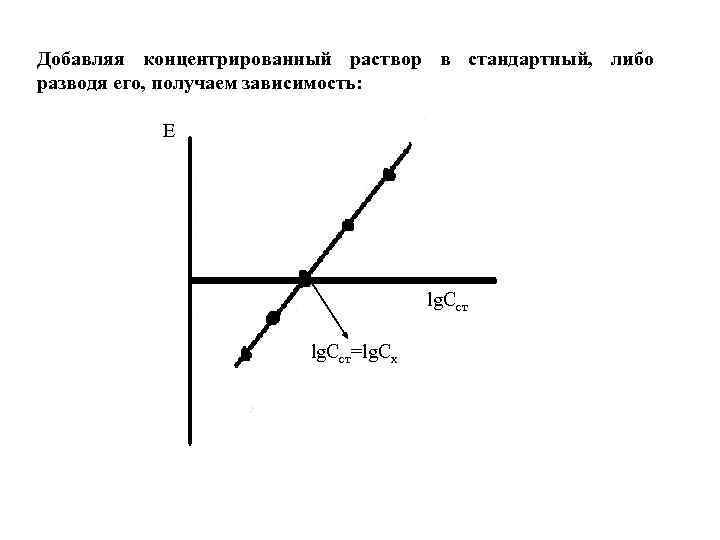 Добавляя концентрированный раствор в стандартный, либо разводя его, получаем зависимость: Е lg. Cст=lg. Cх
Добавляя концентрированный раствор в стандартный, либо разводя его, получаем зависимость: Е lg. Cст=lg. Cх
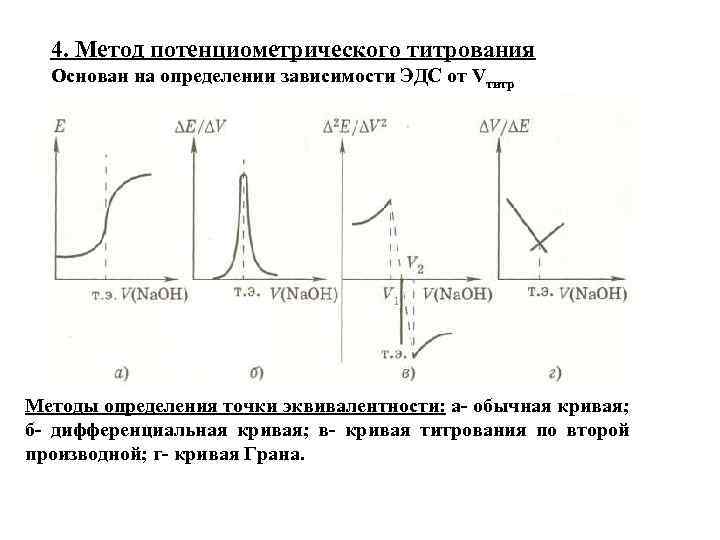 4. Метод потенциометрического титрования Основан на определении зависимости ЭДС от Vтитр Методы определения точки эквивалентности: а- обычная кривая; б- дифференциальная кривая; в- кривая титрования по второй производной; г- кривая Грана.
4. Метод потенциометрического титрования Основан на определении зависимости ЭДС от Vтитр Методы определения точки эквивалентности: а- обычная кривая; б- дифференциальная кривая; в- кривая титрования по второй производной; г- кривая Грана.
 Достоинства метода: 1. Высокая чувствительность, 2. Анализ смеси веществ без предварительного разделения, титрование мутных и окрашенных сред, 3. Анализ в автоматическом режиме (БАТ-15). Недостатки: 1. Значения р. Н и Е устанавливаются не всегда быстро, 2. Выполнение значительного числа опытов при градуировке. Применение: р. Н, жесткость воды, ионного состава биологических жидкостей (кровь, моча), определение катионов и анионов, медицина и физиология (Са 2+), определение Кравн. , Кдис. К уст. , ПР.
Достоинства метода: 1. Высокая чувствительность, 2. Анализ смеси веществ без предварительного разделения, титрование мутных и окрашенных сред, 3. Анализ в автоматическом режиме (БАТ-15). Недостатки: 1. Значения р. Н и Е устанавливаются не всегда быстро, 2. Выполнение значительного числа опытов при градуировке. Применение: р. Н, жесткость воды, ионного состава биологических жидкостей (кровь, моча), определение катионов и анионов, медицина и физиология (Са 2+), определение Кравн. , Кдис. К уст. , ПР.
 ЭЛЕКТРОЛИЗ И КУЛОНОМЕТРИЧЕСКИЙ АНАЛИЗ ЭЛЕКТРОЛИЗ - химическое разложение вещества под действием электрического тока. ЗАКОН ЭЛЕКТРОЛИЗА - закон ФАРАДЕЯ. Выход по току = M – молярная масса анализируемого вещества; Q – количество электричества, Кл; F – число Фарадея равное 96500 Кл/моль; n – количество электронов, участвующих в электрохимическом процессе; I – сила тока, А; t – продолжительность электролиза, с.
ЭЛЕКТРОЛИЗ И КУЛОНОМЕТРИЧЕСКИЙ АНАЛИЗ ЭЛЕКТРОЛИЗ - химическое разложение вещества под действием электрического тока. ЗАКОН ЭЛЕКТРОЛИЗА - закон ФАРАДЕЯ. Выход по току = M – молярная масса анализируемого вещества; Q – количество электричества, Кл; F – число Фарадея равное 96500 Кл/моль; n – количество электронов, участвующих в электрохимическом процессе; I – сила тока, А; t – продолжительность электролиза, с.
 1. Прямая кулонометрия - анализируемое вещество непосредственно подвергается электрохимическим превращениям. 2. Кулонометрическое титрование. Достоинство метода: • Титрант электрохимически генерируется непосредственно в электрохимической ячейке (не готовят). • Рабочий раствор титранта не стандартизируют. Кулонометрические измерения проводят: 1 - при контролируемом потенциале – потенциостатическая кулонометрия. Протекает только одна реакция. Сила тока является функцией времени. Количество электричества определяют электронным интегратором (или кулонометром, соединенным последовательно). 2 - при постоянной силе тока – гальваностатическая кулонометрия. Требуется определить только время электролиза для расчета количества электричества. Ток – предельный диффузионный ток для данного процесса. По возможности исключить протекание побочных процессов. Q=It
1. Прямая кулонометрия - анализируемое вещество непосредственно подвергается электрохимическим превращениям. 2. Кулонометрическое титрование. Достоинство метода: • Титрант электрохимически генерируется непосредственно в электрохимической ячейке (не готовят). • Рабочий раствор титранта не стандартизируют. Кулонометрические измерения проводят: 1 - при контролируемом потенциале – потенциостатическая кулонометрия. Протекает только одна реакция. Сила тока является функцией времени. Количество электричества определяют электронным интегратором (или кулонометром, соединенным последовательно). 2 - при постоянной силе тока – гальваностатическая кулонометрия. Требуется определить только время электролиза для расчета количества электричества. Ток – предельный диффузионный ток для данного процесса. По возможности исключить протекание побочных процессов. Q=It
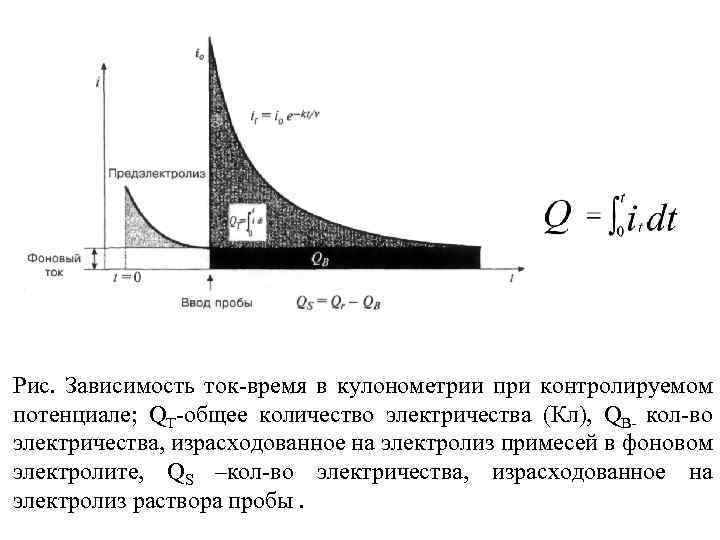 Рис. Зависимость ток-время в кулонометрии при контролируемом потенциале; QT-общее количество электричества (Кл), QВ- кол-во электричества, израсходованное на электролиз примесей в фоновом электролите, QS –кол-во электричества, израсходованное на электролиз раствора пробы.
Рис. Зависимость ток-время в кулонометрии при контролируемом потенциале; QT-общее количество электричества (Кл), QВ- кол-во электричества, израсходованное на электролиз примесей в фоновом электролите, QS –кол-во электричества, израсходованное на электролиз раствора пробы.
 Общая характеристика метода: 1. Концентрации с 10 -6 М определяют с точностью 0, 1 -0, 05%. 2. Высокая селективность. 3. Анализ без предварительного разделения. 4. Не требуется градуировочных графиков. 5. Простое аппаратурное оформление Ограничения. 1. Метод применим к ограниченному числу элементов (подвергающихся процессам окисления-восстановления) 2. Длительность анализа.
Общая характеристика метода: 1. Концентрации с 10 -6 М определяют с точностью 0, 1 -0, 05%. 2. Высокая селективность. 3. Анализ без предварительного разделения. 4. Не требуется градуировочных графиков. 5. Простое аппаратурное оформление Ограничения. 1. Метод применим к ограниченному числу элементов (подвергающихся процессам окисления-восстановления) 2. Длительность анализа.
 КОНДУКТОМЕТРИЯ Кондуктометрический метод анализа – это метод, основанный на измерении электропроводности (электрической проводимости) растворов. Электропроводность (электрическая проводимость) раствора – это величина, обратная его сопротивлению. Если сопротивление раствора R, то его электропроводность W будет равна: W = 1/R Единицей измерения электропроводности является Ом-1 или См (Сименс).
КОНДУКТОМЕТРИЯ Кондуктометрический метод анализа – это метод, основанный на измерении электропроводности (электрической проводимости) растворов. Электропроводность (электрическая проводимость) раствора – это величина, обратная его сопротивлению. Если сопротивление раствора R, то его электропроводность W будет равна: W = 1/R Единицей измерения электропроводности является Ом-1 или См (Сименс).
 Электропроводность растворов зависит: 1. От числа ионов в единице объема раствора, т. е. от концентрации С 2. От подвижности l этих ионов, т. е. от легкости, с которой они движутся в электрическом поле 3. От расстояния между электродами L (обратно пропорциональная зависимость) 4. От площади электродов S Математически эта зависимость выражается формулой: W = k. SCl/L Для конкретной пары электродов при неизменном расстоянии между ними L и S постоянны. После объединения всех постоянных величин в одну константу k получим: W = k. Cl Электропроводность раствора прямо пропорциональна концентрации и подвижности ионов в растворе
Электропроводность растворов зависит: 1. От числа ионов в единице объема раствора, т. е. от концентрации С 2. От подвижности l этих ионов, т. е. от легкости, с которой они движутся в электрическом поле 3. От расстояния между электродами L (обратно пропорциональная зависимость) 4. От площади электродов S Математически эта зависимость выражается формулой: W = k. SCl/L Для конкретной пары электродов при неизменном расстоянии между ними L и S постоянны. После объединения всех постоянных величин в одну константу k получим: W = k. Cl Электропроводность раствора прямо пропорциональна концентрации и подвижности ионов в растворе
 æ - Удельная электрическая проводимость равна электрической проводимости раствора, находящегося между параллельными электродами площадью 1 м 2 при расстоянии между ними 1 м, или, другими словами – это электрическая проводимость столба раствора длиной 1 м и площадью поперечного сечения 1 м 2. Единицей измерения удельной электропроводности растворов См/м. Удельная электропроводность раствора зависит - от концентрации раствора, - природы электролита - температуры является
æ - Удельная электрическая проводимость равна электрической проводимости раствора, находящегося между параллельными электродами площадью 1 м 2 при расстоянии между ними 1 м, или, другими словами – это электрическая проводимость столба раствора длиной 1 м и площадью поперечного сечения 1 м 2. Единицей измерения удельной электропроводности растворов См/м. Удельная электропроводность раствора зависит - от концентрации раствора, - природы электролита - температуры является
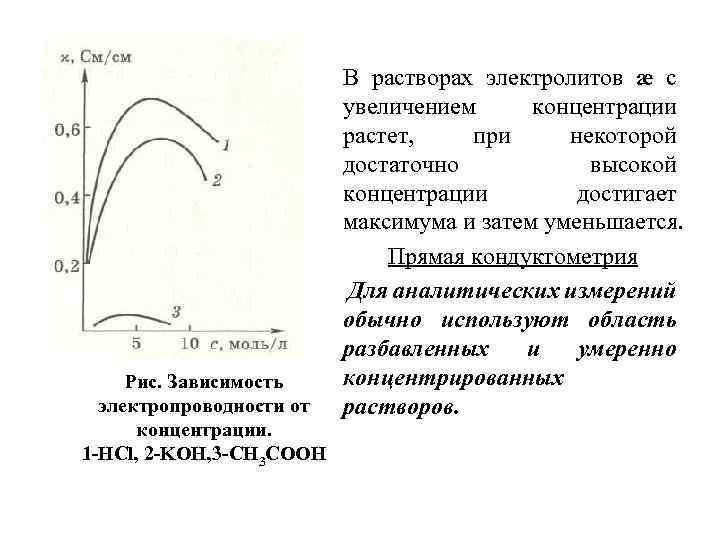 Рис. Зависимость электропроводности от концентрации. 1 -HCl, 2 -KOH, 3 -CH 3 COOH В растворах электролитов æ с увеличением концентрации растет, при некоторой достаточно высокой концентрации достигает максимума и затем уменьшается. Прямая кондуктометрия Для аналитических измерений обычно используют область разбавленных и умеренно концентрированных растворов.
Рис. Зависимость электропроводности от концентрации. 1 -HCl, 2 -KOH, 3 -CH 3 COOH В растворах электролитов æ с увеличением концентрации растет, при некоторой достаточно высокой концентрации достигает максимума и затем уменьшается. Прямая кондуктометрия Для аналитических измерений обычно используют область разбавленных и умеренно концентрированных растворов.
 λ - Эквивалентная электрическая проводимость – проводимость раствора, содержащего 1 кмоль эквивалента вещества, заключенного между двумя параллельными электродами, находящимися друг от друга на расстоянии 1 м. Единицей измерения эквивалентной электрической проводимости λ является См·м 2/(кмоль- экв). Эквивалентная и удельная электрические проводимости связаны между собой соотношением: λ = 1000æ /С С - молярная концентрация эквивалента, моль/л Эквивалентная электрическая - температуры, - концентрации - природы вещества. проводимость зависит от
λ - Эквивалентная электрическая проводимость – проводимость раствора, содержащего 1 кмоль эквивалента вещества, заключенного между двумя параллельными электродами, находящимися друг от друга на расстоянии 1 м. Единицей измерения эквивалентной электрической проводимости λ является См·м 2/(кмоль- экв). Эквивалентная и удельная электрические проводимости связаны между собой соотношением: λ = 1000æ /С С - молярная концентрация эквивалента, моль/л Эквивалентная электрическая - температуры, - концентрации - природы вещества. проводимость зависит от
 • Для сильных электролитов, в области разбавленных растворов, наблюдается линейная зависимость эквивалентной электрической проводимости от концентрации: • ° - предельная экв. эл. проводимость при бесконечном разведении Рис. Зависимость эквивалентной электрической проводимости от концентрации. 1 - сильного, 2 - слабого электролитов. λ = λ∞ - а√С Из теории Дебая - Хюккеля, развитой Онзагером, уравнение преобразуется: λ = λ∞ - (А λ∞ + В)√С где А – коэффициент, характеризующий электрофоретический эффект; В – коэффициент, характеризующий релаксационный эффект.
• Для сильных электролитов, в области разбавленных растворов, наблюдается линейная зависимость эквивалентной электрической проводимости от концентрации: • ° - предельная экв. эл. проводимость при бесконечном разведении Рис. Зависимость эквивалентной электрической проводимости от концентрации. 1 - сильного, 2 - слабого электролитов. λ = λ∞ - а√С Из теории Дебая - Хюккеля, развитой Онзагером, уравнение преобразуется: λ = λ∞ - (А λ∞ + В)√С где А – коэффициент, характеризующий электрофоретический эффект; В – коэффициент, характеризующий релаксационный эффект.
 ЗАКОН АДДИТИВНОСТИ - закон независимости движения ионов ( Ф. Кольрауш) Предельная эквивалентная электрическая проводимость λ∞ является суммой предельных электрических проводимостей или предельных подвижностей ионов (катионов и анионов). λ∞ = λ∞(+) + λ∞(-)
ЗАКОН АДДИТИВНОСТИ - закон независимости движения ионов ( Ф. Кольрауш) Предельная эквивалентная электрическая проводимость λ∞ является суммой предельных электрических проводимостей или предельных подвижностей ионов (катионов и анионов). λ∞ = λ∞(+) + λ∞(-)
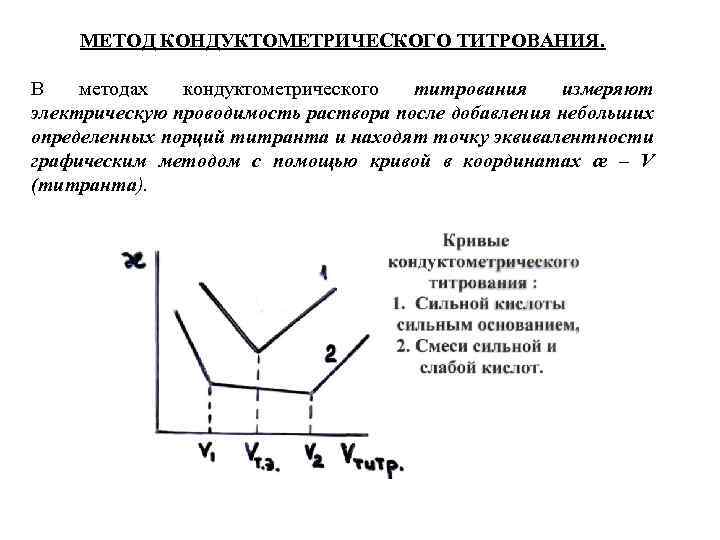 МЕТОД КОНДУКТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ. В методах кондуктометрического титрования измеряют электрическую проводимость раствора после добавления небольших определенных порций титранта и находят точку эквивалентности графическим методом с помощью кривой в координатах æ – V (титранта).
МЕТОД КОНДУКТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ. В методах кондуктометрического титрования измеряют электрическую проводимость раствора после добавления небольших определенных порций титранта и находят точку эквивалентности графическим методом с помощью кривой в координатах æ – V (титранта).
 Практически могут быть использованы такие химические реакции, в ходе которых достаточно заметно изменяется электрическая проводимость раствора или происходит резкое изменение (обычно возрастание) электрической проводимости после точки эквивалентности. Реакции осаждения. Реакции комплексообразования Реакции окисления-восстановления Реакции кислотно-основного взаимодействия а) Титрование сильной кислоты сильным основанием (или сильного основания сильной кислотой) б) Титрование слабой кислоты сильным основанием (слабого основания сильной кислотой) в) Титрование слабой кислоты слабым основанием (слабого основания слабой кислотой) г) Титрование смеси кислот и оснований
Практически могут быть использованы такие химические реакции, в ходе которых достаточно заметно изменяется электрическая проводимость раствора или происходит резкое изменение (обычно возрастание) электрической проводимости после точки эквивалентности. Реакции осаждения. Реакции комплексообразования Реакции окисления-восстановления Реакции кислотно-основного взаимодействия а) Титрование сильной кислоты сильным основанием (или сильного основания сильной кислотой) б) Титрование слабой кислоты сильным основанием (слабого основания сильной кислотой) в) Титрование слабой кислоты слабым основанием (слабого основания слабой кислотой) г) Титрование смеси кислот и оснований
 Метод высокочастотного титрования. (Используются токи высокой частоты, электроды не соприкасаются с анализируемым раствором - бесконтактный метод). Преимущества: 1. Возможность анализа агрессивных сред, пасты, эмульсии. 2. Нет химического взаимодействия электродов с раствором. 3. Простота. 4. Точность — погрешность 2 -3 %. Рис. Типы ячеек для высокочастотного титрования: а – подключается к генератору в качестве ёмкости; б – в качестве индуктивности
Метод высокочастотного титрования. (Используются токи высокой частоты, электроды не соприкасаются с анализируемым раствором - бесконтактный метод). Преимущества: 1. Возможность анализа агрессивных сред, пасты, эмульсии. 2. Нет химического взаимодействия электродов с раствором. 3. Простота. 4. Точность — погрешность 2 -3 %. Рис. Типы ячеек для высокочастотного титрования: а – подключается к генератору в качестве ёмкости; б – в качестве индуктивности
 . Практическое применение кондуктометрии Прямое измерение электрической проводимости – наиболее эффективный метод контроля качества дистиллированной воды в лабораториях, технической воды в так называемых тонких химических или фармацевтических производствах, в технологии водоочистки и оценке загрязненности сточных вод, теплотехнике (питание котлов) и т. д. Кондуктометрические датчики – в автоматизированных схемах контроля производства в некоторых отраслях химической, текстильной и пищевой промышленности, гидроэлектрометаллургии. Определение малых количеств углерода (10 -2 – 10 -3%) в сталях и металлах. Контроль качества молока, различных напитков и пищевых продуктов. Кондуктометрическое титрование: 1. определение кислот, оснований, фенолятов, ацетатов, аминокислот, смесей кислот и оснований не только в водной среде, но и в среде органических и водноорганических растворителей (например, смесь HCl + CH 3 COOH + NH 4 Cl + C 6 H 5 OH); 2. определение многих анионов и катионов Например, нитратом серебра титруют хлорид, иодид, цианид, тиоцианат, оксалат, салицилат и некоторые другие ионы. Титрование раствором ЭДТА используют для определения Fe 3+, Cu 2+, Ni 2+, Co 2+ и др. 3. определение общей жесткости воды.
. Практическое применение кондуктометрии Прямое измерение электрической проводимости – наиболее эффективный метод контроля качества дистиллированной воды в лабораториях, технической воды в так называемых тонких химических или фармацевтических производствах, в технологии водоочистки и оценке загрязненности сточных вод, теплотехнике (питание котлов) и т. д. Кондуктометрические датчики – в автоматизированных схемах контроля производства в некоторых отраслях химической, текстильной и пищевой промышленности, гидроэлектрометаллургии. Определение малых количеств углерода (10 -2 – 10 -3%) в сталях и металлах. Контроль качества молока, различных напитков и пищевых продуктов. Кондуктометрическое титрование: 1. определение кислот, оснований, фенолятов, ацетатов, аминокислот, смесей кислот и оснований не только в водной среде, но и в среде органических и водноорганических растворителей (например, смесь HCl + CH 3 COOH + NH 4 Cl + C 6 H 5 OH); 2. определение многих анионов и катионов Например, нитратом серебра титруют хлорид, иодид, цианид, тиоцианат, оксалат, салицилат и некоторые другие ионы. Титрование раствором ЭДТА используют для определения Fe 3+, Cu 2+, Ni 2+, Co 2+ и др. 3. определение общей жесткости воды.
 Общая характеристика метода. Кондуктометрические методы характеризуются: высокой экспрессностью, простотой, доступностью измерительных приборов, удобством работы, достаточной точностью Прямые кондуктометрические измерения имеют погрешность 1 – 2%, при соблюдении специальных условий она снижается до 0, 2%. Погрешность кондуктометрического титрования без термостатирования растворов ± (2 - 3) %. Термостатирование растворов существенно увеличивает точность метода.
Общая характеристика метода. Кондуктометрические методы характеризуются: высокой экспрессностью, простотой, доступностью измерительных приборов, удобством работы, достаточной точностью Прямые кондуктометрические измерения имеют погрешность 1 – 2%, при соблюдении специальных условий она снижается до 0, 2%. Погрешность кондуктометрического титрования без термостатирования растворов ± (2 - 3) %. Термостатирование растворов существенно увеличивает точность метода.


