Смоленская государственная медицинская академия Кафедра неврологии и нейрохирургии










































Лекция 1. генетика.ppt
- Количество слайдов: 53
 Смоленская государственная медицинская академия Кафедра неврологии и нейрохирургии Доцент Павлов В. А. МЕДИЦИНСКАЯ ГЕНЕТИКА.
Смоленская государственная медицинская академия Кафедра неврологии и нейрохирургии Доцент Павлов В. А. МЕДИЦИНСКАЯ ГЕНЕТИКА.
 В структуре болезней наблюдается неуклонное увеличение доли наследственной патологии, отрицательно влияющей на состояние здоровья. Врожденные и наследственные болезни встречаются с частотой 40 -60 на 1000 родившихся Число наследственных болезней составляет около 7 тыс. , из них около 2 тыс. – это болезни обмена веществ. В мировой литературе представлено описание 18. 981 фенотипов, из которых более 12 тыс. с известной нуклеотидной последовательностью генов и установленным типом наследственной передачи.
В структуре болезней наблюдается неуклонное увеличение доли наследственной патологии, отрицательно влияющей на состояние здоровья. Врожденные и наследственные болезни встречаются с частотой 40 -60 на 1000 родившихся Число наследственных болезней составляет около 7 тыс. , из них около 2 тыс. – это болезни обмена веществ. В мировой литературе представлено описание 18. 981 фенотипов, из которых более 12 тыс. с известной нуклеотидной последовательностью генов и установленным типом наследственной передачи.
 Медицинская генетика изучает 1. роль наследственности в патологии человека, 2. закономерности передачи от поколения к поколению наследственных болезней, 3. разрабатывает методы диагностики, лечения, профилактики и прогнозирования наследственных болезней. В длительной эволюции человека появилось множество полиморфизмов, создающих его индивидуальную уникальность. Наряду с положительными мутациями, позволяющими лучше приспособиться к меняющимся условиям существования, возникали патологические мутации, вызывающие наследственные болезни.
Медицинская генетика изучает 1. роль наследственности в патологии человека, 2. закономерности передачи от поколения к поколению наследственных болезней, 3. разрабатывает методы диагностики, лечения, профилактики и прогнозирования наследственных болезней. В длительной эволюции человека появилось множество полиморфизмов, создающих его индивидуальную уникальность. Наряду с положительными мутациями, позволяющими лучше приспособиться к меняющимся условиям существования, возникали патологические мутации, вызывающие наследственные болезни.
 Среди наследственных заболеваний обширную группу составляют болезни ЦНС, включающие в себя наследственно-дегенеративные заболевания, врожденные пороки развития ЦНС, а также наследственные болезни обмена и наследственные синдромы с поражением ЦНС. Наследственные болезни являются частью общей наследственной изменчивости человека. В развитии наследственных признаков или болезней принимают участие наследственная конституция – генотип и внешняя среда. Человек постоянно сталкивается с новыми факторами среды, ранее никогда не встречавшимися. Это приводит к появлению экогенетических болезней. Постоянно протекающий мутационных процесс поставляет новые мутации , а естественный отбор сохраняет, умножает их или приводит к их исчезновению.
Среди наследственных заболеваний обширную группу составляют болезни ЦНС, включающие в себя наследственно-дегенеративные заболевания, врожденные пороки развития ЦНС, а также наследственные болезни обмена и наследственные синдромы с поражением ЦНС. Наследственные болезни являются частью общей наследственной изменчивости человека. В развитии наследственных признаков или болезней принимают участие наследственная конституция – генотип и внешняя среда. Человек постоянно сталкивается с новыми факторами среды, ранее никогда не встречавшимися. Это приводит к появлению экогенетических болезней. Постоянно протекающий мутационных процесс поставляет новые мутации , а естественный отбор сохраняет, умножает их или приводит к их исчезновению.
 Наследственная отягощенность современного человечества состоит из двух компонентов: 1. патологических мутаций, накопленных в процессе эволюции ; 2. вновь возникших изменений в половых клетках под влиянием мутагенных факторов (радиация, химические вещества).
Наследственная отягощенность современного человечества состоит из двух компонентов: 1. патологических мутаций, накопленных в процессе эволюции ; 2. вновь возникших изменений в половых клетках под влиянием мутагенных факторов (радиация, химические вещества).
 Причины относительного увеличения q физические наследственной патологии (радиоактивные и ультрафиолетовые излучения), q химические (промышленные и бытовые химические вещества, медикаменты, косметика), q биологические мутагены : вирусы оспы, кори, ветряной оспы, простого герпеса вызывают хромосомные аберрации, подавляют репарационные системы. v Токсины плесневых грибов, злаков (проросшее зерно) в ничтожных количествах (5 -7 мкг) вызывают рак печени. v Появление генетически модифицированных продуктов – трансгенов, вызывающих мутацию бактерий желудочно-кишечного тракта, превращая их из сапрофитов в патологические формы. При этом изменяется их устойчивость к антибактериальной терапии.
Причины относительного увеличения q физические наследственной патологии (радиоактивные и ультрафиолетовые излучения), q химические (промышленные и бытовые химические вещества, медикаменты, косметика), q биологические мутагены : вирусы оспы, кори, ветряной оспы, простого герпеса вызывают хромосомные аберрации, подавляют репарационные системы. v Токсины плесневых грибов, злаков (проросшее зерно) в ничтожных количествах (5 -7 мкг) вызывают рак печени. v Появление генетически модифицированных продуктов – трансгенов, вызывающих мутацию бактерий желудочно-кишечного тракта, превращая их из сапрофитов в патологические формы. При этом изменяется их устойчивость к антибактериальной терапии.
 q Лекарственный мутагенез, тератогенез, 1. противоопухолевые препараты (сарколизин, 5 -бромурацил, 5 -фторурацил) 2. Седативные ЛС: мепробамат, хлорпромазин, клозепин, галоперидол, противосудорожные препараты (барбитураты и др. ) имеют мутагенный и тератогенный эффекты; 3. антиметаболиты: антагонисты фолиевой кислоты (метотрексат), аналоги пуриновых оснований (меркаптопурин), аналоги пиримидиновых оснований (фторурацил) имеют мутагенный эффект; 4. цитостатики (винкрестин) вызывают анеуплоидию и полиплоидию;
q Лекарственный мутагенез, тератогенез, 1. противоопухолевые препараты (сарколизин, 5 -бромурацил, 5 -фторурацил) 2. Седативные ЛС: мепробамат, хлорпромазин, клозепин, галоперидол, противосудорожные препараты (барбитураты и др. ) имеют мутагенный и тератогенный эффекты; 3. антиметаболиты: антагонисты фолиевой кислоты (метотрексат), аналоги пуриновых оснований (меркаптопурин), аналоги пиримидиновых оснований (фторурацил) имеют мутагенный эффект; 4. цитостатики (винкрестин) вызывают анеуплоидию и полиплоидию;
 5. антибиотики: актиномицин-D, митомицин-С индуцируют хромосомные аберрации; стрептомицин, неомицин, тетрациклин, эритромицин, левомецитин, каномицин - -- -изменяют процесс реализации генетической информации. Наиболее опасны они у беременных женщин. Нарушая синтез белка антибиотики оказывают тератогенный эффект на плод; 6. аскорбиновая кислота – умеренный мутаген, однако в первые дни беременности 5 -6 г витамина С могут привести к выкидышу; 7. гормоны (эстрадиол, прогестерон), оральные контрацептивы; 8. нестероидные противовоспалительные средства; 9. сульфаниламидные препараты вызывают ипритоподобный эффект. 10. Слабые мутагены – кофеин, теобромин.
5. антибиотики: актиномицин-D, митомицин-С индуцируют хромосомные аберрации; стрептомицин, неомицин, тетрациклин, эритромицин, левомецитин, каномицин - -- -изменяют процесс реализации генетической информации. Наиболее опасны они у беременных женщин. Нарушая синтез белка антибиотики оказывают тератогенный эффект на плод; 6. аскорбиновая кислота – умеренный мутаген, однако в первые дни беременности 5 -6 г витамина С могут привести к выкидышу; 7. гормоны (эстрадиол, прогестерон), оральные контрацептивы; 8. нестероидные противовоспалительные средства; 9. сульфаниламидные препараты вызывают ипритоподобный эффект. 10. Слабые мутагены – кофеин, теобромин.
 Перечисленные факторы, помимо мутагенного эффекта, обладают тератогенностью, что увеличивает число новорожденных с врожденными пороками развития (ВПР). По данным ВОЗ ежегодно в мире рождается 3% детей с генными болезнями (ГБ), 1% детей с хромосомными болезнями (ХБ), 2, 5 -3% детей с ВПР. Кроме физических, химических и биологических факторов важное значение в мутагенезе приобретают медико-социальные причины - Чем выше уровень развития медицины, тем больше изменяется структура наследственной заболеваемости: стали выживать и давать потомство люди, ранее обреченные на смерть.
Перечисленные факторы, помимо мутагенного эффекта, обладают тератогенностью, что увеличивает число новорожденных с врожденными пороками развития (ВПР). По данным ВОЗ ежегодно в мире рождается 3% детей с генными болезнями (ГБ), 1% детей с хромосомными болезнями (ХБ), 2, 5 -3% детей с ВПР. Кроме физических, химических и биологических факторов важное значение в мутагенезе приобретают медико-социальные причины - Чем выше уровень развития медицины, тем больше изменяется структура наследственной заболеваемости: стали выживать и давать потомство люди, ранее обреченные на смерть.
 Генетикачеловека– имеет много разделов: Биохимическая генетика человека включает биохимию нуклеиновых кислот, белков и ферментов у здоровых и больных людей. Здесь применяются такие методы исследования как хроматография, анализ ферментов, расщепление ДНК рестриктазамии др. Цитогенетика человека занимается изучением хромосом человека в норме и патологии. Иммуногенетика человека – это в значительной мере генетика групп крови и тканевых антигенов, типа HLA. Клиническая генетика решает задачи диагностики, прогнозирования, лечения и профилактики различных наследственных заболеваний. Популяционная генетика человека изучает поведение генов в больших популяциях, а также исследует действие таких факторов как дрейф, миграции, мутации и отбор. Фармакогенетика занимается генетическими факторами, обусловливающими распределение и метаболизм лекарств в организме.
Генетикачеловека– имеет много разделов: Биохимическая генетика человека включает биохимию нуклеиновых кислот, белков и ферментов у здоровых и больных людей. Здесь применяются такие методы исследования как хроматография, анализ ферментов, расщепление ДНК рестриктазамии др. Цитогенетика человека занимается изучением хромосом человека в норме и патологии. Иммуногенетика человека – это в значительной мере генетика групп крови и тканевых антигенов, типа HLA. Клиническая генетика решает задачи диагностики, прогнозирования, лечения и профилактики различных наследственных заболеваний. Популяционная генетика человека изучает поведение генов в больших популяциях, а также исследует действие таких факторов как дрейф, миграции, мутации и отбор. Фармакогенетика занимается генетическими факторами, обусловливающими распределение и метаболизм лекарств в организме.
 Задачи медицинской генетики и ее раздела клинической генетики : 1. Изучение причин возникновения наследственных болезней 2. Исследование генома человека 3. Изучение характера наследственной патологии в семьях и распространения этих заболеваний в популяциях; 4. Изучение патогенеза, клиники, лечения, профилактики и прогнозирования наследственных болезней. 5. Исследование механизма наследственной предрасположенности и врожденной резистентности, 6. Установление генетических причин в развитии ненаследственных форм патологии; 7. Разработка генетических аспектов аллергии, иммунитета, канцерогенеза; 8. Изучение условий возникновения и путей профилактики наследственной изменчивости (геномные, хромосомные, генные мутации); 9. Совершенствование методов генной инженерии, методов пренатальной диагностики и медико-генетического консультирования.
Задачи медицинской генетики и ее раздела клинической генетики : 1. Изучение причин возникновения наследственных болезней 2. Исследование генома человека 3. Изучение характера наследственной патологии в семьях и распространения этих заболеваний в популяциях; 4. Изучение патогенеза, клиники, лечения, профилактики и прогнозирования наследственных болезней. 5. Исследование механизма наследственной предрасположенности и врожденной резистентности, 6. Установление генетических причин в развитии ненаследственных форм патологии; 7. Разработка генетических аспектов аллергии, иммунитета, канцерогенеза; 8. Изучение условий возникновения и путей профилактики наследственной изменчивости (геномные, хромосомные, генные мутации); 9. Совершенствование методов генной инженерии, методов пренатальной диагностики и медико-генетического консультирования.
 Классические признаки наследственных заболеваний Наличие в семье больных с подобной патологией; Рецидивирующий хронический характер течения заболевания, особенно у детей; Вовлеченность в патологический процесс многих органов и систем
Классические признаки наследственных заболеваний Наличие в семье больных с подобной патологией; Рецидивирующий хронический характер течения заболевания, особенно у детей; Вовлеченность в патологический процесс многих органов и систем
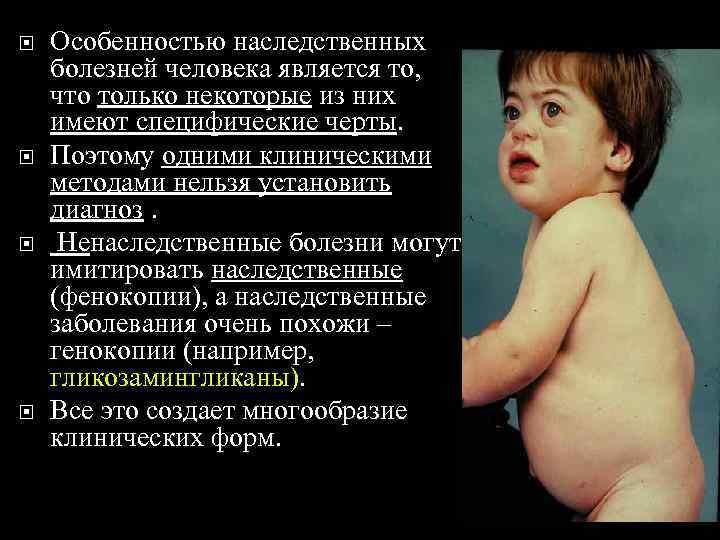
 Особенностью наследственных болезней человека является то, что только некоторые из них имеют специфические черты. Поэтому одними клиническими методами нельзя установить диагноз. Ненаследственные болезни могут имитировать наследственные (фенокопии), а наследственные заболевания очень похожи – генокопии (например, гликозамингликаны). Все это создает многообразие клинических форм.
Особенностью наследственных болезней человека является то, что только некоторые из них имеют специфические черты. Поэтому одними клиническими методами нельзя установить диагноз. Ненаследственные болезни могут имитировать наследственные (фенокопии), а наследственные заболевания очень похожи – генокопии (например, гликозамингликаны). Все это создает многообразие клинических форм.
 С. Н. Давиденков выделил две причины полиморфизма: o Сходное проявление разных мутаций (генокопии); o колебания в выраженности мутантного гена в зависимости от внешней и генотипической среды. Это приводит: o к многообразию отдельных симптомов; o к изменчивости этих признаков; o к появлению переходных и стертых форм; o к возникновению половых и возрастных различий в частоте проявления заболевания в целом и отдельных его симптомов; o к различной тяжести и выраженности клинических, биохимических, иммунологических признаков заболевания; o к неодинаковой прогредиентности и исходу заболевания у разных людей
С. Н. Давиденков выделил две причины полиморфизма: o Сходное проявление разных мутаций (генокопии); o колебания в выраженности мутантного гена в зависимости от внешней и генотипической среды. Это приводит: o к многообразию отдельных симптомов; o к изменчивости этих признаков; o к появлению переходных и стертых форм; o к возникновению половых и возрастных различий в частоте проявления заболевания в целом и отдельных его симптомов; o к различной тяжести и выраженности клинических, биохимических, иммунологических признаков заболевания; o к неодинаковой прогредиентности и исходу заболевания у разных людей
 В рамках одной нозологической формы возможно существование многих клинических вариантов, отличающихся по симптомам, по течению и даже по типу наследования. Наряду с классическими типичными формами заболевания выделяют рудиментарные и атипичные формы. 1. Рудиментарные формы патологии характеризуются наличием стертых симптомов и более доброкачественным течением. 2. Атипичные формы проявляются признаками, которые в классических случаях обычно стоят на втором месте.
В рамках одной нозологической формы возможно существование многих клинических вариантов, отличающихся по симптомам, по течению и даже по типу наследования. Наряду с классическими типичными формами заболевания выделяют рудиментарные и атипичные формы. 1. Рудиментарные формы патологии характеризуются наличием стертых симптомов и более доброкачественным течением. 2. Атипичные формы проявляются признаками, которые в классических случаях обычно стоят на втором месте.
 С усовершенствованием методов исследования отдельные нозологические формы заболеваний все больше дробятся на ряд различных вариантов, иногда совершенно самостоятельных в этиологическом и патогенетическом отношении (например , нервно- мышечные заболевания и гликозаминогликаны). главная причина клинического полиморфизма - генотипический полиморфизм, т. е. изменения на уровне различных генов приводят к очень сходным клиническим проявлениям – генокопиям, когда за внешним сходством клинических проявлений могут скрываться различные генетические дефекты: 1. определенные свойства организма могут контролироваться группой генов. Мутация в одном из генов этой группы приводит к одинаковым фенотипическим эффектам.
С усовершенствованием методов исследования отдельные нозологические формы заболеваний все больше дробятся на ряд различных вариантов, иногда совершенно самостоятельных в этиологическом и патогенетическом отношении (например , нервно- мышечные заболевания и гликозаминогликаны). главная причина клинического полиморфизма - генотипический полиморфизм, т. е. изменения на уровне различных генов приводят к очень сходным клиническим проявлениям – генокопиям, когда за внешним сходством клинических проявлений могут скрываться различные генетические дефекты: 1. определенные свойства организма могут контролироваться группой генов. Мутация в одном из генов этой группы приводит к одинаковым фенотипическим эффектам.
 2. Некоторые гены контролируют различные звенья одного и того же метаболического процесса, а клинически это может проявляться одинаково. 3. Генная детерминация. Некоторые нормальные и палогические признаки обусловлены группой генов аддитивного, т. е. суммарного действия. В частности интеллект контролируется группой генов аддитивного действия, поэтому олигофрении разнородны. 4. Клиническую картину заболеваний могут видоизменять гены - модификаторы.
2. Некоторые гены контролируют различные звенья одного и того же метаболического процесса, а клинически это может проявляться одинаково. 3. Генная детерминация. Некоторые нормальные и палогические признаки обусловлены группой генов аддитивного, т. е. суммарного действия. В частности интеллект контролируется группой генов аддитивного действия, поэтому олигофрении разнородны. 4. Клиническую картину заболеваний могут видоизменять гены - модификаторы.
 Основные термины Генетическая гетерогенность обусловлена тем, что мутации в одном и том же гене приводят к разным последствиям. Плейотропия (полифения гена) – способность оказывать влияние одновременно на несколько признаков. “основной дефект” химической природы имеет многообразные проявления. Плейотропия скорее патогенетическая, чем генетическая концепция. Многие аномальные гены плейотропны. При этом клинически обнаруживаемый симптом указывает на другие, прежде всего скрытые, патологические измениения.
Основные термины Генетическая гетерогенность обусловлена тем, что мутации в одном и том же гене приводят к разным последствиям. Плейотропия (полифения гена) – способность оказывать влияние одновременно на несколько признаков. “основной дефект” химической природы имеет многообразные проявления. Плейотропия скорее патогенетическая, чем генетическая концепция. Многие аномальные гены плейотропны. При этом клинически обнаруживаемый симптом указывает на другие, прежде всего скрытые, патологические измениения.
 Пенетрантность – частота проявляемости гена в признак, выраженная в %. Пенетрантность определяется отношением числа носителей признака к числу носителей соответствующего гена. Пенетрантность считается полной, если поражена половина потомства. Пенетрантность имеет значение почти исключительно в случаях а/д признаков экспрессивность - степень выраженности фенотипа, соответствующего генотипу. Экспрессивность гена варьирует, что зависит от остальных генов и внешней среды.
Пенетрантность – частота проявляемости гена в признак, выраженная в %. Пенетрантность определяется отношением числа носителей признака к числу носителей соответствующего гена. Пенетрантность считается полной, если поражена половина потомства. Пенетрантность имеет значение почти исключительно в случаях а/д признаков экспрессивность - степень выраженности фенотипа, соответствующего генотипу. Экспрессивность гена варьирует, что зависит от остальных генов и внешней среды.
 Гипотеза условного тропизма дефектных генов Суть этой гипотезы заключается в том, что помимо своего прямого влияние на развитие нервной системы патологический ген обладает еще способностью усиливать эффект других наследственных факторов, обладающих сходно направленным тропизмом. Здесь проявляется аллиированный эффект, когда какой-либо наследственный фактор в состоянии резко усилить фенотипическое проявление остальных особенностей генотипа, идущих в том же направлении.
Гипотеза условного тропизма дефектных генов Суть этой гипотезы заключается в том, что помимо своего прямого влияние на развитие нервной системы патологический ген обладает еще способностью усиливать эффект других наследственных факторов, обладающих сходно направленным тропизмом. Здесь проявляется аллиированный эффект, когда какой-либо наследственный фактор в состоянии резко усилить фенотипическое проявление остальных особенностей генотипа, идущих в том же направлении.
 Таким образом интенсивность развития признака определяется не только плейотропным действием основного гена, но и его корреляцией с микрогенотипом. Патологический ген является одновременно условным усилителем разнообразных легких аномалий строения. На этой основе было сформулировано понятие об условном тропизме, который является специфичным для каждой болезненной формы. ( по концепции Давыденкова С. Н. ).
Таким образом интенсивность развития признака определяется не только плейотропным действием основного гена, но и его корреляцией с микрогенотипом. Патологический ген является одновременно условным усилителем разнообразных легких аномалий строения. На этой основе было сформулировано понятие об условном тропизме, который является специфичным для каждой болезненной формы. ( по концепции Давыденкова С. Н. ).
 Методы медико-генетического исследования I. Генеалогический метод или анализ родословных, являясь одним из первых научных методов исследования в медицинской генетике, Этот метод помогает: o установить, является ли данный признак или заболевание единичным или есть другие случаи данной патологии; o определить тип наследования; o Выявить лиц, нуждающихся в МГК; o Разработать план обследования, лечения и профилактики; Основу генеалогического метода составляет анализ родословных таблиц (условные обозначения предложил Г. Юст в 1931 г. ). В конце родословной дается письменное приложение (легенда).
Методы медико-генетического исследования I. Генеалогический метод или анализ родословных, являясь одним из первых научных методов исследования в медицинской генетике, Этот метод помогает: o установить, является ли данный признак или заболевание единичным или есть другие случаи данной патологии; o определить тип наследования; o Выявить лиц, нуждающихся в МГК; o Разработать план обследования, лечения и профилактики; Основу генеалогического метода составляет анализ родословных таблиц (условные обозначения предложил Г. Юст в 1931 г. ). В конце родословной дается письменное приложение (легенда).
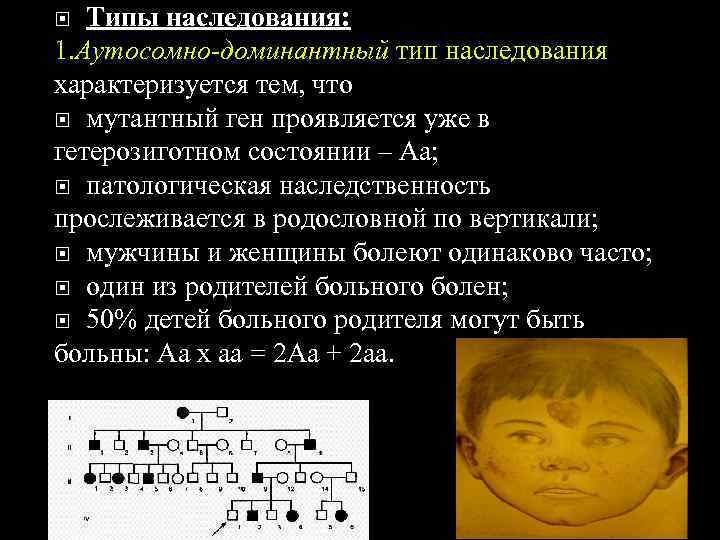
 Типы наследования: 1. Аутосомно-доминантный тип наследования характеризуется тем, что мутантный ген проявляется уже в гетерозиготном состоянии – Aa; патологическая наследственность прослеживается в родословной по вертикали; мужчины и женщины болеют одинаково часто; один из родителей больного болен; 50% детей больного родителя могут быть больны: Aa х aa = 2 Aa + 2 aa.
Типы наследования: 1. Аутосомно-доминантный тип наследования характеризуется тем, что мутантный ген проявляется уже в гетерозиготном состоянии – Aa; патологическая наследственность прослеживается в родословной по вертикали; мужчины и женщины болеют одинаково часто; один из родителей больного болен; 50% детей больного родителя могут быть больны: Aa х aa = 2 Aa + 2 aa.
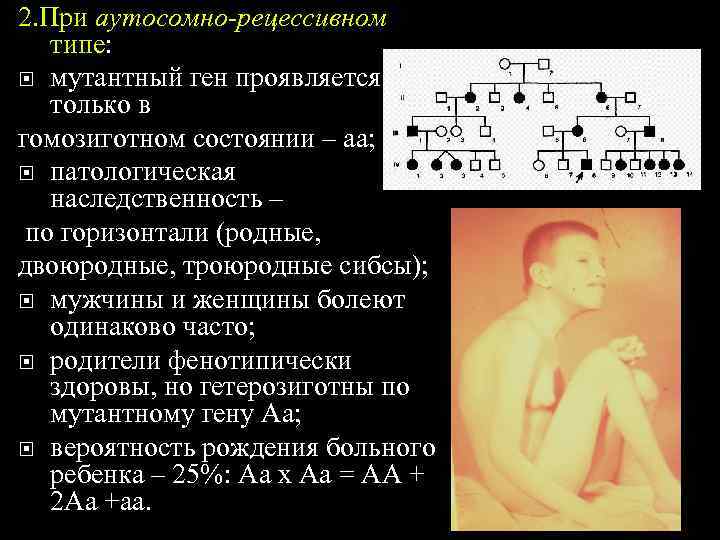
 2. При аутосомно-рецессивном типе: мутантный ген проявляется только в гомозиготном состоянии – аа; патологическая наследственность – по горизонтали (родные, двоюродные, троюродные сибсы); мужчины и женщины болеют одинаково часто; родители фенотипически здоровы, но гетерозиготны по мутантному гену Аа; вероятность рождения больного ребенка – 25%: Аа х Aa = АА + 2 Aa +aa.
2. При аутосомно-рецессивном типе: мутантный ген проявляется только в гомозиготном состоянии – аа; патологическая наследственность – по горизонтали (родные, двоюродные, троюродные сибсы); мужчины и женщины болеют одинаково часто; родители фенотипически здоровы, но гетерозиготны по мутантному гену Аа; вероятность рождения больного ребенка – 25%: Аа х Aa = АА + 2 Aa +aa.
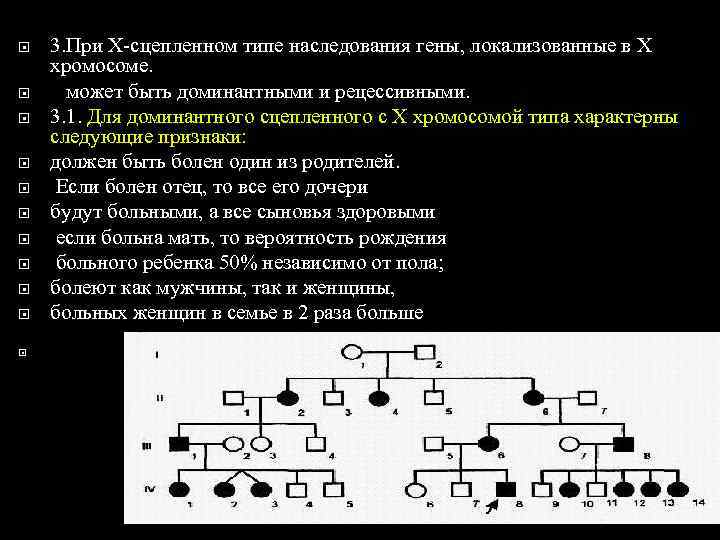
 3. При Х-сцепленном типе наследования гены, локализованные в Х хромосоме. может быть доминантными и рецессивными. 3. 1. Для доминантного сцепленного с Х хромосомой типа характерны следующие признаки: должен быть болен один из родителей. Если болен отец, то все его дочери будут больными, а все сыновья здоровыми если больна мать, то вероятность рождения больного ребенка 50% независимо от пола; болеют как мужчины, так и женщины, больных женщин в семье в 2 раза больше
3. При Х-сцепленном типе наследования гены, локализованные в Х хромосоме. может быть доминантными и рецессивными. 3. 1. Для доминантного сцепленного с Х хромосомой типа характерны следующие признаки: должен быть болен один из родителей. Если болен отец, то все его дочери будут больными, а все сыновья здоровыми если больна мать, то вероятность рождения больного ребенка 50% независимо от пола; болеют как мужчины, так и женщины, больных женщин в семье в 2 раза больше
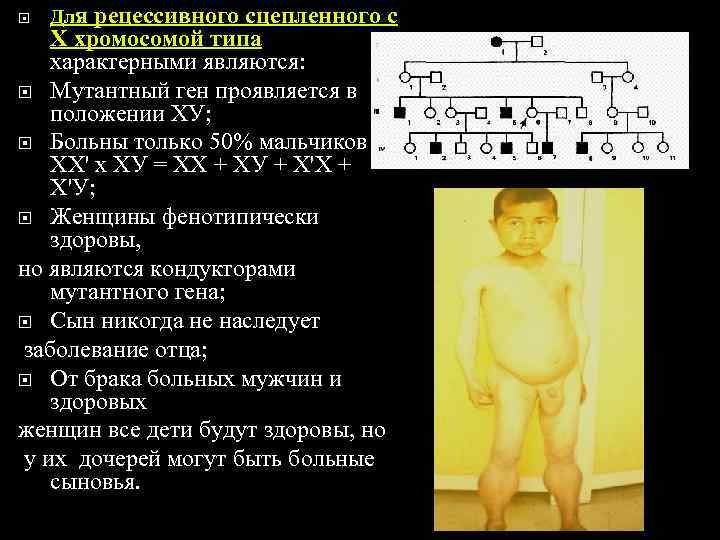
 Для рецессивногосцепленного с Х хромосомой типа характерными являются: Мутантный ген проявляется в положении ХУ; Больны только 50% мальчиков ХХ' х ХУ = ХХ + ХУ + Х'Х + Х'У; Женщины фенотипически здоровы, но являются кондукторами мутантного гена; Сын никогда не наследует заболевание отца; От брака больных мужчин и здоровых женщин все дети будут здоровы, но у их дочерей могут быть больные сыновья.
Для рецессивногосцепленного с Х хромосомой типа характерными являются: Мутантный ген проявляется в положении ХУ; Больны только 50% мальчиков ХХ' х ХУ = ХХ + ХУ + Х'Х + Х'У; Женщины фенотипически здоровы, но являются кондукторами мутантного гена; Сын никогда не наследует заболевание отца; От брака больных мужчин и здоровых женщин все дети будут здоровы, но у их дочерей могут быть больные сыновья.
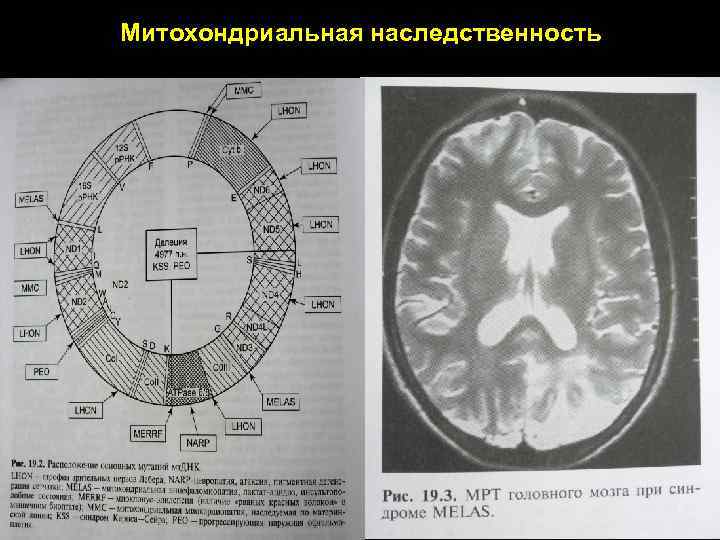
 При сцепленном с полом наследовании, когда патологический ген локализован в У хромосоме, заболевание передается непосредственно от больных мужчин и их сыновьям из поколения в поколение. Митохондриальная наследственность Митохондрии передаются с цитоплазмой яйцеклеток. Спермии не имеют митохондрий. В каждой яйцеклетке содержится около 25000 митохондрий. Каждая митохондрия имеет кольцевую хромосому. Описаны мутации различных генов митохондрий. характерны следующие признаки: передается только от матери; Больны и девочки и мальчики; Больные отцы не передают болезнь ни дочерям, ни сыновьям.
При сцепленном с полом наследовании, когда патологический ген локализован в У хромосоме, заболевание передается непосредственно от больных мужчин и их сыновьям из поколения в поколение. Митохондриальная наследственность Митохондрии передаются с цитоплазмой яйцеклеток. Спермии не имеют митохондрий. В каждой яйцеклетке содержится около 25000 митохондрий. Каждая митохондрия имеет кольцевую хромосому. Описаны мутации различных генов митохондрий. характерны следующие признаки: передается только от матери; Больны и девочки и мальчики; Больные отцы не передают болезнь ни дочерям, ни сыновьям.
 Митохондриальная наследственность
Митохондриальная наследственность
 II. Дерматоглифический метод Изучает рисунок гребешковой кожи ладоней и стоп, который генетически детерминирован. формирование рисунка идет в эмбриогенезе параллельно с органогенезом структур эктодермального происхождения (в том числе нервной системы) и не изменяется в течение жизни, являясь строго индивидуальным. Мутации, нарушающие органогенез, вызывают изменение характера основных элементов кожного узора.
II. Дерматоглифический метод Изучает рисунок гребешковой кожи ладоней и стоп, который генетически детерминирован. формирование рисунка идет в эмбриогенезе параллельно с органогенезом структур эктодермального происхождения (в том числе нервной системы) и не изменяется в течение жизни, являясь строго индивидуальным. Мутации, нарушающие органогенез, вызывают изменение характера основных элементов кожного узора.
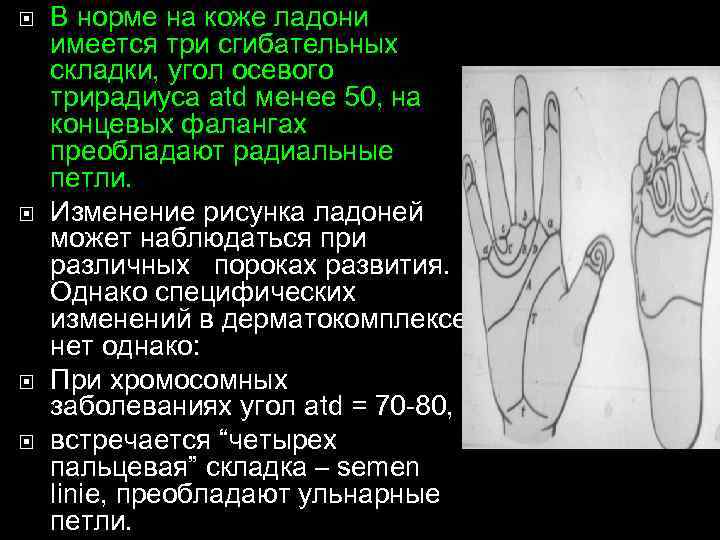
 В норме на коже ладони имеется три сгибательных складки, угол осевого трирадиуса atd менее 50, на концевых фалангах преобладают радиальные петли. Изменение рисунка ладоней может наблюдаться при различных пороках развития. Однако специфических изменений в дерматокомплексе нет однако: При хромосомных заболеваниях угол atd = 70 -80, встречается “четырех пальцевая” складка – semen linie, преобладают ульнарные петли.
В норме на коже ладони имеется три сгибательных складки, угол осевого трирадиуса atd менее 50, на концевых фалангах преобладают радиальные петли. Изменение рисунка ладоней может наблюдаться при различных пороках развития. Однако специфических изменений в дерматокомплексе нет однако: При хромосомных заболеваниях угол atd = 70 -80, встречается “четырех пальцевая” складка – semen linie, преобладают ульнарные петли.
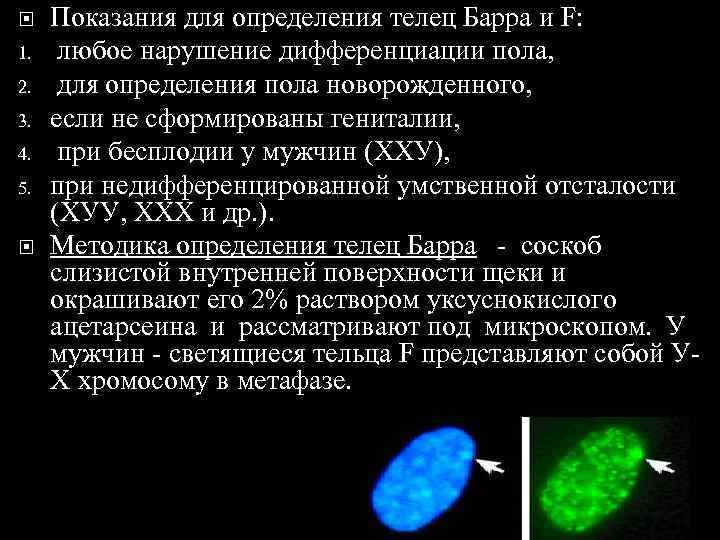
 III. Цитогенетическое исследование проводится в двух вариантах: 1. определение полового хроматина 2. ределение кариотипа клетки. Исследование полового хроматина: женского – телец Барра и мужского – телец F. В клетках женских организмов (46 ХХ) одна Х хромосома в интерфазе инактивирована и находится в спирализованном состоянии, она при окраске клеток ядерными красителями определяется у ядерной оболочки в виде глыбки – тельце Барра (половой хроматин). Тельце Барра является обязательным компонентом клеток, имеющих две Х хромосомы. Увеличение числа Х хромосом сопровождается появлением новых телец Барра, и их всегда на одно меньше, чем половых Х хромосом. При исследовании клеток амниотической жидкости, если телец Барра больше 15%, то плод женского рода, а если меньше 5%, то мужского.
III. Цитогенетическое исследование проводится в двух вариантах: 1. определение полового хроматина 2. ределение кариотипа клетки. Исследование полового хроматина: женского – телец Барра и мужского – телец F. В клетках женских организмов (46 ХХ) одна Х хромосома в интерфазе инактивирована и находится в спирализованном состоянии, она при окраске клеток ядерными красителями определяется у ядерной оболочки в виде глыбки – тельце Барра (половой хроматин). Тельце Барра является обязательным компонентом клеток, имеющих две Х хромосомы. Увеличение числа Х хромосом сопровождается появлением новых телец Барра, и их всегда на одно меньше, чем половых Х хромосом. При исследовании клеток амниотической жидкости, если телец Барра больше 15%, то плод женского рода, а если меньше 5%, то мужского.
 Показания для определения телец Барра и F: 1. любое нарушение дифференциации пола, 2. для определения пола новорожденного, 3. если не сформированы гениталии, 4. при бесплодии у мужчин (ХХУ), 5. при недифференцированной умственной отсталости (ХУУ, ХХХ и др. ). Методика определения телец Барра - соскоб слизистой внутренней поверхности щеки и окрашивают его 2% раствором уксуснокислого ацетарсеина и рассматривают под микроскопом. У мужчин - светящиеся тельца F представляют собой У- Х хромосому в метафазе.
Показания для определения телец Барра и F: 1. любое нарушение дифференциации пола, 2. для определения пола новорожденного, 3. если не сформированы гениталии, 4. при бесплодии у мужчин (ХХУ), 5. при недифференцированной умственной отсталости (ХУУ, ХХХ и др. ). Методика определения телец Барра - соскоб слизистой внутренней поверхности щеки и окрашивают его 2% раствором уксуснокислого ацетарсеина и рассматривают под микроскопом. У мужчин - светящиеся тельца F представляют собой У- Х хромосому в метафазе.
 Для изучения хромосом используется кариотипирование с различной окраской. Сплошная окраска. Способ позволяет распознать только хромосому в целом и определить хромосомный набор 46 ХХ (ХУ). Как известно, в соматических клетках в норме имеет место диплоидный (двойной 23 х2) набор хромосом. Увеличение его в кратное число гаплоидному (одиночному) набору носит название полиплоидии (23 х3 и т. д. ), а в некратное число – анеуплоидии (47 ХХ + 21 и др. ).
Для изучения хромосом используется кариотипирование с различной окраской. Сплошная окраска. Способ позволяет распознать только хромосому в целом и определить хромосомный набор 46 ХХ (ХУ). Как известно, в соматических клетках в норме имеет место диплоидный (двойной 23 х2) набор хромосом. Увеличение его в кратное число гаплоидному (одиночному) набору носит название полиплоидии (23 х3 и т. д. ), а в некратное число – анеуплоидии (47 ХХ + 21 и др. ).
 Для выявления структурных изменений хромосом (делеция, инверсия, транслокация) применяют дифференцированную окраску. Разница в окраске участков хромосом обусловлена структурой ДНК, содержащейся в хромосоме. Q-сегменты соответствуют участкам ДНК богатым аденин- тимином, R-сегменты – гуанин-цитозином. дифференцированная окраска позволяет распознать оба плеча хромосомы и отдельные сегменты (от 20 до 1200 сегментов). Q-метод – специальное окрашивание хромосом с использованием флуоресцентного вещества акрихин- иприта.
Для выявления структурных изменений хромосом (делеция, инверсия, транслокация) применяют дифференцированную окраску. Разница в окраске участков хромосом обусловлена структурой ДНК, содержащейся в хромосоме. Q-сегменты соответствуют участкам ДНК богатым аденин- тимином, R-сегменты – гуанин-цитозином. дифференцированная окраска позволяет распознать оба плеча хромосомы и отдельные сегменты (от 20 до 1200 сегментов). Q-метод – специальное окрашивание хромосом с использованием флуоресцентного вещества акрихин- иприта.
 Показания для кариотипирования Множественные ВПР (внутриутробные пороки развития) Привычные аборты (более 3 абортов) в сроки до 12 недель – исследуются оба супруга; Недифференцированная умственная отсталость Уточнение диагноза при нарушениях в системе половых хромосом; Подозрение на семейную сбалансированную перестройку хромосом. возраст матери >35 лет или носительства одним из родителей сбалансированной структурной перестройки;
Показания для кариотипирования Множественные ВПР (внутриутробные пороки развития) Привычные аборты (более 3 абортов) в сроки до 12 недель – исследуются оба супруга; Недифференцированная умственная отсталость Уточнение диагноза при нарушениях в системе половых хромосом; Подозрение на семейную сбалансированную перестройку хромосом. возраст матери >35 лет или носительства одним из родителей сбалансированной структурной перестройки;
 Лабораторные методы исследования. IV. направлена на идентификацию одной из трех ступеней болезни: Определение конкретной мутации у индивида (генной, хромосомной, геномной). Это достигается с помощью цитогенетических или молекулярно-генетических методов; Регистрация первичного продукта гена(белка)с помощью биохимических и иммунологических методов; Выявление специфических метаболитов измененного обмена, возникших в результате мутации. применяют биохимических, иммунологических и цитологических методов.
Лабораторные методы исследования. IV. направлена на идентификацию одной из трех ступеней болезни: Определение конкретной мутации у индивида (генной, хромосомной, геномной). Это достигается с помощью цитогенетических или молекулярно-генетических методов; Регистрация первичного продукта гена(белка)с помощью биохимических и иммунологических методов; Выявление специфических метаболитов измененного обмена, возникших в результате мутации. применяют биохимических, иммунологических и цитологических методов.
 Биохимические методы. Биохимические исследования многоступенчаты (в отличие от цитогенетических). Объектами биохимического исследования могут быть кровь, моча, пот, культуры клеток и др. Просеивающий метод – скрининг – применяется для первичной диагностики наследственных болезней. Скрининг может быть массовым (при диагностике ФКУ, гипотиреоза, б. Дауна и др. ) и селективным. Селективные методы предусматривают проверку биохимических аномалий обмена у пациентов с подозрением на генные наследственные болезни. Биохимические методы подразделяют на качественные и количественные. С помощью количественных методов проводят: количественное определение метаболитов, путей их превращения, степени накопления; прямое измерение концентрации, физико- химических качеств измененных Качественные методы основаны на определении продуктов нарушенного метаболизма (при ФКУ фенилаланин не превращается в тирозин ).
Биохимические методы. Биохимические исследования многоступенчаты (в отличие от цитогенетических). Объектами биохимического исследования могут быть кровь, моча, пот, культуры клеток и др. Просеивающий метод – скрининг – применяется для первичной диагностики наследственных болезней. Скрининг может быть массовым (при диагностике ФКУ, гипотиреоза, б. Дауна и др. ) и селективным. Селективные методы предусматривают проверку биохимических аномалий обмена у пациентов с подозрением на генные наследственные болезни. Биохимические методы подразделяют на качественные и количественные. С помощью количественных методов проводят: количественное определение метаболитов, путей их превращения, степени накопления; прямое измерение концентрации, физико- химических качеств измененных Качественные методы основаны на определении продуктов нарушенного метаболизма (при ФКУ фенилаланин не превращается в тирозин ).
 На основе биохимических методов создаются просеивающие (скрининг) программы, проводимые в два этапа: 1 -й этап – используются качественные и полуколичественные методы с обследованием всего намеченного контингента. 2 -ой этап- количественные методы. Скрининг применяется в выявлении ФКУ (частота 1: 10000), гипотиреоз (1: 4500), адрено-генитальный синдром (1: 5000), дефекты нервной трубки (1: 200 – 1: 1500) – @ -фетопротеин. Показания для биохимических методов исследования: 1. Диагностика болезней обмена веществ; 2. Выявление гетерозиготных носителей; 3. Пренатальная диагностика; 4. Проведение скрининг-программ; 5. УМО (умственная отсталость)
На основе биохимических методов создаются просеивающие (скрининг) программы, проводимые в два этапа: 1 -й этап – используются качественные и полуколичественные методы с обследованием всего намеченного контингента. 2 -ой этап- количественные методы. Скрининг применяется в выявлении ФКУ (частота 1: 10000), гипотиреоз (1: 4500), адрено-генитальный синдром (1: 5000), дефекты нервной трубки (1: 200 – 1: 1500) – @ -фетопротеин. Показания для биохимических методов исследования: 1. Диагностика болезней обмена веществ; 2. Выявление гетерозиготных носителей; 3. Пренатальная диагностика; 4. Проведение скрининг-программ; 5. УМО (умственная отсталость)
 6. Нарушение психического статуса; 7. Нарушение физического развития (у детей), деформация костей и суставов, снижение слуха, зрения; 8. Судороги, гипо- и гиперпигментация, мышечная гипо- и гипертония, нарушение координации движений; 9. Непереносимость отдельных пищевых продуктов и лекарственных средств; 10. Почечнокаменная болезнь (у детей) 11. Гемолитическая анемия.
6. Нарушение психического статуса; 7. Нарушение физического развития (у детей), деформация костей и суставов, снижение слуха, зрения; 8. Судороги, гипо- и гиперпигментация, мышечная гипо- и гипертония, нарушение координации движений; 9. Непереносимость отдельных пищевых продуктов и лекарственных средств; 10. Почечнокаменная болезнь (у детей) 11. Гемолитическая анемия.
 Иммуногенетические методы Применяются для обследования при подозрении на иммунодефицитные состояния, на антигенную несовместимость плода и матери, при установлении истинного родства , при необходимости изучения генетических маркеров при диагностике методов сцепления генов или для определения наследственной предрасположенности к болезням. Благодаря этому методу были обнаружены многие нарушения функций ферментов. В частности у больного галактоземией выявлено нарушение активности галактозо-1 -фосфат-уридилтрансферазы. Создание на животных морфологической и биохимической модели.
Иммуногенетические методы Применяются для обследования при подозрении на иммунодефицитные состояния, на антигенную несовместимость плода и матери, при установлении истинного родства , при необходимости изучения генетических маркеров при диагностике методов сцепления генов или для определения наследственной предрасположенности к болезням. Благодаря этому методу были обнаружены многие нарушения функций ферментов. В частности у больного галактоземией выявлено нарушение активности галактозо-1 -фосфат-уридилтрансферазы. Создание на животных морфологической и биохимической модели.
 ДНК-диагностика Метод выявления количественных и качественных изменений нуклеотидного состава участка ДНК. С помощью ДНК-исследований можно подтвердить диагноз наследственного заболевания , выявить носителей мутации в доклиническом периоде болезни, определить прогноз здоровья плода в семье, определить наличие мутации в ДНК бластомера при оплодотворении in vitro, При моногенных наследственных болезнях исследуемым участком ДНК является ген и полиморфные локусы, составляющие с ним единую группу сцепления.
ДНК-диагностика Метод выявления количественных и качественных изменений нуклеотидного состава участка ДНК. С помощью ДНК-исследований можно подтвердить диагноз наследственного заболевания , выявить носителей мутации в доклиническом периоде болезни, определить прогноз здоровья плода в семье, определить наличие мутации в ДНК бластомера при оплодотворении in vitro, При моногенных наследственных болезнях исследуемым участком ДНК является ген и полиморфные локусы, составляющие с ним единую группу сцепления.
 Термин “ген” - фрагмент ДНК, соответствующий определенной единице транскрипции и ассоциированный с регуляторными последовательностями. Полиморфные локусы, сцепленные с геном, как правило, представлены мини- (2 -8 пар нуклеотидов) и макросателлитными (10 -100 тыс. пар нуклеотидов) сайтами рестрикции. Объектом изучения являются ядросодержащие клетки (лейкоциты, ворсины хориона и др. ). Выделенная ДНК представляет собой весь геном организма, поэтому ее называют геномной. Она используется в качестве матрицы для синтеза in vitro большого количества копий исследуемого участка ДНК – ПЦР (полимеразная цепная реакция). Для оценки длины амплифицированного участка ДНК и его нуклеотидного состава применяют методы электрофореза рестрикции и секвенирования – расшифровки первичной последовательности нуклеотидов.
Термин “ген” - фрагмент ДНК, соответствующий определенной единице транскрипции и ассоциированный с регуляторными последовательностями. Полиморфные локусы, сцепленные с геном, как правило, представлены мини- (2 -8 пар нуклеотидов) и макросателлитными (10 -100 тыс. пар нуклеотидов) сайтами рестрикции. Объектом изучения являются ядросодержащие клетки (лейкоциты, ворсины хориона и др. ). Выделенная ДНК представляет собой весь геном организма, поэтому ее называют геномной. Она используется в качестве матрицы для синтеза in vitro большого количества копий исследуемого участка ДНК – ПЦР (полимеразная цепная реакция). Для оценки длины амплифицированного участка ДНК и его нуклеотидного состава применяют методы электрофореза рестрикции и секвенирования – расшифровки первичной последовательности нуклеотидов.
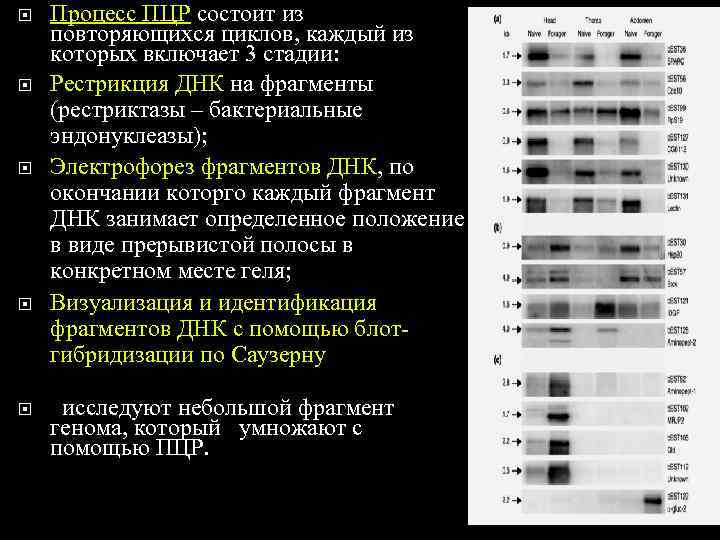
 Процесс ПЦР состоит из повторяющихся циклов, каждый из которых включает 3 стадии: Рестрикция ДНК на фрагменты (рестриктазы – бактериальные эндонуклеазы); Электрофорез фрагментов ДНК, по окончании которго каждый фрагмент ДНК занимает определенное положение в виде прерывистой полосы в конкретном месте геля; Визуализация и идентификация фрагментов ДНК с помощью блот- гибридизации по Саузерну исследуют небольшой фрагмент генома, который умножают с помощью ПЦР.
Процесс ПЦР состоит из повторяющихся циклов, каждый из которых включает 3 стадии: Рестрикция ДНК на фрагменты (рестриктазы – бактериальные эндонуклеазы); Электрофорез фрагментов ДНК, по окончании которго каждый фрагмент ДНК занимает определенное положение в виде прерывистой полосы в конкретном месте геля; Визуализация и идентификация фрагментов ДНК с помощью блот- гибридизации по Саузерну исследуют небольшой фрагмент генома, который умножают с помощью ПЦР.
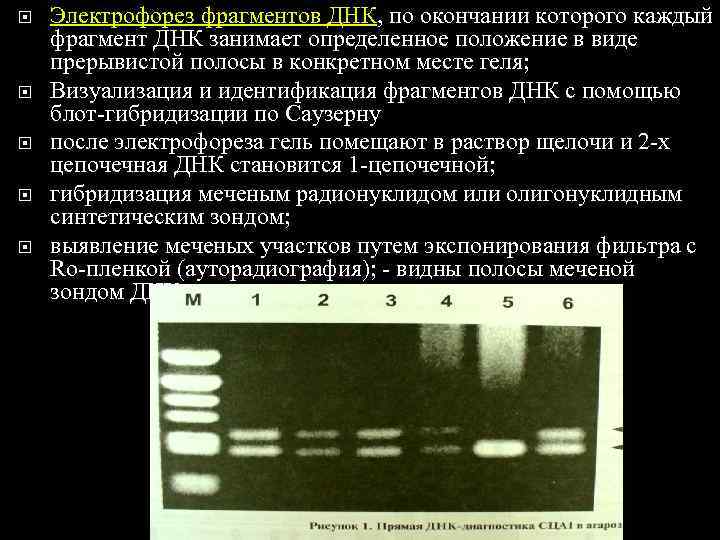
 Электрофорез фрагментов ДНК, по окончании которого каждый фрагмент ДНК занимает определенное положение в виде прерывистой полосы в конкретном месте геля; Визуализация и идентификация фрагментов ДНК с помощью блот-гибридизации по Саузерну после электрофореза гель помещают в раствор щелочи и 2 -х цепочечная ДНК становится 1 -цепочечной; гибридизация меченым радионуклидом или олигонуклидным синтетическим зондом; выявление меченых участков путем экспонирования фильтра с Ro-пленкой (ауторадиография); - видны полосы меченой зондом ДНК.
Электрофорез фрагментов ДНК, по окончании которого каждый фрагмент ДНК занимает определенное положение в виде прерывистой полосы в конкретном месте геля; Визуализация и идентификация фрагментов ДНК с помощью блот-гибридизации по Саузерну после электрофореза гель помещают в раствор щелочи и 2 -х цепочечная ДНК становится 1 -цепочечной; гибридизация меченым радионуклидом или олигонуклидным синтетическим зондом; выявление меченых участков путем экспонирования фильтра с Ro-пленкой (ауторадиография); - видны полосы меченой зондом ДНК.
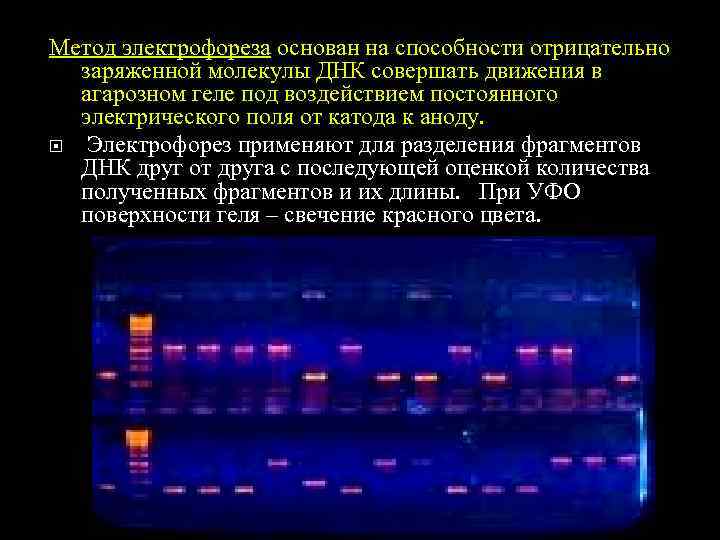
 Метод электрофореза основан на способности отрицательно заряженной молекулы ДНК совершать движения в агарозном геле под воздействием постоянного электрического поля от катода к аноду. Электрофорез применяют для разделения фрагментов ДНК друг от друга с последующей оценкой количества полученных фрагментов и их длины. При УФО поверхности геля – свечение красного цвета.
Метод электрофореза основан на способности отрицательно заряженной молекулы ДНК совершать движения в агарозном геле под воздействием постоянного электрического поля от катода к аноду. Электрофорез применяют для разделения фрагментов ДНК друг от друга с последующей оценкой количества полученных фрагментов и их длины. При УФО поверхности геля – свечение красного цвета.
 ДНК-диагностики. Сущетвует два разных подхода проведения ДНК- диагностики: 1. прямой направлен на исследование гена; 2. косвенный – на изучение сцепленных с геном полиморфных маркеров. Преимущества прямой ДНК-диагностики: обладает абсолютной точностью; требует для анализа только образец ДНК обследуемого лица; может проводиться как в спородических, так и семейных случаях заболевания. позволяет выявить изменения нуклеотидного состава гена: нуклеотидные замены (точковые и мажорные мутации); делеции; дупликации гена или его части; экспансия три- и пентануклеотидных повторов (динамические мутации).
ДНК-диагностики. Сущетвует два разных подхода проведения ДНК- диагностики: 1. прямой направлен на исследование гена; 2. косвенный – на изучение сцепленных с геном полиморфных маркеров. Преимущества прямой ДНК-диагностики: обладает абсолютной точностью; требует для анализа только образец ДНК обследуемого лица; может проводиться как в спородических, так и семейных случаях заболевания. позволяет выявить изменения нуклеотидного состава гена: нуклеотидные замены (точковые и мажорные мутации); делеции; дупликации гена или его части; экспансия три- и пентануклеотидных повторов (динамические мутации).
 Недостатки прямых методов: требуют знания структуры гена, не всегда информативны. Преимущества косвенных методов : не требуют знания гена и мутации в нем, информативны для большинства семей, при невозможности проведения прямой ДНК- диагностики, Недостатки косвенных методов : требуют абсолютной уверенности в клиническом диагнозе, применимы только для монолокусных заболевания, обязателен семейный анализ (в случае отсутствия больных родственников, доступных для обследования, проведение ДНК-диагностики невозможно), неприменима для спорадических случаев заболевания; вероятность ошибки в 1 -5%.
Недостатки прямых методов: требуют знания структуры гена, не всегда информативны. Преимущества косвенных методов : не требуют знания гена и мутации в нем, информативны для большинства семей, при невозможности проведения прямой ДНК- диагностики, Недостатки косвенных методов : требуют абсолютной уверенности в клиническом диагнозе, применимы только для монолокусных заболевания, обязателен семейный анализ (в случае отсутствия больных родственников, доступных для обследования, проведение ДНК-диагностики невозможно), неприменима для спорадических случаев заболевания; вероятность ошибки в 1 -5%.
 Открыт новый тип мутаций, характерный для нейрогередитарных заболеваний – феномен экспансии три- и пентануклеотидных повторов. в некоторых участках генов нуклеотидная последовательность представлена цепочкой тандемных три- или пентануклеотидных повторов (ЦАГ и др. ), число которых норме варьирует в строго определенных пределах. При мутации чаще нарастает число копий таких повторов и мутантный удлиненный ген становится нестабильным, увеличиваясь из поколения в поколение – явление динамической мутации.
Открыт новый тип мутаций, характерный для нейрогередитарных заболеваний – феномен экспансии три- и пентануклеотидных повторов. в некоторых участках генов нуклеотидная последовательность представлена цепочкой тандемных три- или пентануклеотидных повторов (ЦАГ и др. ), число которых норме варьирует в строго определенных пределах. При мутации чаще нарастает число копий таких повторов и мутантный удлиненный ген становится нестабильным, увеличиваясь из поколения в поколение – явление динамической мутации.
 К настоящему времени известно более 15 наследственных заболеваний нервной системы, обусловленными динамическими мутациями (Хорея Гентингтона, АДые атаксии, миотоническая дистрофия (а/д), атаксия Фридрейха (а/р); спинально-бульбарная амиотрофия Кеннеди (Х/р), синдром Мартина-Белла (Х/р). Экспансия три- и пентануклеотидных повторов в гене приводит или к его удлинению и появлению у белка цитотоксических свойств. При этом тяжесть заболевания бывает пропорциональна степени генетического дефекта и сопровождается антиципацией – утяжелению заболевания в следующих поколениях. Прямая ДНК-диагностика три- и пентануклеотидных заболеваний проводится на клинической, доклинической и пренатальной стадиях носительства мутации, что позволяет проводить профилактику повторных случаев заболевания в отягощенных семьях.
К настоящему времени известно более 15 наследственных заболеваний нервной системы, обусловленными динамическими мутациями (Хорея Гентингтона, АДые атаксии, миотоническая дистрофия (а/д), атаксия Фридрейха (а/р); спинально-бульбарная амиотрофия Кеннеди (Х/р), синдром Мартина-Белла (Х/р). Экспансия три- и пентануклеотидных повторов в гене приводит или к его удлинению и появлению у белка цитотоксических свойств. При этом тяжесть заболевания бывает пропорциональна степени генетического дефекта и сопровождается антиципацией – утяжелению заболевания в следующих поколениях. Прямая ДНК-диагностика три- и пентануклеотидных заболеваний проводится на клинической, доклинической и пренатальной стадиях носительства мутации, что позволяет проводить профилактику повторных случаев заболевания в отягощенных семьях.
 Косвенное выявление мутаций Применяется , когда ген не клонирован или нуклеотидная последовательность гена еще не известна, но имеется информация об относительном положении гена на генетической карте. Фактически, это соответствует диагностике с помощью метода сцепления генов. Косвенная ДНК-диагностика по существу сводится к анализу полиморфных генетических маркеров у больных и здоровых членов семьи. Маркерами могут быть участки ДНК, существующие в популяции в нескольких аллельных вариантах. Отличия могут быть по составу нуклеотидов, по числу динуклеотидных повторов. Они передаются в составе одного хромосомного сегмента. Благодаря анализу полиморфных генетических маркеров можно проследить в ряду поколений наследование каждой из родительских хромосом.
Косвенное выявление мутаций Применяется , когда ген не клонирован или нуклеотидная последовательность гена еще не известна, но имеется информация об относительном положении гена на генетической карте. Фактически, это соответствует диагностике с помощью метода сцепления генов. Косвенная ДНК-диагностика по существу сводится к анализу полиморфных генетических маркеров у больных и здоровых членов семьи. Маркерами могут быть участки ДНК, существующие в популяции в нескольких аллельных вариантах. Отличия могут быть по составу нуклеотидов, по числу динуклеотидных повторов. Они передаются в составе одного хромосомного сегмента. Благодаря анализу полиморфных генетических маркеров можно проследить в ряду поколений наследование каждой из родительских хромосом.
 Расположенный вблизи изучаемого гена или внутри него полиморфный сайт может служить маркером аллельных вариантов этого гена, в том числе патологических мутаций. При проведении косвенной ДНК-диагностики могут использоваться как маркеры, сцепленные с геном болезни, так и внутренние маркеры. Косвенная ДНК-диагностика применяется 1. при гепатоцеребральной дистрофии, 2. атаксии-телеангиэктазии, а/р миопатиях, 3. в качестве дополнительного метода у лиц из группы риска при отрицательных результатах традиционного мутационного скрининга (при ПМД Дюшенна-Беккера). Это позволяет определить генетический статус лиц из группы риска (родственники пробанда мужского пола) или плода (при пренатальной диагностике у женщин- носительниц мутантного гена).
Расположенный вблизи изучаемого гена или внутри него полиморфный сайт может служить маркером аллельных вариантов этого гена, в том числе патологических мутаций. При проведении косвенной ДНК-диагностики могут использоваться как маркеры, сцепленные с геном болезни, так и внутренние маркеры. Косвенная ДНК-диагностика применяется 1. при гепатоцеребральной дистрофии, 2. атаксии-телеангиэктазии, а/р миопатиях, 3. в качестве дополнительного метода у лиц из группы риска при отрицательных результатах традиционного мутационного скрининга (при ПМД Дюшенна-Беккера). Это позволяет определить генетический статус лиц из группы риска (родственники пробанда мужского пола) или плода (при пренатальной диагностике у женщин- носительниц мутантного гена).
 Описанные методы широко применяются в клинической практике при пренатальной диагностике целого ряда наследственных болезней, при генетической экспертизе, а так же при обследовании больных с наследственной патологией и подозрением на неё.
Описанные методы широко применяются в клинической практике при пренатальной диагностике целого ряда наследственных болезней, при генетической экспертизе, а так же при обследовании больных с наследственной патологией и подозрением на неё.
 Спасибо за внимание!
Спасибо за внимание!

