Смоленская государственная медицинская академия Кафедра неврологии и






























Лекция 2. Наследственные нервно-мышечные 2.ppt
- Количество слайдов: 36
 Смоленская государственная медицинская академия Кафедра неврологии и нейрохирургии Наследственные нервно-мышечные заболевания Доцент Павлов В. А.
Смоленская государственная медицинская академия Кафедра неврологии и нейрохирургии Наследственные нервно-мышечные заболевания Доцент Павлов В. А.
 Ø Наследственные НМБ насчитывают около 500 форм. Они отличаются генетической гетерогенностью и клиническим полиморфизмом. Ø В группу ННМБ входят: 1) Первичные прогрессирующие мышечные дистрофии(ПМД); 2) Вторичные амиотрофии (спинальные и невральные); 3) Болезни с миотоническим компонентом(миотония Томсона и дистрофическая миотония Штейнера- Баттена); 4) Периодические семейные параличи(пароксизмальные миоплегии).
Ø Наследственные НМБ насчитывают около 500 форм. Они отличаются генетической гетерогенностью и клиническим полиморфизмом. Ø В группу ННМБ входят: 1) Первичные прогрессирующие мышечные дистрофии(ПМД); 2) Вторичные амиотрофии (спинальные и невральные); 3) Болезни с миотоническим компонентом(миотония Томсона и дистрофическая миотония Штейнера- Баттена); 4) Периодические семейные параличи(пароксизмальные миоплегии).
 Прогрессирующие мышечные дистрофии(ПМД) Характерно: Первичная прогрессирующая мышечная дегенерация при отсутствии первичной патологии периферического мотонейрона; Клинические маркёры – «утиная» походка, преимущественное поражение мышц туловища, лица и проксимальных отделов конечностей, лёгкая утомляемость, частые падения, медленное моторное развитие и специфические двигательные ограничения ( подъём рук, вставание с пола, подъём по лестнице); Патологические гены обнаружены в 14 аутосомах(1, 2, 4, 5, 8, 9, 12, 13, 14, 15, 17, 19, 21) и Х-хромосоме.
Прогрессирующие мышечные дистрофии(ПМД) Характерно: Первичная прогрессирующая мышечная дегенерация при отсутствии первичной патологии периферического мотонейрона; Клинические маркёры – «утиная» походка, преимущественное поражение мышц туловища, лица и проксимальных отделов конечностей, лёгкая утомляемость, частые падения, медленное моторное развитие и специфические двигательные ограничения ( подъём рук, вставание с пола, подъём по лестнице); Патологические гены обнаружены в 14 аутосомах(1, 2, 4, 5, 8, 9, 12, 13, 14, 15, 17, 19, 21) и Х-хромосоме.
 Патогенез основных прогрессирующих мышечных дистрофий Зависит от пострадавшего гена –белка и степени дефицита белка-фермента. I. Дефицит аденилатциклазы (нарушен обмен АТФ и ц. АМФ нарушен синтез мышечных белков и клеточная проницаемость = гиперферментемия (КФК и др. ) и гипераминоацидурия). II. Дефицит саркогликана (α, β, Ɣ, σ), присоединяющего белок дистрофин = конечно- поясная форма б. Эрба-Рота. III. Дефицит белка дистрофина. (при этом клеточная проницаемость нарушение работы ионных каналов и накопление внутриклточного Са). ф. Дюшенна, Беккера-Киннера. Мышечные белки попадают в кровь, развивается иммунный ответ с выработкой АТ к белкам мышц и вторичное повреждение мембран миоцитов (порочный круг). Со временем миоциты замещаются соединительной тканью.
Патогенез основных прогрессирующих мышечных дистрофий Зависит от пострадавшего гена –белка и степени дефицита белка-фермента. I. Дефицит аденилатциклазы (нарушен обмен АТФ и ц. АМФ нарушен синтез мышечных белков и клеточная проницаемость = гиперферментемия (КФК и др. ) и гипераминоацидурия). II. Дефицит саркогликана (α, β, Ɣ, σ), присоединяющего белок дистрофин = конечно- поясная форма б. Эрба-Рота. III. Дефицит белка дистрофина. (при этом клеточная проницаемость нарушение работы ионных каналов и накопление внутриклточного Са). ф. Дюшенна, Беккера-Киннера. Мышечные белки попадают в кровь, развивается иммунный ответ с выработкой АТ к белкам мышц и вторичное повреждение мембран миоцитов (порочный круг). Со временем миоциты замещаются соединительной тканью.
 Критерии клинической диагностики: Миопатический синдром; Тип наследования; Возраст появления первых симптомов; Локализация мышечных атрофий; Характер распространения миодистрофического процесса; Наличие или отсутствие псевдогипертрофий. Важны результаты ДНК-диагностики, ЭКГ, ЭНМГ, б/х, иммунологических методов и исследование биоптатов мышц.
Критерии клинической диагностики: Миопатический синдром; Тип наследования; Возраст появления первых симптомов; Локализация мышечных атрофий; Характер распространения миодистрофического процесса; Наличие или отсутствие псевдогипертрофий. Важны результаты ДНК-диагностики, ЭКГ, ЭНМГ, б/х, иммунологических методов и исследование биоптатов мышц.
 Миопатический синдром: лицо миопата - амимия, поперечная улыбка(Джоконды), псевдогипертрофия и слабость круговой мышцы рта(губы тапира), слабость круговых мышц глаз; слабость и атрофия мышц тазового пояса, туловища, живота, проксимальных, а затем дистальных мышц конечностей – вставание лесенкой
Миопатический синдром: лицо миопата - амимия, поперечная улыбка(Джоконды), псевдогипертрофия и слабость круговой мышцы рта(губы тапира), слабость круговых мышц глаз; слабость и атрофия мышц тазового пояса, туловища, живота, проксимальных, а затем дистальных мышц конечностей – вставание лесенкой
 крыловидные лопатки, симптом свободных надплечий, осиная талия, лягушиный живот, поза павлина, утиная походка; Снижение механической возбудимости мышц; Псевдогипертрофии икроножных, ягодичных, дельтовидных и мышц языка.
крыловидные лопатки, симптом свободных надплечий, осиная талия, лягушиный живот, поза павлина, утиная походка; Снижение механической возбудимости мышц; Псевдогипертрофии икроножных, ягодичных, дельтовидных и мышц языка.
 Прогрессирующая мышечная дистрофия Ø Частота 1: 3500 новорожденных мальчиков; Ø Критический возраст 3 -5 лет; ДЮШЕННА Ø Быстро прогрессирует с нарастанием мышечной слабости; Ø Раннее нарушение походки(утиная); Ø Псевдогипертрофии икроножных, ягодичных, дельтовидных и мышц языка; Ø В 10 -13 лет утрачивается способность ходить; Ø Формирование контрактур суставов, деформаций позвоночника и грудной клетки; Ø Эндокринные нарушения – кахексия или ожирение типа Иценко – Кушинга; Ø У 30% - умственная отсталость; Ø В б/х - КФК (в начале заболевания), на ЭНМГ- снижение амплитуды , при нормальной частоте осцилляций; ДНК-диагностика –мутация в локусе Хр21; Ø 18 -20 лет – смерть от ДН и ССН (гипертрофическая и дилатационная кардиомиопатия с аритмией).
Прогрессирующая мышечная дистрофия Ø Частота 1: 3500 новорожденных мальчиков; Ø Критический возраст 3 -5 лет; ДЮШЕННА Ø Быстро прогрессирует с нарастанием мышечной слабости; Ø Раннее нарушение походки(утиная); Ø Псевдогипертрофии икроножных, ягодичных, дельтовидных и мышц языка; Ø В 10 -13 лет утрачивается способность ходить; Ø Формирование контрактур суставов, деформаций позвоночника и грудной клетки; Ø Эндокринные нарушения – кахексия или ожирение типа Иценко – Кушинга; Ø У 30% - умственная отсталость; Ø В б/х - КФК (в начале заболевания), на ЭНМГ- снижение амплитуды , при нормальной частоте осцилляций; ДНК-диагностика –мутация в локусе Хр21; Ø 18 -20 лет – смерть от ДН и ССН (гипертрофическая и дилатационная кардиомиопатия с аритмией).
 Прогрессирующая мышечная дистрофия Беккера-Киннера Ø Частота в 5 -10 меньше формы Дюшенна; Ø Более мягкое течение. Уровень дистрофина 3 -20% от нормы; Ø Аллельный вариант формы Дюшенна (мутация гена Хр21); Ø Критический возраст 12 -20 лет; Ø Псвдогипертрофии мышц сочетаются с симметричными атрофиями с первичной локализацией в мышцах тазового пояса и бёдер, с восходящим распространением на туловище и плечевой пояс; Ø Интеллект не страдает; Ø Способность двигаться сохраняется до 35 -40 лет; Дифференциальный диагноз – определение носительства гена, пренатальная диагностика, иммуногистохимическое исследование мышц на содержание белка дистрофина.
Прогрессирующая мышечная дистрофия Беккера-Киннера Ø Частота в 5 -10 меньше формы Дюшенна; Ø Более мягкое течение. Уровень дистрофина 3 -20% от нормы; Ø Аллельный вариант формы Дюшенна (мутация гена Хр21); Ø Критический возраст 12 -20 лет; Ø Псвдогипертрофии мышц сочетаются с симметричными атрофиями с первичной локализацией в мышцах тазового пояса и бёдер, с восходящим распространением на туловище и плечевой пояс; Ø Интеллект не страдает; Ø Способность двигаться сохраняется до 35 -40 лет; Дифференциальный диагноз – определение носительства гена, пренатальная диагностика, иммуногистохимическое исследование мышц на содержание белка дистрофина.
 Конечностно-поясная форма Эрба-Рота Ø Частота 1, 5: 100 тыс. человек; Ø Генетически гетерогенная – 2 типа и 10 подтипов. (1 А и В типы – аутосомно доминантное наследование, 2 А-Н тип-аутосомно рециссивное); Ø Критический возраст – 3 -5 лет и 16 -17 лет(раннее начало – более тяжелое течение); Ø Выделяют 2 варианта в зависимости от локализации первичной слабости и атрофии мышц : 1)восходящий, 2)нисходящий; Ø Кардиомиопатии- редко; Ø КФК умеренно Ø ЭНМГ – миопатический тип;
Конечностно-поясная форма Эрба-Рота Ø Частота 1, 5: 100 тыс. человек; Ø Генетически гетерогенная – 2 типа и 10 подтипов. (1 А и В типы – аутосомно доминантное наследование, 2 А-Н тип-аутосомно рециссивное); Ø Критический возраст – 3 -5 лет и 16 -17 лет(раннее начало – более тяжелое течение); Ø Выделяют 2 варианта в зависимости от локализации первичной слабости и атрофии мышц : 1)восходящий, 2)нисходящий; Ø Кардиомиопатии- редко; Ø КФК умеренно Ø ЭНМГ – миопатический тип;
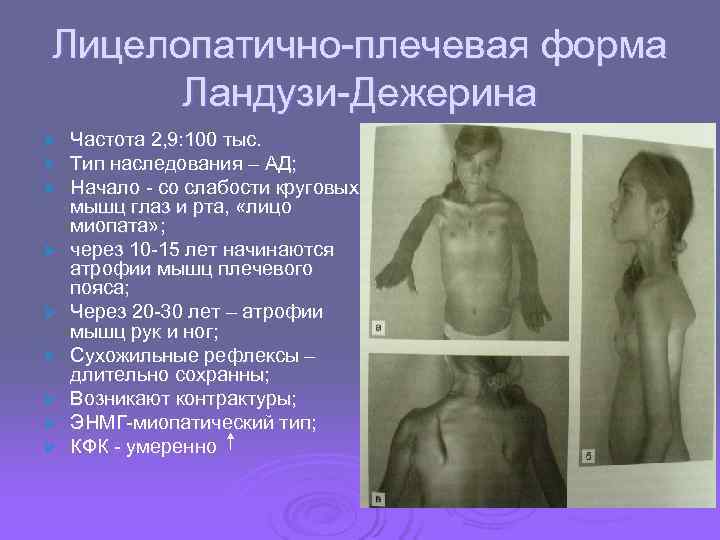
 Лицелопатично-плечевая форма Ландузи-Дежерина Ø Частота 2, 9: 100 тыс. Ø Тип наследования – АД; Ø Начало - со слабости круговых мышц глаз и рта, «лицо миопата» ; Ø через 10 -15 лет начинаются атрофии мышц плечевого пояса; Ø Через 20 -30 лет – атрофии мышц рук и ног; Ø Сухожильные рефлексы – длительно сохранны; Ø Возникают контрактуры; Ø ЭНМГ-миопатический тип; Ø КФК - умеренно
Лицелопатично-плечевая форма Ландузи-Дежерина Ø Частота 2, 9: 100 тыс. Ø Тип наследования – АД; Ø Начало - со слабости круговых мышц глаз и рта, «лицо миопата» ; Ø через 10 -15 лет начинаются атрофии мышц плечевого пояса; Ø Через 20 -30 лет – атрофии мышц рук и ног; Ø Сухожильные рефлексы – длительно сохранны; Ø Возникают контрактуры; Ø ЭНМГ-миопатический тип; Ø КФК - умеренно
 Лечение прогрессирующих мышечных дистрофий: • БЕМИТИЛ (0, 25 х3 р. д. № 15, перерыв 10 дней-до 3 мес) – активация глюконеогенеза и повышение энергопродукции в метохондриях; • ЦИТОХРОМ С (10 -20 мг+ 5% р-р. глюкозы в/в, № 12)потенцирует глюконеогенез; • ЛЕВОДОЗИН –(в/в № 5, затем в/м и сублингвально) – смесь нуклеотидов и нуклеозидов; • ЭНКАРД (1 -1, 5 мл 3, 5% р-ра в/м –в 3 -5 лет, 1, 5 -2 мл – в 5 -8 лет, 4 мл-в 9 -14 лет, № 15 -20) – комплекс олигонуклеотидов дрожжевой РНК. • ПРЕДНИЗОЛОН (0, 35 -0, 75 мг/кг/сут. ) • Клеточная терапия (одноядерные клетки, выращенные in vitro в миобласты в миофибриллы).
Лечение прогрессирующих мышечных дистрофий: • БЕМИТИЛ (0, 25 х3 р. д. № 15, перерыв 10 дней-до 3 мес) – активация глюконеогенеза и повышение энергопродукции в метохондриях; • ЦИТОХРОМ С (10 -20 мг+ 5% р-р. глюкозы в/в, № 12)потенцирует глюконеогенез; • ЛЕВОДОЗИН –(в/в № 5, затем в/м и сублингвально) – смесь нуклеотидов и нуклеозидов; • ЭНКАРД (1 -1, 5 мл 3, 5% р-ра в/м –в 3 -5 лет, 1, 5 -2 мл – в 5 -8 лет, 4 мл-в 9 -14 лет, № 15 -20) – комплекс олигонуклеотидов дрожжевой РНК. • ПРЕДНИЗОЛОН (0, 35 -0, 75 мг/кг/сут. ) • Клеточная терапия (одноядерные клетки, выращенные in vitro в миобласты в миофибриллы).
 Наследственные моторно- сенсорные невропатии (НМСН) Ø - гетерогенная группа генетически детерминированных заболеваний с множественным поражением двигательных, чувствительных и вегетативных волокон периферических нервов. Ø Согласно современной классификации выделяют 7 типов НМСН (1 и 2 типы НМСН с вариантами – болезнь Шарко-Мари).
Наследственные моторно- сенсорные невропатии (НМСН) Ø - гетерогенная группа генетически детерминированных заболеваний с множественным поражением двигательных, чувствительных и вегетативных волокон периферических нервов. Ø Согласно современной классификации выделяют 7 типов НМСН (1 и 2 типы НМСН с вариантами – болезнь Шарко-Мари).
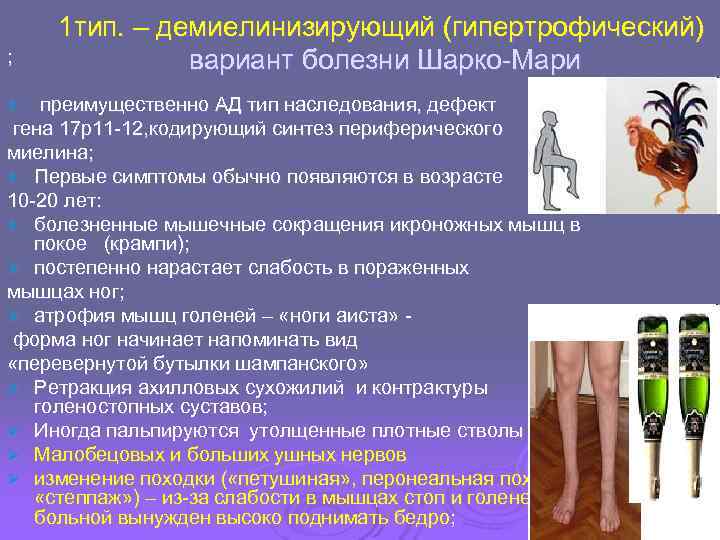
 1 тип. – демиелинизирующий (гипертрофический) ; вариант болезни Шарко-Мари Ø преимущественно АД тип наследования, дефект гена 17 р11 -12, кодирующий синтез периферического миелина; Ø Первые симптомы обычно появляются в возрасте 10 -20 лет: Ø болезненные мышечные сокращения икроножных мышц в покое (крампи); Ø постепенно нарастает слабость в пораженных мышцах ног; Ø атрофия мышц голеней – «ноги аиста» - форма ног начинает напоминать вид «перевернутой бутылки шампанского» Ø Ретракция ахилловых сухожилий и контрактуры голеностопных суставов; Ø Иногда пальпируются утолщенные плотные стволы Ø Малобецовых и больших ушных нервов Ø изменение походки ( «петушиная» , перонеальная походка, «степпаж» ) – из-за слабости в мышцах стоп и голеней , больной вынужден высоко поднимать бедро;
1 тип. – демиелинизирующий (гипертрофический) ; вариант болезни Шарко-Мари Ø преимущественно АД тип наследования, дефект гена 17 р11 -12, кодирующий синтез периферического миелина; Ø Первые симптомы обычно появляются в возрасте 10 -20 лет: Ø болезненные мышечные сокращения икроножных мышц в покое (крампи); Ø постепенно нарастает слабость в пораженных мышцах ног; Ø атрофия мышц голеней – «ноги аиста» - форма ног начинает напоминать вид «перевернутой бутылки шампанского» Ø Ретракция ахилловых сухожилий и контрактуры голеностопных суставов; Ø Иногда пальпируются утолщенные плотные стволы Ø Малобецовых и больших ушных нервов Ø изменение походки ( «петушиная» , перонеальная походка, «степпаж» ) – из-за слабости в мышцах стоп и голеней , больной вынужден высоко поднимать бедро;
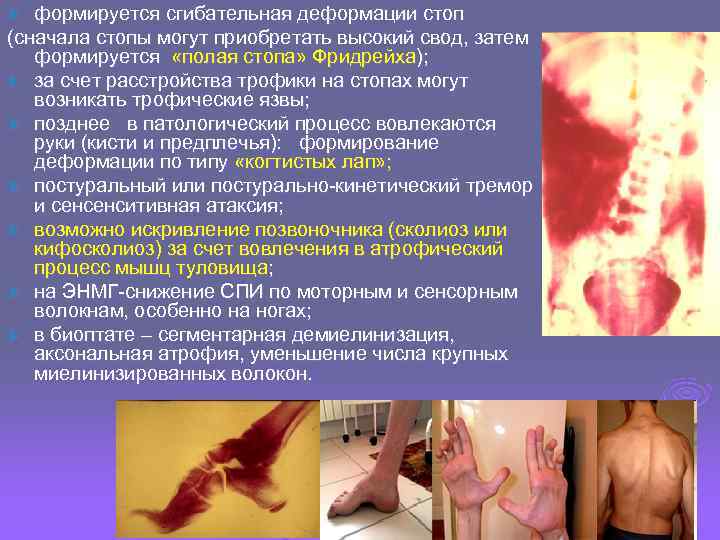
 Ø формируется сгибательная деформации стоп (сначала стопы могут приобретать высокий свод, затем формируется «полая стопа» Фридрейха); Ø за счет расстройства трофики на стопах могут возникать трофические язвы; Ø позднее в патологический процесс вовлекаются руки (кисти и предплечья): формирование деформации по типу «когтистых лап» ; Ø постуральный или постурально-кинетический тремор и сенсенситивная атаксия; Ø возможно искривление позвоночника (сколиоз или кифосколиоз) за счет вовлечения в атрофический процесс мышц туловища; Ø на ЭНМГ-снижение СПИ по моторным и сенсорным волокнам, особенно на ногах; Ø в биоптате – сегментарная демиелинизация, аксональная атрофия, уменьшение числа крупных миелинизированных волокон.
Ø формируется сгибательная деформации стоп (сначала стопы могут приобретать высокий свод, затем формируется «полая стопа» Фридрейха); Ø за счет расстройства трофики на стопах могут возникать трофические язвы; Ø позднее в патологический процесс вовлекаются руки (кисти и предплечья): формирование деформации по типу «когтистых лап» ; Ø постуральный или постурально-кинетический тремор и сенсенситивная атаксия; Ø возможно искривление позвоночника (сколиоз или кифосколиоз) за счет вовлечения в атрофический процесс мышц туловища; Ø на ЭНМГ-снижение СПИ по моторным и сенсорным волокнам, особенно на ногах; Ø в биоптате – сегментарная демиелинизация, аксональная атрофия, уменьшение числа крупных миелинизированных волокон.
 2 тип – нейрональная (аксональная) форма болезни Шарко-Мари дебютирует в 20 -30 лет; Ø тяжелое клиническое течение с выраженными вегетативно-трофическими нарушениями; Ø на ЭНМГ – незначительное снижение СПИ, а на чувствительных волокнах –снижение амплитуды и отсутствие потенциалов действия; Ø в биоптате – уменьшение числа миелинизированных волокон, аксональная атрофия и отсутствие признаков демиелинизации; Ø для идентификации 1 и 2 типов проводится ДНК- исследование.
2 тип – нейрональная (аксональная) форма болезни Шарко-Мари дебютирует в 20 -30 лет; Ø тяжелое клиническое течение с выраженными вегетативно-трофическими нарушениями; Ø на ЭНМГ – незначительное снижение СПИ, а на чувствительных волокнах –снижение амплитуды и отсутствие потенциалов действия; Ø в биоптате – уменьшение числа миелинизированных волокон, аксональная атрофия и отсутствие признаков демиелинизации; Ø для идентификации 1 и 2 типов проводится ДНК- исследование.
 Ø 3 тип – гипертрофический неврит Дежерина – Сотта. Патологический локус выявлен в хромосомах 17 р11 - IIIа и 1 q 22 - 23 с, как и при НМСН I, что исключает нозологическую самостоятельность НМСН 3. Ø НМСН 4 типа (болезнь Рефсума)- болезнь накопления фитановой кислоты. Наследуется по АР типу, мутантные локусы 4 а (8 q 13 -21), 4 b (11 q 22 - 23), 4 c (5 q 23 -33). Проявляется в детском/юношеском возрасте, характерно наличие пигментной дегенерацией сетчатки, ихтиозом, нейросенсорной тугоухостью. Ø НМСН 5 типа наследуются по АД, АР, р/Х типу (р/Х тип похож на болезнь Штрюмпеля) – хq 13 - белок коннексин. Клинически НМСН 5 проявляется на втором-третьем десятилетии жизни медленно нарастающим спастическим парапарезом в сочетании с полиневропатией. Ø НМСН 6 типа наследуется по АД и АР типу, проявляется сочетанием полиневропатии с атрофией зрительных нервов. Ø НМСН 7 типа наследуется по АД типу проявляется сочетанием полиневропатии с пигментным ретинитом, кардиомиопатией и нейросенсорной тугоухостью.
Ø 3 тип – гипертрофический неврит Дежерина – Сотта. Патологический локус выявлен в хромосомах 17 р11 - IIIа и 1 q 22 - 23 с, как и при НМСН I, что исключает нозологическую самостоятельность НМСН 3. Ø НМСН 4 типа (болезнь Рефсума)- болезнь накопления фитановой кислоты. Наследуется по АР типу, мутантные локусы 4 а (8 q 13 -21), 4 b (11 q 22 - 23), 4 c (5 q 23 -33). Проявляется в детском/юношеском возрасте, характерно наличие пигментной дегенерацией сетчатки, ихтиозом, нейросенсорной тугоухостью. Ø НМСН 5 типа наследуются по АД, АР, р/Х типу (р/Х тип похож на болезнь Штрюмпеля) – хq 13 - белок коннексин. Клинически НМСН 5 проявляется на втором-третьем десятилетии жизни медленно нарастающим спастическим парапарезом в сочетании с полиневропатией. Ø НМСН 6 типа наследуется по АД и АР типу, проявляется сочетанием полиневропатии с атрофией зрительных нервов. Ø НМСН 7 типа наследуется по АД типу проявляется сочетанием полиневропатии с пигментным ретинитом, кардиомиопатией и нейросенсорной тугоухостью.
 Проксимальные спинальные амиотрофии детского возраста( ПСАДВ) Ø Наследуются по АР типу. Ø Выделяют 3 фенотипически варианта ПСАВД, отличающиеся возрастом клинической манифестации, течением и прогнозом: Ø в их основе лежит единая генетическая мутация- делеция 7 -8 экзонов на хромосоме 5 q 1, 3; Ø тип I или острая злокачественная инфантильная спинальная амиотрофия Вердинга-Гоффманна; Ø тип II или хроническая инфантильная спинальная амиотрофия (промежуточный тип); Ø тип III или ювенильная спинальная амиотрофия Кугельберга-Веландер.
Проксимальные спинальные амиотрофии детского возраста( ПСАДВ) Ø Наследуются по АР типу. Ø Выделяют 3 фенотипически варианта ПСАВД, отличающиеся возрастом клинической манифестации, течением и прогнозом: Ø в их основе лежит единая генетическая мутация- делеция 7 -8 экзонов на хромосоме 5 q 1, 3; Ø тип I или острая злокачественная инфантильная спинальная амиотрофия Вердинга-Гоффманна; Ø тип II или хроническая инфантильная спинальная амиотрофия (промежуточный тип); Ø тип III или ювенильная спинальная амиотрофия Кугельберга-Веландер.
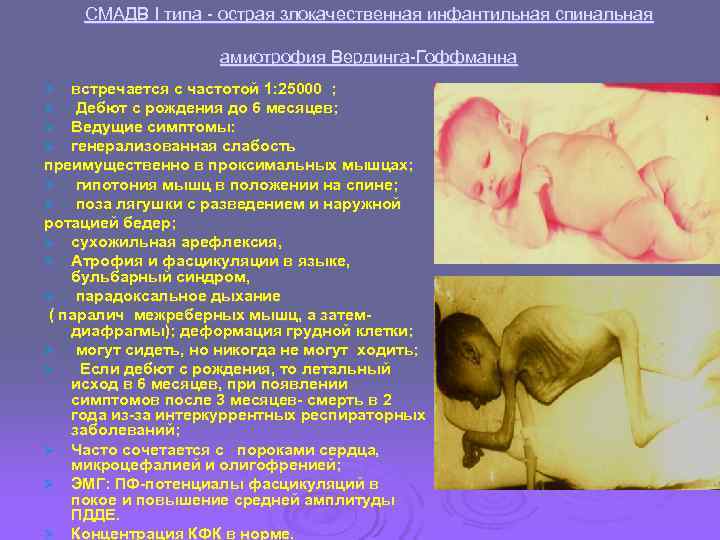
 СМАДВ I типа - острая злокачественная инфантильная спинальная амиотрофия Вердинга-Гоффманна Ø встречается с частотой 1: 25000 ; Ø Дебют с рождения до 6 месяцев; Ø Ведущие симптомы: Ø генерализованная слабость преимущественно в проксимальных мышцах; Ø гипотония мышц в положении на спине; Ø поза лягушки с разведением и наружной ротацией бедер; Ø сухожильная арефлексия, Ø Атрофия и фасцикуляции в языке, бульбарный синдром, Ø парадоксальное дыхание ( паралич межреберных мышц, а затем- диафрагмы); деформация грудной клетки; Ø могут сидеть, но никогда не могут ходить; Ø Если дебют с рождения, то летальный исход в 6 месяцев, при появлении симптомов после 3 месяцев- смерть в 2 года из-за интеркуррентных респираторных заболеваний; Ø Часто сочетается с пороками сердца, микроцефалией и олигофренией; Ø ЭМГ: ПФ-потенциалы фасцикуляций в покое и повышение средней амплитуды ПДДЕ. Ø Концентрация КФК в норме.
СМАДВ I типа - острая злокачественная инфантильная спинальная амиотрофия Вердинга-Гоффманна Ø встречается с частотой 1: 25000 ; Ø Дебют с рождения до 6 месяцев; Ø Ведущие симптомы: Ø генерализованная слабость преимущественно в проксимальных мышцах; Ø гипотония мышц в положении на спине; Ø поза лягушки с разведением и наружной ротацией бедер; Ø сухожильная арефлексия, Ø Атрофия и фасцикуляции в языке, бульбарный синдром, Ø парадоксальное дыхание ( паралич межреберных мышц, а затем- диафрагмы); деформация грудной клетки; Ø могут сидеть, но никогда не могут ходить; Ø Если дебют с рождения, то летальный исход в 6 месяцев, при появлении симптомов после 3 месяцев- смерть в 2 года из-за интеркуррентных респираторных заболеваний; Ø Часто сочетается с пороками сердца, микроцефалией и олигофренией; Ø ЭМГ: ПФ-потенциалы фасцикуляций в покое и повышение средней амплитуды ПДДЕ. Ø Концентрация КФК в норме.
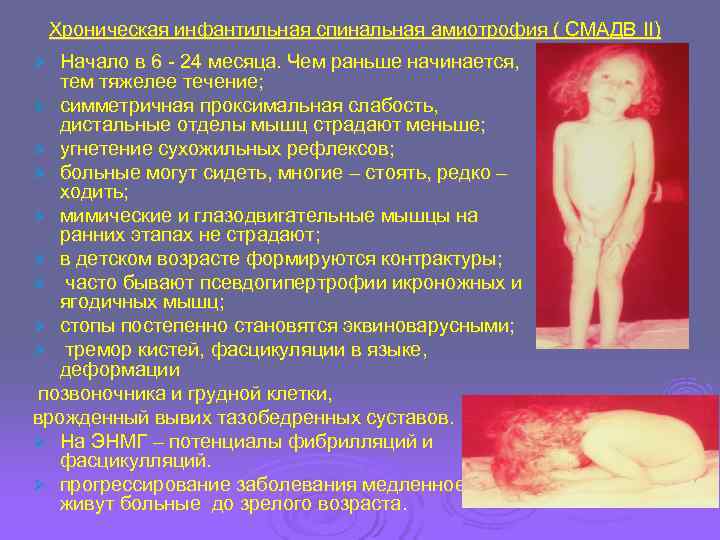
 Хроническая инфантильная спинальная амиотрофия ( СМАДВ II) Ø Начало в 6 - 24 месяца. Чем раньше начинается, тем тяжелее течение; Ø симметричная проксимальная слабость, дистальные отделы мышц страдают меньше; Ø угнетение сухожильных рефлексов; Ø больные могут сидеть, многие – стоять, редко – ходить; Ø мимические и глазодвигательные мышцы на ранних этапах не страдают; Ø в детском возрасте формируются контрактуры; Ø часто бывают псевдогипертрофии икроножных и ягодичных мышц; Ø стопы постепенно становятся эквиноварусными; Ø тремор кистей, фасцикуляции в языке, деформации позвоночника и грудной клетки, врожденный вывих тазобедренных суставов. Ø На ЭНМГ – потенциалы фибрилляций и фасцикулляций. Ø прогрессирование заболевания медленное, живут больные до зрелого возраста.
Хроническая инфантильная спинальная амиотрофия ( СМАДВ II) Ø Начало в 6 - 24 месяца. Чем раньше начинается, тем тяжелее течение; Ø симметричная проксимальная слабость, дистальные отделы мышц страдают меньше; Ø угнетение сухожильных рефлексов; Ø больные могут сидеть, многие – стоять, редко – ходить; Ø мимические и глазодвигательные мышцы на ранних этапах не страдают; Ø в детском возрасте формируются контрактуры; Ø часто бывают псевдогипертрофии икроножных и ягодичных мышц; Ø стопы постепенно становятся эквиноварусными; Ø тремор кистей, фасцикуляции в языке, деформации позвоночника и грудной клетки, врожденный вывих тазобедренных суставов. Ø На ЭНМГ – потенциалы фибрилляций и фасцикулляций. Ø прогрессирование заболевания медленное, живут больные до зрелого возраста.
 Ювенильная спинальная амиотрофия Кугельберга-Веландер(СМАДВ II ) Ø частота 1, 2: 100000; Ø Дебют между 2 и 15 годами, чаще в 5 лет; Ø Характерно: Ø нарастающая слабость в проксимальных отделах ног, а затем и рук; Ø иногда псевдогипертрофии икроножных мышц; Ø умеренная слабость мимических мышц; Ø костные деформации ( примерно в 50%), сухожильные ретракции; Ø сухожильная гипо-, арефлексия; Ø постуральный тремор кистей; Ø концентрация КФК превышает норму в 2 -4 раза; Ø на ЭМГ - спонтанная активность (фасцикуляции, фибрилляции). При напряжении мышц – повышение амплитуды , увеличение длительности и снижение числа ПДДЕ.
Ювенильная спинальная амиотрофия Кугельберга-Веландер(СМАДВ II ) Ø частота 1, 2: 100000; Ø Дебют между 2 и 15 годами, чаще в 5 лет; Ø Характерно: Ø нарастающая слабость в проксимальных отделах ног, а затем и рук; Ø иногда псевдогипертрофии икроножных мышц; Ø умеренная слабость мимических мышц; Ø костные деформации ( примерно в 50%), сухожильные ретракции; Ø сухожильная гипо-, арефлексия; Ø постуральный тремор кистей; Ø концентрация КФК превышает норму в 2 -4 раза; Ø на ЭМГ - спонтанная активность (фасцикуляции, фибрилляции). При напряжении мышц – повышение амплитуды , увеличение длительности и снижение числа ПДДЕ.
 Спинальные амиотрофии взрослых 1. Классическая проксимальная спинальная амиотрофия Ø наследуется по АР типу, начинается на 3 -м десятилетии жизни. Ø АД вариант – тип Финкеля. • Дебют болезни от 10 до 40 -50 лет. • Проксимальные мышцы поражаются тяжелее, чем дистальные. • Заболевание прогрессирует медленно. • Слабость бульбарных мышц нехарактерна. • Сухожильные рефлексы угнетены. 2. Бульбоспинальная амиотрофия Кеннеди: • редкое Х – сцепленное заболевание ( xq 21 -22). • Прогрессирует медленно: поражены бульбарные ядра и ядра передних рогов спинного мозга. • Периоральные фасцикуляции • Постуральный тремор рук. • Центральный нейрон всегда интактен (в отличие от БАС). • Экстраневральные симптомы: гинекомастия, гипогонадизм, сахарный диабет. Ø Диагноз подтверждается при обнаружении мутации гена ( ДНК- диагностика).
Спинальные амиотрофии взрослых 1. Классическая проксимальная спинальная амиотрофия Ø наследуется по АР типу, начинается на 3 -м десятилетии жизни. Ø АД вариант – тип Финкеля. • Дебют болезни от 10 до 40 -50 лет. • Проксимальные мышцы поражаются тяжелее, чем дистальные. • Заболевание прогрессирует медленно. • Слабость бульбарных мышц нехарактерна. • Сухожильные рефлексы угнетены. 2. Бульбоспинальная амиотрофия Кеннеди: • редкое Х – сцепленное заболевание ( xq 21 -22). • Прогрессирует медленно: поражены бульбарные ядра и ядра передних рогов спинного мозга. • Периоральные фасцикуляции • Постуральный тремор рук. • Центральный нейрон всегда интактен (в отличие от БАС). • Экстраневральные симптомы: гинекомастия, гипогонадизм, сахарный диабет. Ø Диагноз подтверждается при обнаружении мутации гена ( ДНК- диагностика).
 Миотонии Ø Миотонии – группа нервно-мышечных заболеваний с нарушением способности мышц расслабляться после сокращения. Ø Врожденная миотония (ВМ) – гетерогенное наследственоое заболевание с мышечной скованностью и истинной мышечной гипертрофией. Ø Патологический ген в хромосоме 7 q 23 -35 Ø АД тип наследования в 19% - болезнь Томсена, АР тип – редко, болезнь Беккера (1 -2%). Ø Миотония генерализованная: большинство случаев – мутации de novo. Ø В патогенезе заболевания основную роль играет нарушение синаптической передачи вследствие дефекта мышечных мембран. Ø Дебют при АД форме в грудном возрасте. Ø Первым симптомом - изменение голоса при плаче. Заболевание протекает мягко. Ø Скованность мышц не сопровождается болью и нарастает при пребывании больного на холоде. Ø При перкуссии мышцы (m. thenar, мышц языка – с. Делла) выявляется мышечный спазм. Ø Миотоническая задержка после отдыха и вначале движений – миотонический спазм. Ø Чаще страдают мышцы кистей, пальцев рук, жеватели. На втром месте – мышцы ног.
Миотонии Ø Миотонии – группа нервно-мышечных заболеваний с нарушением способности мышц расслабляться после сокращения. Ø Врожденная миотония (ВМ) – гетерогенное наследственоое заболевание с мышечной скованностью и истинной мышечной гипертрофией. Ø Патологический ген в хромосоме 7 q 23 -35 Ø АД тип наследования в 19% - болезнь Томсена, АР тип – редко, болезнь Беккера (1 -2%). Ø Миотония генерализованная: большинство случаев – мутации de novo. Ø В патогенезе заболевания основную роль играет нарушение синаптической передачи вследствие дефекта мышечных мембран. Ø Дебют при АД форме в грудном возрасте. Ø Первым симптомом - изменение голоса при плаче. Заболевание протекает мягко. Ø Скованность мышц не сопровождается болью и нарастает при пребывании больного на холоде. Ø При перкуссии мышцы (m. thenar, мышц языка – с. Делла) выявляется мышечный спазм. Ø Миотоническая задержка после отдыха и вначале движений – миотонический спазм. Ø Чаще страдают мышцы кистей, пальцев рук, жеватели. На втром месте – мышцы ног.
 Ø Миотония Томсена – гетерогенное заболевание. - АД тип наследования в 19%, 7 q 23 -35, ген сарколемных белков, формирующих каналы для ионов СI. Ø Частота 0, 3 -0, 7 на 100 тыс. Ø Критический возраст 10 -17 лет, редко старше. При миотонии Томсена выявляется: Ø нарушение обмена ацетилхолина с повышением содержания его свободных форм и уменьшением связанных форм в мышцах и крови; Ø Миотонические нарушения : миотонические задержки ( от нескольких секунд до минут). Повышение механической возбудимости m. thenar, языка (с. Делла); Ø Чаще страдают мышцы кистей и пальцев рук, на втором месте – мышцы ног. Страдает функция жевания. Ø Провоцирует спазм холод. Ø Атлетическое телосложение. Ø Твердые на ощупь мышцы при полном их расслаблении. Ø Мышечная сила снижена. Ø Сухожильные рефлексы вначале снижены, а затем нормализуются.
Ø Миотония Томсена – гетерогенное заболевание. - АД тип наследования в 19%, 7 q 23 -35, ген сарколемных белков, формирующих каналы для ионов СI. Ø Частота 0, 3 -0, 7 на 100 тыс. Ø Критический возраст 10 -17 лет, редко старше. При миотонии Томсена выявляется: Ø нарушение обмена ацетилхолина с повышением содержания его свободных форм и уменьшением связанных форм в мышцах и крови; Ø Миотонические нарушения : миотонические задержки ( от нескольких секунд до минут). Повышение механической возбудимости m. thenar, языка (с. Делла); Ø Чаще страдают мышцы кистей и пальцев рук, на втором месте – мышцы ног. Страдает функция жевания. Ø Провоцирует спазм холод. Ø Атлетическое телосложение. Ø Твердые на ощупь мышцы при полном их расслаблении. Ø Мышечная сила снижена. Ø Сухожильные рефлексы вначале снижены, а затем нормализуются.
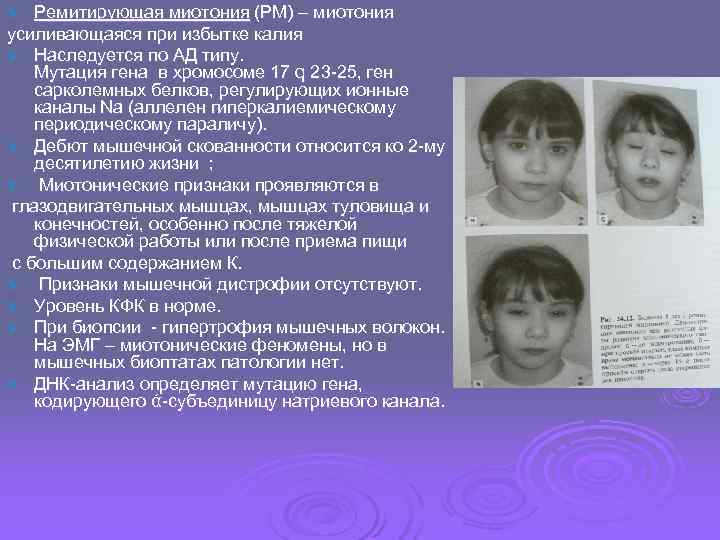
 Ø Ремитирующая миотония (РМ) – миотония усиливающаяся при избытке калия Ø Наследуется по АД типу. Мутация гена в хромосоме 17 q 23 -25, ген сарколемных белков, регулирующих ионные каналы Na (аллелен гиперкалиемическому периодическому параличу). Ø Дебют мышечной скованности относится ко 2 -му десятилетию жизни ; Ø Миотонические признаки проявляются в глазодвигательных мышцах, мышцах туловища и конечностей, особенно после тяжелой физической работы или после приема пищи с большим содержанием К. Ø Признаки мышечной дистрофии отсутствуют. Ø Уровень КФК в норме. Ø При биопсии - гипертрофия мышечных волокон. На ЭМГ – миотонические феномены, но в мышечных биоптатах патологии нет. Ø ДНК-анализ определяет мутацию гена, кодирующего ά-субъединицу натриевого канала.
Ø Ремитирующая миотония (РМ) – миотония усиливающаяся при избытке калия Ø Наследуется по АД типу. Мутация гена в хромосоме 17 q 23 -25, ген сарколемных белков, регулирующих ионные каналы Na (аллелен гиперкалиемическому периодическому параличу). Ø Дебют мышечной скованности относится ко 2 -му десятилетию жизни ; Ø Миотонические признаки проявляются в глазодвигательных мышцах, мышцах туловища и конечностей, особенно после тяжелой физической работы или после приема пищи с большим содержанием К. Ø Признаки мышечной дистрофии отсутствуют. Ø Уровень КФК в норме. Ø При биопсии - гипертрофия мышечных волокон. На ЭМГ – миотонические феномены, но в мышечных биоптатах патологии нет. Ø ДНК-анализ определяет мутацию гена, кодирующего ά-субъединицу натриевого канала.
 Миотоническая дистрофия (МД) Ø МД Куршмана- Штейнерта-Баттена Ø наследуется по АД типу; Ø частота 3 -5: 100 тыс; Ø Мутация в гене 19 q 13. 3, который кодирует белок протеинкиназу- миотонинкиназу; Ø Дебют болезни от перинатального периода до 50 -60 лет. Ø Различают 4 формы МД по возрастному «пику» начала заболевания: врожденная, юношеская, классическая (20 -30 лет) и минимальная (50 -60 лет). Ø в мозге больных обнаружены патологические протеины тау- 55, 64, 69, напоминающие некоторые признаки б. Альцгеймера.
Миотоническая дистрофия (МД) Ø МД Куршмана- Штейнерта-Баттена Ø наследуется по АД типу; Ø частота 3 -5: 100 тыс; Ø Мутация в гене 19 q 13. 3, который кодирует белок протеинкиназу- миотонинкиназу; Ø Дебют болезни от перинатального периода до 50 -60 лет. Ø Различают 4 формы МД по возрастному «пику» начала заболевания: врожденная, юношеская, классическая (20 -30 лет) и минимальная (50 -60 лет). Ø в мозге больных обнаружены патологические протеины тау- 55, 64, 69, напоминающие некоторые признаки б. Альцгеймера.
 Ø Врожденная форма МД • Дебют болезни с первых месяцев жизни и до 10 лет; • диффузная слабость мышц, особенно мимических; • затруднения при сосании и глотании, особенно холодной пищи и жидкости; • развивается дистрофический процесс сначала в мышцах конечностей, а затем в мышцах туловища; • Иногда дети отстают в умственном развитии; • миотонические симптомы – миотоническая задержка и высокая механическая возбудимость.
Ø Врожденная форма МД • Дебют болезни с первых месяцев жизни и до 10 лет; • диффузная слабость мышц, особенно мимических; • затруднения при сосании и глотании, особенно холодной пищи и жидкости; • развивается дистрофический процесс сначала в мышцах конечностей, а затем в мышцах туловища; • Иногда дети отстают в умственном развитии; • миотонические симптомы – миотоническая задержка и высокая механическая возбудимость.
 Ø Юношеская и классическая формы МД • начало в 10 -20 -30 лет; • миодистрофия мышц лица, затем конечностей и в конце - туловища; • миотоническое лицо - удлиненное, утонченное, слабость височных и жевательных мышц; шея тонкая (лебединая) - атрофия грудинно-ключично-сосцевидных мышц); веки и углы рта опущены, нижняя половина лица провисает = выражение его печальное; • нарушается речь, глотание, жевание; Сухожильные рефлексы снижаются и исчезают; • эндокринно-вегетативные нарушения – сухость кожи, раннее облысение со лба, гиперпигментация, снижение активности гонад, гипотиреоз, снижение функции надпочечников и гипофиза, нарушение толерантности к глюкозе; • в сыворотке крови повышена активность γ- глютаматтрансферазы – (транспорт аминокислот через клеточные мембраны); • глюкозурия; Ø прогрессирует умственная отсталость; катаракта; Минимальная форма Мд • появляется в 50 лет и старше. Процесс обычно затрагивает только некоторые группы мышц. Характерно развитие катаракты.
Ø Юношеская и классическая формы МД • начало в 10 -20 -30 лет; • миодистрофия мышц лица, затем конечностей и в конце - туловища; • миотоническое лицо - удлиненное, утонченное, слабость височных и жевательных мышц; шея тонкая (лебединая) - атрофия грудинно-ключично-сосцевидных мышц); веки и углы рта опущены, нижняя половина лица провисает = выражение его печальное; • нарушается речь, глотание, жевание; Сухожильные рефлексы снижаются и исчезают; • эндокринно-вегетативные нарушения – сухость кожи, раннее облысение со лба, гиперпигментация, снижение активности гонад, гипотиреоз, снижение функции надпочечников и гипофиза, нарушение толерантности к глюкозе; • в сыворотке крови повышена активность γ- глютаматтрансферазы – (транспорт аминокислот через клеточные мембраны); • глюкозурия; Ø прогрессирует умственная отсталость; катаракта; Минимальная форма Мд • появляется в 50 лет и старше. Процесс обычно затрагивает только некоторые группы мышц. Характерно развитие катаракты.
 Ø Особенности течения всех форм: 1. Атрофии конечностей наиболее выражены в дистальных отделах предплечья и малоберцовых мышцах; 2. На поздних стадиях заболевания развиваются атрофии мелких мышц кисти; 3. Больные жалуются на затруднения при движении из-за скованности, особенно при охлаждении; 4. Миотонические симптомы уменьшаются по мере нарастания атрофий мышц. 5. В поздних стадиях может развиваться тяжелая кардиомиопатия с сердечной недостаточностью; 6. Часто регистрируются изменения на ЭКГ ; 7. На ЭНМГ- миотонические феномены и миопатические потенциалы;
Ø Особенности течения всех форм: 1. Атрофии конечностей наиболее выражены в дистальных отделах предплечья и малоберцовых мышцах; 2. На поздних стадиях заболевания развиваются атрофии мелких мышц кисти; 3. Больные жалуются на затруднения при движении из-за скованности, особенно при охлаждении; 4. Миотонические симптомы уменьшаются по мере нарастания атрофий мышц. 5. В поздних стадиях может развиваться тяжелая кардиомиопатия с сердечной недостаточностью; 6. Часто регистрируются изменения на ЭКГ ; 7. На ЭНМГ- миотонические феномены и миопатические потенциалы;
 Периодические параличи или пароксизмальные миоплегии Ø Характеризуются приступами вялого паралича скелетных мышц. Ø В зависимости от содержания сывороточного калия подразделяют на: 1. гиперкалиемический, 2. гипокалиемический 3. нормкалиемический.
Периодические параличи или пароксизмальные миоплегии Ø Характеризуются приступами вялого паралича скелетных мышц. Ø В зависимости от содержания сывороточного калия подразделяют на: 1. гиперкалиемический, 2. гипокалиемический 3. нормкалиемический.
 Ø Семейный гиперкалиемический паралич (болезнь Гамстрон) Ø наследуется по АД типу; Ø мутация гена 17 q 23 -25, с нарушением ά-субъединицы Nа-насоса; Ø дебют в раннем детском и грудном возрасте; Ø приступах возникает атония мышц, дети падают и не могут двигаться; Ø приступы провоцируются холодом, голодом, отдыхом после физической нагрузки, приемом хлорида калия, Na. Cl и углеводов. Ø Во время приступа резко выражены вегетативные симптомы: профузный пот, жажда, сердцебиение, повышение АД, в крови содержание калия превышает 5 ммоль/л, а содержание гюкозы снижается; Ø на ЭКГ во время приступа тахикардия, изменение зубца Т, отсутствие зубца Р, интервентрикулярный блок; Ø нет реакции на электрические стимулы ( «трупная реакция» ); Ø ЭНМГ- миотоническая реакция
Ø Семейный гиперкалиемический паралич (болезнь Гамстрон) Ø наследуется по АД типу; Ø мутация гена 17 q 23 -25, с нарушением ά-субъединицы Nа-насоса; Ø дебют в раннем детском и грудном возрасте; Ø приступах возникает атония мышц, дети падают и не могут двигаться; Ø приступы провоцируются холодом, голодом, отдыхом после физической нагрузки, приемом хлорида калия, Na. Cl и углеводов. Ø Во время приступа резко выражены вегетативные симптомы: профузный пот, жажда, сердцебиение, повышение АД, в крови содержание калия превышает 5 ммоль/л, а содержание гюкозы снижается; Ø на ЭКГ во время приступа тахикардия, изменение зубца Т, отсутствие зубца Р, интервентрикулярный блок; Ø нет реакции на электрические стимулы ( «трупная реакция» ); Ø ЭНМГ- миотоническая реакция
 Ø Семейный гипокалиемический паралич (болезнь Вестфаля- Шахновича) • наследуется по АД типу. Ген 1 q 31 -32; • приступы возникают до 16 -летнего возраста (60%) и в 16 -20 лет (40%); • провоцируют приступы отдых после физической нагрузки, обильный прием пищи, богатой углеводами, избыток Na. Cl в пище, прием алкоголя, холод; • длительность приступов от 6 до 12 часов, редко до 2 -3 сут; • во время приступа уровень калия в крови снижен до 1, 5 ммоль/л. • Слабости мышц предшествуют болезненные ощущения в проксимальных группах мышц, жажда, олигоурия. Ø Нормокалиемический периодический паралич (Eilenburg, 1886). • Миоплегия длится от нескольких дней до 2 -3 недель; • сухожильные рефлексы во время приступов исчезают; • иногда бывает гипертрофия отдельных мышц; • прием 8 -10 г Na. Cl ежедневно предупреждает приступы; • Нормокалиемический паралич оценивают как гиперкалиемический периодический паралич с нарушением притока калия в кровь; Диагноз периодического паралича основан на данных клинического обследования: • приступ нарастающей мышечной слабости вплоть до обездвиженности; • длительность приступа от часа до нескольких недель; • изменение концентрации ионов калия сыворотки крови (зависит от формы): при гипокалиемической форме во время атаки концентрация калия ниже 3 ммоль/л, при гиперкалиемической – выше 5 ммоль/л; • семейный характер заболевания;
Ø Семейный гипокалиемический паралич (болезнь Вестфаля- Шахновича) • наследуется по АД типу. Ген 1 q 31 -32; • приступы возникают до 16 -летнего возраста (60%) и в 16 -20 лет (40%); • провоцируют приступы отдых после физической нагрузки, обильный прием пищи, богатой углеводами, избыток Na. Cl в пище, прием алкоголя, холод; • длительность приступов от 6 до 12 часов, редко до 2 -3 сут; • во время приступа уровень калия в крови снижен до 1, 5 ммоль/л. • Слабости мышц предшествуют болезненные ощущения в проксимальных группах мышц, жажда, олигоурия. Ø Нормокалиемический периодический паралич (Eilenburg, 1886). • Миоплегия длится от нескольких дней до 2 -3 недель; • сухожильные рефлексы во время приступов исчезают; • иногда бывает гипертрофия отдельных мышц; • прием 8 -10 г Na. Cl ежедневно предупреждает приступы; • Нормокалиемический паралич оценивают как гиперкалиемический периодический паралич с нарушением притока калия в кровь; Диагноз периодического паралича основан на данных клинического обследования: • приступ нарастающей мышечной слабости вплоть до обездвиженности; • длительность приступа от часа до нескольких недель; • изменение концентрации ионов калия сыворотки крови (зависит от формы): при гипокалиемической форме во время атаки концентрация калия ниже 3 ммоль/л, при гиперкалиемической – выше 5 ммоль/л; • семейный характер заболевания;
 Миастения Ø - это синаптическая аутоиммунная болезнь поперечно-полосатых мышц, характеризующаяся преходящей мышечной слабостью и патологической утомляемостью; Ø Эпидемиология: Частота 0, 5 -5 : 100 тыс. ; Заболевают главным образом молодые люди до 40 лет (женщины в 2 -3 раза чаще, чем мужчины); около 15% больных составляют дети; Ø Этиология: наследственная предрасположенность, (В 8 системы HLA), вирусное поражение вилочковой железы, опухоль тимуса. В редких случаях – первичное поражение головного мозга.
Миастения Ø - это синаптическая аутоиммунная болезнь поперечно-полосатых мышц, характеризующаяся преходящей мышечной слабостью и патологической утомляемостью; Ø Эпидемиология: Частота 0, 5 -5 : 100 тыс. ; Заболевают главным образом молодые люди до 40 лет (женщины в 2 -3 раза чаще, чем мужчины); около 15% больных составляют дети; Ø Этиология: наследственная предрасположенность, (В 8 системы HLA), вирусное поражение вилочковой железы, опухоль тимуса. В редких случаях – первичное поражение головного мозга.
 Ø Главные симптомы: Ø патологическая утомляемость (и слабость) поперечно-полосатых мышц. Нарушаются функции мышц глаз, конечностей, особенно проксимальных мышц, шеи и туловища; Ø опасные для жизни расстройства дыхания и сердечной деятельности. Ø Проба Walker – длительное сжатие пальцев руки усиливает птоз. Ø Течение заболевания прогрессирующее иногда с ремиссиями.
Ø Главные симптомы: Ø патологическая утомляемость (и слабость) поперечно-полосатых мышц. Нарушаются функции мышц глаз, конечностей, особенно проксимальных мышц, шеи и туловища; Ø опасные для жизни расстройства дыхания и сердечной деятельности. Ø Проба Walker – длительное сжатие пальцев руки усиливает птоз. Ø Течение заболевания прогрессирующее иногда с ремиссиями.
 Ø Для диагностики имеет значение прозериновая проба, р. Жолли, ЭНМГ, КТ- исследование вилочковой железы. При стимуляции нерва при ЭНМГ характерно прогрессирующее снижение амплитуды потенциала действия. Кроме того применяют фармакологические пробы с кураре или эндрофонием (тензилом). Эти изменения наблюдаются более чем у 85% больных с генерализованной и у 10% больных с глазной формой миастении. Ø Серологическая диагностика миастении основана на выявление антител к ХР. Наиболее информативно исследование связывающих, блокирующих и моделирующих антител. Связывающие антитела выявляются более, чем у 90% больных генерализованной миастенией.
Ø Для диагностики имеет значение прозериновая проба, р. Жолли, ЭНМГ, КТ- исследование вилочковой железы. При стимуляции нерва при ЭНМГ характерно прогрессирующее снижение амплитуды потенциала действия. Кроме того применяют фармакологические пробы с кураре или эндрофонием (тензилом). Эти изменения наблюдаются более чем у 85% больных с генерализованной и у 10% больных с глазной формой миастении. Ø Серологическая диагностика миастении основана на выявление антител к ХР. Наиболее информативно исследование связывающих, блокирующих и моделирующих антител. Связывающие антитела выявляются более, чем у 90% больных генерализованной миастенией.
 Спасибо за внимание!!!
Спасибо за внимание!!!

