 *
*
 *Сложные вещества, состоящие из атомов водорода, соединенных с кислотным остатком *Электролиты, диссоциирующие с образованием катионов водорода и анионов кислотного остатка *
*Сложные вещества, состоящие из атомов водорода, соединенных с кислотным остатком *Электролиты, диссоциирующие с образованием катионов водорода и анионов кислотного остатка *
 * Признаки классификации Группы кислот Примеры Наличие кислорода в кислотном остатке А) кислородные; Б) бескислородные А) H 3 PO 4, H 2 SO 4; , Б) HBr, H 2 S Основность А) одноосновные; Б) многоосновные А) HNO 3, HCl; Б) H 2 SO 4, H 3 PO 4 Растворимость в воде А) растворимые; Б) нерастворимые А) HNO 3, HCl; Б) H 2 Si. O 3 Летучесть А) летучие; Б) нелетучие А) H 2 S, HNO 3 Б) H 2 SO 4, H 3 PO 4 Степень диссоциации А) сильные; Б) слабые А) HNO 3, HCl; Б) H 2 SO 3, H 2 CO 3 Стабильность А) стабильные; Б) нестабильные А) H 2 SO 4, HCl Б) H 2 SO 3, H 2 CO 3
* Признаки классификации Группы кислот Примеры Наличие кислорода в кислотном остатке А) кислородные; Б) бескислородные А) H 3 PO 4, H 2 SO 4; , Б) HBr, H 2 S Основность А) одноосновные; Б) многоосновные А) HNO 3, HCl; Б) H 2 SO 4, H 3 PO 4 Растворимость в воде А) растворимые; Б) нерастворимые А) HNO 3, HCl; Б) H 2 Si. O 3 Летучесть А) летучие; Б) нелетучие А) H 2 S, HNO 3 Б) H 2 SO 4, H 3 PO 4 Степень диссоциации А) сильные; Б) слабые А) HNO 3, HCl; Б) H 2 SO 3, H 2 CO 3 Стабильность А) стабильные; Б) нестабильные А) H 2 SO 4, HCl Б) H 2 SO 3, H 2 CO 3
 * *Диссоциация; *Взаимодействие с индикаторами; *Взаимодействие с металлами; *Взаимодействие с основными оксидами; *Взаимодействие с основаниями; *Взаимодействие с солями.
* *Диссоциация; *Взаимодействие с индикаторами; *Взаимодействие с металлами; *Взаимодействие с основными оксидами; *Взаимодействие с основаниями; *Взаимодействие с солями.
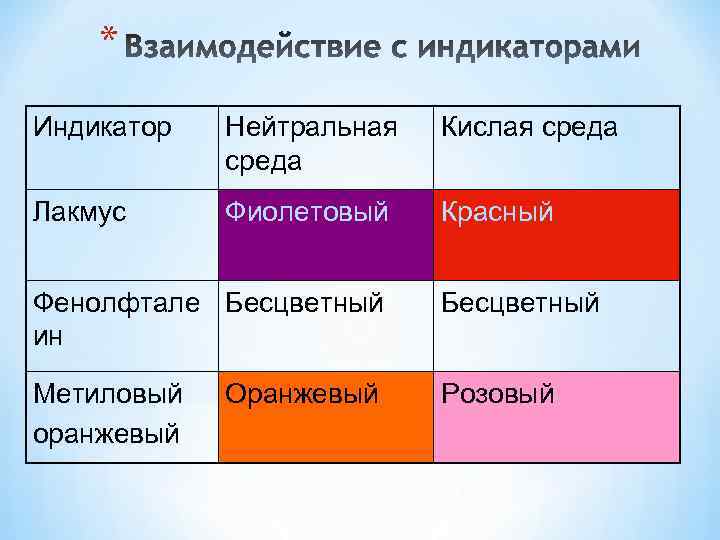 * Индикатор Нейтральная среда Кислая среда Лакмус Фиолетовый Красный Фенолфтале Бесцветный ин Бесцветный Метиловый оранжевый Розовый Оранжевый
* Индикатор Нейтральная среда Кислая среда Лакмус Фиолетовый Красный Фенолфтале Бесцветный ин Бесцветный Метиловый оранжевый Розовый Оранжевый
 * Ме + Нn. Кост → Меn. Костm+ Н 2 металл + кислота→соль + водород 2 Al + 3 H 2 SO 4 → Al 2(SO 4)3 + 3 H 2 Реакция возможна, если: 1. Металл находится в ряду активности до водорода; 2. В результате реакции получается растворимая соль; 3. Кислота растворима
* Ме + Нn. Кост → Меn. Костm+ Н 2 металл + кислота→соль + водород 2 Al + 3 H 2 SO 4 → Al 2(SO 4)3 + 3 H 2 Реакция возможна, если: 1. Металл находится в ряду активности до водорода; 2. В результате реакции получается растворимая соль; 3. Кислота растворима
 * Меx. Oy + Hn. Кост → Меn. Костy + H 2 O Основный оксид + кислота → соль + вода Mg. O + 2 HCl → Mg. Cl 2 + H 2 O Mg. O + 2 H+ + 2 Cl- → Mg 2+ + 2 Cl- + H 2 O Mg. O + 2 H+ → Mg 2+ + H 2 O Реакция возможна, если в результате получается растворимая соль
* Меx. Oy + Hn. Кост → Меn. Костy + H 2 O Основный оксид + кислота → соль + вода Mg. O + 2 HCl → Mg. Cl 2 + H 2 O Mg. O + 2 H+ + 2 Cl- → Mg 2+ + 2 Cl- + H 2 O Mg. O + 2 H+ → Mg 2+ + H 2 O Реакция возможна, если в результате получается растворимая соль
 * Ме(ОН)m + Нn. Кост → Men. Костm + H 2 O Основание + кислота → соль + вода 3 Na. OH + H 3 PO 4→ Na 3 PO 4 + 3 H 2 O 3 Na+ + 3 OH- + 3 H+ + PO 43 - → 3 Na+ + PO 43 - + 3 H 2 O H+ + OH- → H 2 O Реакция между щелочью и кислотой с образованием соли и воды называется реакцией нейтрализации.
* Ме(ОН)m + Нn. Кост → Men. Костm + H 2 O Основание + кислота → соль + вода 3 Na. OH + H 3 PO 4→ Na 3 PO 4 + 3 H 2 O 3 Na+ + 3 OH- + 3 H+ + PO 43 - → 3 Na+ + PO 43 - + 3 H 2 O H+ + OH- → H 2 O Реакция между щелочью и кислотой с образованием соли и воды называется реакцией нейтрализации.
 * Меx. Костy + Hn. Кост → Hх. Кост + Меn. Костy Соль + кислота → новая кислота + новая соль 3 Li 2 CO 3 + 2 H 3 PO 4 → 2 Li 3 PO 4 + 3 H 2 O + 3 CO 2 6 Li+ + 3 CO 32 - + 6 H+ + PO 43 - → 6 Li+ + 2 PO 43 - + 3 H 2 O + 3 CO 2 2 H+ + CO 32 - → H 2 O + CO 2 Реакция возможна, если в результате образуется осадок, газ или слабый электролит
* Меx. Костy + Hn. Кост → Hх. Кост + Меn. Костy Соль + кислота → новая кислота + новая соль 3 Li 2 CO 3 + 2 H 3 PO 4 → 2 Li 3 PO 4 + 3 H 2 O + 3 CO 2 6 Li+ + 3 CO 32 - + 6 H+ + PO 43 - → 6 Li+ + 2 PO 43 - + 3 H 2 O + 3 CO 2 2 H+ + CO 32 - → H 2 O + CO 2 Реакция возможна, если в результате образуется осадок, газ или слабый электролит
 * Лимонная кислота содержится в лимонах. * Яблочная- в яблоках. * Щавелевая - в листьях щавеля. * Муравьиная содержится в выделениях муравьев, пчелином яде и в жгучих волосках крапивы. * Уксусная кислота образуется при скисании виноградного вина. * Молочная – при скисании молока, квашении капусты и силосовании кормов для скота. * Аскорбиновая( витамин С) - в черной смородине, * малине, лимонах, апельсинах, томатах. Недостаток его в пище вызывает заболевание цынгу. *
* Лимонная кислота содержится в лимонах. * Яблочная- в яблоках. * Щавелевая - в листьях щавеля. * Муравьиная содержится в выделениях муравьев, пчелином яде и в жгучих волосках крапивы. * Уксусная кислота образуется при скисании виноградного вина. * Молочная – при скисании молока, квашении капусты и силосовании кормов для скота. * Аскорбиновая( витамин С) - в черной смородине, * малине, лимонах, апельсинах, томатах. Недостаток его в пище вызывает заболевание цынгу. *