 «СЛОЖНЫЕ ЭФИРЫ. ЖИРЫ»
«СЛОЖНЫЕ ЭФИРЫ. ЖИРЫ»
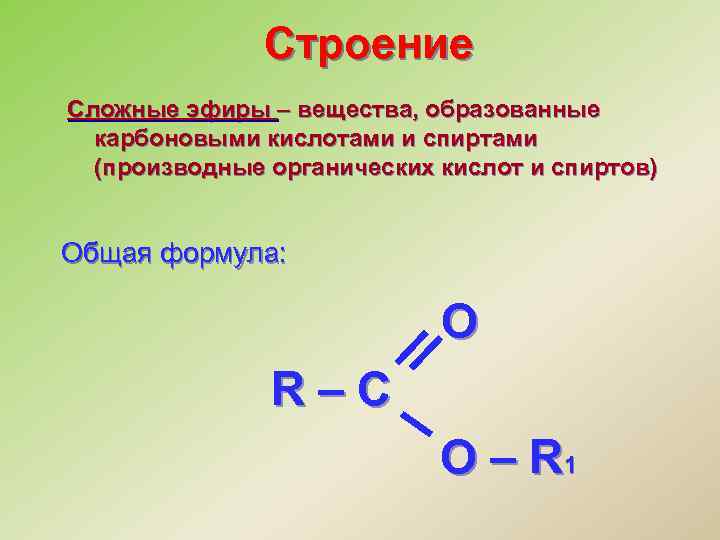 Строение Сложные эфиры – вещества, образованные карбоновыми кислотами и спиртами (производные органических кислот и спиртов) Общая формула: O R–C O – R 1
Строение Сложные эфиры – вещества, образованные карбоновыми кислотами и спиртами (производные органических кислот и спиртов) Общая формула: O R–C O – R 1
 Сложными эфирами - называют производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал. Их состав соответствует общей формуле R–COOR'
Сложными эфирами - называют производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал. Их состав соответствует общей формуле R–COOR'
 Номенклатура Название создается следующим образом: в начале указывается группа R, присоединенная к кислоте, затем – название кислоты с суффиксом «ат» (как и в названиях неорганических солей: карбонат натрия, нитрат хрома).
Номенклатура Название создается следующим образом: в начале указывается группа R, присоединенная к кислоте, затем – название кислоты с суффиксом «ат» (как и в названиях неорганических солей: карбонат натрия, нитрат хрома).
 Номенклатура В основе номенклатуры лежат два способа названия сложных эфиров: 1) по названию радикала спирта и кислотного остатка кислоты (как соли). Например: этил-ацетат 2) полное название эфира по радикалу спирта и названию кислоты. Например: этиловый эфир уксусной кислоты.
Номенклатура В основе номенклатуры лежат два способа названия сложных эфиров: 1) по названию радикала спирта и кислотного остатка кислоты (как соли). Например: этил-ацетат 2) полное название эфира по радикалу спирта и названию кислоты. Например: этиловый эфир уксусной кислоты.
 Агрегатные состояния Сложные эфиры имеют следующие физические свойства: • Жидкое (жидкости) • • • Бесцветные или слабоокрашенные; Нерастворимые в воде; Растворимые в органических растворителях (спиртах); Легче воды; Имеющие характерные запахи; Летучие и горючие.
Агрегатные состояния Сложные эфиры имеют следующие физические свойства: • Жидкое (жидкости) • • • Бесцветные или слабоокрашенные; Нерастворимые в воде; Растворимые в органических растворителях (спиртах); Легче воды; Имеющие характерные запахи; Летучие и горючие.
 Сложные эфиры. Физические свойства Сложные эфиры – жидкости, обладающие приятными фруктовыми запахами. Их плотность меньше плотности воды, они практически не растворяются в воде. Хорошо растворимы в спиртах.
Сложные эфиры. Физические свойства Сложные эфиры – жидкости, обладающие приятными фруктовыми запахами. Их плотность меньше плотности воды, они практически не растворяются в воде. Хорошо растворимы в спиртах.
 Реакции этерификации Реакция образования сложного эфира из спирта и кислоты этерификация гидролиз Реакция получения этилового эфира муравьиной кислоты Реакция получения пропилового эфира уксусной кислоты
Реакции этерификации Реакция образования сложного эфира из спирта и кислоты этерификация гидролиз Реакция получения этилового эфира муравьиной кислоты Реакция получения пропилового эфира уксусной кислоты
 Химические свойства Основное свойство сложных эфиров – гидролиз или разложение водой O R–C + H 2 O → R – COOH + HO – R 1 сложный эфир исходная кислота исходный спирт Условия процесса: нагревание с H 2 SO 4 (концентрированная).
Химические свойства Основное свойство сложных эфиров – гидролиз или разложение водой O R–C + H 2 O → R – COOH + HO – R 1 сложный эфир исходная кислота исходный спирт Условия процесса: нагревание с H 2 SO 4 (концентрированная).
 Специфический аромат ягод, плодов и фруктов Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Сложные эфиры широко распространены в природе. Специфический аромат ягод, плодов и фруктов в значительной степени обусловлен представителями этого класса органических соединений.
Специфический аромат ягод, плодов и фруктов Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Сложные эфиры широко распространены в природе. Специфический аромат ягод, плодов и фруктов в значительной степени обусловлен представителями этого класса органических соединений.
 Зависимость свойств от строения: Запах хризантем НССООСН 2 СН С Н 2 6 5 2 - фенилэтилформиат
Зависимость свойств от строения: Запах хризантем НССООСН 2 СН С Н 2 6 5 2 - фенилэтилформиат
 Зависимость свойств от строения: Запах вишни O H–C O – C 5 H 11 Пентил-формиат (амил-формиат) или Пентиловый (амиловый) эфир муравьиной кислоты
Зависимость свойств от строения: Запах вишни O H–C O – C 5 H 11 Пентил-формиат (амил-формиат) или Пентиловый (амиловый) эфир муравьиной кислоты
 Зависимость свойств от строения: Запах абрикосов О С 3 Н 7 – С О – С 2 Н 5 Этил-пропионат или Этиловый эфир пропионовой кислоты
Зависимость свойств от строения: Запах абрикосов О С 3 Н 7 – С О – С 2 Н 5 Этил-пропионат или Этиловый эфир пропионовой кислоты
 Зависимость свойств от строения: Запах груш О Н 3 С – С О – изо-С 5 Н 11 Изоамилацетат или Изоамиловый (пентиловый) эфир уксусной кислоты
Зависимость свойств от строения: Запах груш О Н 3 С – С О – изо-С 5 Н 11 Изоамилацетат или Изоамиловый (пентиловый) эфир уксусной кислоты
 Зависимость свойств от строения: Запах яблок О Изо-С 4 Н 9 – С О – С 2 Н 5 Этиловый эфир изовалериановой кислоты
Зависимость свойств от строения: Запах яблок О Изо-С 4 Н 9 – С О – С 2 Н 5 Этиловый эфир изовалериановой кислоты
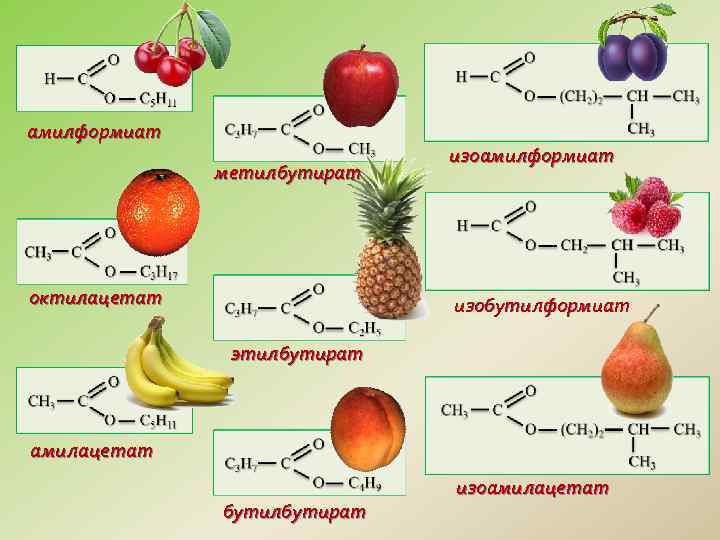 амилформиат метилбутират октилацетат изоамилформиат изобутилформиат этилбутират амилацетат бутилбутират изоамилацетат
амилформиат метилбутират октилацетат изоамилформиат изобутилформиат этилбутират амилацетат бутилбутират изоамилацетат
 Применение лаки синтетические и искусственные волокна производство напитков и кондитерских изделий лекарственные средства парфюмерия и косметика
Применение лаки синтетические и искусственные волокна производство напитков и кондитерских изделий лекарственные средства парфюмерия и косметика
 Нахождение в природе Сложные эфиры входят в состав различных плодов, ягод, фруктов. Запах может определять только один сложный эфир (ананас, вишня, слива, яблоки и др. ) или сложное сочетание разных сложных эфиров «букет» (в землянике аромат 40 разных сложных эфиров).
Нахождение в природе Сложные эфиры входят в состав различных плодов, ягод, фруктов. Запах может определять только один сложный эфир (ананас, вишня, слива, яблоки и др. ) или сложное сочетание разных сложных эфиров «букет» (в землянике аромат 40 разных сложных эфиров).
 Воски Сложные эфиры жирных кислот и спиртов с длинными углеводородными радикалами называют восками. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта CH 3(CH 2)14–CO–OCH 2(CH 2)29 CH 3.
Воски Сложные эфиры жирных кислот и спиртов с длинными углеводородными радикалами называют восками. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта CH 3(CH 2)14–CO–OCH 2(CH 2)29 CH 3.
 Нахождение в природе Пчелиный воск –эфир пальмитиновой кислоты и мирицилового спирта С 15 Н 31 СООС 31 Н 63
Нахождение в природе Пчелиный воск –эфир пальмитиновой кислоты и мирицилового спирта С 15 Н 31 СООС 31 Н 63
 Сложные эфиры имеют большое практическое значение 1. Их применяют в промышленности в качестве растворителей и промежуточных продуктов при синтезе различных органических соединений. 2. Сложные эфиры с приятным запахом используют в парфюмерии и пищевой промышленности. 3. Сложные эфиры часто служат исходными веществами в производстве многих фармацевтических препаратов.
Сложные эфиры имеют большое практическое значение 1. Их применяют в промышленности в качестве растворителей и промежуточных продуктов при синтезе различных органических соединений. 2. Сложные эфиры с приятным запахом используют в парфюмерии и пищевой промышленности. 3. Сложные эфиры часто служат исходными веществами в производстве многих фармацевтических препаратов.
 Применение сложных эфиров Ароматизаторы применяемые в пищевой промышленности сладости йогурты газированные напитки
Применение сложных эфиров Ароматизаторы применяемые в пищевой промышленности сладости йогурты газированные напитки
 Применение сложных эфиров В бытовой химии: парфюмерия растворители, лаки, краски и др.
Применение сложных эфиров В бытовой химии: парфюмерия растворители, лаки, краски и др.
 Из истории: Впервые химический состав жиров определил в начале прошлого века французский химик Мишель Эжен Шеврель
Из истории: Впервые химический состав жиров определил в начале прошлого века французский химик Мишель Эжен Шеврель
 Из истории: То, что в состав жиров и масел входит глицерин, впервые выяснил в 1779 г знаменитый шведский химик Карл Вильгельм Шееле.
Из истории: То, что в состав жиров и масел входит глицерин, впервые выяснил в 1779 г знаменитый шведский химик Карл Вильгельм Шееле.
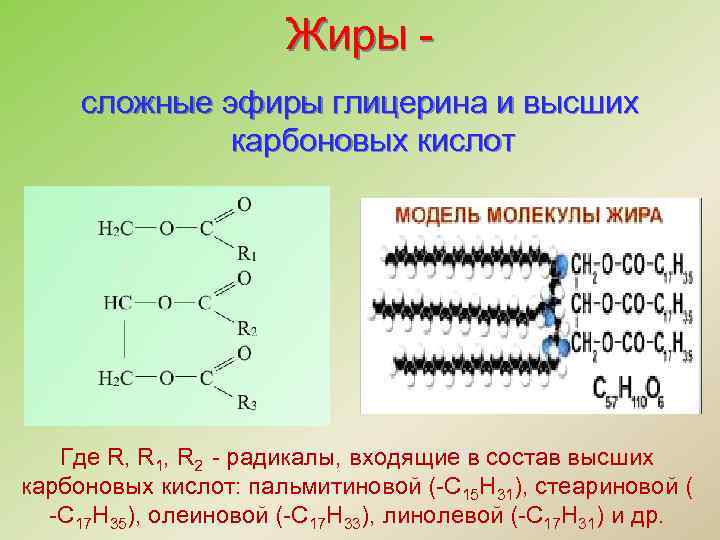 Жиры сложные эфиры глицерина и высших карбоновых кислот Где R, R 1, R 2 - радикалы, входящие в состав высших карбоновых кислот: пальмитиновой (-С 15 Н 31), стеариновой ( -С 17 Н 35), олеиновой (-С 17 Н 33), линолевой (-С 17 Н 31) и др.
Жиры сложные эфиры глицерина и высших карбоновых кислот Где R, R 1, R 2 - радикалы, входящие в состав высших карбоновых кислот: пальмитиновой (-С 15 Н 31), стеариновой ( -С 17 Н 35), олеиновой (-С 17 Н 33), линолевой (-С 17 Н 31) и др.
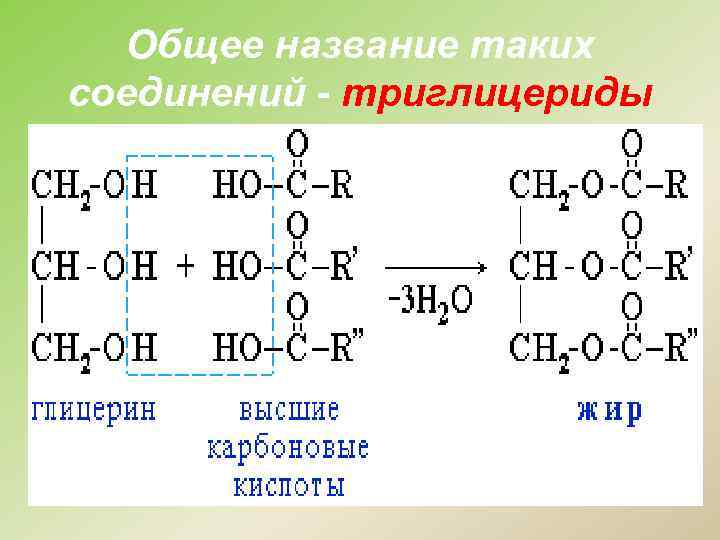 Общее название таких соединений - триглицериды
Общее название таких соединений - триглицериды
 Состав жиров В состав жиров могут входить остатки предельных и непредельных кислот, содержащих четное число атомов углерода и неразветвленный углеродный скелет. Природные жиры, как правило, являются смешанными сложными эфирами, т. е. их молекулы образованны различными карбоновыми кислотами.
Состав жиров В состав жиров могут входить остатки предельных и непредельных кислот, содержащих четное число атомов углерода и неразветвленный углеродный скелет. Природные жиры, как правило, являются смешанными сложными эфирами, т. е. их молекулы образованны различными карбоновыми кислотами.
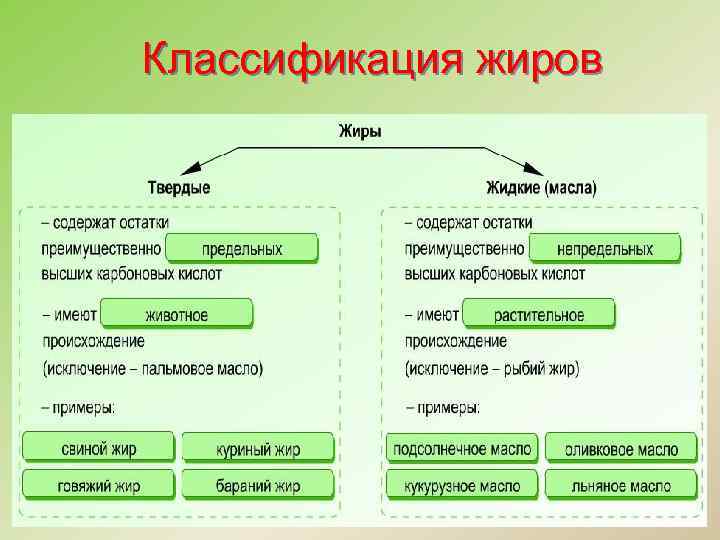 Классификация жиров
Классификация жиров
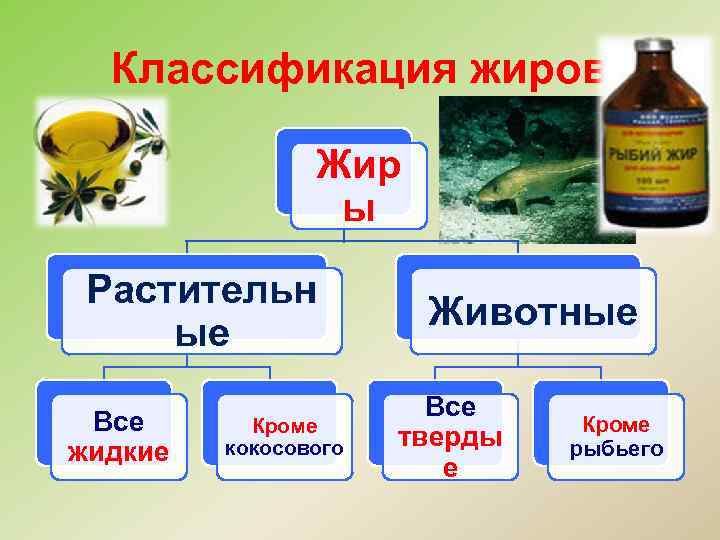 Классификация жиров Жир ы Растительн ые Все жидкие Кроме кокосового Животные Все тверды е Кроме рыбьего
Классификация жиров Жир ы Растительн ые Все жидкие Кроме кокосового Животные Все тверды е Кроме рыбьего
 Жиры получают: Сепаратированием. Является наиболее эффективным методом очистки жиров. Вытапливанием. Гидрирование проводится в специальных автоклавах. Используется этот процесс для получения маргарина. Экстрагированием или прессованием. Сущность процессов прессования заключается в отжимании масла из измельченных семян.
Жиры получают: Сепаратированием. Является наиболее эффективным методом очистки жиров. Вытапливанием. Гидрирование проводится в специальных автоклавах. Используется этот процесс для получения маргарина. Экстрагированием или прессованием. Сущность процессов прессования заключается в отжимании масла из измельченных семян.
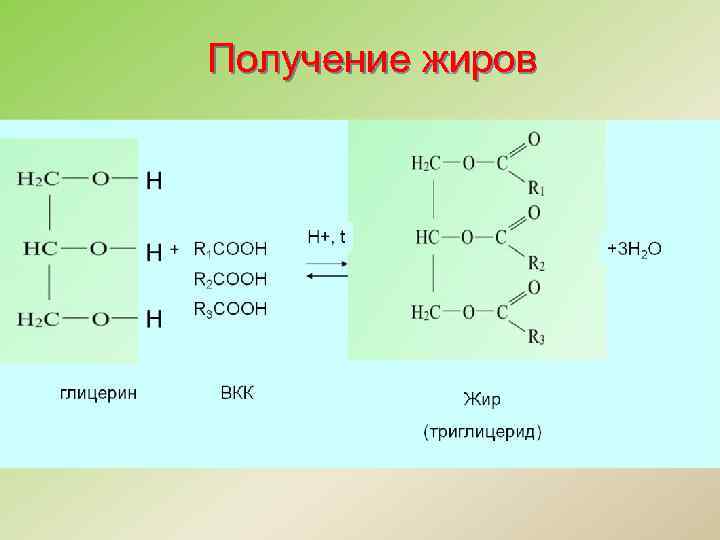 Получение жиров
Получение жиров
 Физические свойства жиров: Жиры не растворимы в воде, но хорошо растворяются в органических растворителях – бензоле, гексане. (эта способность используется для чистки одежды от жировых пятен ) Плотность их меньше 1 г/см 3 Если при комнатной температуре они имеют твердое агрегатное состояние, то их называют жирами, а если жидкое, то – маслами. У жиров низкие температуры кипения. С увеличением длины УВ-радикала температура плавления жира увеличивается.
Физические свойства жиров: Жиры не растворимы в воде, но хорошо растворяются в органических растворителях – бензоле, гексане. (эта способность используется для чистки одежды от жировых пятен ) Плотность их меньше 1 г/см 3 Если при комнатной температуре они имеют твердое агрегатное состояние, то их называют жирами, а если жидкое, то – маслами. У жиров низкие температуры кипения. С увеличением длины УВ-радикала температура плавления жира увеличивается.
 Твердые жиры
Твердые жиры
 Жидкие жиры Оливковое, подсолнечное, льняное масла
Жидкие жиры Оливковое, подсолнечное, льняное масла
 Применение жиров
Применение жиров
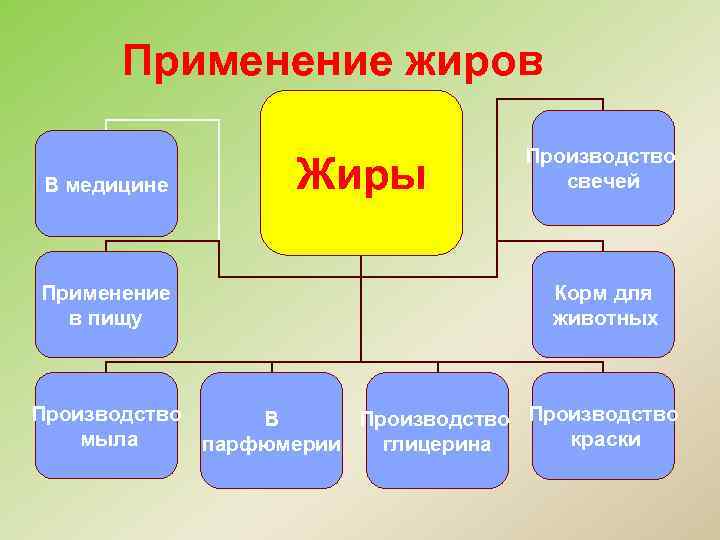 Применение жиров В медицине Применение в пищу Жиры Производство свечей Корм для животных Производство В Производство мыла краски парфюмерии глицерина
Применение жиров В медицине Применение в пищу Жиры Производство свечей Корм для животных Производство В Производство мыла краски парфюмерии глицерина
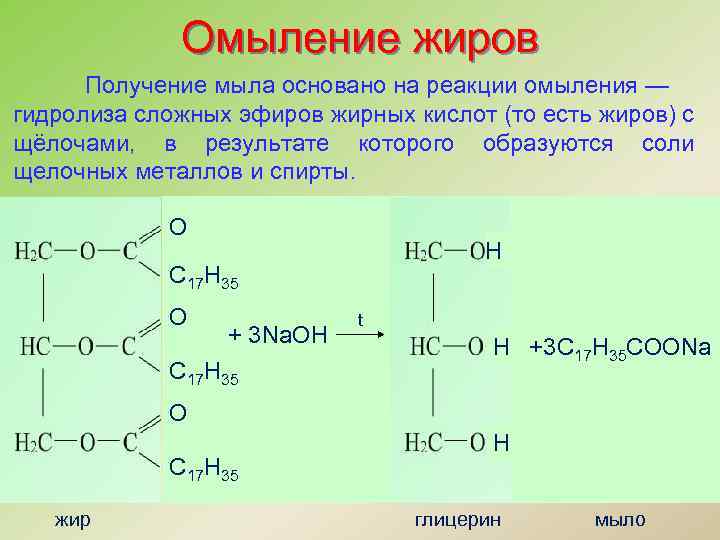 Омыление жиров Получение мыла основано на реакции омыления — гидролиза сложных эфиров жирных кислот (то есть жиров) с щёлочами, в результате которого образуются соли щелочных металлов и спирты. О H С 17 Н 35 О + 3 Na. OH С 17 Н 35 t H +3 C 17 H 35 COONa О С 17 Н 35 жир H глицерин мыло
Омыление жиров Получение мыла основано на реакции омыления — гидролиза сложных эфиров жирных кислот (то есть жиров) с щёлочами, в результате которого образуются соли щелочных металлов и спирты. О H С 17 Н 35 О + 3 Na. OH С 17 Н 35 t H +3 C 17 H 35 COONa О С 17 Н 35 жир H глицерин мыло
 Продукт гидрогенизации масел - твердый жир (искусственное сало, саломас). Маргарин – пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др. ), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др. ).
Продукт гидрогенизации масел - твердый жир (искусственное сало, саломас). Маргарин – пищевой жир, состоит из смеси гидрогенизированных масел (подсолнечного, кукурузного, хлопкого и др. ), животных жиров, молока и вкусовых добавок (соли, сахара, витаминов и др. ).
 Натриевые соли - твердые мыла, калиевые - жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
Натриевые соли - твердые мыла, калиевые - жидкие. Реакция щелочного гидролиза жиров, и вообще всех сложных эфиров, называется также омылением.
 Значение жиров: Жиры имеют большое значение в жизни человека: они выполняют очень важные функции в организме, такие как энергетическая, защитная, строительная.
Значение жиров: Жиры имеют большое значение в жизни человека: они выполняют очень важные функции в организме, такие как энергетическая, защитная, строительная.
 Функции жиров ü Энергетическая (при полном расщеплении 1 г жира до СО 2 и Н 2 О освобождается 38, 9 к. Дж энергии); ü Структурная (жиры – важный компонент каждой клетки); ü Защитная (жиры накапливаются в подкожных тканях и тканях, окружающих внутренние органы).
Функции жиров ü Энергетическая (при полном расщеплении 1 г жира до СО 2 и Н 2 О освобождается 38, 9 к. Дж энергии); ü Структурная (жиры – важный компонент каждой клетки); ü Защитная (жиры накапливаются в подкожных тканях и тканях, окружающих внутренние органы).
 Задание № 1 Составить формулы и дать названия эфирам, образованным 1 вариант: бутановой кислотой и метиловым спиртом; 2 вариант: метановой кислотой и пропиловым спиртом;
Задание № 1 Составить формулы и дать названия эфирам, образованным 1 вариант: бутановой кислотой и метиловым спиртом; 2 вариант: метановой кислотой и пропиловым спиртом;
 Ответ задание № 1 1 вариант: О // СН 3 – СН 2 – СООН + СН 3–ОН → СН 3 – СН 2 – С + Н 2 О бутановая кислота метанол метиловый эфир бутановой кислоты О - СН 3 2 вариант: О // Н – С + СН 3– СН 2 - ОН → Н – С + Н 2 О пропанол ОН О - СН 2 - СН 3 метановая пропиловый эфир метановой кислота кислоты
Ответ задание № 1 1 вариант: О // СН 3 – СН 2 – СООН + СН 3–ОН → СН 3 – СН 2 – С + Н 2 О бутановая кислота метанол метиловый эфир бутановой кислоты О - СН 3 2 вариант: О // Н – С + СН 3– СН 2 - ОН → Н – С + Н 2 О пропанол ОН О - СН 2 - СН 3 метановая пропиловый эфир метановой кислота кислоты
 Задание № 2 Закончите реакцию, назовите полученные вещества 1 вариант: С 5 Н 11 СООН + С 4 Н 9 ОН → 2 вариант: С 7 Н 13 СООН + С 2 Н 5 ОН →
Задание № 2 Закончите реакцию, назовите полученные вещества 1 вариант: С 5 Н 11 СООН + С 4 Н 9 ОН → 2 вариант: С 7 Н 13 СООН + С 2 Н 5 ОН →
 Ответ задание № 2 1 вариант: С 5 Н 11 СООН + С 4 Н 9 ОН → С 5 Н 11 СООС 4 Н 9 + Н 2 О 2 вариант: С 7 Н 13 СООН + С 2 Н 5 ОН → С 7 Н 13 СООС 2 Н 5+ Н 2 О
Ответ задание № 2 1 вариант: С 5 Н 11 СООН + С 4 Н 9 ОН → С 5 Н 11 СООС 4 Н 9 + Н 2 О 2 вариант: С 7 Н 13 СООН + С 2 Н 5 ОН → С 7 Н 13 СООС 2 Н 5+ Н 2 О
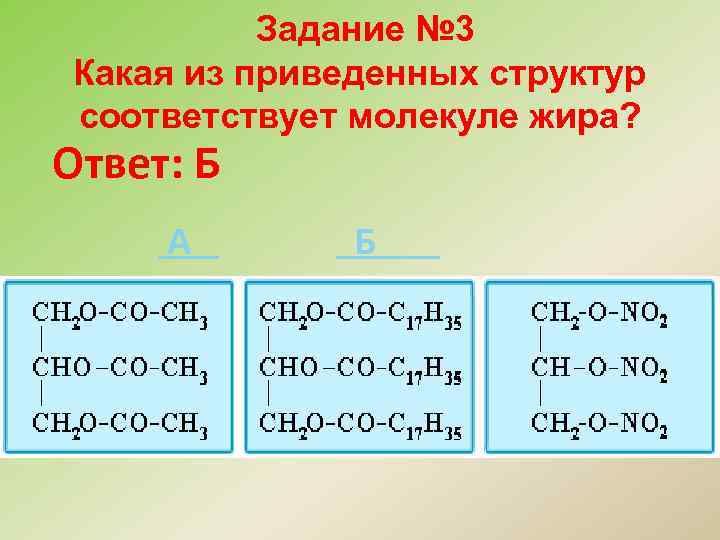 Задание № 3 Какая из приведенных структур соответствует молекуле жира? Ответ: Б А Б В
Задание № 3 Какая из приведенных структур соответствует молекуле жира? Ответ: Б А Б В
 Задание № 4 Какой из приведённых жиров жидкий?
Задание № 4 Какой из приведённых жиров жидкий?
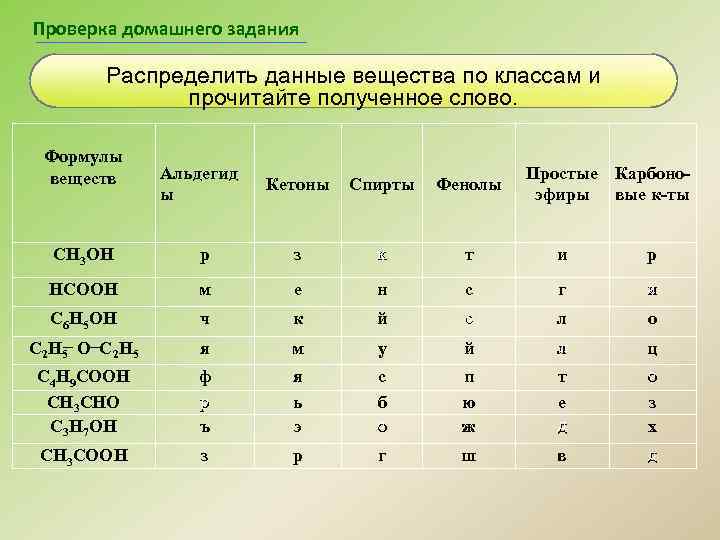 Проверка домашнего задания Распределить данные вещества по классам и прочитайте полученное слово. Формулы веществ Альдегид ы Кетоны Спирты Фенолы Простые Карбоноэфиры вые к-ты СН 3 ОН р з к т и р НСООН м е н с г и и С 6 Н 5 ОН ч к й с л о С 2 Н 5 О С 2 Н 5 я м у й л л ц С 4 Н 9 СООН СН 3 СНО С 3 Н 7 ОН ф р ъ я ь э с б о о п ю ж т е д о о з х СH 3 СООH з р г ш в д
Проверка домашнего задания Распределить данные вещества по классам и прочитайте полученное слово. Формулы веществ Альдегид ы Кетоны Спирты Фенолы Простые Карбоноэфиры вые к-ты СН 3 ОН р з к т и р НСООН м е н с г и и С 6 Н 5 ОН ч к й с л о С 2 Н 5 О С 2 Н 5 я м у й л л ц С 4 Н 9 СООН СН 3 СНО С 3 Н 7 ОН ф р ъ я ь э с б о о п ю ж т е д о о з х СH 3 СООH з р г ш в д
 Проверка домашнего задания Общая формула карбоновых кислот: R - COOH R - COH R - OH R – COOR 1
Проверка домашнего задания Общая формула карбоновых кислот: R - COOH R - COH R - OH R – COOR 1
 Проверка домашнего задания Дайте название кислоте CH 3 – CH 2 – COOH метановая бутановая этановая пропановая
Проверка домашнего задания Дайте название кислоте CH 3 – CH 2 – COOH метановая бутановая этановая пропановая
 Проверка домашнего задания С чем реагирует уксусная кислота CH 3 – COOH C 2 H 5 COOH CH 3 COH СH 3 OH CH 4
Проверка домашнего задания С чем реагирует уксусная кислота CH 3 – COOH C 2 H 5 COOH CH 3 COH СH 3 OH CH 4
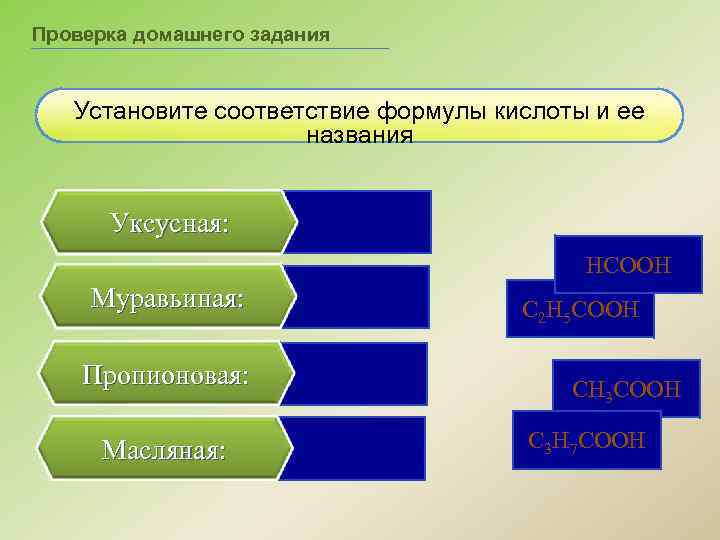 Проверка домашнего задания Установите соответствие формулы кислоты и ее названия Уксусная: HСOOH Муравьиная: Пропионовая: Масляная: C 2 H 5 COOH CH 3 COOH С 3 H 7 COOH
Проверка домашнего задания Установите соответствие формулы кислоты и ее названия Уксусная: HСOOH Муравьиная: Пропионовая: Масляная: C 2 H 5 COOH CH 3 COOH С 3 H 7 COOH
 Проверка домашнего задания Установите соответствие формулы кислоты и ее названия Уксусная: HСOOH Муравьиная: C 2 H 5 COOH Пропионовая: CH 3 COOH Масляная: С 3 H 7 COOH Для перемещения объекта щёлкните по нему левой кнопкой мыши, переместите объект, для фиксации объекта снова щёлкните левой кнопкой мыши.
Проверка домашнего задания Установите соответствие формулы кислоты и ее названия Уксусная: HСOOH Муравьиная: C 2 H 5 COOH Пропионовая: CH 3 COOH Масляная: С 3 H 7 COOH Для перемещения объекта щёлкните по нему левой кнопкой мыши, переместите объект, для фиксации объекта снова щёлкните левой кнопкой мыши.
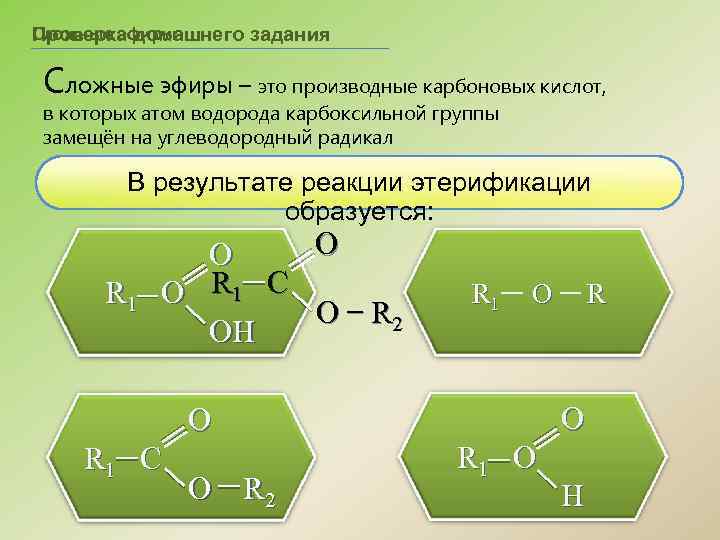 Сложные эфиры Проверка домашнего задания Сложные эфиры – это производные карбоновых кислот, в которых атом водорода карбоксильной группы замещён на углеводородный радикал В результате реакции этерификации образуется: R 1 O O O R 1 C O R 2 OH R 1 O O O R 1 C O R 2 R R 1 O H
Сложные эфиры Проверка домашнего задания Сложные эфиры – это производные карбоновых кислот, в которых атом водорода карбоксильной группы замещён на углеводородный радикал В результате реакции этерификации образуется: R 1 O O O R 1 C O R 2 OH R 1 O O O R 1 C O R 2 R R 1 O H
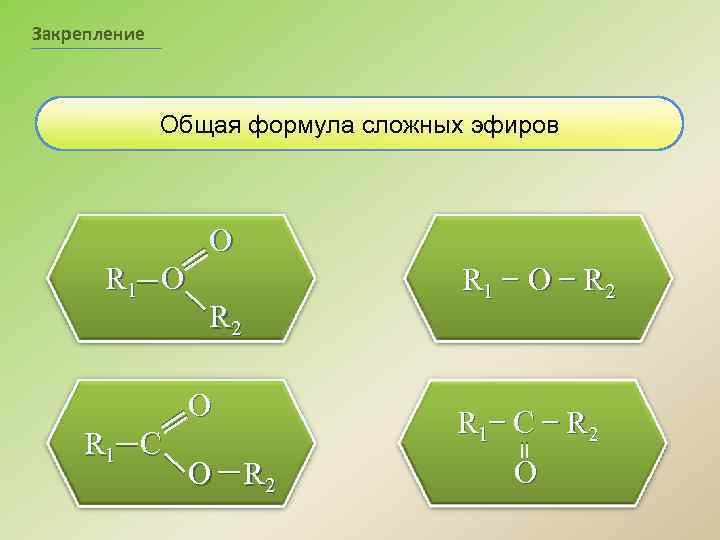 Закрепление Общая формула сложных эфиров O R 1 O R 2 O R 1 C ПРАВИЛЬНО! O R 2 R 1 O R 2 R 1 C R 2 O
Закрепление Общая формула сложных эфиров O R 1 O R 2 O R 1 C ПРАВИЛЬНО! O R 2 R 1 O R 2 R 1 C R 2 O
 Закрепление Реакция получения сложных эфиров называется Гидрирование Этерификация ПРАВИЛЬНО! Полимеризация Гидратация
Закрепление Реакция получения сложных эфиров называется Гидрирование Этерификация ПРАВИЛЬНО! Полимеризация Гидратация
 Закрепление Жиры это сложные эфиры… высших карбоновых кислот и одноатомных спиртов высших карбоновых кислот и многоатомных спиртов карбоновых кислот и глицерина высших карбоновых кислот и глицерина ПРАВИЛЬНО!
Закрепление Жиры это сложные эфиры… высших карбоновых кислот и одноатомных спиртов высших карбоновых кислот и многоатомных спиртов карбоновых кислот и глицерина высших карбоновых кислот и глицерина ПРАВИЛЬНО!
 Закрепление Какой жир является жидким? Свиной Рыбий ПРАВИЛЬНО! Куриный Говяжий
Закрепление Какой жир является жидким? Свиной Рыбий ПРАВИЛЬНО! Куриный Говяжий
 Закрепление Какое масло является твердым? Льняное Подсолнечное Пальмовое ПРАВИЛЬНО! Оливковое
Закрепление Какое масло является твердым? Льняное Подсолнечное Пальмовое ПРАВИЛЬНО! Оливковое
 Спасибо за внимание!
Спасибо за внимание!


