пептиды-2.ppt
- Количество слайдов: 37

Сложные белки Класс: Хромомпротеины 1. 1. Флавопротеины 1. 2. Магнийпорфирины 1. 3. Родопсины: А) зрительный родопсин Б) бактериородопсин 1. 4. Белки фотосистем А) белки реакционных центров фотосистем I и II Б) белки бактериальных реакционных центров 1. 5. Пептиды

Сложные белки – это двухкомпонентные белки, состоящие простого белка и небелкового компонента (простетической группы). Класс: Хромопротеины (от греч. chroma – краска) состоят из простого белка и, связанного с ним, окрашенного небелкового компонента. • гемопротеины (содержат в качестве простетической группы железо) • флавопротеины (содержат производные изоаллоксазина) • магнийпорфирины (содержат производные изоаллоксазина)
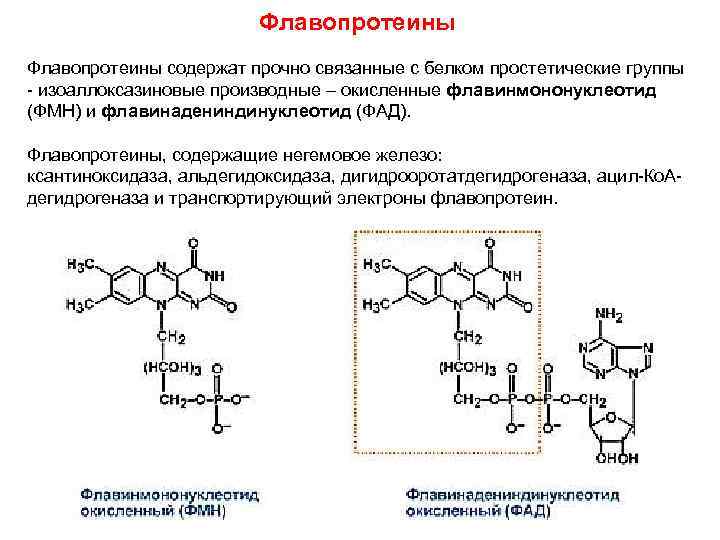
Флавопротеины содержат прочно связанные с белком простетические группы - изоаллоксазиновые производные – окисленные флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Флавопротеины, содержащие негемовое железо: ксантиноксидаза, альдегидоксидаза, дигидрооротатдегидрогеназа, ацил-Ко. Адегидрогеназа и транспортирующий электроны флавопротеин.
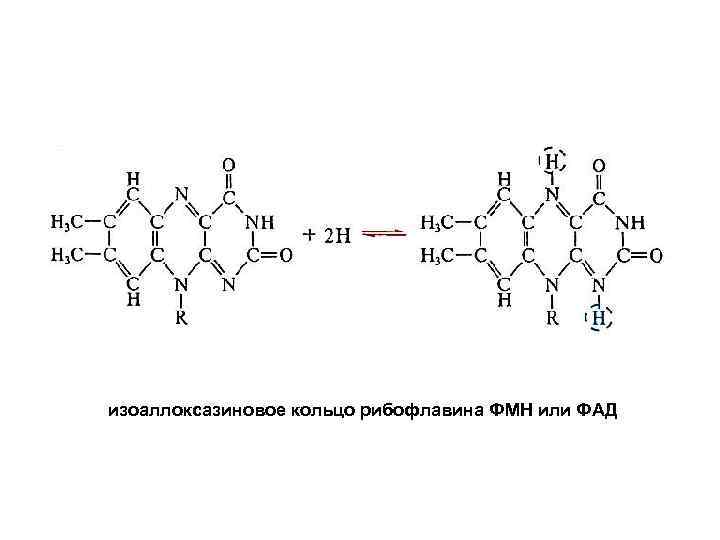
изоаллоксазиновое кольцо рибофлавина ФМН или ФАД
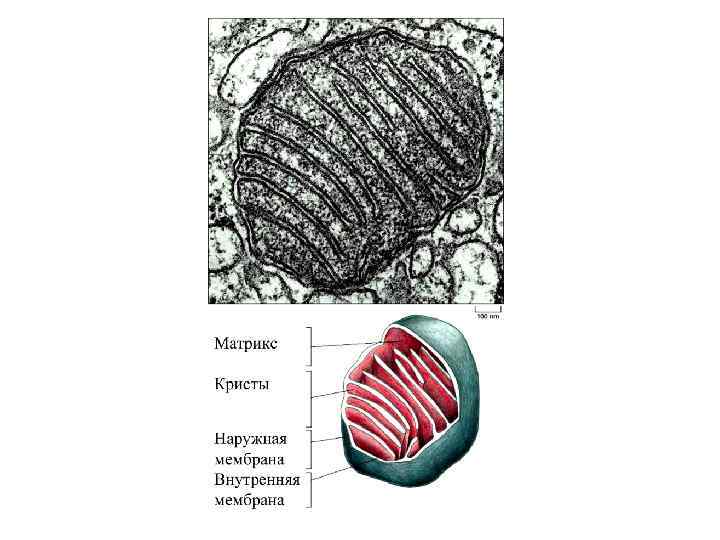
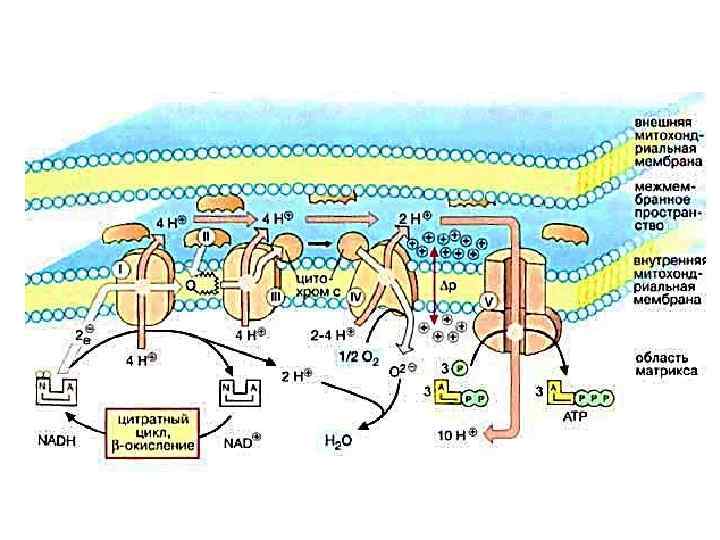
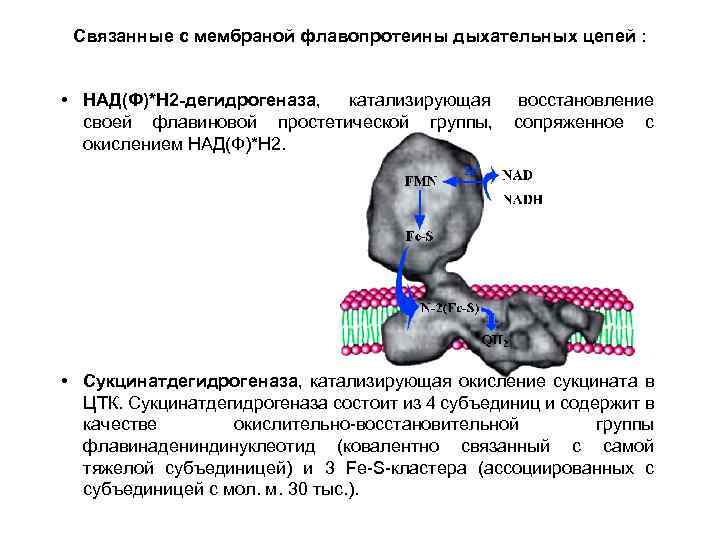
Связанные с мембраной флавопротеины дыхательных цепей : • НАД(Ф)*Н 2 -дегидрогеназа, катализирующая восстановление своей флавиновой простетической группы, сопряженное с окислением НАД(Ф)*Н 2. • Сукцинатдегидрогеназа, катализирующая окисление сукцината в ЦТК. Сукцинатдегидрогеназа состоит из 4 субъединиц и содержит в качестве окислительно-восстановительной группы флавинадениндинуклеотид (ковалентно связанный с самой тяжелой субъединицей) и 3 Fe-S-кластера (ассоциированных с субъединицей с мол. м. 30 тыс. ).
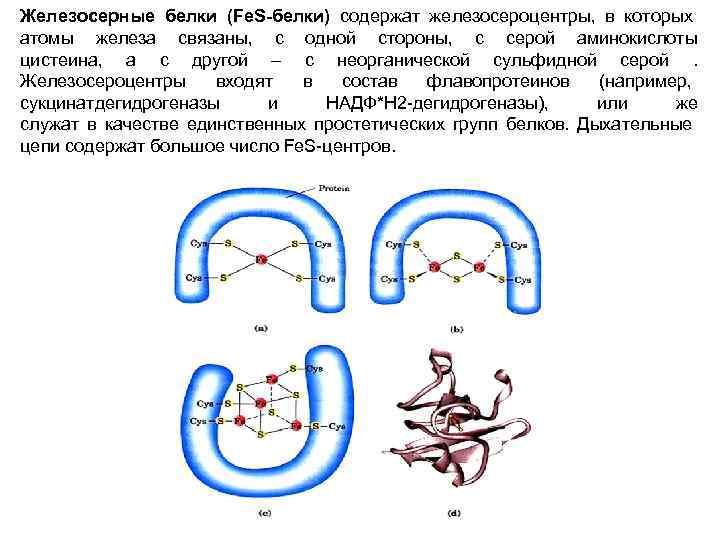
Железосерные белки (Fe. S-белки) содержат железосероцентры, в которых атомы железа связаны, с одной стороны, с серой аминокислоты цистеина, а с другой – с неорганической сульфидной серой . Железосероцентры входят в состав флавопротеинов (например, сукцинатдегидрогеназы и НАДФ*Н 2 -дегидрогеназы), или же служат в качестве единственных простетических групп белков. Дыхательные цепи содержат большое число Fe. S-центров.

Цитохромы (гемопротеины) — это маленькие глобулярные белки, которые содержат ковалентно связанный гем, расположенный во внутреннем кармане, образованном аминокислотными остатками. Известно около 30 видов цитохромов. Все они содержат гем в качестве простетической группы и различаются структурами боковых и полипептидных цепей. В зависимости от типа гема выделяют 8 классов цитохромов. В зависимости от спектров поглощения, цитохромы делят на группы a, b, c. Цитохром c
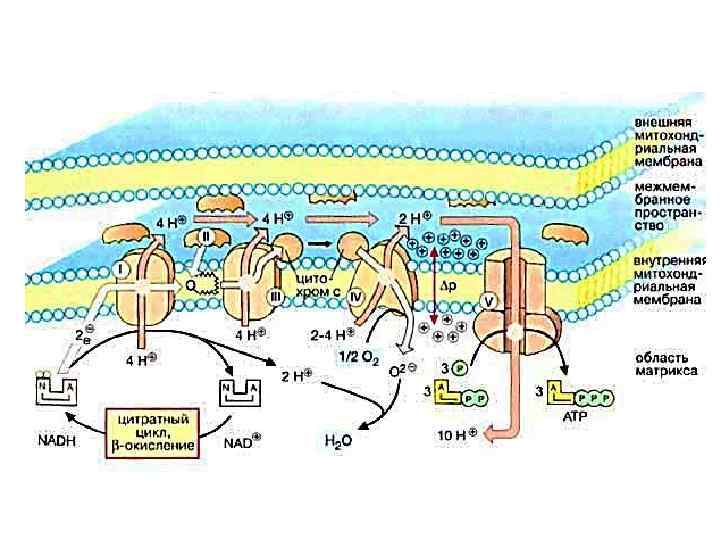

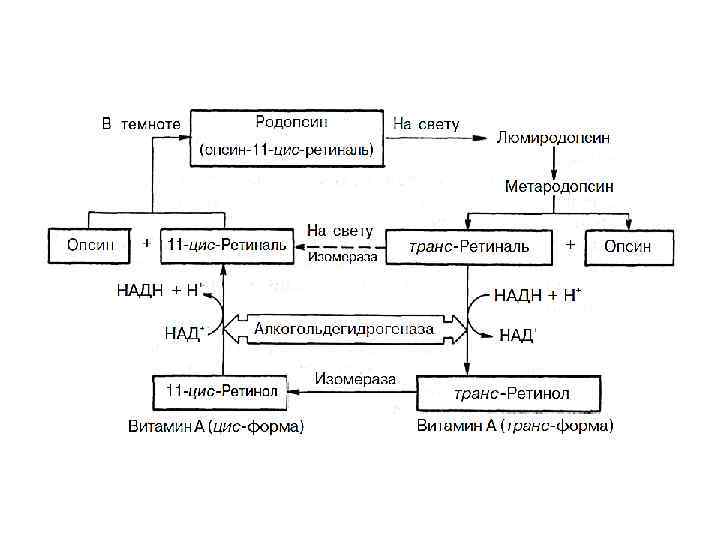
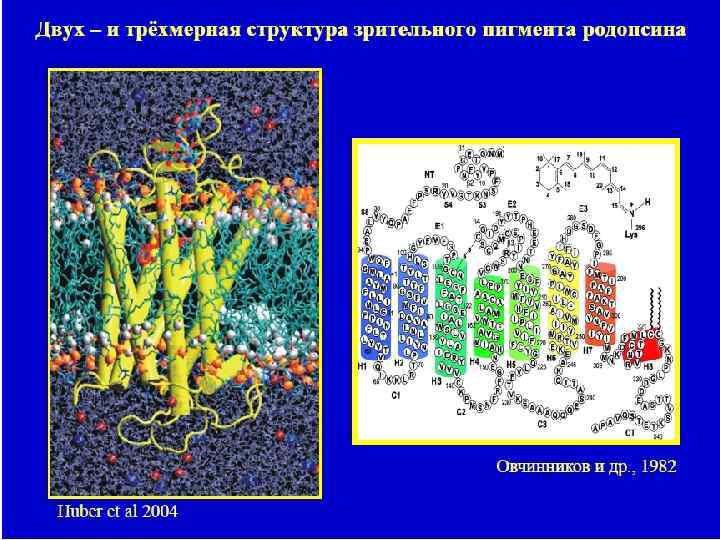
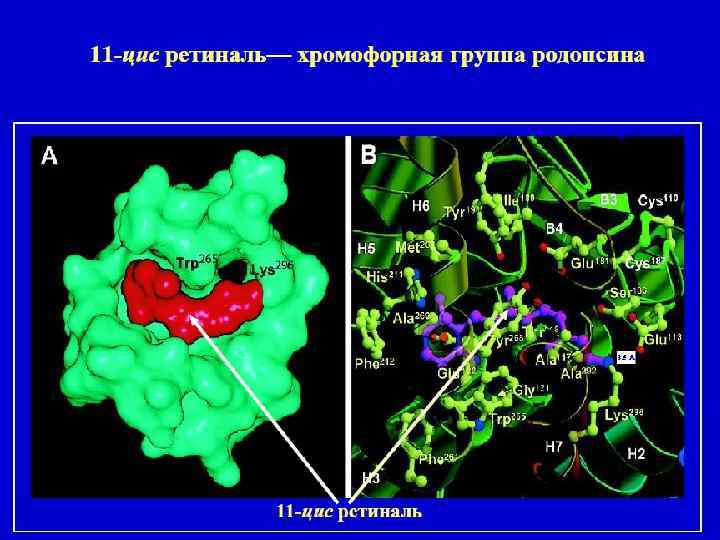
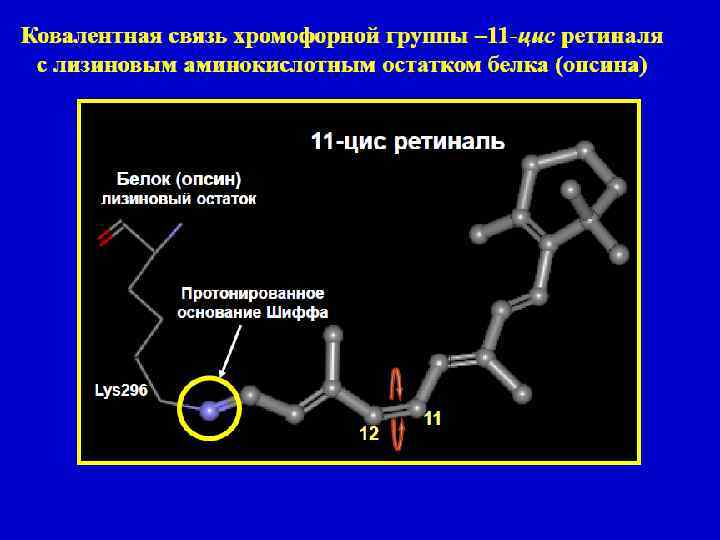
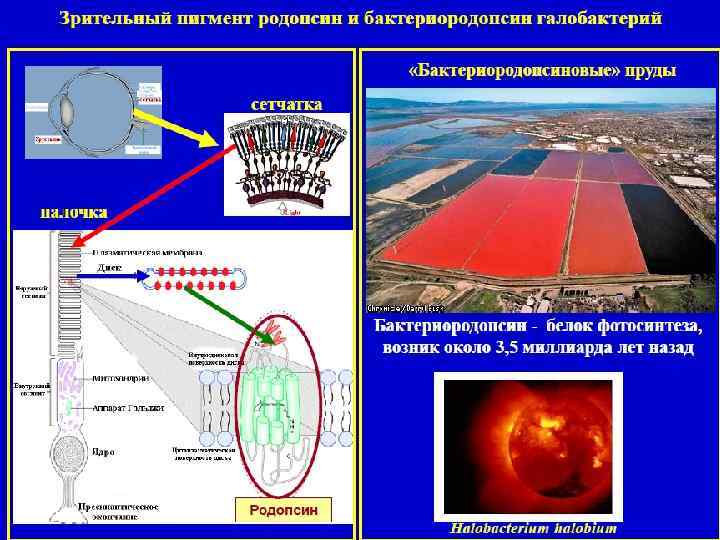
Родопсины 1. Зрительный родопсин 2. Бактериородопсин Зрительный родопсин Содержится в палочках сетчатки глаза морских беспозвоночных, рыб, почти всех наземных позвоночных и человека. Родопсин - основной светочувствительный пигмент сетчатки, в частности палочек. Родопсин состоит из липопротеина опсина и простетической группы, представленной альдегидом витамина A 1 (ретиналь).
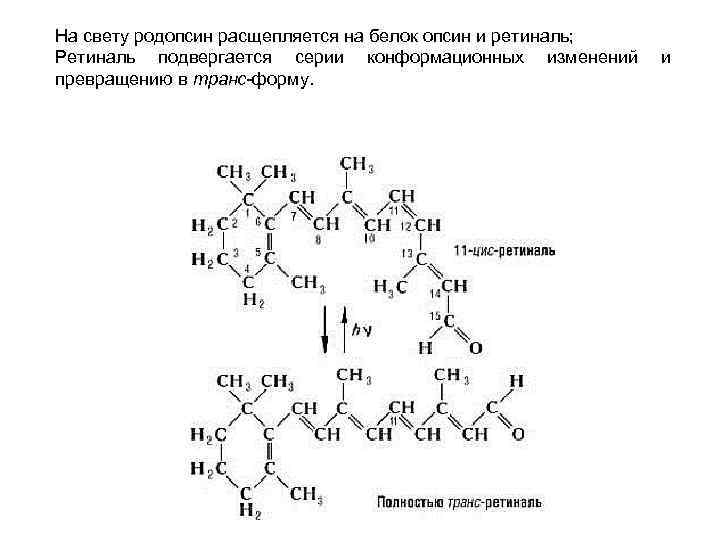
На свету родопсин расщепляется на белок опсин и ретиналь; Ретиналь подвергается серии конформационных изменений превращению в транс-форму. и
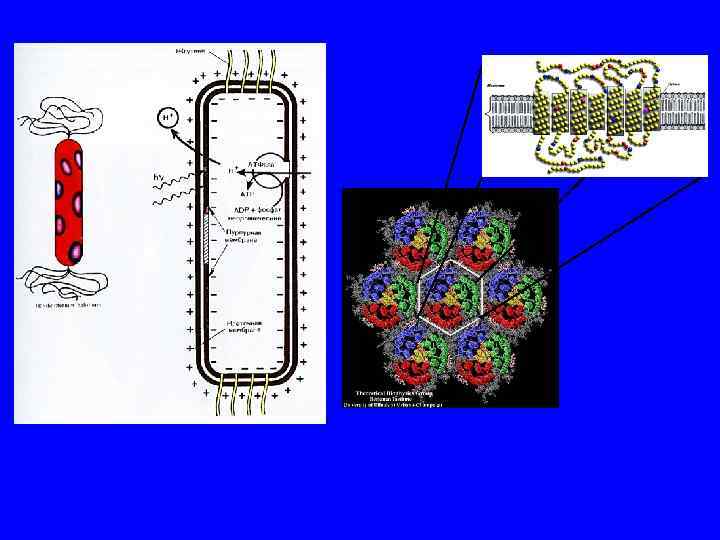
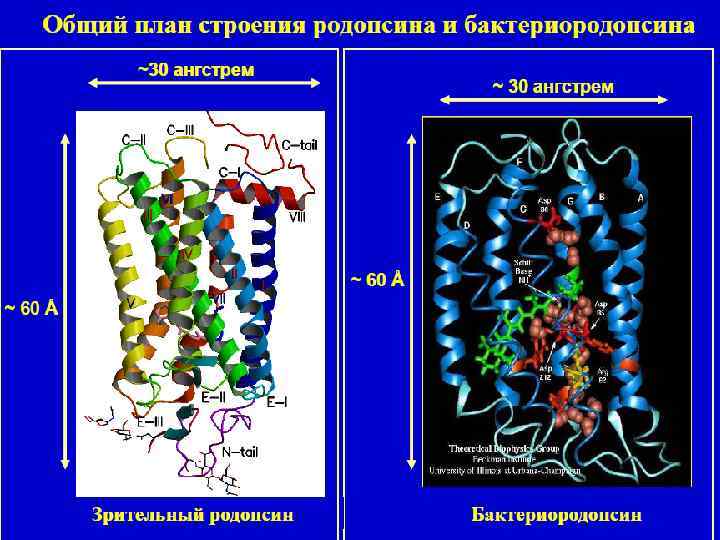

Бактериородопсин
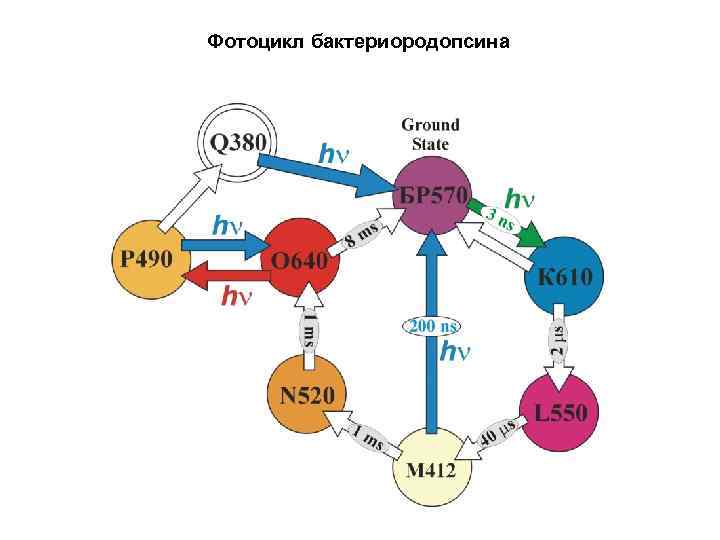
Фотоцикл бактериородопсина
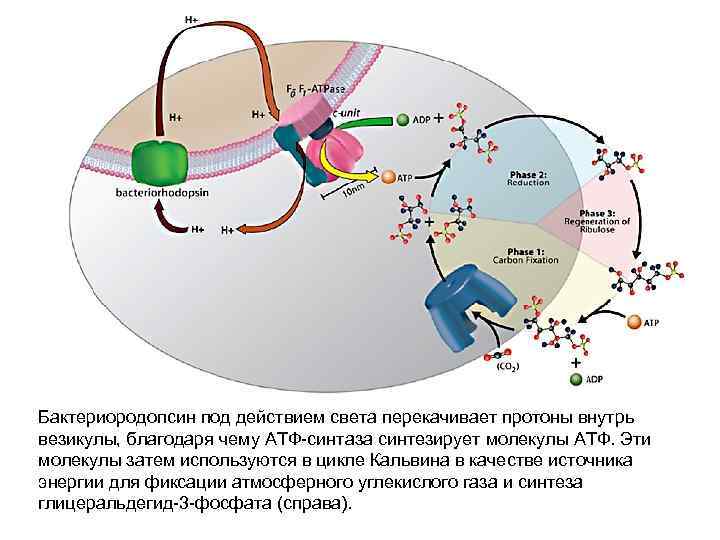
Бактериородопсин под действием света перекачивает протоны внутрь везикулы, благодаря чему АТФ-синтаза синтезирует молекулы АТФ. Эти молекулы затем используются в цикле Кальвина в качестве источника энергии для фиксации атмосферного углекислого газа и синтеза глицеральдегид-3 -фосфата (справа).

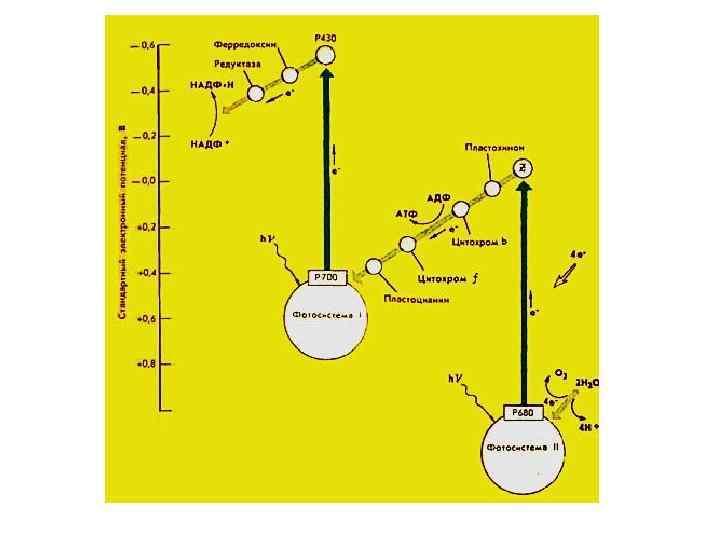
Белки реакционных центров фотосистем I и II растений Пигменты растений, участвующие в фотосинтезе, "упакованы" в тилакоиды хлоропластов в виде функциональных фотосинтетических единиц, называемых фотосистемами I и II. Каждая фотосистема содержит 250 -400 молекул пигментов. Все пигменты фотосистемы могут поглощать кванты света, но только одна молекула хлорофилла данной фотосистемы может использовать поглощенную энергию в фотохимических реакциях - реакционный центр фотосистемы, другие молекулы пигментов называются антенными, поскольку они улавливают энергию света. Белки, содержащие длинноволновые формы хлорофиллов (Р 680 в ФС II и Р 700 в ФС I) в количестве одна молекула на 200 — 400 молекул других хлорофиллов и способные к первичному фотохимическому разделению зарядов, называют реакционными центрами.
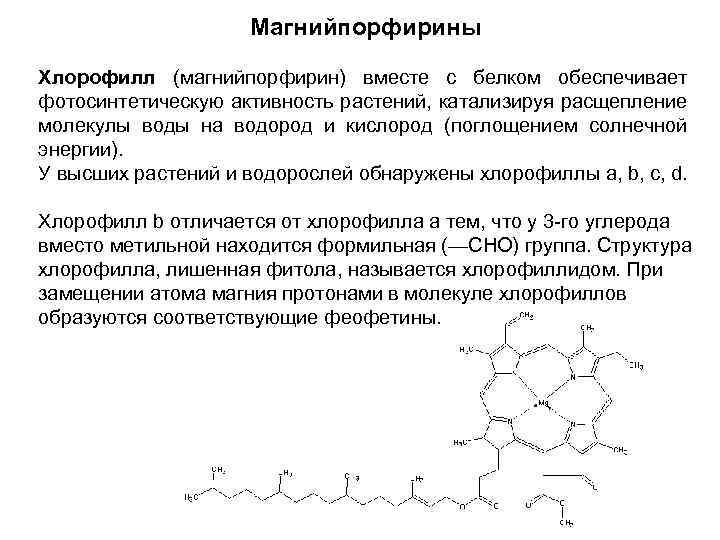
Магнийпорфирины Хлорофилл (магнийпорфирин) вместе с белком обеспечивает фотосинтетическую активность растений, катализируя расщепление молекулы воды на водород и кислород (поглощением солнечной энергии). У высших растений и водорослей обнаружены хлорофиллы а, b, с, d. Хлорофилл b отличается от хлорофилла а тем, что у 3 -го углерода вместо метильной находится формильная (—СНО) группа. Структура хлорофилла, лишенная фитола, называется хлорофиллидом. При замещении атома магния протонами в молекуле хлорофиллов образуются соответствующие феофетины.
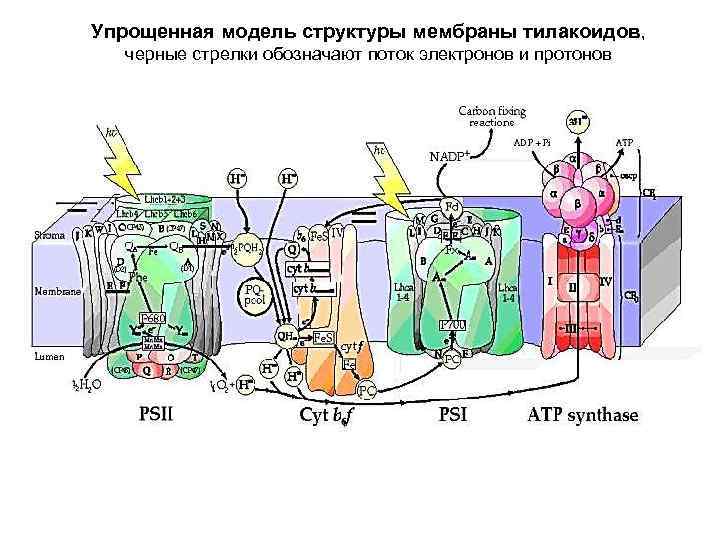
Упрощенная модель структуры мембраны тилакоидов, черные стрелки обозначают поток электронов и протонов

Фотосистема I В состав ФС I в качестве реакционного центра входит димер пигмента Р 700 (хлорофилл а с максимумом поглощения 700 нм), а также хлорофиллы а 675 -695, играющие роль антенного компонента фотосистемы I.
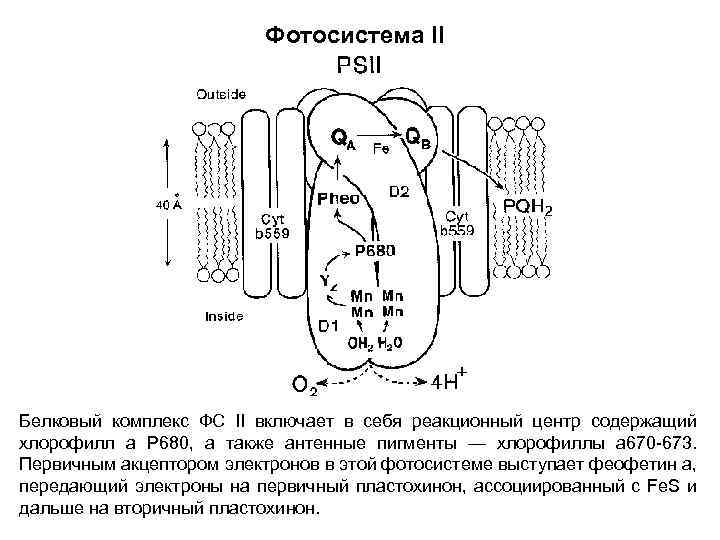
Фотосистема II Белковый комплекс ФС II включает в себя реакционный центр содержащий хлорофилл а Р 680, а также антенные пигменты — хлорофиллы a 670 -673. Первичным акцептором электронов в этой фотосистеме выступает феофетин а, передающий электроны на первичный пластохинон, ассоциированный с Fe. S и дальше на вторичный пластохинон.

Реакционные центры бактерий РЦ бактерий представляют собой интегральные мембранные белки, способные при поглощении кванта света осуществлять разделение и перенос зарядов (электронов) в фотосинтетических мембранах. Фотосинтез у бактерий осуществляется без разложения воды и выделения 02 (фоторедукция). В этом случае функцию доноров электронов для световой фазы фотосинтеза выполняют легко окисляемые соединения, такие, как H 2 S, Н 2, СН 4 и др. РЦ состоит из трех полипептидов, L, M и H, и десяти кофакторов – 4 -х молекул бактериохлорофилла a, 2 -х молекул бактериофеофитина a, 2 -х молекул убихинона, иона негемового железа Fe 2+ и молекулы каротиноида
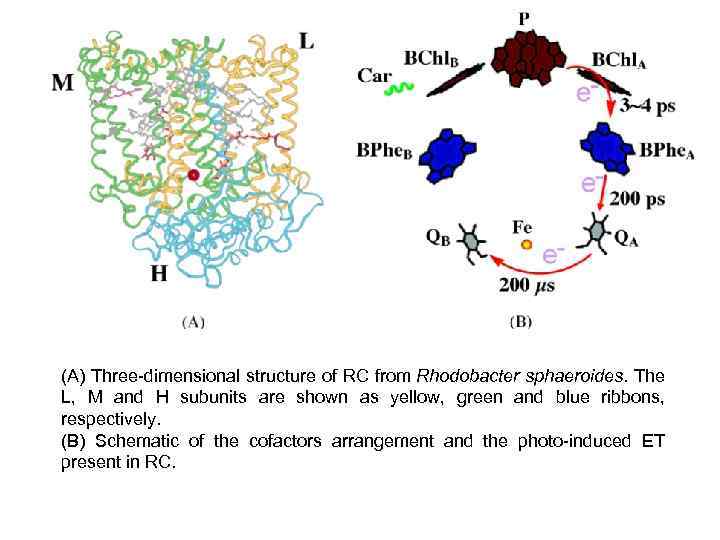
(A) Three-dimensional structure of RC from Rhodobacter sphaeroides. The L, M and H subunits are shown as yellow, green and blue ribbons, respectively. (B) Schematic of the cofactors arrangement and the photo-induced ET present in RC.
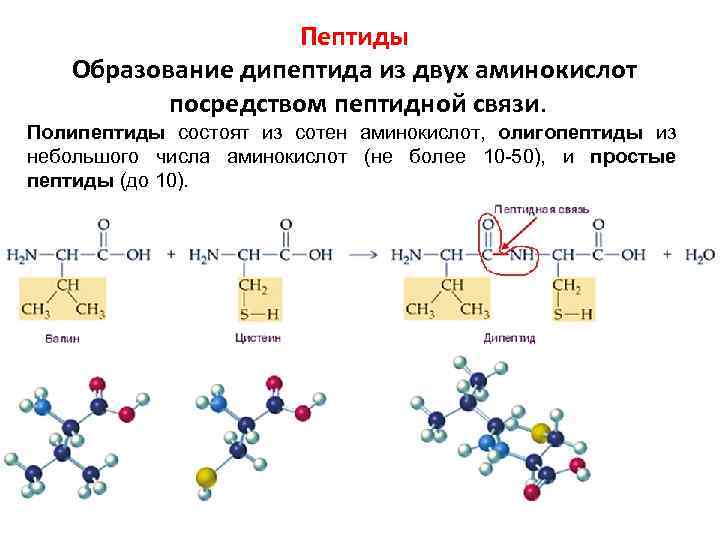
Пептиды Образование дипептида из двух аминокислот посредством пептидной связи. Полипептиды состоят из сотен аминокислот, олигопептиды из небольшого числа аминокислот (не более 10 -50), и простые пептиды (до 10).

Классификация пептидов: По количеству аминокислот в пептиде различают: • олигопептиды — молекулы, содержащие до десяти аминокислотных остатков; иногда в их названии упоминается количество входящих в их состав аминокислот, например, дипептид, трипептид, пентапептид и др. ; • полипептиды — молекулы, в состав которых входит более десяти аминокислот. По качественному составу различают: • гомомерные пептиды — соединения, состоящие только из аминокислотных остатков; • гетеромерные пептиды — вещества, в состав которых входят также небелковые компоненты. По способу связи аминокислот между собой: • гомодетные — пептиды, аминокислотные остатки которых соединены только пептидными связями; • гетеродетные пептиды — те соединения, в которых помимо пептидных связей встречаются ещё и дисульфидные, эфирные и тиоэфирные связи.
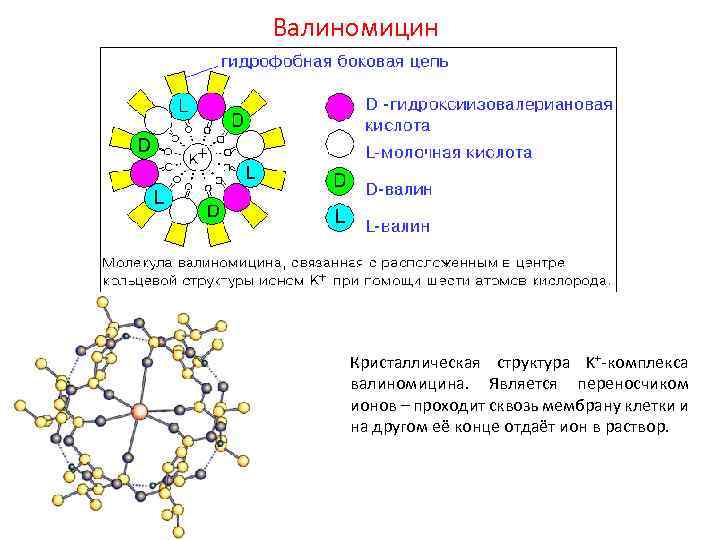
Валиномицин Кристаллическая структура K+-комплекса валиномицина. Является переносчиком ионов – проходит сквозь мембрану клетки и на другом её конце отдаёт ион в раствор.
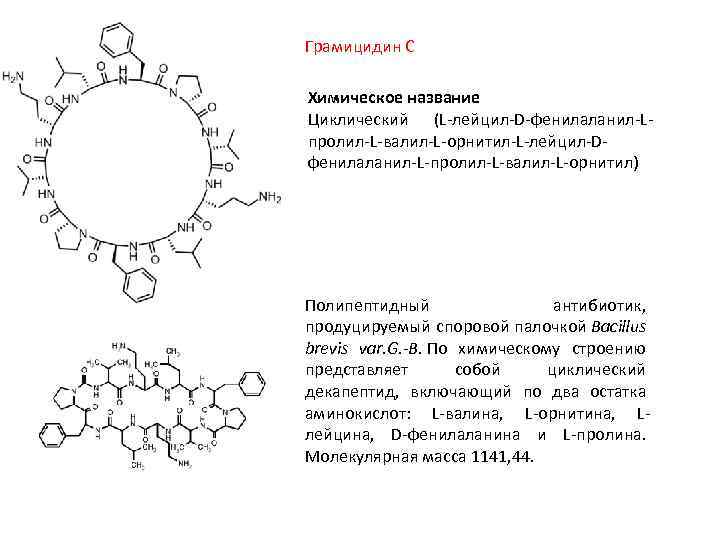
Грамицидин С Химическое название Циклический (L-лейцил-D-фенилаланил-Lпролил-L-валил-L-орнитил-L-лейцил-Dфенилаланил-L-пролил-L-валил-L-орнитил) Полипептидный антибиотик, продуцируемый споровой палочкой Bacillus brevis var. G. -B. По химическому строению представляет собой циклический декапептид, включающий по два остатка аминокислот: L-валина, L-орнитина, Lлейцина, D-фенилаланина и L-пролина. Молекулярная масса 1141, 44.

Мелитин пептид пчелиного яда — линейный пептид (26 аминокислот), обладающий свойствами поверхностно-активного вещества, выделенный из яда медоносной пчелы. Обнаружено несколько семейств цитотоксических пептидов, обладающих выраженным антибактериальным и цитотоксическим (гемолитическим) действием. При высоких концентрациях мелитин вызывает лизис мембран, а при сублитических — образует ионные каналы в липидном биослое клетки. Физикохимические свойства мелитина обусловливают его значительную антибактериальную активность против многих видов микроорганизмов, включая микоплазмы.
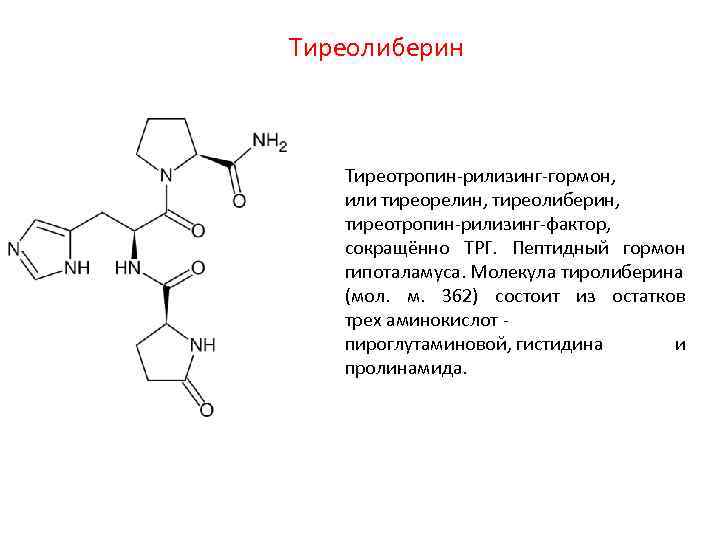
Тиреолиберин Тиреотропин-рилизинг-гормон, или тиреорелин, тиреолиберин, тиреотропин-рилизинг-фактор, сокращённо ТРГ. Пептидный гормон гипоталамуса. Молекула тиролиберина (мол. м. 362) состоит из остатков трех аминокислот пироглутаминовой, гистидина и пролинамида.
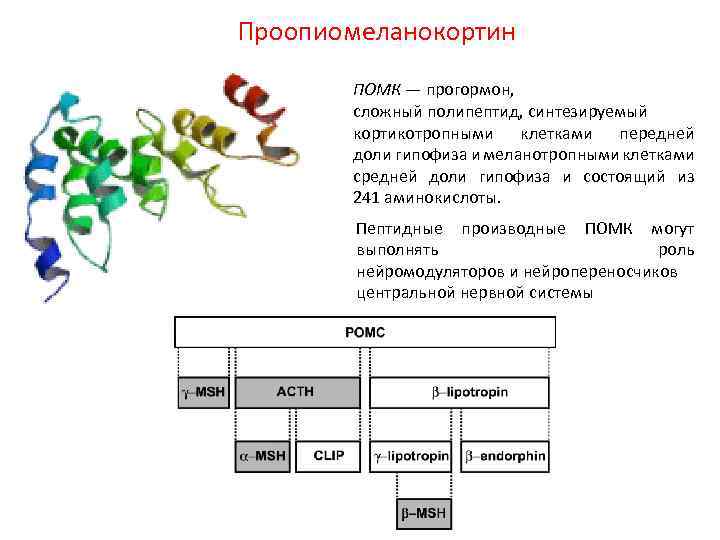
Проопиомеланокортин ПОМК — прогормон, сложный полипептид, синтезируемый кортикотропными клетками передней доли гипофиза и меланотропными клетками средней доли гипофиза и состоящий из 241 аминокислоты. Пептидные производные ПОМК могут выполнять роль нейромодуляторов и нейропереносчиков центральной нервной системы
пептиды-2.ppt