сложные белки.ppt
- Количество слайдов: 28

Сложные белки. Функционирование сложных белков на примере гемоглобина. Автор – доцент Рыскина Е. А.

Сложные белки • Сложные белки содержат два компонента – белковый и небелковый компонент. • Небелковый компонент называют простетической группой (от греч. prostheto – присоединяю). • Простетические группы могут быть связаны с белковой молекулой ковалентными и нековалентными связями. • Белковую часть называют – апобелок. • Апобелок + простетическая группа = холобелок
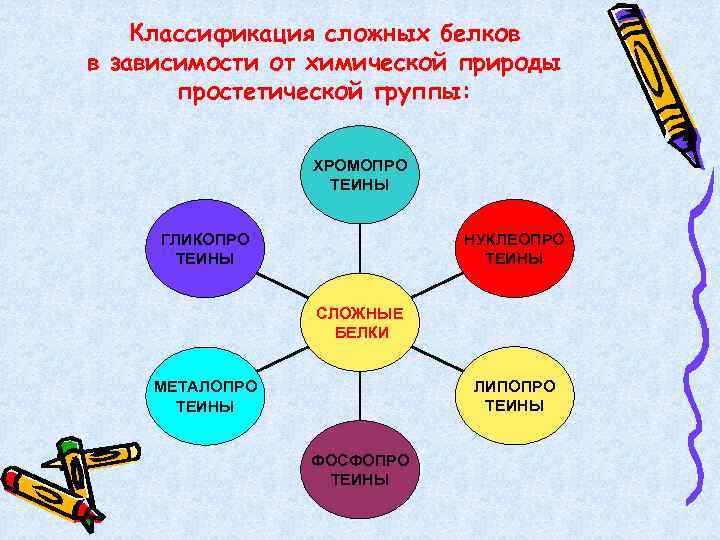
Классификация сложных белков в зависимости от химической природы простетической группы: ХРОМОПРО ТЕИНЫ НУКЛЕОПРО ТЕИНЫ ГЛИКОПРО ТЕИНЫ СЛОЖНЫЕ БЕЛКИ ЛИПОПРО ТЕИНЫ МЕТАЛОПРО ТЕИНЫ ФОСФОПРО ТЕИНЫ
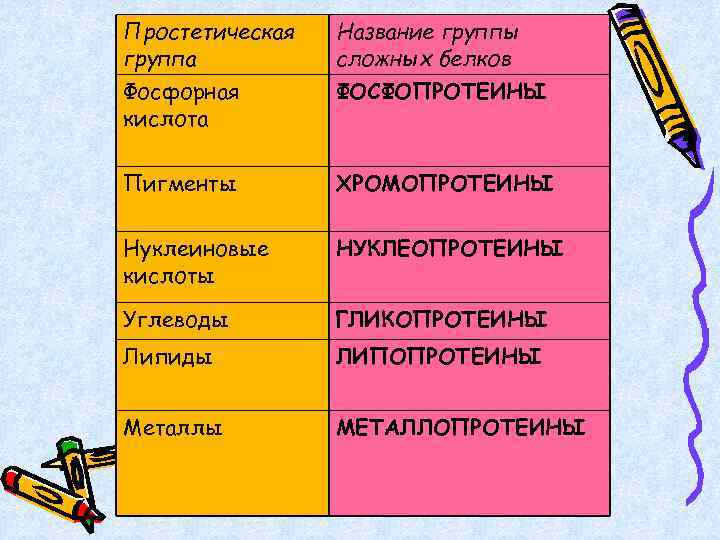
Простетическая группа Название группы сложных белков Фосфорная кислота ФОСФОПРОТЕИНЫ Пигменты ХРОМОПРОТЕИНЫ Нуклеиновые кислоты НУКЛЕОПРОТЕИНЫ Углеводы ГЛИКОПРОТЕИНЫ Липиды ЛИПОПРОТЕИНЫ Металлы МЕТАЛЛОПРОТЕИНЫ
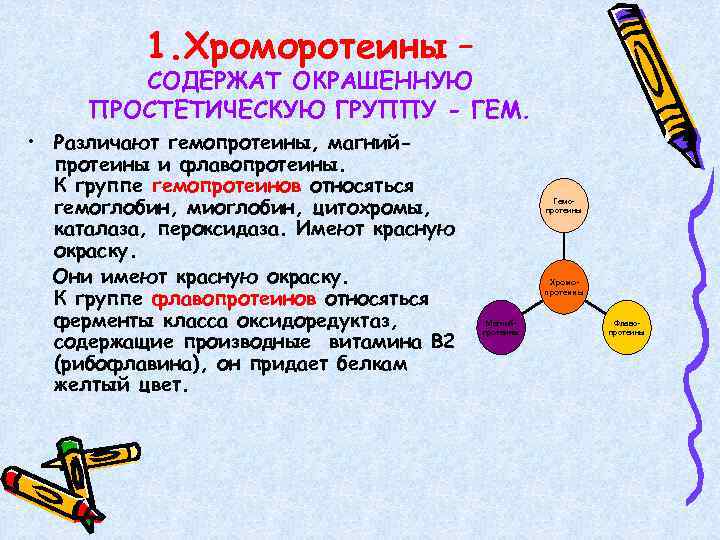
1. Хроморотеины – СОДЕРЖАТ ОКРАШЕННУЮ ПРОСТЕТИЧЕСКУЮ ГРУППУ - ГЕМ. • Различают гемопротеины, магнийпротеины и флавопротеины. К группе гемопротеинов относяться гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза. Имеют красную окраску. Они имеют красную окраску. К группе флавопротеинов относяться ферменты класса оксидоредуктаз, содержащие производные витамина B 2 (рибофлавина), он придает белкам желтый цвет. Гемопротеины Хромопротеины Магнийпротеины Флавопротеины

v 2. Нуклеопротеины. Простетическая группа у таких белков — нуклеиновая кислота. Различают дезоксирибонуклеопротеины (простетическая группа — ДНК) и рибонуклеопротеины (простетичесая группа — РНК). Им принадлежит важная роль в хранении, передаче и реализации генетической информации. Между белком и молекулой нуклеиновой кислоты образуются ионные связи. Известные нуклеопротеины – хроматин (с ДНК), рибосома (с РНК)

v 3. Липопротеины. Это белки, простетическая группа которых содержит липиды. Они обеспечивают транспорт липидов в крови, являются компонентами биологических мембран. Связи между белковой частью молекулы и липидом — гидрофобные или ионные. Липопротеины – это основные компоненты биологических мембран и транспортные белки крови.

v 4. Фосфопротеины. • Белки, которые содержат в своем составе фосфорную кислоту. Используются для регуляции процессов жизнедеятельности (фосфорилирование / дефосфорилирование). • Между белком и остатком фосфорной кислоты формируются сложноэфирные связи, в образовании которых участвует OH-группа серина, треонина и тирозина. • Вителлинин в желтке куриного яйца • Фосвитин • Овальбумин (в белке куриного яйца) • Ихтулин (в икре рыб)

v 5. Металлопротеины. Это белки, простетическая группа которых представлена металлами. Они транспортируют или участвуют в депонировании металлов (ферритин, трансферрин, церуллоплазмин). Между белком и простетической группой образуются координационные связи.

6. Гликопротеины и протеогликаны Это белки, простетическая группа которых содержит углеводы (глюкоза, глюкозамин и др. ) Углевод соединяется с белковой частью ковалентными связями. В соединении с углеводом участвует OH-группа аминокислоты серина или треонина. Этим белкам принадлежит важная роль в структурной организации клеток и тканей, они выполняют защитные функции. Основная часть внеклеточных белков — это гликопротеины.

Функционирование белков. • Свойство белка, обеспечивающим его функцию, является избирательное взаимодействие с определенном веществом – лигандом. • Лигандом – м. б. белки, низкомолекулярные вещества и др. соединения. • На белках есть участки к которым присоединяются лиганды – центры связывания или активные центры. • Активные центры формируются из аминокислотных остатков, сближенных в результате формирования третичной структуры.

Принцип комплиментарности • Под комплиментарностью понимают химическое и пространственное соответствие структуры активного центра белка структуре лиганда. • Высокая специфичность взаимодействия (узнавания) белка и лиганда обеспечивается комплиментарностью структуры активного центра и лигандом.

Гемоглобин человека • Известны следующие виды гемоглобина человека: • Нb А - (2α 2β), 98% от всего гемоглобина. • Нb А 2 - (2α 2δ), 2% от всего гемоглобина. • Нb Агл - (2α 2β), гликозилированный Hb. А, присоединяется глюкоза к Нb. А (при диабете) • Нb F - (2α 2γ), после рождения ребенка и замещается на Нв А.
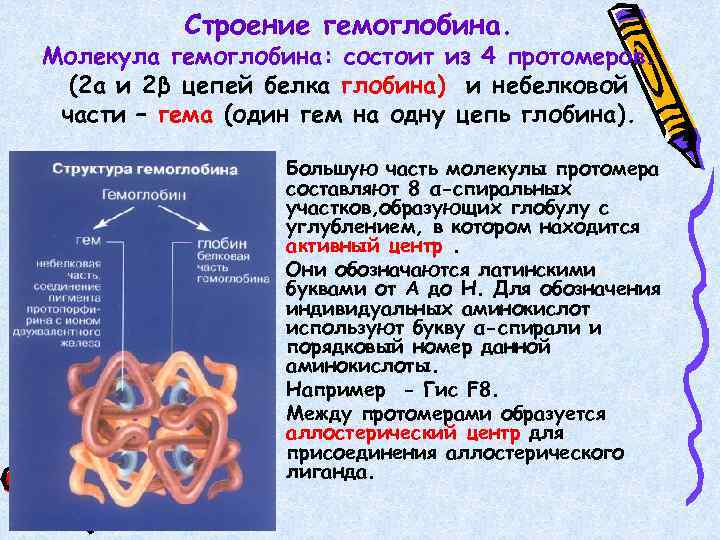
Строение гемоглобина. Молекула гемоглобина: состоит из 4 протомеров. (2 a и 2β цепей белка глобина) и небелковой части – гема (один гем на одну цепь глобина). • Большую часть молекулы протомера составляют 8 α-спиральных участков, образующих глобулу с углублением, в котором находится активный центр. • Они обозначаются латинскими буквами от А до Н. Для обозначения индивидуальных аминокислот используют букву α-спирали и порядковый номер данной аминокислоты. • Например - Гис F 8. • Между протомерами образуется аллостерический центр для присоединения аллостерического лиганда.

Функция гемоглобина • Основная функция Нb – перенос О 2 из легких в ткани и удалении СО 2 из тканей. • Атом железа гема способен присоединять и отдавать молекулу кислорода. При этом валентность железа не меняется, т. е. он остается двухвалентным. • В крови здоровых мужчин содержится в среднем 14, 5 г% гемоглобина (145 г/л). Эта величина может меняться в пределах от 13 до 16 (130 -160 г/л). • В крови здоровых женщин содержится в среднем 13 г гемоглобина (130 г/л). Может меняться в пределах от 12 до 14.
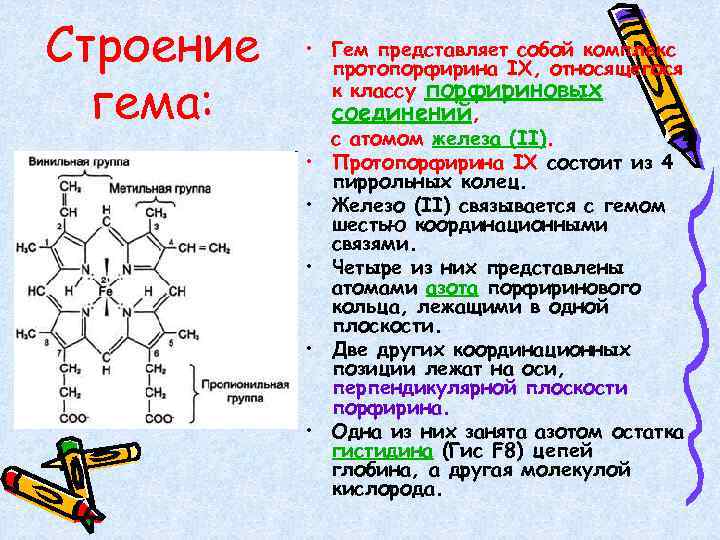
Строение гема: • Гем представляет собой комплекс протопорфирина IX, относящегося к классу порфириновых соединений, с атомом железа (II). • Протопорфирина IX состоит из 4 пиррольных колец. • Железо (II) связывается с гемом шестью координационными связями. • Четыре из них представлены атомами азота порфиринового кольца, лежащими в одной плоскости. • Две других координационных позиции лежат на оси, перпендикулярной плоскости порфирина. • Одна из них занята азотом остатка гистидина (Гис F 8) цепей глобина, а другая молекулой кислорода.

Связывание О 2 с железом (II) • Пиррольные кольца гема расположены в одной плоскости, а ион железа выступает над плоскостью. • При присоединении кислорода к первому гему, ион железа погружается в плоскость колец гема. • В результате сдвигается участок полипептидной цепи, нарушаются слабые связи в молекуле Нb и изменяется конформация всей цепи глобина (первый протомер).
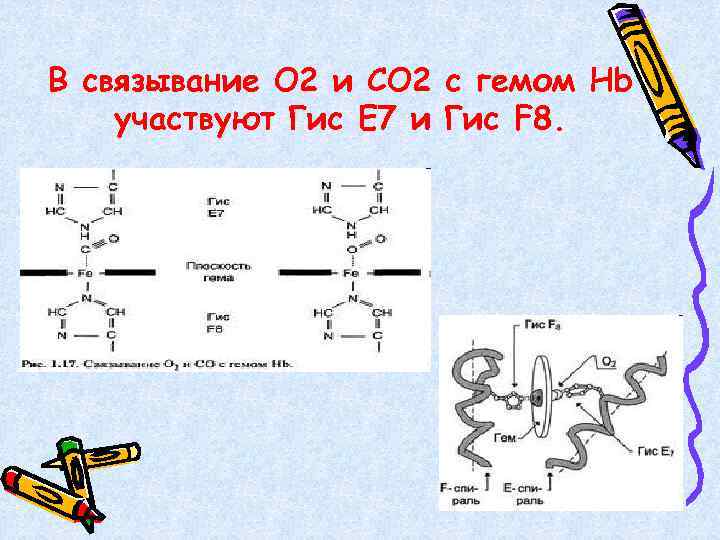
В связывание О 2 и СО 2 с гемом Hb участвуют Гис Е 7 и Гис F 8.

Кооперативные изменения конформации молекулы Нb при взаимодействии с кислородом. • Взаимодействие с 1 - протомером вызывает конформационные изменения всех протомеров и сродство к кислороду возрастает. • Присоединение кислорода к 2 – ому протомеру становиться легче, а 4 – ая молекула кислорода присоединяется в 300 раз легче. Подобные взаимосвязанные изменения структуры белка называются кооперативными конформационными изменениями. Таким образом, присоединение кислорода вызывает изменение пространственной структуры всей молекулы гемоглобина.

Кривая насыщения О 2 для гемоглобина • Гемоглобин имеет S-образную кривую насыщения, которая показывает, что протомеры белка работают кооперативно. Этот процесс зависит от парциального давления. • Hb присоединяет О 2 в легких при высоком парциальном давлении, где насыщение доходит до 100 %, и отдает в тканях О 2 в зависимости от парциального давления. • Гемоглобин доставляет в сутки 600 л О 2 в ткани и удаляет 500 л СО 2. • Движущей силой этих потоков является градиент концентрации О 2.
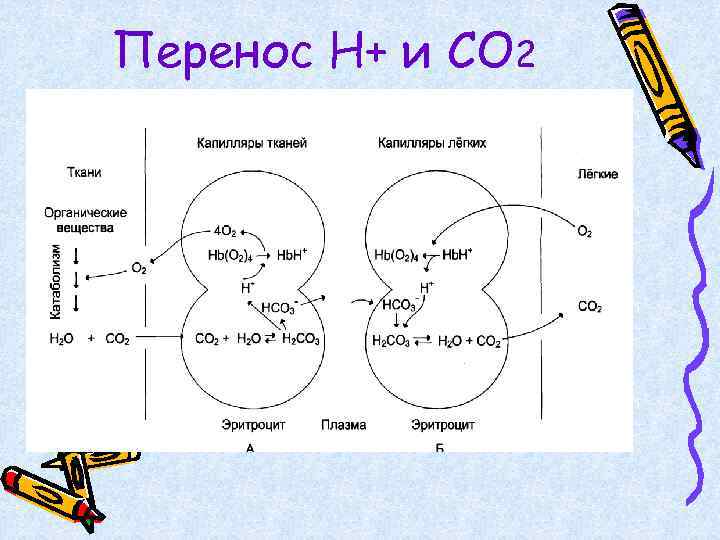
Перенос Н+ и СО 2

В регуляции работы Нb основная роль принадлежит протонам - Н+. • В мышцах: образуется много СО 2, который под действием карбоангидразы превращается в угольную кислоту, она диссоциирует до Н+ и НСО 3 - • СО 2 + Н 2 О = Н 2 СО 3 = Н+ + НСО 3 • Ионы Н протонируют Нb, что приводит к снижению его сродства к О 2. • Нb(О 2) + Н+ = Нb. Н+ + О 2 • Итого: Нb(О 2)4 - Нb(О 2)3 - Нb(О 2)2 - Нb(О 2) – Hb. H+

В легких поступает много кислорода и высокое парциальное давление приводит к оксигенированию гемоглобина и удалению протонов. Hb. H+ - Нb(О 2)2 - Нb(О 2)3 Нb(О 2)4 Освободившиеся протоны, соединяются с НСО 3 - с образованием угольной кислоты, которая диссоциирует на воду и углекислый газ. СО 2 удаляется с выдыхаемым воздухом. Н+ + НСО 3 - = Н 2 СО 3 = СО 2 + Н 2 О

Эффект Бора В легкие поступает кровь в высоким содержанием НB, протонированного Н+ или с БФГ. В такой форме Нb имеет низкое сродство к О 2. Из каппиляров диффундирует СО 2, это стимулирует депротенирование Нb. Высокое парциальное давление О 2 приводит к оксигенированию Нb, и при этом вытесняется БФГ. Зависимость сродства Нb к кислороду от концентрации ионов водорода получила название эффект Бора.

Аллостерическая регуляция • Изменение функциональной активности белка при взаимодействии с другими лигандами вследствии конформационных изменений называется аллостерической регуляцией. • Молекула гемоглобина способны свызываться с несколькими лигандами – О 2, Н+, СО 2, 2, 3 – бисфосфоглицерат (БФГ). • Н+, СО 2, БФГ – являются аллостерическими регуляторами активности Нb и присоединяются к участкам аллостерического центра. • Эти аллостерические регуляторы снижают сродство Нb к кислороду. • 2, 3 – бисфосфоглицерат (БФГ) образуется из глюкозы в эритроцитах. • Формула 2, 3 – бисфосфоглицерата:
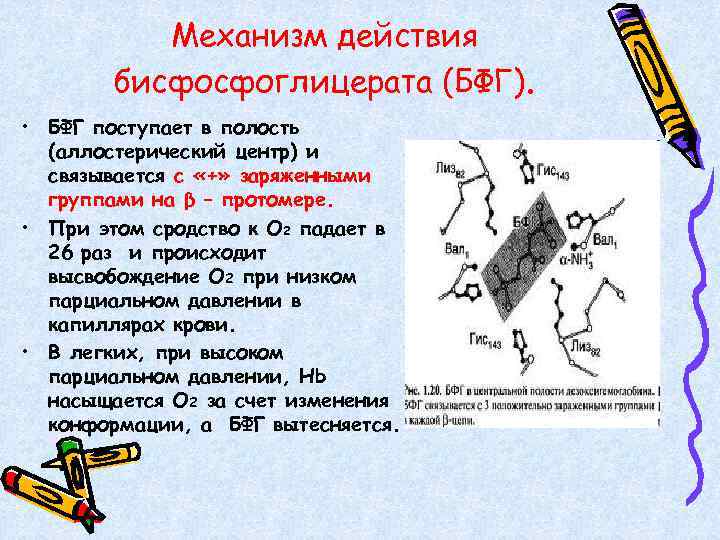
Механизм действия бисфосфоглицерата (БФГ). • БФГ поступает в полость (аллостерический центр) и связывается с «+» заряженными группами на β – протомере. • При этом сродство к О 2 падает в 26 раз и происходит высвобождение О 2 при низком парциальном давлении в капиллярах крови. • В легких, при высоком парциальном давлении, Нb насыщается О 2 за счет изменения конформации, а БФГ вытесняется.

Серповидноклеточная анемия – появление гидрофобного валина в 6 положении обеспечивает «склеивание молекул гемоглобина» и эритроциты принимают форму серпа.

Серповидноклеточные эритроциты
сложные белки.ppt