Катализ диффузия методы.ppt
- Количество слайдов: 12
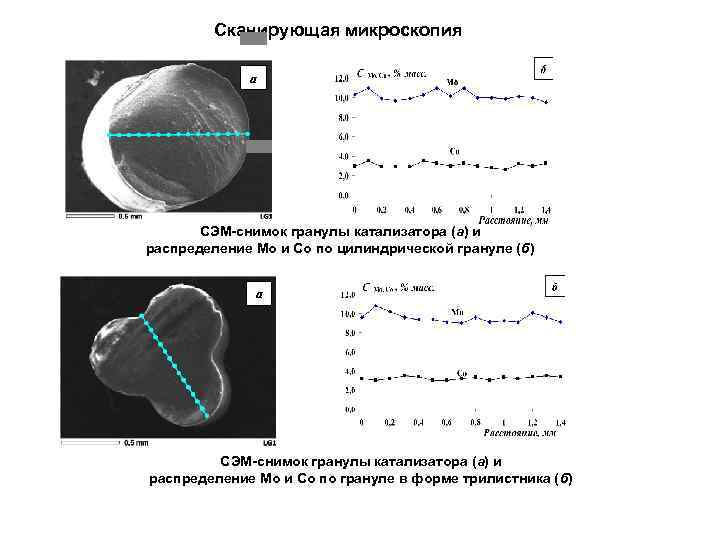 Сканирующая микроскопия a СЭМ-снимок гранулы катализатора (а) и распределение Мо и Со по цилиндрической грануле (б) a СЭМ-снимок гранулы катализатора (а) и распределение Мо и Со по грануле в форме трилистника (б)
Сканирующая микроскопия a СЭМ-снимок гранулы катализатора (а) и распределение Мо и Со по цилиндрической грануле (б) a СЭМ-снимок гранулы катализатора (а) и распределение Мо и Со по грануле в форме трилистника (б)
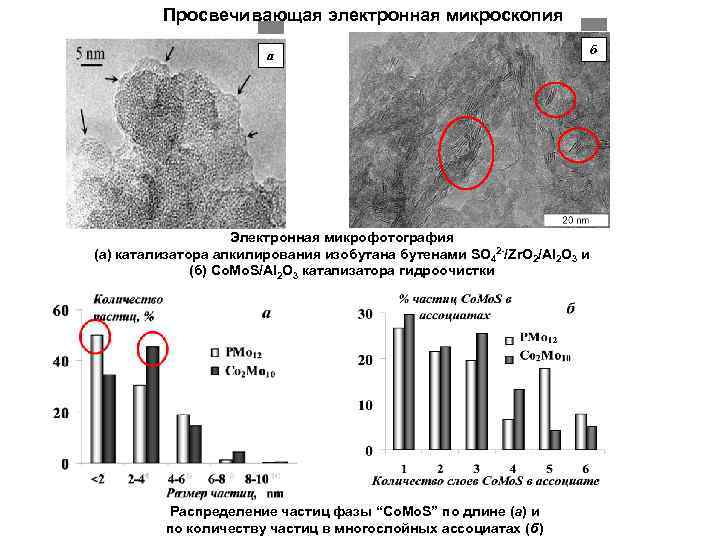 Просвечивающая электронная микроскопия a Электронная микрофотография (а) катализатора алкилирования изобутана бутенами SO 42 -/Zr. O 2/Al 2 O 3 и (б) Со. Mo. S/Al 2 O 3 катализатора гидроочистки Распределение частиц фазы “Co. Mo. S” по длине (а) и по количеству частиц в многослойных ассоциатах (б) б
Просвечивающая электронная микроскопия a Электронная микрофотография (а) катализатора алкилирования изобутана бутенами SO 42 -/Zr. O 2/Al 2 O 3 и (б) Со. Mo. S/Al 2 O 3 катализатора гидроочистки Распределение частиц фазы “Co. Mo. S” по длине (а) и по количеству частиц в многослойных ассоциатах (б) б
 Сканирующая туннельная микроскопия a б STM – изображения кластеров Mo. S 2, нанесенных на подложку Au а – 404 х409 Ǻ 2; б – 67 х69 Ǻ 2 Схема работы сканирующего туннельного микроскопа Слева - консоль; справа - острие иглы
Сканирующая туннельная микроскопия a б STM – изображения кластеров Mo. S 2, нанесенных на подложку Au а – 404 х409 Ǻ 2; б – 67 х69 Ǻ 2 Схема работы сканирующего туннельного микроскопа Слева - консоль; справа - острие иглы
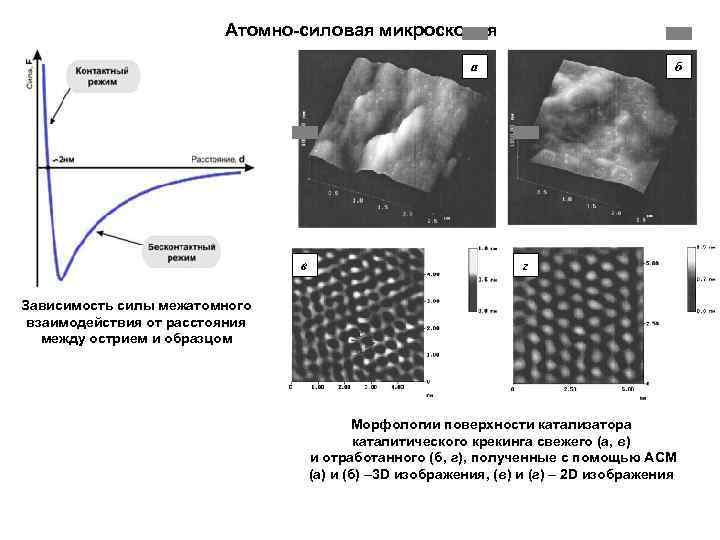 Атомно-силовая микроскопия a в б г Зависимость силы межатомного взаимодействия от расстояния между острием и образцом Морфологии поверхности катализатора каталитического крекинга свежего (а, в) и отработанного (б, г), полученные с помощью АСМ (а) и (б) – 3 D изображения, (в) и (г) – 2 D изображения
Атомно-силовая микроскопия a в б г Зависимость силы межатомного взаимодействия от расстояния между острием и образцом Морфологии поверхности катализатора каталитического крекинга свежего (а, в) и отработанного (б, г), полученные с помощью АСМ (а) и (б) – 3 D изображения, (в) и (г) – 2 D изображения
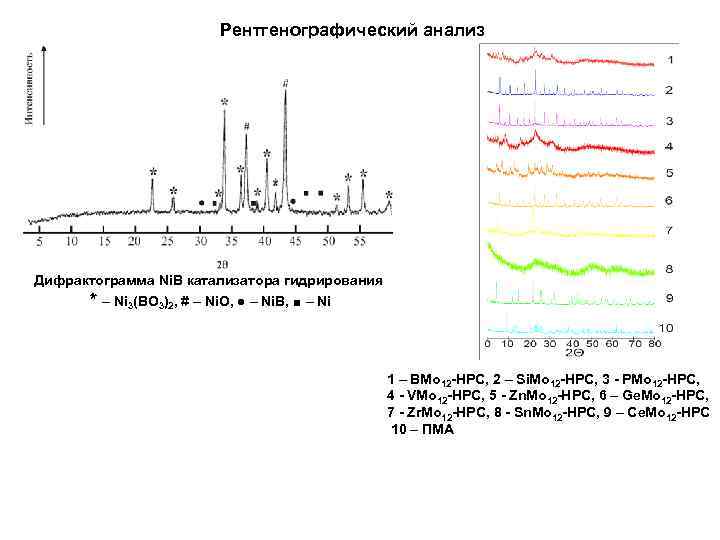 Рентгенографический анализ Дифрактограмма Ni. B катализатора гидрирования * – Ni 3(BO 3)2, # – Ni. O, ● – Ni. B, ■ – Ni 1 – BMo 12 -HPC, 2 – Si. Mo 12 -HPC, 3 - PMo 12 -HPC, 4 - VMo 12 -HPC, 5 - Zn. Mo 12 -HPC, 6 – Ge. Mo 12 -HPC, 7 - Zr. Mo 12 -HPC, 8 - Sn. Mo 12 -HPC, 9 – Ce. Mo 12 -HPC 10 – ПМА
Рентгенографический анализ Дифрактограмма Ni. B катализатора гидрирования * – Ni 3(BO 3)2, # – Ni. O, ● – Ni. B, ■ – Ni 1 – BMo 12 -HPC, 2 – Si. Mo 12 -HPC, 3 - PMo 12 -HPC, 4 - VMo 12 -HPC, 5 - Zn. Mo 12 -HPC, 6 – Ge. Mo 12 -HPC, 7 - Zr. Mo 12 -HPC, 8 - Sn. Mo 12 -HPC, 9 – Ce. Mo 12 -HPC 10 – ПМА
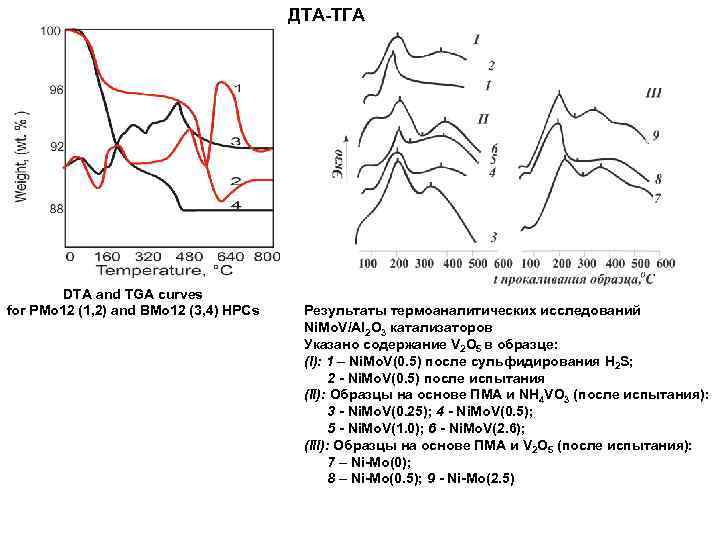 ДТА-ТГА DTA and TGA curves for PMo 12 (1, 2) and BMo 12 (3, 4) HPCs Результаты термоаналитических исследований Ni. Mo. V/Al 2 O 3 катализаторов Указано содержание V 2 O 5 в образце: (I): 1 – Ni. Mo. V(0. 5) после сульфидирования H 2 S; 2 - Ni. Mo. V(0. 5) после испытания (II): Образцы на основе ПМА и NH 4 VO 3 (после испытания): 3 - Ni. Mo. V(0. 25); 4 - Ni. Mo. V(0. 5); 5 - Ni. Mo. V(1. 0); 6 - Ni. Mo. V(2. 6); (III): Образцы на основе ПМА и V 2 O 5 (после испытания): 7 – Ni-Mo(0); 8 – Ni-Mo(0. 5); 9 - Ni-Mo(2. 5)
ДТА-ТГА DTA and TGA curves for PMo 12 (1, 2) and BMo 12 (3, 4) HPCs Результаты термоаналитических исследований Ni. Mo. V/Al 2 O 3 катализаторов Указано содержание V 2 O 5 в образце: (I): 1 – Ni. Mo. V(0. 5) после сульфидирования H 2 S; 2 - Ni. Mo. V(0. 5) после испытания (II): Образцы на основе ПМА и NH 4 VO 3 (после испытания): 3 - Ni. Mo. V(0. 25); 4 - Ni. Mo. V(0. 5); 5 - Ni. Mo. V(1. 0); 6 - Ni. Mo. V(2. 6); (III): Образцы на основе ПМА и V 2 O 5 (после испытания): 7 – Ni-Mo(0); 8 – Ni-Mo(0. 5); 9 - Ni-Mo(2. 5)
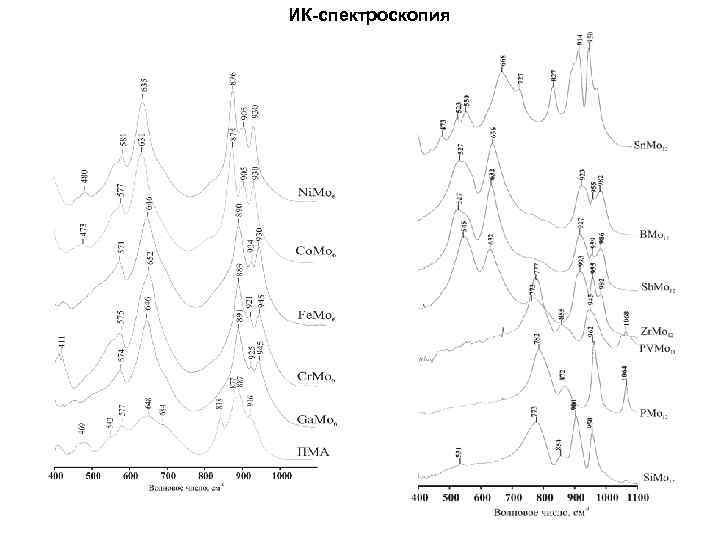 ИК-спектроскопия
ИК-спектроскопия
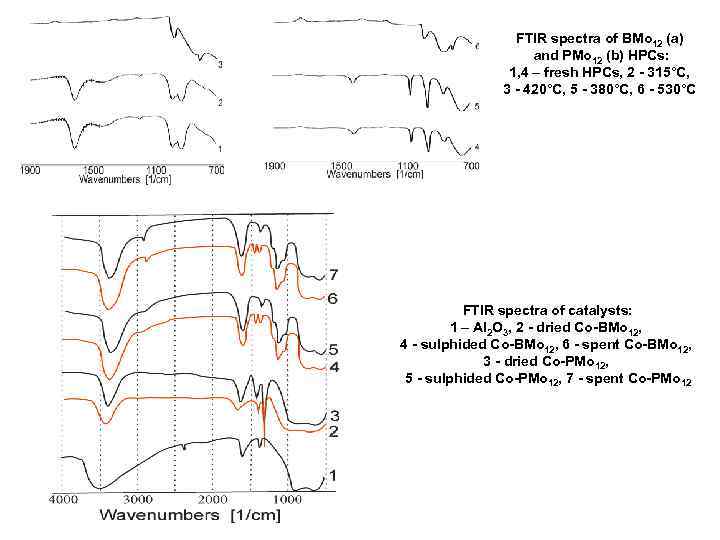 FTIR spectra of BMo 12 (a) and PMo 12 (b) HPCs: 1, 4 – fresh HPCs, 2 - 315°C, 3 - 420°C, 5 - 380°C, 6 - 530°C FTIR spectra of catalysts: 1 – Al 2 O 3, 2 - dried Co-BMo 12, 4 - sulphided Co-BMo 12, 6 - spent Co-BMo 12, 3 - dried Co-PMo 12, 5 - sulphided Co-PMo 12, 7 - spent Co-PMo 12
FTIR spectra of BMo 12 (a) and PMo 12 (b) HPCs: 1, 4 – fresh HPCs, 2 - 315°C, 3 - 420°C, 5 - 380°C, 6 - 530°C FTIR spectra of catalysts: 1 – Al 2 O 3, 2 - dried Co-BMo 12, 4 - sulphided Co-BMo 12, 6 - spent Co-BMo 12, 3 - dried Co-PMo 12, 5 - sulphided Co-PMo 12, 7 - spent Co-PMo 12
 Диффузия и катализ Гетерогенно-каталитический процесс - ряд последовательных стадий: - диффузия к внешней поверхности катализатора; - диффузия к внутренней поверхности катализатора (внутри пор); - адсорбция реагентов; - реакция на поверхности; - десорбция продуктов реакции; - диффузия внутри пор к поверхности зерна катализатора; - диффузия в газе (жидкости), окружающем катализатор. Любая из этих стадий может оказаться самой медленной (лимитирующей) и, таким образом, определяющей скорость гетерогенно-каталитического процесса. Общая скорость реакции не может быть больше скорости самой медленной из этих стадий.
Диффузия и катализ Гетерогенно-каталитический процесс - ряд последовательных стадий: - диффузия к внешней поверхности катализатора; - диффузия к внутренней поверхности катализатора (внутри пор); - адсорбция реагентов; - реакция на поверхности; - десорбция продуктов реакции; - диффузия внутри пор к поверхности зерна катализатора; - диффузия в газе (жидкости), окружающем катализатор. Любая из этих стадий может оказаться самой медленной (лимитирующей) и, таким образом, определяющей скорость гетерогенно-каталитического процесса. Общая скорость реакции не может быть больше скорости самой медленной из этих стадий.
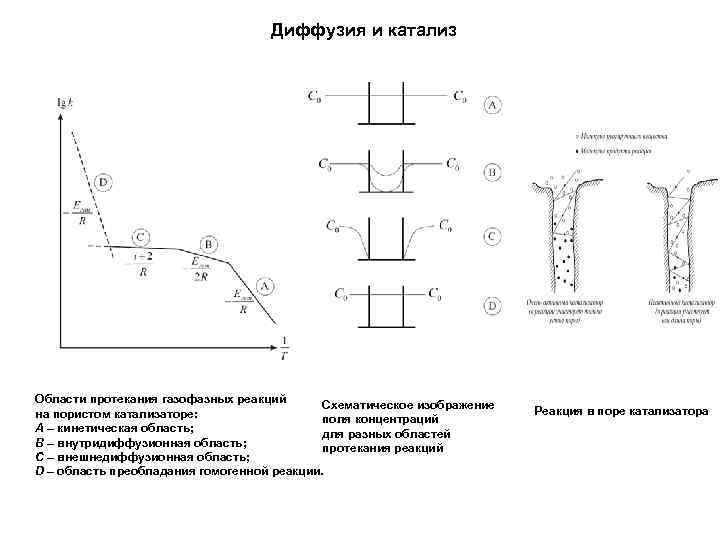 Диффузия и катализ Области протекания газофазных реакций Схематическое изображение на пористом катализаторе: поля концентраций А – кинетическая область; для разных областей B – внутридиффузионная область; протекания реакций С – внешнедиффузионная область; D – область преобладания гомогенной реакции. Реакция в поре катализатора
Диффузия и катализ Области протекания газофазных реакций Схематическое изображение на пористом катализаторе: поля концентраций А – кинетическая область; для разных областей B – внутридиффузионная область; протекания реакций С – внешнедиффузионная область; D – область преобладания гомогенной реакции. Реакция в поре катализатора
 Критерии внешнедиффузионной области: 1. Увеличение линейной скорости потока повышает скорость процесса. 2. Малый температурный коэффициент скорости реакции. Скорость процесса в этой области слабо зависит от температуры. 3. Наблюдаемый первый порядок реакции. 4. Пропорциональность наблюдаемой скорости реакции размеру внешней поверхности зерен. Скорость процесса возрастает при уменьшении размера гранул. 5. Наличие значительного перепада температур между катализатором и реакционной смесью. 6. До некоторого предела изменение активности катализатора не влияет на скорость реакции. Критерии внутренне-диффузионной области: 1. 2. 3. Влияние изменений размеров гранул катализатора на скорость процесса. Если скорости реакции, измеренные на зернах разной величины, одинаковы, то внутреннедиффузионного торможения нет. Зависимость скорости реакции от радиуса пор. Пропорциональность скорости реакции количеству активных компонентов катализатора свидетельствует об отсутствии диффузионного торможения.
Критерии внешнедиффузионной области: 1. Увеличение линейной скорости потока повышает скорость процесса. 2. Малый температурный коэффициент скорости реакции. Скорость процесса в этой области слабо зависит от температуры. 3. Наблюдаемый первый порядок реакции. 4. Пропорциональность наблюдаемой скорости реакции размеру внешней поверхности зерен. Скорость процесса возрастает при уменьшении размера гранул. 5. Наличие значительного перепада температур между катализатором и реакционной смесью. 6. До некоторого предела изменение активности катализатора не влияет на скорость реакции. Критерии внутренне-диффузионной области: 1. 2. 3. Влияние изменений размеров гранул катализатора на скорость процесса. Если скорости реакции, измеренные на зернах разной величины, одинаковы, то внутреннедиффузионного торможения нет. Зависимость скорости реакции от радиуса пор. Пропорциональность скорости реакции количеству активных компонентов катализатора свидетельствует об отсутствии диффузионного торможения.
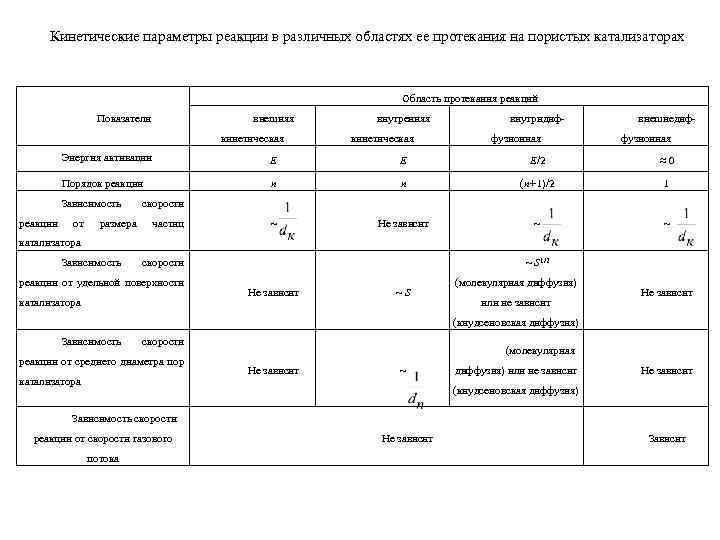 Кинетические параметры реакции в различных областях ее протекания на пористых катализаторах Область протекания реакций внешняя Показатели кинетическая внутренняя кинетическая внутридиффузионная внешнедиффузионная Энергия активации E E E/2 ≈0 Порядок реакции n n (n+1)/2 1 ~ Не зависит ~ ~ Зависимость реакции от размера скорости частиц катализатора Зависимость скорости реакции от удельной поверхности катализатора ~ S 1/2 Не зависит ~S (молекулярная диффузия) или не зависит Не зависит (кнудсеновская диффузия) Зависимость скорости реакции от среднего диаметра пор катализатора (молекулярная Не зависит ~ диффузия) или не зависит Не зависит (кнудсеновская диффузия) Зависимость скорости реакции от скорости газового потока Не зависит Зависит
Кинетические параметры реакции в различных областях ее протекания на пористых катализаторах Область протекания реакций внешняя Показатели кинетическая внутренняя кинетическая внутридиффузионная внешнедиффузионная Энергия активации E E E/2 ≈0 Порядок реакции n n (n+1)/2 1 ~ Не зависит ~ ~ Зависимость реакции от размера скорости частиц катализатора Зависимость скорости реакции от удельной поверхности катализатора ~ S 1/2 Не зависит ~S (молекулярная диффузия) или не зависит Не зависит (кнудсеновская диффузия) Зависимость скорости реакции от среднего диаметра пор катализатора (молекулярная Не зависит ~ диффузия) или не зависит Не зависит (кнудсеновская диффузия) Зависимость скорости реакции от скорости газового потока Не зависит Зависит


