рецепция_сигнальные системы.pptx
- Количество слайдов: 33
 Система рецепции и внутриклеточная сигнализация
Система рецепции и внутриклеточная сигнализация
 Молекулярная внутриклеточная сигнализация обеспечивает координацию работы белковых молекул, участвующих в реализации сложных мультимолекулярных процессов в ответ на различные стимулы. Внешние стимулы: 1) химической природы(ионы, гормоны, факторы роста и нейромедиаторы) 2) нехимической природы (механические, физические воздействия, изменения температуры и свет), которые преобразовываются в химический сигнал.
Молекулярная внутриклеточная сигнализация обеспечивает координацию работы белковых молекул, участвующих в реализации сложных мультимолекулярных процессов в ответ на различные стимулы. Внешние стимулы: 1) химической природы(ионы, гормоны, факторы роста и нейромедиаторы) 2) нехимической природы (механические, физические воздействия, изменения температуры и свет), которые преобразовываются в химический сигнал.
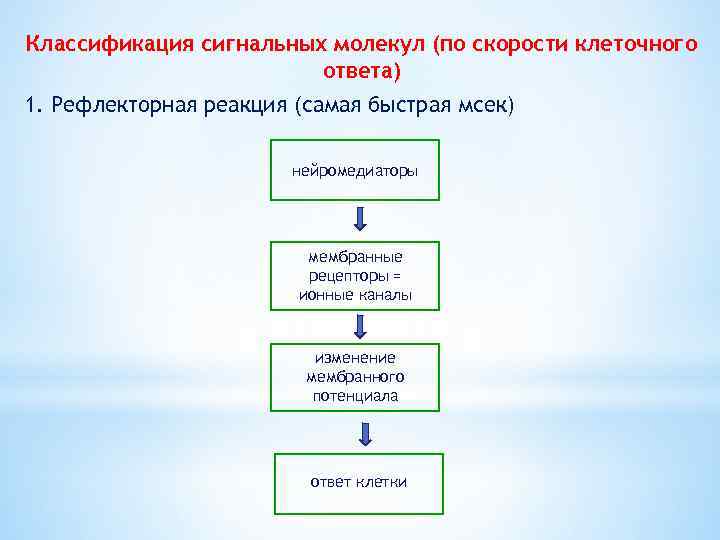 Классификация сигнальных молекул (по скорости клеточного ответа) 1. Рефлекторная реакция (самая быстрая мсек) нейромедиаторы мембранные рецепторы = ионные каналы изменение мембранного потенциала ответ клетки
Классификация сигнальных молекул (по скорости клеточного ответа) 1. Рефлекторная реакция (самая быстрая мсек) нейромедиаторы мембранные рецепторы = ионные каналы изменение мембранного потенциала ответ клетки
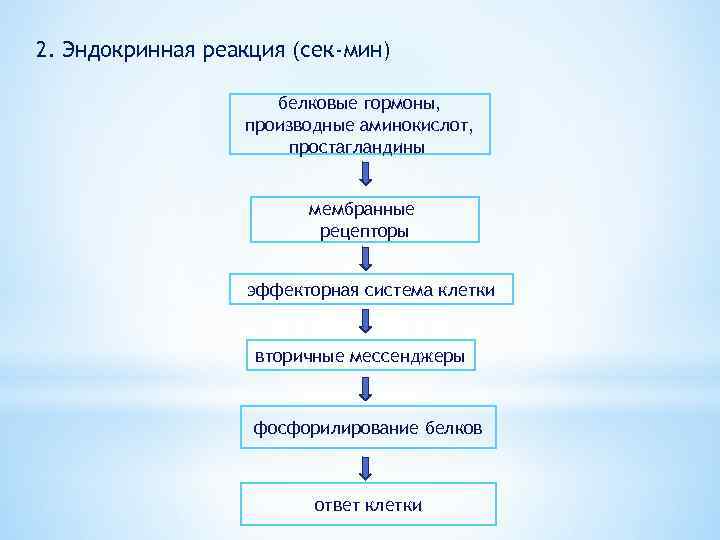 2. Эндокринная реакция (сек-мин) белковые гормоны, производные аминокислот, простагландины мембранные рецепторы эффекторная система клетки вторичные мессенджеры фосфорилирование белков ответ клетки
2. Эндокринная реакция (сек-мин) белковые гормоны, производные аминокислот, простагландины мембранные рецепторы эффекторная система клетки вторичные мессенджеры фосфорилирование белков ответ клетки
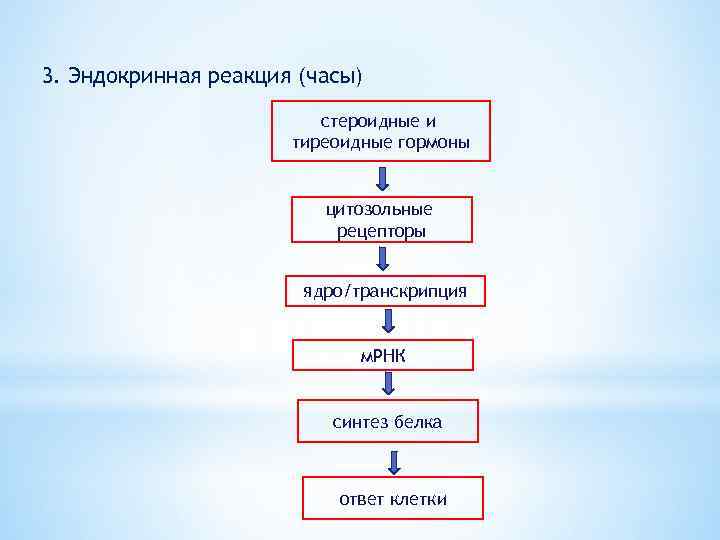 3. Эндокринная реакция (часы) стероидные и тиреоидные гормоны цитозольные рецепторы ядро/транскрипция м. РНК синтез белка ответ клетки
3. Эндокринная реакция (часы) стероидные и тиреоидные гормоны цитозольные рецепторы ядро/транскрипция м. РНК синтез белка ответ клетки
 Рецепторы - специализированные белковые молекулы, локализованные, как на цитоплазматической мембране, так и внутри клетки, обеспечивающие специфическое распознавание внешних молекулярных сигналов и определяющие специфичность клеточных реакций. Молекула, несущая внешний стимул является лигандом рецептора. Лиганд-рецепторное взаимодействие обладает специфичностью.
Рецепторы - специализированные белковые молекулы, локализованные, как на цитоплазматической мембране, так и внутри клетки, обеспечивающие специфическое распознавание внешних молекулярных сигналов и определяющие специфичность клеточных реакций. Молекула, несущая внешний стимул является лигандом рецептора. Лиганд-рецепторное взаимодействие обладает специфичностью.
 Аффинность или сродство – сила связывания лиганда с участком связывания рецептора. Различают: 1) аффинность лиганда по отношению к участку связывания 2) аффинность участка связывания по отношению к лиганду Мерой сродства участка связывания к лиганду является концентрация лиганда, необходимая для обеспечения 50% насыщения. Чем более низкая концентрация лиганда необходима для связывания его с половиной рецепторов, тем больше аффинность участка связывания к лиганду.
Аффинность или сродство – сила связывания лиганда с участком связывания рецептора. Различают: 1) аффинность лиганда по отношению к участку связывания 2) аффинность участка связывания по отношению к лиганду Мерой сродства участка связывания к лиганду является концентрация лиганда, необходимая для обеспечения 50% насыщения. Чем более низкая концентрация лиганда необходима для связывания его с половиной рецепторов, тем больше аффинность участка связывания к лиганду.
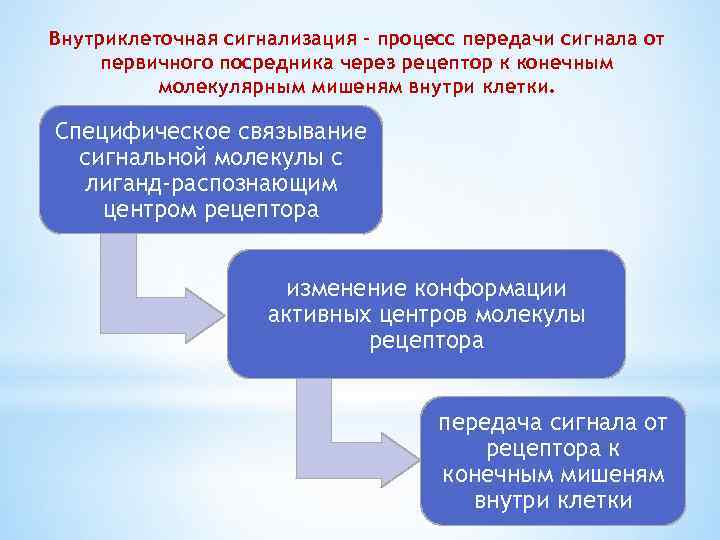 Внутриклеточная сигнализация – процесс передачи сигнала от первичного посредника через рецептор к конечным молекулярным мишеням внутри клетки. Специфическое связывание сигнальной молекулы с лиганд-распознающим центром рецептора изменение конформации активных центров молекулы рецептора передача сигнала от рецептора к конечным мишеням внутри клетки
Внутриклеточная сигнализация – процесс передачи сигнала от первичного посредника через рецептор к конечным молекулярным мишеням внутри клетки. Специфическое связывание сигнальной молекулы с лиганд-распознающим центром рецептора изменение конформации активных центров молекулы рецептора передача сигнала от рецептора к конечным мишеням внутри клетки
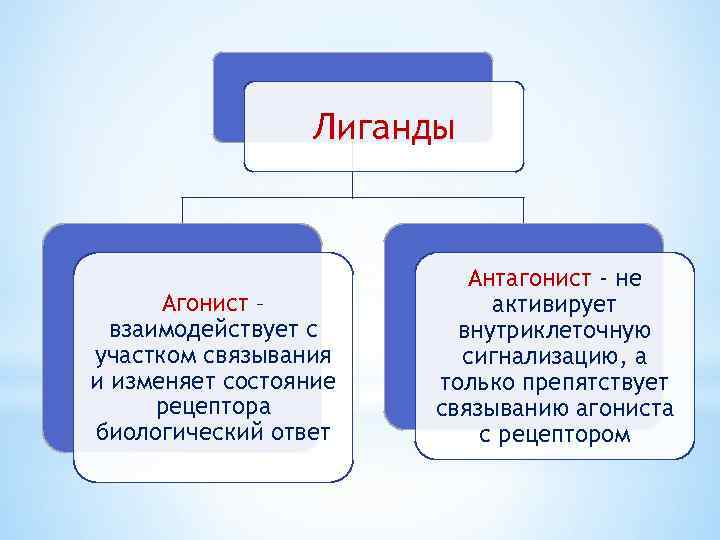 Лиганды Агонист – взаимодействует с участком связывания и изменяет состояние рецептора биологический ответ Антагонист - не активирует внутриклеточную сигнализацию, а только препятствует связыванию агониста с рецептором
Лиганды Агонист – взаимодействует с участком связывания и изменяет состояние рецептора биологический ответ Антагонист - не активирует внутриклеточную сигнализацию, а только препятствует связыванию агониста с рецептором
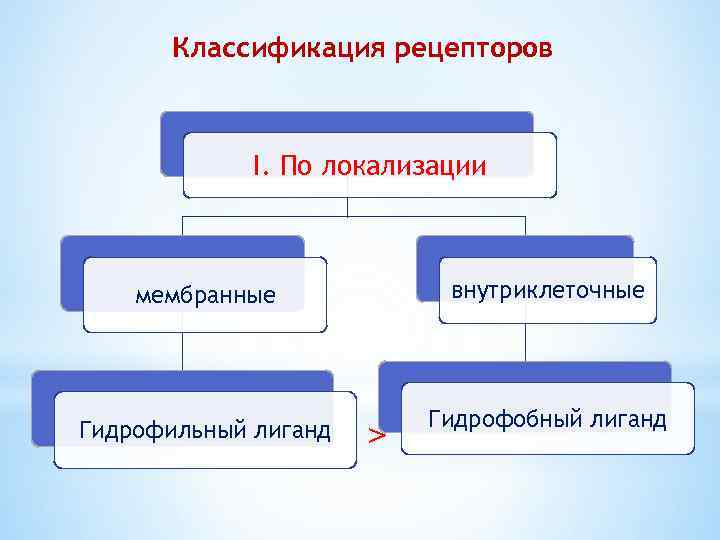 Классификация рецепторов I. По локализации мембранные внутриклеточные Гидрофильный лиганд Гидрофобный лиганд >
Классификация рецепторов I. По локализации мембранные внутриклеточные Гидрофильный лиганд Гидрофобный лиганд >
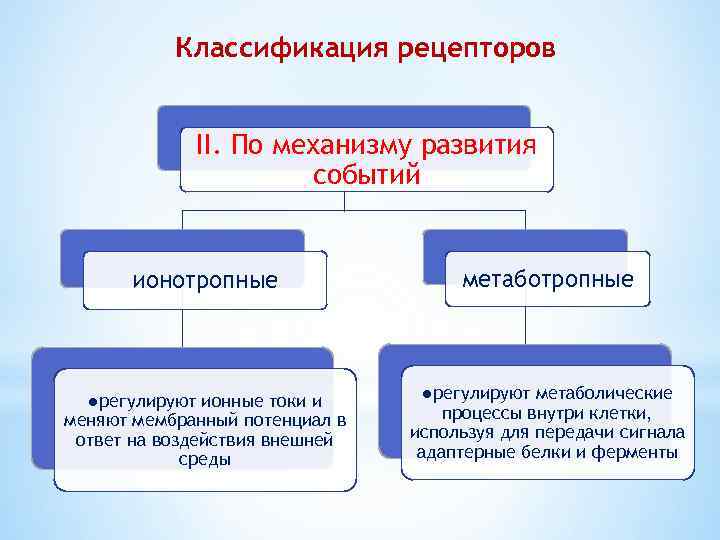 Классификация рецепторов II. По механизму развития событий ионотропные метаботропные ●регулируют ионные токи и меняют мембранный потенциал в ответ на воздействия внешней среды ●регулируют метаболические процессы внутри клетки, используя для передачи сигнала адаптерные белки и ферменты
Классификация рецепторов II. По механизму развития событий ионотропные метаботропные ●регулируют ионные токи и меняют мембранный потенциал в ответ на воздействия внешней среды ●регулируют метаболические процессы внутри клетки, используя для передачи сигнала адаптерные белки и ферменты
 Метаботропные рецепторы (MR) ●каталитические рецепторы ●связанные с G-белком ●ядерные ●рецепторы, освобождающие факторы транскрипции
Метаботропные рецепторы (MR) ●каталитические рецепторы ●связанные с G-белком ●ядерные ●рецепторы, освобождающие факторы транскрипции
 Ионотропные рецепторы (каналоформеры) ●интегральные мембранные белки ●ассоциированные субъединицы, образующие канал ●при отсутствии лиганда канал закрыт ●L+R= изменение конформации субъединиц Ионотропные R: к ацетилхолину, серотонину, -аминомасляной кислоте и глицину. Взаимодействие с лигандом непосредственно контролирует открытие и закрытие ионного канала открытие канала NH 3 S S PO О PO 4 4 С О
Ионотропные рецепторы (каналоформеры) ●интегральные мембранные белки ●ассоциированные субъединицы, образующие канал ●при отсутствии лиганда канал закрыт ●L+R= изменение конформации субъединиц Ионотропные R: к ацетилхолину, серотонину, -аминомасляной кислоте и глицину. Взаимодействие с лигандом непосредственно контролирует открытие и закрытие ионного канала открытие канала NH 3 S S PO О PO 4 4 С О
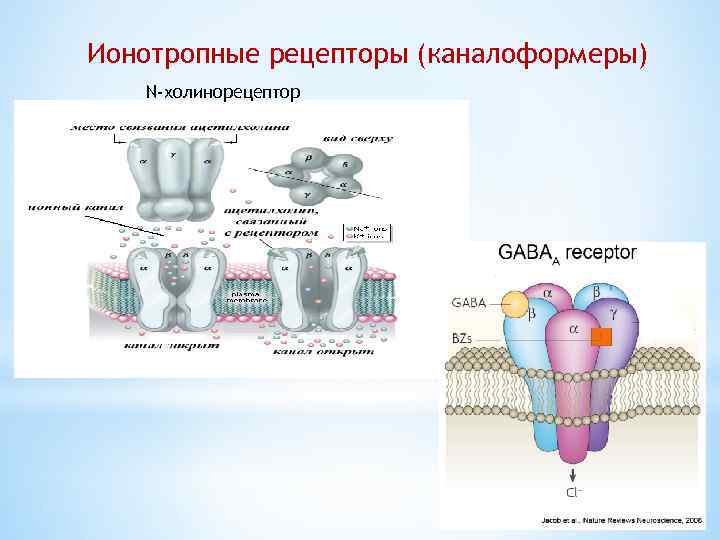 Ионотропные рецепторы (каналоформеры) N-холинорецептор
Ионотропные рецепторы (каналоформеры) N-холинорецептор
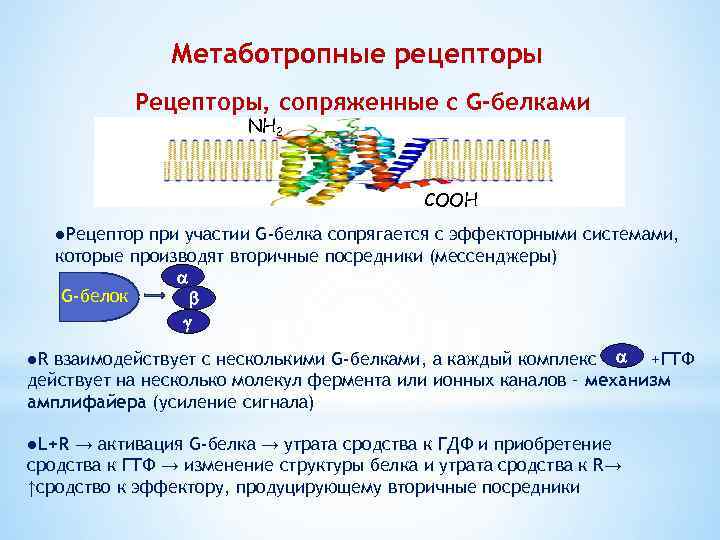 Метаботропные рецепторы Рецепторы, сопряженные с G-белками NH 2 СООН ●Рецептор при участии G-белка сопрягается с эффекторными системами, которые производят вторичные посредники (мессенджеры) G-белок ●R взаимодействует с несколькими G-белками, а каждый комплекс +ГТФ действует на несколько молекул фермента или ионных каналов – механизм амплифайера (усиление сигнала) ●L+R → активация G-белка → утрата сродства к ГДФ и приобретение сродства к ГТФ → изменение структуры белка и утрата сродства к R→ ↑сродство к эффектору, продуцирующему вторичные посредники
Метаботропные рецепторы Рецепторы, сопряженные с G-белками NH 2 СООН ●Рецептор при участии G-белка сопрягается с эффекторными системами, которые производят вторичные посредники (мессенджеры) G-белок ●R взаимодействует с несколькими G-белками, а каждый комплекс +ГТФ действует на несколько молекул фермента или ионных каналов – механизм амплифайера (усиление сигнала) ●L+R → активация G-белка → утрата сродства к ГДФ и приобретение сродства к ГТФ → изменение структуры белка и утрата сродства к R→ ↑сродство к эффектору, продуцирующему вторичные посредники
 Классификация G-белков ● 1981 г. – выделен первый G-белок (трансдуцин - Gt), участвующий в процессе передачи сигнала в фоторецепторах. ● 1983 г. - выделен Gs-белок, сопрягающий мембранные рецепторы с аденилатциклазой. ● 1985 -1988 гг. выделены Gq-белки, регулирующие активность фосфолипаз С и А 2 В 1994 г. Мартино Родбелл и Альфред Гудман Гилма получили Нобелевскую премию по физиологии и медицине «За открытие G-белков и роли этих белков в сигнальной трансдукции в клетке» . тип белка мишени локализация I. Gs Аденилатциклаза, Ca-каналы L-типа, Na-каналы повсеместно Gso К-каналы, потенциал-зависимые Caканалы НС и Эн. С Gst Фосфодиэстераза ц. ГМФ зрительные рецепторы Аденилатциклаза, К каналы, фосфолипаза повсеместно III. Gq Фосфолипаза С НС, тромбоциты IV. G 12 Аденилатциклаза (Golf) Фосфодиэстеразы (Ggust) обонятельные (Golf) вкусовые (Ggust) II. Gi (olf и gust)
Классификация G-белков ● 1981 г. – выделен первый G-белок (трансдуцин - Gt), участвующий в процессе передачи сигнала в фоторецепторах. ● 1983 г. - выделен Gs-белок, сопрягающий мембранные рецепторы с аденилатциклазой. ● 1985 -1988 гг. выделены Gq-белки, регулирующие активность фосфолипаз С и А 2 В 1994 г. Мартино Родбелл и Альфред Гудман Гилма получили Нобелевскую премию по физиологии и медицине «За открытие G-белков и роли этих белков в сигнальной трансдукции в клетке» . тип белка мишени локализация I. Gs Аденилатциклаза, Ca-каналы L-типа, Na-каналы повсеместно Gso К-каналы, потенциал-зависимые Caканалы НС и Эн. С Gst Фосфодиэстераза ц. ГМФ зрительные рецепторы Аденилатциклаза, К каналы, фосфолипаза повсеместно III. Gq Фосфолипаза С НС, тромбоциты IV. G 12 Аденилатциклаза (Golf) Фосфодиэстеразы (Ggust) обонятельные (Golf) вкусовые (Ggust) II. Gi (olf и gust)
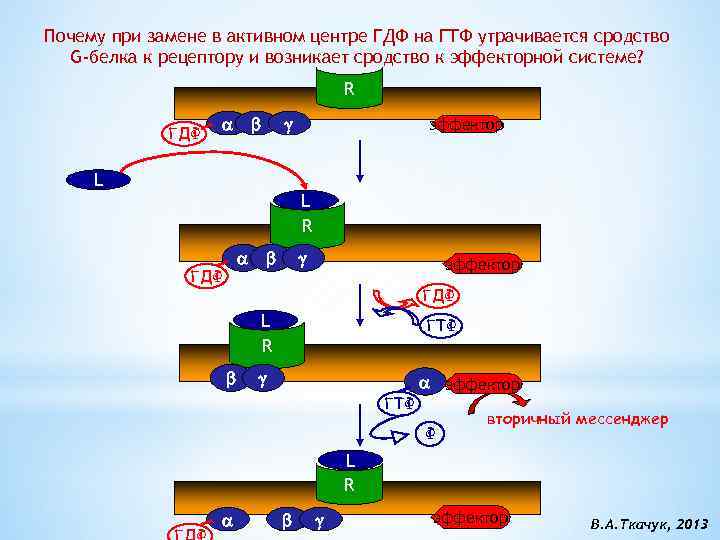 Почему при замене в активном центре ГДФ на ГТФ утрачивается сродство G-белка к рецептору и возникает сродство к эффекторной системе? R ГДФ L эффектор L R ГДФ эффектор ГДФ L R ГТФ эффектор Ф вторичный мессенджер L R эффектор В. А. Ткачук, 2013
Почему при замене в активном центре ГДФ на ГТФ утрачивается сродство G-белка к рецептору и возникает сродство к эффекторной системе? R ГДФ L эффектор L R ГДФ эффектор ГДФ L R ГТФ эффектор Ф вторичный мессенджер L R эффектор В. А. Ткачук, 2013
 Вторичные мессенджеры ● ионы кальция ● циклические нуклеотиды (ц. ГМФ, ц. АМФ) ● липофильные молекулы (инозитол-1, 4, 5 -три-фосфат (IP 3) и диацилглицерол (DAG) ● газы (NO, CO, H 2 S) Имеют небольшую молекулярную массу, высокую скорость диффузии внутри клетки, характерен короткий биохимический полупериод.
Вторичные мессенджеры ● ионы кальция ● циклические нуклеотиды (ц. ГМФ, ц. АМФ) ● липофильные молекулы (инозитол-1, 4, 5 -три-фосфат (IP 3) и диацилглицерол (DAG) ● газы (NO, CO, H 2 S) Имеют небольшую молекулярную массу, высокую скорость диффузии внутри клетки, характерен короткий биохимический полупериод.
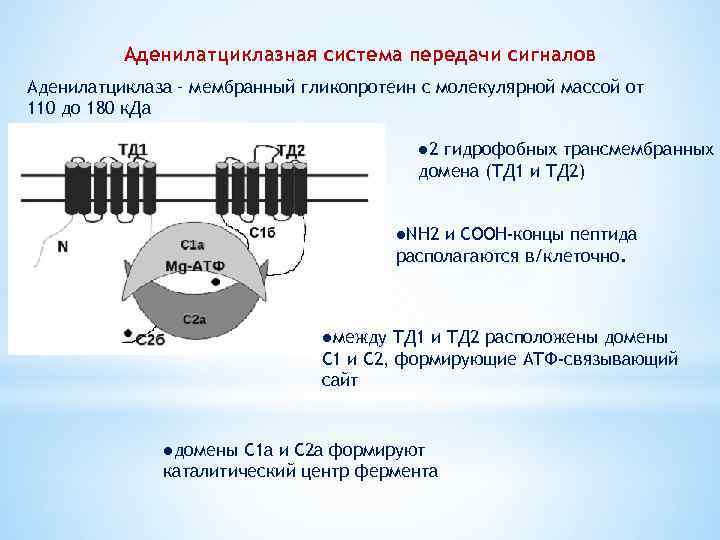 Аденилатциклазная система передачи сигналов Аденилатциклаза – мембранный гликопротеин с молекулярной массой от 110 до 180 к. Да ● 2 гидрофобных трансмембранных домена (ТД 1 и ТД 2) ●NH 2 и СOOH-концы пептида располагаются в/клеточно. ●между ТД 1 и ТД 2 расположены домены С 1 и С 2, формирующие АТФ-связывающий сайт ●домены С 1 а и С 2 а формируют каталитический центр фермента
Аденилатциклазная система передачи сигналов Аденилатциклаза – мембранный гликопротеин с молекулярной массой от 110 до 180 к. Да ● 2 гидрофобных трансмембранных домена (ТД 1 и ТД 2) ●NH 2 и СOOH-концы пептида располагаются в/клеточно. ●между ТД 1 и ТД 2 расположены домены С 1 и С 2, формирующие АТФ-связывающий сайт ●домены С 1 а и С 2 а формируют каталитический центр фермента
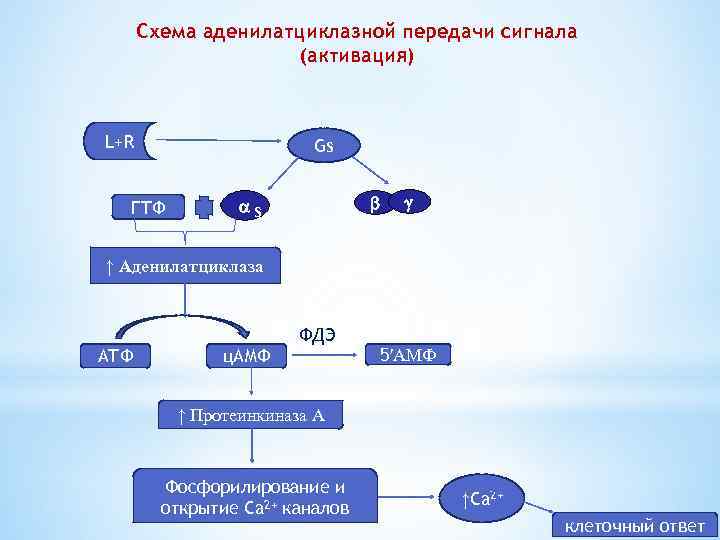 Схема аденилатциклазной передачи сигнала (активация) L+R Gs ГТФ s ↑ Аденилатциклаза ФДЭ АТФ ц. АМФ 5′АМФ ↑ Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↑Ca 2+ клеточный ответ
Схема аденилатциклазной передачи сигнала (активация) L+R Gs ГТФ s ↑ Аденилатциклаза ФДЭ АТФ ц. АМФ 5′АМФ ↑ Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↑Ca 2+ клеточный ответ
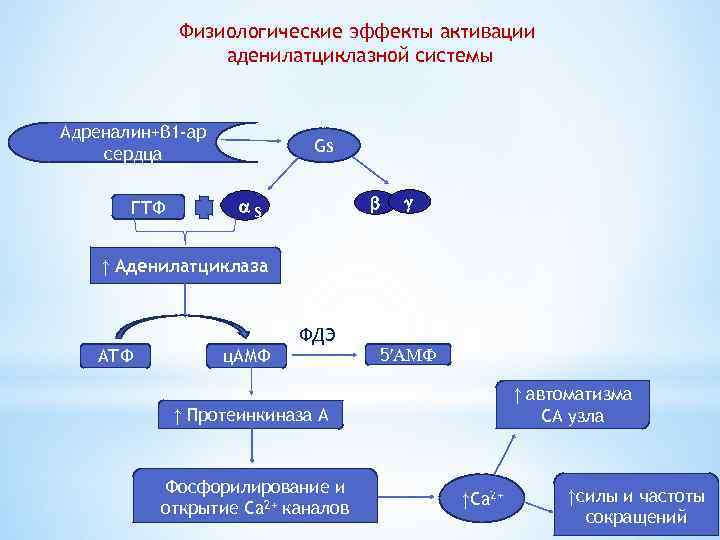 Физиологические эффекты активации аденилатциклазной системы Адреналин+β 1 -ар сердца ГТФ Gs s ↑ Аденилатциклаза ФДЭ АТФ ц. АМФ 5′АМФ ↑ автоматизма СА узла ↑ Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↑Ca 2+ ↑силы и частоты сокращений
Физиологические эффекты активации аденилатциклазной системы Адреналин+β 1 -ар сердца ГТФ Gs s ↑ Аденилатциклаза ФДЭ АТФ ц. АМФ 5′АМФ ↑ автоматизма СА узла ↑ Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↑Ca 2+ ↑силы и частоты сокращений
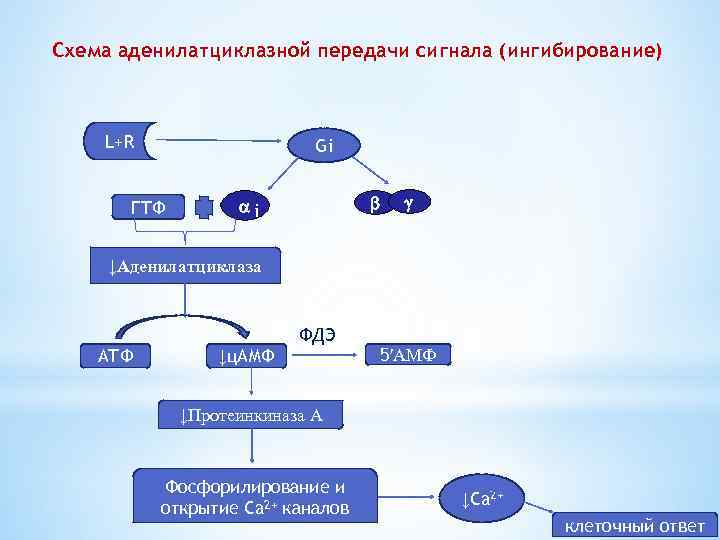 Схема аденилатциклазной передачи сигнала (ингибирование) L+R Gi ГТФ i ↓Аденилатциклаза ФДЭ АТФ ↓ц. АМФ 5′АМФ ↓Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↓Ca 2+ клеточный ответ
Схема аденилатциклазной передачи сигнала (ингибирование) L+R Gi ГТФ i ↓Аденилатциклаза ФДЭ АТФ ↓ц. АМФ 5′АМФ ↓Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↓Ca 2+ клеточный ответ
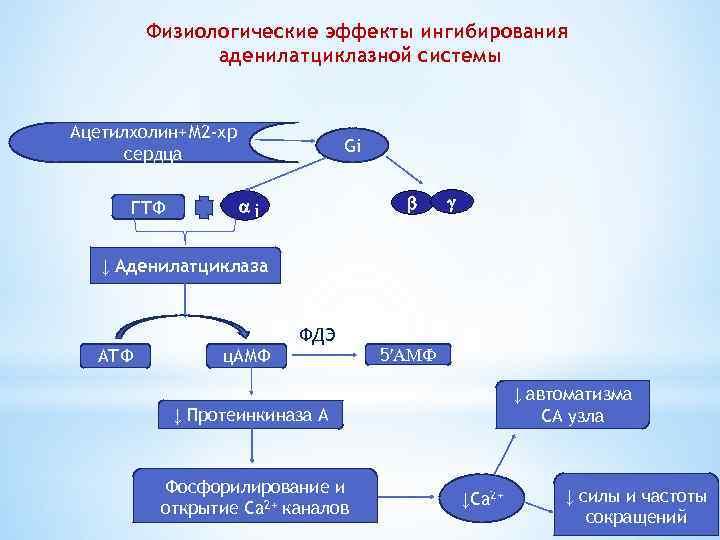 Физиологические эффекты ингибирования аденилатциклазной системы Ацетилхолин+М 2 -хр сердца ГТФ Gi i ↓ Аденилатциклаза ФДЭ АТФ ц. АМФ 5′АМФ ↓ автоматизма СА узла ↓ Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↓Ca 2+ ↓ силы и частоты сокращений
Физиологические эффекты ингибирования аденилатциклазной системы Ацетилхолин+М 2 -хр сердца ГТФ Gi i ↓ Аденилатциклаза ФДЭ АТФ ц. АМФ 5′АМФ ↓ автоматизма СА узла ↓ Протеинкиназа А Фосфорилирование и открытие Ca 2+ каналов ↓Ca 2+ ↓ силы и частоты сокращений
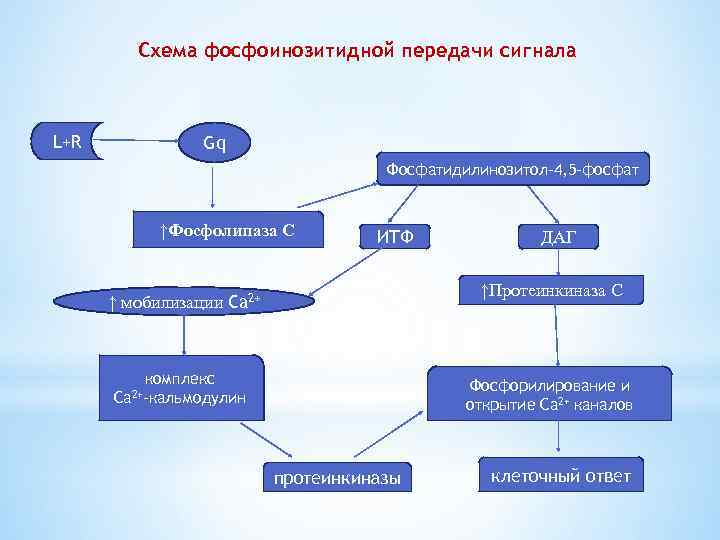 Схема фосфоинозитидной передачи сигнала L+R Gq Фосфатидилинозитол-4, 5 -фосфат ↑Фосфолипаза С ИТФ ДАГ ↑Протеинкиназа С ↑ мобилизации Ca 2+ комплекс Ca 2+-кальмодулин Фосфорилирование и открытие Ca 2+ каналов протеинкиназы клеточный ответ
Схема фосфоинозитидной передачи сигнала L+R Gq Фосфатидилинозитол-4, 5 -фосфат ↑Фосфолипаза С ИТФ ДАГ ↑Протеинкиназа С ↑ мобилизации Ca 2+ комплекс Ca 2+-кальмодулин Фосфорилирование и открытие Ca 2+ каналов протеинкиназы клеточный ответ
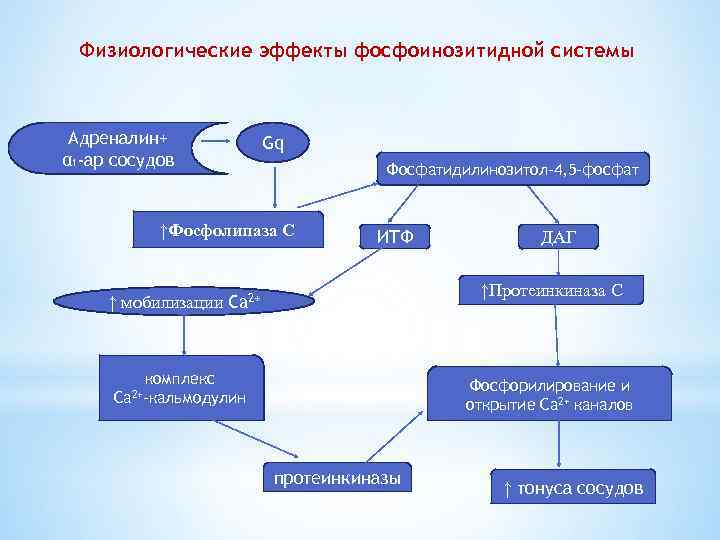 Физиологические эффекты фосфоинозитидной системы Адреналин+ α 1 -ар сосудов Gq Фосфатидилинозитол-4, 5 -фосфат ↑Фосфолипаза С ИТФ ДАГ ↑Протеинкиназа С ↑ мобилизации Ca 2+ комплекс Ca 2+-кальмодулин Фосфорилирование и открытие Ca 2+ каналов протеинкиназы ↑ тонуса сосудов
Физиологические эффекты фосфоинозитидной системы Адреналин+ α 1 -ар сосудов Gq Фосфатидилинозитол-4, 5 -фосфат ↑Фосфолипаза С ИТФ ДАГ ↑Протеинкиназа С ↑ мобилизации Ca 2+ комплекс Ca 2+-кальмодулин Фосфорилирование и открытие Ca 2+ каналов протеинкиназы ↑ тонуса сосудов
 Каталитические рецепторы ●с собственной гуанилатциклазной активностью обладают способнос тью реализовывать сигнал через ц. ГМФ опосредован ныйпуть (н-р, рецепторы к предсердному натрийуретическому пептиду) ●с собственной тирозинкиназной активностью рецепторы инсулина, цитокинов, факторов роста, активация которых вызывает фосфорилирование различных групп внут риклеточных белков, которые, меняя свою биологи ческую активность, вызывают широкий спектр реакций
Каталитические рецепторы ●с собственной гуанилатциклазной активностью обладают способнос тью реализовывать сигнал через ц. ГМФ опосредован ныйпуть (н-р, рецепторы к предсердному натрийуретическому пептиду) ●с собственной тирозинкиназной активностью рецепторы инсулина, цитокинов, факторов роста, активация которых вызывает фосфорилирование различных групп внут риклеточных белков, которые, меняя свою биологи ческую активность, вызывают широкий спектр реакций
 Каталитические рецепторы с собственной гуанилатциклазной активностью Гуанилатциклаза: ▪ катализирует образование ц. ГМФ (вторичный мессенджер) из ГТФ ▪ мембранная и цитозольная формы Цитозольная выполняет широкий спектр физиологических функций: ингибирование агрегации тромбоцитов расслабление гладкой мускулатуры вазодилятация нейрональная сигнальная трансдукция и иммуномодуляция Мембранная гуанилатциклаза - трансмембранный гликопротеин. Внутриклеточный домен гуанилатциклазы проявляет каталитическую активность, внеклеточный домен служит рецептором. L+R вызывает изменение конформации в мембранном и цитозольном доменах и, как следствие, активацию гуанилатиклазы.
Каталитические рецепторы с собственной гуанилатциклазной активностью Гуанилатциклаза: ▪ катализирует образование ц. ГМФ (вторичный мессенджер) из ГТФ ▪ мембранная и цитозольная формы Цитозольная выполняет широкий спектр физиологических функций: ингибирование агрегации тромбоцитов расслабление гладкой мускулатуры вазодилятация нейрональная сигнальная трансдукция и иммуномодуляция Мембранная гуанилатциклаза - трансмембранный гликопротеин. Внутриклеточный домен гуанилатциклазы проявляет каталитическую активность, внеклеточный домен служит рецептором. L+R вызывает изменение конформации в мембранном и цитозольном доменах и, как следствие, активацию гуанилатиклазы.
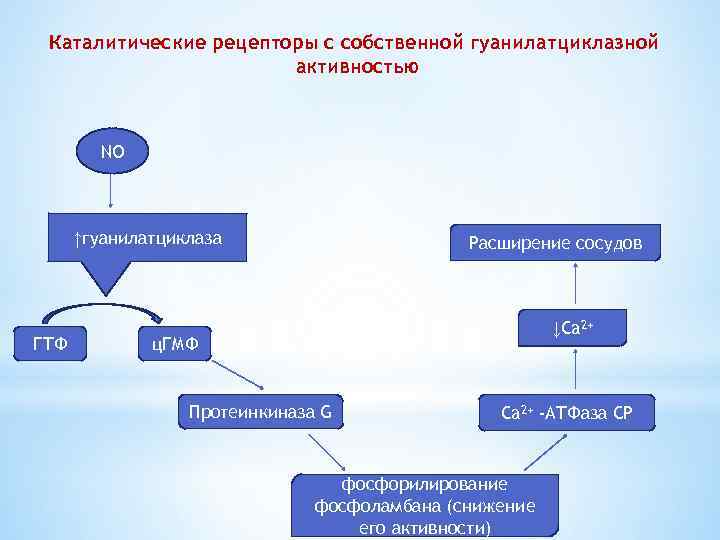 Каталитические рецепторы с собственной гуанилатциклазной активностью NO ↑гуанилатциклаза ГТФ Расширение сосудов ↓Ca 2+ ц. ГМФ Протеинкиназа G Ca 2+ -АТФаза СР фосфорилирование фосфоламбана (снижение его активности)
Каталитические рецепторы с собственной гуанилатциклазной активностью NO ↑гуанилатциклаза ГТФ Расширение сосудов ↓Ca 2+ ц. ГМФ Протеинкиназа G Ca 2+ -АТФаза СР фосфорилирование фосфоламбана (снижение его активности)
 Каталитические рецепторы с собственной тирозинкиназной активностью Тирозиновые протеинкиназы фосфорилируют специфические белки по тирозину мембранные (рецепторные) участие трансмембранной передаче сигналов цитоплазматические участие в процессах передачи сигнала в ядро
Каталитические рецепторы с собственной тирозинкиназной активностью Тирозиновые протеинкиназы фосфорилируют специфические белки по тирозину мембранные (рецепторные) участие трансмембранной передаче сигналов цитоплазматические участие в процессах передачи сигнала в ядро
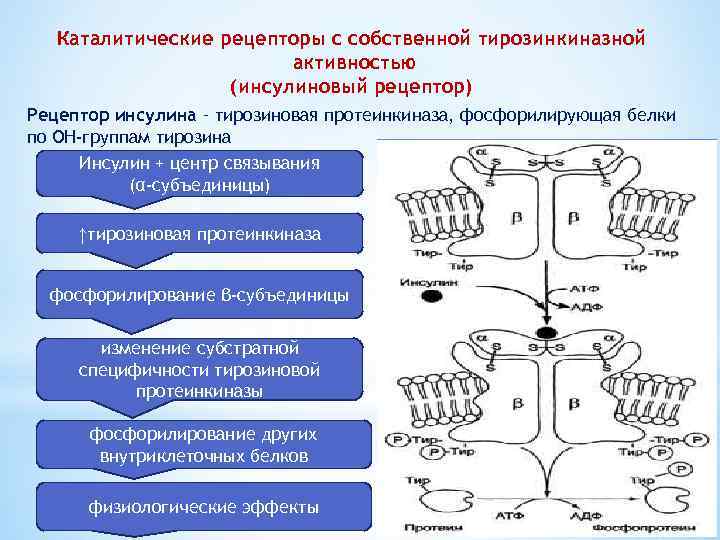 Каталитические рецепторы с собственной тирозинкиназной активностью (инсулиновый рецептор) Рецептор инсулина – тирозиновая протеинкиназа, фосфорилирующая белки по ОН-группам тирозина Инсулин + центр связывания (α-субъединицы) ↑тирозиновая протеинкиназа фосфорилирование β-субъединицы изменение субстратной специфичности тирозиновой протеинкиназы фосфорилирование других внутриклеточных белков физиологические эффекты
Каталитические рецепторы с собственной тирозинкиназной активностью (инсулиновый рецептор) Рецептор инсулина – тирозиновая протеинкиназа, фосфорилирующая белки по ОН-группам тирозина Инсулин + центр связывания (α-субъединицы) ↑тирозиновая протеинкиназа фосфорилирование β-субъединицы изменение субстратной специфичности тирозиновой протеинкиназы фосфорилирование других внутриклеточных белков физиологические эффекты
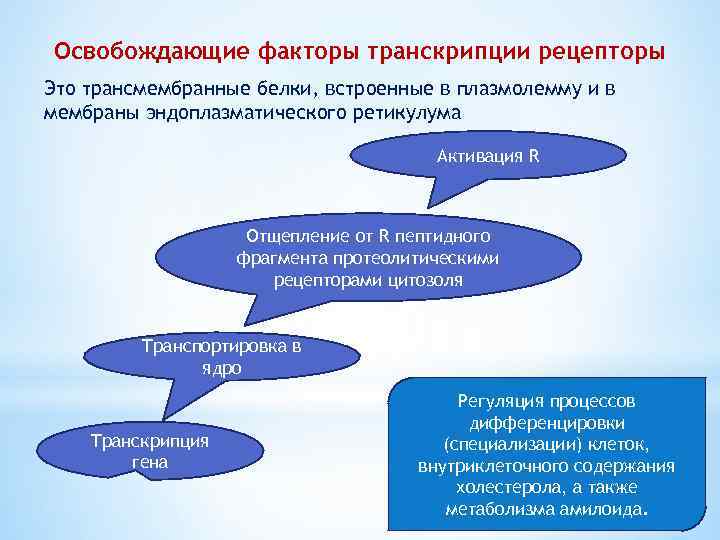 Освобождающие факторы транскрипции рецепторы Это трансмембранные белки, встроенные в плазмолемму и в мембраны эндоплазматического ретикулума Активация R Отщепление от R пептидного фрагмента протеолитическими рецепторами цитозоля Транспортировка в ядро Транскрипция гена Регуляция процессов дифференцировки (специализации) клеток, внутриклеточного содержания холестерола, а также метаболизма амилоида.
Освобождающие факторы транскрипции рецепторы Это трансмембранные белки, встроенные в плазмолемму и в мембраны эндоплазматического ретикулума Активация R Отщепление от R пептидного фрагмента протеолитическими рецепторами цитозоля Транспортировка в ядро Транскрипция гена Регуляция процессов дифференцировки (специализации) клеток, внутриклеточного содержания холестерола, а также метаболизма амилоида.
 Внутриклеточные (ядерные) рецепторы Локализуются цитоплазме или в ядре Лиганды – гидрофобные молекулы: стероидные гормоны, тиреоидные гормоны, простагландины, витамин D и др. Транспортируются через ЦПМ белками-переносчиками LRK в ядре в цитоплазме действие LRK реализуется в ядре . При связывании лиганда рецепторы активируются и действуют как регуляторы транскрипции
Внутриклеточные (ядерные) рецепторы Локализуются цитоплазме или в ядре Лиганды – гидрофобные молекулы: стероидные гормоны, тиреоидные гормоны, простагландины, витамин D и др. Транспортируются через ЦПМ белками-переносчиками LRK в ядре в цитоплазме действие LRK реализуется в ядре . При связывании лиганда рецепторы активируются и действуют как регуляторы транскрипции
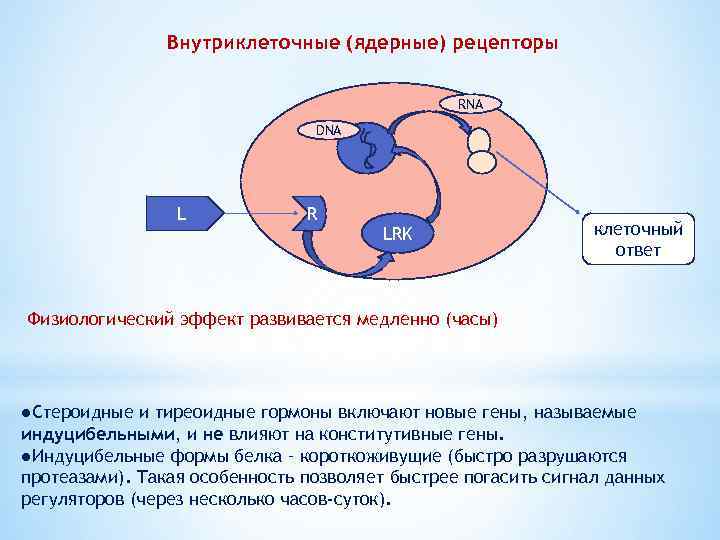 Внутриклеточные (ядерные) рецепторы RNA DNA L R LRK клеточный ответ Физиологический эффект развивается медленно (часы) ●Стероидные и тиреоидные гормоны включают новые гены, называемые индуцибельными, и не влияют на конститутивные гены. ●Индуцибельные формы белка – короткоживущие (быстро разрушаются протеазами). Такая особенность позволяет быстрее погасить сигнал данных регуляторов (через несколько часов-суток).
Внутриклеточные (ядерные) рецепторы RNA DNA L R LRK клеточный ответ Физиологический эффект развивается медленно (часы) ●Стероидные и тиреоидные гормоны включают новые гены, называемые индуцибельными, и не влияют на конститутивные гены. ●Индуцибельные формы белка – короткоживущие (быстро разрушаются протеазами). Такая особенность позволяет быстрее погасить сигнал данных регуляторов (через несколько часов-суток).


