Функционирование_гемостаза_бз2+.ppt
- Количество слайдов: 109
 Система гемостаза – функционирование и методы исследования
Система гемостаза – функционирование и методы исследования
 СИСТЕМА ГЕМОСТАЗА – это биологическая система, основной функцией которой является поддержание равновесия между антагонистически действующими механизмами: I - обеспечивающими сохранение крови в жидком состоянии и II - предотвращающими потерю крови путем образования тромбов.
СИСТЕМА ГЕМОСТАЗА – это биологическая система, основной функцией которой является поддержание равновесия между антагонистически действующими механизмами: I - обеспечивающими сохранение крови в жидком состоянии и II - предотвращающими потерю крови путем образования тромбов.
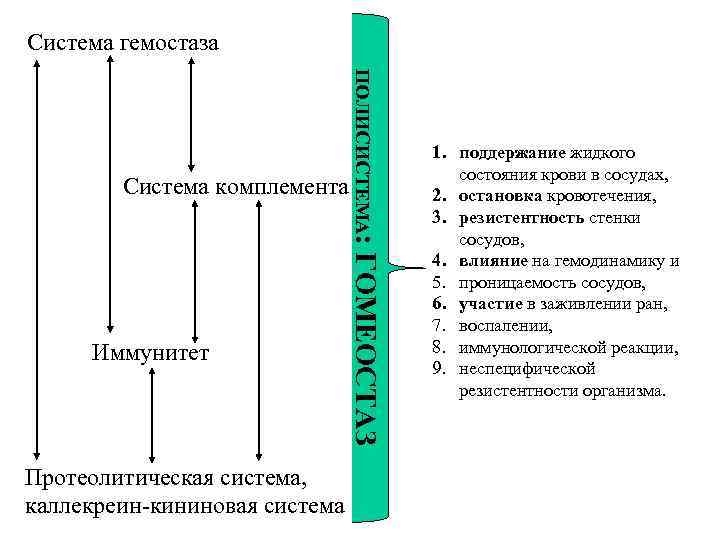 Система гемостаза Иммунитет Протеолитическая система, каллекреин-кининовая система ПОЛИСИСТЕМА: ГОМЕОСТАЗ Система комплемента 1. поддержание жидкого состояния крови в сосудах, 2. остановка кровотечения, 3. резистентность стенки сосудов, 4. влияние на гемодинамику и 5. проницаемость сосудов, 6. участие в заживлении ран, 7. воспалении, 8. иммунологической реакции, 9. неспецифической резистентности организма.
Система гемостаза Иммунитет Протеолитическая система, каллекреин-кининовая система ПОЛИСИСТЕМА: ГОМЕОСТАЗ Система комплемента 1. поддержание жидкого состояния крови в сосудах, 2. остановка кровотечения, 3. резистентность стенки сосудов, 4. влияние на гемодинамику и 5. проницаемость сосудов, 6. участие в заживлении ран, 7. воспалении, 8. иммунологической реакции, 9. неспецифической резистентности организма.
 ИНТЕГРАЛЬНАЯ СХЕМА ПРЕДСТАВЛЕНИЙ О СТРОЕНИИ И ФУНКЦИОНИРОВАНИИ СИСТЕМЫ ГЕМОСТАЗА
ИНТЕГРАЛЬНАЯ СХЕМА ПРЕДСТАВЛЕНИЙ О СТРОЕНИИ И ФУНКЦИОНИРОВАНИИ СИСТЕМЫ ГЕМОСТАЗА
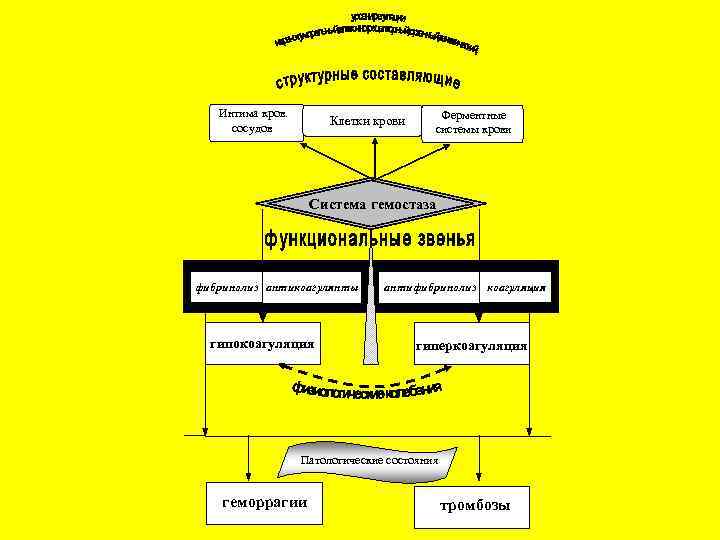 Интима кров. сосудов Клетки крови Ферментные системы крови Система гемостаза фибринолиз антикоагулянты гипокоагуляция антифибринолиз коагуляция гиперкоагуляция Патологические состояния геморрагии тромбозы
Интима кров. сосудов Клетки крови Ферментные системы крови Система гемостаза фибринолиз антикоагулянты гипокоагуляция антифибринолиз коагуляция гиперкоагуляция Патологические состояния геморрагии тромбозы
 КОАГУЛЯЦИОННОЕ ЗВЕНО СИСТЕМЫ ГЕМОСТАЗА
КОАГУЛЯЦИОННОЕ ЗВЕНО СИСТЕМЫ ГЕМОСТАЗА
 Коагуляция (свертывание крови) – процесс инициации и дальнейшего взаимодействия форменных элементов крови и факторов свертывания с образованием тромбина, при достижении критического уровня которого происходит в агрегате и на поверхности агрегата форменных элементов превращение фибриногена в фибрин. Результатом коагуляции является образование сгустка – агрегата из форменных элементов крови, укрепленного нитями фибрина.
Коагуляция (свертывание крови) – процесс инициации и дальнейшего взаимодействия форменных элементов крови и факторов свертывания с образованием тромбина, при достижении критического уровня которого происходит в агрегате и на поверхности агрегата форменных элементов превращение фибриногена в фибрин. Результатом коагуляции является образование сгустка – агрегата из форменных элементов крови, укрепленного нитями фибрина.
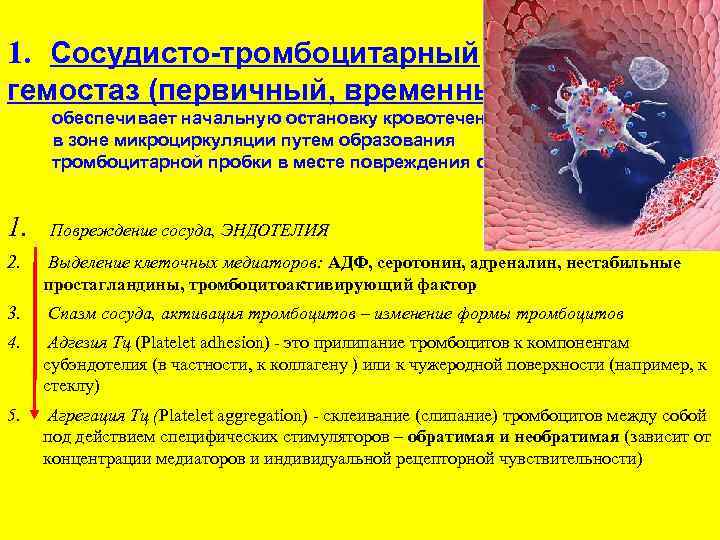 1. Сосудисто-тромбоцитарный гемостаз (первичный, временный) обеспечивает начальную остановку кровотечения в зоне микроциркуляции путем образования тромбоцитарной пробки в месте повреждения сосуда 1. Повреждение сосуда, ЭНДОТЕЛИЯ 2. Выделение клеточных медиаторов: АДФ, серотонин, адреналин, нестабильные простагландины, тромбоцитоактивирующий фактор 3. Спазм сосуда, активация тромбоцитов – изменение формы тромбоцитов 4. Адгезия Тц (Platelet adhesion) - это прилипание тромбоцитов к компонентам субэндотелия (в частности, к коллагену ) или к чужеродной поверхности (например, к стеклу) 5. Агрегация Тц (Platelet aggregation) - склеивание (слипание) тромбоцитов между собой под действием специфических стимуляторов – обратимая и необратимая (зависит от концентрации медиаторов и индивидуальной рецепторной чувствительности)
1. Сосудисто-тромбоцитарный гемостаз (первичный, временный) обеспечивает начальную остановку кровотечения в зоне микроциркуляции путем образования тромбоцитарной пробки в месте повреждения сосуда 1. Повреждение сосуда, ЭНДОТЕЛИЯ 2. Выделение клеточных медиаторов: АДФ, серотонин, адреналин, нестабильные простагландины, тромбоцитоактивирующий фактор 3. Спазм сосуда, активация тромбоцитов – изменение формы тромбоцитов 4. Адгезия Тц (Platelet adhesion) - это прилипание тромбоцитов к компонентам субэндотелия (в частности, к коллагену ) или к чужеродной поверхности (например, к стеклу) 5. Агрегация Тц (Platelet aggregation) - склеивание (слипание) тромбоцитов между собой под действием специфических стимуляторов – обратимая и необратимая (зависит от концентрации медиаторов и индивидуальной рецепторной чувствительности)
 Участие в гемостатическом балансе эндотелиальных клеток
Участие в гемостатическом балансе эндотелиальных клеток
 Общепринято, что: ТРОМБОРЕЗИСТЕНТНОСТЬ эндотелия обусловлена: • Способностью образовывать и выделять в кровь ингибитор агрегации тромбоцитов – простациклин (метаболит арахидоновой кислоты, простагландин); • Неспособностью к контактной активации системы свертывания крови; • Созданием антикоагулянтного потенциала на границе кровь/ткань путем фиксации на эндотелии комплекса гепарин – антитромбин ; • Продукцией тканевого активатора плазминогена; • Способностью удалять из кровотока активированные факторы свертывания. Повреждение эндотелия - ТРОМБООБРАЗОВАНИЕ за счет: • выделения в кровь тканевого тромбопластина и стимуляторов тромбоцитов – адреналина, АДФ, норадреналина (обладают также сосудоссуживающими свойствами); • контактной активации коллагеном и другими компонентами субэндотелия как тромбоцитов (адгезия) • свертыванию крови (активация фактора ); • продукции плазменных факторов адгезии и агрегации тромбоцитов – фактора Виллебранда.
Общепринято, что: ТРОМБОРЕЗИСТЕНТНОСТЬ эндотелия обусловлена: • Способностью образовывать и выделять в кровь ингибитор агрегации тромбоцитов – простациклин (метаболит арахидоновой кислоты, простагландин); • Неспособностью к контактной активации системы свертывания крови; • Созданием антикоагулянтного потенциала на границе кровь/ткань путем фиксации на эндотелии комплекса гепарин – антитромбин ; • Продукцией тканевого активатора плазминогена; • Способностью удалять из кровотока активированные факторы свертывания. Повреждение эндотелия - ТРОМБООБРАЗОВАНИЕ за счет: • выделения в кровь тканевого тромбопластина и стимуляторов тромбоцитов – адреналина, АДФ, норадреналина (обладают также сосудоссуживающими свойствами); • контактной активации коллагеном и другими компонентами субэндотелия как тромбоцитов (адгезия) • свертыванию крови (активация фактора ); • продукции плазменных факторов адгезии и агрегации тромбоцитов – фактора Виллебранда.
 Однако оголение субэндотелия происходит постоянно, так как в день может обновляться около миллиона эндотелиальных клеток !!! НЕПРЕРЫВНОЕ СВЕРТЫВАНИЕ КРОВИ ? В общем кровотоке обнаруживается только при массивном кровотечении
Однако оголение субэндотелия происходит постоянно, так как в день может обновляться около миллиона эндотелиальных клеток !!! НЕПРЕРЫВНОЕ СВЕРТЫВАНИЕ КРОВИ ? В общем кровотоке обнаруживается только при массивном кровотечении
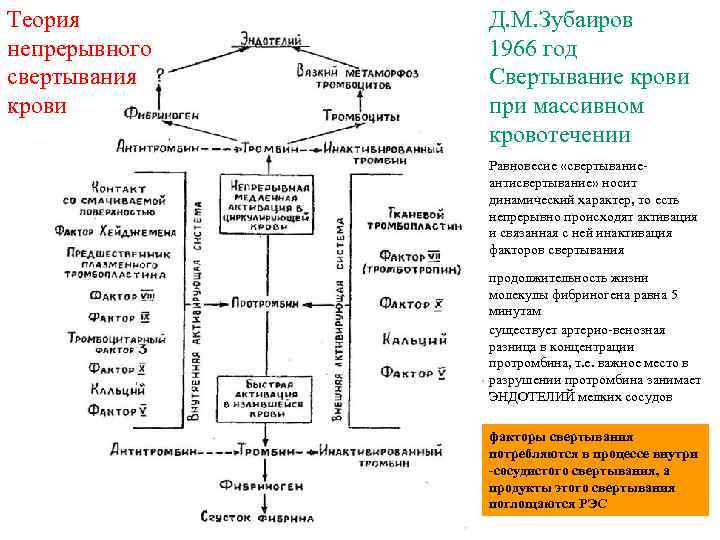 Теория непрерывного свертывания крови Д. М. Зубаиров 1966 год Свертывание крови при массивном кровотечении Равновесие «свертываниеантисвертывание» носит динамический характер, то есть непрерывно происходят активация и связанная с ней инактивация факторов свертывания продолжительность жизни молекулы фибриногена равна 5 минутам существует артерио-венозная разница в концентрации протромбина, т. е. важное место в разрушении протромбина занимает ЭНДОТЕЛИЙ мелких сосудов факторы свертывания потребляются в процессе внутри -сосудистого свертывания, а продукты этого свертывания поглощаются РЭС
Теория непрерывного свертывания крови Д. М. Зубаиров 1966 год Свертывание крови при массивном кровотечении Равновесие «свертываниеантисвертывание» носит динамический характер, то есть непрерывно происходят активация и связанная с ней инактивация факторов свертывания продолжительность жизни молекулы фибриногена равна 5 минутам существует артерио-венозная разница в концентрации протромбина, т. е. важное место в разрушении протромбина занимает ЭНДОТЕЛИЙ мелких сосудов факторы свертывания потребляются в процессе внутри -сосудистого свертывания, а продукты этого свертывания поглощаются РЭС
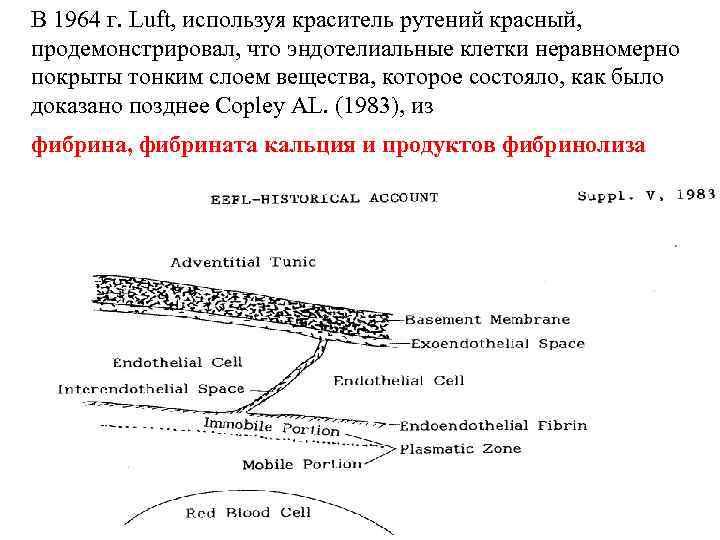 В 1964 г. Luft, используя краситель рутений красный, продемонстрировал, что эндотелиальные клетки неравномерно покрыты тонким слоем вещества, которое состояло, как было доказано позднее Copley AL. (1983), из фибрина, фибрината кальция и продуктов фибринолиза
В 1964 г. Luft, используя краситель рутений красный, продемонстрировал, что эндотелиальные клетки неравномерно покрыты тонким слоем вещества, которое состояло, как было доказано позднее Copley AL. (1983), из фибрина, фибрината кальция и продуктов фибринолиза
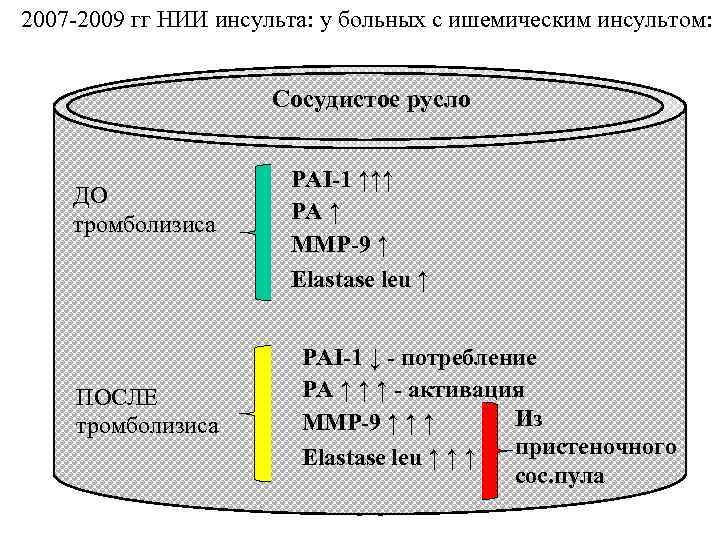 2007 -2009 гг НИИ инсульта: у больных с ишемическим инсультом: Сосудистое русло ДО тромболизиса ПОСЛЕ тромболизиса PAI-1 ↑↑↑ PA ↑ MMP-9 ↑ Elastase leu ↑ PAI-1 ↓ - потребление PA ↑ ↑ ↑ - активация Из MMP-9 ↑ ↑ ↑ пристеночного Elastase leu ↑ ↑ ↑ сос. пула
2007 -2009 гг НИИ инсульта: у больных с ишемическим инсультом: Сосудистое русло ДО тромболизиса ПОСЛЕ тромболизиса PAI-1 ↑↑↑ PA ↑ MMP-9 ↑ Elastase leu ↑ PAI-1 ↓ - потребление PA ↑ ↑ ↑ - активация Из MMP-9 ↑ ↑ ↑ пристеночного Elastase leu ↑ ↑ ↑ сос. пула
 Концепция внутрисосудистой морфо-функциональности системы гемостаза 1. Мозаичность морфо-функционального состояния системы гемостаза обусловлена типом, калибром сосуда, его расположением (органным включительно), двигательной активности, а также скорости и ламинарности кровотока 3. Взаимообусловлены активность, концентрация маркеров коагуляции, воспаления, эндотелиальной/сосудистой деструкции и их соотношения с внутрисосудистой мозаичностью морфо-функционального состояния системы гемостаза 4. Наличие особенностей атеро- и тромбогенеза в различных сосудах зависит от механизмов поддержания внутрисосудистой мозаичности морфофункционального состояния системы гемостаза 5. Эффективности антиатеротромботической терапии зависит от учета влияния терапии на особенности механизмов поддержания внутрисосудистой мозаичности морфо-функционального состояния системы гемостаза
Концепция внутрисосудистой морфо-функциональности системы гемостаза 1. Мозаичность морфо-функционального состояния системы гемостаза обусловлена типом, калибром сосуда, его расположением (органным включительно), двигательной активности, а также скорости и ламинарности кровотока 3. Взаимообусловлены активность, концентрация маркеров коагуляции, воспаления, эндотелиальной/сосудистой деструкции и их соотношения с внутрисосудистой мозаичностью морфо-функционального состояния системы гемостаза 4. Наличие особенностей атеро- и тромбогенеза в различных сосудах зависит от механизмов поддержания внутрисосудистой мозаичности морфофункционального состояния системы гемостаза 5. Эффективности антиатеротромботической терапии зависит от учета влияния терапии на особенности механизмов поддержания внутрисосудистой мозаичности морфо-функционального состояния системы гемостаза
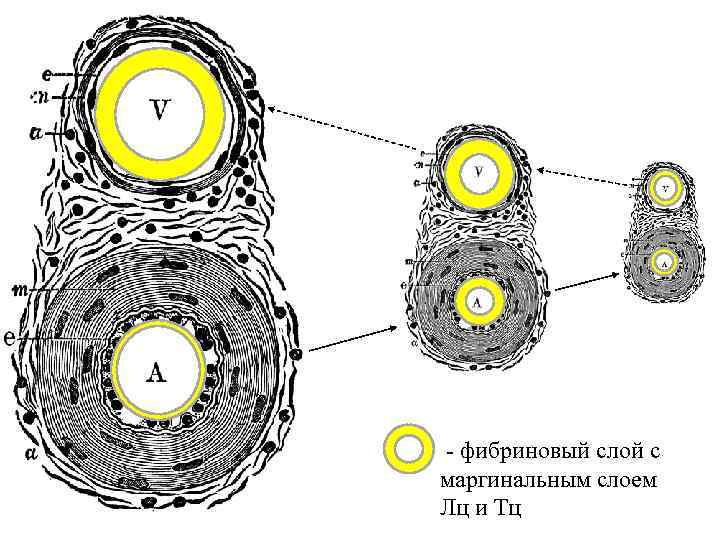 - фибриновый слой с маргинальным слоем Лц и Тц
- фибриновый слой с маргинальным слоем Лц и Тц
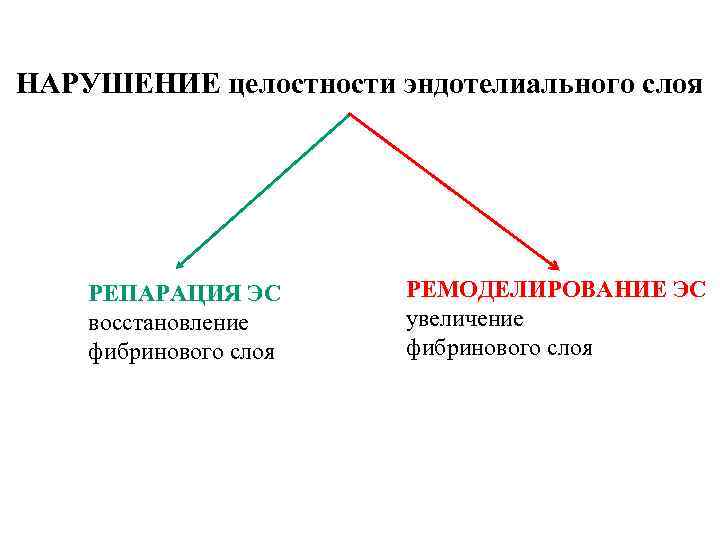 НАРУШЕНИЕ целостности эндотелиального слоя РЕПАРАЦИЯ ЭС восстановление фибринового слоя РЕМОДЕЛИРОВАНИЕ ЭС увеличение фибринового слоя
НАРУШЕНИЕ целостности эндотелиального слоя РЕПАРАЦИЯ ЭС восстановление фибринового слоя РЕМОДЕЛИРОВАНИЕ ЭС увеличение фибринового слоя
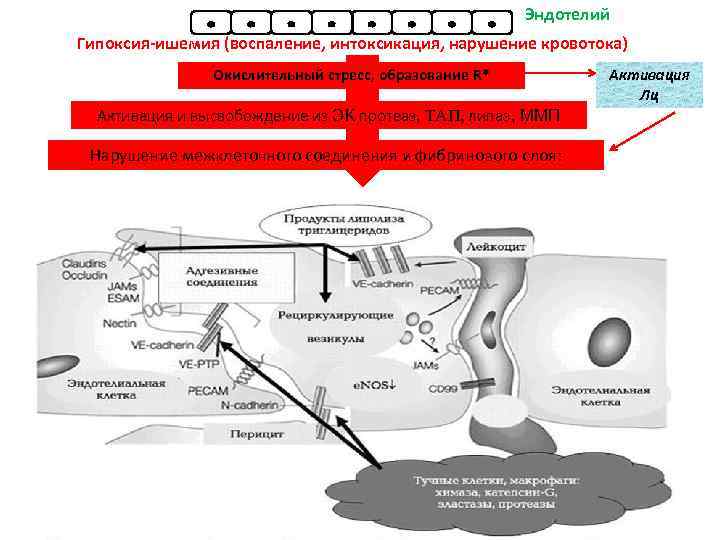 Эндотелий Гипоксия-ишемия (воспаление, интоксикация, нарушение кровотока) Окислительный стресс, образование R* Активация и высвобождение из ЭК протеаз, ТАП, липаз, ММП Нарушение межклеточного соединения и фибринового слоя: Активация Лц
Эндотелий Гипоксия-ишемия (воспаление, интоксикация, нарушение кровотока) Окислительный стресс, образование R* Активация и высвобождение из ЭК протеаз, ТАП, липаз, ММП Нарушение межклеточного соединения и фибринового слоя: Активация Лц
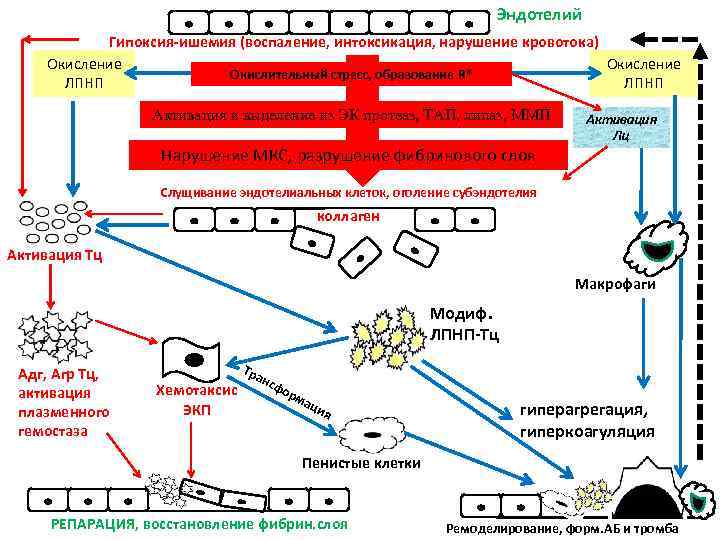 Эндотелий Гипоксия-ишемия (воспаление, интоксикация, нарушение кровотока) Окисление Окислительный стресс, образование R* ЛПНП Активация и выделение из ЭК протеаз, ТАП, липаз, ММП Нарушение МКС, разрушение фибринового слоя Активация Лц Слущивание эндотелиальных клеток, оголение субэндотелия коллаген Активация Тц Макрофаги Модиф. ЛПНП-Тц Адг, Агр Тц, активация плазменного гемостаза Хемотаксис ЭКП Тра н сф ор ма ци я гиперагрегация, гиперкоагуляция Пенистые клетки РЕПАРАЦИЯ, восстановление фибрин. слоя Ремоделирование, форм. АБ и тромба
Эндотелий Гипоксия-ишемия (воспаление, интоксикация, нарушение кровотока) Окисление Окислительный стресс, образование R* ЛПНП Активация и выделение из ЭК протеаз, ТАП, липаз, ММП Нарушение МКС, разрушение фибринового слоя Активация Лц Слущивание эндотелиальных клеток, оголение субэндотелия коллаген Активация Тц Макрофаги Модиф. ЛПНП-Тц Адг, Агр Тц, активация плазменного гемостаза Хемотаксис ЭКП Тра н сф ор ма ци я гиперагрегация, гиперкоагуляция Пенистые клетки РЕПАРАЦИЯ, восстановление фибрин. слоя Ремоделирование, форм. АБ и тромба
 Участие тромбоцитов в формировании тромба
Участие тромбоцитов в формировании тромба
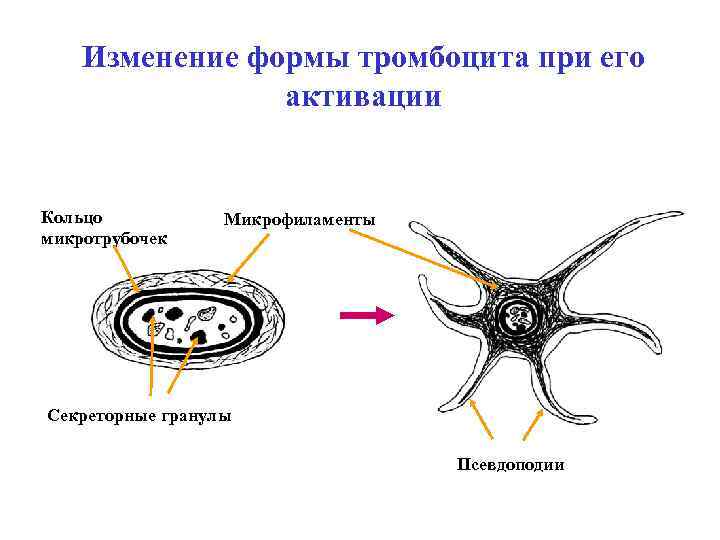 Изменение формы тромбоцита при его активации Кольцо микротрубочек Микрофиламенты Секреторные гранулы Псевдоподии
Изменение формы тромбоцита при его активации Кольцо микротрубочек Микрофиламенты Секреторные гранулы Псевдоподии
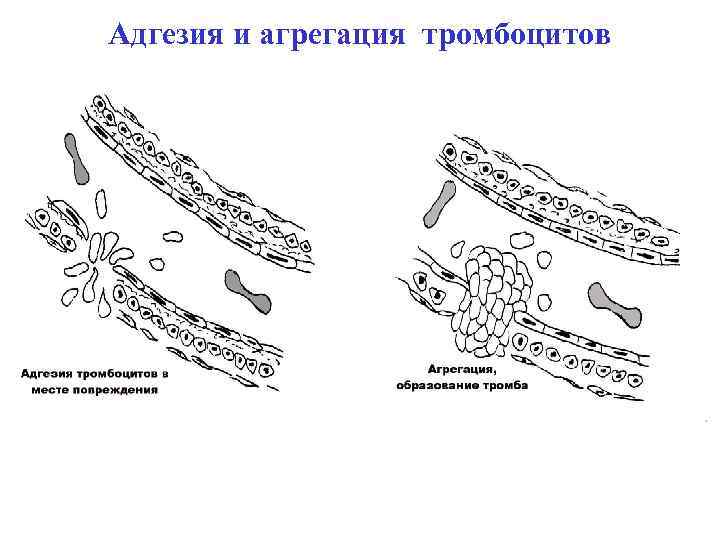 Адгезия и агрегация тромбоцитов
Адгезия и агрегация тромбоцитов
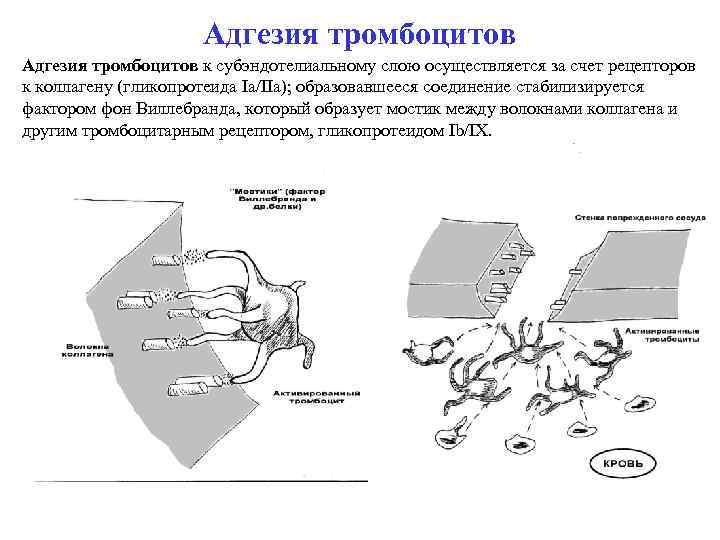 Адгезия тромбоцитов к субэндотелиальному слою осуществляется за счет рецепторов к коллагену (гликопротеида Ia/IIа); образовавшееся соединение стабилизируется фактором фон Виллебранда, который образует мостик между волокнами коллагена и другим тромбоцитарным рецептором, гликопротеидом Ib/IX.
Адгезия тромбоцитов к субэндотелиальному слою осуществляется за счет рецепторов к коллагену (гликопротеида Ia/IIа); образовавшееся соединение стабилизируется фактором фон Виллебранда, который образует мостик между волокнами коллагена и другим тромбоцитарным рецептором, гликопротеидом Ib/IX.
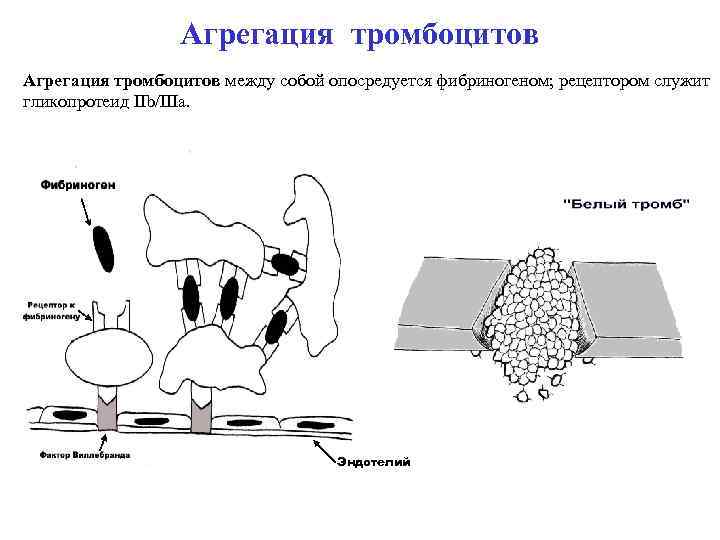 Агрегация тромбоцитов между собой опосредуется фибриногеном; рецептором служит гликопротеид IIb/IIIa. Эндотелий
Агрегация тромбоцитов между собой опосредуется фибриногеном; рецептором служит гликопротеид IIb/IIIa. Эндотелий
 Реакция освобождения (высвобождения) предшествует необратимой агрегации тромбоцитов и приводит к выделению из них индукторов агрегации ( АДФ, серотонин, адреналин, нестабильные простагландины, тромбоксан А 2, тромбоцитоактивирующий фактор ). Наряду со стимуляторами и сигнальными молекулами, попадающими в кровоток из поврежденных тканей и других форменных элементов крови, они вызывают агрегацию других тромбоцитов, которые быстро покидают кровоток и оседают на уже адгезировавших и начавших агрегировать тромбоцитах (хемотаксис).
Реакция освобождения (высвобождения) предшествует необратимой агрегации тромбоцитов и приводит к выделению из них индукторов агрегации ( АДФ, серотонин, адреналин, нестабильные простагландины, тромбоксан А 2, тромбоцитоактивирующий фактор ). Наряду со стимуляторами и сигнальными молекулами, попадающими в кровоток из поврежденных тканей и других форменных элементов крови, они вызывают агрегацию других тромбоцитов, которые быстро покидают кровоток и оседают на уже адгезировавших и начавших агрегировать тромбоцитах (хемотаксис).
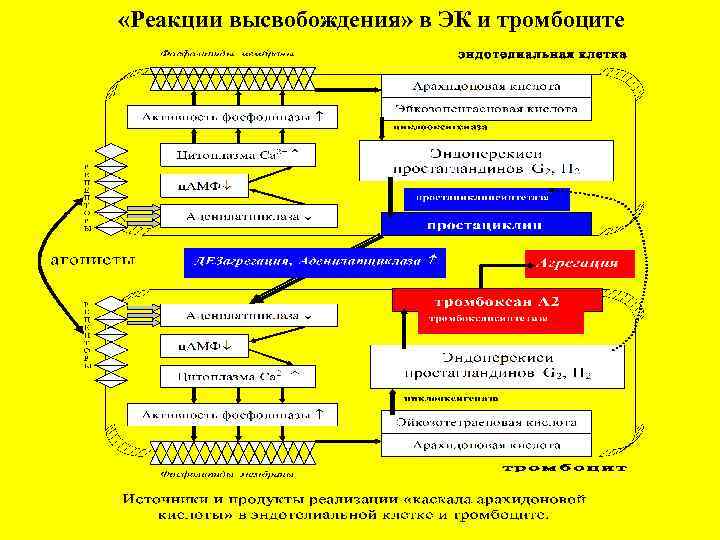 «Реакции высвобождения» в ЭК и тромбоците
«Реакции высвобождения» в ЭК и тромбоците
 • Тромбоциты в больших количествах поглощаются эндотелием, поддерживая таким образом нормальную структуру и и функцию микрососудов, их устойчивость к повреждающим воздействиям, непроницаемость по отношению к эритроцитам. В этом заключается их ангиотрофическая функция. • Поэтому патология тромбоцитов приводит как к различным формам кровоточивости, так и к тромбофилическому состоянию вследствие метаболической недостаточности эндотелиальных клеток.
• Тромбоциты в больших количествах поглощаются эндотелием, поддерживая таким образом нормальную структуру и и функцию микрососудов, их устойчивость к повреждающим воздействиям, непроницаемость по отношению к эритроцитам. В этом заключается их ангиотрофическая функция. • Поэтому патология тромбоцитов приводит как к различным формам кровоточивости, так и к тромбофилическому состоянию вследствие метаболической недостаточности эндотелиальных клеток.
 Врожденные формы кровоточивости, обусловленные нарушениями адгезии тромбоцитов: дефицит гликопротеина Ib мембран тромбоцитов ( болезнь Бернара-Сулье), недоразвитие субэндотелия ( болезнь Рандю-Ослера) и дефицит одного из компонентов комплекса фактора VIII - фактора Виллебранда (болезнь Виллебранда). Кровоточивость в случае врожденной недостаточности гликопротеинов агрегации - болезнь Гланцмана; или фибриногена - афибриногенемия, гипофибриногенемия, дисфибриногенемия.
Врожденные формы кровоточивости, обусловленные нарушениями адгезии тромбоцитов: дефицит гликопротеина Ib мембран тромбоцитов ( болезнь Бернара-Сулье), недоразвитие субэндотелия ( болезнь Рандю-Ослера) и дефицит одного из компонентов комплекса фактора VIII - фактора Виллебранда (болезнь Виллебранда). Кровоточивость в случае врожденной недостаточности гликопротеинов агрегации - болезнь Гланцмана; или фибриногена - афибриногенемия, гипофибриногенемия, дисфибриногенемия.
 Методы исследования сосудисто-тромбоцитарного компонента системы гемостаза 1. in vivo Время кровотечения по Дуке определяется длительность кровотечения из поверхностных микрососудов мочки уха после нарушения их целостности с помощью плоского ланцета или скарификатора. Время кровотечения характеризует функциональную активность тромбоцитов и капилляров и не зависит от процессов свертывания крови. N до 4 минут. 2. in vitro Подсчет количества тромбоцитов 3. in vitro Оценка ретенции тромбоцитов на стекле ИР –индекс ретенции А – количество тромбоцитов до фильтрования, В – то же после фильтрования. 4. in vitro Оценка агрегационной активности тромбоцитов с различными концентрациями индуктора и с разными индукторами агрегации
Методы исследования сосудисто-тромбоцитарного компонента системы гемостаза 1. in vivo Время кровотечения по Дуке определяется длительность кровотечения из поверхностных микрососудов мочки уха после нарушения их целостности с помощью плоского ланцета или скарификатора. Время кровотечения характеризует функциональную активность тромбоцитов и капилляров и не зависит от процессов свертывания крови. N до 4 минут. 2. in vitro Подсчет количества тромбоцитов 3. in vitro Оценка ретенции тромбоцитов на стекле ИР –индекс ретенции А – количество тромбоцитов до фильтрования, В – то же после фильтрования. 4. in vitro Оценка агрегационной активности тромбоцитов с различными концентрациями индуктора и с разными индукторами агрегации
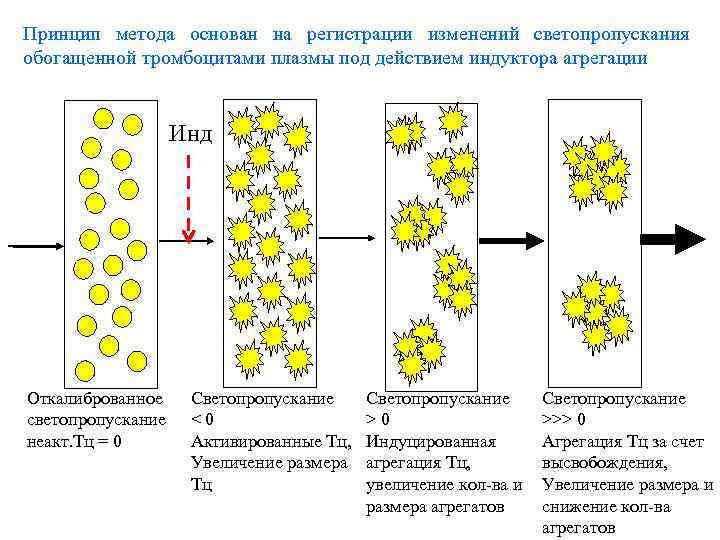 Принцип метода основан на регистрации изменений светопропускания обогащенной тромбоцитами плазмы под действием индуктора агрегации Инд Откалиброванное светопропускание неакт. Тц = 0 Светопропускание < 0 Активированные Тц, Увеличение размера Тц Светопропускание > 0 Индуцированная агрегация Тц, увеличение кол-ва и размера агрегатов Светопропускание >>> 0 Агрегация Тц за счет высвобождения, Увеличение размера и снижение кол-ва агрегатов
Принцип метода основан на регистрации изменений светопропускания обогащенной тромбоцитами плазмы под действием индуктора агрегации Инд Откалиброванное светопропускание неакт. Тц = 0 Светопропускание < 0 Активированные Тц, Увеличение размера Тц Светопропускание > 0 Индуцированная агрегация Тц, увеличение кол-ва и размера агрегатов Светопропускание >>> 0 Агрегация Тц за счет высвобождения, Увеличение размера и снижение кол-ва агрегатов
 ТИПОВЫЕ АГРЕГАТОГРАММЫ
ТИПОВЫЕ АГРЕГАТОГРАММЫ
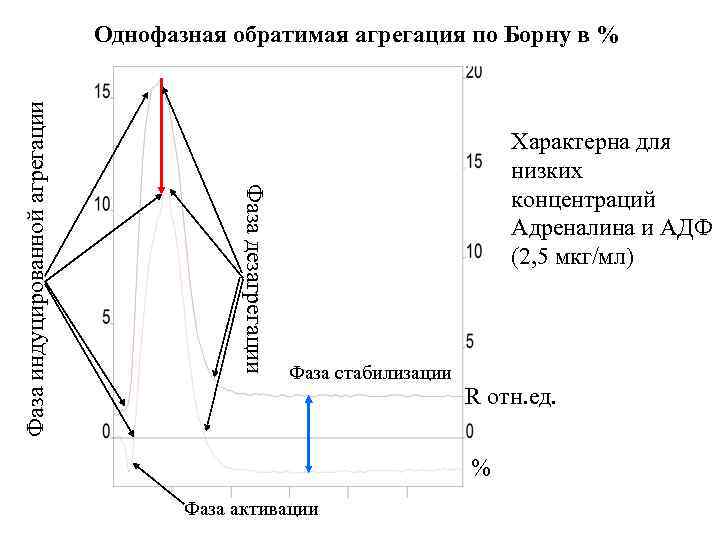 Фаза дезагрегации Фаза индуцированной агрегации Однофазная обратимая агрегация по Борну в % Характерна для низких концентраций Адреналина и АДФ (2, 5 мкг/мл) Фаза стабилизации R отн. ед. % Фаза активации
Фаза дезагрегации Фаза индуцированной агрегации Однофазная обратимая агрегация по Борну в % Характерна для низких концентраций Адреналина и АДФ (2, 5 мкг/мл) Фаза стабилизации R отн. ед. % Фаза активации
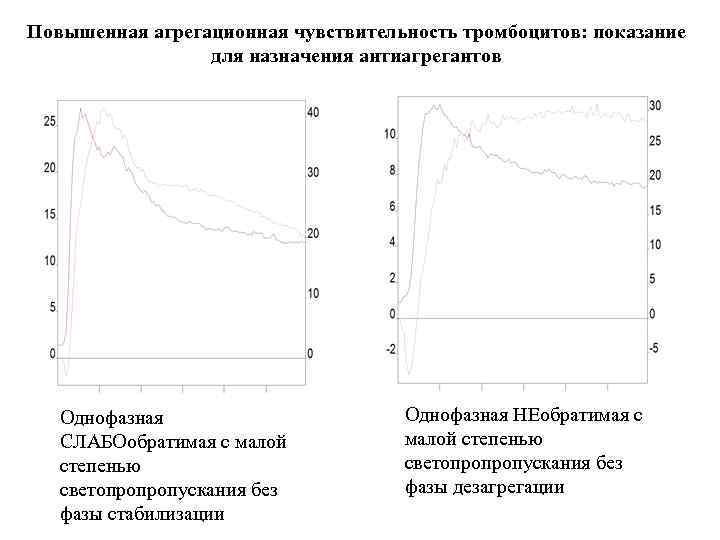 Повышенная агрегационная чувствительность тромбоцитов: показание для назначения антиагрегантов Однофазная СЛАБОобратимая с малой степенью светопропропускания без фазы стабилизации Однофазная НЕобратимая с малой степенью светопропропускания без фазы дезагрегации
Повышенная агрегационная чувствительность тромбоцитов: показание для назначения антиагрегантов Однофазная СЛАБОобратимая с малой степенью светопропропускания без фазы стабилизации Однофазная НЕобратимая с малой степенью светопропропускания без фазы дезагрегации
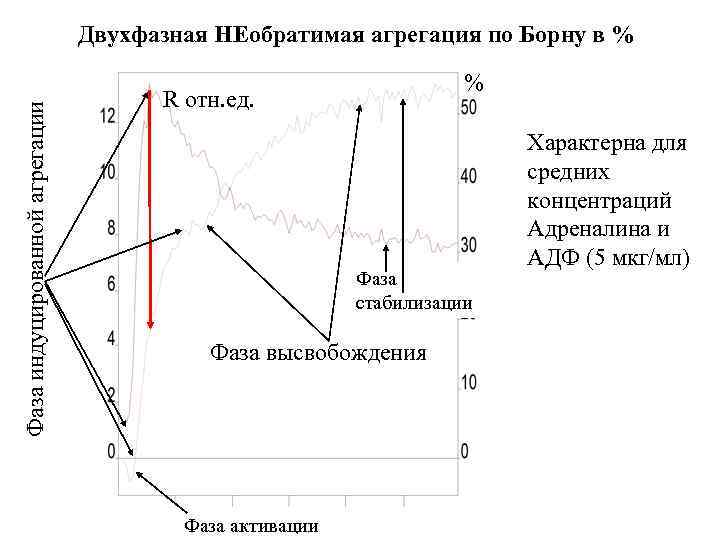 Фаза индуцированной агрегации Двухфазная НЕобратимая агрегация по Борну в % % R отн. ед. Фаза стабилизации Фаза высвобождения Фаза активации Характерна для средних концентраций Адреналина и АДФ (5 мкг/мл)
Фаза индуцированной агрегации Двухфазная НЕобратимая агрегация по Борну в % % R отн. ед. Фаза стабилизации Фаза высвобождения Фаза активации Характерна для средних концентраций Адреналина и АДФ (5 мкг/мл)
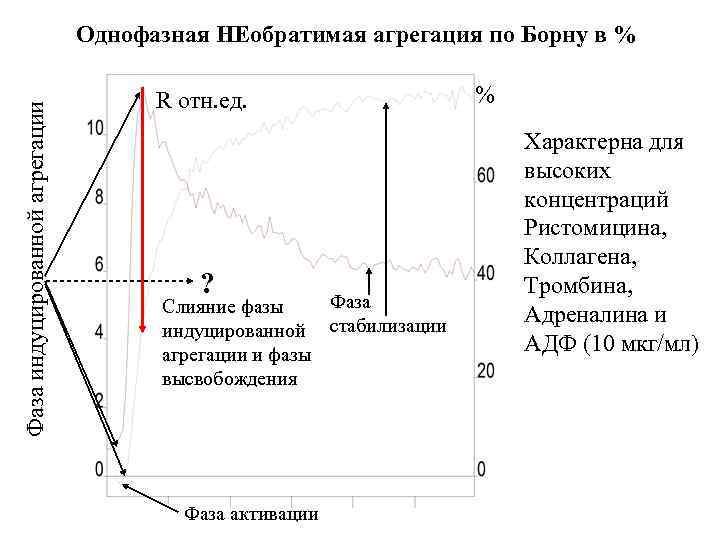 Фаза индуцированной агрегации Однофазная НЕобратимая агрегация по Борну в % R отн. ед. ? Фаза Слияние фазы индуцированной стабилизации агрегации и фазы высвобождения Фаза активации % Характерна для высоких концентраций Ристомицина, Коллагена, Тромбина, Адреналина и АДФ (10 мкг/мл)
Фаза индуцированной агрегации Однофазная НЕобратимая агрегация по Борну в % R отн. ед. ? Фаза Слияние фазы индуцированной стабилизации агрегации и фазы высвобождения Фаза активации % Характерна для высоких концентраций Ристомицина, Коллагена, Тромбина, Адреналина и АДФ (10 мкг/мл)
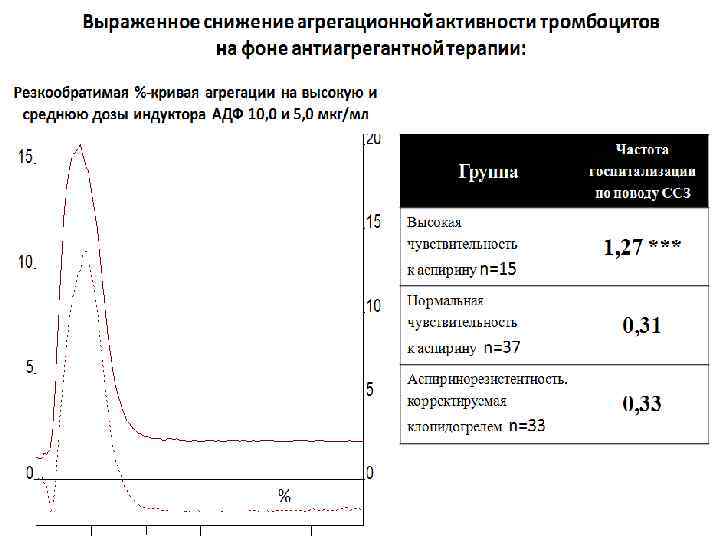
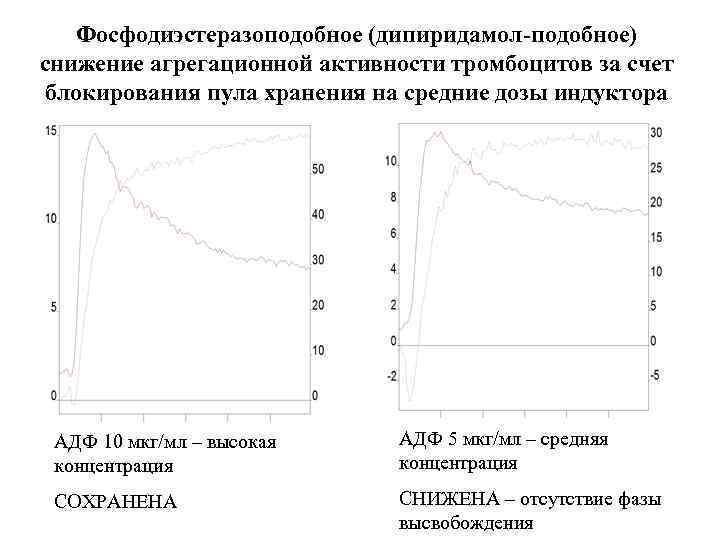 Фосфодиэстеразоподобное (дипиридамол-подобное) снижение агрегационной активности тромбоцитов за счет блокирования пула хранения на средние дозы индуктора АДФ 10 мкг/мл – высокая концентрация АДФ 5 мкг/мл – средняя концентрация СОХРАНЕНА СНИЖЕНА – отсутствие фазы высвобождения
Фосфодиэстеразоподобное (дипиридамол-подобное) снижение агрегационной активности тромбоцитов за счет блокирования пула хранения на средние дозы индуктора АДФ 10 мкг/мл – высокая концентрация АДФ 5 мкг/мл – средняя концентрация СОХРАНЕНА СНИЖЕНА – отсутствие фазы высвобождения
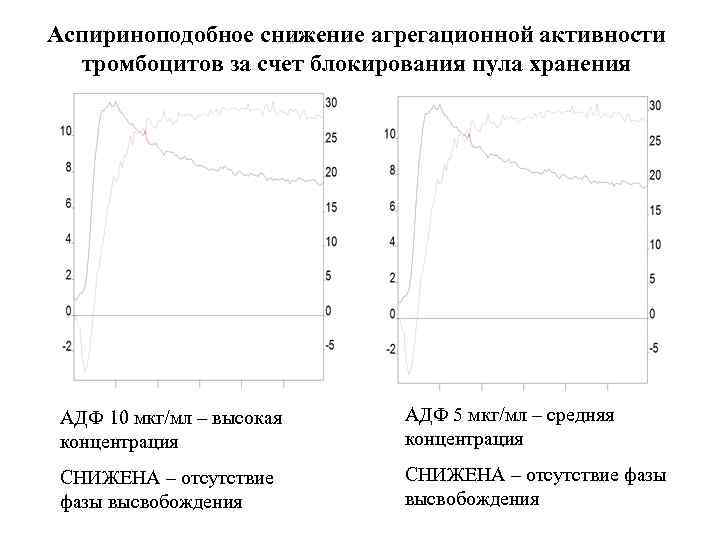 Аспириноподобное снижение агрегационной активности тромбоцитов за счет блокирования пула хранения АДФ 10 мкг/мл – высокая концентрация АДФ 5 мкг/мл – средняя концентрация СНИЖЕНА – отсутствие фазы высвобождения
Аспириноподобное снижение агрегационной активности тромбоцитов за счет блокирования пула хранения АДФ 10 мкг/мл – высокая концентрация АДФ 5 мкг/мл – средняя концентрация СНИЖЕНА – отсутствие фазы высвобождения
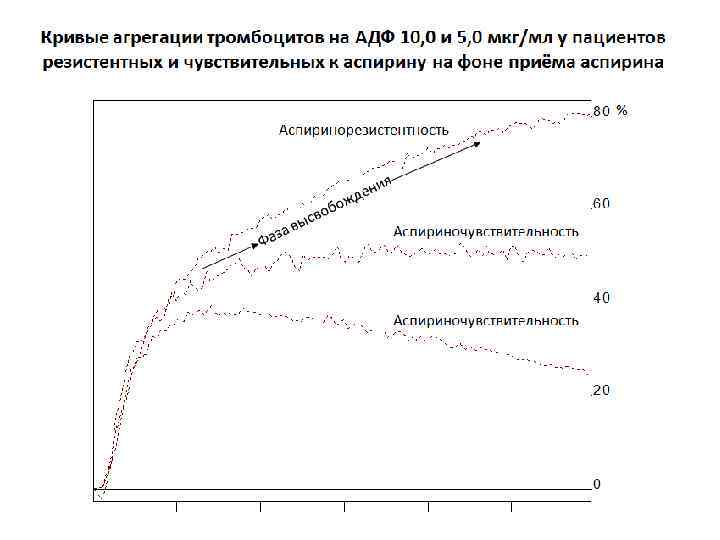
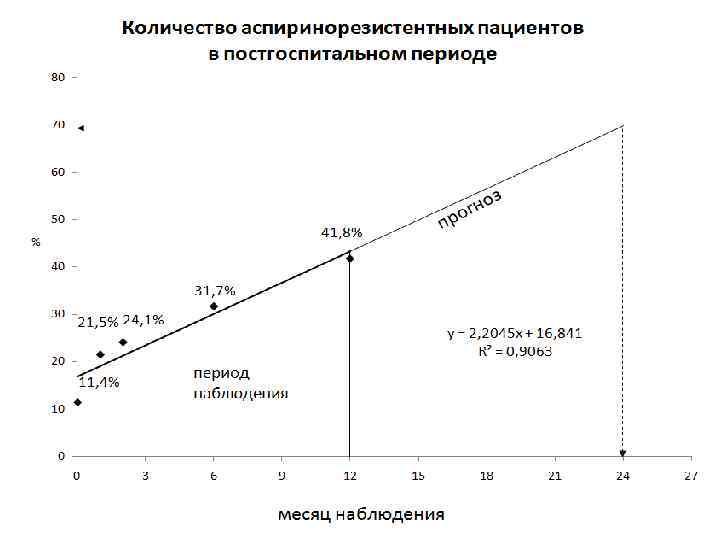
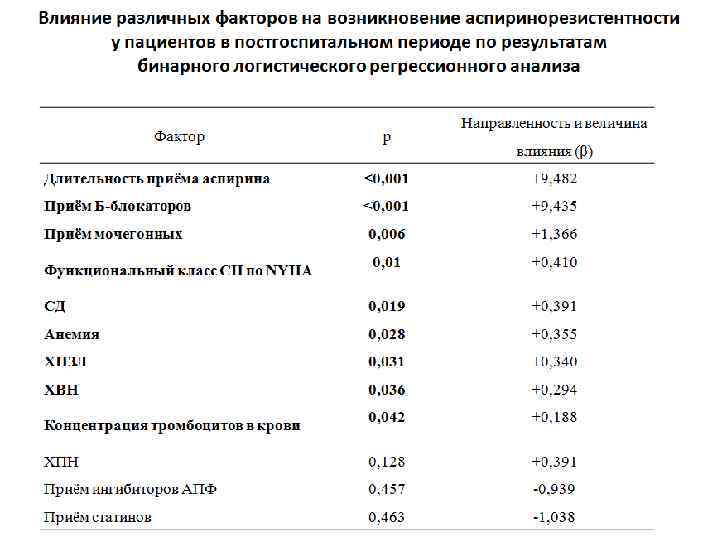
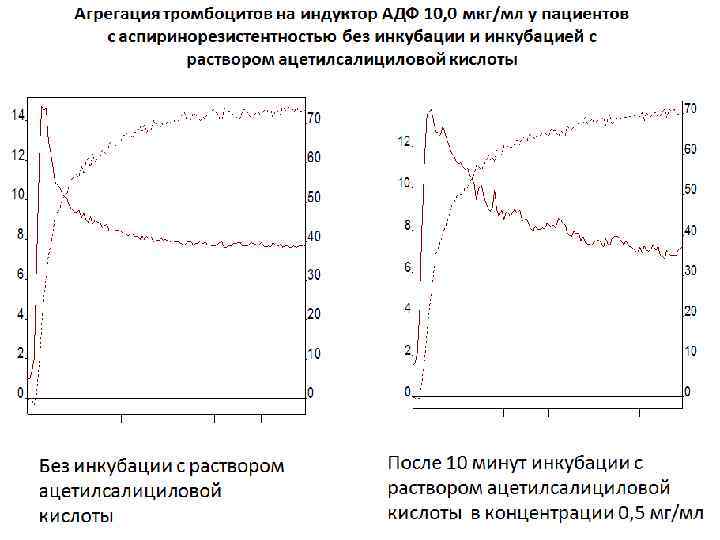
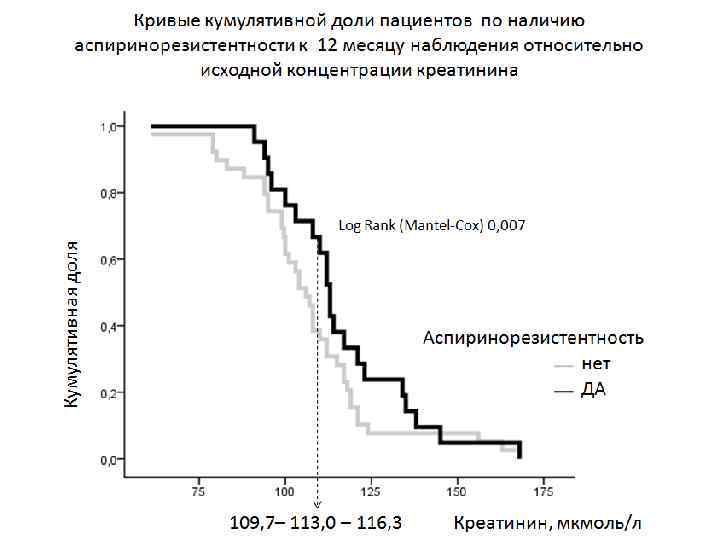
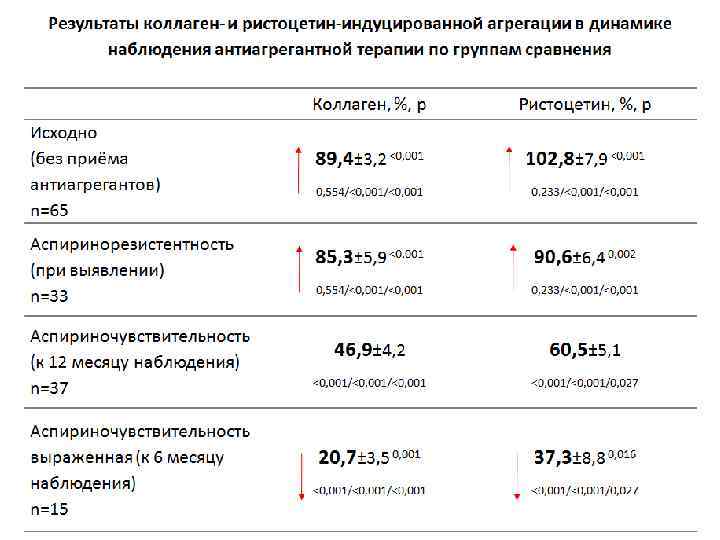
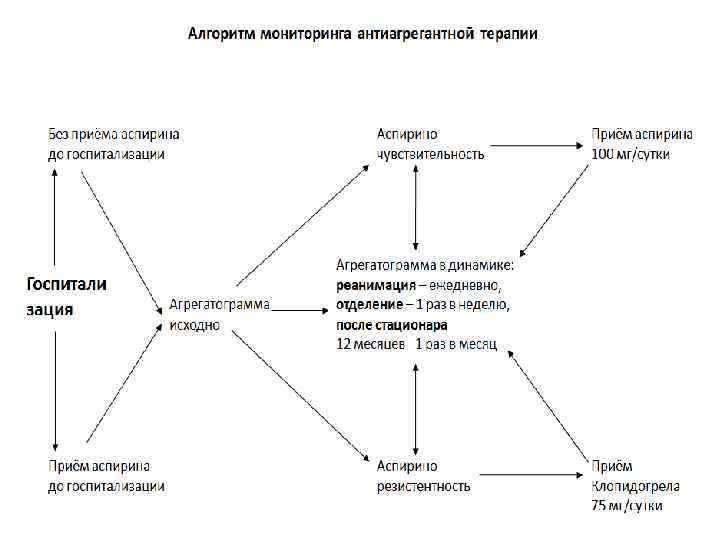
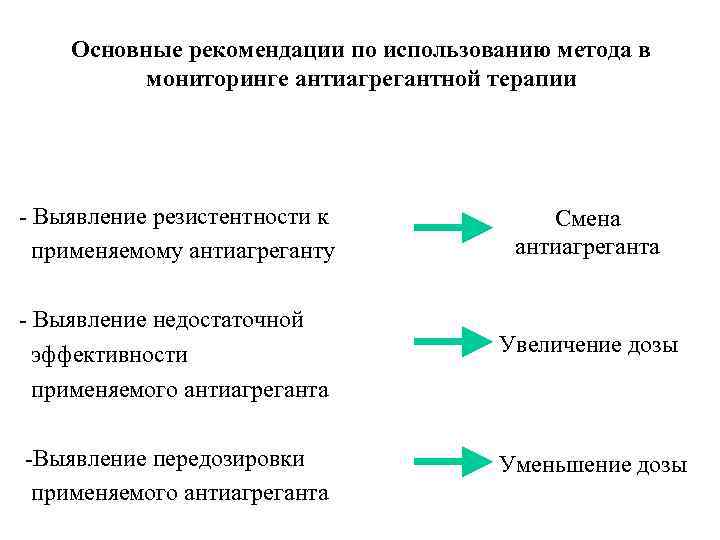 Основные рекомендации по использованию метода в мониторинге антиагрегантной терапии - Выявление резистентности к применяемому антиагреганту Смена антиагреганта - Выявление недостаточной эффективности применяемого антиагреганта Увеличение дозы -Выявление передозировки применяемого антиагреганта Уменьшение дозы
Основные рекомендации по использованию метода в мониторинге антиагрегантной терапии - Выявление резистентности к применяемому антиагреганту Смена антиагреганта - Выявление недостаточной эффективности применяемого антиагреганта Увеличение дозы -Выявление передозировки применяемого антиагреганта Уменьшение дозы
 Сосудисто-тромбоцитарный и плазменный (вторичный, окончательный) коагуляционный гемостаз тесно связаны друг с другом. Так, активированные тромбоциты ускоряют процесс свертывания, а продукты свертывания (например, тромбин) активируют тромбоциты. 2. Плазменный гемостаз многоэтапный ферментативный процесс, в котором учавствует ряд белков – протеаз, ионы кальция, а также неферментные белкиакцелераторы, обеспечивающие взаимодействие факторов свертывания на фосфолипидных матрицах, конечным результатом которого является образование нерастворимого фибринового сгустка 2. 1 Многоступенчатый этап условно состоящий из 2 путей «внутреннего» и «внешнего» , приводящий к активации протромбина и превращения его в активный фермент – тромбин 2. 2 Конечный этап, в котором под влиянием тромбина из фибриногена образуется фибрин
Сосудисто-тромбоцитарный и плазменный (вторичный, окончательный) коагуляционный гемостаз тесно связаны друг с другом. Так, активированные тромбоциты ускоряют процесс свертывания, а продукты свертывания (например, тромбин) активируют тромбоциты. 2. Плазменный гемостаз многоэтапный ферментативный процесс, в котором учавствует ряд белков – протеаз, ионы кальция, а также неферментные белкиакцелераторы, обеспечивающие взаимодействие факторов свертывания на фосфолипидных матрицах, конечным результатом которого является образование нерастворимого фибринового сгустка 2. 1 Многоступенчатый этап условно состоящий из 2 путей «внутреннего» и «внешнего» , приводящий к активации протромбина и превращения его в активный фермент – тромбин 2. 2 Конечный этап, в котором под влиянием тромбина из фибриногена образуется фибрин
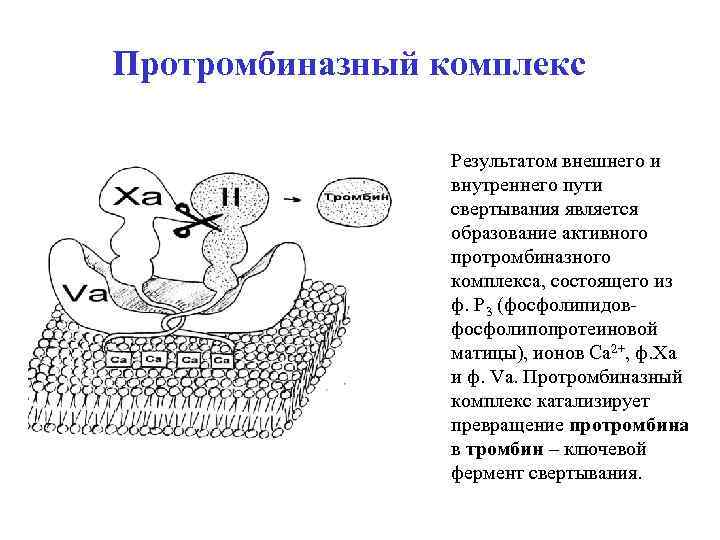 Протромбиназный комплекс Результатом внешнего и внутреннего пути свертывания является образование активного протромбиназного комплекса, состоящего из ф. Р 3 (фосфолипидовфосфолипопротеиновой матицы), ионов Са 2+, ф. Ха и ф. Va. Протромбиназный комплекс катализирует превращение протромбина в тромбин – ключевой фермент свертывания.
Протромбиназный комплекс Результатом внешнего и внутреннего пути свертывания является образование активного протромбиназного комплекса, состоящего из ф. Р 3 (фосфолипидовфосфолипопротеиновой матицы), ионов Са 2+, ф. Ха и ф. Va. Протромбиназный комплекс катализирует превращение протромбина в тромбин – ключевой фермент свертывания.
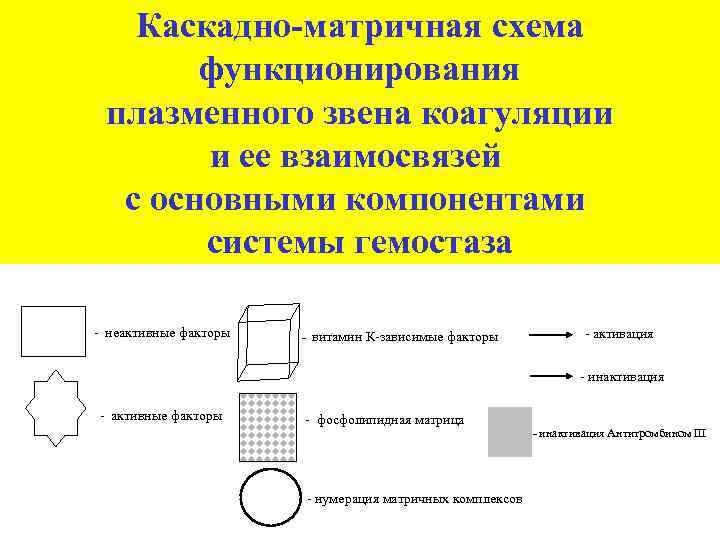 Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активация - инактивация - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - инактивация Антитромбином III
Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активация - инактивация - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - инактивация Антитромбином III
 Внутренний путь образования протромбиназы
Внутренний путь образования протромбиназы
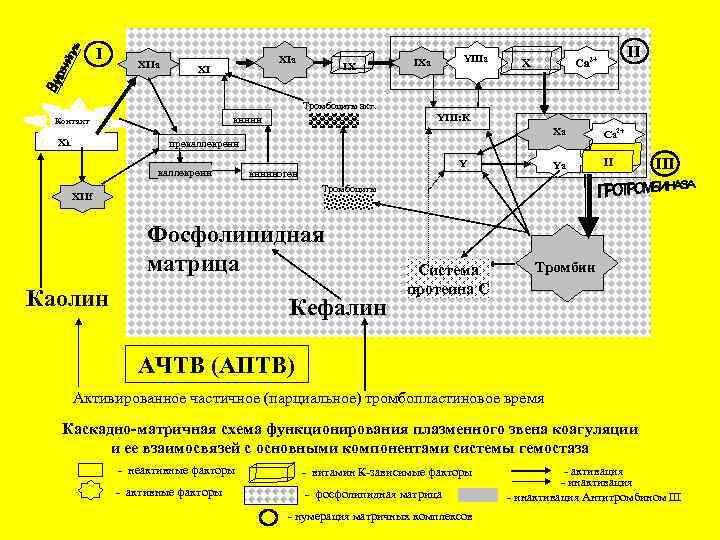 I XIIa XI IX YIIIa IXa II Ca 2+ X Тромбоциты акт. XII YIII: K кинин Контакт Xa Са 2+ Ya II прекаллекреин Y кининоген III Тромбоциты XIIf Фосфолипидная матрица Каолин Кефалин Система протеина С Тромбин АЧТВ (АПТВ) Активированное частичное (парциальное) тромбопластиновое время Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
I XIIa XI IX YIIIa IXa II Ca 2+ X Тромбоциты акт. XII YIII: K кинин Контакт Xa Са 2+ Ya II прекаллекреин Y кининоген III Тромбоциты XIIf Фосфолипидная матрица Каолин Кефалин Система протеина С Тромбин АЧТВ (АПТВ) Активированное частичное (парциальное) тромбопластиновое время Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
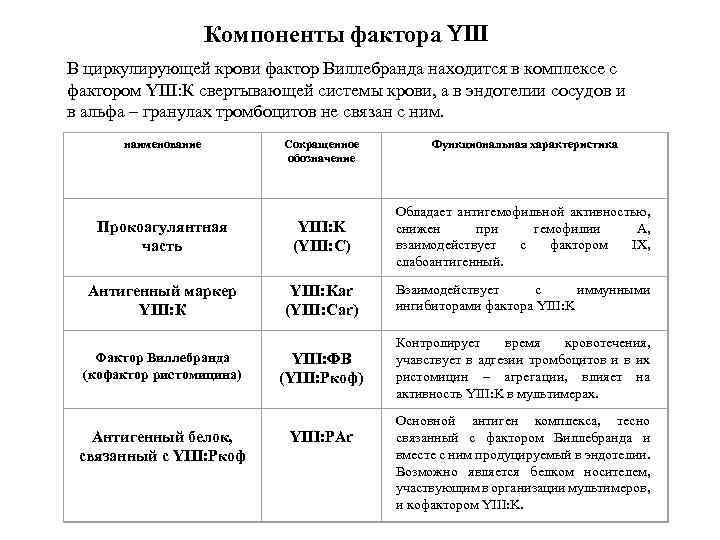 Компоненты фактора В циркулирующей крови фактор Виллебранда находится в комплексе с фактором YIII: К свертывающей системы крови, а в эндотелии сосудов и в альфа – гранулах тромбоцитов не связан с ним. наименование Сокращенное обозначение Функциональная характеристика Прокоагулянтная часть YIII: K (YIII: C) Обладает антигемофильной активностью, снижен при гемофилии А, взаимодействует с фактором IX, слабоантигенный. Антигенный маркер YIII: К YIII: Kar (YIII: Car) Взаимодействует с иммунными ингибиторами фактора YIII: K Фактор Виллебранда (кофактор ристомицина) YIII: ФВ (YIII: Pкоф) Контролирует время кровотечения, учавствует в адгезии тромбоцитов и в их ристомицин – агрегации, влияет на активность YIII: K в мультимерах. Антигенный белок, связанный с YIII: Ркоф YIII: PAr Основной антиген комплекса, тесно связанный с фактором Виллебранда и вместе с ним продуцируемый в эндотелии. Возможно является белком носителем, участвующим в организации мультимеров, и кофактором YIII: K.
Компоненты фактора В циркулирующей крови фактор Виллебранда находится в комплексе с фактором YIII: К свертывающей системы крови, а в эндотелии сосудов и в альфа – гранулах тромбоцитов не связан с ним. наименование Сокращенное обозначение Функциональная характеристика Прокоагулянтная часть YIII: K (YIII: C) Обладает антигемофильной активностью, снижен при гемофилии А, взаимодействует с фактором IX, слабоантигенный. Антигенный маркер YIII: К YIII: Kar (YIII: Car) Взаимодействует с иммунными ингибиторами фактора YIII: K Фактор Виллебранда (кофактор ристомицина) YIII: ФВ (YIII: Pкоф) Контролирует время кровотечения, учавствует в адгезии тромбоцитов и в их ристомицин – агрегации, влияет на активность YIII: K в мультимерах. Антигенный белок, связанный с YIII: Ркоф YIII: PAr Основной антиген комплекса, тесно связанный с фактором Виллебранда и вместе с ним продуцируемый в эндотелии. Возможно является белком носителем, участвующим в организации мультимеров, и кофактором YIII: K.
 Внешний путь образования протромбиназы
Внешний путь образования протромбиназы
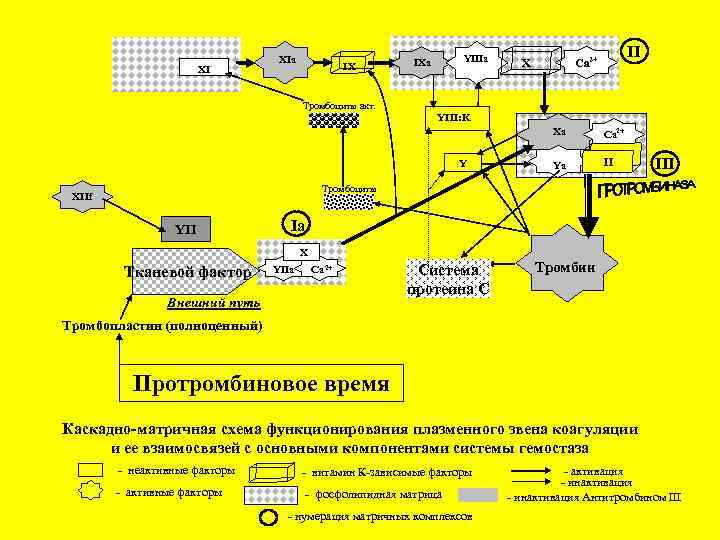 XI XIa IX Тромбоциты акт. YIIIa IXa II Ca 2+ X YIII: K Xa Y Са 2+ Ya II III Тромбоциты XIIf YII Ia X Тканевой фактор YIIa Ca 2+ Внешний путь Система протеина С Тромбин Тромбопластин (полноценный) Протромбиновое время Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
XI XIa IX Тромбоциты акт. YIIIa IXa II Ca 2+ X YIII: K Xa Y Са 2+ Ya II III Тромбоциты XIIf YII Ia X Тканевой фактор YIIa Ca 2+ Внешний путь Система протеина С Тромбин Тромбопластин (полноценный) Протромбиновое время Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
 Способы выражения протромбинового времени (ПВ) 1. ПВ в секундах 2. Протромбиновый индекс: (N 80 -120%) 3. ПВ по Квику (активность факторов протромбинового комплекса по кривой разведения донорской плазмы) N 70 -110 % 4. Протромбиновое отношение: (N 0. 8 -1. 2) 5. Международное Нормализованное Отношение: N 0. 9 -1. 3 МИЧ
Способы выражения протромбинового времени (ПВ) 1. ПВ в секундах 2. Протромбиновый индекс: (N 80 -120%) 3. ПВ по Квику (активность факторов протромбинового комплекса по кривой разведения донорской плазмы) N 70 -110 % 4. Протромбиновое отношение: (N 0. 8 -1. 2) 5. Международное Нормализованное Отношение: N 0. 9 -1. 3 МИЧ
 Конечный этап – образование фибрина
Конечный этап – образование фибрина
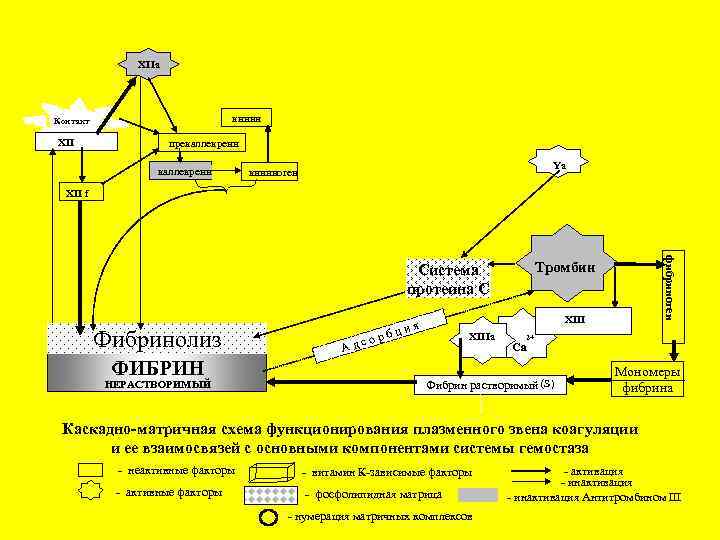 XIIa кинин Контакт XII прекаллекреин Ya кининоген XII f Фибринолиз ФИБРИН НЕРАСТВОРИМЫЙ фибриноген Тромбин Система протеина С XIII я ц и о р б XIIIa с А д 2+ Ca Фибрин растворимый (S) Мономеры фибрина Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
XIIa кинин Контакт XII прекаллекреин Ya кининоген XII f Фибринолиз ФИБРИН НЕРАСТВОРИМЫЙ фибриноген Тромбин Система протеина С XIII я ц и о р б XIIIa с А д 2+ Ca Фибрин растворимый (S) Мономеры фибрина Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
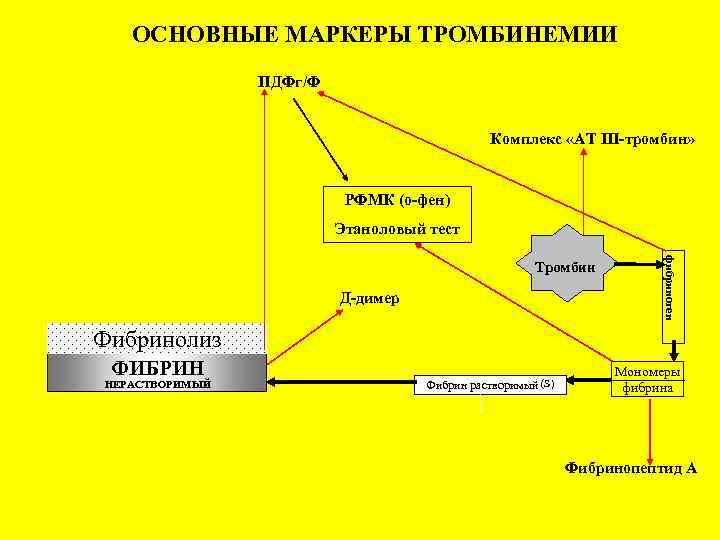 ОСНОВНЫЕ МАРКЕРЫ ТРОМБИНЕМИИ ПДФг/Ф Комплекс «АТ III-тромбин» РФМК (о-фен) Этаноловый тест Д-димер фибриноген Тромбин Фибринолиз ФИБРИН НЕРАСТВОРИМЫЙ Фибрин растворимый (S) Мономеры фибрина Фибринопептид А
ОСНОВНЫЕ МАРКЕРЫ ТРОМБИНЕМИИ ПДФг/Ф Комплекс «АТ III-тромбин» РФМК (о-фен) Этаноловый тест Д-димер фибриноген Тромбин Фибринолиз ФИБРИН НЕРАСТВОРИМЫЙ Фибрин растворимый (S) Мономеры фибрина Фибринопептид А
 ОБЩАЯ СХЕМА ПЛАЗМЕННОЙ КОАГУЛЯЦИИ
ОБЩАЯ СХЕМА ПЛАЗМЕННОЙ КОАГУЛЯЦИИ
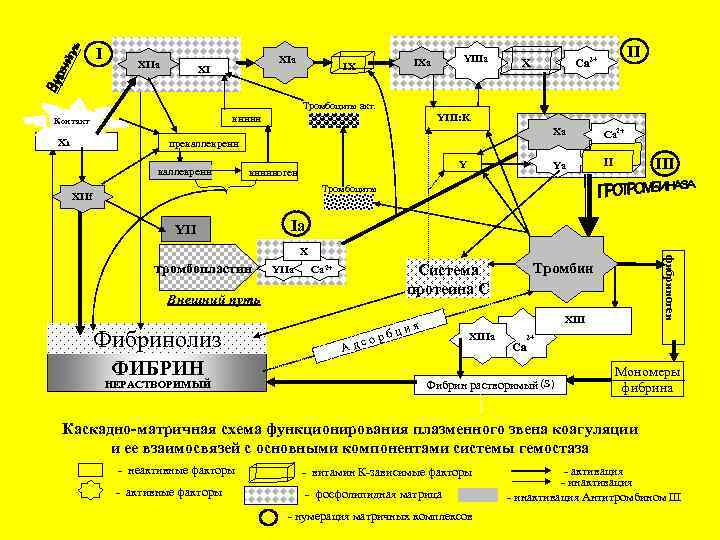 I XIIa XI Тромбоциты акт. XII Xa Y кининоген Са 2+ Ya прекаллекреин II Ca 2+ X YIII: K кинин Контакт YIIIa IX II III Тромбоциты XIIf YII Ia тромбопластин YIIa Внешний путь Фибринолиз ФИБРИН НЕРАСТВОРИМЫЙ Тромбин Система протеина С Ca 2+ фибриноген X XIII я ц и о р б XIIIa с А д 2+ Ca Фибрин растворимый (S) Мономеры фибрина Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
I XIIa XI Тромбоциты акт. XII Xa Y кининоген Са 2+ Ya прекаллекреин II Ca 2+ X YIII: K кинин Контакт YIIIa IX II III Тромбоциты XIIf YII Ia тромбопластин YIIa Внешний путь Фибринолиз ФИБРИН НЕРАСТВОРИМЫЙ Тромбин Система протеина С Ca 2+ фибриноген X XIII я ц и о р б XIIIa с А д 2+ Ca Фибрин растворимый (S) Мономеры фибрина Каскадно-матричная схема функционирования плазменного звена коагуляции и ее взаимосвязей с основными компонентами системы гемостаза - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - нумерация матричных комплексов - активация - инактивация Антитромбином III
 Естественные антикоагулянты (АК)
Естественные антикоагулянты (АК)
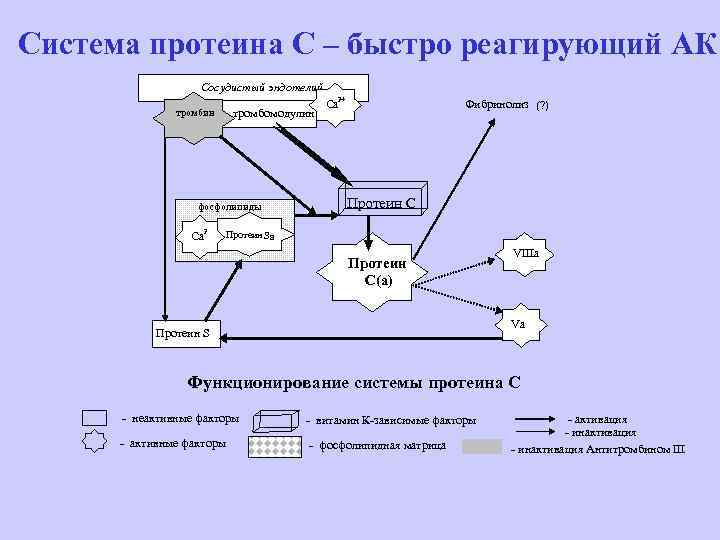 Система протеина С – быстро реагирующий АК Сосудистый эндотелий тромбин тромбомодулин фосфолипиды Са 2+ Фибринолиз (? ) Протеин С Протеин S а Протеин С(а) VIIIa Va Протеин S Функционирование системы протеина С - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - активация - инактивация Антитромбином III
Система протеина С – быстро реагирующий АК Сосудистый эндотелий тромбин тромбомодулин фосфолипиды Са 2+ Фибринолиз (? ) Протеин С Протеин S а Протеин С(а) VIIIa Va Протеин S Функционирование системы протеина С - неактивные факторы - витамин К-зависимые факторы - активные факторы - фосфолипидная матрица - активация - инактивация Антитромбином III
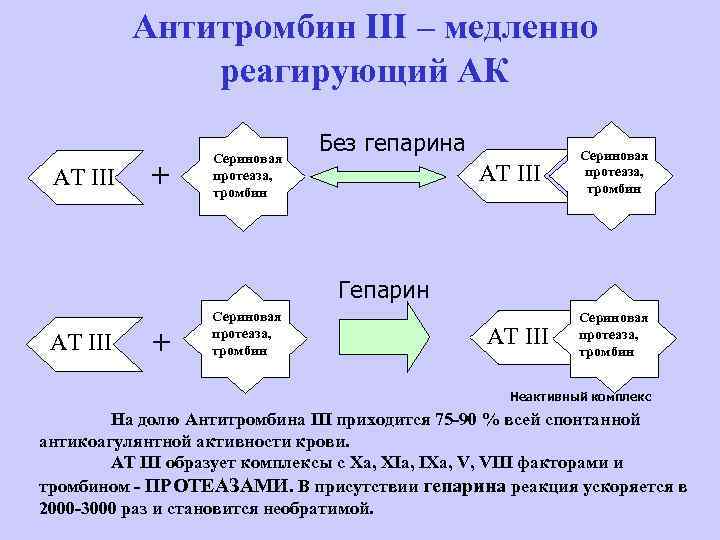 Антитромбин III – медленно реагирующий АК АТ III + Сериновая протеаза, тромбин Без гепарина АТ III Сериновая протеаза, тромбин Гепарин АТ III + Сериновая протеаза, тромбин АТ III Сериновая протеаза, тромбин Неактивный комплекс На долю Антитромбина III приходится 75 -90 % всей спонтанной антикоагулянтной активности крови. АТ III образует комплексы с Ха, ХIa, IXa, V, VIII факторами и тромбином - ПРОТЕАЗАМИ. В присутствии гепарина реакция ускоряется в 2000 -3000 раз и становится необратимой.
Антитромбин III – медленно реагирующий АК АТ III + Сериновая протеаза, тромбин Без гепарина АТ III Сериновая протеаза, тромбин Гепарин АТ III + Сериновая протеаза, тромбин АТ III Сериновая протеаза, тромбин Неактивный комплекс На долю Антитромбина III приходится 75 -90 % всей спонтанной антикоагулянтной активности крови. АТ III образует комплексы с Ха, ХIa, IXa, V, VIII факторами и тромбином - ПРОТЕАЗАМИ. В присутствии гепарина реакция ускоряется в 2000 -3000 раз и становится необратимой.
 Фибринолиз и антифибринолиз
Фибринолиз и антифибринолиз
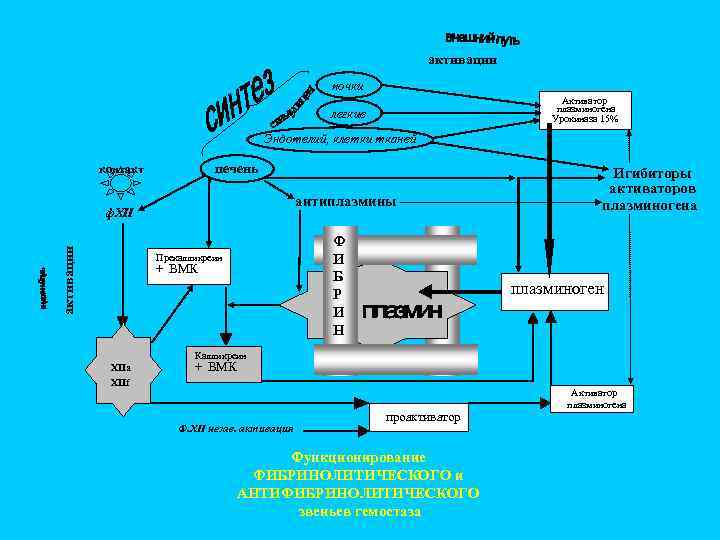 активации почки Активатор плазминогена Урокиназа 15% легкие Эндотелий, клетки тканей печень контакт антиплазмины активации ф. XII Ф И Б Р И Н Прекалликреин + ВМК Игибиторы активаторов плазминогена плазминоген Калликреин XIIa XIIf + ВМК Ф. XII незав. активация проактиватор Функционирование ФИБРИНОЛИТИЧЕСКОГО и АНТИФИБРИНОЛИТИЧЕСКОГО звеньев гемостаза Активатор плазминогена
активации почки Активатор плазминогена Урокиназа 15% легкие Эндотелий, клетки тканей печень контакт антиплазмины активации ф. XII Ф И Б Р И Н Прекалликреин + ВМК Игибиторы активаторов плазминогена плазминоген Калликреин XIIa XIIf + ВМК Ф. XII незав. активация проактиватор Функционирование ФИБРИНОЛИТИЧЕСКОГО и АНТИФИБРИНОЛИТИЧЕСКОГО звеньев гемостаза Активатор плазминогена
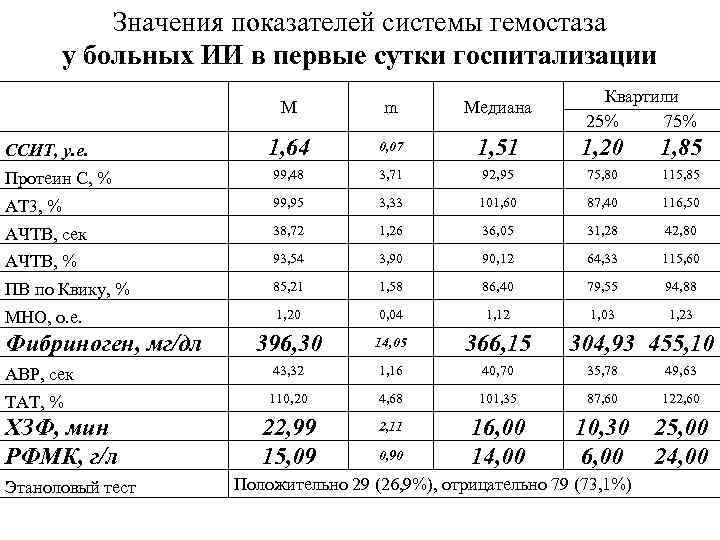 Значения показателей системы гемостаза у больных ИИ в первые сутки госпитализации Квартили 25% 75% M m Медиана 1, 64 0, 07 1, 51 1, 20 1, 85 Протеин С, % 99, 48 3, 71 92, 95 75, 80 115, 85 АТ 3, % 99, 95 3, 33 101, 60 87, 40 116, 50 АЧТВ, сек 38, 72 1, 26 36, 05 31, 28 42, 80 АЧТВ, % 93, 54 3, 90 90, 12 64, 33 115, 60 ПВ по Квику, % 85, 21 1, 58 86, 40 79, 55 94, 88 МНО, о. е. 1, 20 0, 04 1, 12 1, 03 1, 23 396, 30 14, 05 366, 15 АВР, сек 43, 32 1, 16 40, 70 35, 78 49, 63 ТАТ, % 110, 20 4, 68 101, 35 87, 60 122, 60 22, 99 15, 09 2, 11 16, 00 14, 00 10, 30 6, 00 25, 00 24, 00 ССИТ, у. е. Фибриноген, мг/дл ХЗФ, мин РФМК, г/л Этаноловый тест 0, 90 304, 93 455, 10 Положительно 29 (26, 9%), отрицательно 79 (73, 1%)
Значения показателей системы гемостаза у больных ИИ в первые сутки госпитализации Квартили 25% 75% M m Медиана 1, 64 0, 07 1, 51 1, 20 1, 85 Протеин С, % 99, 48 3, 71 92, 95 75, 80 115, 85 АТ 3, % 99, 95 3, 33 101, 60 87, 40 116, 50 АЧТВ, сек 38, 72 1, 26 36, 05 31, 28 42, 80 АЧТВ, % 93, 54 3, 90 90, 12 64, 33 115, 60 ПВ по Квику, % 85, 21 1, 58 86, 40 79, 55 94, 88 МНО, о. е. 1, 20 0, 04 1, 12 1, 03 1, 23 396, 30 14, 05 366, 15 АВР, сек 43, 32 1, 16 40, 70 35, 78 49, 63 ТАТ, % 110, 20 4, 68 101, 35 87, 60 122, 60 22, 99 15, 09 2, 11 16, 00 14, 00 10, 30 6, 00 25, 00 24, 00 ССИТ, у. е. Фибриноген, мг/дл ХЗФ, мин РФМК, г/л Этаноловый тест 0, 90 304, 93 455, 10 Положительно 29 (26, 9%), отрицательно 79 (73, 1%)
 Прогностическая значимость коагулологических показателей у больных ИИ в первые сутки госпитализации Вне зависимости от примененной антитромботической терапии высокую значимость в прогнозе выживаемости показали: -ССИТ, -концентрация фибриногена, -концентрация РФМК, -Активность ХЗФ
Прогностическая значимость коагулологических показателей у больных ИИ в первые сутки госпитализации Вне зависимости от примененной антитромботической терапии высокую значимость в прогнозе выживаемости показали: -ССИТ, -концентрация фибриногена, -концентрация РФМК, -Активность ХЗФ
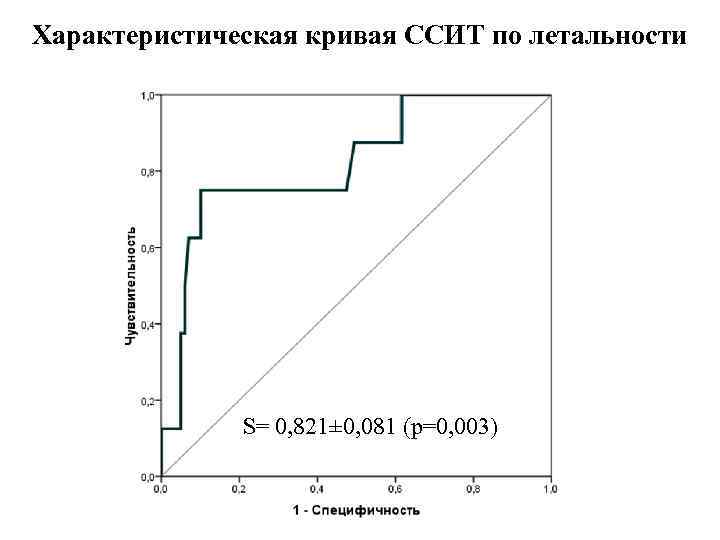 Характеристическая кривая ССИТ по летальности S= 0, 821± 0, 081 (р=0, 003)
Характеристическая кривая ССИТ по летальности S= 0, 821± 0, 081 (р=0, 003)
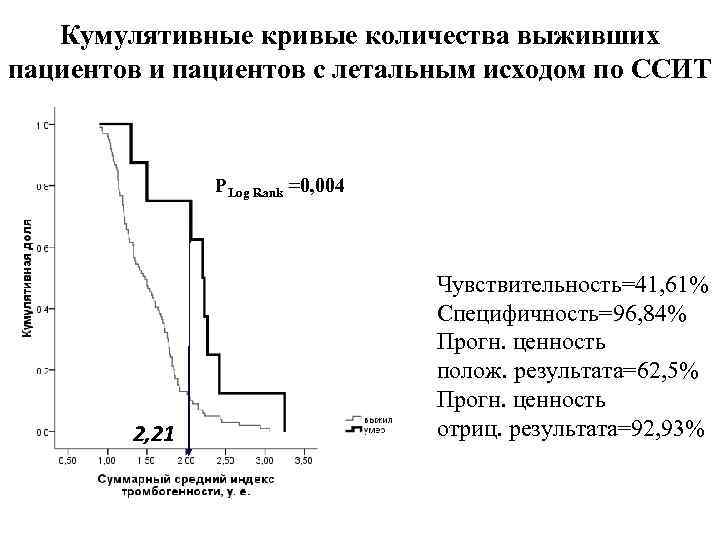 Кумулятивные кривые количества выживших пациентов и пациентов с летальным исходом по ССИТ РLog Rank =0, 004 2, 21 Чувствительность=41, 61% Специфичность=96, 84% Прогн. ценность полож. результата=62, 5% Прогн. ценность отриц. результата=92, 93%
Кумулятивные кривые количества выживших пациентов и пациентов с летальным исходом по ССИТ РLog Rank =0, 004 2, 21 Чувствительность=41, 61% Специфичность=96, 84% Прогн. ценность полож. результата=62, 5% Прогн. ценность отриц. результата=92, 93%
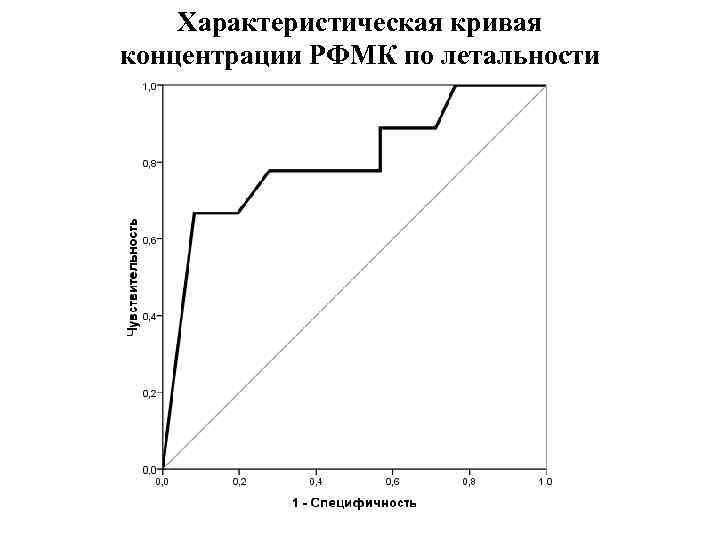 Характеристическая кривая концентрации РФМК по летальности S= 0, 801± 0, 087 (р=0, 003).
Характеристическая кривая концентрации РФМК по летальности S= 0, 801± 0, 087 (р=0, 003).
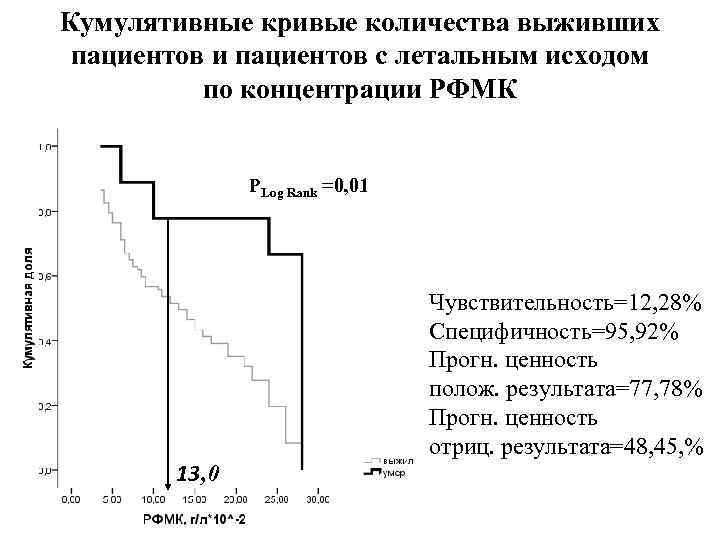 Кумулятивные кривые количества выживших пациентов и пациентов с летальным исходом по концентрации РФМК РLog Rank =0, 01 13, 0 Чувствительность=12, 28% Специфичность=95, 92% Прогн. ценность полож. результата=77, 78% Прогн. ценность отриц. результата=48, 45, %
Кумулятивные кривые количества выживших пациентов и пациентов с летальным исходом по концентрации РФМК РLog Rank =0, 01 13, 0 Чувствительность=12, 28% Специфичность=95, 92% Прогн. ценность полож. результата=77, 78% Прогн. ценность отриц. результата=48, 45, %
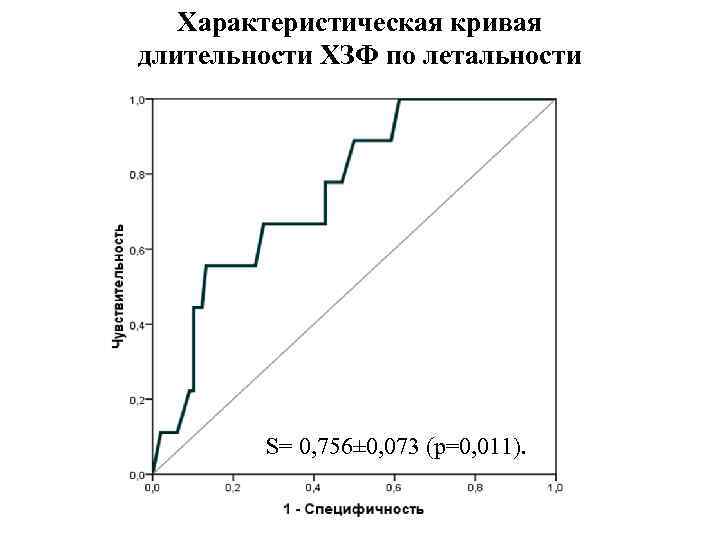 Характеристическая кривая длительности ХЗФ по летальности S= 0, 756± 0, 073 (р=0, 011).
Характеристическая кривая длительности ХЗФ по летальности S= 0, 756± 0, 073 (р=0, 011).
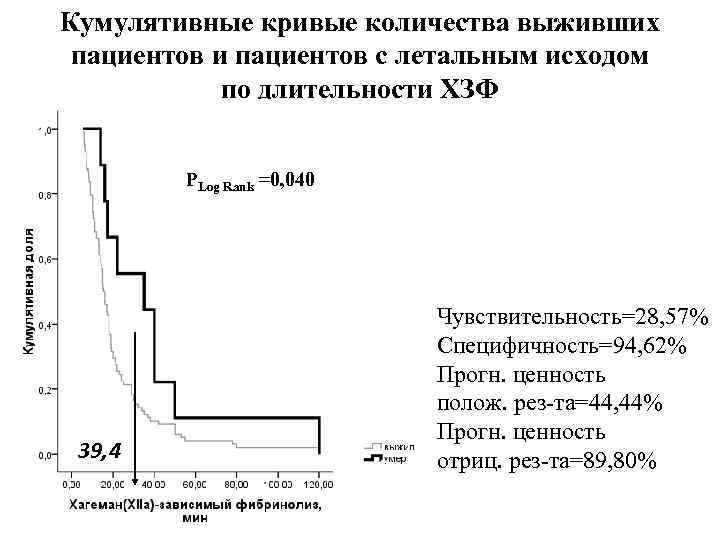 Кумулятивные кривые количества выживших пациентов и пациентов с летальным исходом по длительности ХЗФ РLog Rank =0, 040 39, 4 Чувствительность=28, 57% Специфичность=94, 62% Прогн. ценность полож. рез-та=44, 44% Прогн. ценность отриц. рез-та=89, 80%
Кумулятивные кривые количества выживших пациентов и пациентов с летальным исходом по длительности ХЗФ РLog Rank =0, 040 39, 4 Чувствительность=28, 57% Специфичность=94, 62% Прогн. ценность полож. рез-та=44, 44% Прогн. ценность отриц. рез-та=89, 80%
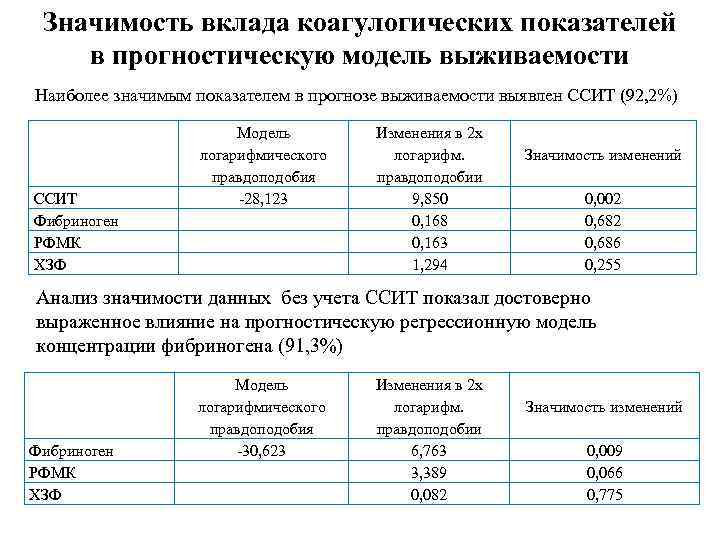 Значимость вклада коагулогических показателей в прогностическую модель выживаемости Наиболее значимым показателем в прогнозе выживаемости выявлен ССИТ (92, 2%) ССИТ Фибриноген РФМК ХЗФ Модель логарифмического правдоподобия -28, 123 Изменения в 2 х логарифм. правдоподобии 9, 850 0, 168 0, 163 1, 294 Значимость изменений 0, 002 0, 686 0, 255 Анализ значимости данных без учета ССИТ показал достоверно выраженное влияние на прогностическую регрессионную модель концентрации фибриногена (91, 3%) Фибриноген РФМК ХЗФ Модель логарифмического правдоподобия -30, 623 Изменения в 2 х логарифм. правдоподобии 6, 763 3, 389 0, 082 Значимость изменений 0, 009 0, 066 0, 775
Значимость вклада коагулогических показателей в прогностическую модель выживаемости Наиболее значимым показателем в прогнозе выживаемости выявлен ССИТ (92, 2%) ССИТ Фибриноген РФМК ХЗФ Модель логарифмического правдоподобия -28, 123 Изменения в 2 х логарифм. правдоподобии 9, 850 0, 168 0, 163 1, 294 Значимость изменений 0, 002 0, 686 0, 255 Анализ значимости данных без учета ССИТ показал достоверно выраженное влияние на прогностическую регрессионную модель концентрации фибриногена (91, 3%) Фибриноген РФМК ХЗФ Модель логарифмического правдоподобия -30, 623 Изменения в 2 х логарифм. правдоподобии 6, 763 3, 389 0, 082 Значимость изменений 0, 009 0, 066 0, 775
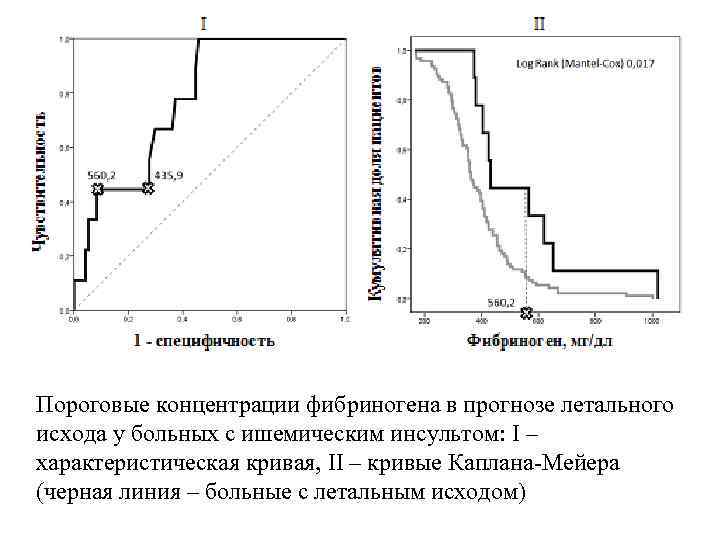 Пороговые концентрации фибриногена в прогнозе летального исхода у больных с ишемическим инсультом: I – характеристическая кривая, II – кривые Каплана-Мейера (черная линия – больные с летальным исходом)
Пороговые концентрации фибриногена в прогнозе летального исхода у больных с ишемическим инсультом: I – характеристическая кривая, II – кривые Каплана-Мейера (черная линия – больные с летальным исходом)
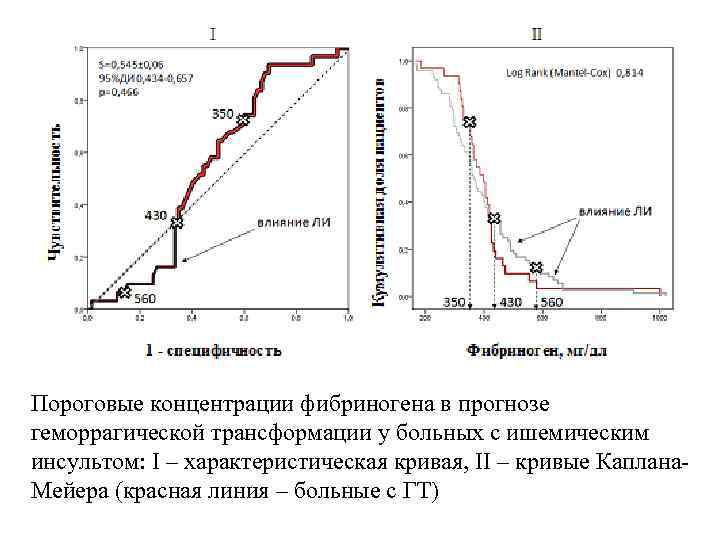 Пороговые концентрации фибриногена в прогнозе геморрагической трансформации у больных с ишемическим инсультом: I – характеристическая кривая, II – кривые Каплана. Мейера (красная линия – больные с ГТ)
Пороговые концентрации фибриногена в прогнозе геморрагической трансформации у больных с ишемическим инсультом: I – характеристическая кривая, II – кривые Каплана. Мейера (красная линия – больные с ГТ)
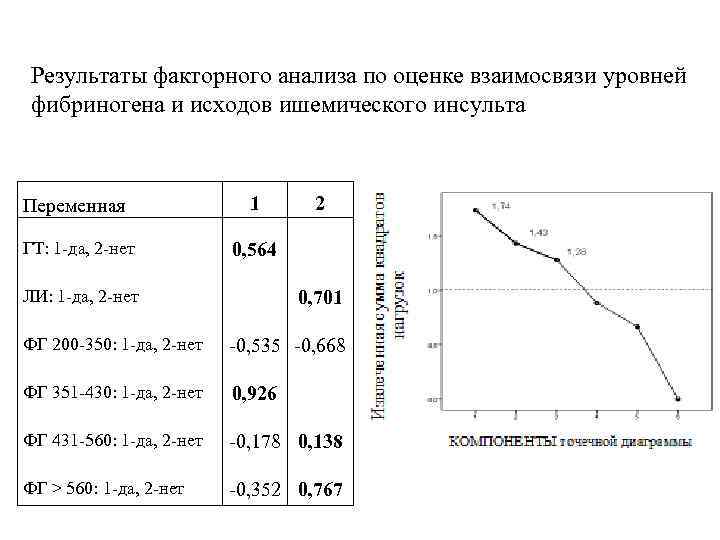 Результаты факторного анализа по оценке взаимосвязи уровней фибриногена и исходов ишемического инсульта Переменная 1 ГТ: 1 -да, 2 -нет 2 0, 564 0, 701 ЛИ: 1 -да, 2 -нет ФГ 200 -350: 1 -да, 2 -нет -0, 535 -0, 668 ФГ 351 -430: 1 -да, 2 -нет 0, 926 ФГ 431 -560: 1 -да, 2 -нет -0, 178 0, 138 ФГ > 560: 1 -да, 2 -нет -0, 352 0, 767
Результаты факторного анализа по оценке взаимосвязи уровней фибриногена и исходов ишемического инсульта Переменная 1 ГТ: 1 -да, 2 -нет 2 0, 564 0, 701 ЛИ: 1 -да, 2 -нет ФГ 200 -350: 1 -да, 2 -нет -0, 535 -0, 668 ФГ 351 -430: 1 -да, 2 -нет 0, 926 ФГ 431 -560: 1 -да, 2 -нет -0, 178 0, 138 ФГ > 560: 1 -да, 2 -нет -0, 352 0, 767
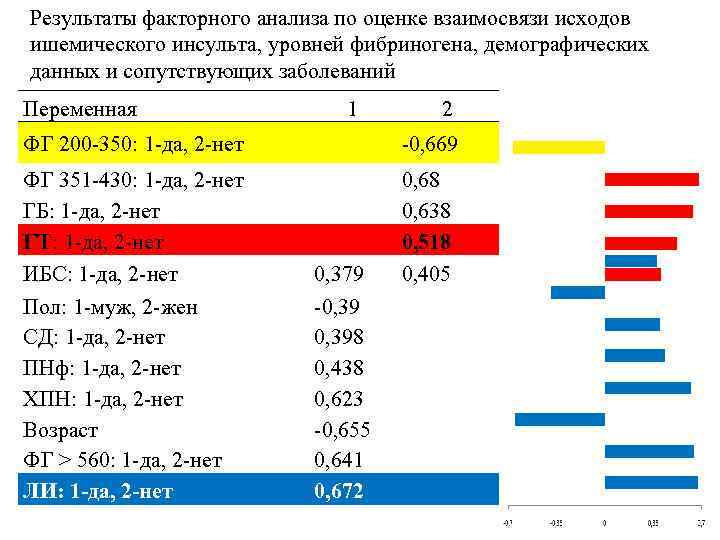 Результаты факторного анализа по оценке взаимосвязи исходов ишемического инсульта, уровней фибриногена, демографических данных и сопутствующих заболеваний Переменная 1 2 ФГ 200 -350: 1 -да, 2 -нет -0, 669 ФГ 351 -430: 1 -да, 2 -нет ГБ: 1 -да, 2 -нет ГТ: 1 -да, 2 -нет ИБС: 1 -да, 2 -нет Пол: 1 -муж, 2 -жен СД: 1 -да, 2 -нет ПНф: 1 -да, 2 -нет ХПН: 1 -да, 2 -нет Возраст ФГ > 560: 1 -да, 2 -нет ЛИ: 1 -да, 2 -нет 0, 68 0, 638 0, 518 0, 405 0, 379 -0, 398 0, 438 0, 623 -0, 655 0, 641 0, 672
Результаты факторного анализа по оценке взаимосвязи исходов ишемического инсульта, уровней фибриногена, демографических данных и сопутствующих заболеваний Переменная 1 2 ФГ 200 -350: 1 -да, 2 -нет -0, 669 ФГ 351 -430: 1 -да, 2 -нет ГБ: 1 -да, 2 -нет ГТ: 1 -да, 2 -нет ИБС: 1 -да, 2 -нет Пол: 1 -муж, 2 -жен СД: 1 -да, 2 -нет ПНф: 1 -да, 2 -нет ХПН: 1 -да, 2 -нет Возраст ФГ > 560: 1 -да, 2 -нет ЛИ: 1 -да, 2 -нет 0, 68 0, 638 0, 518 0, 405 0, 379 -0, 398 0, 438 0, 623 -0, 655 0, 641 0, 672
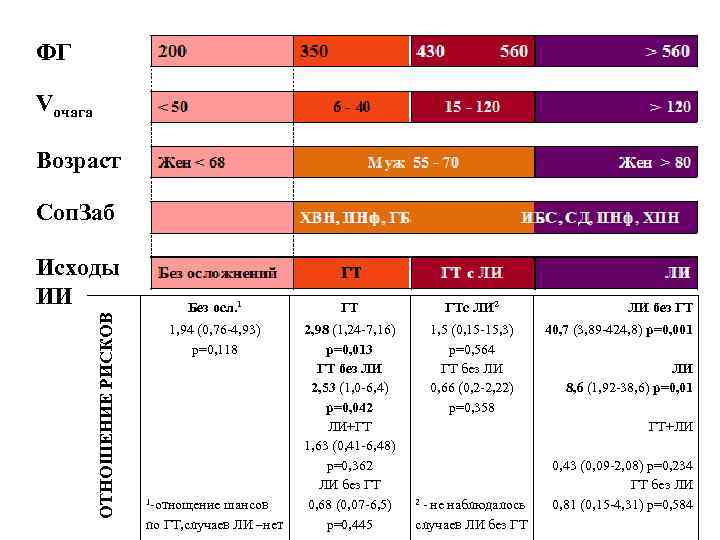 ФГ Vочага Возраст Соп. Заб ОТНОШЕНИЕ РИСКОВ Исходы ИИ Без осл. 1 ГТ ГТс ЛИ 2 1, 94 (0, 76 -4, 93) р=0, 118 2, 98 (1, 24 -7, 16) р=0, 013 ГТ без ЛИ 2, 53 (1, 0 -6, 4) р=0, 042 ЛИ+ГТ 1, 63 (0, 41 -6, 48) р=0, 362 ЛИ без ГТ 0, 68 (0, 07 -6, 5) р=0, 445 1, 5 (0, 15 -15, 3) р=0, 564 ГТ без ЛИ 0, 66 (0, 2 -2, 22) р=0, 358 1 -отнощение шансов по ГТ, случаев ЛИ –нет ЛИ без ГТ 40, 7 (3, 89 -424, 8) р=0, 001 ЛИ 8, 6 (1, 92 -38, 6) р=0, 01 ГТ+ЛИ 2 - не наблюдалось случаев ЛИ без ГТ 0, 43 (0, 09 -2, 08) р=0, 234 ГТ без ЛИ 0, 81 (0, 15 -4, 31) р=0, 584
ФГ Vочага Возраст Соп. Заб ОТНОШЕНИЕ РИСКОВ Исходы ИИ Без осл. 1 ГТ ГТс ЛИ 2 1, 94 (0, 76 -4, 93) р=0, 118 2, 98 (1, 24 -7, 16) р=0, 013 ГТ без ЛИ 2, 53 (1, 0 -6, 4) р=0, 042 ЛИ+ГТ 1, 63 (0, 41 -6, 48) р=0, 362 ЛИ без ГТ 0, 68 (0, 07 -6, 5) р=0, 445 1, 5 (0, 15 -15, 3) р=0, 564 ГТ без ЛИ 0, 66 (0, 2 -2, 22) р=0, 358 1 -отнощение шансов по ГТ, случаев ЛИ –нет ЛИ без ГТ 40, 7 (3, 89 -424, 8) р=0, 001 ЛИ 8, 6 (1, 92 -38, 6) р=0, 01 ГТ+ЛИ 2 - не наблюдалось случаев ЛИ без ГТ 0, 43 (0, 09 -2, 08) р=0, 234 ГТ без ЛИ 0, 81 (0, 15 -4, 31) р=0, 584
 Динамика концентрации маркеров воспаления и деструкции у больных с ишемическим инсультом при проведении тромболитической терапии
Динамика концентрации маркеров воспаления и деструкции у больных с ишемическим инсультом при проведении тромболитической терапии
 Лабораторные исследования Статус Эндотелиальная дисфункция Маркер гомоцистеин эндотелин-1 Воспаление, некроз тканей фактор некроза опухоли - альфа интерлейкин-6 С-реактивный белок высокочувствительный Деструкция тканей эластаза лейкоцитарная матриксная металлопротеиназа-9 Воспаление, деструкция тканей фибронектин Деструкция нейронов нейроспецифическая енолаза
Лабораторные исследования Статус Эндотелиальная дисфункция Маркер гомоцистеин эндотелин-1 Воспаление, некроз тканей фактор некроза опухоли - альфа интерлейкин-6 С-реактивный белок высокочувствительный Деструкция тканей эластаза лейкоцитарная матриксная металлопротеиназа-9 Воспаление, деструкция тканей фибронектин Деструкция нейронов нейроспецифическая енолаза
 Гомоцистеин - серосодержащая аминокислота, продукт деметилирования незаменимой аминокислоты метионина Повышение концентрации - быстро окисляется, что приводит к образованию большого количества радикалов, содержащих активный кислород: происходит повреждение клеток эндотелия окисление ЛПНП усиливается синтез интерлейкина-6
Гомоцистеин - серосодержащая аминокислота, продукт деметилирования незаменимой аминокислоты метионина Повышение концентрации - быстро окисляется, что приводит к образованию большого количества радикалов, содержащих активный кислород: происходит повреждение клеток эндотелия окисление ЛПНП усиливается синтез интерлейкина-6
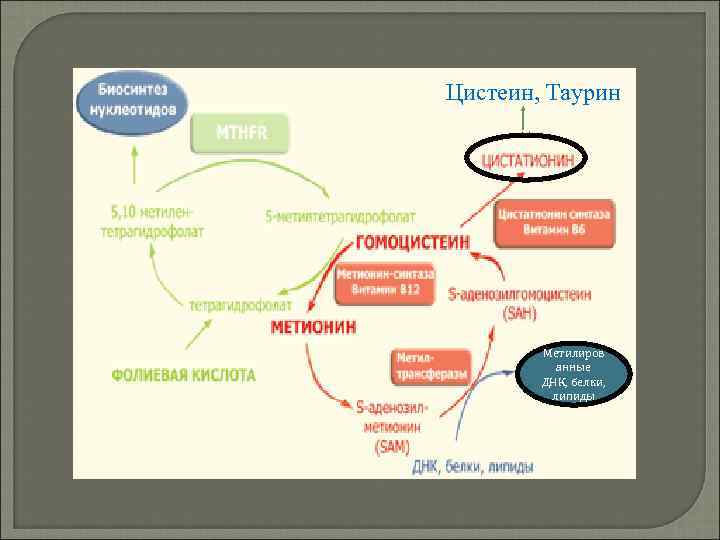 Цистеин, Таурин Метилиров анные ДНК, белки, липиды
Цистеин, Таурин Метилиров анные ДНК, белки, липиды
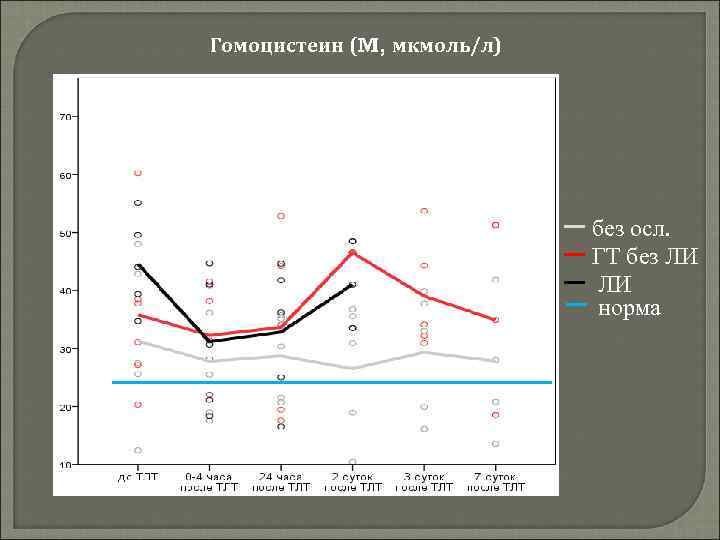 Гомоцистеин (M, мкмоль/л) без осл. ГТ без ЛИ ЛИ норма
Гомоцистеин (M, мкмоль/л) без осл. ГТ без ЛИ ЛИ норма
 эндотелин– 1 пептид, выделяемый эндотелием сосудов, активирует в физиологических концентрациях рецепторы на эндотелии (вазодилятатор) и в высоких - на гладкомышечных клетках (ВАЗОКОНСТРИКТОР) очень быстро образуется под воздействием адреналина, ангиотензина-II, вазопрессина, тромбина, цитокинов и механических воздействий
эндотелин– 1 пептид, выделяемый эндотелием сосудов, активирует в физиологических концентрациях рецепторы на эндотелии (вазодилятатор) и в высоких - на гладкомышечных клетках (ВАЗОКОНСТРИКТОР) очень быстро образуется под воздействием адреналина, ангиотензина-II, вазопрессина, тромбина, цитокинов и механических воздействий
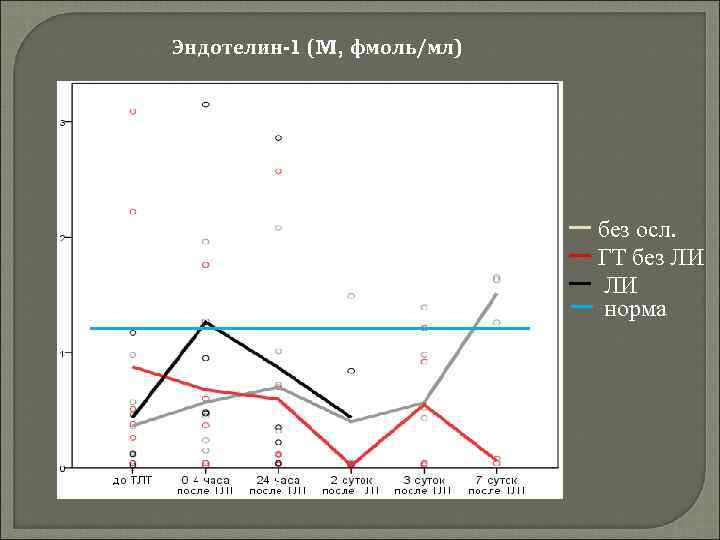 Эндотелин-1 (M, фмоль/мл) без осл. ГТ без ЛИ ЛИ норма
Эндотелин-1 (M, фмоль/мл) без осл. ГТ без ЛИ ЛИ норма
 Фактор некроза опухоли - альфа - цитокин продуцируется моноцитами/макрофагами, эндотелиальными и тучными клетками индуцирует апоптоз вызывает генерализацию в клеточной мембране активных форм кислорода, супероксид-радикалов, а также оксида азота оказывает хемотаксическое действие на различные клетки обусловливает синтез белков острой фазы воспаления
Фактор некроза опухоли - альфа - цитокин продуцируется моноцитами/макрофагами, эндотелиальными и тучными клетками индуцирует апоптоз вызывает генерализацию в клеточной мембране активных форм кислорода, супероксид-радикалов, а также оксида азота оказывает хемотаксическое действие на различные клетки обусловливает синтез белков острой фазы воспаления
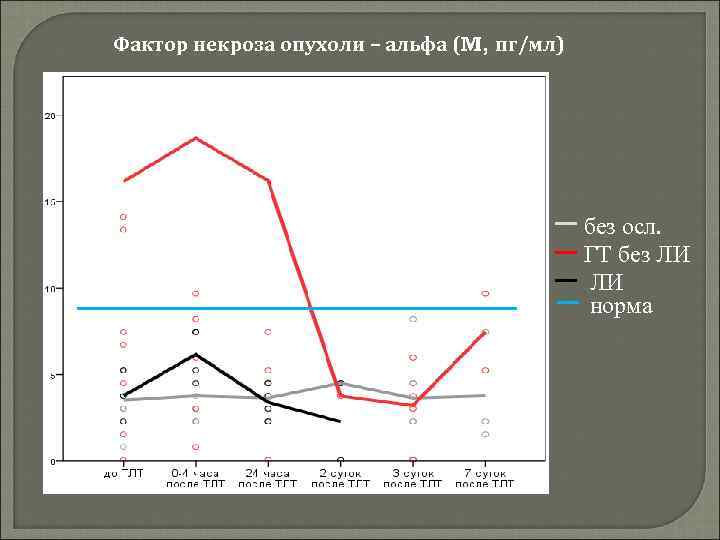 Фактор некроза опухоли – альфа (M, пг/мл) без осл. ГТ без ЛИ ЛИ норма
Фактор некроза опухоли – альфа (M, пг/мл) без осл. ГТ без ЛИ ЛИ норма
 Интерлейкин-6 медиатор межлейкоцитарного взаимодействия Продуцируется моноцитами, макрофагами, лимфоцитами, фибробластами и эндотелиальными клетками Выделяется позже ФНО-альфа В умеренных концентрациях стимулирует секрецию СТГ (анаболический эффект) и ингибирует секрецию ТТГ (антикатаболический эффект) В высоких концентрациях – цитокин, стимулирует синтез белков острой фазы
Интерлейкин-6 медиатор межлейкоцитарного взаимодействия Продуцируется моноцитами, макрофагами, лимфоцитами, фибробластами и эндотелиальными клетками Выделяется позже ФНО-альфа В умеренных концентрациях стимулирует секрецию СТГ (анаболический эффект) и ингибирует секрецию ТТГ (антикатаболический эффект) В высоких концентрациях – цитокин, стимулирует синтез белков острой фазы
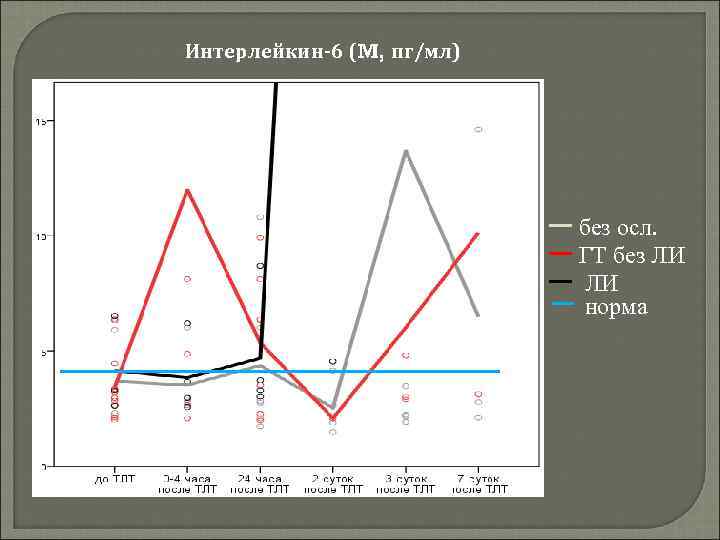 Интерлейкин-6 (M, пг/мл) без осл. ГТ без ЛИ ЛИ норма
Интерлейкин-6 (M, пг/мл) без осл. ГТ без ЛИ ЛИ норма
 С-реактивный протеин – белок острой фазы воспаления синтезируется гепатоцитами под влиянием ИЛ 6 и присутствующими в атеросклеротической бляшке макрофагами, лимфоцитами является высокочувствительным маркером воспаления и тканевой деструкции.
С-реактивный протеин – белок острой фазы воспаления синтезируется гепатоцитами под влиянием ИЛ 6 и присутствующими в атеросклеротической бляшке макрофагами, лимфоцитами является высокочувствительным маркером воспаления и тканевой деструкции.
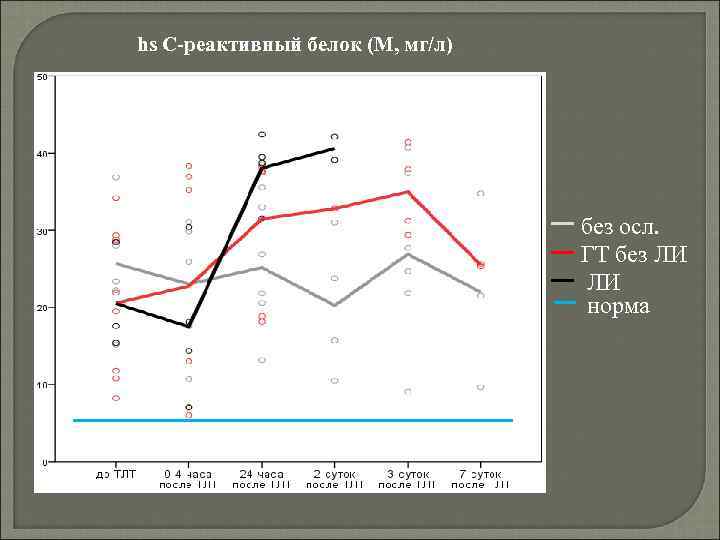 hs С-реактивный белок (M, мг/л) без осл. ГТ без ЛИ ЛИ норма
hs С-реактивный белок (M, мг/л) без осл. ГТ без ЛИ ЛИ норма
 Эластаза лейкоцитарная – протеаза, высвобождается при дегрануляции нейтрофилов расщепляет эластиновые и коллагеновые волокна базальной сосудистой мембраны, увеличивает проницаемость ГЭБ и деструкцию ткани мозга при ишемии и инсультах
Эластаза лейкоцитарная – протеаза, высвобождается при дегрануляции нейтрофилов расщепляет эластиновые и коллагеновые волокна базальной сосудистой мембраны, увеличивает проницаемость ГЭБ и деструкцию ткани мозга при ишемии и инсультах
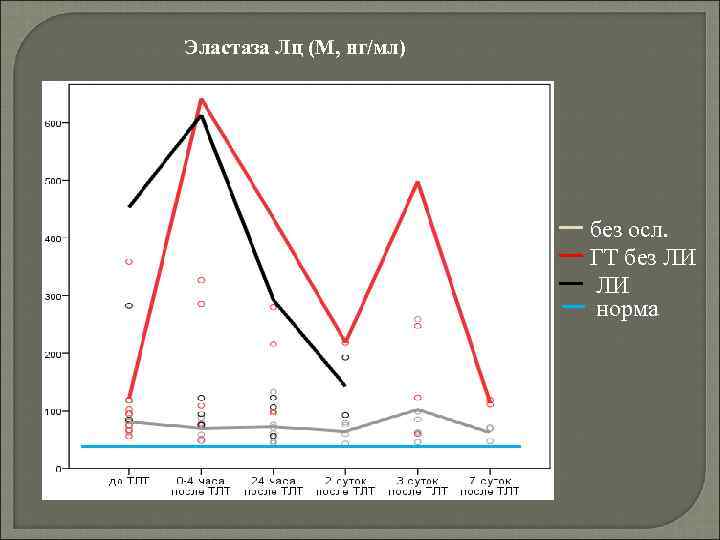 Эластаза Лц (M, нг/мл) без осл. ГТ без ЛИ ЛИ норма
Эластаза Лц (M, нг/мл) без осл. ГТ без ЛИ ЛИ норма
 Матриксная металлопротеиназа - 9 внеклеточная, цинк- содержащая протеиназа. Синтезируется эндотелиальными клетками в виде неактивного профермента активируется многими протеиназами, в том числе эластазами и тромбином после активации обладает способностью гидролизовать все основные белки матрикса
Матриксная металлопротеиназа - 9 внеклеточная, цинк- содержащая протеиназа. Синтезируется эндотелиальными клетками в виде неактивного профермента активируется многими протеиназами, в том числе эластазами и тромбином после активации обладает способностью гидролизовать все основные белки матрикса
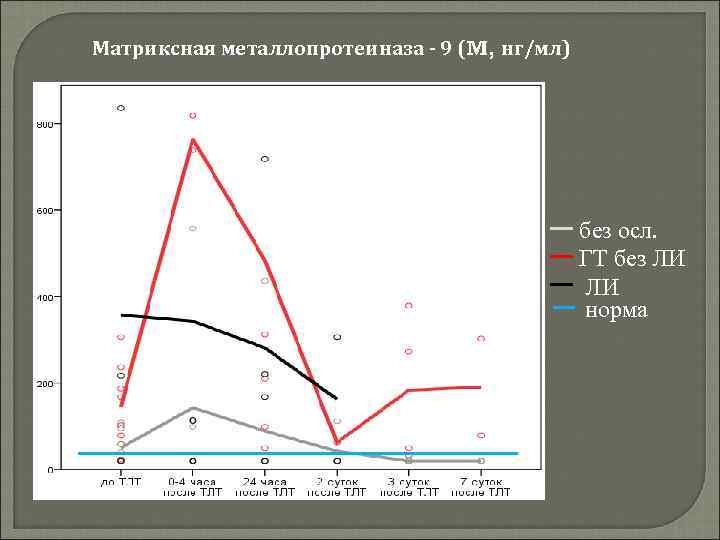 Матриксная металлопротеиназа - 9 (M, нг/мл) без осл. ГТ без ЛИ ЛИ норма
Матриксная металлопротеиназа - 9 (M, нг/мл) без осл. ГТ без ЛИ ЛИ норма
 Фибронектин гликопротеид, продуцируется клетками печени и почек играет главную роль в процессе миграции клеток и последующей их адгезии к подлежащему субстрату существует в двух формах -тканевой и плазменной в плазме крови он усиливает фагоцитоз (опсонизирующая функция) – маркер воспаления и тканевой деструкции на поверхности клетки усиливает образование белковых связей, в частности: участвует в агрегации тромбоцитов и взаимодействии факторов коагуляции – маркер тромбообразования
Фибронектин гликопротеид, продуцируется клетками печени и почек играет главную роль в процессе миграции клеток и последующей их адгезии к подлежащему субстрату существует в двух формах -тканевой и плазменной в плазме крови он усиливает фагоцитоз (опсонизирующая функция) – маркер воспаления и тканевой деструкции на поверхности клетки усиливает образование белковых связей, в частности: участвует в агрегации тромбоцитов и взаимодействии факторов коагуляции – маркер тромбообразования
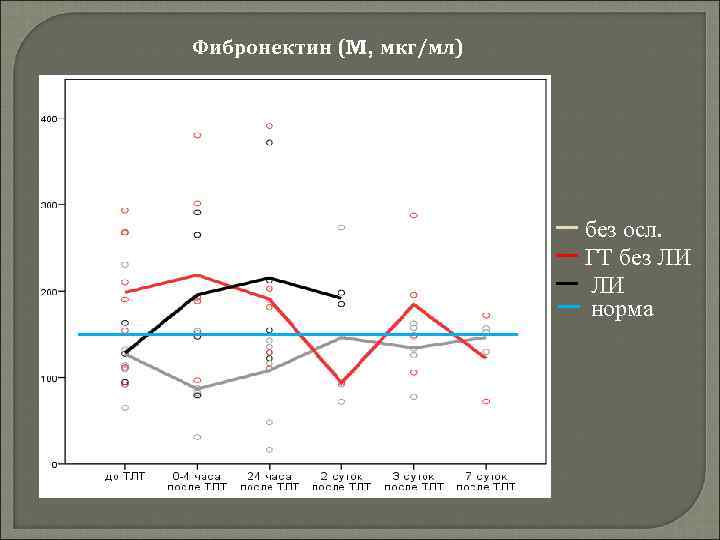 Фибронектин (M, мкг/мл) без осл. ГТ без ЛИ ЛИ норма
Фибронектин (M, мкг/мл) без осл. ГТ без ЛИ ЛИ норма
 Нейронспецифическая енолаза (NSE) – специфический внутриклеточный фермент всех дифференцированных нейронов позволяет оценить нарушение общей целостности гематоэнцефалического барьера и степень выраженности повреждений нейронов т. е. характеризует степень постишемического повреждения мозга
Нейронспецифическая енолаза (NSE) – специфический внутриклеточный фермент всех дифференцированных нейронов позволяет оценить нарушение общей целостности гематоэнцефалического барьера и степень выраженности повреждений нейронов т. е. характеризует степень постишемического повреждения мозга
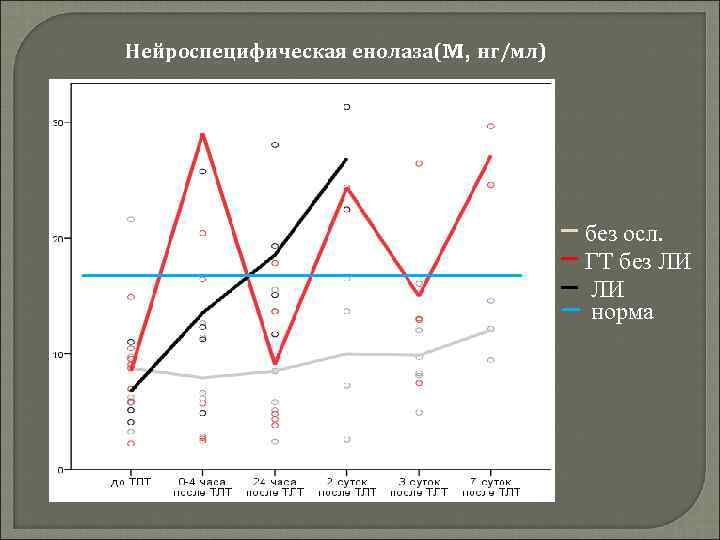 Нейроспецифическая енолаза(M, нг/мл) без осл. ГТ без ЛИ ЛИ норма
Нейроспецифическая енолаза(M, нг/мл) без осл. ГТ без ЛИ ЛИ норма
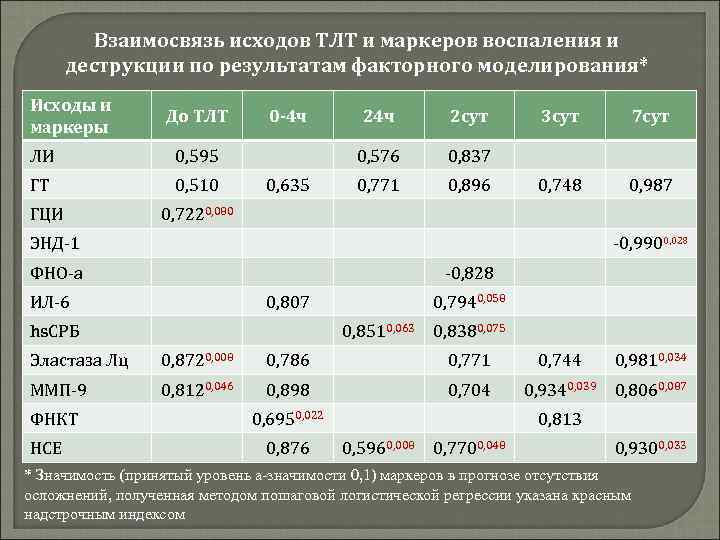 Взаимосвязь исходов ТЛТ и маркеров воспаления и деструкции по результатам факторного моделирования* Исходы и маркеры До ТЛТ ЛИ 0, 510 ГЦИ 0, 635 24 ч 2 сут 0, 576 0, 595 ГТ 0 -4 ч 0, 837 0, 771 0, 896 3 сут 7 сут 0, 748 0, 987 0, 7220, 080 ЭНД-1 -0, 9900, 028 ФНО-а -0, 828 ИЛ-6 0, 807 hs. СРБ 0, 7940, 058 0, 8510, 063 0, 8380, 075 Эластаза Лц 0, 8720, 008 0, 786 0, 771 0, 744 0, 9810, 034 ММП-9 0, 8120, 046 0, 898 0, 704 0, 9340, 039 0, 8060, 087 ФНКТ НСЕ 0, 6950, 022 0, 876 0, 813 0, 5960, 008 0, 7700, 048 0, 9300, 033 * Значимость (принятый уровень а-значимости 0, 1) маркеров в прогнозе отсутствия осложнений, полученная методом пошаговой логистической регрессии указана красным надстрочным индексом
Взаимосвязь исходов ТЛТ и маркеров воспаления и деструкции по результатам факторного моделирования* Исходы и маркеры До ТЛТ ЛИ 0, 510 ГЦИ 0, 635 24 ч 2 сут 0, 576 0, 595 ГТ 0 -4 ч 0, 837 0, 771 0, 896 3 сут 7 сут 0, 748 0, 987 0, 7220, 080 ЭНД-1 -0, 9900, 028 ФНО-а -0, 828 ИЛ-6 0, 807 hs. СРБ 0, 7940, 058 0, 8510, 063 0, 8380, 075 Эластаза Лц 0, 8720, 008 0, 786 0, 771 0, 744 0, 9810, 034 ММП-9 0, 8120, 046 0, 898 0, 704 0, 9340, 039 0, 8060, 087 ФНКТ НСЕ 0, 6950, 022 0, 876 0, 813 0, 5960, 008 0, 7700, 048 0, 9300, 033 * Значимость (принятый уровень а-значимости 0, 1) маркеров в прогнозе отсутствия осложнений, полученная методом пошаговой логистической регрессии указана красным надстрочным индексом
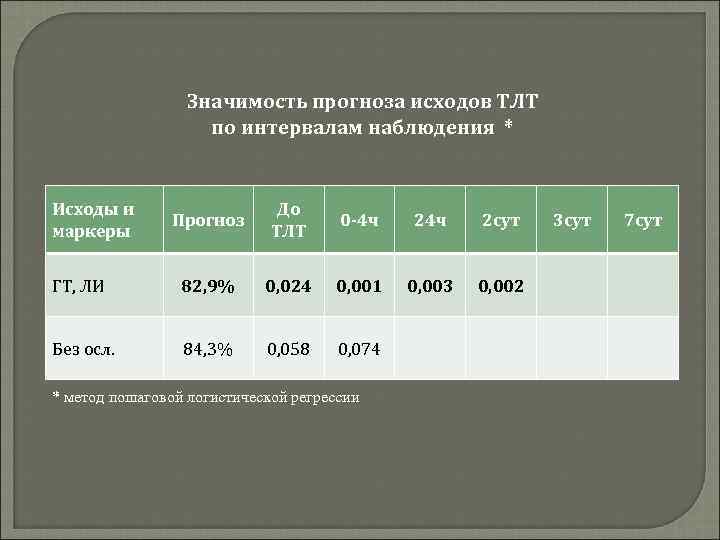 Значимость прогноза исходов ТЛТ по интервалам наблюдения * Исходы и маркеры Прогноз До ТЛТ 0 -4 ч 2 сут ГТ, ЛИ 82, 9% 0, 024 0, 001 0, 003 0, 002 Без осл. 84, 3% 0, 058 0, 074 * метод пошаговой логистической регрессии 3 сут 7 сут
Значимость прогноза исходов ТЛТ по интервалам наблюдения * Исходы и маркеры Прогноз До ТЛТ 0 -4 ч 2 сут ГТ, ЛИ 82, 9% 0, 024 0, 001 0, 003 0, 002 Без осл. 84, 3% 0, 058 0, 074 * метод пошаговой логистической регрессии 3 сут 7 сут
 Таким образом: 1. В прогнозе ГТ и ЛИ у больных с ИИ после проведения ТЛТ наблюдаются высокие концентрации гомоцистеина, СРБ, Лц эластазы, ММП-9, фибронектина, нейроспецифической енолазы и ИЛ-6. Нет превышения значений ФНО и эндотелина-1.
Таким образом: 1. В прогнозе ГТ и ЛИ у больных с ИИ после проведения ТЛТ наблюдаются высокие концентрации гомоцистеина, СРБ, Лц эластазы, ММП-9, фибронектина, нейроспецифической енолазы и ИЛ-6. Нет превышения значений ФНО и эндотелина-1.
 2. Ассоциацию с ГТ и ЛИ до проведения ТЛТ показывают гомоцистеин, Лц эластаза и ММП-9. Через сутки после ТЛТ – СРБ и нейроспецифическая енолаза. Через 2 и 3 суток - СРБ, Лц эластаза, ММП -9, фибронектин, нейроспецифическая енолаза и ИЛ-6.
2. Ассоциацию с ГТ и ЛИ до проведения ТЛТ показывают гомоцистеин, Лц эластаза и ММП-9. Через сутки после ТЛТ – СРБ и нейроспецифическая енолаза. Через 2 и 3 суток - СРБ, Лц эластаза, ММП -9, фибронектин, нейроспецифическая енолаза и ИЛ-6.
 3. Непосредственно после проведения ТЛТ высокие концентрации Лц эластазы, ММП-9, фибронектина, нейроспецифической енолазы и ИЛ-6 не являются фатальными и могут служить маркерами эффективной реканализации.
3. Непосредственно после проведения ТЛТ высокие концентрации Лц эластазы, ММП-9, фибронектина, нейроспецифической енолазы и ИЛ-6 не являются фатальными и могут служить маркерами эффективной реканализации.
 4. В прогнозе ГТ и ЛИ у больных с ИИ после проведения ТЛТ сохраняется значимость определения маркеров воспаления и деструкции в течение 2 суток
4. В прогнозе ГТ и ЛИ у больных с ИИ после проведения ТЛТ сохраняется значимость определения маркеров воспаления и деструкции в течение 2 суток
 5. В прогнозе отсутствия осложнений наибольшая значимость определения маркеров воспаления и деструкции выявлена до проведения ТЛТ и непосредственно после проведения ТЛТ
5. В прогнозе отсутствия осложнений наибольшая значимость определения маркеров воспаления и деструкции выявлена до проведения ТЛТ и непосредственно после проведения ТЛТ
 Задачами последующих исследований остаются: 1. Определение пороговых значений концентрации маркеров воспаления и деструкции в прогнозе ГТ и ЛИ при проведении ТЛТ у больных с ИИ 2. Сопоставление пороговых значений маркеров с клиническими данными, результатами функциональных и Кт-исследований 3. Создание экспертной клинико-лабораторной системы прогноза выживаемости больных с ИИ при проведении ТЛТ
Задачами последующих исследований остаются: 1. Определение пороговых значений концентрации маркеров воспаления и деструкции в прогнозе ГТ и ЛИ при проведении ТЛТ у больных с ИИ 2. Сопоставление пороговых значений маркеров с клиническими данными, результатами функциональных и Кт-исследований 3. Создание экспертной клинико-лабораторной системы прогноза выживаемости больных с ИИ при проведении ТЛТ


