83825.ppt
- Количество слайдов: 94
 «Система цитокинов. Классификация. Основные свойства. Механизмы действия. Типы цитокиновой регуляции. Клетки-продуценты и клетки-мишени. Цитокиновая регуляция воспаления и иммунного ответа» . Цикл 1 – иммунология. Занятие № 3 а.
«Система цитокинов. Классификация. Основные свойства. Механизмы действия. Типы цитокиновой регуляции. Клетки-продуценты и клетки-мишени. Цитокиновая регуляция воспаления и иммунного ответа» . Цикл 1 – иммунология. Занятие № 3 а.
 Цитокины Сигнальные (биорегуляторные) молекулы, управляющие практически всеми процессами в организме – эмбриогенезом, гемопоэзом, процессами созревания и дифференцировки клеток, активации и гибели клеток, инициацией и поддержанием разных типов иммунного ответа, развитием воспаления, процессами репарации, ремоделирования тканей, координацией работы иммуно – нейро - эндокринной систем на уровне организма в целом.
Цитокины Сигнальные (биорегуляторные) молекулы, управляющие практически всеми процессами в организме – эмбриогенезом, гемопоэзом, процессами созревания и дифференцировки клеток, активации и гибели клеток, инициацией и поддержанием разных типов иммунного ответа, развитием воспаления, процессами репарации, ремоделирования тканей, координацией работы иммуно – нейро - эндокринной систем на уровне организма в целом.
 Цитокины Растворимые гликопротеины (более 1300 молекул, 550 к. Da) неиммуноглобулиновой природы, освобождаемые клетками организма – хозяина, обладающие неферментативным действием в низких концентрациях (от пикомолярных до наномолярных), действующие через специфические рецепторы на клетках-мишенях, регулирующие различные функции клеток организма. В настоящее время известно около 200 цитокинов.
Цитокины Растворимые гликопротеины (более 1300 молекул, 550 к. Da) неиммуноглобулиновой природы, освобождаемые клетками организма – хозяина, обладающие неферментативным действием в низких концентрациях (от пикомолярных до наномолярных), действующие через специфические рецепторы на клетках-мишенях, регулирующие различные функции клеток организма. В настоящее время известно около 200 цитокинов.
 Цитокины и жизненный цикл клеток Цитокины –биорегуляторные молекулы, контролирующие разные этапы жизненного цикла клеток: • процессы дифференцировки. • процессы пролиферации. • процессы функциональной активации. • процессы гибели клеток. Цитокины и иммунный ответ Цитокины играют важную роль в осуществлении реакций как врожденного, так и адаптивного иммунитета. Цитокины обеспечивают взаимосвязь врожденного и адаптивного иммунных ответов.
Цитокины и жизненный цикл клеток Цитокины –биорегуляторные молекулы, контролирующие разные этапы жизненного цикла клеток: • процессы дифференцировки. • процессы пролиферации. • процессы функциональной активации. • процессы гибели клеток. Цитокины и иммунный ответ Цитокины играют важную роль в осуществлении реакций как врожденного, так и адаптивного иммунитета. Цитокины обеспечивают взаимосвязь врожденного и адаптивного иммунных ответов.
 Свойства цитокинов • Характерен короткий период Плейотропность – единственная полужизни: молекула может вызывать цитокины быстро множество эффектов путем инактивируются и активации различных генов в разрушаются. клетках-мишенях • Большинство из цитокинов действует на местном уровне Конвергенция функций – разные (паракринно – на клетки цитокиновые молекулы могут микроокружения). выполнять в организме • Цитокинов больше, чем их сходные функции рецепторов (многие цитокины Полисферизм – множество используют общие цитокинов могут субъединицы рецепторов) на клетках-мишенях для продуцироваться одной и той передачи сигналов в ядро же клеткой в ответ на один клетки-мишени стимул
Свойства цитокинов • Характерен короткий период Плейотропность – единственная полужизни: молекула может вызывать цитокины быстро множество эффектов путем инактивируются и активации различных генов в разрушаются. клетках-мишенях • Большинство из цитокинов действует на местном уровне Конвергенция функций – разные (паракринно – на клетки цитокиновые молекулы могут микроокружения). выполнять в организме • Цитокинов больше, чем их сходные функции рецепторов (многие цитокины Полисферизм – множество используют общие цитокинов могут субъединицы рецепторов) на клетках-мишенях для продуцироваться одной и той передачи сигналов в ядро же клеткой в ответ на один клетки-мишени стимул
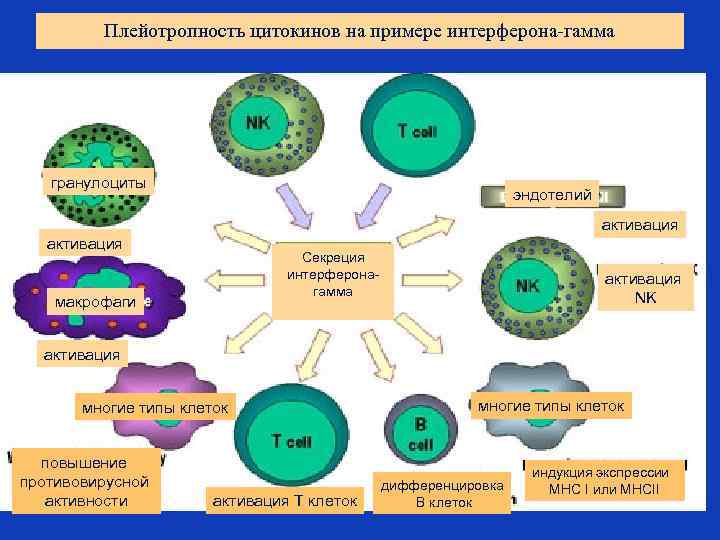 Плейотропность цитокинов на примере интерферона-гамма гранулоциты эндотелий активация Секреция интерферонагамма макрофаги активация NK активация многие типы клеток повышение противовирусной активности активация Т клеток многие типы клеток дифференцировка В клеток индукция экспрессии MHC I или MHCII
Плейотропность цитокинов на примере интерферона-гамма гранулоциты эндотелий активация Секреция интерферонагамма макрофаги активация NK активация многие типы клеток повышение противовирусной активности активация Т клеток многие типы клеток дифференцировка В клеток индукция экспрессии MHC I или MHCII
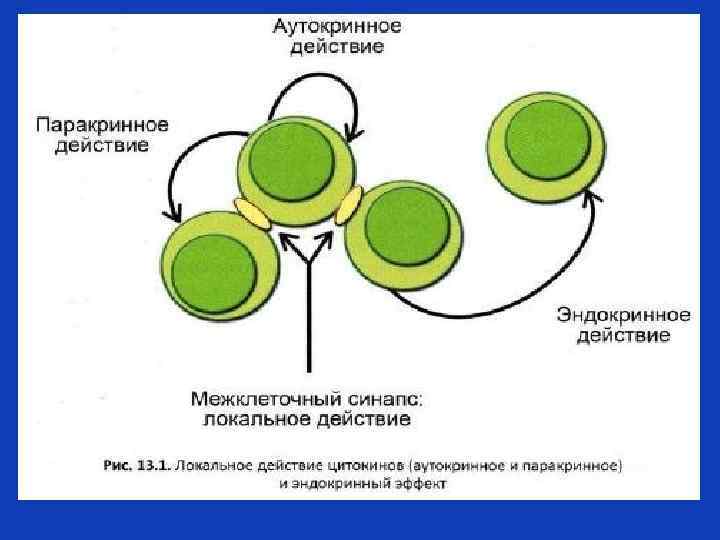
 Типы цитокиновой регуляции Паракринная регуляция (в большинстве случаев цитокины действуют местно, в очаге воспаления). Аутокринная регуляция – цитокин производится клеткой, к нему клеткапроизводитель данного цитокина экспрессирует рецепторы, вследствие этого цитокин действует на клетку, его производящую. Эндокринная регуляция – отставленное действие: интерлейкин 1 –бета – эндогенный пироген (действует на центр терморегуляции в головном мозге), интерлейкин 6 действует на гепатоциты, вызывая синтез белков острой фазы, ростовые факторы действуют на костный мозг, активируют гемопоэз и т. д.
Типы цитокиновой регуляции Паракринная регуляция (в большинстве случаев цитокины действуют местно, в очаге воспаления). Аутокринная регуляция – цитокин производится клеткой, к нему клеткапроизводитель данного цитокина экспрессирует рецепторы, вследствие этого цитокин действует на клетку, его производящую. Эндокринная регуляция – отставленное действие: интерлейкин 1 –бета – эндогенный пироген (действует на центр терморегуляции в головном мозге), интерлейкин 6 действует на гепатоциты, вызывая синтез белков острой фазы, ростовые факторы действуют на костный мозг, активируют гемопоэз и т. д.
 Представление о системе цитокинов в клинической практике Для клинической практики важно отследить основную цепь взаимодействий в иммунопатогенезе заболеваний : 1. Клетки- продуценты цитокинов. 2. Цитокины и их антагонисты. 3. Клетки-мишени, экспрессирующие рецепторы цитокинов. 4. Производимые цитокинами эффекты на уровне организма. Цель: разработка и внедрение в практику новых стратегий терапии заболеваний: цитокиновая терапия (применение в клинике препаратов цитокинов), либо антицитокиновая терапия (применение в клинике антагонистов цитокинов или моноклональных антител к цитокинам).
Представление о системе цитокинов в клинической практике Для клинической практики важно отследить основную цепь взаимодействий в иммунопатогенезе заболеваний : 1. Клетки- продуценты цитокинов. 2. Цитокины и их антагонисты. 3. Клетки-мишени, экспрессирующие рецепторы цитокинов. 4. Производимые цитокинами эффекты на уровне организма. Цель: разработка и внедрение в практику новых стратегий терапии заболеваний: цитокиновая терапия (применение в клинике препаратов цитокинов), либо антицитокиновая терапия (применение в клинике антагонистов цитокинов или моноклональных антител к цитокинам).
 Основные типы цитокинов –общепринятые сокращения: интерлейкины В более ранних классификациях цитокинов использовалось их деление по принципу клеток, синтезирующих цитокины: • лимфокины (цитокины, секретируемые в основном активированными Т лимфоцитами –хелперами) и • монокины (цитокины, секретируемые клетками моноцитарномакрофагал. ьного ряда) Такой подход не всегда оправдан, так как для цитокинов характерно частичное перекрывание функций. Вследствие этого был введен единый термин «интерлейкины» IL (или ИЛ): 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 1 5, 16, 17 …. . 35 Термин «интерлейкины» означает «молекулы, участвующие во взаимоотношениях, «беседах» между лейкоцитами» .
Основные типы цитокинов –общепринятые сокращения: интерлейкины В более ранних классификациях цитокинов использовалось их деление по принципу клеток, синтезирующих цитокины: • лимфокины (цитокины, секретируемые в основном активированными Т лимфоцитами –хелперами) и • монокины (цитокины, секретируемые клетками моноцитарномакрофагал. ьного ряда) Такой подход не всегда оправдан, так как для цитокинов характерно частичное перекрывание функций. Вследствие этого был введен единый термин «интерлейкины» IL (или ИЛ): 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 1 5, 16, 17 …. . 35 Термин «интерлейкины» означает «молекулы, участвующие во взаимоотношениях, «беседах» между лейкоцитами» .
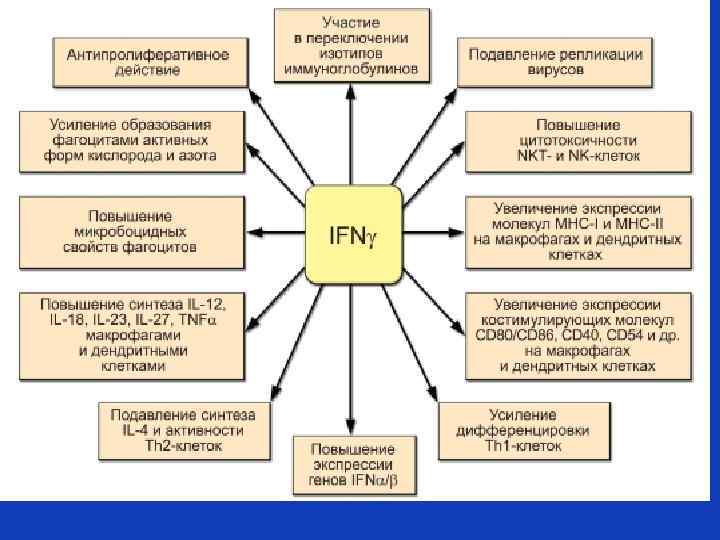
 Основные типы цитокинов –общепринятые сокращения: факторы некроза опухолей (ФНО или TNF) • TNF - (кахектин) • TNF- ( лимфотоксин) • Интерфероны (ИФН или IFN) • IFN и IFN • IFN трансформирующие ростовые факторы: • Трансформирующий ростовый фактор –альфа – TGF - • Трансформирующий ростовый фактор –бета – TGF - -хемокины: • IL-8 • NAP -2 (neutrophil – activating protein -2) • PF -4 (platelet factor 4)
Основные типы цитокинов –общепринятые сокращения: факторы некроза опухолей (ФНО или TNF) • TNF - (кахектин) • TNF- ( лимфотоксин) • Интерфероны (ИФН или IFN) • IFN и IFN • IFN трансформирующие ростовые факторы: • Трансформирующий ростовый фактор –альфа – TGF - • Трансформирующий ростовый фактор –бета – TGF - -хемокины: • IL-8 • NAP -2 (neutrophil – activating protein -2) • PF -4 (platelet factor 4)
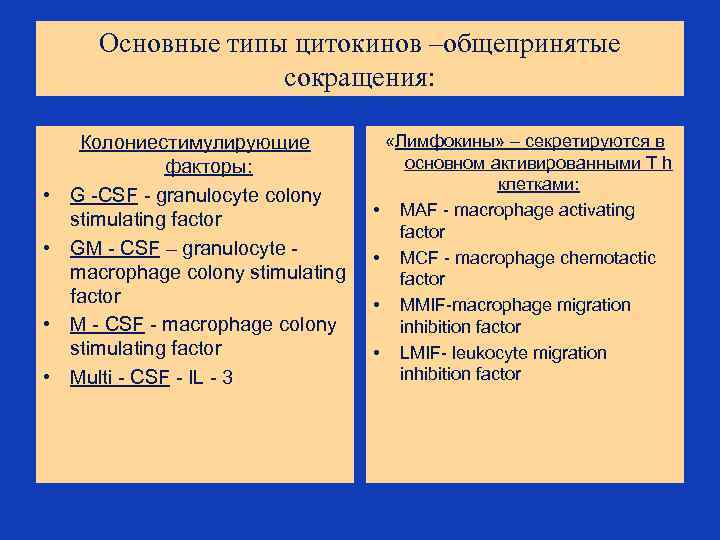 Основные типы цитокинов –общепринятые сокращения: • • Колониестимулирующие факторы: G -CSF - granulocyte colony stimulating factor GM - CSF – granulocyte - macrophage colony stimulating factor M - CSF - macrophage colony stimulating factor Multi - CSF - IL - 3 • • «Лимфокины» – секретируются в основном активированными Т h клетками: MAF - macrophage activating factor MCF - macrophage chemotactic factor MMIF-macrophage migration inhibition factor LMIF- leukocyte migration inhibition factor
Основные типы цитокинов –общепринятые сокращения: • • Колониестимулирующие факторы: G -CSF - granulocyte colony stimulating factor GM - CSF – granulocyte - macrophage colony stimulating factor M - CSF - macrophage colony stimulating factor Multi - CSF - IL - 3 • • «Лимфокины» – секретируются в основном активированными Т h клетками: MAF - macrophage activating factor MCF - macrophage chemotactic factor MMIF-macrophage migration inhibition factor LMIF- leukocyte migration inhibition factor
 Основные типы цитокинов –общепринятые сокращения: Полипептидные ростовые факторы клеток: • a FGF – acidic fibroblast growth factor • b FGF – basic fibroblast growth factor • EGF – epidermal growth factor • NGF – nerve growth factor • PDGF – platelet - derived growth factor • VEGF – vascular endothelial growth factor Современные отечественные книги и журналы
Основные типы цитокинов –общепринятые сокращения: Полипептидные ростовые факторы клеток: • a FGF – acidic fibroblast growth factor • b FGF – basic fibroblast growth factor • EGF – epidermal growth factor • NGF – nerve growth factor • PDGF – platelet - derived growth factor • VEGF – vascular endothelial growth factor Современные отечественные книги и журналы
 Классификация цитокинов на основе их биологических эффектов 1. Интерлейкины (ИЛ-1 ÷ ИЛ- 35) - сигнальные молекулы, действующие между лейкоцитами. 2. Факторы некроза опухоли - цитокины с цитотоксическим и регуляторным действием (ФНО). 3. Интерфероны – противовирусные цитокины: 1 типа –ИФН α, β и др. 2 типа –ИФН γ 4. Факторы роста стволовых клеток (ИЛ-3, ИЛ - 7, ИЛ-11, эритропоэтин, тромбопоэтин, колониестимулирующие факторы (КСФ): ГМКСФ (гранулоцитарно-макрофагальный колониестимулирующий фактор), Г-КСФ (гранулоцитарный КСФ), М-КСФ (макрофагальный КСФ), регулирующие гемопоэз. 5. Хемокины (CC, CXC (ИЛ-8), CX 3 C, С) , регулирующие хемотаксис различных клеток. 6. Факторы роста клеток (фактор роста фибробластов, фактор роста эндотелиальных клеток, фактор роста эпидермиса и др. ), трансформирующий ростовый фактор - участвуют в регуляции роста, дифференцировки разных клеток.
Классификация цитокинов на основе их биологических эффектов 1. Интерлейкины (ИЛ-1 ÷ ИЛ- 35) - сигнальные молекулы, действующие между лейкоцитами. 2. Факторы некроза опухоли - цитокины с цитотоксическим и регуляторным действием (ФНО). 3. Интерфероны – противовирусные цитокины: 1 типа –ИФН α, β и др. 2 типа –ИФН γ 4. Факторы роста стволовых клеток (ИЛ-3, ИЛ - 7, ИЛ-11, эритропоэтин, тромбопоэтин, колониестимулирующие факторы (КСФ): ГМКСФ (гранулоцитарно-макрофагальный колониестимулирующий фактор), Г-КСФ (гранулоцитарный КСФ), М-КСФ (макрофагальный КСФ), регулирующие гемопоэз. 5. Хемокины (CC, CXC (ИЛ-8), CX 3 C, С) , регулирующие хемотаксис различных клеток. 6. Факторы роста клеток (фактор роста фибробластов, фактор роста эндотелиальных клеток, фактор роста эпидермиса и др. ), трансформирующий ростовый фактор - участвуют в регуляции роста, дифференцировки разных клеток.
 Классификация цитокинов на основе их роли в процессе регуляции воспаления Провоспалительные Синтезируются преимущественно активированными клетками моноцитарно/макрофагально го ряда и повышают активность воспалительного процесса. Провоспалительных цитокинов намного больше, чем противовоспалительных. Противовоспалительные В основном, Т- клеточные цитокины, снижающие активность воспаления – • ИЛ-10, • ТГФ β (трансформирующий фактор роста бета); • а также -рецепторный антагонист интерлейкина-1 (РАИЛ).
Классификация цитокинов на основе их роли в процессе регуляции воспаления Провоспалительные Синтезируются преимущественно активированными клетками моноцитарно/макрофагально го ряда и повышают активность воспалительного процесса. Провоспалительных цитокинов намного больше, чем противовоспалительных. Противовоспалительные В основном, Т- клеточные цитокины, снижающие активность воспаления – • ИЛ-10, • ТГФ β (трансформирующий фактор роста бета); • а также -рецепторный антагонист интерлейкина-1 (РАИЛ).
 Цитокины с регуляторной (противовоспалительной) активностью цитокин эффект ИЛ-10 подавляет продукцию цитокинов, подавляет активацию Т-хелперов 1 типа ТРФ - бета 1 (трансформирующий ростовый фактор-бета 1) подавляет активацию Тхелперов 1 и 2 типа, стимулирует рост фибробластов
Цитокины с регуляторной (противовоспалительной) активностью цитокин эффект ИЛ-10 подавляет продукцию цитокинов, подавляет активацию Т-хелперов 1 типа ТРФ - бета 1 (трансформирующий ростовый фактор-бета 1) подавляет активацию Тхелперов 1 и 2 типа, стимулирует рост фибробластов
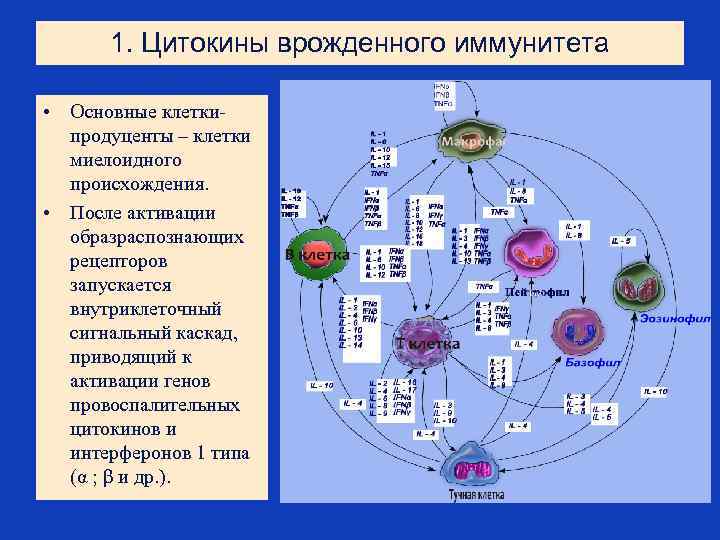 1. Цитокины врожденного иммунитета • Основные клеткипродуценты – клетки миелоидного происхождения. • После активации образраспознающих рецепторов запускается внутриклеточный сигнальный каскад, приводящий к активации генов провоспалительных цитокинов и интерферонов 1 типа (α ; β и др. ).
1. Цитокины врожденного иммунитета • Основные клеткипродуценты – клетки миелоидного происхождения. • После активации образраспознающих рецепторов запускается внутриклеточный сигнальный каскад, приводящий к активации генов провоспалительных цитокинов и интерферонов 1 типа (α ; β и др. ).
 РАСПОЗНАВАНИЕ ПАТОГЕНОВ РЕЦЕПТОРАМИ ВРОЖДЕННОГО ИММУНИТЕТА Патогены Патоген-ассоциированные молекулярные структуры или паттерны (РАМРs) Паттерн распознающие рецепторы (PRRs): 1. Растворимые (система комплемента) 2. Мембранные (TLRs –Толл- подобные рецепторы, CD 14) 3. Внутриклеточные (NOD и др. ).
РАСПОЗНАВАНИЕ ПАТОГЕНОВ РЕЦЕПТОРАМИ ВРОЖДЕННОГО ИММУНИТЕТА Патогены Патоген-ассоциированные молекулярные структуры или паттерны (РАМРs) Паттерн распознающие рецепторы (PRRs): 1. Растворимые (система комплемента) 2. Мембранные (TLRs –Толл- подобные рецепторы, CD 14) 3. Внутриклеточные (NOD и др. ).
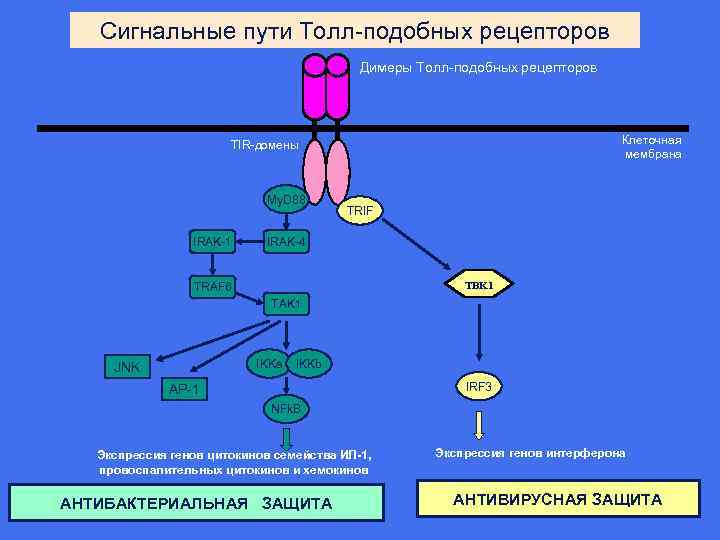 Сигнальные пути Толл-подобных рецепторов Димеры Толл-подобных рецепторов Клеточная мембрана TIR-домены My. D 88 IRAK-1 TRIF IRAK-4 TBK 1 TRAF 6 TAK 1 IKKa JNK IKKb IRF 3 AP-1 NFk. B Экспрессия генов цитокинов семейства ИЛ-1, провоспалительных цитокинов и хемокинов АНТИБАКТЕРИАЛЬНАЯ ЗАЩИТА Экспрессия генов интерферона АНТИВИРУСНАЯ ЗАЩИТА
Сигнальные пути Толл-подобных рецепторов Димеры Толл-подобных рецепторов Клеточная мембрана TIR-домены My. D 88 IRAK-1 TRIF IRAK-4 TBK 1 TRAF 6 TAK 1 IKKa JNK IKKb IRF 3 AP-1 NFk. B Экспрессия генов цитокинов семейства ИЛ-1, провоспалительных цитокинов и хемокинов АНТИБАКТЕРИАЛЬНАЯ ЗАЩИТА Экспрессия генов интерферона АНТИВИРУСНАЯ ЗАЩИТА
 Функциональная активность провоспалительных цитокинов в зависимости от их концентрации –местное и системное действие На местном уровне Самым ранним эффектом провоспалительных цитокинов является повышение адгезивных свойств эндотелия и привлечение активированных клеток в очаг воспаления из периферической крови. Провоспалительные цитокины управляют местным воспалением с его типичными проявлениями (отек, покраснение, появление болевого синдрома). На системном уровне При повышении концентрации провоспалительных цитокинов в крови , они действуют практически на все органы и системы, участвующие в поддержании гомеостаза Примером зависимости эффектов провоспалительных цитокинов от их концентрации в крови может служить фактор некроза опухолей-альфа
Функциональная активность провоспалительных цитокинов в зависимости от их концентрации –местное и системное действие На местном уровне Самым ранним эффектом провоспалительных цитокинов является повышение адгезивных свойств эндотелия и привлечение активированных клеток в очаг воспаления из периферической крови. Провоспалительные цитокины управляют местным воспалением с его типичными проявлениями (отек, покраснение, появление болевого синдрома). На системном уровне При повышении концентрации провоспалительных цитокинов в крови , они действуют практически на все органы и системы, участвующие в поддержании гомеостаза Примером зависимости эффектов провоспалительных цитокинов от их концентрации в крови может служить фактор некроза опухолей-альфа
 УРОВНИ ПРОВОСПАЛИТЕЛЬНЫХ ЦИТОКИНОВ В ПЛАЗМЕ КРОВИ ФНО 10 -7 М 10 -8 М 10 -9 М Местное воспаление Системная воспалительная реакция Септический шок Активация фагоцитоза и продукции кислородных радикалов. Усиление экспрессии молекул адгезии на эндотелии. Стимуляция синтеза цитокинов и хемокинов. Увеличение метаболизма соединительной ткани. Лихорадка. Увеличение уровней стероидных гормонов. Лейкоцитоз. Увеличение синтеза остро-фазовых белков. Снижение сократимос-ти миокарда и гладкомышечных клеток сосудов. Увеличение проницаемости эндотелия. Нарушение микроциркуляции. Падение артериального давления. Гипогликемия.
УРОВНИ ПРОВОСПАЛИТЕЛЬНЫХ ЦИТОКИНОВ В ПЛАЗМЕ КРОВИ ФНО 10 -7 М 10 -8 М 10 -9 М Местное воспаление Системная воспалительная реакция Септический шок Активация фагоцитоза и продукции кислородных радикалов. Усиление экспрессии молекул адгезии на эндотелии. Стимуляция синтеза цитокинов и хемокинов. Увеличение метаболизма соединительной ткани. Лихорадка. Увеличение уровней стероидных гормонов. Лейкоцитоз. Увеличение синтеза остро-фазовых белков. Снижение сократимос-ти миокарда и гладкомышечных клеток сосудов. Увеличение проницаемости эндотелия. Нарушение микроциркуляции. Падение артериального давления. Гипогликемия.
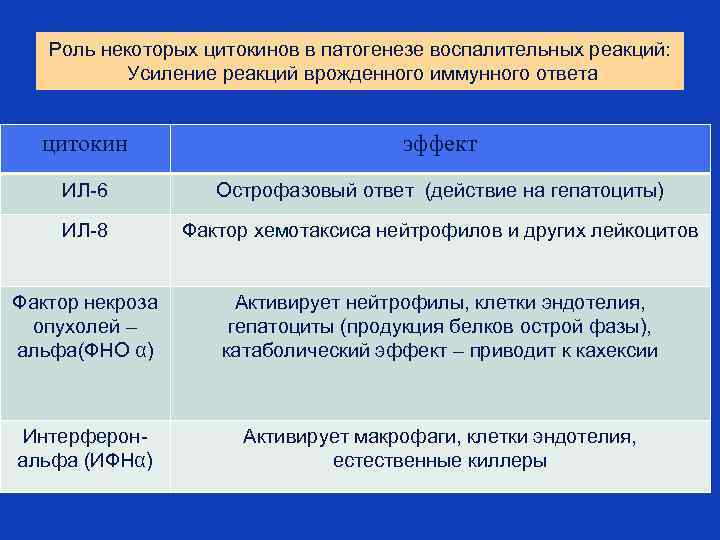 Роль некоторых цитокинов в патогенезе воспалительных реакций: Усиление реакций врожденного иммунного ответа цитокин эффект ИЛ-6 Острофазовый ответ (действие на гепатоциты) ИЛ-8 Фактор хемотаксиса нейтрофилов и других лейкоцитов Фактор некроза опухолей – альфа(ФНО α) Активирует нейтрофилы, клетки эндотелия, гепатоциты (продукция белков острой фазы), катаболический эффект – приводит к кахексии Интерферональфа (ИФНα) Активирует макрофаги, клетки эндотелия, естественные киллеры
Роль некоторых цитокинов в патогенезе воспалительных реакций: Усиление реакций врожденного иммунного ответа цитокин эффект ИЛ-6 Острофазовый ответ (действие на гепатоциты) ИЛ-8 Фактор хемотаксиса нейтрофилов и других лейкоцитов Фактор некроза опухолей – альфа(ФНО α) Активирует нейтрофилы, клетки эндотелия, гепатоциты (продукция белков острой фазы), катаболический эффект – приводит к кахексии Интерферональфа (ИФНα) Активирует макрофаги, клетки эндотелия, естественные киллеры
 Интерлейкин-1 -бета: свойства Клетка - мишень Эффект Макрофаги, фибробласты, остеобласты, эпителий Пролиферация, активация Остеокласты Усиление процессов реабсорбции в костях Гепатоциты Синтез белков острой фазы воспаления Клетки гипоталамуса Синтез простагландинов и последующий подъем температуры тела
Интерлейкин-1 -бета: свойства Клетка - мишень Эффект Макрофаги, фибробласты, остеобласты, эпителий Пролиферация, активация Остеокласты Усиление процессов реабсорбции в костях Гепатоциты Синтез белков острой фазы воспаления Клетки гипоталамуса Синтез простагландинов и последующий подъем температуры тела
 Интерлейкин-1 -бета: свойства Клетка-мишень Эффект Т-лимфоциты Пролиферация, дифференцировка, синтез и секреция цитокинов, повышение уровня экспрессии рецепторов к ИЛ-2 В-лимфоциты Пролиферация, дифференцировка Нейтрофилы Высвобождение из костного мозга, хемотаксис, активация Эндотелий Активация экспрессии молекул адгезии
Интерлейкин-1 -бета: свойства Клетка-мишень Эффект Т-лимфоциты Пролиферация, дифференцировка, синтез и секреция цитокинов, повышение уровня экспрессии рецепторов к ИЛ-2 В-лимфоциты Пролиферация, дифференцировка Нейтрофилы Высвобождение из костного мозга, хемотаксис, активация Эндотелий Активация экспрессии молекул адгезии
 Биологический смысл действия цитокинов при системном воспалении Ø На уровне целостного организма цитокины осуществляют связь между иммунной, нервной, эндокринной, кроветворной и другими системами регуляции гомеостаза и служат для их вовлечения в организацию единой защитной реакции. Ø Цитокины обеспечивают «сигнал тревоги» , означающий, что настало время включить все резервы, переключить энергетические потоки и перестроить работу всех систем для выполнения одной, но важнейшей для выживания задачи – борьбы с внедрившимся патогеном. Примером множественности эффектов провоспалительных цитокинов в запуске системного воспаления может служить интерлейкин 1 бета
Биологический смысл действия цитокинов при системном воспалении Ø На уровне целостного организма цитокины осуществляют связь между иммунной, нервной, эндокринной, кроветворной и другими системами регуляции гомеостаза и служат для их вовлечения в организацию единой защитной реакции. Ø Цитокины обеспечивают «сигнал тревоги» , означающий, что настало время включить все резервы, переключить энергетические потоки и перестроить работу всех систем для выполнения одной, но важнейшей для выживания задачи – борьбы с внедрившимся патогеном. Примером множественности эффектов провоспалительных цитокинов в запуске системного воспаления может служить интерлейкин 1 бета
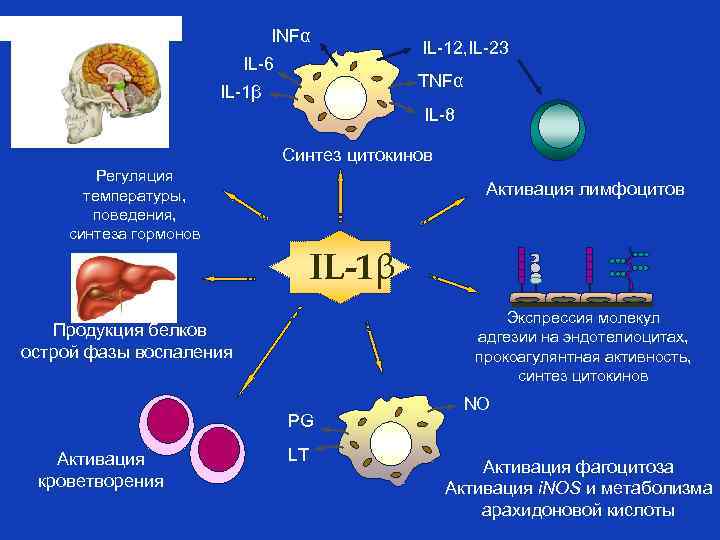 INFα IL-6 IL-12, IL-23 TNFα IL-1β IL-8 Синтез цитокинов Регуляция температуры, поведения, синтеза гормонов Активация лимфоцитов IL-1β Экспрессия молекул адгезии на эндотелиоцитах, прокоагулянтная активность, синтез цитокинов Продукция белков острой фазы воспаления PG Активация кроветворения LT NO Активация фагоцитоза Активация i. NOS и метаболизма арахидоновой кислоты
INFα IL-6 IL-12, IL-23 TNFα IL-1β IL-8 Синтез цитокинов Регуляция температуры, поведения, синтеза гормонов Активация лимфоцитов IL-1β Экспрессия молекул адгезии на эндотелиоцитах, прокоагулянтная активность, синтез цитокинов Продукция белков острой фазы воспаления PG Активация кроветворения LT NO Активация фагоцитоза Активация i. NOS и метаболизма арахидоновой кислоты
 IL-1 и TNF- Интерлейкин -1 – бета(IL-1 ) и фактор некроза опухолей –альфа (TNF- ) играют основную роль в воспалительных ответах, так как введение рецепторного антагониста интерлейкина 1(IL -1 ra) , а также моноклональных антител или растворимых рецепторов TNF- блокирует острые и хронические воспалительные ответы в экспериментах на животных. . Некоторые их таких антагонистов и моноклональных антител уже используются в клинике – например, при лечении сепсиса, ревматоидного артрита, системной красной волчанки и других заболеваний человека.
IL-1 и TNF- Интерлейкин -1 – бета(IL-1 ) и фактор некроза опухолей –альфа (TNF- ) играют основную роль в воспалительных ответах, так как введение рецепторного антагониста интерлейкина 1(IL -1 ra) , а также моноклональных антител или растворимых рецепторов TNF- блокирует острые и хронические воспалительные ответы в экспериментах на животных. . Некоторые их таких антагонистов и моноклональных антител уже используются в клинике – например, при лечении сепсиса, ревматоидного артрита, системной красной волчанки и других заболеваний человека.
 Ростовые факторы цитокин ГМ-КСФ (гранулоцитарно-макрофагальный колониестимулирующий фактор) эффект стимулируют рост и дифференцировку клетокпредшественников М-КСФ моноцитов и (Макрофаг- колониестимулирующий полиморфнофактор) ядерных лейкоцитов Г-КСФ (Гранулоцит- колониестимулирующий фактор)
Ростовые факторы цитокин ГМ-КСФ (гранулоцитарно-макрофагальный колониестимулирующий фактор) эффект стимулируют рост и дифференцировку клетокпредшественников М-КСФ моноцитов и (Макрофаг- колониестимулирующий полиморфнофактор) ядерных лейкоцитов Г-КСФ (Гранулоцит- колониестимулирующий фактор)
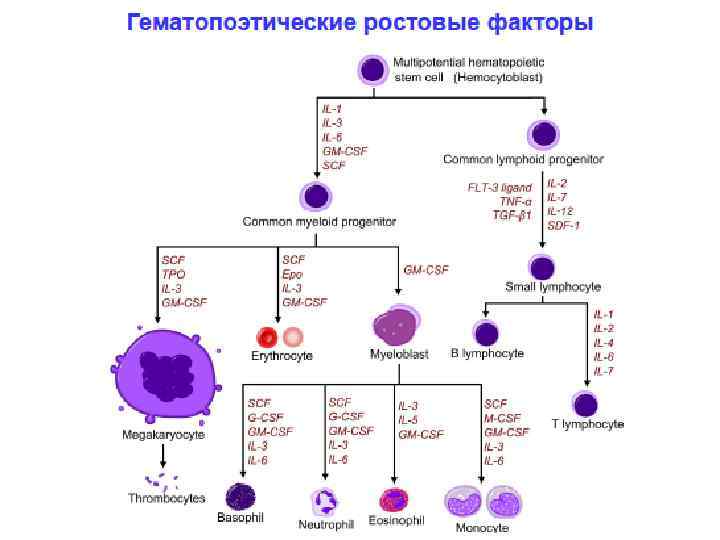
 РЕГУЛЯЦИЯ ПРИОБРЕТЕННОГО ИММУНИТЕТА Цитокины – ростовые и дифференцировочные факторы всех типов Т- и В-лимфоцитов Главные функции: регуляция дифференцировки Т-хелперных клонов - определение типов тканевого воспаления, Т-клеток эффекторов и классов антител Тh 1 – клеточный тип с участием макрофагов и Т-лимфоцитов (гранулема при туберкулезе; при саркоидозе, контактном дерматите, болезни Крона) Тh 2 – аллергический тип ответа с участием гистамина и простагландинов Т h 17 – нейтрофильное воспаление Tfn (фолликулярные Т хелперы)- гуморальный иммунный ответ T reg –T h регуляторный (ограничение силы всех типов иммунного ответа и воспаления)
РЕГУЛЯЦИЯ ПРИОБРЕТЕННОГО ИММУНИТЕТА Цитокины – ростовые и дифференцировочные факторы всех типов Т- и В-лимфоцитов Главные функции: регуляция дифференцировки Т-хелперных клонов - определение типов тканевого воспаления, Т-клеток эффекторов и классов антител Тh 1 – клеточный тип с участием макрофагов и Т-лимфоцитов (гранулема при туберкулезе; при саркоидозе, контактном дерматите, болезни Крона) Тh 2 – аллергический тип ответа с участием гистамина и простагландинов Т h 17 – нейтрофильное воспаление Tfn (фолликулярные Т хелперы)- гуморальный иммунный ответ T reg –T h регуляторный (ограничение силы всех типов иммунного ответа и воспаления)
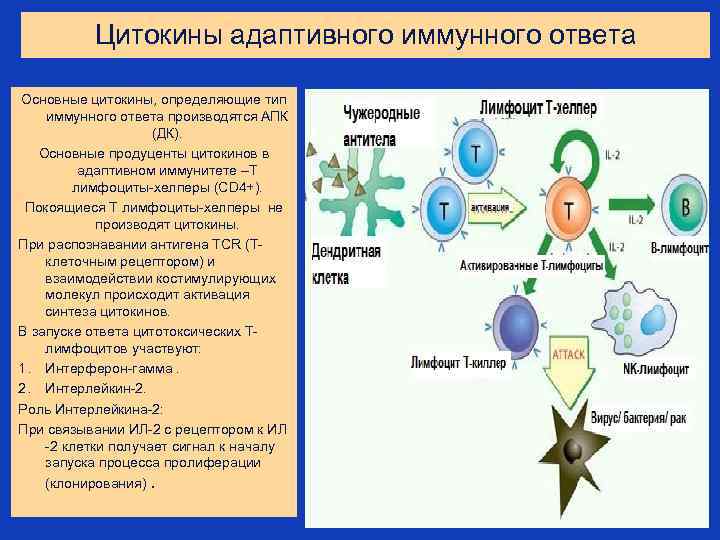 Цитокины адаптивного иммунного ответа Основные цитокины, определяющие тип иммунного ответа производятся АПК (ДК). Основные продуценты цитокинов в адаптивном иммунитете –Т лимфоциты-хелперы (CD 4+). Покоящиеся Т лимфоциты-хелперы не производят цитокины. При распознавании антигена TCR (Тклеточным рецептором) и взаимодействии костимулирующих молекул происходит активация синтеза цитокинов. В запуске ответа цитотоксических Тлимфоцитов участвуют: 1. Интерферон-гамма. 2. Интерлейкин-2. Роль Интерлейкина-2: При связывании ИЛ-2 с рецептором к ИЛ -2 клетки получает сигнал к началу запуска процесса пролиферации (клонирования).
Цитокины адаптивного иммунного ответа Основные цитокины, определяющие тип иммунного ответа производятся АПК (ДК). Основные продуценты цитокинов в адаптивном иммунитете –Т лимфоциты-хелперы (CD 4+). Покоящиеся Т лимфоциты-хелперы не производят цитокины. При распознавании антигена TCR (Тклеточным рецептором) и взаимодействии костимулирующих молекул происходит активация синтеза цитокинов. В запуске ответа цитотоксических Тлимфоцитов участвуют: 1. Интерферон-гамма. 2. Интерлейкин-2. Роль Интерлейкина-2: При связывании ИЛ-2 с рецептором к ИЛ -2 клетки получает сигнал к началу запуска процесса пролиферации (клонирования).
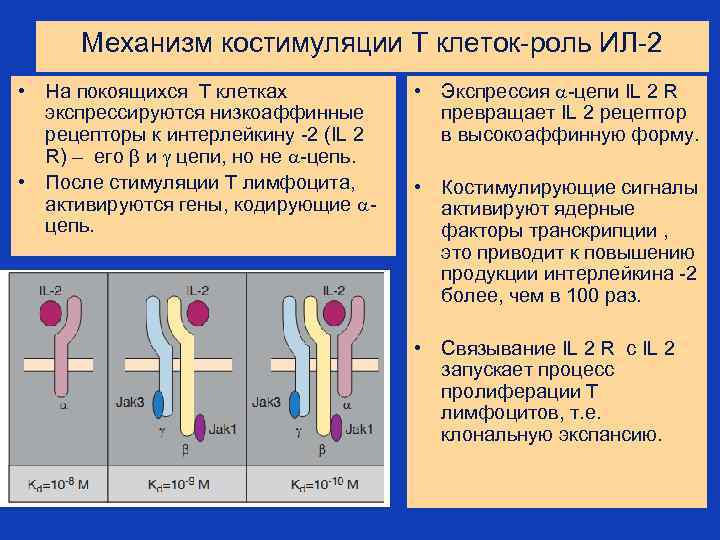 Механизм костимуляции Т клеток-роль ИЛ-2 • На покоящихся Т клетках экспрессируются низкоаффинные рецепторы к интерлейкину -2 (IL 2 R) – его и цепи, но не -цепь. • После стимуляции Т лимфоцита, активируются гены, кодирующие цепь. • Экспрессия -цепи IL 2 R превращает IL 2 рецептор в высокоаффинную форму. • Костимулирующие сигналы активируют ядерные факторы транскрипции , это приводит к повышению продукции интерлейкина -2 более, чем в 100 раз. • Связывание IL 2 R с IL 2 запускает процесс пролиферации Т лимфоцитов, т. е. клональную экспансию.
Механизм костимуляции Т клеток-роль ИЛ-2 • На покоящихся Т клетках экспрессируются низкоаффинные рецепторы к интерлейкину -2 (IL 2 R) – его и цепи, но не -цепь. • После стимуляции Т лимфоцита, активируются гены, кодирующие цепь. • Экспрессия -цепи IL 2 R превращает IL 2 рецептор в высокоаффинную форму. • Костимулирующие сигналы активируют ядерные факторы транскрипции , это приводит к повышению продукции интерлейкина -2 более, чем в 100 раз. • Связывание IL 2 R с IL 2 запускает процесс пролиферации Т лимфоцитов, т. е. клональную экспансию.
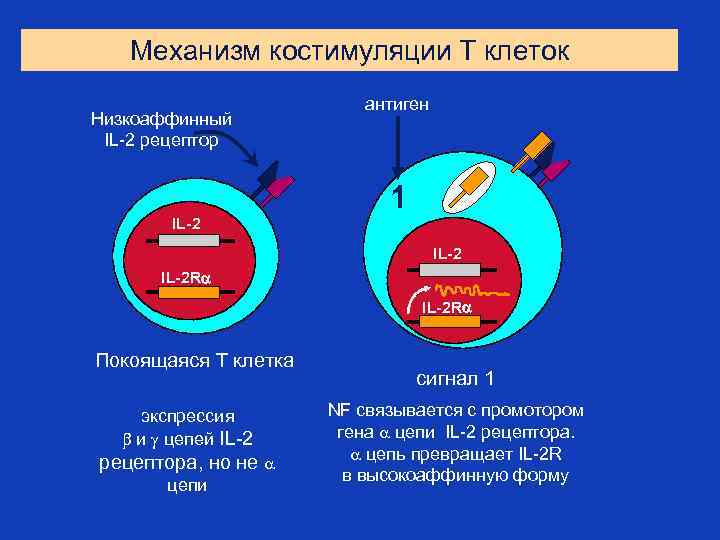 Механизм костимуляции Т клеток Низкоаффинный IL-2 рецептор антиген 1 IL-2 R Покоящаяся Т клетка экспрессия и цепей IL-2 рецептора, но не цепи сигнал 1 NF связывается с промотором гена цепи IL-2 рецептора. цепь превращает IL-2 R в высокоаффинную форму
Механизм костимуляции Т клеток Низкоаффинный IL-2 рецептор антиген 1 IL-2 R Покоящаяся Т клетка экспрессия и цепей IL-2 рецептора, но не цепи сигнал 1 NF связывается с промотором гена цепи IL-2 рецептора. цепь превращает IL-2 R в высокоаффинную форму
 Роль цитокинов в усилении реакций адаптивного иммунного ответа: активация, пролиферация и дифференцировка лимфоцитов цитокин эффект ИЛ-2 Пролиферация и созревание Т-клеток, повышение уровня экспрессии рецептора к ИЛ-2 ИЛ-4 Повышение уровня экспрессии молекул МНС II класса, Fc-рецепторов и рецепторов к ИЛ-2 на поверхности Т- и В-лимфоцитов. Способствует переключению классов Ig на Ig. Eизотип. ИЛ-6 Созревание и дифференцировка Т- и Влимфоцитов
Роль цитокинов в усилении реакций адаптивного иммунного ответа: активация, пролиферация и дифференцировка лимфоцитов цитокин эффект ИЛ-2 Пролиферация и созревание Т-клеток, повышение уровня экспрессии рецептора к ИЛ-2 ИЛ-4 Повышение уровня экспрессии молекул МНС II класса, Fc-рецепторов и рецепторов к ИЛ-2 на поверхности Т- и В-лимфоцитов. Способствует переключению классов Ig на Ig. Eизотип. ИЛ-6 Созревание и дифференцировка Т- и Влимфоцитов
 «Старая» парадигма поляризации иммунного ответа: путь Th 1(клеточный ответ) или путь Th 2(гуморальный ответ). После созревания в тимусе наивные CD 4+Т лимфоциты –хелперы (Th 0) дифференцируются на периферии в эффекторные клетки - Th 1 или Th 2: • Th 1 запускают клеточный ответ, • Th 2 –гуморальный. ответ. «Уникальная особенность иммунологии состоит в том, что ее «сердцевина» не вполне стабилизировалась и меняется во времени в большей степени, чем основы других наук. Достаточно сказать, что на протяжении полувека парадигма иммунологии менялась по меньшей мере два раза — сначала при рождении «неинфекционной» (по преимуществу клеточной) иммунологии в 50– 60 -е годы ХХ века и затем — совсем недавно, при формировании новых представлений об иерархии и взаимодействии врожденного и адаптивного иммунитета. Читатели с большим стажем знакомства с руководствами и учебниками по иммунологии, написанными в разное время, согласятся, что книги по иммунологии, опубликованные в 30 -х, 60 -х и 2000 -х годах, порой как будто излагают основы разных наук» А. А. Ярилин, 2010 год.
«Старая» парадигма поляризации иммунного ответа: путь Th 1(клеточный ответ) или путь Th 2(гуморальный ответ). После созревания в тимусе наивные CD 4+Т лимфоциты –хелперы (Th 0) дифференцируются на периферии в эффекторные клетки - Th 1 или Th 2: • Th 1 запускают клеточный ответ, • Th 2 –гуморальный. ответ. «Уникальная особенность иммунологии состоит в том, что ее «сердцевина» не вполне стабилизировалась и меняется во времени в большей степени, чем основы других наук. Достаточно сказать, что на протяжении полувека парадигма иммунологии менялась по меньшей мере два раза — сначала при рождении «неинфекционной» (по преимуществу клеточной) иммунологии в 50– 60 -е годы ХХ века и затем — совсем недавно, при формировании новых представлений об иерархии и взаимодействии врожденного и адаптивного иммунитета. Читатели с большим стажем знакомства с руководствами и учебниками по иммунологии, написанными в разное время, согласятся, что книги по иммунологии, опубликованные в 30 -х, 60 -х и 2000 -х годах, порой как будто излагают основы разных наук» А. А. Ярилин, 2010 год.
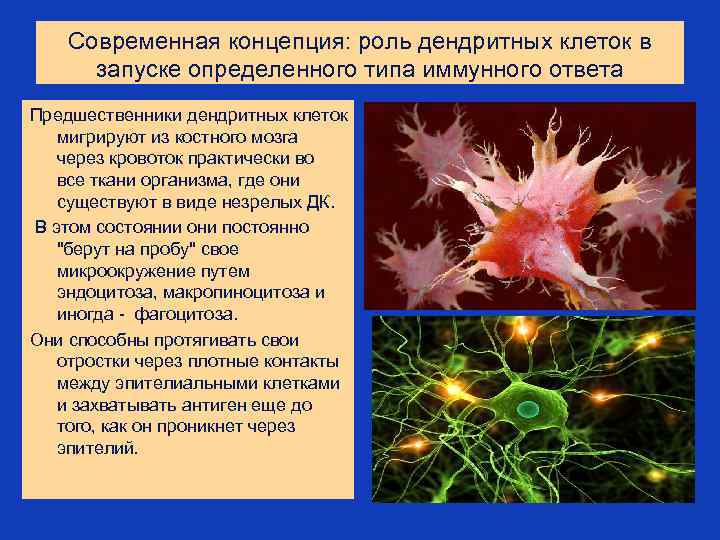 Современная концепция: роль дендритных клеток в запуске определенного типа иммунного ответа Предшественники дендритных клеток мигрируют из костного мозга через кровоток практически во все ткани организма, где они существуют в виде незрелых ДК. В этом состоянии они постоянно "берут на пробу" свое микроокружение путем эндоцитоза, макропиноцитоза и иногда - фагоцитоза. Они способны протягивать свои отростки через плотные контакты между эпителиальными клетками и захватывать антиген еще до того, как он проникнет через эпителий.
Современная концепция: роль дендритных клеток в запуске определенного типа иммунного ответа Предшественники дендритных клеток мигрируют из костного мозга через кровоток практически во все ткани организма, где они существуют в виде незрелых ДК. В этом состоянии они постоянно "берут на пробу" свое микроокружение путем эндоцитоза, макропиноцитоза и иногда - фагоцитоза. Они способны протягивать свои отростки через плотные контакты между эпителиальными клетками и захватывать антиген еще до того, как он проникнет через эпителий.
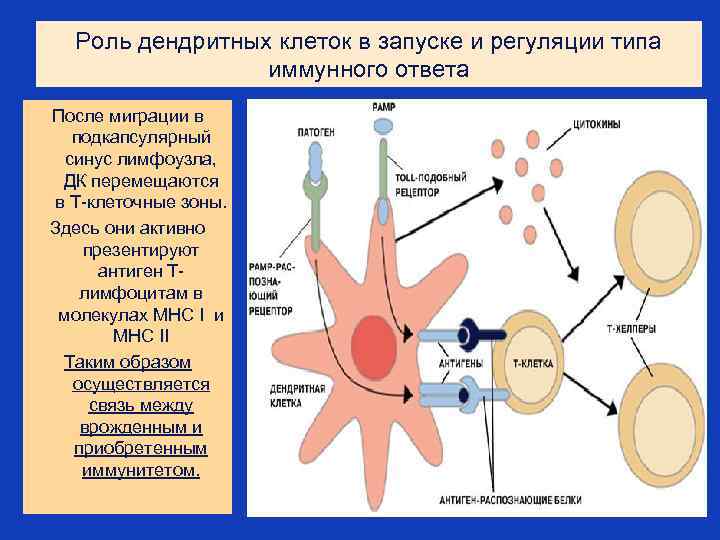 Роль дендритных клеток в запуске и регуляции типа иммунного ответа После миграции в подкапсулярный синус лимфоузла, ДК перемещаются в Т-клеточные зоны. Здесь они активно презентируют антиген Тлимфоцитам в молекулах MHC I и MHC II Таким образом осуществляется связь между врожденным и приобретенным иммунитетом.
Роль дендритных клеток в запуске и регуляции типа иммунного ответа После миграции в подкапсулярный синус лимфоузла, ДК перемещаются в Т-клеточные зоны. Здесь они активно презентируют антиген Тлимфоцитам в молекулах MHC I и MHC II Таким образом осуществляется связь между врожденным и приобретенным иммунитетом.
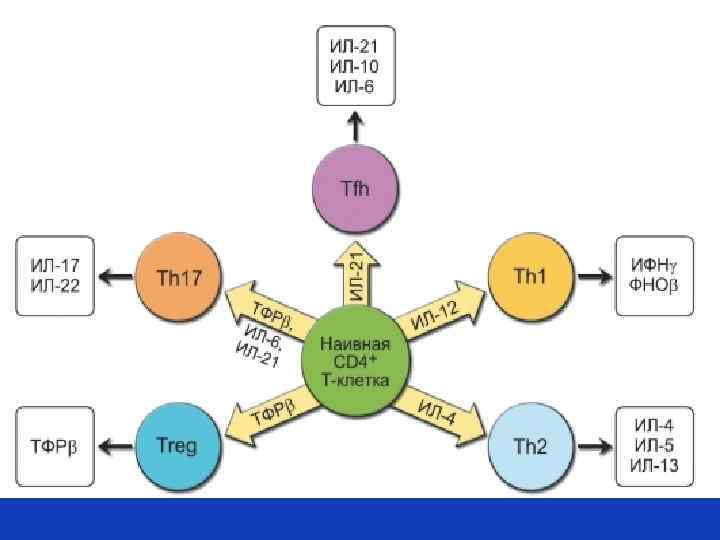
 Субпопуляции Т хелперов, дифференцирующиеся из Th 0 –наивного Т хелпера под действием цитокинов дендритных клеток (ДК) РОЛЬ синтезируемых ДК цитокинов в формировании оптимального типа адаптивного иммунного ответа: Разные типы цитокинов, синтезируемые ДК, направляют дифференцировку Т наивного хелпера по пути либо Th 1, либо Th 2, либо. Th 17, либо. Th 9, либо Th 22 – в зависимости от необходимости развития наиболее оптимального для данного патогена типа иммунного ответа с целью его скорейшей элиминации из организма. После дифференцировки Т наивного хелпера в один из перечисленных типов хелперов, строго регламентируется тип синтезируемых этими типами хелперов цитокинов. По профилю продуцируемых цитокинов выделяют следующие субпопуляции CD 4+ лимфоцитов: Th 1, Th 2, Th 17, Th fn, Th 9, Th 22, а также индуцибельные регуляторные Т-клетки (i. Treg). Биологический смысл столь сложной регуляции типов адаптивного иммунного ответа: уникальный набор цитокинов каждого типа Т хелперов действует на разные клетки-мишени, которые обеспечивают элиминацию патогенов с разными типами паразитирования.
Субпопуляции Т хелперов, дифференцирующиеся из Th 0 –наивного Т хелпера под действием цитокинов дендритных клеток (ДК) РОЛЬ синтезируемых ДК цитокинов в формировании оптимального типа адаптивного иммунного ответа: Разные типы цитокинов, синтезируемые ДК, направляют дифференцировку Т наивного хелпера по пути либо Th 1, либо Th 2, либо. Th 17, либо. Th 9, либо Th 22 – в зависимости от необходимости развития наиболее оптимального для данного патогена типа иммунного ответа с целью его скорейшей элиминации из организма. После дифференцировки Т наивного хелпера в один из перечисленных типов хелперов, строго регламентируется тип синтезируемых этими типами хелперов цитокинов. По профилю продуцируемых цитокинов выделяют следующие субпопуляции CD 4+ лимфоцитов: Th 1, Th 2, Th 17, Th fn, Th 9, Th 22, а также индуцибельные регуляторные Т-клетки (i. Treg). Биологический смысл столь сложной регуляции типов адаптивного иммунного ответа: уникальный набор цитокинов каждого типа Т хелперов действует на разные клетки-мишени, которые обеспечивают элиминацию патогенов с разными типами паразитирования.
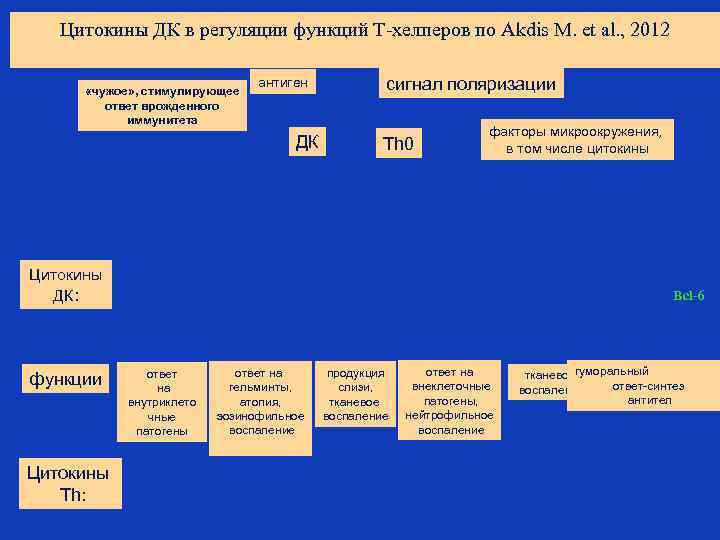 Цитокины ДК в регуляции функций Т-хелперов по Akdis M. et al. , 2012 «чужое» , стимулирующее ответ врожденного иммунитета антиген ДК сигнал поляризации Th 0 факторы микроокружения, в том числе цитокины Цитокины ДК: функции Цитокины Th: Bcl-6 ответ на внутриклето чные патогены ответ на гельминты, атопия, эозинофильное воспаление продукция слизи, тканевое воспаление ответ на внеклеточные патогены, нейтрофильное воспаление тканевоегуморальный ответ-синтез воспаление антител
Цитокины ДК в регуляции функций Т-хелперов по Akdis M. et al. , 2012 «чужое» , стимулирующее ответ врожденного иммунитета антиген ДК сигнал поляризации Th 0 факторы микроокружения, в том числе цитокины Цитокины ДК: функции Цитокины Th: Bcl-6 ответ на внутриклето чные патогены ответ на гельминты, атопия, эозинофильное воспаление продукция слизи, тканевое воспаление ответ на внеклеточные патогены, нейтрофильное воспаление тканевоегуморальный ответ-синтез воспаление антител
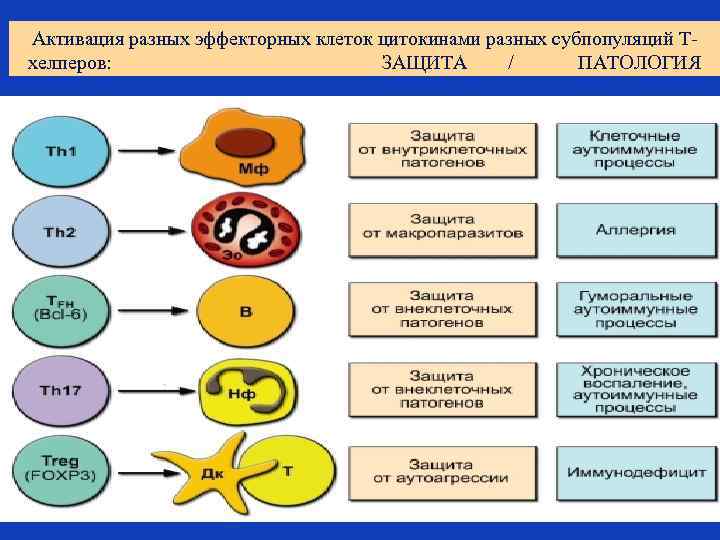 Активация разных эффекторных клеток цитокинами разных субпопуляций Тхелперов: ЗАЩИТА / ПАТОЛОГИЯ
Активация разных эффекторных клеток цитокинами разных субпопуляций Тхелперов: ЗАЩИТА / ПАТОЛОГИЯ
 Субпопуляции Т-хелперов Th 17 Если в микроокружении наивного Т хелпера присутствуют ИЛ-1β и ИЛ-23, то образуются Т – лимфоциты-хелперы, синтезирующие ИЛ-17. Th 17 участвуют в развитии нейтрофильного воспаления на внеклеточные патогены, в том числе, в противогрибковом ответе, а также в развитии аутоиммунных процессов. Th fn (T-follicular helper) CD 4+ fn выполняют хелперную функцию в отношении В лимфоцитов. Локализуются в В-клеточных фолликулах. Вырабатывают хелперный цитокин ИЛ-21, стимулирующий через рецептор к ИЛ-21 на Влимфоцитах, их активацию и дифференцировку в плазматические клетки, синтезирующие антитела.
Субпопуляции Т-хелперов Th 17 Если в микроокружении наивного Т хелпера присутствуют ИЛ-1β и ИЛ-23, то образуются Т – лимфоциты-хелперы, синтезирующие ИЛ-17. Th 17 участвуют в развитии нейтрофильного воспаления на внеклеточные патогены, в том числе, в противогрибковом ответе, а также в развитии аутоиммунных процессов. Th fn (T-follicular helper) CD 4+ fn выполняют хелперную функцию в отношении В лимфоцитов. Локализуются в В-клеточных фолликулах. Вырабатывают хелперный цитокин ИЛ-21, стимулирующий через рецептор к ИЛ-21 на Влимфоцитах, их активацию и дифференцировку в плазматические клетки, синтезирующие антитела.
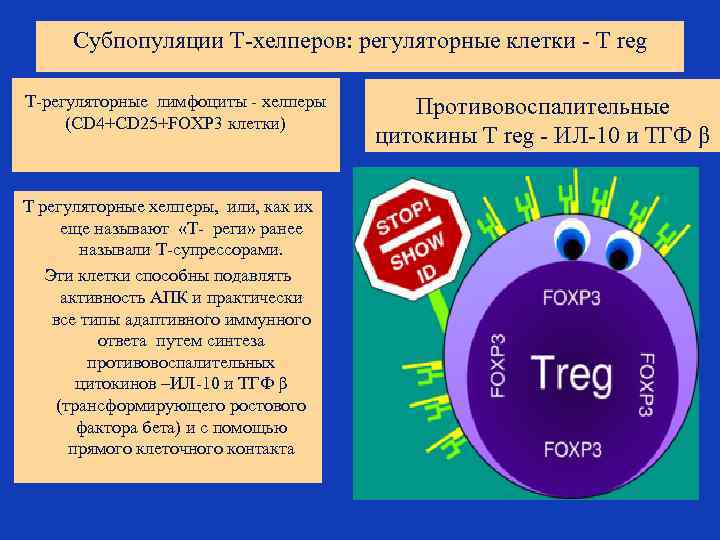 Субпопуляции Т-хелперов: регуляторные клетки - T reg Т-регуляторные лимфоциты - хелперы (CD 4+CD 25+FOXP 3 клетки) Т регуляторные хелперы, или, как их еще называют «Т- реги» ранее называли Т-супрессорами. Эти клетки способны подавлять активность АПК и практически все типы адаптивного иммунного ответа путем синтеза противовоспалительных цитокинов –ИЛ-10 и ТГФ β (трансформирующего ростового фактора бета) и с помощью прямого клеточного контакта Противовоспалительные цитокины T reg - ИЛ-10 и ТГФ β
Субпопуляции Т-хелперов: регуляторные клетки - T reg Т-регуляторные лимфоциты - хелперы (CD 4+CD 25+FOXP 3 клетки) Т регуляторные хелперы, или, как их еще называют «Т- реги» ранее называли Т-супрессорами. Эти клетки способны подавлять активность АПК и практически все типы адаптивного иммунного ответа путем синтеза противовоспалительных цитокинов –ИЛ-10 и ТГФ β (трансформирующего ростового фактора бета) и с помощью прямого клеточного контакта Противовоспалительные цитокины T reg - ИЛ-10 и ТГФ β
 Механизмы действия цитокинов На первом этапе: На последующих этапах: Цитокины взаимодействуют с высокоаффинными рецепторами, расположенными на мембране клеток-мишеней (аффинность –сила связи вещества с его рецептором). Цитокиновые рецепторы – трансмембранные гликопротеины, включающие несколько цепей. Цитокины регулируют транскрипцию генов в клеткахмишенях с помощью вторичных сигналов. Действие вторичных сигналов изменяет транскрипцию генов в клетках –мишенях (активирует или ингибирует), что приводит к изменению «поведения» клетки-мишени в целом.
Механизмы действия цитокинов На первом этапе: На последующих этапах: Цитокины взаимодействуют с высокоаффинными рецепторами, расположенными на мембране клеток-мишеней (аффинность –сила связи вещества с его рецептором). Цитокиновые рецепторы – трансмембранные гликопротеины, включающие несколько цепей. Цитокины регулируют транскрипцию генов в клеткахмишенях с помощью вторичных сигналов. Действие вторичных сигналов изменяет транскрипцию генов в клетках –мишенях (активирует или ингибирует), что приводит к изменению «поведения» клетки-мишени в целом.
 Классификация цитокинов по типу рецепторов. Цитокиновые рецепторы по их структуре подразделяют как минимум на 5 семейств: 1. Рецепторы цитокинов семейства гематопоэтинов интерлейкинов (ИЛ 2, 3, 4, 5, 7, 11, 15 и др. ). 2. Рецепторы, относящиеся к суперсемейству иммуноглобулиновых молекул (рецепторы ИЛ-1, М-КСФ, рецептор фактора роста стволовых клеток). 3. Рецепторы семейства фактора некроза опухолей (наличие домена смерти). 4. Рецепторы семейства интерферонов и ИЛ-10. 5. Рецепторы хемокинов.
Классификация цитокинов по типу рецепторов. Цитокиновые рецепторы по их структуре подразделяют как минимум на 5 семейств: 1. Рецепторы цитокинов семейства гематопоэтинов интерлейкинов (ИЛ 2, 3, 4, 5, 7, 11, 15 и др. ). 2. Рецепторы, относящиеся к суперсемейству иммуноглобулиновых молекул (рецепторы ИЛ-1, М-КСФ, рецептор фактора роста стволовых клеток). 3. Рецепторы семейства фактора некроза опухолей (наличие домена смерти). 4. Рецепторы семейства интерферонов и ИЛ-10. 5. Рецепторы хемокинов.
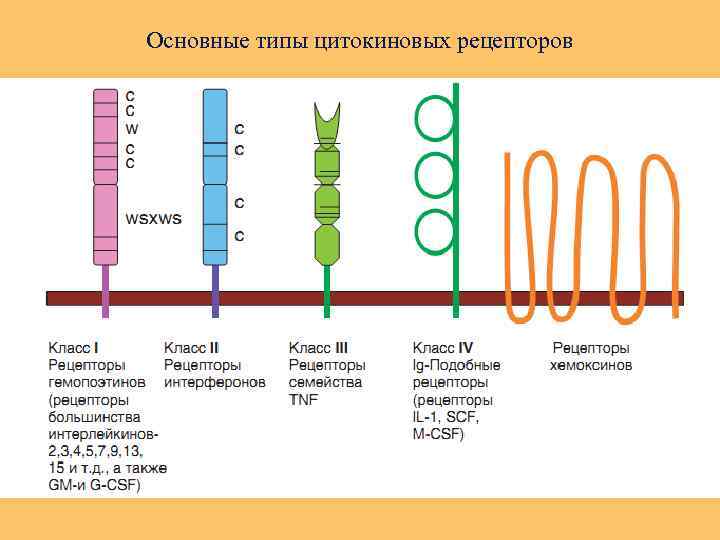 Основные типы цитокиновых рецепторов
Основные типы цитокиновых рецепторов

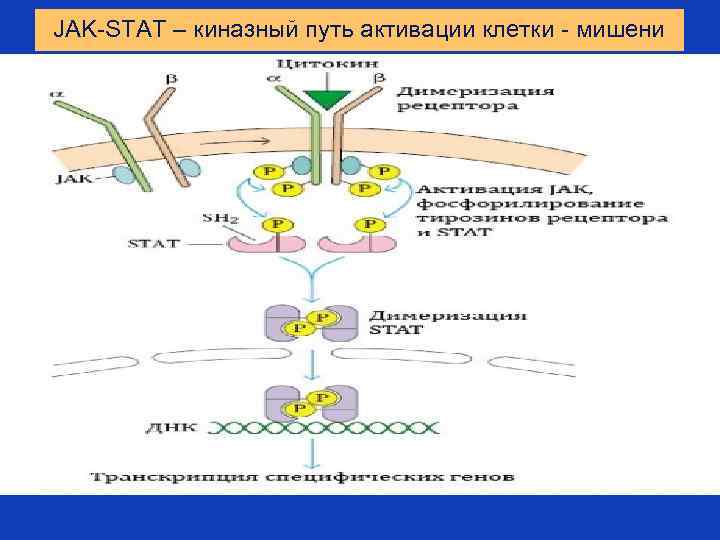 JAK-STAT – киназный путь активации клетки - мишени
JAK-STAT – киназный путь активации клетки - мишени
 Цитокиновая сеть Межклеточная сигнальная сеть, в которой сигналы от отдельных цитокинов обычно трансформируются (не обязательно все свойства цитокинов, проявляющиеся в условиях in vitro, будут проявляться in vivo в условиях цитокиновой сети). • В сети реальные функции того или иного цитокина зависят от типа суммарных регуляторных воздействий на клетку-мишень , а не от отдельных свойств данного цитокина. • Цитокиновая сеть - сеть коммуникационных сигналов между клетками иммунной системы и другими органами.
Цитокиновая сеть Межклеточная сигнальная сеть, в которой сигналы от отдельных цитокинов обычно трансформируются (не обязательно все свойства цитокинов, проявляющиеся в условиях in vitro, будут проявляться in vivo в условиях цитокиновой сети). • В сети реальные функции того или иного цитокина зависят от типа суммарных регуляторных воздействий на клетку-мишень , а не от отдельных свойств данного цитокина. • Цитокиновая сеть - сеть коммуникационных сигналов между клетками иммунной системы и другими органами.
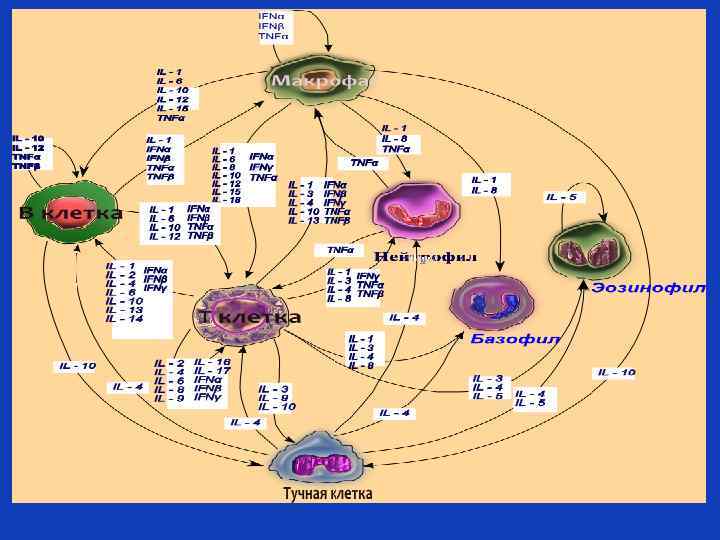
 Хемокины • Хемокины – это цитокины, обладающие малой молекулярной массой (8 -10 к. Да) и влияющие на хемотаксис лейкоцитов. • Малая молекулярная масса обеспечивает им высокую диффузионную способность и формирует градиент концентрации, уменьшающийся о мере отдаления от места их синтеза – феномен, лежащий в основе хемоаатракции. Характеристика структуры хемокинов и их семейств: • м. м. = 5 -20 k. Da • катионные белки • связывают гепарин и гликозаминогликаны • имеют между собой 20 -70% гомологии • содержат преимущественно четыре консервативных цистеина, связанных между собой дисульфидными связями: первый с третьим, второй с четвертым (называют их семейства –по расположению цистеина- СС, СХС и др. )
Хемокины • Хемокины – это цитокины, обладающие малой молекулярной массой (8 -10 к. Да) и влияющие на хемотаксис лейкоцитов. • Малая молекулярная масса обеспечивает им высокую диффузионную способность и формирует градиент концентрации, уменьшающийся о мере отдаления от места их синтеза – феномен, лежащий в основе хемоаатракции. Характеристика структуры хемокинов и их семейств: • м. м. = 5 -20 k. Da • катионные белки • связывают гепарин и гликозаминогликаны • имеют между собой 20 -70% гомологии • содержат преимущественно четыре консервативных цистеина, связанных между собой дисульфидными связями: первый с третьим, второй с четвертым (называют их семейства –по расположению цистеина- СС, СХС и др. )
 БИОЛОГИЧЕСКИЕ ФУНКЦИИ ХЕМОКИНОВ • ХЕМОТАКСИС ЛЕЙКОЦИТОВ • ДЕГРАНУЛЯЦИЯ ЛЕЙКОЦИТОВ • АКТИВАЦИЯ РЕСПИРАТОРНОГО ВЗРЫВА • АКТИВАЦИЯ ИНТЕГРИНОВ Общая биологическая активность: хемоаттрактанты. • Хемокины привлекают: – СХС хемокины – нейтрофилы и Тлимфоциты – СС хемокины – моноциты, базофилы и эозинофилы
БИОЛОГИЧЕСКИЕ ФУНКЦИИ ХЕМОКИНОВ • ХЕМОТАКСИС ЛЕЙКОЦИТОВ • ДЕГРАНУЛЯЦИЯ ЛЕЙКОЦИТОВ • АКТИВАЦИЯ РЕСПИРАТОРНОГО ВЗРЫВА • АКТИВАЦИЯ ИНТЕГРИНОВ Общая биологическая активность: хемоаттрактанты. • Хемокины привлекают: – СХС хемокины – нейтрофилы и Тлимфоциты – СС хемокины – моноциты, базофилы и эозинофилы
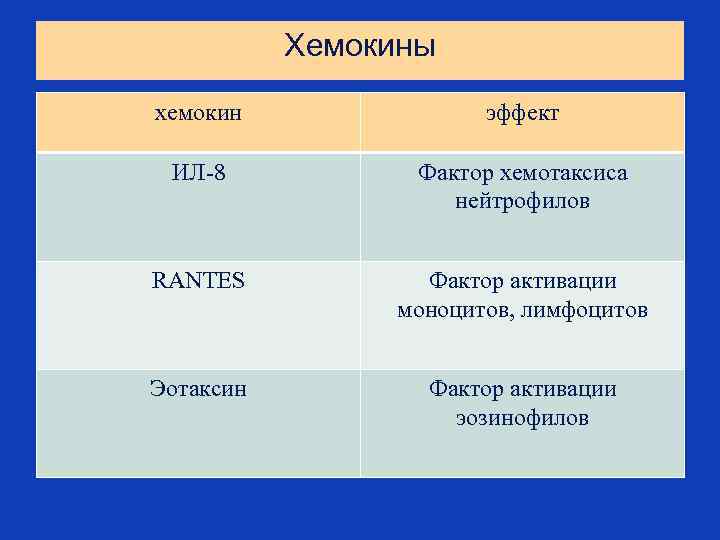 Хемокины хемокин эффект ИЛ-8 Фактор хемотаксиса нейтрофилов RANTES Фактор активации моноцитов, лимфоцитов Эотаксин Фактор активации эозинофилов
Хемокины хемокин эффект ИЛ-8 Фактор хемотаксиса нейтрофилов RANTES Фактор активации моноцитов, лимфоцитов Эотаксин Фактор активации эозинофилов
 Основные направления современной цитокиновой терапии Цитокиновая терапия Использование препаратов цитокинов с целью повышения их концентрации в организме: Заместительная терапия – восполнение недостатка эндогенных цитокинов, в т. ч. генотерапия первичных иммунодефицитов. Иммуностимулирующее действие – при вторичных иммунодефицитных состояниях, вызванных инфекциями. Иммуномодулирующее действие - коррекция дисбаланса эндогенных цитокинов. Антицитокиновая терапия Использование рецепторов цитокинов; моноклональных антител, блокирующих нежелательное действие цитокинов. Удаление или блокирование действия эндогенных цитокинов.
Основные направления современной цитокиновой терапии Цитокиновая терапия Использование препаратов цитокинов с целью повышения их концентрации в организме: Заместительная терапия – восполнение недостатка эндогенных цитокинов, в т. ч. генотерапия первичных иммунодефицитов. Иммуностимулирующее действие – при вторичных иммунодефицитных состояниях, вызванных инфекциями. Иммуномодулирующее действие - коррекция дисбаланса эндогенных цитокинов. Антицитокиновая терапия Использование рецепторов цитокинов; моноклональных антител, блокирующих нежелательное действие цитокинов. Удаление или блокирование действия эндогенных цитокинов.
 РАЗРЕШЕННЫЕ К ПРИМЕНЕНИЮ И РАЗРАБАТЫВАЕМЫЕ ПРЕПАРАТЫ НА ОСНОВЕ РЕКОМБИНАНТНЫХ ЦИТОКИНОВ ЧЕЛОВЕКА • • • • Эритропоэтин Гранулоцитарный колониестимулирующий фактор (Г-КСФ) Гранулоцитарно-моноцитарный колониестимулирующий фактор (ГМ-КСФ) Интерферон альфа, лямбда, в т. ч. ПЕГилированные (ИФН 1 и 3 типа) Интерферон гамма Интерлейкин-1 бета Интерлейкин-2 Интерлейкин-7 Интерлейкин-10 Интерлейкин-15 Интерлейкин-17 Интерлейкин-21 Эпидермальный ростовой фактор Bone morphogenetic proteins (BMP-2, BMP-7)
РАЗРЕШЕННЫЕ К ПРИМЕНЕНИЮ И РАЗРАБАТЫВАЕМЫЕ ПРЕПАРАТЫ НА ОСНОВЕ РЕКОМБИНАНТНЫХ ЦИТОКИНОВ ЧЕЛОВЕКА • • • • Эритропоэтин Гранулоцитарный колониестимулирующий фактор (Г-КСФ) Гранулоцитарно-моноцитарный колониестимулирующий фактор (ГМ-КСФ) Интерферон альфа, лямбда, в т. ч. ПЕГилированные (ИФН 1 и 3 типа) Интерферон гамма Интерлейкин-1 бета Интерлейкин-2 Интерлейкин-7 Интерлейкин-10 Интерлейкин-15 Интерлейкин-17 Интерлейкин-21 Эпидермальный ростовой фактор Bone morphogenetic proteins (BMP-2, BMP-7)
 ОБЛАСТИ ПРИМЕНЕНИЯ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА(ЭПО) • НЕФРОЛОГИЯ - дефицит ЭПО у больных ХПН • ОНКОЛОГИЯ - анемия у больных, получающих радио- и химиотерапию • ИНФЕКЦИОННЫЕ БОЛЕЗНИ - анемия вызванная применением ВААРТ у ВИЧ-пациентов • РЕВМАТОЛОГИЯ - анемия у больных ревматоидным артритом • ХИРУРГИЯ - применение ЭПО для уменьшения объема переливаемой крови • АКУШЕРСТВО - лечение анемии беременных • ПЕДИАТРИЯ - лечение анемии недоношенных новорожденных, нейропротекторное действие
ОБЛАСТИ ПРИМЕНЕНИЯ РЕКОМБИНАНТНОГО ЭРИТРОПОЭТИНА(ЭПО) • НЕФРОЛОГИЯ - дефицит ЭПО у больных ХПН • ОНКОЛОГИЯ - анемия у больных, получающих радио- и химиотерапию • ИНФЕКЦИОННЫЕ БОЛЕЗНИ - анемия вызванная применением ВААРТ у ВИЧ-пациентов • РЕВМАТОЛОГИЯ - анемия у больных ревматоидным артритом • ХИРУРГИЯ - применение ЭПО для уменьшения объема переливаемой крови • АКУШЕРСТВО - лечение анемии беременных • ПЕДИАТРИЯ - лечение анемии недоношенных новорожденных, нейропротекторное действие
 ЛЕЧЕБНОЕ ПРИМЕНЕНИЕ ЦИТОКИНОВ СТИМУЛЯЦИЯ КРОВЕТВОРЕНИЯ • Эритропоэз – эритропоэтин. • Лейкопоэз – Г-КСФ, ГМ-КСФ, ИЛ-1 бета. • Тромбопоэз – тромбопоэтин, ИЛ-11 - ? • Лимфопоэз – ИЛ-7.
ЛЕЧЕБНОЕ ПРИМЕНЕНИЕ ЦИТОКИНОВ СТИМУЛЯЦИЯ КРОВЕТВОРЕНИЯ • Эритропоэз – эритропоэтин. • Лейкопоэз – Г-КСФ, ГМ-КСФ, ИЛ-1 бета. • Тромбопоэз – тромбопоэтин, ИЛ-11 - ? • Лимфопоэз – ИЛ-7.
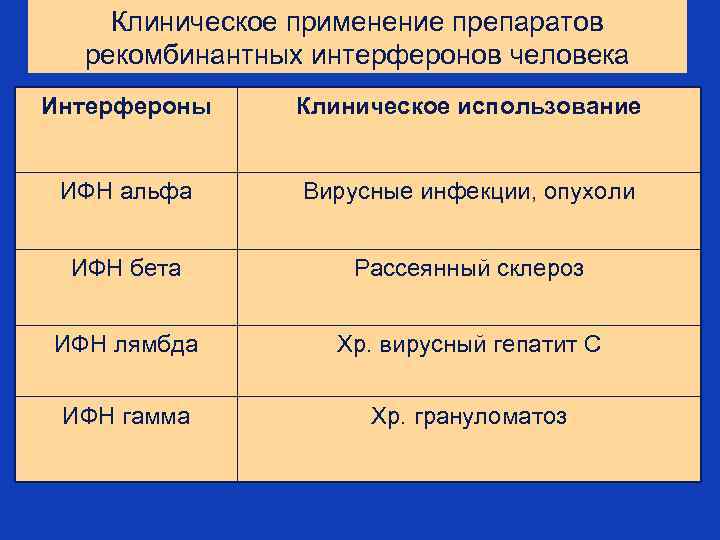 Клиническое применение препаратов рекомбинантных интерферонов человека Интерфероны Клиническое использование ИФН альфа Вирусные инфекции, опухоли ИФН бета Рассеянный склероз ИФН лямбда Хр. вирусный гепатит С ИФН гамма Хр. грануломатоз
Клиническое применение препаратов рекомбинантных интерферонов человека Интерфероны Клиническое использование ИФН альфа Вирусные инфекции, опухоли ИФН бета Рассеянный склероз ИФН лямбда Хр. вирусный гепатит С ИФН гамма Хр. грануломатоз
 Вирусы, вызывающие ОРВИ, при которых показана клиническая эффективность применения интраназального ИФН альфа • • Риновирус ( в т. ч. тип 13, тип 39) Вирус гриппа А (H 1 N 1 и H 3 N 2) Вирус гриппа В Вирус парагриппа Респираторный синцитиальный вирус Аденовирус Коронавирус Лекарственные формы: - Капли в нос - Спрей - Аэрозоль
Вирусы, вызывающие ОРВИ, при которых показана клиническая эффективность применения интраназального ИФН альфа • • Риновирус ( в т. ч. тип 13, тип 39) Вирус гриппа А (H 1 N 1 и H 3 N 2) Вирус гриппа В Вирус парагриппа Респираторный синцитиальный вирус Аденовирус Коронавирус Лекарственные формы: - Капли в нос - Спрей - Аэрозоль
 Терапевтические схемы противовирусной терапии ХВГС (хронический вирусный гепатит С) 1. Монотерапия альфа-интерфероном только больным ОГС. 2. Комбинированная терапия ПЭГ-интерфероном в сочетании с рибавирином - 48 недель. 3. Комбинированная терапия ПЭГ-интерфероном в сочетании с рибавирином и ингибиторами вирусных протеаз - 24 -48 недель.
Терапевтические схемы противовирусной терапии ХВГС (хронический вирусный гепатит С) 1. Монотерапия альфа-интерфероном только больным ОГС. 2. Комбинированная терапия ПЭГ-интерфероном в сочетании с рибавирином - 48 недель. 3. Комбинированная терапия ПЭГ-интерфероном в сочетании с рибавирином и ингибиторами вирусных протеаз - 24 -48 недель.
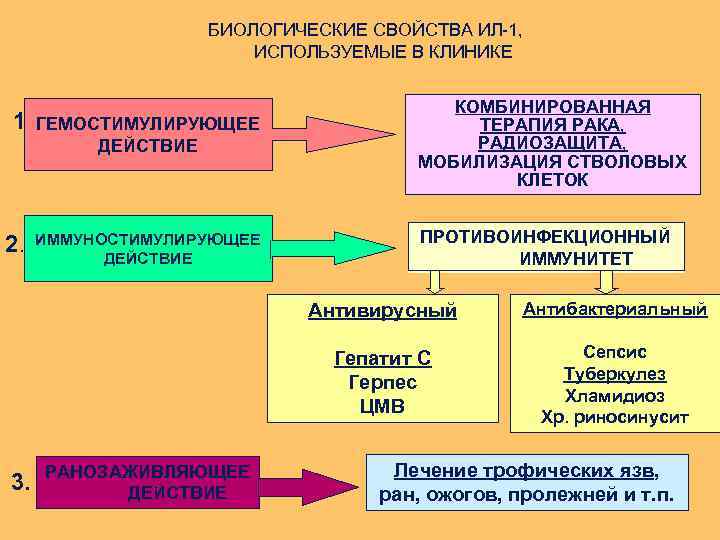 БИОЛОГИЧЕСКИЕ СВОЙСТВА ИЛ-1, ИСПОЛЬЗУЕМЫЕ В КЛИНИКЕ 1. ГЕМОСТИМУЛИРУЮЩЕЕ ДЕЙСТВИЕ 2. ИММУНОСТИМУЛИРУЮЩЕЕ ДЕЙСТВИЕ КОМБИНИРОВАННАЯ ТЕРАПИЯ РАКА, РАДИОЗАЩИТА, МОБИЛИЗАЦИЯ СТВОЛОВЫХ КЛЕТОК ПРОТИВОИНФЕКЦИОННЫЙ ИММУНИТЕТ Антивирусный Гепатит С Герпес ЦМВ 3. РАНОЗАЖИВЛЯЮЩЕЕ ДЕЙСТВИЕ Антибактериальный Сепсис Туберкулез Хламидиоз Хр. риносинусит Лечение трофических язв, ран, ожогов, пролежней и т. п.
БИОЛОГИЧЕСКИЕ СВОЙСТВА ИЛ-1, ИСПОЛЬЗУЕМЫЕ В КЛИНИКЕ 1. ГЕМОСТИМУЛИРУЮЩЕЕ ДЕЙСТВИЕ 2. ИММУНОСТИМУЛИРУЮЩЕЕ ДЕЙСТВИЕ КОМБИНИРОВАННАЯ ТЕРАПИЯ РАКА, РАДИОЗАЩИТА, МОБИЛИЗАЦИЯ СТВОЛОВЫХ КЛЕТОК ПРОТИВОИНФЕКЦИОННЫЙ ИММУНИТЕТ Антивирусный Гепатит С Герпес ЦМВ 3. РАНОЗАЖИВЛЯЮЩЕЕ ДЕЙСТВИЕ Антибактериальный Сепсис Туберкулез Хламидиоз Хр. риносинусит Лечение трофических язв, ран, ожогов, пролежней и т. п.
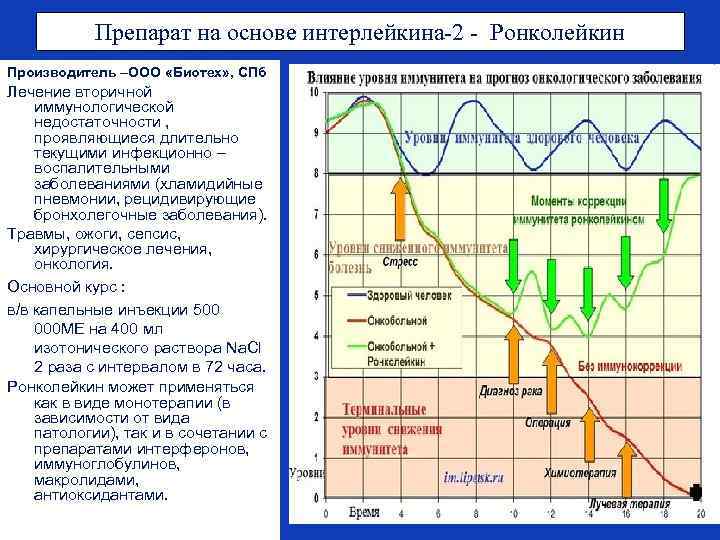 Препарат на основе интерлейкина-2 - Ронколейкин Производитель –ООО «Биотех» , СПб Лечение вторичной иммунологической недостаточности , проявляющиеся длительно текущими инфекционно – воспалительными заболеваниями (хламидийные пневмонии, рецидивирующие бронхолегочные заболевания). Травмы, ожоги, сепсис, хирургическое лечения, онкология. Основной курс : в/в капельные инъекции 500 000 МЕ на 400 мл изотонического раствора Nа. Cl 2 раза с интервалом в 72 часа. Ронколейкин может применяться как в виде монотерапии (в зависимости от вида патологии), так и в сочетании с препаратами интерферонов, иммуноглобулинов, макролидами, антиоксидантами.
Препарат на основе интерлейкина-2 - Ронколейкин Производитель –ООО «Биотех» , СПб Лечение вторичной иммунологической недостаточности , проявляющиеся длительно текущими инфекционно – воспалительными заболеваниями (хламидийные пневмонии, рецидивирующие бронхолегочные заболевания). Травмы, ожоги, сепсис, хирургическое лечения, онкология. Основной курс : в/в капельные инъекции 500 000 МЕ на 400 мл изотонического раствора Nа. Cl 2 раза с интервалом в 72 часа. Ронколейкин может применяться как в виде монотерапии (в зависимости от вида патологии), так и в сочетании с препаратами интерферонов, иммуноглобулинов, макролидами, антиоксидантами.
 Использование ИЛ-2 -активированных клеток в терапии рака LAK – лимфокин-активированные киллеры. ИЛ-2 активированные лимфоциты периферической крови больных раком. TIL – тумор-инфильтрирующие лимфоциты. Лимфоциты, выделенные из удаленной опухоли и стимулированные ИЛ-2 in vitro. CIK – цитокин-индуцированные киллеры. Лимфоциты периферической крови, активированные (ИЛ-2 + ИФНγ + а/CD 3). Применение: Меланома, рак почки, различные виды сарком и ряд других опухолей. Результаты: полный ответ до 50%, 5 -ти летняя выживаемость 40 -72% (Morgan e. a. , 2010; Phan, Rosenberg, 2013)
Использование ИЛ-2 -активированных клеток в терапии рака LAK – лимфокин-активированные киллеры. ИЛ-2 активированные лимфоциты периферической крови больных раком. TIL – тумор-инфильтрирующие лимфоциты. Лимфоциты, выделенные из удаленной опухоли и стимулированные ИЛ-2 in vitro. CIK – цитокин-индуцированные киллеры. Лимфоциты периферической крови, активированные (ИЛ-2 + ИФНγ + а/CD 3). Применение: Меланома, рак почки, различные виды сарком и ряд других опухолей. Результаты: полный ответ до 50%, 5 -ти летняя выживаемость 40 -72% (Morgan e. a. , 2010; Phan, Rosenberg, 2013)
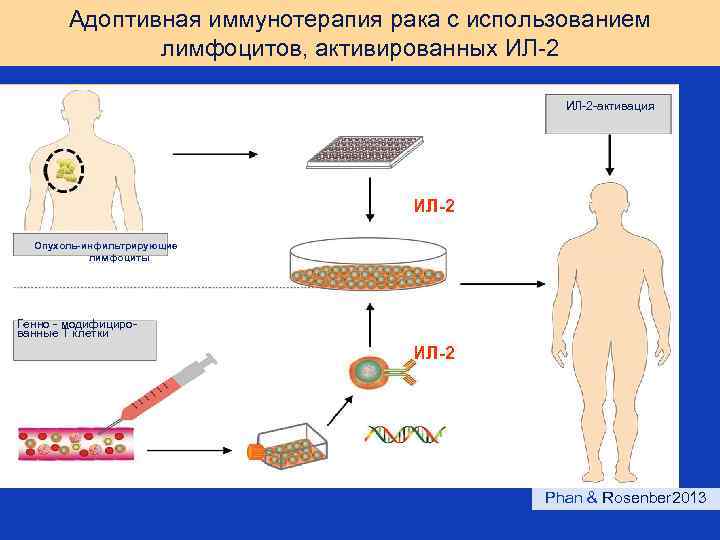 Адоптивная иммунотерапия рака с использованием лимфоцитов, активированных ИЛ-2 -активация ИЛ-2 Опухоль-инфильтрирующие лимфоциты Генно - модифицированные Т клетки ИЛ-2 Phan & Rosenber 2013
Адоптивная иммунотерапия рака с использованием лимфоцитов, активированных ИЛ-2 -активация ИЛ-2 Опухоль-инфильтрирующие лимфоциты Генно - модифицированные Т клетки ИЛ-2 Phan & Rosenber 2013
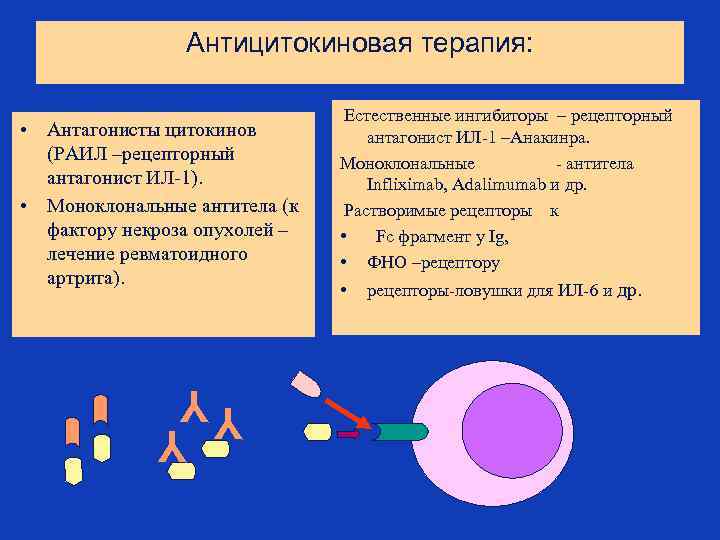 Антицитокиновая терапия: • Антагонисты цитокинов (РАИЛ –рецепторный антагонист ИЛ-1). • Моноклональные антитела (к фактору некроза опухолей – лечение ревматоидного артрита). Естественные ингибиторы – рецепторный антагонист ИЛ-1 –Анакинра. Моноклональные - антитела Infliximab, Adalimumab и др. Растворимые рецепторы к • Fс фрагмент у Ig, • ФНО –рецептору • рецепторы-ловушки для ИЛ-6 и др. Y Y Y
Антицитокиновая терапия: • Антагонисты цитокинов (РАИЛ –рецепторный антагонист ИЛ-1). • Моноклональные антитела (к фактору некроза опухолей – лечение ревматоидного артрита). Естественные ингибиторы – рецепторный антагонист ИЛ-1 –Анакинра. Моноклональные - антитела Infliximab, Adalimumab и др. Растворимые рецепторы к • Fс фрагмент у Ig, • ФНО –рецептору • рецепторы-ловушки для ИЛ-6 и др. Y Y Y
 АНТИЦИТОКИНОВАЯ ТЕРАПИЯ РЕВМАТОИДНОГО АРТРИТА Основные провоспалительные цитокины, участвующие в патогенезе РА Антицитокиновые препараты для терапии ФНО МАТ – инфликсимаб (гуманизированные) - адалимумаб (человеческие) Химерный рецептор - этанерсепт ИЛ-1 Рецепторный антагонист ИЛ-1 МАТ ИЛ-6 МАТ против рецептора ИЛ-6 (тоцилизумаб) ИЛ-17 МАТ в разработке
АНТИЦИТОКИНОВАЯ ТЕРАПИЯ РЕВМАТОИДНОГО АРТРИТА Основные провоспалительные цитокины, участвующие в патогенезе РА Антицитокиновые препараты для терапии ФНО МАТ – инфликсимаб (гуманизированные) - адалимумаб (человеческие) Химерный рецептор - этанерсепт ИЛ-1 Рецепторный антагонист ИЛ-1 МАТ ИЛ-6 МАТ против рецептора ИЛ-6 (тоцилизумаб) ИЛ-17 МАТ в разработке
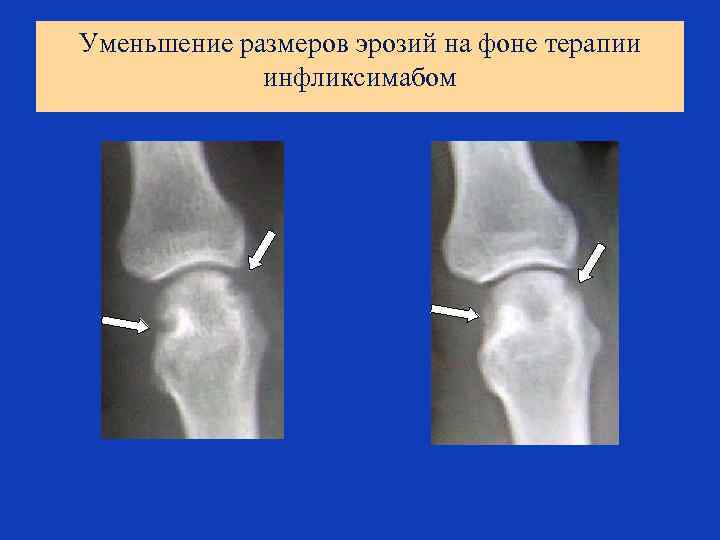 Уменьшение размеров эрозий на фоне терапии инфликсимабом
Уменьшение размеров эрозий на фоне терапии инфликсимабом
 АПОПТОЗ (краткая информация (если на занятии останется время), либо студенты могут сделать сами сообщение – презентацию о механизмах апоптоза) Естественный апоптоз развивается в физиологических условиях: • в периоде эмбриогенеза, • при элиминации повреждённых клеток и клеток в состоянии терминальной дифференцировки, • в процессе инволюции органов, • при дифференцировке некоторых типов клеток, • у новорождённого вследствие родового стр есса. Основное назначение естественного апоптоза ремоделирование тканей и поддержание тканевого (структурного) гомеостаза. Нарушение реализации естественного апоптоза приводит к развитию так называемых апоптоз-ассоциированных заболеваний (аутоиммунные болезни, злокачественные опухоли и др. ). Индуцированный апоптоз обусловлен или усилен внешними факторами, не имеющими физиологического значения ( например, апоптоз клеток злокачественных опухолей усиливается под влиянием лучевой или химиотерапии, апоптоз лимфоидных клеток развивается при дистресс-синдроме). Формы индуцированного апоптоза: • Апоптоз дистресса • Инфекционно-токсический апоптоз • Неинфекционно-токсический апоптоз (в частности, лекарственный апоптоз) • Апоптоз ишемии • Апоптоз гиперчувствительности • Радиогенный апоптоз • Термогенный апоптоз.
АПОПТОЗ (краткая информация (если на занятии останется время), либо студенты могут сделать сами сообщение – презентацию о механизмах апоптоза) Естественный апоптоз развивается в физиологических условиях: • в периоде эмбриогенеза, • при элиминации повреждённых клеток и клеток в состоянии терминальной дифференцировки, • в процессе инволюции органов, • при дифференцировке некоторых типов клеток, • у новорождённого вследствие родового стр есса. Основное назначение естественного апоптоза ремоделирование тканей и поддержание тканевого (структурного) гомеостаза. Нарушение реализации естественного апоптоза приводит к развитию так называемых апоптоз-ассоциированных заболеваний (аутоиммунные болезни, злокачественные опухоли и др. ). Индуцированный апоптоз обусловлен или усилен внешними факторами, не имеющими физиологического значения ( например, апоптоз клеток злокачественных опухолей усиливается под влиянием лучевой или химиотерапии, апоптоз лимфоидных клеток развивается при дистресс-синдроме). Формы индуцированного апоптоза: • Апоптоз дистресса • Инфекционно-токсический апоптоз • Неинфекционно-токсический апоптоз (в частности, лекарственный апоптоз) • Апоптоз ишемии • Апоптоз гиперчувствительности • Радиогенный апоптоз • Термогенный апоптоз.
 Апоптоз как физиологическая смерть клеток Взаимодействие Fas –рецептор ( Fas. R) - Fas лиганды (Fas L) Fas – рецептор (CD 95)- рецептор готовности клетки к апоптозу Fas L или CD 95 L –лиганды Fas - рецептора. Лигандами для таких рецепторов могут служить либо растворимые факторы, либо молекулы, экспрессирующиеся на поверхности клеток –таких, как цитотоксические Т лимфоциты. При связывании Fas – рецептора Fas – лигандом, происходит запуск программируемой гибели клеток организма. Лиганды для Fas – рецептора (Fas L или CD 95 L) , запускающие апоптоз, имеют ряд сходных механизмов, но также ряд отличительных особенностей с активацией рецепторов фактора некроза опухолей - альфа (TNF ). Связывание такого рецептора с лигандом вызывает на поверхности клетки-мишени процесс кластеризации рецепторов. После этого адапторный протеин FADD подходит прямо к внутриклеточному домену смерти поверхностного Fas рецептора, соединяется с ним, после чего происходит запуск каскада каспаз. Fas рецептор активирует только процесс апоптоза в клетке-мишени, и не участвует в сигналлинге TNF рецептора.
Апоптоз как физиологическая смерть клеток Взаимодействие Fas –рецептор ( Fas. R) - Fas лиганды (Fas L) Fas – рецептор (CD 95)- рецептор готовности клетки к апоптозу Fas L или CD 95 L –лиганды Fas - рецептора. Лигандами для таких рецепторов могут служить либо растворимые факторы, либо молекулы, экспрессирующиеся на поверхности клеток –таких, как цитотоксические Т лимфоциты. При связывании Fas – рецептора Fas – лигандом, происходит запуск программируемой гибели клеток организма. Лиганды для Fas – рецептора (Fas L или CD 95 L) , запускающие апоптоз, имеют ряд сходных механизмов, но также ряд отличительных особенностей с активацией рецепторов фактора некроза опухолей - альфа (TNF ). Связывание такого рецептора с лигандом вызывает на поверхности клетки-мишени процесс кластеризации рецепторов. После этого адапторный протеин FADD подходит прямо к внутриклеточному домену смерти поверхностного Fas рецептора, соединяется с ним, после чего происходит запуск каскада каспаз. Fas рецептор активирует только процесс апоптоза в клетке-мишени, и не участвует в сигналлинге TNF рецептора.
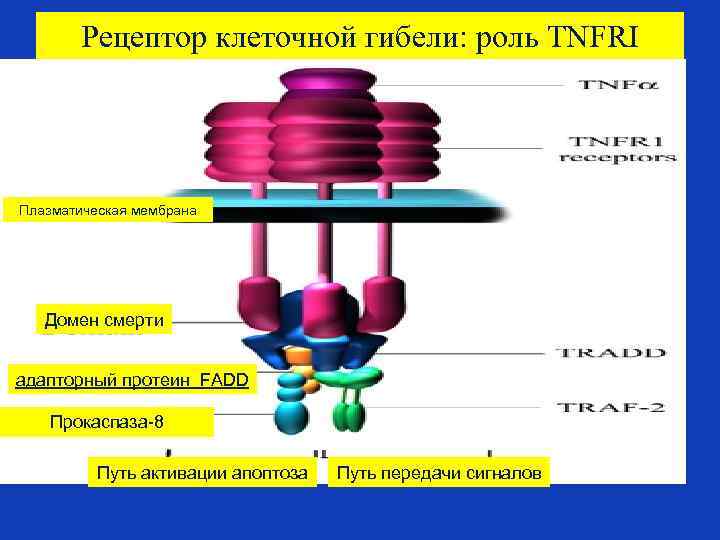 Рецептор клеточной гибели: роль TNFRI Плазматическая мембрана Домен смерти адапторный протеин FADD Прокаспаза-8 Путь активации апоптоза Путь передачи сигналов
Рецептор клеточной гибели: роль TNFRI Плазматическая мембрана Домен смерти адапторный протеин FADD Прокаспаза-8 Путь активации апоптоза Путь передачи сигналов
 Механизмы запуска апоптоза Цитотоксические Т лимфоциты распознают поврежденные , вирустрансформированные или малигнизированные клетки организма –хозяина и запускают в них программу апоптоза. Цитотоксические Т лимфоциты также могут вызывать апоптоз клеток –мишеней с помощью специальных ферментов – гранзимов, которые они впрыскивают в отверстия клеточной мембраны клетки – мишени, созданные перфоринами – полимеризующимися в мембране мишени протеинами. Гранзим B может быть введен в клетку-мишень цитотоксическим Т лимфоцитом с помощью отверстий в мембране мишени, созданных перфоринами. Гранзим B способен прямо активировать каспазы 3, 7, 8 и 10. Митохондрия – также является ключевым регулятором каспазного каскада и апоптоза: освобождение цитохрома C из митохондрии прямо активирует сначала каспазу 9, потом каспазу 3.
Механизмы запуска апоптоза Цитотоксические Т лимфоциты распознают поврежденные , вирустрансформированные или малигнизированные клетки организма –хозяина и запускают в них программу апоптоза. Цитотоксические Т лимфоциты также могут вызывать апоптоз клеток –мишеней с помощью специальных ферментов – гранзимов, которые они впрыскивают в отверстия клеточной мембраны клетки – мишени, созданные перфоринами – полимеризующимися в мембране мишени протеинами. Гранзим B может быть введен в клетку-мишень цитотоксическим Т лимфоцитом с помощью отверстий в мембране мишени, созданных перфоринами. Гранзим B способен прямо активировать каспазы 3, 7, 8 и 10. Митохондрия – также является ключевым регулятором каспазного каскада и апоптоза: освобождение цитохрома C из митохондрии прямо активирует сначала каспазу 9, потом каспазу 3.
 Каспазы и разрушение хроматина Основной механизм запрограммированной гибели клеток – разрушение хромосомальной ДНК до нуклеосом. • Каспазы (ферменты с каскадным принципом действия) играют основную роль в этом процессе: • Активируют ДНКазы • Ингибируют ферменты, участвующие в репарации ДНК • Разрушают структурные протеины ядра
Каспазы и разрушение хроматина Основной механизм запрограммированной гибели клеток – разрушение хромосомальной ДНК до нуклеосом. • Каспазы (ферменты с каскадным принципом действия) играют основную роль в этом процессе: • Активируют ДНКазы • Ингибируют ферменты, участвующие в репарации ДНК • Разрушают структурные протеины ядра
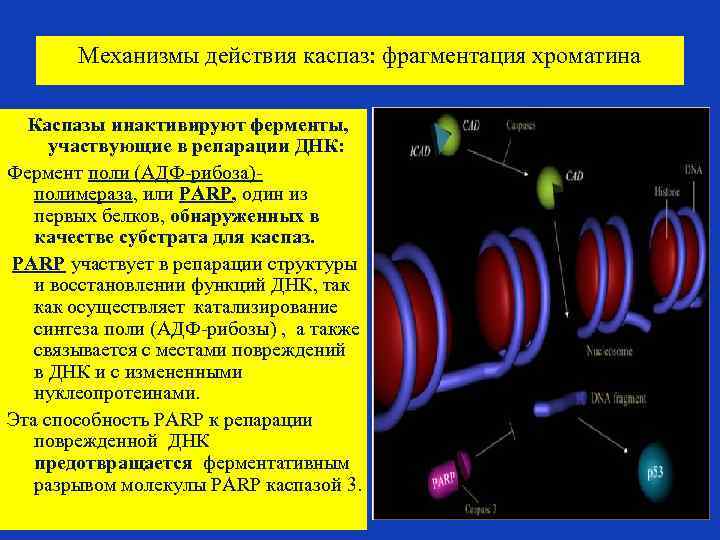 Механизмы действия каспаз: фрагментация хроматина. Каспазы инактивируют ферменты, участвующие в репарации ДНК: Фермент поли (AДФ-рибоза)- полимераза, или PARP, один из первых белков, обнаруженных в качестве субстрата для каспаз. PARP участвует в репарации структуры и восстановлении функций ДНК, так как осуществляет катализирование синтеза поли (AДФ-рибозы) , а также связывается с местами повреждений в ДНК и с измененными нуклеопротеинами. Эта способность PARP к репарации поврежденной ДНК предотвращается ферментативным разрывом молекулы PARP каспазой 3.
Механизмы действия каспаз: фрагментация хроматина. Каспазы инактивируют ферменты, участвующие в репарации ДНК: Фермент поли (AДФ-рибоза)- полимераза, или PARP, один из первых белков, обнаруженных в качестве субстрата для каспаз. PARP участвует в репарации структуры и восстановлении функций ДНК, так как осуществляет катализирование синтеза поли (AДФ-рибозы) , а также связывается с местами повреждений в ДНК и с измененными нуклеопротеинами. Эта способность PARP к репарации поврежденной ДНК предотвращается ферментативным разрывом молекулы PARP каспазой 3.
 Механизмы действия каспаз: разрушение структурных белков ядра и фрагментация ДНК Каспазы разрушают структурные белки ядра Ламины –структурные ядерные белки, которые поддерживают форму ядра и обеспечивают взаимодействие между хроматином и мембраной ядра. Разрушения ламинов каспазой 6 приводит к конденсации хроматина и фрагментации ядра, что и является отличительной особенностью клеток, вошедших в апоптоз. Каспазы вызывают фрагментацию ДНК Радиоизотопные исследования показали, что процесс фрагментации ДНК до нуклеосом обеспечивается ферментом CAD ( каспазой активированная ДНКаза). В норме CAD существует в виде неактивного комплекса с ингибитором- ICAD (ингибитор CAD). Во время апоптоза, ICAD отрывается каспазой 3, и CAD освобождается из комплекса. Вслед за этим происходит быстрая фрагментация ядра
Механизмы действия каспаз: разрушение структурных белков ядра и фрагментация ДНК Каспазы разрушают структурные белки ядра Ламины –структурные ядерные белки, которые поддерживают форму ядра и обеспечивают взаимодействие между хроматином и мембраной ядра. Разрушения ламинов каспазой 6 приводит к конденсации хроматина и фрагментации ядра, что и является отличительной особенностью клеток, вошедших в апоптоз. Каспазы вызывают фрагментацию ДНК Радиоизотопные исследования показали, что процесс фрагментации ДНК до нуклеосом обеспечивается ферментом CAD ( каспазой активированная ДНКаза). В норме CAD существует в виде неактивного комплекса с ингибитором- ICAD (ингибитор CAD). Во время апоптоза, ICAD отрывается каспазой 3, и CAD освобождается из комплекса. Вслед за этим происходит быстрая фрагментация ядра
 Этапы апоптоза Этапы А и В Этапы С и D (А) Разрыв ламинов (ядерных белков) и актинов – белков цитоскелета. (B) Повреждение хроматина в ядре , конденсация хроматина. Ядро как бы «сморщивается» . (C) Клетка уменьшается в размерах, как бы упаковывается в форму, удобную для ее поглощения макрофагом. (D) Маленькие везикулы – все, что остается от клетки на последнем этапе ее физиологической гибели - апоптозные тела, легко поглощаются макрофагами.
Этапы апоптоза Этапы А и В Этапы С и D (А) Разрыв ламинов (ядерных белков) и актинов – белков цитоскелета. (B) Повреждение хроматина в ядре , конденсация хроматина. Ядро как бы «сморщивается» . (C) Клетка уменьшается в размерах, как бы упаковывается в форму, удобную для ее поглощения макрофагом. (D) Маленькие везикулы – все, что остается от клетки на последнем этапе ее физиологической гибели - апоптозные тела, легко поглощаются макрофагами.
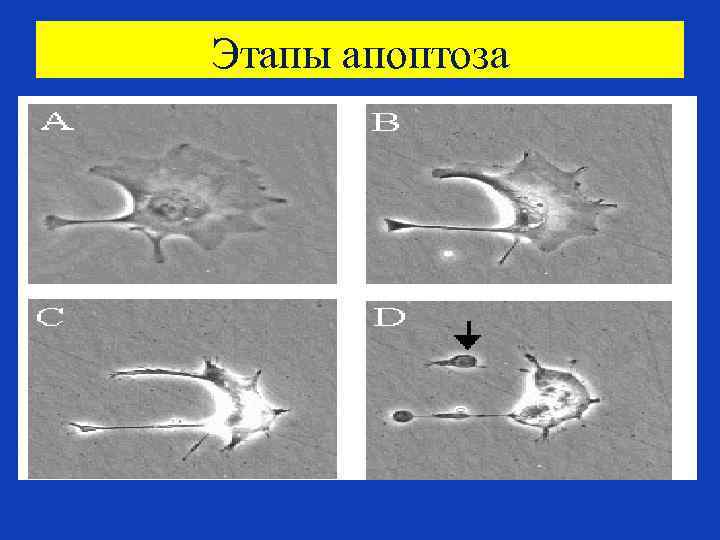 Этапы апоптоза
Этапы апоптоза
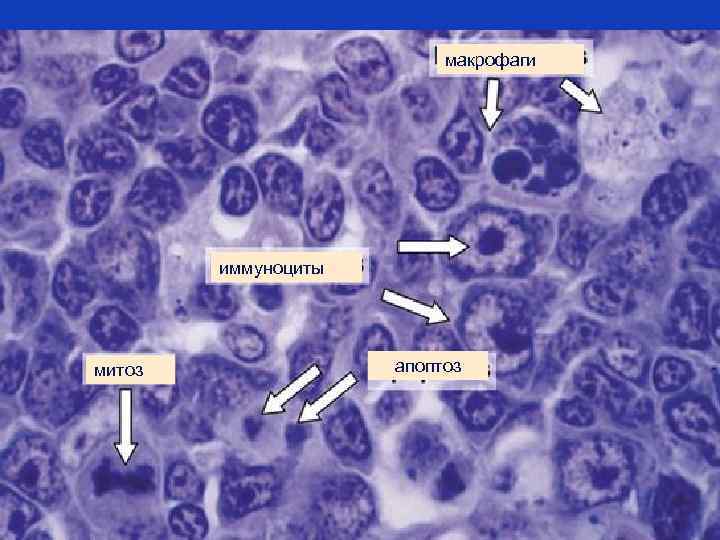 макрофаги иммуноциты митоз апоптоз
макрофаги иммуноциты митоз апоптоз
 Сигналы, вызывающие запуск апоптоза • Существует несколько типов сигналов, запускающих апоптоз. • Чувствительность клетки к таким сигналам зависит от многих факторов : • От экспрессии про- и противоапоптических протеинов (семейства Bcl-2 ). • От выраженности (силы) апоптозных стимулов. • От стадии клеточного цикла.
Сигналы, вызывающие запуск апоптоза • Существует несколько типов сигналов, запускающих апоптоз. • Чувствительность клетки к таким сигналам зависит от многих факторов : • От экспрессии про- и противоапоптических протеинов (семейства Bcl-2 ). • От выраженности (силы) апоптозных стимулов. • От стадии клеточного цикла.
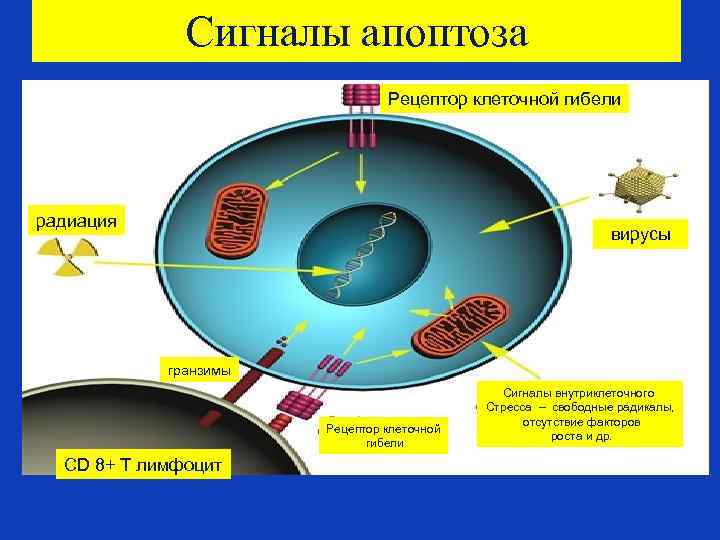 Сигналы апоптоза Рецептор клеточной гибели радиация вирусы гранзимы Рецептор клеточной гибели CD 8+ Т лимфоцит Сигналы внутриклеточного Стресса – свободные радикалы, отсутствие факторов роста и др.
Сигналы апоптоза Рецептор клеточной гибели радиация вирусы гранзимы Рецептор клеточной гибели CD 8+ Т лимфоцит Сигналы внутриклеточного Стресса – свободные радикалы, отсутствие факторов роста и др.
 Внутренние сигналы апоптоза • В других случаях апоптоз клетки может запускаться внутренними сигналами –сигналами стресса. • Клеточный стресс может вызываться при экспозиции клетки к радиации, химическим веществам, либо при вирусной инфекции. • Стресс может быть также оксидативным - в клетке скапливается слишком больное число оксидантов. • В генерацию внутренних сигналов апоптоза всегда вовлечены митохондрии. • Относительное количество антиапоптозных белков - bcl-2 - определяет, насколько интенсивность клеточного стресса достаточна для входа клетки в апоптоз.
Внутренние сигналы апоптоза • В других случаях апоптоз клетки может запускаться внутренними сигналами –сигналами стресса. • Клеточный стресс может вызываться при экспозиции клетки к радиации, химическим веществам, либо при вирусной инфекции. • Стресс может быть также оксидативным - в клетке скапливается слишком больное число оксидантов. • В генерацию внутренних сигналов апоптоза всегда вовлечены митохондрии. • Относительное количество антиапоптозных белков - bcl-2 - определяет, насколько интенсивность клеточного стресса достаточна для входа клетки в апоптоз.
 Роль митохондрий в запуске апоптоза • В митохондриях содержится большинство проапоптозных протеинов –таких, как апоптоз индуцирующий фактор Apoptosis Inducing Factor (AIF), Smac/DIABLO и цитохром C. • Эти факторы освобождаются из митохондрий через отверстия в мембране, называемыми порами. • Эти поры образуются в мембране митохондрии в результате действия проапоптозных белков, которые активируются сигналами клеточного стресса (радиация, повреждение свободными радикалами, отсутствие положительных сигналов – ростовых факторов и т. д. ). • Митохондрии также играют важную роль в усилении сигналов апоптоза , приходящих с домена смерти клеточного рецептора апоптоза, а также в привлечении каспазы 8 к этому домену смерти.
Роль митохондрий в запуске апоптоза • В митохондриях содержится большинство проапоптозных протеинов –таких, как апоптоз индуцирующий фактор Apoptosis Inducing Factor (AIF), Smac/DIABLO и цитохром C. • Эти факторы освобождаются из митохондрий через отверстия в мембране, называемыми порами. • Эти поры образуются в мембране митохондрии в результате действия проапоптозных белков, которые активируются сигналами клеточного стресса (радиация, повреждение свободными радикалами, отсутствие положительных сигналов – ростовых факторов и т. д. ). • Митохондрии также играют важную роль в усилении сигналов апоптоза , приходящих с домена смерти клеточного рецептора апоптоза, а также в привлечении каспазы 8 к этому домену смерти.
 Роль Bcl-2 протеинов • Семейство bcl-2 протеинов участвует в ответе на апоптозные стимулы. • Некоторые из этих протенов (такие, как bcl-2 и bcl-XL) являются антиапоптозными белками. • Другие члены семейства bcl-2 протеинов (такие, как Bad, Bax или Bid) являются проапоптозыми белками. • Чувствительность клетки к апоптозным стимулам зависит от баланса про- и противо- апоптозных bcl-2 протеинов: при преобладании проапоптозных белков, клетка более чувствительна к апоптозу, если преобладают противоапоптозные белки –клетка более устойчива к апоптозным стимулам. • Преобладание проапоптозных bcl-2 белков на поверхностной мембране митохондрий является сигналом для формирования пор, выхода из митохондрии цитохрома С, что служит внутренним сигналом для запуска каскада каспаз.
Роль Bcl-2 протеинов • Семейство bcl-2 протеинов участвует в ответе на апоптозные стимулы. • Некоторые из этих протенов (такие, как bcl-2 и bcl-XL) являются антиапоптозными белками. • Другие члены семейства bcl-2 протеинов (такие, как Bad, Bax или Bid) являются проапоптозыми белками. • Чувствительность клетки к апоптозным стимулам зависит от баланса про- и противо- апоптозных bcl-2 протеинов: при преобладании проапоптозных белков, клетка более чувствительна к апоптозу, если преобладают противоапоптозные белки –клетка более устойчива к апоптозным стимулам. • Преобладание проапоптозных bcl-2 белков на поверхностной мембране митохондрий является сигналом для формирования пор, выхода из митохондрии цитохрома С, что служит внутренним сигналом для запуска каскада каспаз.
 Роль Bcl-2 протеинов • Проапоптозные bcl-2 часто обнаруживаются и в цитозоле клетки, где они выполняют роль сенсоров клеточного повреждения или стресса. • Вслед за развившимся клеточным стрессом они встраиваются в мембрану митохондрии, где локализуются противоапоптозные белки. • Такое взаимодействие между про- и противоапоптозными bcl-2 белками в мембране митохондрий приводит к образованию пори к освобождению цитохрома С и других проапоптозных молекул из внутримембранного пространства. • Это, в свою очередь, приводит к образованию апоптосом и активации каспазного каскада.
Роль Bcl-2 протеинов • Проапоптозные bcl-2 часто обнаруживаются и в цитозоле клетки, где они выполняют роль сенсоров клеточного повреждения или стресса. • Вслед за развившимся клеточным стрессом они встраиваются в мембрану митохондрии, где локализуются противоапоптозные белки. • Такое взаимодействие между про- и противоапоптозными bcl-2 белками в мембране митохондрий приводит к образованию пори к освобождению цитохрома С и других проапоптозных молекул из внутримембранного пространства. • Это, в свою очередь, приводит к образованию апоптосом и активации каспазного каскада.
 Формирование апоптосом • Освобождение цитохрома С в цитозоль приводит также к взаимодействию цитохрома С с белком, названным Apaf-1. • Это приводит к привлечению прокаспазы 9 в формирующийся многобелковый комплекс –с цитохромом С и белком Apaf-1, весь комплекс таких белков называется апоптосомой. • Формирование апоптосом приводит к активации прокаспазы 9 и к запуску апоптоза.
Формирование апоптосом • Освобождение цитохрома С в цитозоль приводит также к взаимодействию цитохрома С с белком, названным Apaf-1. • Это приводит к привлечению прокаспазы 9 в формирующийся многобелковый комплекс –с цитохромом С и белком Apaf-1, весь комплекс таких белков называется апоптосомой. • Формирование апоптосом приводит к активации прокаспазы 9 и к запуску апоптоза.
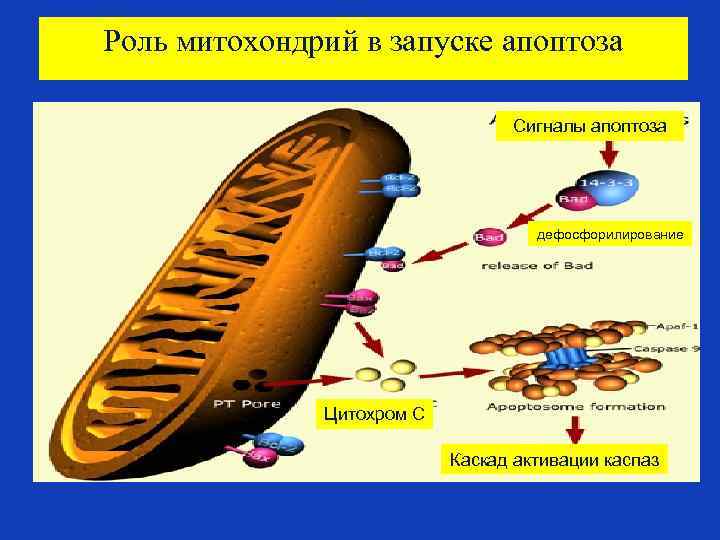 Роль митохондрий в запуске апоптоза Сигналы апоптоза дефосфорилирование Цитохром С Каскад активации каспаз
Роль митохондрий в запуске апоптоза Сигналы апоптоза дефосфорилирование Цитохром С Каскад активации каспаз
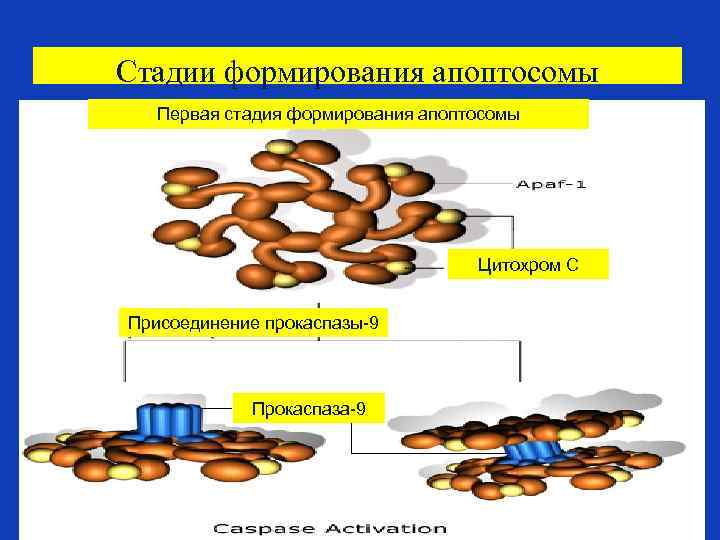 Стадии формирования апоптосомы Первая стадия формирования апоптосомы Цитохром С Присоединение прокаспазы-9 Прокаспаза-9
Стадии формирования апоптосомы Первая стадия формирования апоптосомы Цитохром С Присоединение прокаспазы-9 Прокаспаза-9
 Вопросы к занятию № 3 а 1. 2. 3. 4. Классификация цитокинов. Основные свойства цитокинов. Понятие о цитокиновой сети. Характеристика клеток-продуцентов цитокинов во врожденном иммунитете. 5. Понятие о Т хелперах 1; 2; 17 типов. 6. Характеристика цитокинов и их антагонистов; 7. Семейства рецепторов цитокинов. 8. Цитокины и воспаление. 9. Системные и местные эффекты цитокинов. 10. Препараты на основе цитокинов и их антагонистов.
Вопросы к занятию № 3 а 1. 2. 3. 4. Классификация цитокинов. Основные свойства цитокинов. Понятие о цитокиновой сети. Характеристика клеток-продуцентов цитокинов во врожденном иммунитете. 5. Понятие о Т хелперах 1; 2; 17 типов. 6. Характеристика цитокинов и их антагонистов; 7. Семейства рецепторов цитокинов. 8. Цитокины и воспаление. 9. Системные и местные эффекты цитокинов. 10. Препараты на основе цитокинов и их антагонистов.
 Тестовые задания к занятию № 3 Цитокины – это: 1. Цитотоксические клетки 2. Иммунорегуляторные пептиды 3. Бактериальные токсины 4. Циркулирующие иммунные комплексы 5. Мембранные маркеры Основными индукторами синтеза цитокинов клетками врожденного иммунитета являются: 1. Комплемент 2. Иммуноглобулины 3. Активация образраспознающих рецепторов 4. Взаимодействие адгезионных молекул 5. Циркулирующие иммунные комплексы
Тестовые задания к занятию № 3 Цитокины – это: 1. Цитотоксические клетки 2. Иммунорегуляторные пептиды 3. Бактериальные токсины 4. Циркулирующие иммунные комплексы 5. Мембранные маркеры Основными индукторами синтеза цитокинов клетками врожденного иммунитета являются: 1. Комплемент 2. Иммуноглобулины 3. Активация образраспознающих рецепторов 4. Взаимодействие адгезионных молекул 5. Циркулирующие иммунные комплексы
 Тестовые задания к занятию № 3 Основными цитокинами врожденного иммунитета являются: 1. ИЛ-2 2. ИЛ-3 3. ИЛ-4 4. Интерфероны I типа (αβ) 5. Провоспалительные цитокины Цитокины воздействуют на клетку-мишень через: 1. Молекулы CD 3 ; CD 4 2. Молекулы MHC I и II класса 3. Цитоплазматическую мембрану 4. Растворимые рецепторы цитокинов 5. Мембранные рецепторы цитокинов
Тестовые задания к занятию № 3 Основными цитокинами врожденного иммунитета являются: 1. ИЛ-2 2. ИЛ-3 3. ИЛ-4 4. Интерфероны I типа (αβ) 5. Провоспалительные цитокины Цитокины воздействуют на клетку-мишень через: 1. Молекулы CD 3 ; CD 4 2. Молекулы MHC I и II класса 3. Цитоплазматическую мембрану 4. Растворимые рецепторы цитокинов 5. Мембранные рецепторы цитокинов
 Тестовые задания к занятию № 3 Основными клетками-продуцентами цитокинов в реакциях врожденного иммунитета являются: 1. Клетки миелоидного ряда 2. Т-лимфоциты-хелперы 3. Цитотоксические Т-лимфоциты 4. В-лимфоциты 5. Плазматические клетки Эффекты интерлейкина 1β: 1. Активация лимфоцитов и макрофагов 2. Усиление адгезионной активности лейкоцитов и эндотелия 3. Усиление выработки белков острой фазы 4. Повышение пролиферативной активности клеток 5. Повышение температуры тела
Тестовые задания к занятию № 3 Основными клетками-продуцентами цитокинов в реакциях врожденного иммунитета являются: 1. Клетки миелоидного ряда 2. Т-лимфоциты-хелперы 3. Цитотоксические Т-лимфоциты 4. В-лимфоциты 5. Плазматические клетки Эффекты интерлейкина 1β: 1. Активация лимфоцитов и макрофагов 2. Усиление адгезионной активности лейкоцитов и эндотелия 3. Усиление выработки белков острой фазы 4. Повышение пролиферативной активности клеток 5. Повышение температуры тела
 Тестовые задания к занятию № 3 В классификацию цитокинов входят: 1. Интерлейкины 2. Факторы некроза опухолей 3. Интерфероны 4. Факторы роста 5. Хемокины Основными цитокинами Т хелперов 2 типа являются: 1. ИЛ-2 и ИЛ-3 2. ИЛ-1; ИЛ-4; ИЛ-17 3. ИЛ-4; ИЛ-5; ИЛ-6; ИЛ-10; ИЛ-13 4. ИЛ-1 и ИЛ-12 5. ИЛ-6 и ИЛ-8
Тестовые задания к занятию № 3 В классификацию цитокинов входят: 1. Интерлейкины 2. Факторы некроза опухолей 3. Интерфероны 4. Факторы роста 5. Хемокины Основными цитокинами Т хелперов 2 типа являются: 1. ИЛ-2 и ИЛ-3 2. ИЛ-1; ИЛ-4; ИЛ-17 3. ИЛ-4; ИЛ-5; ИЛ-6; ИЛ-10; ИЛ-13 4. ИЛ-1 и ИЛ-12 5. ИЛ-6 и ИЛ-8
 Тестовые задания к занятию № 3 В запуске ответа цитотоксических Т-лимфоцитов участвуют: 1. ИЛ-1; ИЛ-4; ИЛ-17 2. ИЛ-4; ИЛ-5; ИЛ-6; ИЛ-10; ИЛ-13 3. ИЛ-1 и ИЛ-12 4. ИЛ-6 и ИЛ-8 5. ИЛ-2 и интерферон-γ К провоспалительным цитокинам не относится: 1. ИЛ-1 2. ИЛ-18 3. ИЛ-8 4. ФНО-α 5. ИЛ-10
Тестовые задания к занятию № 3 В запуске ответа цитотоксических Т-лимфоцитов участвуют: 1. ИЛ-1; ИЛ-4; ИЛ-17 2. ИЛ-4; ИЛ-5; ИЛ-6; ИЛ-10; ИЛ-13 3. ИЛ-1 и ИЛ-12 4. ИЛ-6 и ИЛ-8 5. ИЛ-2 и интерферон-γ К провоспалительным цитокинам не относится: 1. ИЛ-1 2. ИЛ-18 3. ИЛ-8 4. ФНО-α 5. ИЛ-10


