Обмен белков3.ppt
- Количество слайдов: 39
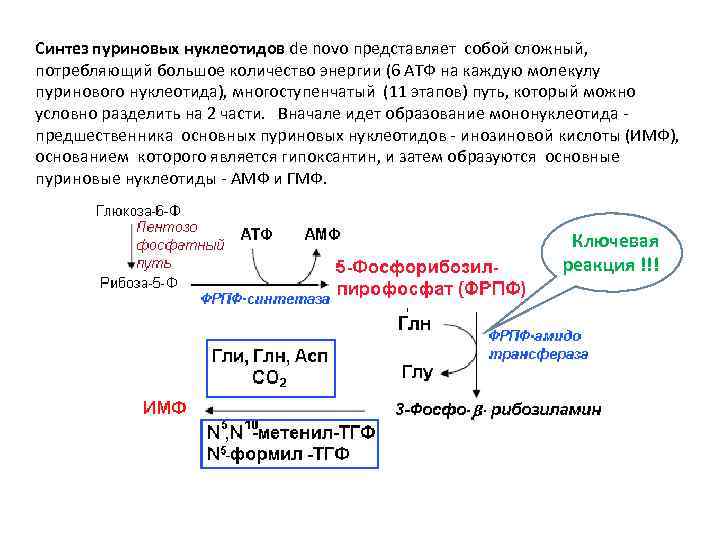
Синтез пуриновых нуклеотидов de novo представляет собой сложный, потребляющий большое количество энергии (6 АТФ на каждую молекулу пуринового нуклеотида), многоступенчатый (11 этапов) путь, который можно условно разделить на 2 части. Вначале идет образование мононуклеотида - предшественника основных пуриновых нуклеотидов - инозиновой кислоты (ИМФ), основанием которого является гипоксантин, и затем образуются основные пуриновые нуклеотиды - АМФ и ГМФ. Ключевая реакция !!!

Образующийся в первом этапе ИМФ служит точкой ветвления, от которой отходят двухшаговые пути синтеза АМФ и ГМФ.
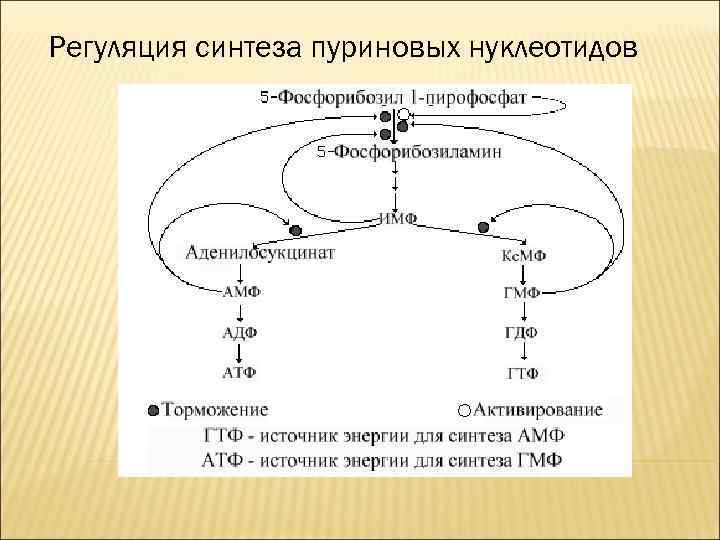
Регуляция синтеза пуриновых нуклеотидов
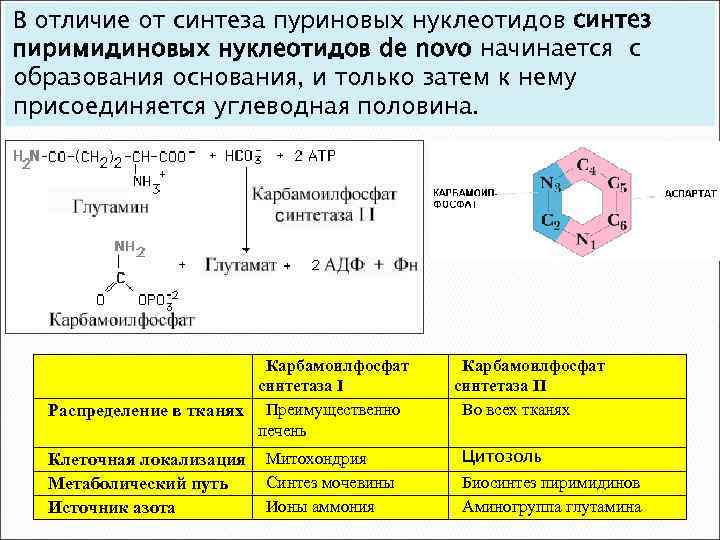
В отличие от синтеза пуриновых нуклеотидов синтез пиримидиновых нуклеотидов de novo начинается с образования основания, и только затем к нему присоединяется углеводная половина. Карбамоилфосфат синтетаза I Распределение в тканях Преимущественно печень Клеточная локализация Метаболический путь Источник азота Митохондрия Синтез мочевины Ионы аммония Карбамоилфосфат синтетаза II Во всех тканях Цитозоль Биосинтез пиримидинов Аминогруппа глутамина
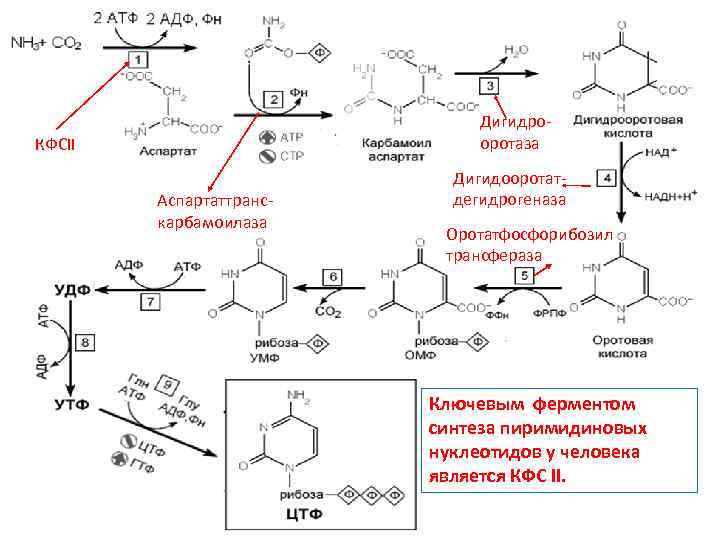
Дигидрооротаза КФСII Аспартаттранскарбамоилаза Дигидооротатдегидрогеназа Оротатфосфорибозил трансфераза Ключевым ферментом синтеза пиримидиновых нуклеотидов у человека является КФС II.
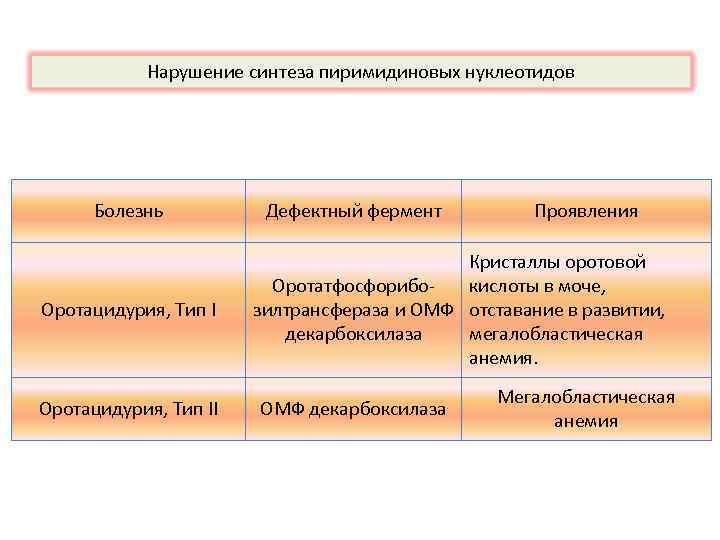
Нарушение синтеза пиримидиновых нуклеотидов Болезнь Оротацидурия, Тип II Дефектный фермент Проявления Кристаллы оротовой Оротатфосфорибокислоты в моче, зилтрансфераза и OMФ отставание в развитии, декарбоксилаза мегалобластическая анемия. ОМФ декарбоксилаза Мегалобластическая анемия

«Запасные» пути синтеза пуриновых нуклеотидов (реутилизация азотистых оснований и нуклеозидов) 1. АО + ФРПФ Е НМФ + Рн. Рн Е – фермент, в случае АМФ – аденинфосфорибозилтрансфераза; в случае образования ИМФ из гипоксантина и ГМФ из гуанина образования – гипоксантин-гуанинфосфорибозилтрансфераза 2. нуклеозид + АТФ Е – нуклеозидкиназа Е у АДФ НМФ + млекопитающих не имеет существенного значения Нарушения в работе ФРДФ синтетазы (гиперактивация) или сниженная активность ферментов «запасного» пути: гипоксантин-гуанин- или аденинфосфорибозилтрансфераз (генетические дефекты) приводят к подагре (вследствие гиперурикемии).

Мочевая кислота • выводится из организма с мочой. Почки активно ее реабсорбируют, поэтому ее концентрация в крови поддерживается на постоянном уровне 0. 15 -0. 50 ммоль/л. • слабая органическая кислота. Ионизированная форма мочевой кислоты (солевая) намного лучше растворяется в воде, чем ее протонированная форма (кислотная). Например, при р. Н 4. 8, когда молекула мочевой кислоты почти полностью протонирована (90%), можно растворить только одну десятую того, что растворяется при р. Н 6. 8, когда мочевая кислота на 90 % ионизирована. Так как р. Н мочи обычно ниже 5. 8, повышение уровня выводимой мочевой кислоты может привести к формированию камней в системе мочевыделения. • обладает антиоксидантными свойствами.
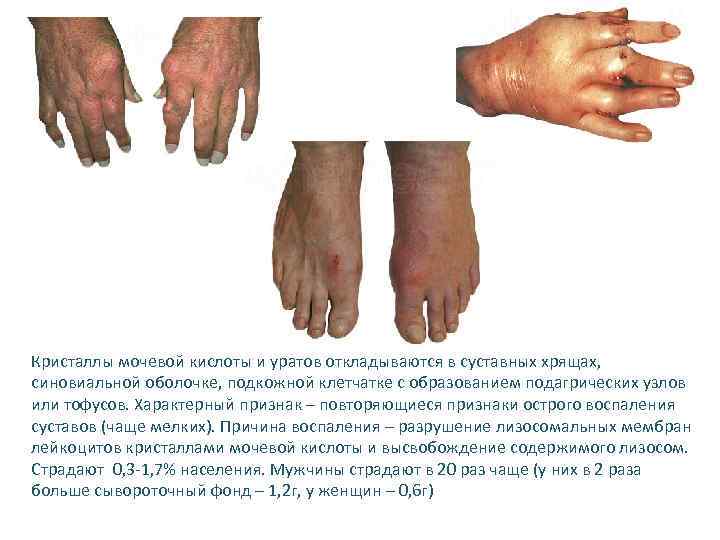
Кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов или тофусов. Характерный признак – повторяющиеся признаки острого воспаления суставов (чаще мелких). Причина воспаления – разрушение лизосомальных мембран лейкоцитов кристаллами мочевой кислоты и высвобождение содержимого лизосом. Страдают 0, 3 -1, 7% населения. Мужчины страдают в 20 раз чаще (у них в 2 раза больше сывороточный фонд – 1, 2 г, у женщин – 0, 6 г)

синдром Лёша-Нихена. Тяжелая форма гиперурикемии – Наследуется как рецессивный признак, сцепленный с Х-хромосомой и проявляется только у мальчиков в раннем возрасте (тофусы, уратные камни в мочевыводящих путях и серьезные неврологические отклонения с нарушением речи, церебраль-ными параличами, снижением интеллекта, склонностью к нанесению себе увечий – укусы губ, языка, пальцев). При отсутствии лечения предельный возраст – 10 лет, смерть – из-за нарушения функции почек. Причина - полное отсутствие активности гипоксантин-гуанинфосфорибозил- трансферазы. Концентрация мочевой кислоты в плазме крови в 2 -3 раза превышает норму. Самый ранний симптом в первые месяцы жизни – розовые и оранжевые пятна на пеленках, вызванные присутствием в моче кристаллов мочевой кислоты.
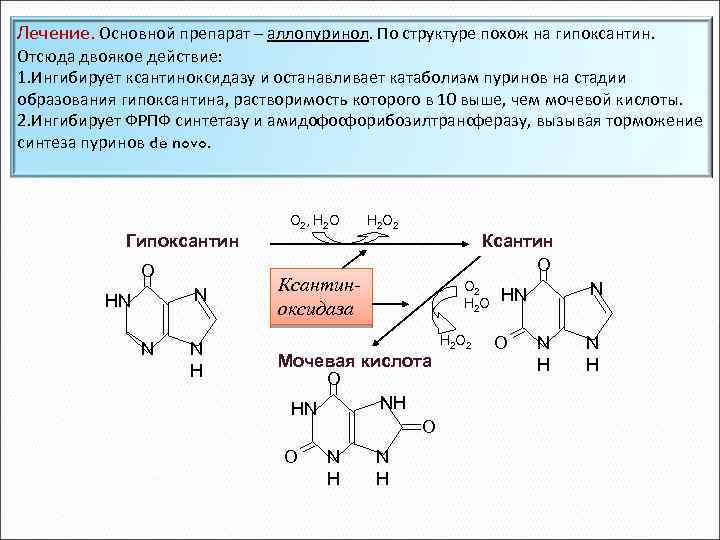
Лечение. Основной препарат – аллопуринол. По структуре похож на гипоксантин. Отсюда двоякое действие: 1. Ингибирует ксантиноксидазу и останавливает катаболизм пуринов на стадии образования гипоксантина, растворимость которого в 10 выше, чем мочевой кислоты. 2. Ингибирует ФРПФ синтетазу и амидофосфорибозилтрансферазу, вызывая торможение синтеза пуринов de novo. О 2, Н 2 О 2 Гипоксантин O N HN N N H Ксантин O Ксантиноксидаза О 2 Н 2 О 2 Мочевая кислота O NH HN O O N H N HN O N H

«Запасные» пути синтеза пиримидиновых нуклеотидов (реутилизация азотистых оснований и нуклеотидов) уридинфосфорилаза 1. Урацил + Рибоза-1 -фосфат Уридин + Н 3 РО 4 Киназа 2. ЦМФ + Н 2 О дезаминаза УМФ + NH 3 УМФ
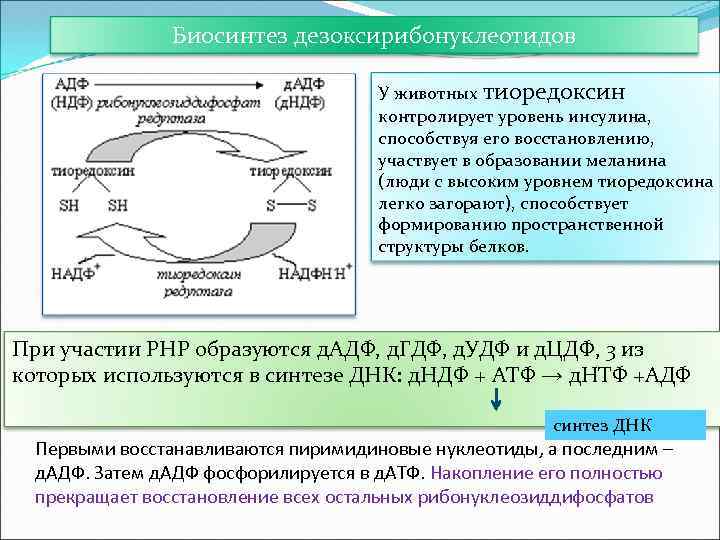
Биосинтез дезоксирибонуклеотидов У животных тиоредоксин контролирует уровень инсулина, способствуя его восстановлению, участвует в образовании меланина (люди с высоким уровнем тиоредоксина легко загорают), способствует формированию пространственной структуры белков. При участии РНР образуются д. АДФ, д. ГДФ, д. УДФ и д. ЦДФ, 3 из которых используются в синтезе ДНК: д. НДФ + АТФ → д. НТФ +AДФ синтез ДНК Первыми восстанавливаются пиримидиновые нуклеотиды, а последним – д. АДФ. Затем д. АДФ фосфорилируется в д. АТФ. Накопление его полностью прекращает восстановление всех остальных рибонуклеозиддифосфатов
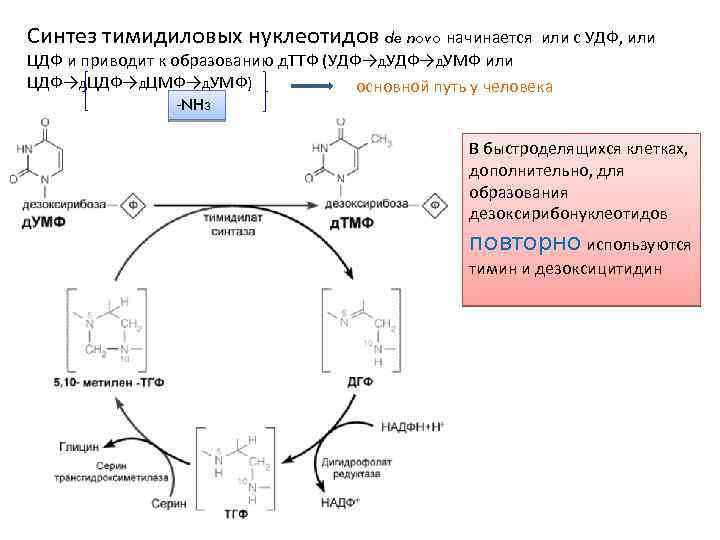
Синтез тимидиловых нуклеотидов de novo начинается или с УДФ, или ЦДФ и приводит к образованию д. ТТФ (УДФ→д. УМФ или ЦДФ→д. ЦМФ→д. УМФ) основной путь у человека -NH 3 В быстроделящихся клетках, дополнительно, для образования дезоксирибонуклеотидов повторно используются тимин и дезоксицитидин

Повтор, для привлечения внимания к работе фосфорилазы в клетках !!!
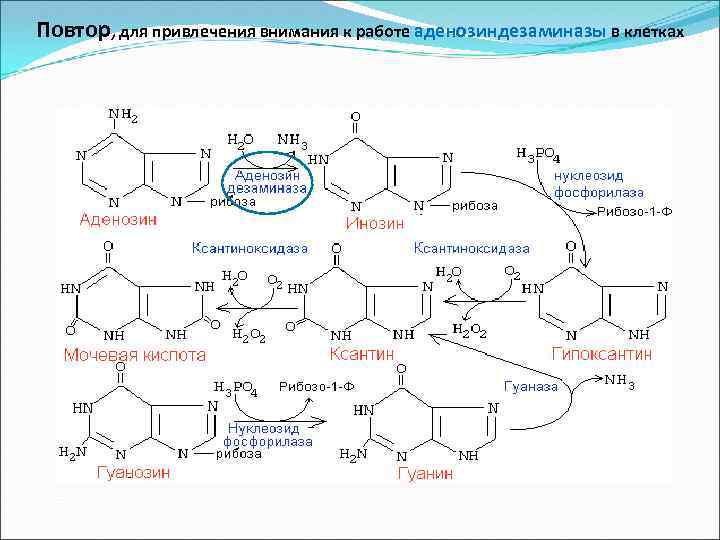
Повтор, для привлечения внимания к работе аденозиндезаминазы в клетках

При недостаточности аденозин дезаминазы страдают T и Bлимфоциты, развивается тяжелый хронический иммунодефицит. Причина – накопление в клетках д. АТФ, который ингибирует рибонуклеозидредуктазу (РНР). Нарушается синтез ДНК. Для клеток нелимфоцит. ряда это не опасно, т. к. работает фосфатаза д. АТФ. При недостаточности фосфорилазы нарушается функция T клеток (там высокая активность дезоксигуанозинкиназы, накапливается д. ГТФ, что тормозит РНР), в то время как B клетки остаются нормальными. Болезнь обычно фатальна у новорожденных , если не предпринимать специальные защитные меры

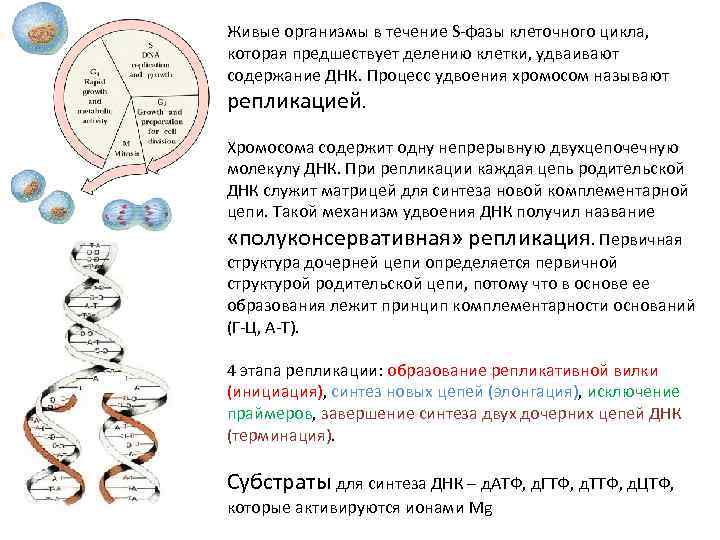
Живые организмы в течение S-фазы клеточного цикла, которая предшествует делению клетки, удваивают содержание ДНК. Процесс удвоения хромосом называют репликацией. Хромосома содержит одну непрерывную двухцепочечную молекулу ДНК. При репликации каждая цепь родительской ДНК служит матрицей для синтеза новой комплементарной цепи. Такой механизм удвоения ДНК получил название «полуконсервативная» репликация. Первичная структура дочерней цепи определяется первичной структурой родительской цепи, потому что в основе ее образования лежит принцип комплементарности оснований (Г-Ц, А-Т). 4 этапа репликации: образование репликативной вилки (инициация), синтез новых цепей (элонгация), исключение праймеров, завершение синтеза двух дочерних цепей ДНК (терминация). Субстраты для синтеза ДНК – д. АТФ, д. ГТФ, д. ТТФ, д. ЦТФ, которые активируются ионами Mg
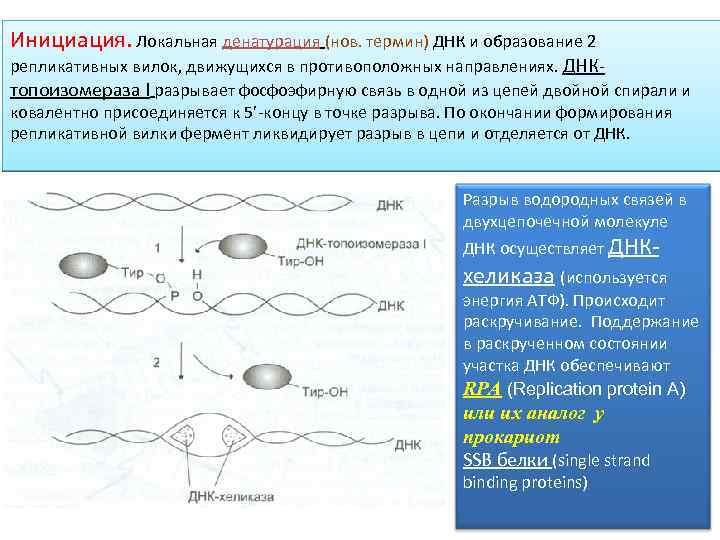
Инициация. Локальная денатурация (нов. термин) ДНК и образование 2 репликативных вилок, движущихся в противоположных направлениях. ДНКтопоизомераза I разрывает фосфоэфирную связь в одной из цепей двойной спирали и ковалентно присоединяется к 5’-концу в точке разрыва. По окончании формирования репликативной вилки фермент ликвидирует разрыв в цепи и отделяется от ДНК. Разрыв водородных связей в двухцепочечной молекуле ДНК осуществляет ДНК- хеликаза (используется энергия АТФ). Происходит раскручивание. Поддержание в раскрученном состоянии участка ДНК обеспечивают RPA (Replication protein A) или их аналог у прокариот SSB белки (single strand binding proteins)

Инициация синтеза ДНК происходит в нескольких сайтах хромосомы, которые называют сайтами инициации репликации, или ориджинами. На ориджинах при участии ДНК-топоизомеразы инициируется двунаправленная репликация. Образуются репликативные вилки, которые перемещаются в противоположных направлениях до тех пор, пока не встретятся со следующим репликоном (последовательность ДНК, ограниченная двумя ориджинами репликации), т. е. когда встретятся две репликативные вилки. Наличие ориджинов сокращает время репликации. После завершения репликации происходит метилирование нуклеотидных остатков вновь образованных цепей ДНК. Количество метилированных оснований 1 -8%. Источник метильных групп – S-аденозилметионин. Это необходимо для формирования структуры хромосом и регуляции транскрипции генов.
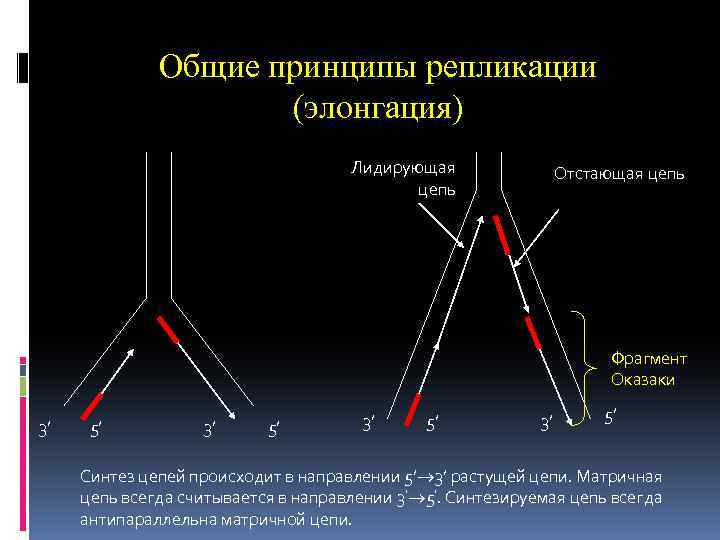
Общие принципы репликации (элонгация) Лидирующая цепь Отстающая цепь Фрагмент Оказаки 3’ 5’ Синтез цепей происходит в направлении 5’ 3’ растущей цепи. Матричная цепь всегда считывается в направлении 3’ 5’. Синтезируемая цепь всегда антипараллельна матричной цепи.

В матричном репликативном синтезе ДНК у эукариот принимают участие 5 ДНКполимераз. ДНК-полимеразы , , (дельта), (эпсилон) участвуют в синтезе ДНК в ядре, ДНК-полимераза (гамма) – в репликации митохондриальной ДНК.
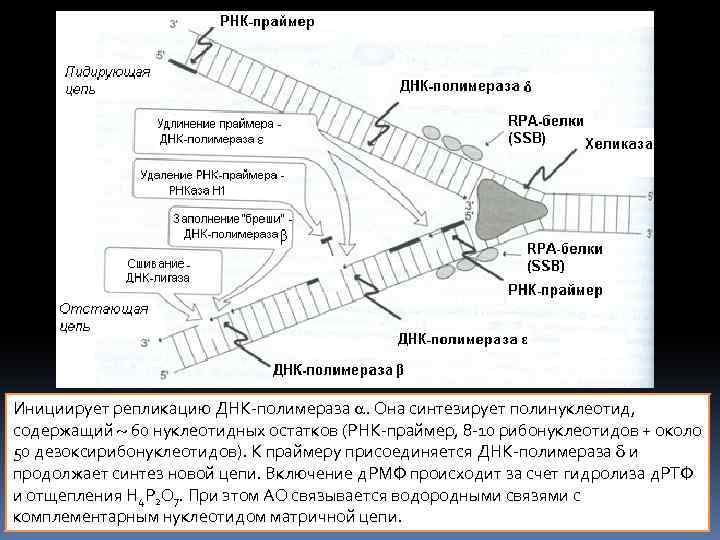
Инициирует репликацию ДНК-полимераза . Она синтезирует полинуклеотид, содержащий 60 нуклеотидных остатков (РНК-праймер, 8 -10 рибонуклеотидов + около 50 дезоксирибонуклеотидов). К праймеру присоединяется ДНК-полимераза и продолжает синтез новой цепи. Включение д. РМФ происходит за счет гидролиза д. РТФ и отщепления Н 4 Р 2 О 7. При этом АО связывается водородными связями с комплементарным нуклеотидом матричной цепи.

Репликация у эукариот Фермент ДНК-полимераза α Функция Инициация, синтез праймеров -- // -- β Репарация ДНК, достройка ДНК на месте удаленных праймеров -- // -- γ Репликация ДНК в митохондриях -- // -- δ Синтез ведущей цепи (основной фермент) -- // -- ε Наращивание отстающей цепи РНКаза Н 1 Удаление праймеров ДНК-лигаза Сшивание синтезированных фрагментов
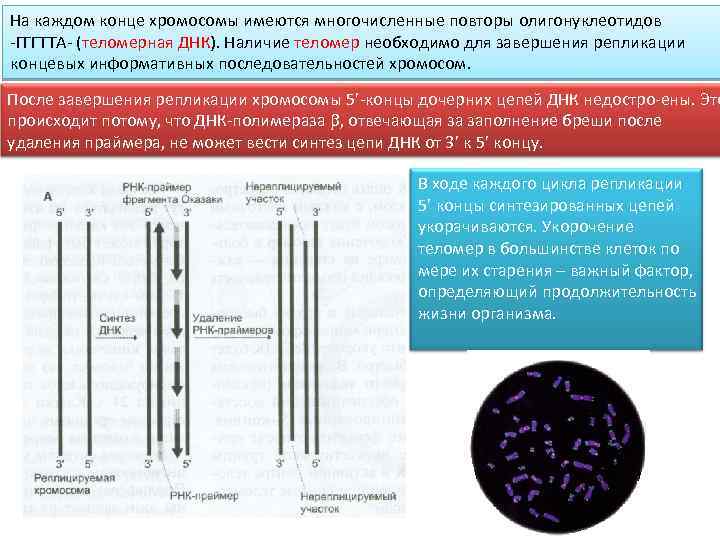
На каждом конце хромосомы имеются многочисленные повторы олигонуклеотидов -ГГГТТА- (теломерная ДНК). Наличие теломер необходимо для завершения репликации концевых информативных последовательностей хромосом. После завершения репликации хромосомы 5’-концы дочерних цепей ДНК недостро-ены. Это происходит потому, что ДНК-полимераза , отвечающая за заполнение бреши после удаления праймера, не может вести синтез цепи ДНК от 3’ к 5’ концу. В ходе каждого цикла репликации 5’ концы синтезированных цепей укорачиваются. Укорочение теломер в большинстве клеток по мере их старения – важный фактор, определяющий продолжительность жизни организма.
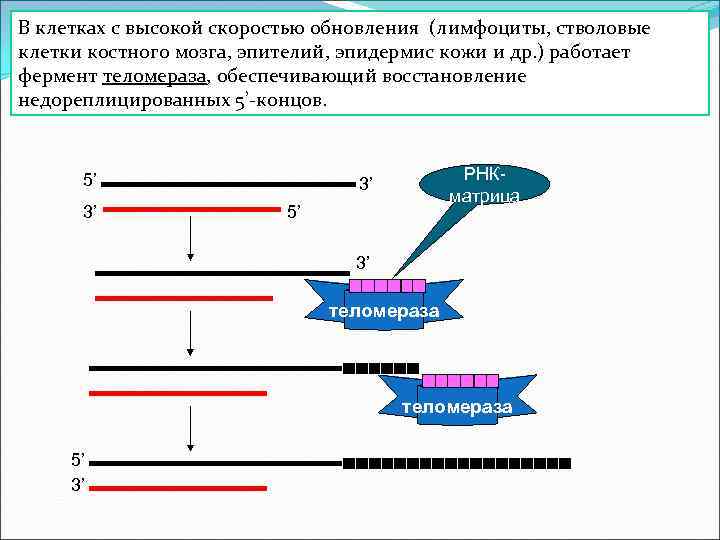
В клетках с высокой скоростью обновления (лимфоциты, стволовые клетки костного мозга, эпителий, эпидермис кожи и др. ) работает фермент теломераза, обеспечивающий восстановление недореплицированных 5’-концов. 5’ 3’ РНКматрица 3’ 5’ 3’ теломераза 5’ 3’

Репарация или репаративный синтез ДНК (исправление повреждений) Все репарационные механизмы основаны на том, что ДНК – двухцепочечная молекула. Если нуклеотидная последовательность одной из двух цепей оказывается поврежденной (измененной), информацию можно восстановить, так как вторая (комплементарная) цепь сохранена. Происходит в несколько этапов. Первый этап – выявляется нарушение комплементарности цепей ДНК. Второй этап – некомплементарный нуклеотид или основание устраняется. Третий и четвертый этапы – идет восстановление целостности цепи по принципу комплементарности. Спонтанные и индуцируемые повреждения. Спонтанные – ошибки репликации, депуринизация, дезаминирование Основные механизмы исправления повреждений: Прямая репарация Эксцизионная репарация (нуклеотидов и азотистых оснований)
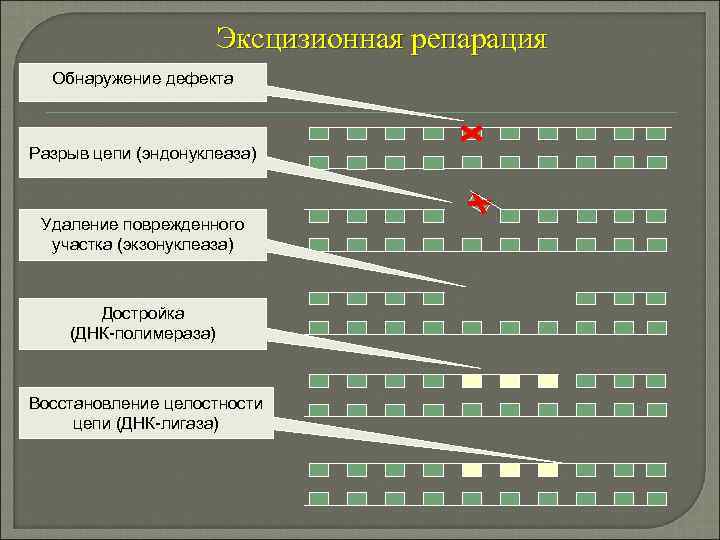
Эксцизионная репарация Обнаружение дефекта Разрыв цепи (эндонуклеаза) Удаление поврежденного участка (экзонуклеаза) Достройка (ДНК-полимераза) Восстановление целостности цепи (ДНК-лигаза)

Ошибки репликации – в дочернюю цепь ДНК включаются нуклеотиды, некомплементарные нуклеотидам матричной цепи. Частота – 1 раз на 105 -106 нуклеотидных остатков. Распознавание и удаление происходит при участи специальных белков mut S, mut L, mut H. Mut S находит неправильную пару и связывается с этим фрагментом. Mut H присоединяется к метилированному участку –ГАТЦ-, расположенному вблизи некомплементарной пары. Связующим между mut S и mut Н служит белок mut L. Его присоединение завершает образование активного фермента и способствует появлению у белка mut H эндонуклеазной активности. Гидролизуется фосфоэфирная связь в неметилированной дочерней цепи
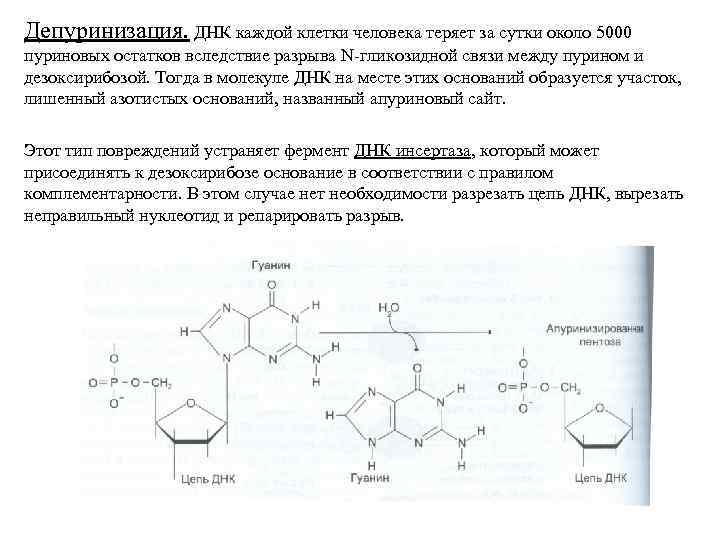
Депуринизация. ДНК каждой клетки человека теряет за сутки около 5000 пуриновых остатков вследствие разрыва N-гликозидной связи между пурином и дезоксирибозой. Тогда в молекуле ДНК на месте этих оснований образуется участок, лишенный азотистых оснований, названный апуриновый сайт. Этот тип повреждений устраняет фермент ДНК инсертаза, который может присоединять к дезоксирибозе основание в соответствии с правилом комплементарности. В этом случае нет необходимости разрезать цепь ДНК, вырезать неправильный нуклеотид и репарировать разрыв.
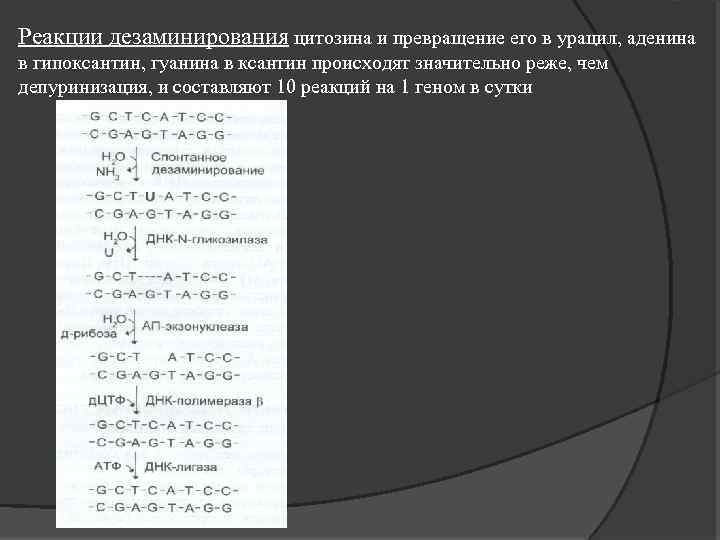
Реакции дезаминирования цитозина и превращение его в урацил, аденина в гипоксантин, гуанина в ксантин происходят значительно реже, чем депуринизация, и составляют 10 реакций на 1 геном в сутки
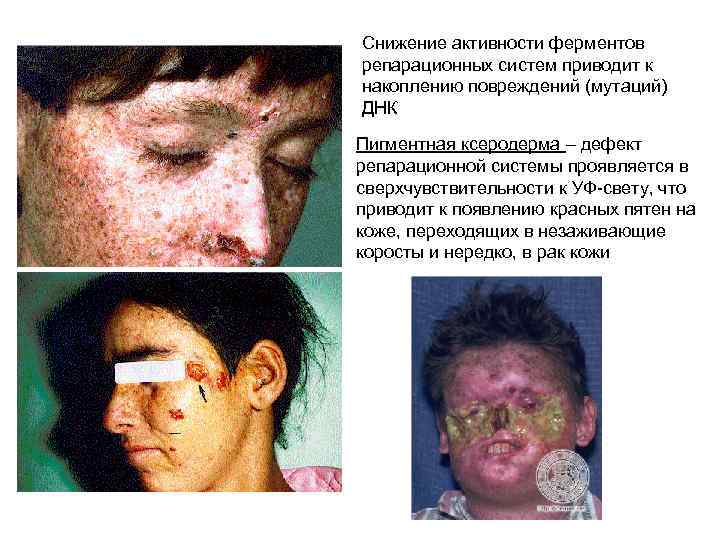
Снижение активности ферментов репарационных систем приводит к накоплению повреждений (мутаций) ДНК Пигментная ксеродерма – дефект репарационной системы проявляется в сверхчувствительности к УФ-свету, что приводит к появлению красных пятен на коже, переходящих в незаживающие коросты и нередко, в рак кожи

Апоптоз Это механизм программируемой и регулируемой гибели клеток. Он включается при повреждениях систем репарации ДНК и накопления повреждений ДНК. Эти изменения активируют ряд специфических протеаз в клетке, которые, в свою очередь, активируют эндонуклеазы. Эндонуклеазы гидролизуют ДНК сначала на крупные фрагменты, а затем – на мелкие (размер участка ДНК в нуклеосоме). Далее клетка распадается на мембранные везикулы (апоптозные тельца), содержащие фрагментированную ДНК; везикулы поглощаются и разрушаются фагоцитирующими клетками. Так устраняются клетки, размножение которых может быть опасным для организма, например, привести к развитию раковой опухоли. Другая функция апоптоза – уничтожение клеток, завершивших свою роль (исчезновение хвоста у головастика при превращении в лягушку и др. )

В настоящее время синтезировано много аналогов д. НТФ, которые включаются ДНК- полимеразами в ДНК и ингибируют репликацию. Мощные противоопухолевые препараты. Их действие основано на том, что 1) через «запасные» пути из них образуются нуклеотиды, которые блокируют тимидилат синтазу - 5 -фторурацил (аналог урацила), 2) тот же эффект, но путем имитации фолиевой кислоты (метотрексат, аминоптерин) или 3) ингибировать ДНКполимеразу – цитозинарабинозид (цитарабин). Антивирусные и антибактериальные препараты: азидотимидин (ретровирусная инфекция – ВИЧ), 5 -йоддезоксиуридин (вирус герпеса), азатиоприн (в организме превращается в 6 -меркаптопурин, оказывающий мощное иммуносупрессорное действие)

ТРАНСКРИПЦИЯ Синтез РНК начинается в определенных последовательностях (сайтах) ДНК, которые называют промоторы, и завершается в терминирующих участках (сайты терминации). Участок ДНК, ограниченный промотором и сайтом терминации, представляет собой единицу транскрипции – транскриптон. У эукариотов в составе транскриптона – 1 ген, у прокариотов несколько. В каждом транскриптоне транскрибируется только одна из двух цепей ДНК, которая называется матричной, вторая, комплементарная ей цепь, называется кодирующей. Синтез цепи РНК идет от 5’ – к 3’ концу, при этом матричная цепь ДНК всегда антипараллельна синтезируемой нуклеиновой кислоте ДНК-зависимые РНК-полимеразы. В ядрах эукариот 3 РНК-полимеразы: РНК -полимераза I, синтезирующая пре-р. РНК; РНК-полимераза II, ответственная за синтез пре-м. РНК; РНК-полимераза III, синтезирующая пре-т. РНК. Каждый фермент состоит из нескольких субъединиц – 2 , , ’, (сигма).
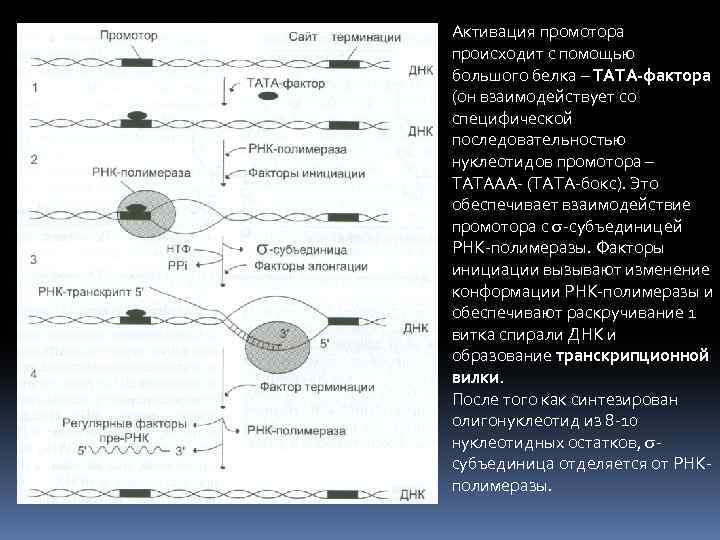
Активация промотора происходит с помощью большого белка – ТАТА-фактора (он взаимодействует со специфической последовательностью нуклеотидов промотора – ТАТААА- (ТАТА-бокс). Это обеспечивает взаимодействие промотора с -субъединицей РНК-полимеразы. Факторы инициации вызывают изменение конформации РНК-полимеразы и обеспечивают раскручивание 1 витка спирали ДНК и образование транскрипционной вилки. После того как синтезирован олигонуклеотид из 8 -10 нуклеотидных остатков, субъединица отделяется от РНКполимеразы.
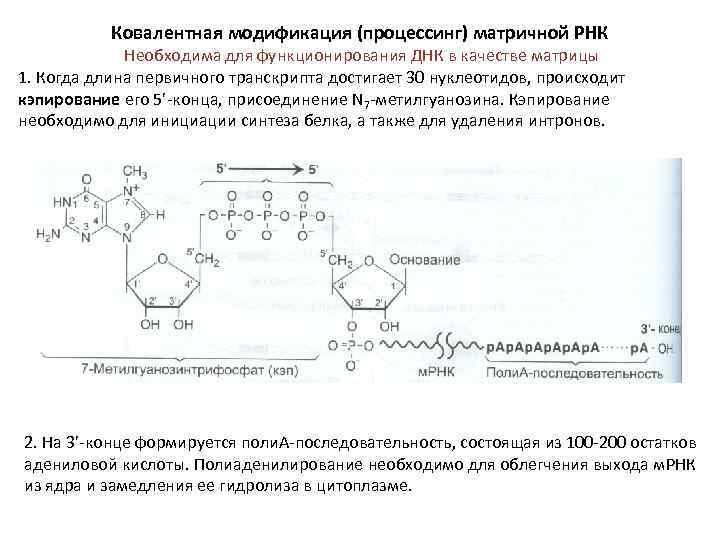
Ковалентная модификация (процессинг) матричной РНК Необходима для функционирования ДНК в качестве матрицы 1. Когда длина первичного транскрипта достигает 30 нуклеотидов, происходит кэпирование его 5’-конца, присоединение N 7 -метилгуанозина. Кэпирование необходимо для инициации синтеза белка, а также для удаления интронов. 2. На 3’-конце формируется поли. А-последовательность, состоящая из 100 -200 остатков адениловой кислоты. Полиаденилирование необходимо для облегчения выхода м. РНК из ядра и замедления ее гидролиза в цитоплазме.

3. Сплайсинг первичных транскриптов м. РНК – происходит в ядре Последовательности нуклеотидов, присутствующие в ДНК, но не входящие в Состав зрелой м. РНК, называются некодирующими или интронами (80 -1000 нуклеотидов), а присутствующие в зрелой м. РНК – кодирующими или экзонами. Соотношение информативной и неинформативной частей в транскриптонах эукариотов 1: 9 (у прокариотов 9: 1) Последовательности интронов вырезаются из первичного транскрипта, концы экзонов соединяются – сплайсинг. Процесс вырезания интронов протекает при участии мя. РНП формируют сплайсосому. Взаимодействую с РНК и друг с другом, они фиксируют и ориентируют реакционные группы первичного транскрипта. Каталитическая функция сплайсосом обусловлена РНКсоставляющими, такие РНК называют «рибозимы»
Обмен белков3.ppt