радикал полым.pptx
- Количество слайдов: 18
 Синтез полімерів. Радикальна полімеризація 1. Загальна характеристика методів отримання ВМС 2. Ланцюгова та ступінчаста полімеризація 3. Радикальна полімеризація. Ініціювання радикальної полімеризації 4. Ріст, обрив та передача ланцюга
Синтез полімерів. Радикальна полімеризація 1. Загальна характеристика методів отримання ВМС 2. Ланцюгова та ступінчаста полімеризація 3. Радикальна полімеризація. Ініціювання радикальної полімеризації 4. Ріст, обрив та передача ланцюга
 Класифікація основних методів отримання полімерів ØРадикальна полімеризація (ланцюговий статистичний процес) ØІонна полімеризація (стереорегулярний каталітичний процес) ØПоліконденсація (хімічні реакції багатофункціональних мономерів з виділенням низькомолекулярних продуктів) ØПоліприєднання (хімічні реакції багатофункціональних мономерів без виділення низькомолекулярних продуктів)
Класифікація основних методів отримання полімерів ØРадикальна полімеризація (ланцюговий статистичний процес) ØІонна полімеризація (стереорегулярний каталітичний процес) ØПоліконденсація (хімічні реакції багатофункціональних мономерів з виділенням низькомолекулярних продуктів) ØПоліприєднання (хімічні реакції багатофункціональних мономерів без виділення низькомолекулярних продуктів)
 Полімеризацією називається ланцюгова реакція, в ході якої молекули мономера послідовно приєднуються до активного центру, що знаходиться на кінці зростаючого ланцюга. Залежно від природи активного центру розрізняють радикальну і іонну полімеризацію. Поліконденсація - процес синтезу полімерів з поліфункціональних (найчастіше біфункціональних) з'єднань, що зазвичай супроводжується виділенням низькомолекулярних побічних продуктів (води, спиртів і т. п. ) при взаємодії функціональних груп.
Полімеризацією називається ланцюгова реакція, в ході якої молекули мономера послідовно приєднуються до активного центру, що знаходиться на кінці зростаючого ланцюга. Залежно від природи активного центру розрізняють радикальну і іонну полімеризацію. Поліконденсація - процес синтезу полімерів з поліфункціональних (найчастіше біфункціональних) з'єднань, що зазвичай супроводжується виділенням низькомолекулярних побічних продуктів (води, спиртів і т. п. ) при взаємодії функціональних груп.
 Особливості процесів полімеризації і поліконденсації Полімеризація Поліконденсація 1. Елементарний акт відбувається в 1. Елементарний акт пов'язаний з результаті реакції приєднання первинної взаємодією двох молекул бі-, активної частки до мономера з розривом поліфункціональних сполук. π-зв’язку 2. У кожному наступному акті 2. У кожному елементарному знову утворюється активний процесі відбувається зникнення двох центр. Продуктом реакції є активна активних центрів (функціональних груп макромолекулярна частка. кожного з мономерів) 3. Зменшення кількості мономера в 3. Зменшення кількості мономера процесі полімеризації відбувається поступово, найбільша миттєво, полімер утворюється вже на кількість його зменшується на початковій стадії реакції. Молекулярна початковій стадії. Молекулярна маса отриманого полімеру надалі не полімера зростає у міру проходження змінюється. реакції. 4. Збільшення тривалості протікання 4. Збільшення тривалості процесу реакції полімеризації призводить до поліконденсації приводить до зростання кількості виходу полімеру. молекулярної маси полімеру до певної Тривалість процесу не впливає на межі. Тривалість процесу не робить молекулярну масу полімеру. впливу на вихід полімеру.
Особливості процесів полімеризації і поліконденсації Полімеризація Поліконденсація 1. Елементарний акт відбувається в 1. Елементарний акт пов'язаний з результаті реакції приєднання первинної взаємодією двох молекул бі-, активної частки до мономера з розривом поліфункціональних сполук. π-зв’язку 2. У кожному наступному акті 2. У кожному елементарному знову утворюється активний процесі відбувається зникнення двох центр. Продуктом реакції є активна активних центрів (функціональних груп макромолекулярна частка. кожного з мономерів) 3. Зменшення кількості мономера в 3. Зменшення кількості мономера процесі полімеризації відбувається поступово, найбільша миттєво, полімер утворюється вже на кількість його зменшується на початковій стадії реакції. Молекулярна початковій стадії. Молекулярна маса отриманого полімеру надалі не полімера зростає у міру проходження змінюється. реакції. 4. Збільшення тривалості протікання 4. Збільшення тривалості процесу реакції полімеризації призводить до поліконденсації приводить до зростання кількості виходу полімеру. молекулярної маси полімеру до певної Тривалість процесу не впливає на межі. Тривалість процесу не робить молекулярну масу полімеру. впливу на вихід полімеру.
 Ланцюгова полімеризація. 1. Утворення активного центру, ініціація: А → А* 2. Ріст ланцюга: А* + А → А 1* + А → А 2* активні частинки Аn-1* + А → Аn* 3. Обрив ланцюга: Аn* + Am* → An. Am (макромолекула)
Ланцюгова полімеризація. 1. Утворення активного центру, ініціація: А → А* 2. Ріст ланцюга: А* + А → А 1* + А → А 2* активні частинки Аn-1* + А → Аn* 3. Обрив ланцюга: Аn* + Am* → An. Am (макромолекула)
 Ступінчаста полімеризація (На прикладі, полімеризації окису етилену 1. Утворення активного центру (СН 2 – СН 2)О + НОН → НО – СН 2 –ОН 2. Ріст ланцюга йде за рахунок перенесення атома водню активного центру до молекули мономера і руйнування циклу або подвійного зв'язку НО – СН 2 – ОН + (СН 2 – СН 2)О → НО – СН 2 – ОН НО – СН 2 ‑ О –СН 2 –ОН + (СН 2 – СН 2 ) О→ НО – СН 2 –О –СН 2 – О –СН 2 - СН 2 –ОН → … Ланцюг, що росте … → НО [СН 2 – СН 2 -О-]n – Н макромолекула
Ступінчаста полімеризація (На прикладі, полімеризації окису етилену 1. Утворення активного центру (СН 2 – СН 2)О + НОН → НО – СН 2 –ОН 2. Ріст ланцюга йде за рахунок перенесення атома водню активного центру до молекули мономера і руйнування циклу або подвійного зв'язку НО – СН 2 – ОН + (СН 2 – СН 2)О → НО – СН 2 – ОН НО – СН 2 ‑ О –СН 2 –ОН + (СН 2 – СН 2 ) О→ НО – СН 2 –О –СН 2 – О –СН 2 - СН 2 –ОН → … Ланцюг, що росте … → НО [СН 2 – СН 2 -О-]n – Н макромолекула
 Радикальна полімеризація ініціюється вільними радикалами - активними частками, що мають неспарений електрон. Стадії радикальної полімеризації Øініціація Ø ріст ланцюга Ø обрив ланцюга Ø передача ланцюга
Радикальна полімеризація ініціюється вільними радикалами - активними частками, що мають неспарений електрон. Стадії радикальної полімеризації Øініціація Ø ріст ланцюга Ø обрив ланцюга Ø передача ланцюга
 Термічна ініціація без ініціатора. Помітна при температурі вище 100°С. Часто обумовлено розкладом випадкових домішок. Чисті мономери (стирол і метилметакрилат) самоініцюються в ході бімолекулярної реакції. Термічна ініціація з ініціатором. В якості ініціаторів широко використовують різні типи перекисів: алкілперекиси (перекис тертбутилу), гідроперекиси (гідроперекис кумолу), ацилперекиси (перекис бензоїлу) та ін. Наприклад: Ph-С(О)-О-О-С(О)-Ph → 2 Ph-С(О)-O • → 2 Ph • + 2 CO 2↑
Термічна ініціація без ініціатора. Помітна при температурі вище 100°С. Часто обумовлено розкладом випадкових домішок. Чисті мономери (стирол і метилметакрилат) самоініцюються в ході бімолекулярної реакції. Термічна ініціація з ініціатором. В якості ініціаторів широко використовують різні типи перекисів: алкілперекиси (перекис тертбутилу), гідроперекиси (гідроперекис кумолу), ацилперекиси (перекис бензоїлу) та ін. Наприклад: Ph-С(О)-О-О-С(О)-Ph → 2 Ph-С(О)-O • → 2 Ph • + 2 CO 2↑
 . Фотохімічна ініціація 1. При дії УФ-світла з мономера можуть утворитися вільні радикали (стирол): 2. Використання фотоініціаторів – добавка розпадається на радикали, наприклад, фотохімічне ініціювання можна використовувати для полімеризації в присутності кетонів чи перекисів: НО-ОН → 2 НО • Радикал, що утворюється при розпаді молекули ініціатора, приєднується до подвійного зв'язку мономера і починає реакційний ланцюг: R • + CH 2 = CHX → R -CHX •
. Фотохімічна ініціація 1. При дії УФ-світла з мономера можуть утворитися вільні радикали (стирол): 2. Використання фотоініціаторів – добавка розпадається на радикали, наприклад, фотохімічне ініціювання можна використовувати для полімеризації в присутності кетонів чи перекисів: НО-ОН → 2 НО • Радикал, що утворюється при розпаді молекули ініціатора, приєднується до подвійного зв'язку мономера і починає реакційний ланцюг: R • + CH 2 = CHX → R -CHX •
 3. Використання фотосенсибілізаторів (сполук з розвиненою системою спряження, наприклад, бензофенон С 6 Н 5 СОС 6 Н 5). Де С – мономер або ініціатор.
3. Використання фотосенсибілізаторів (сполук з розвиненою системою спряження, наприклад, бензофенон С 6 Н 5 СОС 6 Н 5). Де С – мономер або ініціатор.
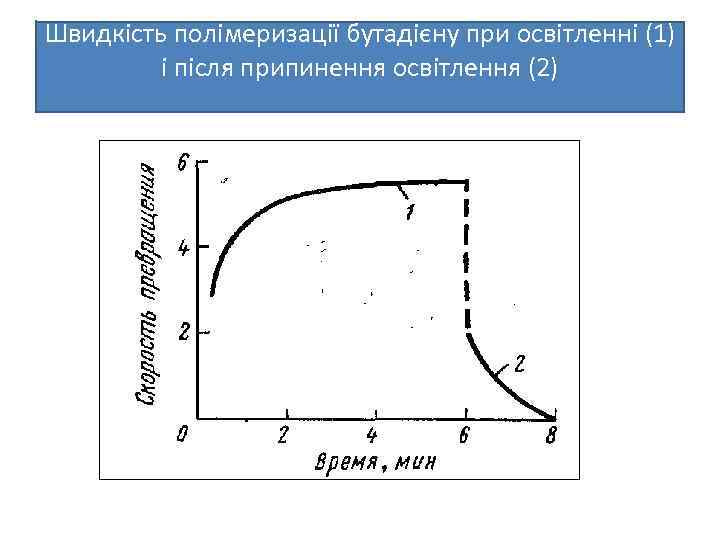 Швидкість полімеризації бутадієну при освітленні (1) і після припинення освітлення (2)
Швидкість полімеризації бутадієну при освітленні (1) і після припинення освітлення (2)
 Радіаційно-хімічна ініціація. Молекули мономера при дії прискорених електронів або гама -променів іонізуються, а потім дають радикали: Енергія збудження може перевищити енергію розриву хімічного зв'язку, в результаті молекула розпадається на радикали. Таким чином можна ініціювати прищеплену полімеризацію.
Радіаційно-хімічна ініціація. Молекули мономера при дії прискорених електронів або гама -променів іонізуються, а потім дають радикали: Енергія збудження може перевищити енергію розриву хімічного зв'язку, в результаті молекула розпадається на радикали. Таким чином можна ініціювати прищеплену полімеризацію.
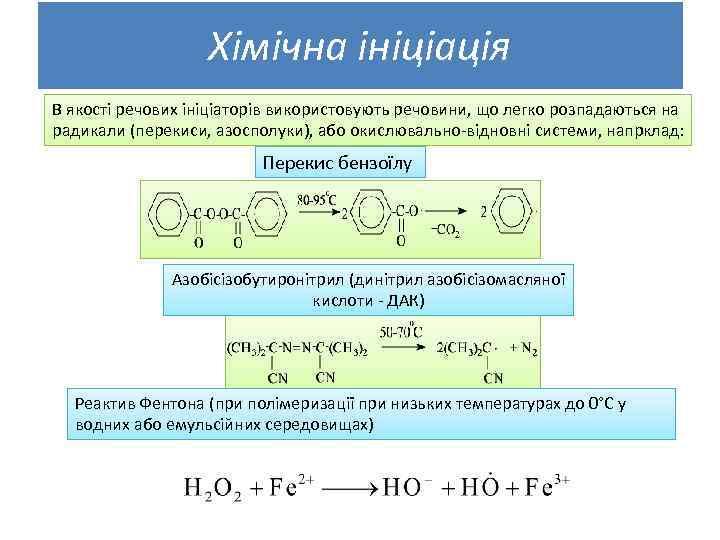 Хімічна ініціація В якості речових ініціаторів використовують речовини, що легко розпадаються на радикали (перекиси, азосполуки), або окислювально-відновні системи, напрклад: Перекис бензоїлу Азобісізобутиронітрил (динітрил азобісізомасляної кислоти - ДАК) Реактив Фентона (при полімеризації при низьких температурах до 0°С у водних або емульсійних середовищах)
Хімічна ініціація В якості речових ініціаторів використовують речовини, що легко розпадаються на радикали (перекиси, азосполуки), або окислювально-відновні системи, напрклад: Перекис бензоїлу Азобісізобутиронітрил (динітрил азобісізомасляної кислоти - ДАК) Реактив Фентона (при полімеризації при низьких температурах до 0°С у водних або емульсійних середовищах)
 Ріст ланцюга полягає в послідовному приєднанні молекул мономера до активного центру, що утворюється.
Ріст ланцюга полягає в послідовному приєднанні молекул мономера до активного центру, що утворюється.
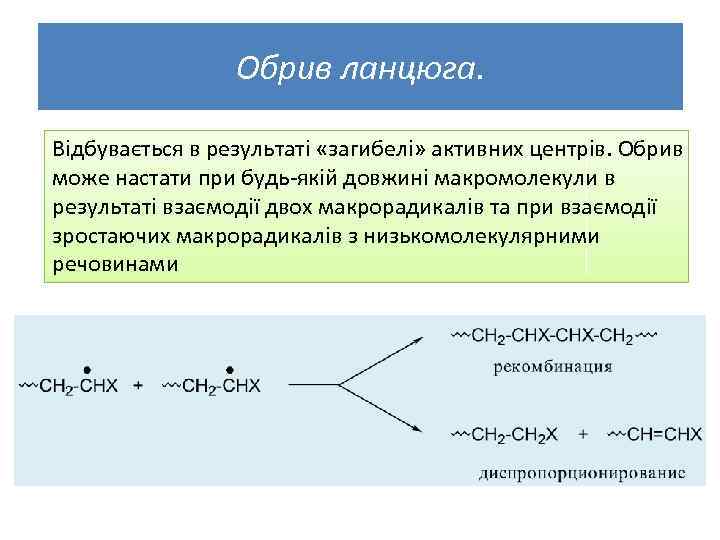 Обрив ланцюга. Відбувається в результаті «загибелі» активних центрів. Обрив може настати при будь-якій довжині макромолекули в результаті взаємодії двох макрорадикалів та при взаємодії зростаючих макрорадикалів з низькомолекулярними речовинами
Обрив ланцюга. Відбувається в результаті «загибелі» активних центрів. Обрив може настати при будь-якій довжині макромолекули в результаті взаємодії двох макрорадикалів та при взаємодії зростаючих макрорадикалів з низькомолекулярними речовинами
 Передача ланцюга . Відбувається при відриві радикалом. атома або групи атомів від якоїнебудь молекули (передавача ланцюга). Наприклад, передача ланцюга може здійснюватися через молекулу мономера (вінілацетату) : чи через молекулу розчинника (толуолу): чи через речовини (регулятори росту), що спеціально вводяться, наприклад, меркаптани:
Передача ланцюга . Відбувається при відриві радикалом. атома або групи атомів від якоїнебудь молекули (передавача ланцюга). Наприклад, передача ланцюга може здійснюватися через молекулу мономера (вінілацетату) : чи через молекулу розчинника (толуолу): чи через речовини (регулятори росту), що спеціально вводяться, наприклад, меркаптани:
 Ініціювання, ріст та обрив ланцюга на прикладі вінілпохідних: НО-ОН → 2 НО • (нагрівання) 1. Ініціювання 2. Ріст ланцюга
Ініціювання, ріст та обрив ланцюга на прикладі вінілпохідних: НО-ОН → 2 НО • (нагрівання) 1. Ініціювання 2. Ріст ланцюга
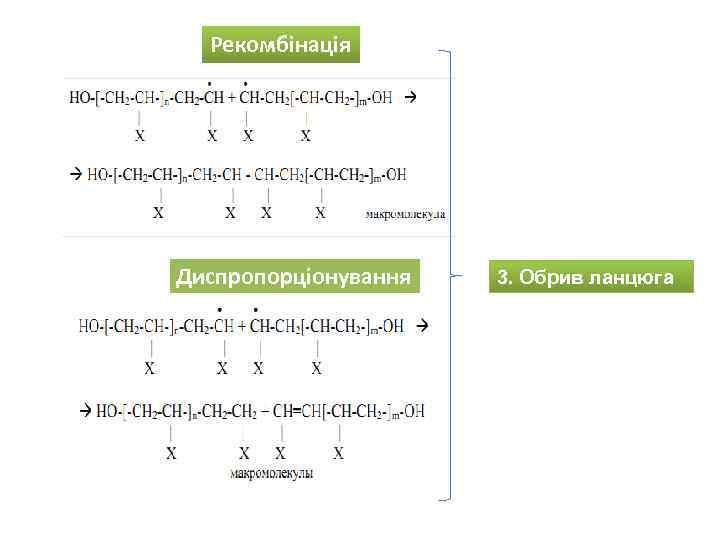 Рекомбінація Диспропорціонування 3. Обрив ланцюга
Рекомбінація Диспропорціонування 3. Обрив ланцюга


