синтез НК лекция март 2012.ppt
- Количество слайдов: 67
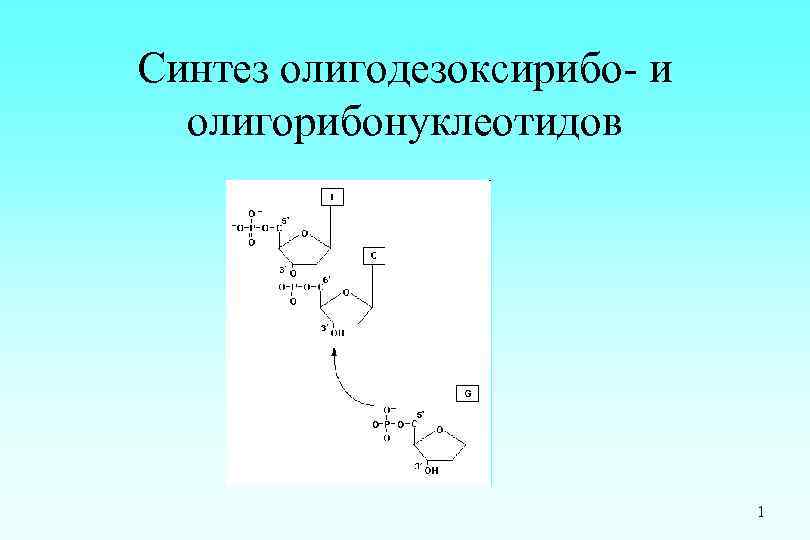
Синтез олигодезоксирибо- и олигорибонуклеотидов 1

April 25 th 2003 50 th Anniversary of publications in Nature on the structure of the DNA double helix Watson and Crick Franklin and Gosling Wilkins, Stokes and Wilson 2
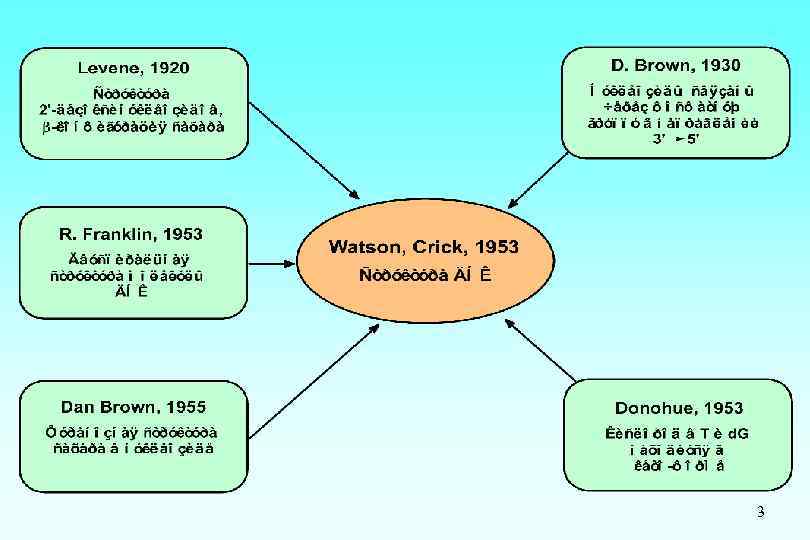
3

Click to edit Master title style • Click to edit Master text styles – Second level • Third level – Fourth level » Fifth level Herbert Wilson 06/02/2018 James Watson Jennifer Glynn (sister of Rosalind Franklin) 4

A. M. Michelson and Sir A. R. Todd. (1955) J. Chem. Soc. 2632 -2638 5

H. G. Khorana 6
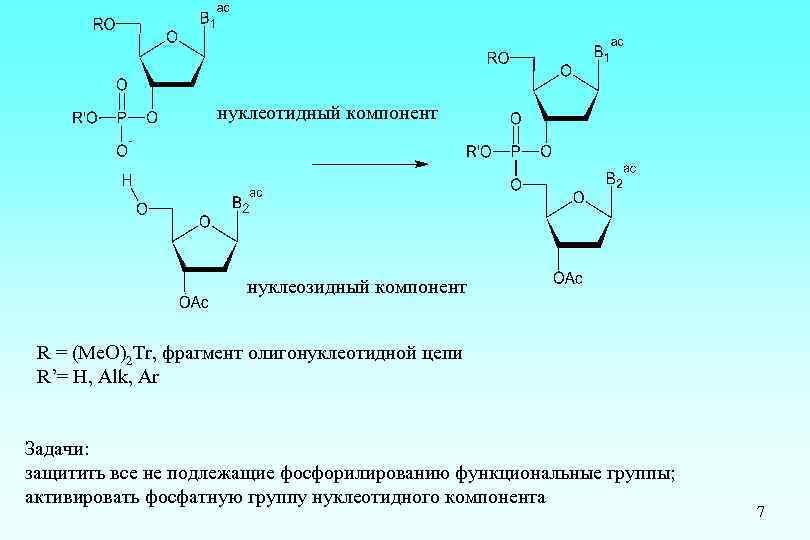
нуклеотидный компонент нуклеозидный компонент R = (Me. O)2 Tr, фрагмент олигонуклеотидной цепи R’= H, Alk, Ar Задачи: защитить все не подлежащие фосфорилированию функциональные группы; активировать фосфатную группу нуклеотидного компонента 7
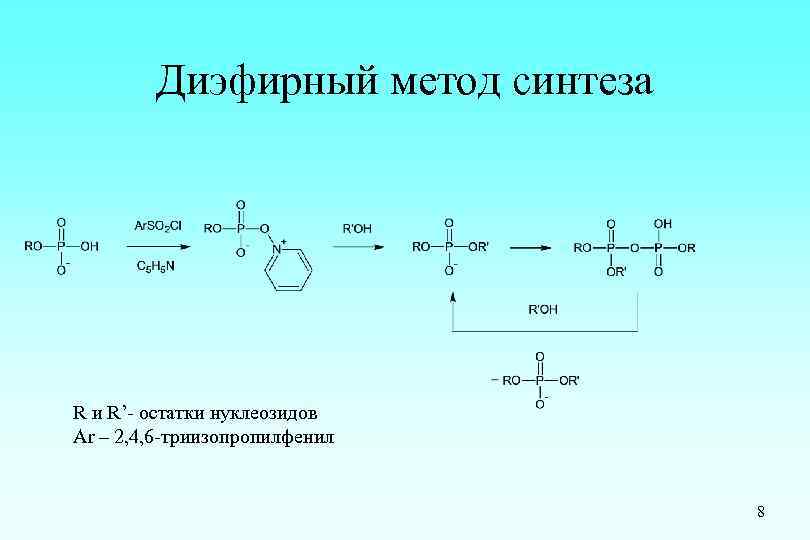
Диэфирный метод синтеза R и R’- остатки нуклеозидов Ar – 2, 4, 6 -триизопропилфенил 8
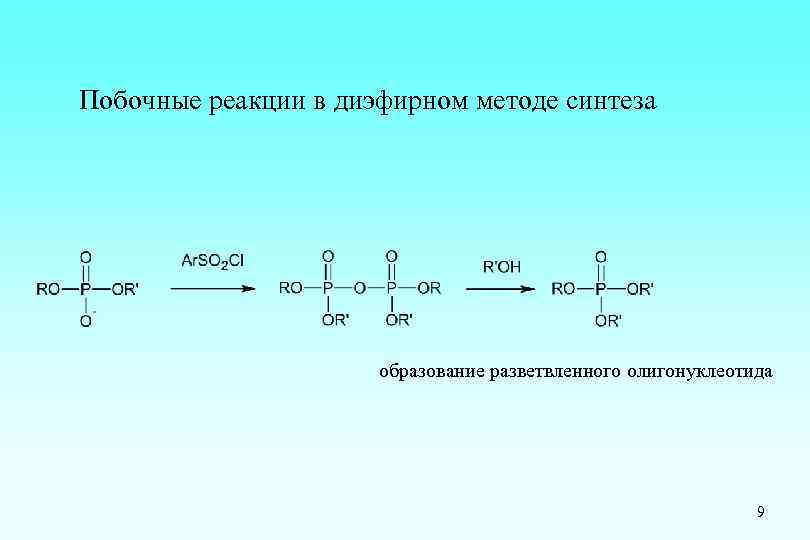
Побочные реакции в диэфирном методе синтеза образование разветвленного олигонуклеотида 9
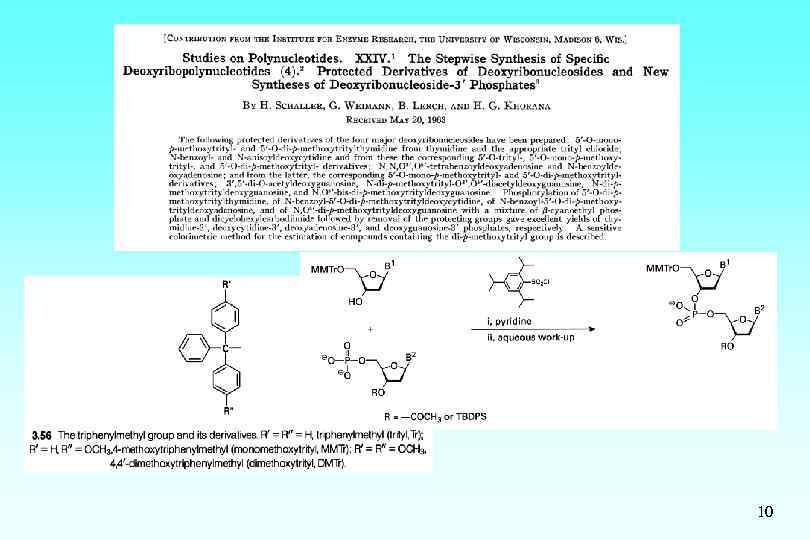
10
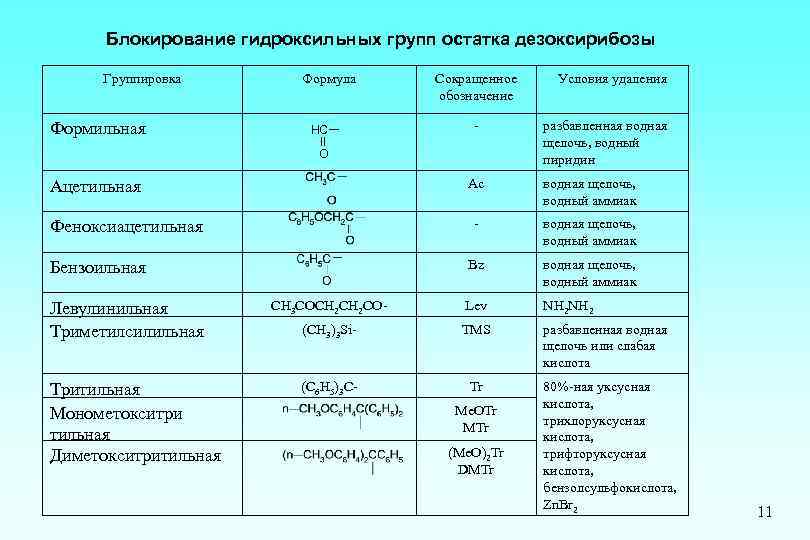
Блокирование гидроксильных групп остатка дезоксирибозы Группировка Формильная Формула HC Сокращенное обозначение - O водная щелочь, водный аммиак - водная щелочь, водный аммиак Bz водная щелочь, водный аммиак CH 3 COCH 2 CO- Lev NH 2 (CH 3)3 Si- TMS разбавленная водная щелочь или слабая кислота (C 6 H 5)3 C- Tr Феноксиацетильная Бензоильная Тритильная Монометокситри тильная Диметокситритильная разбавленная водная щелочь, водный пиридин Ас Ацетильная Левулинильная Триметилсилильная Условия удаления Me. OTr MTr (Me. O)2 Tr DMTr 80%-ная уксусная кислота, трихлоруксусная кислота, трифторуксусная кислота, бензолсульфокислота, Zn. Br 2 11
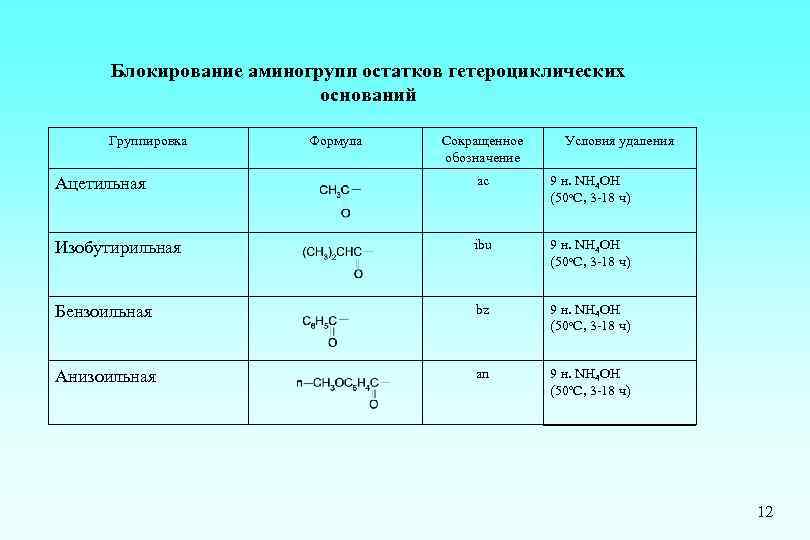
Блокирование аминогрупп остатков гетероциклических оснований Группировка Формула Сокращенное обозначение Условия удаления Ацетильная ac 9 н. NH 4 OH (50 o. C, 3 -18 ч) Изобутирильная ibu 9 н. NH 4 OH (50 o. C, 3 -18 ч) Бензоильная bz 9 н. NH 4 OH (50 o. C, 3 -18 ч) Анизоильная an 9 н. NH 4 OH (50 o. C, 3 -18 ч) 12
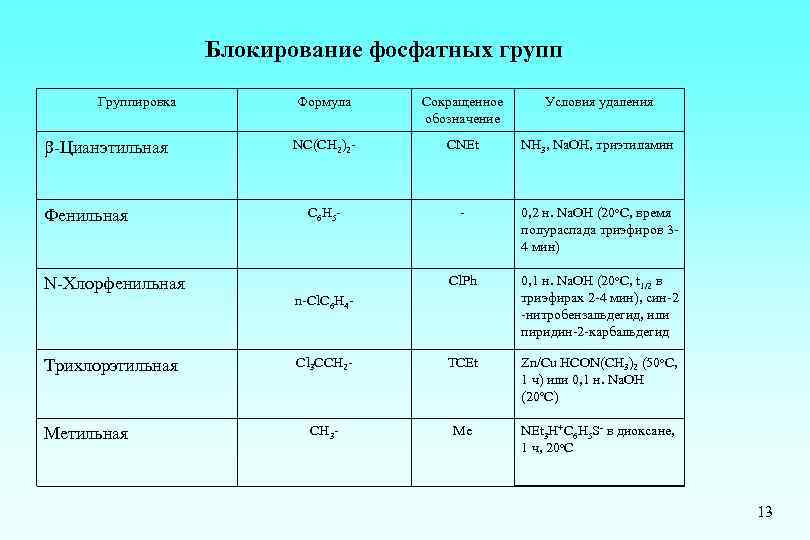
Блокирование фосфатных групп Группировка -Цианэтильная Фенильная N-Хлорфенильная Трихлорэтильная Метильная Формула Сокращенное обозначение Условия удаления NC(CH 2)2 - CNEt NH 3, Na. OH, триэтиламин C 6 H 5 - - 0, 2 н. Na. OH (20 о. С, время полураспада триэфиров 34 мин) Cl. Ph 0, 1 н. Na. OH (20 о. С, t 1/2 в триэфирах 2 -4 мин), син-2 -нитробензальдегид, или пиридин-2 -карбальдегид Cl 3 CCH 2 - TCEt Zn/Cu HCON(CH 3)2 (50 o. C, 1 ч) или 0, 1 н. Na. OH (20 o. C) CH 3 - Me NЕt 3 H+C 6 H 5 S- в диоксане, 1 ч, 20 о. С n-Cl. C 6 H 4 - 13
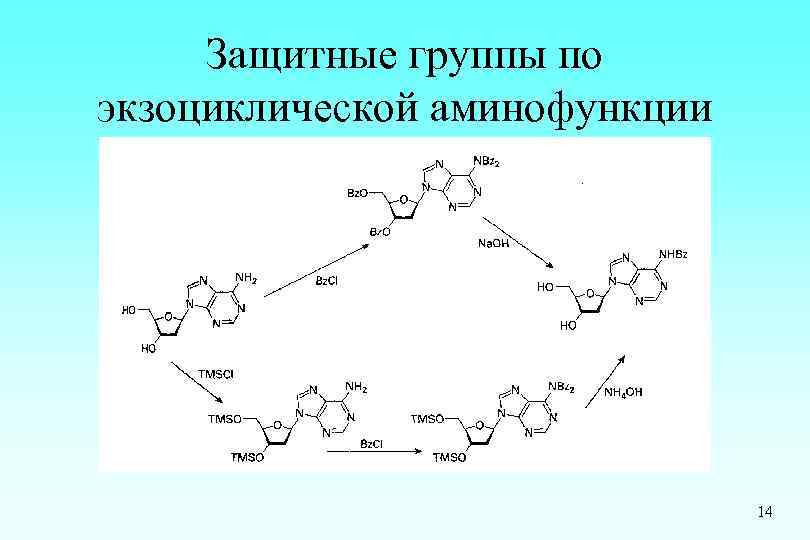
Защитные группы по экзоциклической аминофункции 14
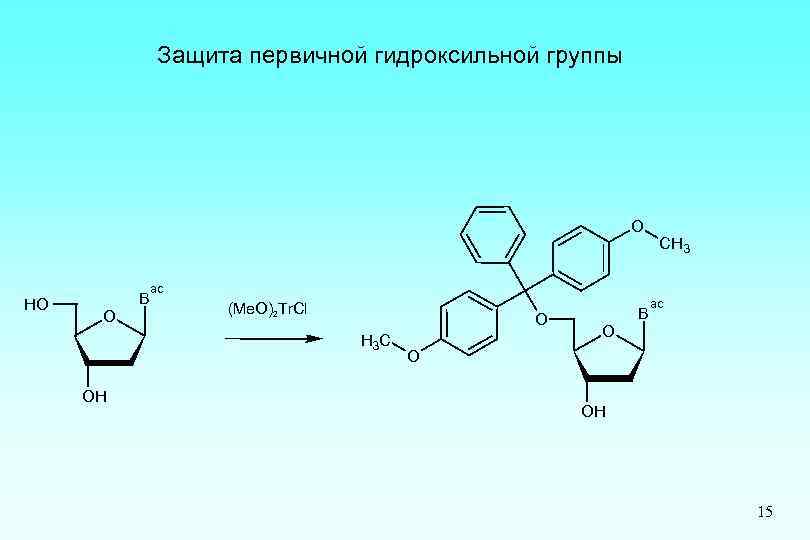
Защита первичной гидроксильной группы O HO B O ac (Me. O)2 Tr. Cl O H 3 C OH CH 3 B ac O O OH 15
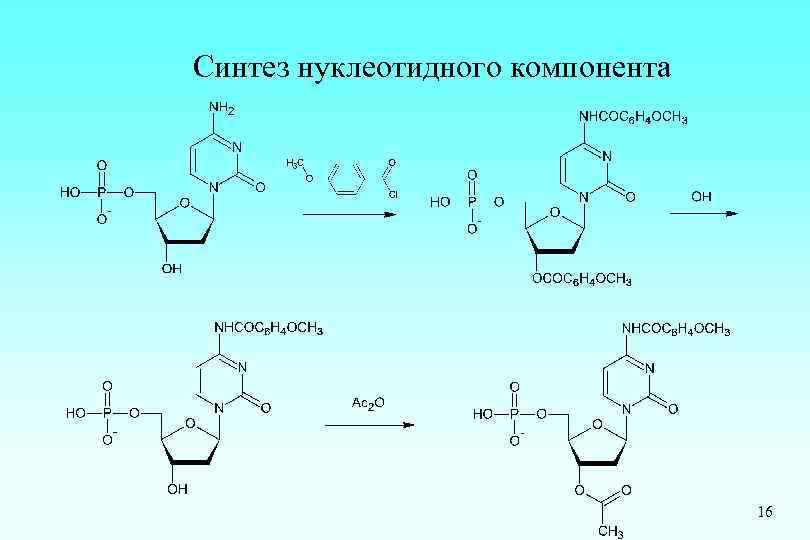
Синтез нуклеотидного компонента 16
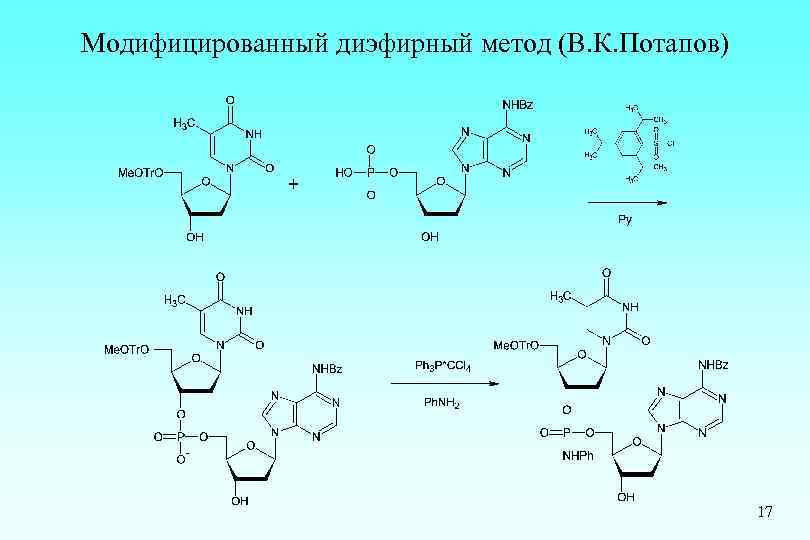
Модифицированный диэфирный метод (В. К. Потапов) 17

Khorana’s group 1970 Madison, Wisconsin 18
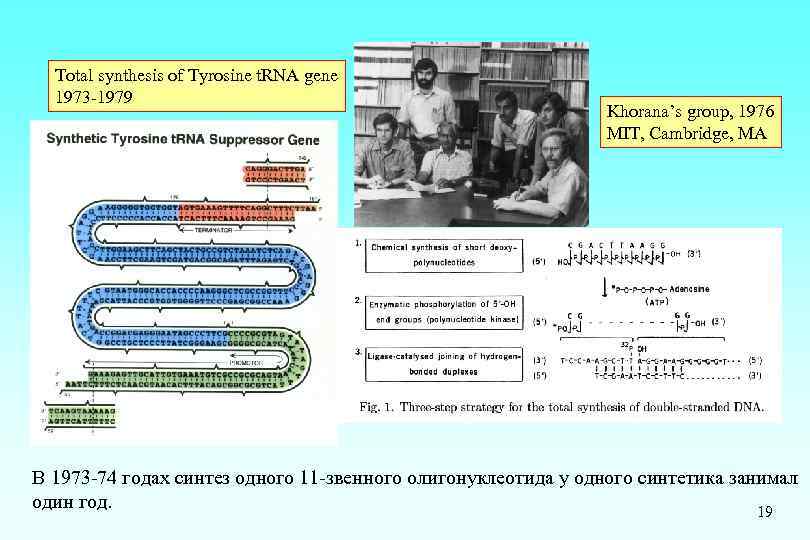
Total synthesis of Tyrosine t. RNA gene 1973 -1979 Khorana’s group, 1976 MIT, Cambridge, MA В 1973 -74 годах синтез одного 11 -звенного олигонуклеотида у одного синтетика занимал один год. 19

Недостатки диэфирного метода синтеза: наличие побочных продуктов; продолжительное время реакции (4 -5 часов); относительно низкий выход целевого продукта (30 -60%); сложность выделения коротких фрагментов ДНК, используемых на последующих стадиях синтеза 20
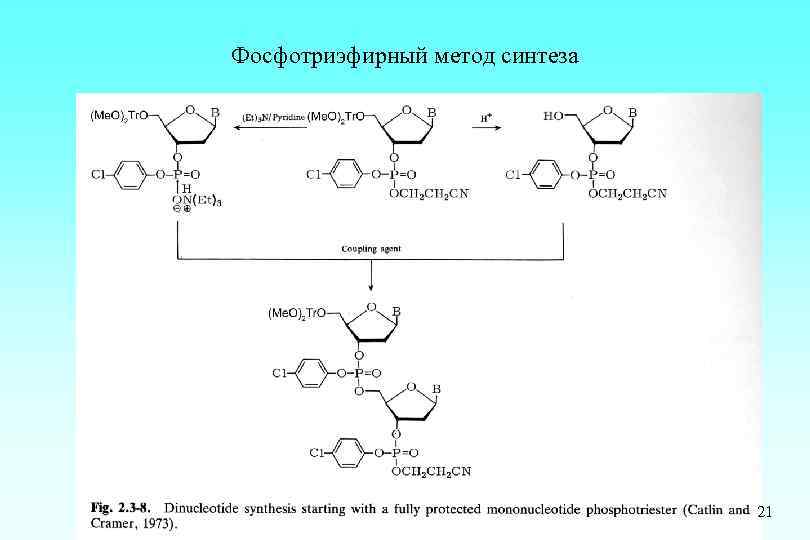
Фосфотриэфирный метод синтеза 21
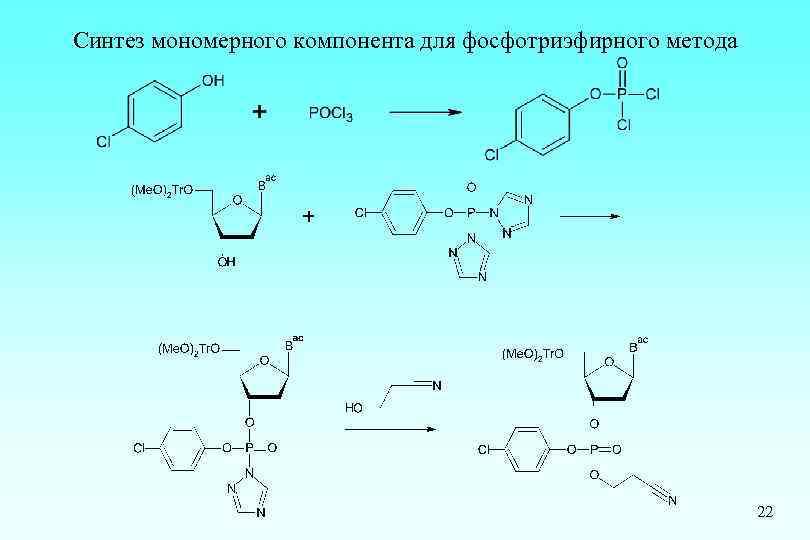
Синтез мономерного компонента для фосфотриэфирного метода 22
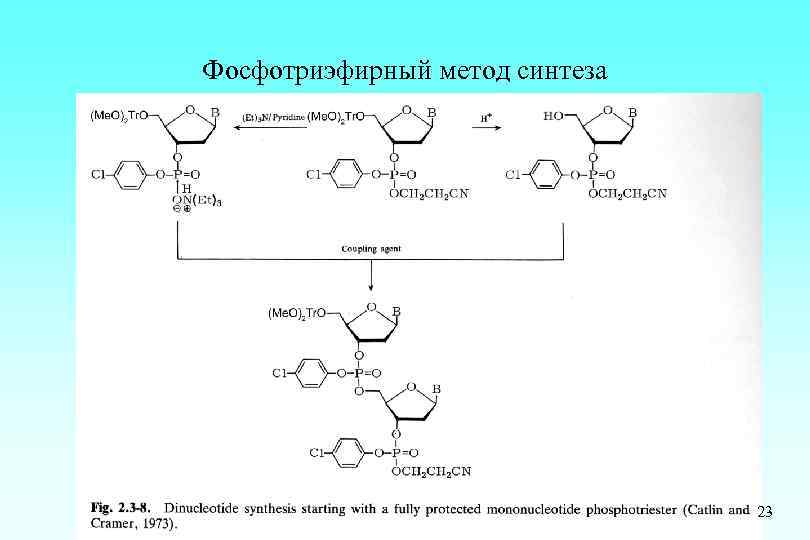
Фосфотриэфирный метод синтеза 23
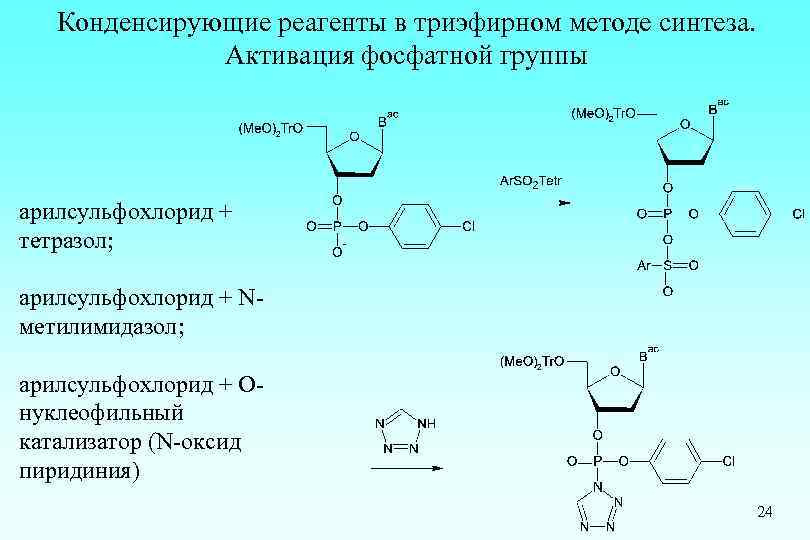
Конденсирующие реагенты в триэфирном методе синтеза. Активация фосфатной группы арилсульфохлорид + тетразол; арилсульфохлорид + Nметилимидазол; арилсульфохлорид + Онуклеофильный катализатор (N-оксид пиридиния) 24
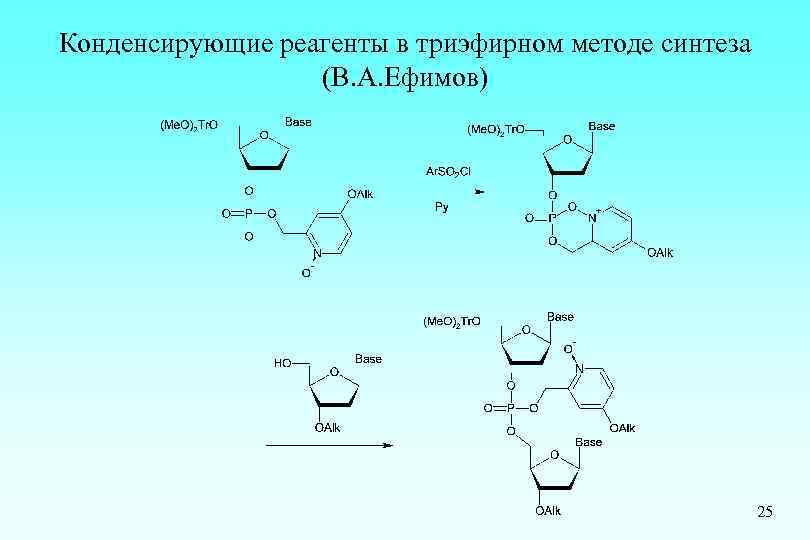
Конденсирующие реагенты в триэфирном методе синтеза (В. А. Ефимов) 25

Недостатки диэфирного метода синтеза: наличие побочных продуктов; продолжительное время реакции (4 -5 часов); относительно низкий выход целевого продукта (30 -60%); сложность выделения коротких фрагментов ДНК, используемых на последующих стадиях синтеза 26

Преимущества триэфирного метода синтеза Отсутствие побочных продуктов; Сокращение времени реакции до 15 -30 минут; Повышение выхода целевого продукта до 80 -90%; Эффективное выделение промежуточных и целевых продуктов адсорбционной хроматографией на силикагеле в органических растворителях 27
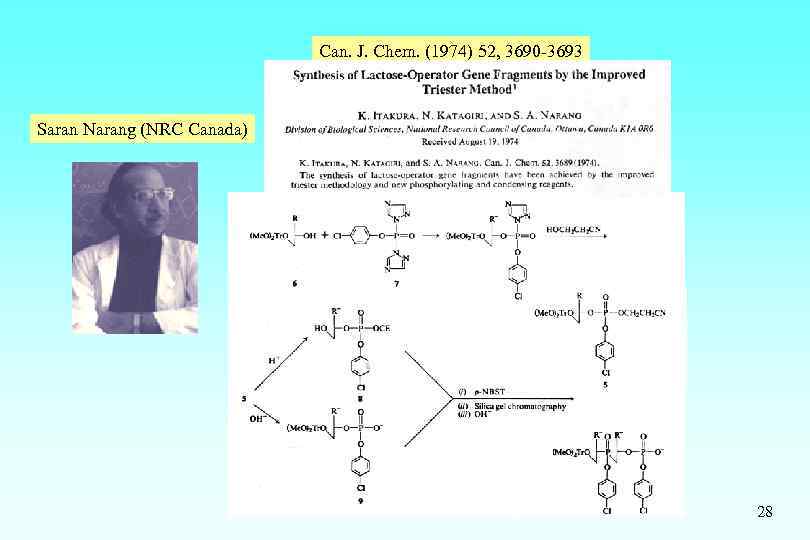
Can. J. Chem. (1974) 52, 3690 -3693 Saran Narang (NRC Canada) 28

Keiichi Itakura Science Dec. 1977 Развитие компаний по синтезу генов – Genetech, ICI Pharmaceuticals (Astra-Zeneca). 29
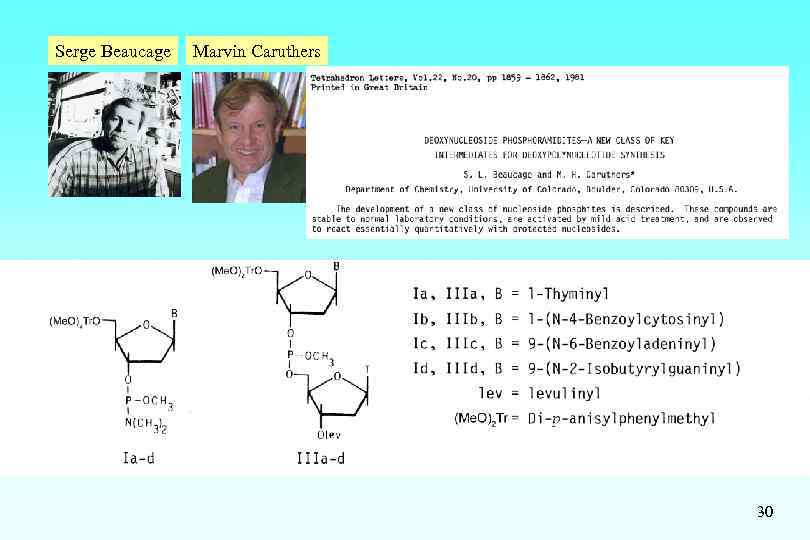
Serge Beaucage Marvin Caruthers 30
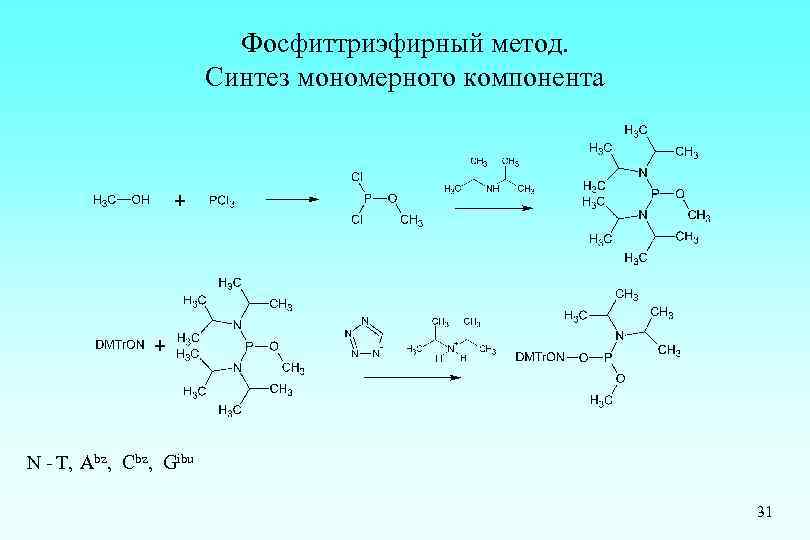
Фосфиттриэфирный метод. Синтез мономерного компонента N - T, Abz, Cbz, Gibu 31
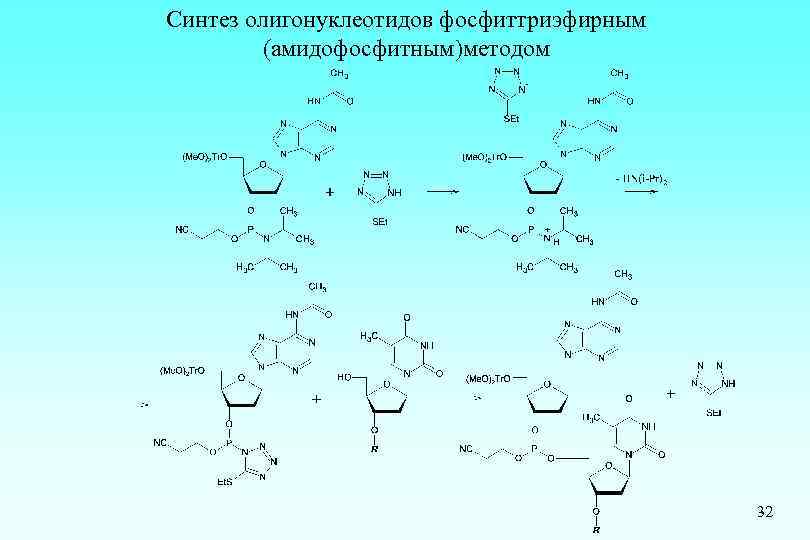
Синтез олигонуклеотидов фосфиттриэфирным (амидофосфитным)методом 32
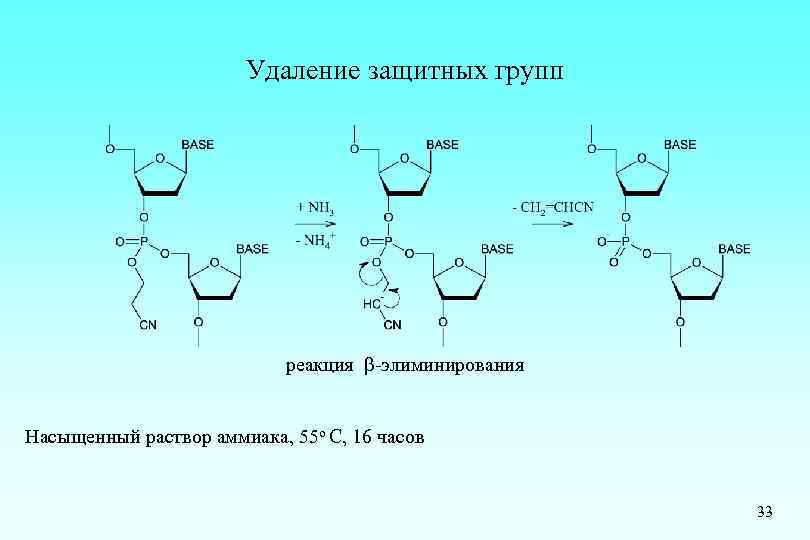
Удаление защитных групп реакция -элиминирования Насыщенный раствор аммиака, 55 о С, 16 часов 33
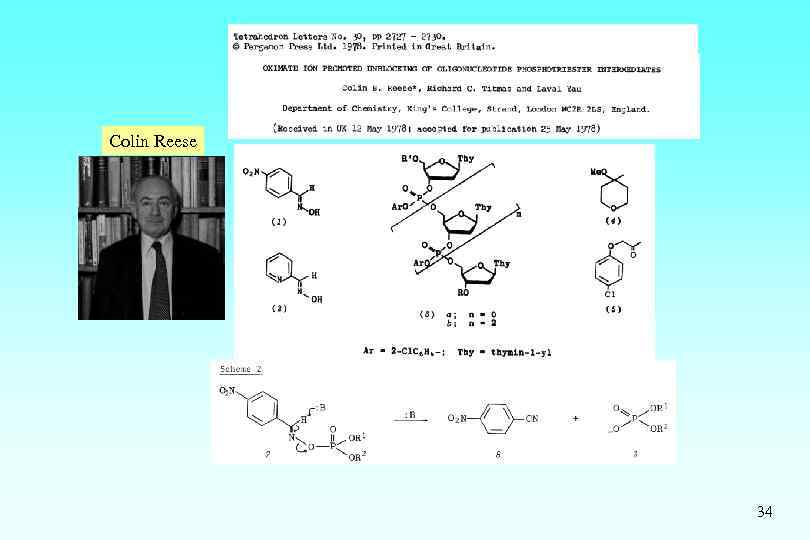
Colin Reese 34
EARLY GENE SYNTHESIS 1979 -1981 Expression in E. coli of chemically synthesised genes for human insulin. Goeddel et al (1979) Proc. Natl. Acad. Sci. USA, 76, 106. 110 Synthesis of the human insulin gene. Part III. HM Hsiung, WL Sung, R Brousseau, R Wu, and SA Narang, (1980) Nucleic Acids Res. , 8, 5753 - 5765. Total synthesis of a human leukocyte interferon gene. Edge et al. (1981) Nature, 292, 756 -761 35

За разработку методов синтеза фрагментов ДНК Нобелевская премия не была присуждена В 1968 г. Хару Гобинду Корана, Роберту Холли и Маршаллу Ниренбергу была присуждена Нобелевская премия по физиологии и медицине «за расшифровку генетического кода и его роли в синтезе белков» . В поздравительной речи исследователь из Каролинского института Петер Рейхард сравнил нуклеиновые кислоты и белки с языком, а их составные элементы – с буквами алфавита. Он отметил: «Химическая структура нуклеиновых кислот определяет химическую структуру белка, а алфавит нуклеиновых кислот – алфавит белков. Генетический код – это словарь, благодаря которому возможен переход с одного алфавита на другой» . 36

Синтез олигодезоксирибонуклеотидов на полимерном носителе Требования к полимерному носителю: носитель должен быть химически инертным и не влиять на ход реакций, протекающих в процессе синтеза олигонуклеотида; носитель должен обладать минимальной адсорбционной способностью для быстрой и количественной отмывки полимера от избытка реагентов и растворителей; иметь достаточный размер пор для доставки реагентов к поверхности; быть механически стабильным и не набухать в растворителях, применяемых в олигонуклеотидном синтезе 37
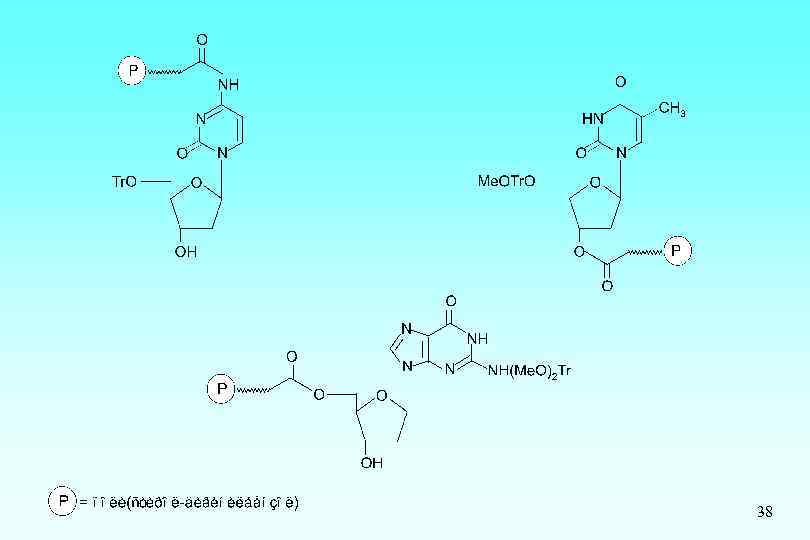
38
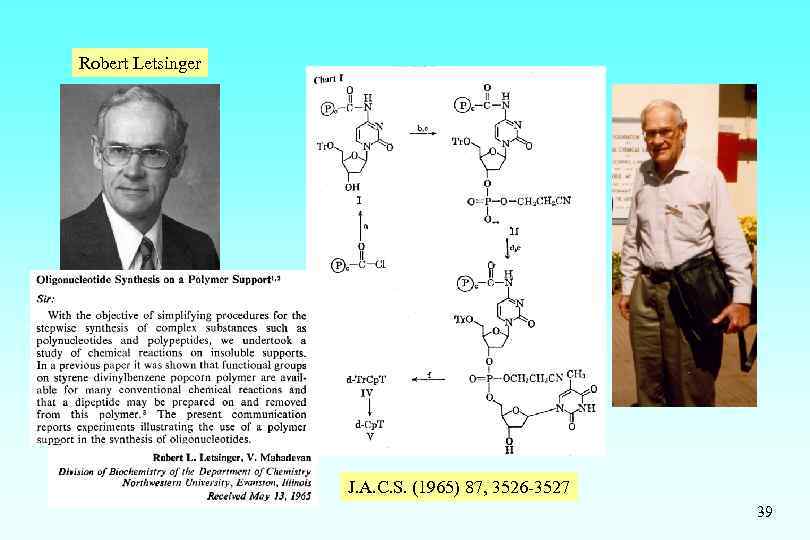
Robert Letsinger J. A. C. S. (1965) 87, 3526 -3527 39
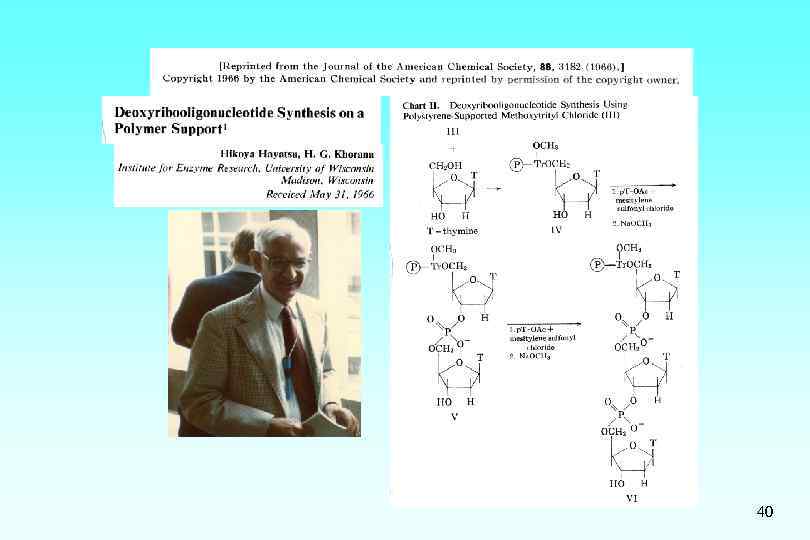
40

Fritz Cramer Hartmut Seliger Angew. Chemie Int. Ed. (1966) 5, 601 41

Kelvin Ogilvie: Mc. Gill, then President of Acadia 1981: First “gene machine” (Biologicals) Marvin Caruthers 42

Hubert Köster 43
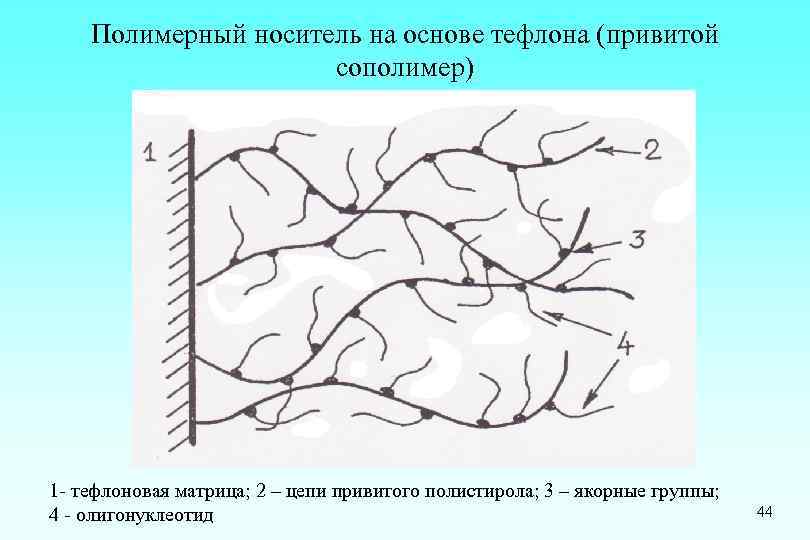
Полимерный носитель на основе тефлона (привитой сополимер) 1 - тефлоновая матрица; 2 – цепи привитого полистирола; 3 – якорные группы; 4 - олигонуклеотид 44
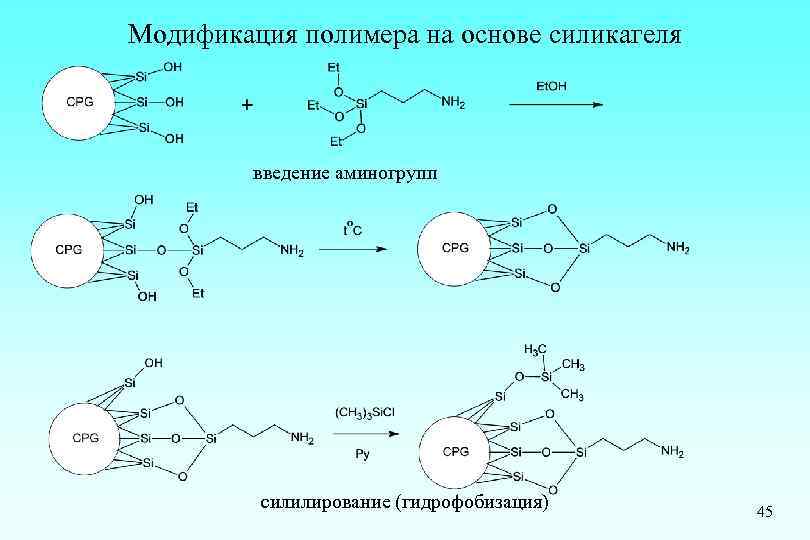
Модификация полимера на основе силикагеля введение аминогрупп силилирование (гидрофобизация) 45
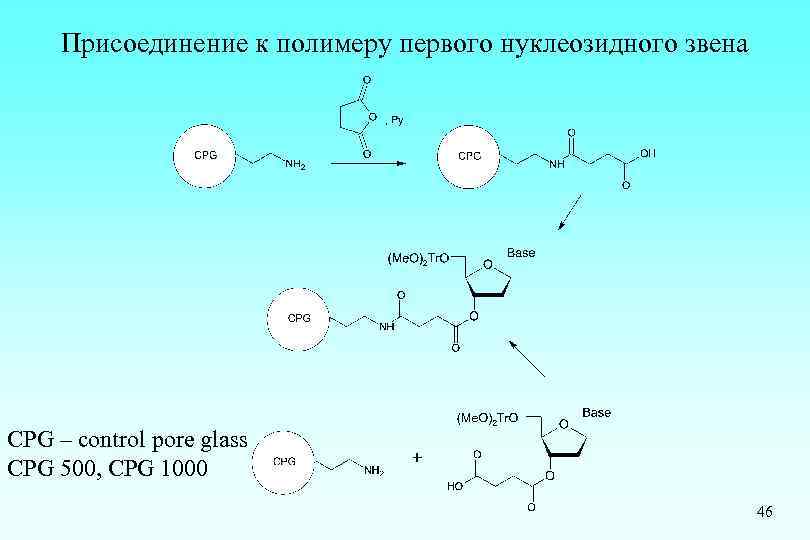
Присоединение к полимеру первого нуклеозидного звена CPG – control pore glass CPG 500, CPG 1000 46
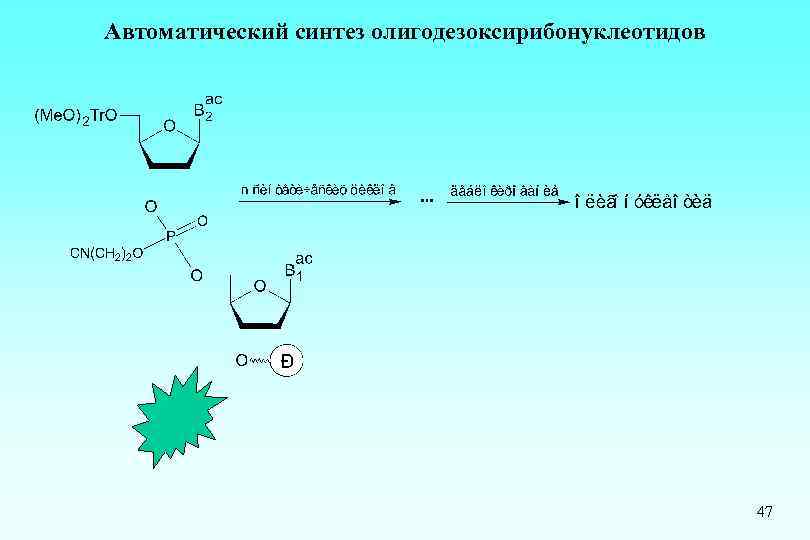
Автоматический синтез олигодезоксирибонуклеотидов 47
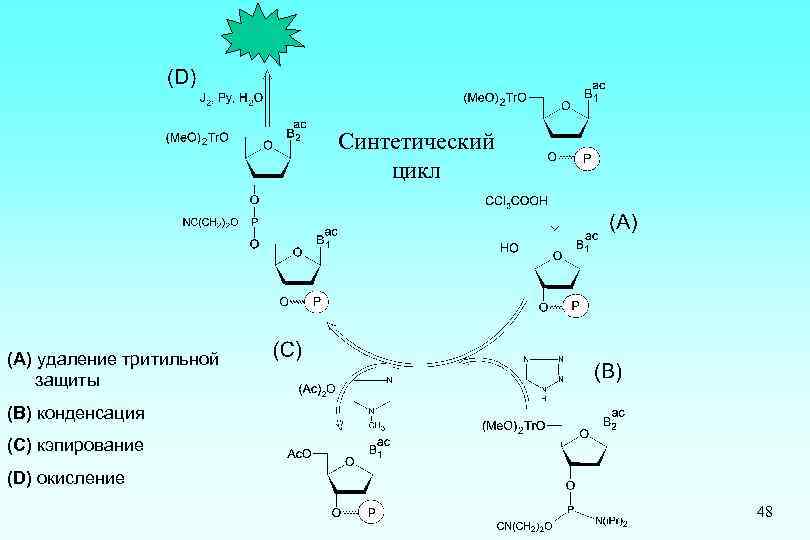
Синтетический цикл (А) удаление тритильной защиты (В) конденсация (С) кэпирование (D) окисление 48
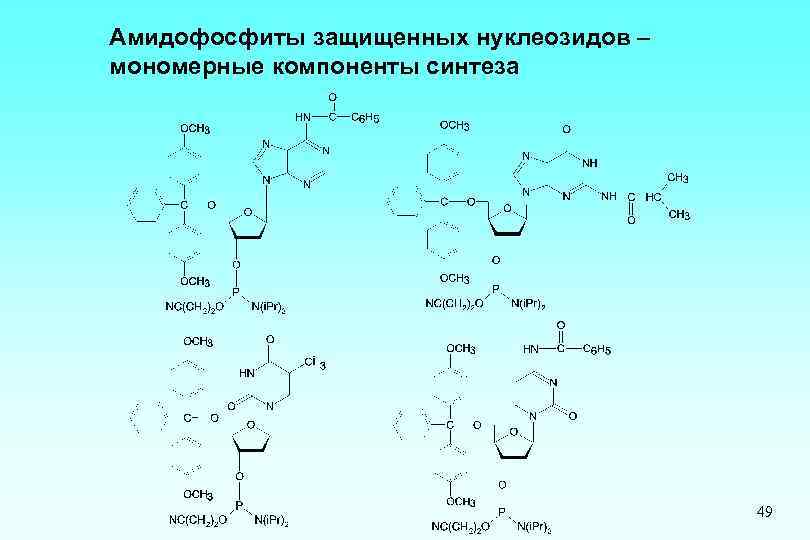
Амидофосфиты защищенных нуклеозидов – мономерные компоненты синтеза 49

РНК/ДНК-синтезатор Первый отечественный синтезатор «Виктория» был создан в 1980 году в СКТБ специальной электроники и аналитического приборостроения СО АН СССР (Новосибирск). Синтетический цикл для синтезатора «Виктория» был разработан З. А. Шабаровой, В. К. Потаповым (МГУ имени М. В. Ломоносова), Д. Г. Кнорре (ИБОХ СО АН СССР, Новосибирск) 50
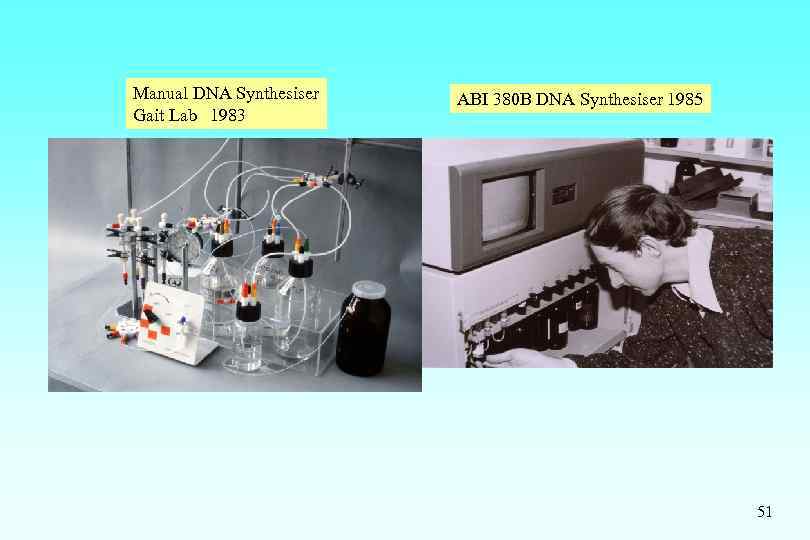
Manual DNA Synthesiser Gait Lab 1983 ABI 380 B DNA Synthesiser 1985 51

Синтезатор ДНК ASM-800 Эффективный синтез природных и модифицированных олигонуклеотидов • До 16 высококачественных олигонуклеотидов за 8 часов • Затраты на 1 шаг менее 0. 10 $ • Удобный и надежный инструмент по доступной цене • Прибор позволяет вести экономичный синтез природных и модифицированных ДНК, РНК. Восемь различных олигонуклеотидов могут быть одновременно синтезированы за 3. 5 часа. Синтезатор ДНК ASM-800 может быть успешно использован для синтеза олигонуклеотидов с длиной до 250 мономеров. Оригинальная конструкция синтезатора позволяет существенно снизить расход реактивов и растворителей. 52
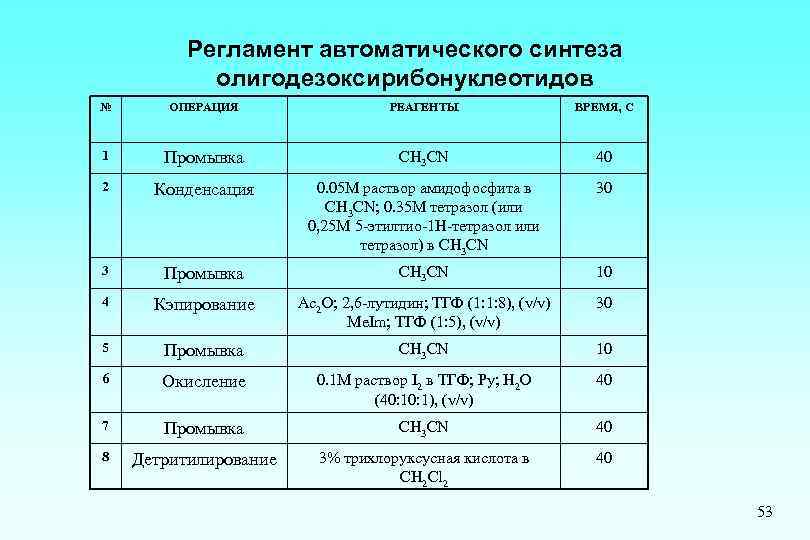
Регламент автоматического синтеза олигодезоксирибонуклеотидов № ОПЕРАЦИЯ РЕАГЕНТЫ ВРЕМЯ, С 1 Промывка СН 3 СN 40 2 Конденсация 0. 05 М раствор амидофосфита в СН 3 СN; 0. 35 М тетразол (или 0, 25 М 5 -этилтио-1 Н-тетразол или тетразол) в СН 3 СN 30 3 Промывка СН 3 СN 10 4 Кэпирование Ac 2 O; 2, 6 -лутидин; ТГФ (1: 1: 8), (v/v) Me. Im; ТГФ (1: 5), (v/v) 30 5 Промывка СН 3 СN 10 6 Окисление 0. 1 М раствор I 2 в ТГФ; Py; H 2 O (40: 1), (v/v) 40 7 Промывка СН 3 СN 40 8 Детритилирование 3% трихлоруксусная кислота в CH 2 Cl 2 40 53
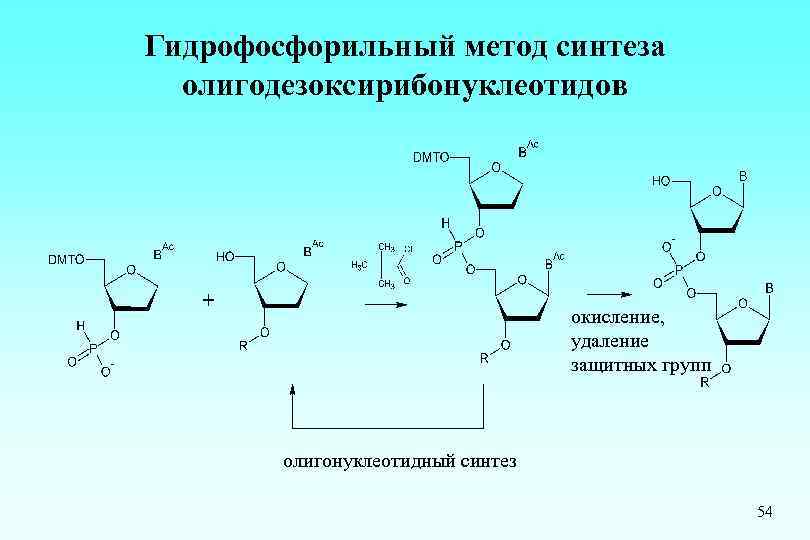
Гидрофосфорильный метод синтеза олигодезоксирибонуклеотидов окисление, удаление защитных групп олигонуклеотидный синтез 54
![Синтез олигонуклеотидов, модифицированных по фосфатной группе [a] - гидрофосфорильный синтез; [в] - окисление в Синтез олигонуклеотидов, модифицированных по фосфатной группе [a] - гидрофосфорильный синтез; [в] - окисление в](https://present5.com/presentation/51975572_63737064/image-55.jpg)
Синтез олигонуклеотидов, модифицированных по фосфатной группе [a] - гидрофосфорильный синтез; [в] - окисление в присутствии N-1 -трифрорацетилгександиамина; [с] - продолжение синтеза; [d] - удаление защитных групп 55
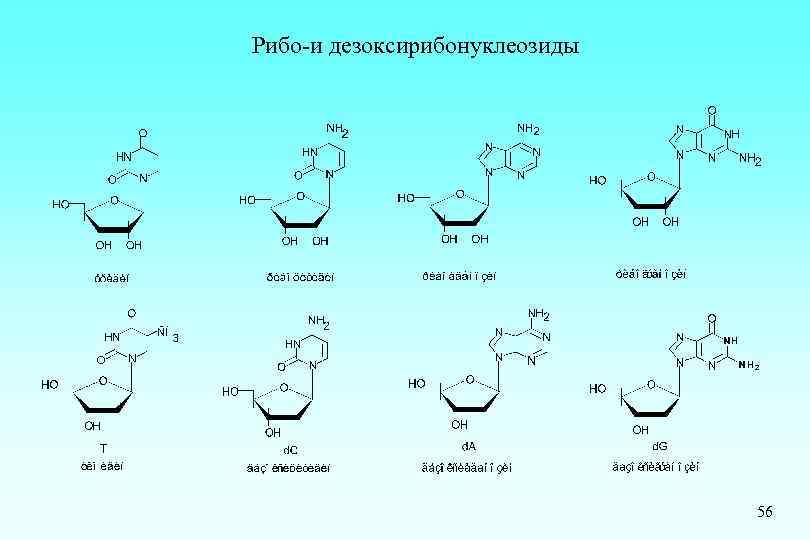
Рибо-и дезоксирибонуклеозиды 56

В отличие от дезоксирибонуклеотидов, молекулы рибонуклеотидов содержат дополнительную требующую защиты 2´-OH функцию, что значительно осложняет процесс получения их олигомеров и приводит к тому, что выбор 2´-O-защитной группы является одним из определяющих моментов синтеза олигорибонуклеотидов. К 2´-O-защитным группам предъявляются три основных требования : (1)они должны легко вводиться, причем введение должно осуществляться с использованием легкодоступных реагентов. (2) данные группы должны быть стабильными и сохраняться незатронутыми в процессе синтеза до стадии их удаления. (3) они должны относительно быстро удаляться в условиях, при которых целевой олигонуклеотид является полностью стабильным.
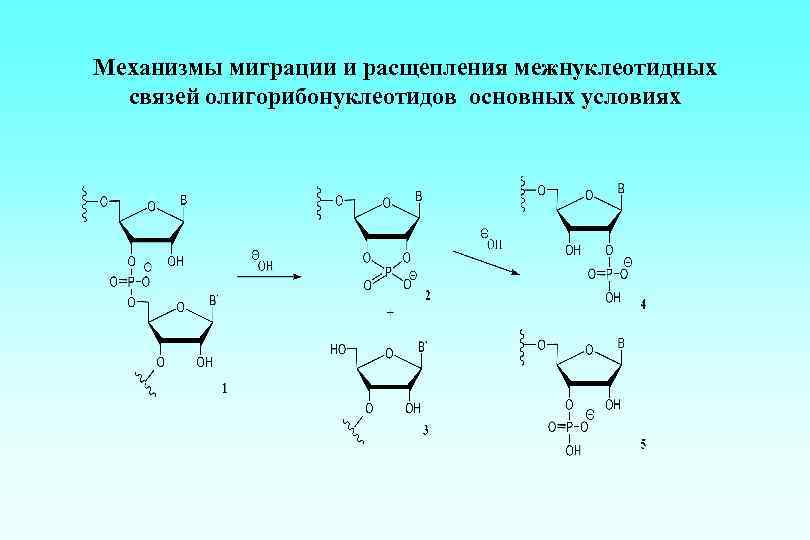
Механизмы миграции и расщепления межнуклеотидных связей олигорибонуклеотидов основных условиях

Защитные группы 2´-гидроксилов нуклеотидов • 2´-О-защитные группы с эфирным типом связи • 2´-O-ацетальные защитные группы • 2´-O-ацетильные защитные группы • 2´-O-защитные группы силильного типа

57
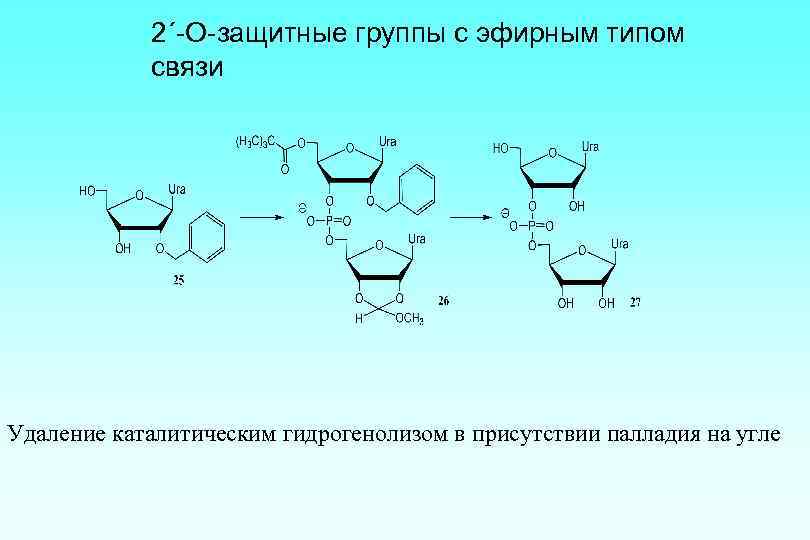
2´-О-защитные группы с эфирным типом связи Удаление каталитическим гидрогенолизом в присутствии палладия на угле
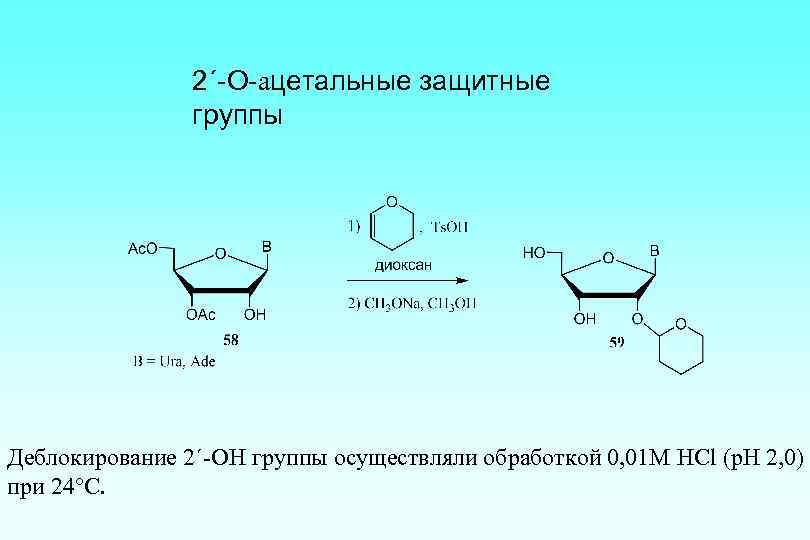
2´-O-ацетальные защитные группы Деблокирование 2´-OH группы осуществляли обработкой 0, 01 М HCl (p. H 2, 0) при 24°С.
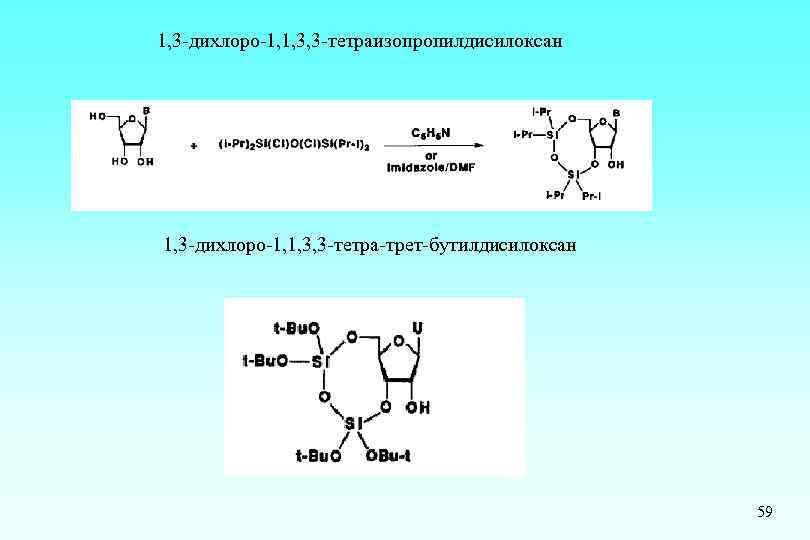
1, 3 -дихлоро-1, 1, 3, 3 -тетраизопропилдисилоксан 1, 3 -дихлоро-1, 1, 3, 3 -тетра-трет-бутилдисилоксан 59
![Мономерные синтоны, использующиеся в настоящее время для синтеза олигорибонуклеотидов 5'-диметокситритил-N-ацил-2'-O-триизопропилсилилоксиметил-3'-[(2 -цианэтил)-(N, Nдиизопропил)]-амидофосфит 5'-диметокситритил-N-ацил-2'-O-диметилизопропилсилил-3'-[(2 -цианэтил)-(N, Мономерные синтоны, использующиеся в настоящее время для синтеза олигорибонуклеотидов 5'-диметокситритил-N-ацил-2'-O-триизопропилсилилоксиметил-3'-[(2 -цианэтил)-(N, Nдиизопропил)]-амидофосфит 5'-диметокситритил-N-ацил-2'-O-диметилизопропилсилил-3'-[(2 -цианэтил)-(N,](https://present5.com/presentation/51975572_63737064/image-64.jpg)
Мономерные синтоны, использующиеся в настоящее время для синтеза олигорибонуклеотидов 5'-диметокситритил-N-ацил-2'-O-триизопропилсилилоксиметил-3'-[(2 -цианэтил)-(N, Nдиизопропил)]-амидофосфит 5'-диметокситритил-N-ацил-2'-O-диметилизопропилсилил-3'-[(2 -цианэтил)-(N, Nдиизопропил)]-амидофосфит 60

Изменение синтетической процедуры при синтезе РНК Применение более активного конденсирующего реагента (5 -этилтио-1 Н-тетразол); Увеличение времени конденсации (до 10 минут); Изменение деблокирующего реагента

Процедура деблокирования олигорибонуклеотидов, полученных с использованием 2'-О-TBDMS-защищенных групп 1. NH 4 OH (aq) : Et. OH (3 : 1), 55 o. C, 12 ч или безв. NH 3 в Et. OH, 55 о. С, 16 ч или (АМА-реагент) NH 4 OH (aq) : 40%-ный водный CH 3 NH 2 (1 : 1), 55 o. C, 10 мин 2. 1 М тетрабутиламмоний фторид в ТГФ, RT, 20 -24 ч Или Et 3 N • 3 HF, 40 о. C, 16 ч 3. Обессоливание 61
62
синтез НК лекция март 2012.ppt