лекция 4.pptx
- Количество слайдов: 29

Сильные и слабые электролиты. Электропроводимость растворов электролитов. Кондуктометрия Лекция № 4 Лектор: кандидат химических наук, доцент ИВАНОВА Надежда Семёновна

Введение Вещества, находящиеся в растворе или расплаве, условно делят на электролиты и неэлектролиты. Обоснованием для такого разделения служит: 1. электропроводимость растворов электролитов; 2. коллигативные свойства растворов неэлектролитов.

Теория электролитической диссоциации 1. В растворе Э распадаются на ионы, имеющие заряд; 2. Распадается на ионы только часть Э, которую характеризуют величиной степени диссоциации (α): АРРЕНИУС Сванте Август (1859 – 1927) 3. Раствор – механическая смесь ионов и молекул растворителя и его свойства определяются свойствами ионов.

Недостатки теории Аррениуса: v не объясняла резкое изменение свойств при переходе от атома к иону, что впоследствии объяснила электронная теория строения атома; v не показывала источник энергии, необходимый для диссоциации; v не объясняла отсутствие электростатического притяжения «+» и «–» ионов друг у другу. В объяснении 2 и 3 пунктов следовало учитывать взаимодействие ионов с молекулами растворителя.

Классификация электролитов по силе Сильные α > 70%; Средней силы 70% > α > 30%; Слабые α < 30%. Основополагающая концепция для слабых электролитов – взаимодействием между ионами в растворе можно пренебречь, так количество их а б в очень мало. а – разбавленный р-р сильного Э; б – конц. р-р сильного Э; в – р-р слабого Э.

Степень и const. диссоциации слабого электролита α – количественная характеристика способности слабого электролита диссоциировать. Главный недостаток – непостоянна, зависит от концентрации электролита. Пример: СН 3 СООН α = 1, 3% для С = 0, 1 моль/дм 3 α = 4, 2% для С = 0, 01 моль/дм 3 для характеристики слабого Э вводится Кдисс. , численное значение которой зависит только от температуры.
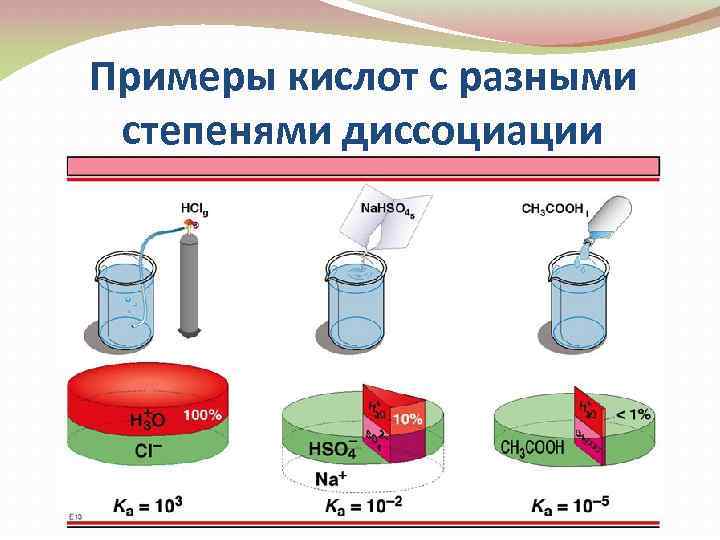
Примеры кислот с разными степенями диссоциации
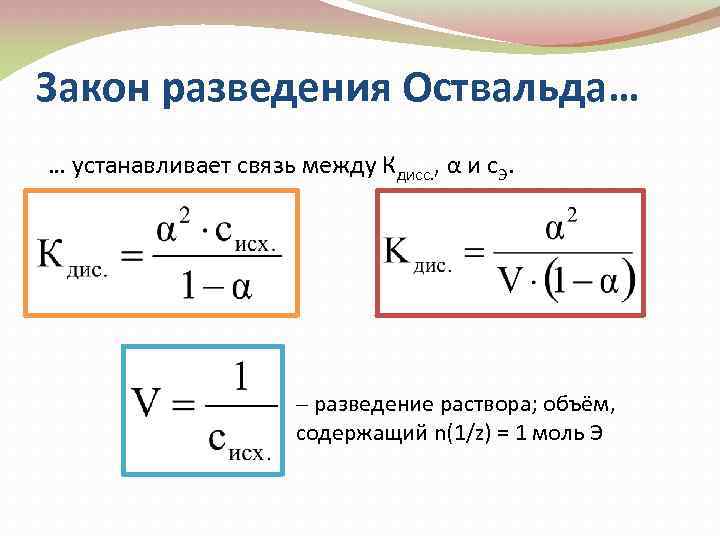
Закон разведения Оствальда… … устанавливает связь между Кдисс. , α и с. Э. ‒ разведение раствора; объём, содержащий n(1/z) = 1 моль Э

Основополагающая концепция для сильных электролитов ‒ высокая концентрация ионов в растворе и, как результат, электростатическое взаимодействие между ионами разного заряда. Теория сильных электролитов (1923 г. ) Дебая и Хюккеля имела целью отразить влияние этого взаимодействия на различные свойства растворов электролитов. 9

Эрих Арманд Артур Йозеф Хюккель (1896 — 1980) Дебай Петер Йозеф Вильгельм (1884 ‒ 1966) 10 10

Активность (а) – … Гилберт Ньютон Льюис (1875 -1946) … концентрационный параметр; определяется как величина, подстановка которой вместо концентрации в термодинамические уравнения делает их применимыми к растворам электролитов. 11

Активность а=γ·с а – активность вещества, моль/дм 3; γ – молярный коэффициент (безразмерная величина); с – молярная концентрация вещества, моль/дм 3. Для разбавленных растворов γ = 1, а = с. γ – мера отклонения свойств реального раствора электролита от идеального. – мера различия поведения электролита в данном растворе и его поведения в идеальном. 12

Ионная сила раствора (I) – … … величина, характеризующая силу электростатического взаимодействия ионов в растворе электролита. I = ½ (C 1 Z 12 + C 2 Z 22 + C 3 Z 32 + …) ионная сила равна полу-сумме произведения концентраций всех ионов на квадрат их заряда. γ – мало зависит от природы вещества, определяется лишь ионной силой раствора: один и тот же во всех разбавленных растворах с одинаковой ионной силой. 13

Правило ионной силы (закон постоянства I) Ø «Коэффициенты активности электролита, следовательно, и коэффициенты активности его ионов зависят от ионной силы, но не зависят от вида остальных ионов в данном растворе» ; Ø «γ электролита (или его ионов) одинаковы в растворах равной ионной силы независимо от того, какие ещё ионы есть в растворе» . Выполняется в растворах с I ≤ 0, 05. 14

Положения теории сильных электролитов 1. Вокруг каждого иона в растворе образуется ионная атмосфера за счёт электростатического притяжения ионов различного заряда. Ионная атмосфера содержит ионы разных знаков, но вокруг катиона больше анионов и наоборот; 2. Плотность ионной атмосферы max у + – центрального иона и уменьшается при удалении от него за счёт теплового движения ионов. На границе ионной атмосферы количество ионов каждого знака становится одинаковым. 15

Предельный закон Дебая – Хюккеля … … связывает размер и плотность ионной атмосферы с термодинамической характеристикой электролита ‒ коэффициентом активности (γ). γ± – средний коэффициент активности; А – предельный коэффициент; для 1, 1 – валентного электролита равен: А = 0, 508 (0, 509; 0, 511). Предельный закон в I-ом приближении – для 1, 1 валентного электролита. 16

Электропроводимость За счёт диссоциации на ионы растворы электролитов являются проводниками электрического тока. L – электропроводимость раствора; R – сопротивление раствора. - удельное сопротивление раствора. ℓ - расстояние между электродами; S – площадь электрода.
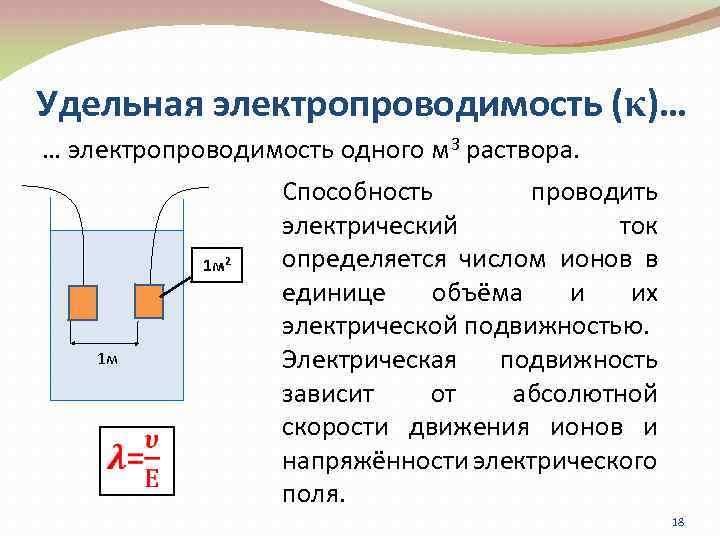
Удельная электропроводимость (κ)… … электропроводимость одного м 3 раствора. Способность проводить электрический ток определяется числом ионов в 1 м 2 единице объёма и их электрической подвижностью. 1 м Электрическая подвижность зависит от абсолютной скорости движения ионов и напряжённости электрического поля. 18

Связь между , сионов и электрической подвижностью определяется уравнением: = c·α (λ+ + λ–)· 103 α – степень диссоциации для слабого электролита; λ+ - электрическая подвижность катиона; λ- - электрическая подвижность аниона. Факторы, влияющие на • Природа электролита: обусловлена разной α электролита и разной подвижностью ионов; • Природа растворителя: влияет на подвижность ионов через вязкость и сольватирующую способность. 19

Температура: ↑t°С ↓ вязкость растворителя, что ведёт к ↑подвижности ионов и ↑. t = t ·[1+a(t 2 – t 1)] 2 1 а – температурный коэффициент электропроводимости: 0, 016 – для сильных кислот; 0, 019 – для щелочей; 0, 022 – для солей. С увеличением t° на каждый градус ↑ на 2 – 2, 5% из-за уменьшения вязкости раствора. 20
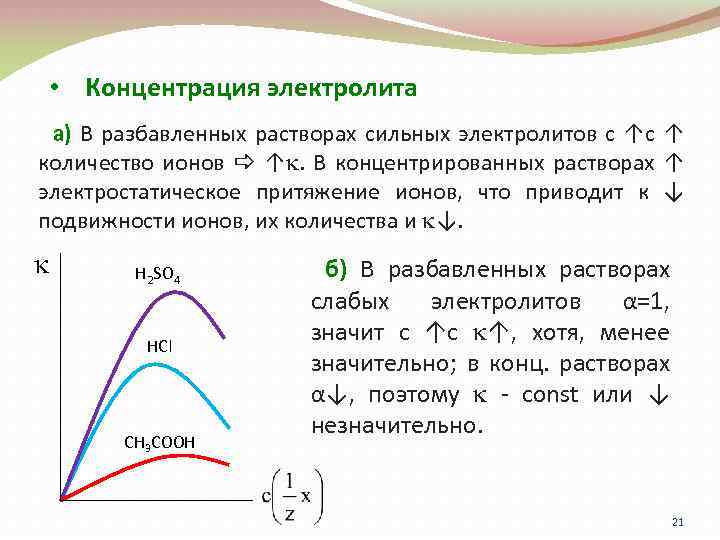
• Концентрация электролита а) В разбавленных растворах сильных электролитов с ↑с ↑ количество ионов ↑. В концентрированных растворах ↑ электростатическое притяжение ионов, что приводит к ↓ подвижности ионов, их количества и ↓. H 2 SO 4 HCl CH 3 COOH б) В разбавленных растворах слабых электролитов α=1, значит с ↑с ↑, хотя, менее значительно; в конц. растворах α↓, поэтому - const или ↓ незначительно. 21

Молярная электропроводимость (λ)… … электропроводимость объёма раствора, содержащего 1 моль электролита; … численно равна электропроводимости объёма раствора, заключённого между 2 -я // электродами с межэлектродным расстоянием 1 м и такой площади, чтобы в этом объёме содержался 1 моль растворённого вещества. Для слабых электролитов: λ = α (λ+ + λ–) (1) Для сильных электролитов: λ = (λ+ + λ–) (2) Молярная электропроводимость и подвижности ионов имеют одинаковую размерность (См·м 2/моль), поэтому обозначаются одной буквой. 22
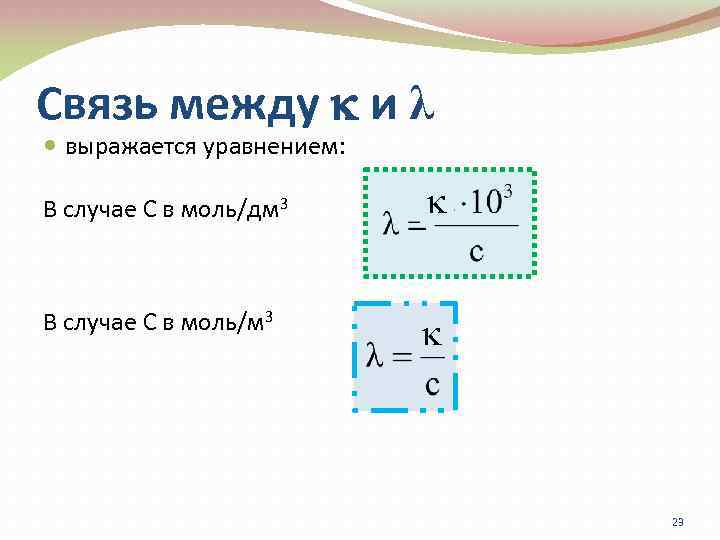
Связь между и λ выражается уравнением: В случае С в моль/дм 3 В случае С в моль/м 3 23
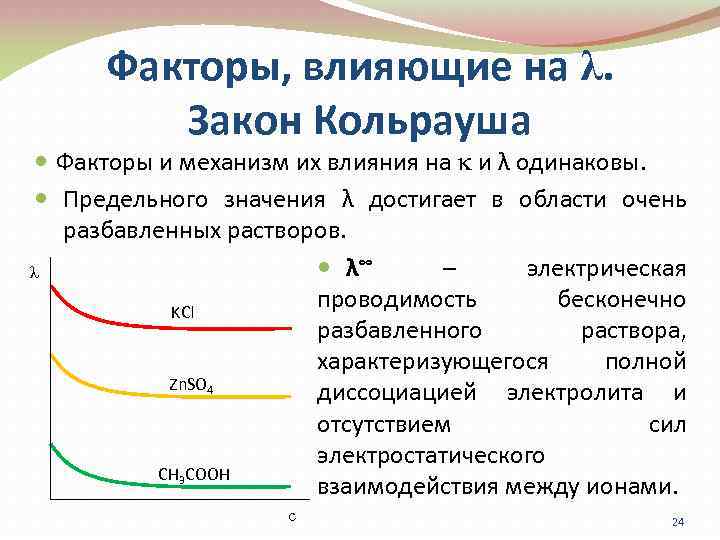
Факторы, влияющие на λ. Закон Кольрауша Факторы и механизм их влияния на и λ одинаковы. Предельного значения λ достигает в области очень разбавленных растворов. λ∞ – электрическая λ проводимость бесконечно KCl разбавленного раствора, характеризующегося полной Zn. SO 4 диссоциацией электролита и отсутствием сил электростатического CH 3 COOH взаимодействия между ионами. с 24

(3) λ+∞ и λ-∞ – предельная подвижность ионов Уравнение 3 применимо и для сильных и для слабых электролитов и называется законом независимого движения ионов (закон Ф. Кольрауша): в Кольрауша бесконечно разбавленном растворе ионы движутся независимо один от другого. Комбинируя 1 и 3 можно получить для слабого электролита: Тогда . Для очень разбавленных растворов = 1 λ – экспериментально определяемая L при данном разбавлении λ∞ – предельная L, определяемая из уравнения 3. 25

Прямая кондуктометрия… … метод определения ф-х величин (α и Кдис. ) на основе электропроводимости раствора электролита. = R – экспериментально найденное электрическое сопротивление. ; ; 26

Кондуктометрическое титрование … … метод определения концентрации электролита по кондуктометрическим кривым титрования, которые получают многократным измерением электропроводимости (L=1/R) после каждого прибавления небольшой порции титранта (0, 1 – 0, 2 см 3) к анализируемому раствору, находящемуся в кондуктометрической ячейке. 27
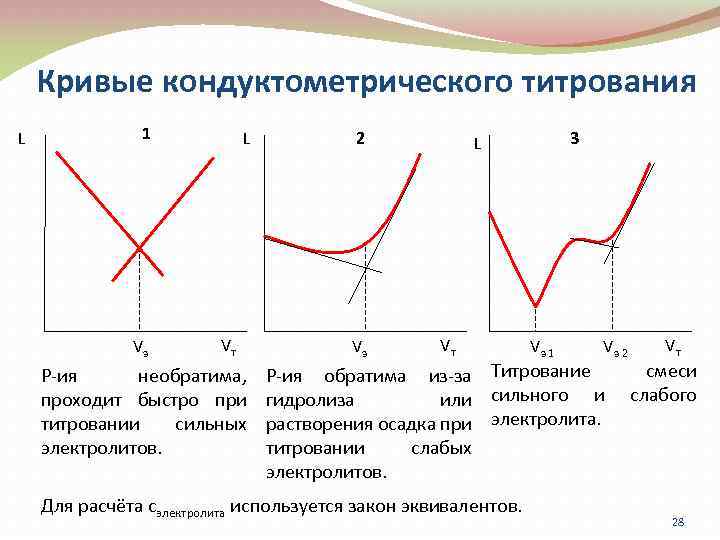
Кривые кондуктометрического титрования L 1 Vэ L Vт Р-ия необратима, проходит быстро при титровании сильных электролитов. 2 Vэ 3 L Vт Vэ 1 Vэ 2 Р-ия обратима из-за Титрование гидролиза или сильного и растворения осадка при электролита. титровании слабых электролитов. Для расчёта сэлектролита используется закон эквивалентов. Vт смеси слабого 28

Спасибо за внимание! 29
лекция 4.pptx