Презентация Lection 2.ppt
- Количество слайдов: 39
Сиб. ГТУ ЛЕКЦИЯ № 2 ОСНОВЫ ТЕОРИИ СПЛАВОВ (фазовое и структурное состояние сплавов) План лекции 1. Основные типы структур сплавов 2. Диаграммы фазового равновесия сплавов 3. Правило фаз (Гиббса) 4. Правило отрезков (рычага) 5. Понятие ликвации в сплавах Автор: к. п. н. , доц. Гиннэ С. В.

Сиб. ГТУ 1 Основные типы структур сплавов 1. 1 Физико-химическая (механическая) смесь Условное обозначение: А + В, где А и В – исходные компоненты Например: Перлит = Феррит + Цементит; П=(Ф+Ц) 1. 2 Твердый раствор Условное обозначение: А (В), Например: Аустенит = где А – растворитель, В – растворенный компонент Feγ(C) – твердый раствор углерода в Feγ 1. 3 Химическое соединение Условное обозначение: Am. Bn , где А и В – исходные компоненты, Например: Цементит m и n – число атомов исходных компонентов = Fe 3 C – карбид железа

Сиб. ГТУ 1. 2 Классификация твердых растворов 1. 2. 1 По степени растворимости компонентов друге Неограниченные твердые растворы Ограниченные твердые растворы 1. 2. 2 По расположению атомов растворенного компонента в кристаллической решетке растворителя Твердые растворы замещения Твердые растворы внедрения Твердые растворы вычитания

Сиб. ГТУ 2 Диаграммы фазового равновесия двух компонентных систем 2. 1 Понятие о диаграмме фазового равновесия (диаграмме состояния) 2. 1. 1 Диаграмма фазового равновесия (д. ф. р. ) – графическое изображение зависимости внутреннего строения (фазового состава) сплава от температуры и концентрации исходных компонентов (химического состава) сплава.

Сиб. ГТУ 2. 1 Понятие о диаграмме фазового равновесия Д. ф. р. системы Cu – Zn Д. ф. р. системы Al – Si Д. ф. р. системы Cu – Sn

Сиб. ГТУ 2. 1 Понятие о диаграмме фазового равновесия 2. 1. 2 Критические точки – ТЕМПЕРАТУРЫ начала или конца структурных превращений в сплаве: • температура начала кристаллизации; • температура конца кристаллизации; • температура начала плавления; • температура конца плавления;

Сиб. ГТУ 2. 1 Понятие о диаграмме фазового равновесия 2. 1. 3 Линии диаграмм фазового равновесия Линия ликвидус – (от лат. слова «ликва» , означающего «жидкий» ) линия началакристаллизации сплава Линия солидус – (от лат. слова «солид» , означающего «твердый» ) линия окончания кристаллизации сплава

Сиб. ГТУ 2. 1 Понятие о диаграмме фазового равновесия 2. 1. 4 Равновесное состояние – такое состояние сплава, при котором его внутреннее строение не может самопроизвольно (без воздействия внешних факторов) изменяться с течением времени.

Сиб. ГТУ 2 Диаграммы фазового равновесия двух компонентных систем 2. 2 Основные типы диаграмм фазового равновесия двойных систем 2. 2. 1 Диаграмма фазового равновесия систем, компоненты которых образуют эвтектику (физико-химические смеси) 2. 2. 2 Диаграмма фазового равновесия систем, компоненты которых образуют непрерывный ряд твердых и жидких растворов 2. 2. 3 Диаграмма фазового равновесия систем, компоненты которых ограниченно растворимы в твердом состоянии и образуют эвтектику 2. 2. 4 Диаграммы состояния систем, компоненты которых образуют химические соединения

Сиб. ГТУ 2. 2. 1 Д. ф. р. систем, компоненты которых образуют эвтектику (физико-химические смеси) Эвтектика (от греч. слова «eutektos» , в переводе обозначающего легкоплавкий) – мелкодисперсная (мелкозернистая) физико-химическая смесь кристаллов двух видов, одновременно образующихся из жидкой фазы сплава строго постоянного химического состава при постоянной температуре.

Сиб. ГТУ 2. 2. 1 Д. ф. р. систем, компоненты которых образуют эвтектику (физико-химические смеси) Отличительные особенности эвтектики v обладает самой низкой температурой плавления (кристаллизации) среди сплавов одной системы v имеет строго постоянный химический состав v образуется из жидкой фазы сплава v кристаллизуется (плавится) как чистый металл при постоянной температуре

Сиб. ГТУ 2. 2. 1 Д. ф. р. систем, компоненты которых образуют эвтектику (физико-химические смеси) Д. ф. р. эвтектического типа «Свинец – Сурьма» t, о. С В Жидкий сплав 327 С Э+ кр. Pb Эвт-ка Ж + кр. Sb D 246 0 10 13 20 30 100 90 87 80 70 доэвтектические 631 л. ACB – линия ликвидус; А Ж+ кр. Pb t, о. С л. DCE – линия солидус, E 246 Эвтектика + кр. Sb 40 60 50 50 60 70 80 90 100 Sb, % 40 30 20 10 0 Pb, % заэвтекти ческие эвтектический – линия эвтектических превращений
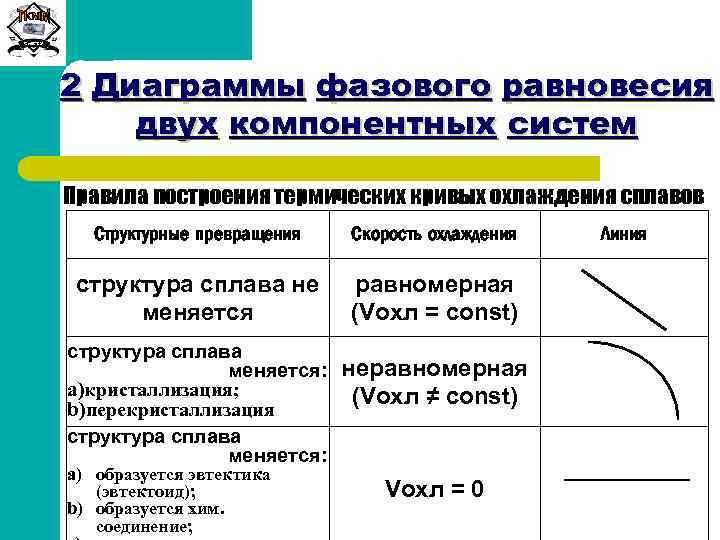
Сиб. ГТУ 2 Диаграммы фазового равновесия двух компонентных систем Правила построения термических кривых охлаждения сплавов Структурные превращения Скорость охлаждения структура сплава не меняется равномерная (Vохл = const) структура сплава меняется: a)кристаллизация; b)перекристаллизация структура сплава меняется: a) образуется эвтектика (эвтектоид); b) образуется хим. соединение; неравномерная (Vохл ≠ const) Vохл = 0 Линия

Сиб. ГТУ 2. 2. 1 Д. ф. р. систем, компоненты которых образуют эвтектику (физико-химические смеси) t, о. С В Жидкий сплав 631 1 Ж + кр. Sb / 22– 2// m Ж 40% Sb+кр. Sb n E 246 2// b р. S Эвтектика + кр. Sb 2/ +к 0 10 13 20 30 100 90 87 80 70 Ж 13% Sb+кр. Sb Sb Э+ кр. Pb Эвт-ка С Ж 62% Sb+кр. Sb Э 13% Ж+ кр. Pb Ж 70% Sb 1 m n 327 А D 246 t, о. С 40 60 50 50 60 70 80 90 100 Sb, % 40 30 20 10 0 Pb, % Д. ф. р. эвтектического типа «Свинец – Сурьма» τ, с Термическая кривая охлаждения сплава 30% Pb – 70% Sb

Сиб. ГТУ 2. 2. 1 Д. ф. р. систем, компоненты которых образуют эвтектику (физико-химические смеси) t, о. С В t, о. С 631 Жидкий сплав 327 А 1/ 1// τ, с Термическая кривая охлаждения сплава 13% Pb – 87% Sb D 246 Ж+ кр. Pb С Э+ кр. Pb Эвт-ка Ж + кр. Sb E 246 1/– 1// 0 10 13 20 30 100 90 87 80 70 Эвтектика + кр. Sb 40 60 50 50 60 70 80 40 30 20 90 100 Sb, % 10 0 Pb, % Д. ф. р. эвтектического типа «Свинец – Сурьма»
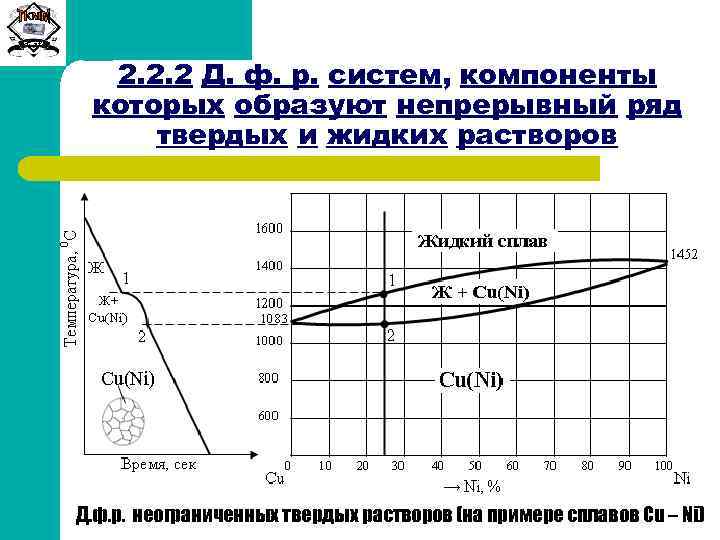
Сиб. ГТУ 2. 2. 2 Д. ф. р. систем, компоненты которых образуют непрерывный ряд твердых и жидких растворов Д. ф. р. неограниченных твердых растворов (на примере сплавов Cu – Ni)
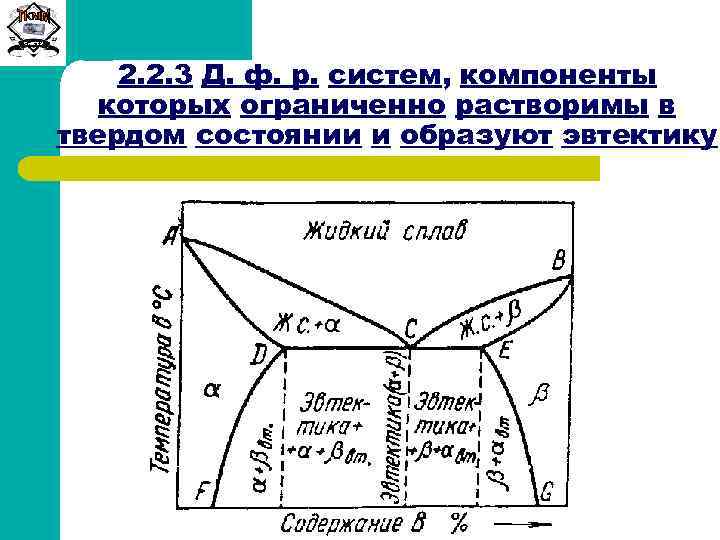
Сиб. ГТУ 2. 2. 3 Д. ф. р. систем, компоненты которых ограниченно растворимы в твердом состоянии и образуют эвтектику
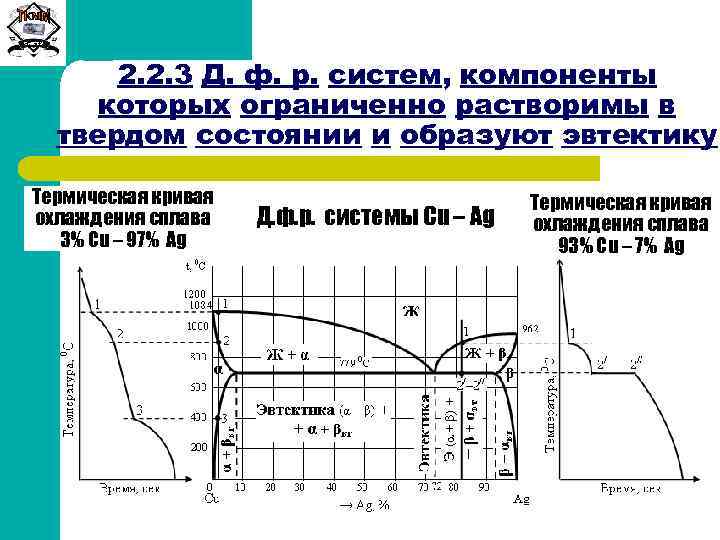
Сиб. ГТУ 2. 2. 3 Д. ф. р. систем, компоненты которых ограниченно растворимы в твердом состоянии и образуют эвтектику Термическая кривая охлаждения сплава 3% Cu – 97% Ag Д. ф. р. системы Cu – Ag Термическая кривая охлаждения сплава 93% Cu – 7% Ag
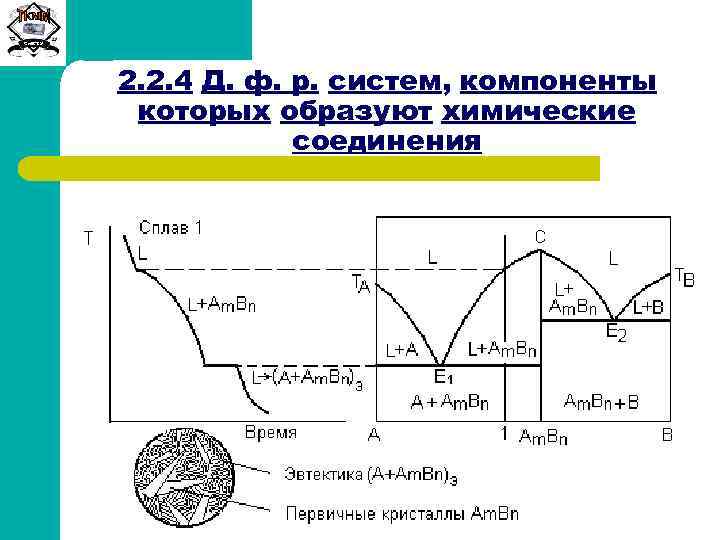
Сиб. ГТУ 2. 2. 4 Д. ф. р. систем, компоненты которых образуют химические соединения
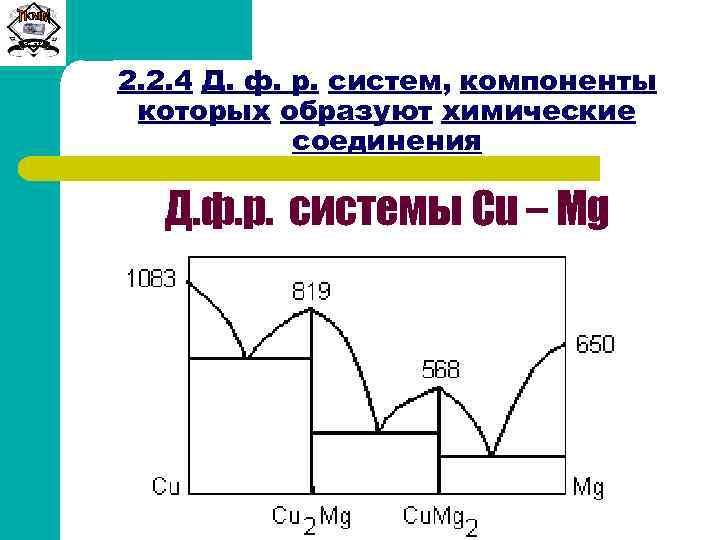
Сиб. ГТУ 2. 2. 4 Д. ф. р. систем, компоненты которых образуют химические соединения Д. ф. р. системы Cu – Mg

Сиб. ГТУ 3 Правило фаз Гиббса устанавливает зависимость между числом фаз системы, числом ее компонентов и числом степеней свободы системы.

Сиб. ГТУ 3 Правило фаз Гиббса Система – это совокупность фаз в твердом и жидком состоянии, которая взята для исследования в известных внешних факторах и занимает общий объем. Число степеней свободы (вариантность) системы – число независимых переменных (внутренних и внешних факторов: состав фаз, температура, давление), которые можно изменять без изменения числа фаз, находящихся в равновесии.

Сиб. ГТУ 3 Правило фаз Гиббса С = К + Р – Ф, где С – число степеней свободы (вариантность системы), К – число компонентов системы, Р – количество независимых переменных (число внешних факторов равновесия), Ф – число фаз в системе. Вариантность системы не может быть отрицательной.

Сиб. ГТУ 3 Правило фаз Гиббса Внешними факторами равновесия (внешними независимыми переменными) являются температура и давление. Действие каких-либо дополнительных параметров увеличивает значение Р каждый на единицу. Поскольку диаграммы фазового равновесия строят обычно при постоянном (атмосферном) давлении (Р = 1), то правило фаз выражается следующим уравнением: С=К+1 -Ф

Сиб. ГТУ 3 Правило фаз Гиббса Если С = 0, то система называется безвариантной: изменение температуры или концентрации фаз приведет к изменению числа фаз (какая-то фаза исчезнет или появится новая). Такое состояние называют нонвариантным.

Сиб. ГТУ 3 Правило фаз Гиббса Если С = 1, то система называется одновариантной: можно изменить температуру или концентрацию фаз (в определенных пределах) без изменения числа фаз в системе. Такое состояние называется моновариантным.

Сиб. ГТУ 3 Правило фаз Гиббса При С = 2 система является двухвариантной: можно одновременно менять и температуру и концентрацию фаз (в известных пределах) и это не вызовет изменения числа фаз. Такое состояние называется бивариантным.

Сиб. ГТУ 3 Правило фаз Гиббса Экспериментально (эмпирически) построенные диаграммы состояния проверяют по правилу фаз (Гиббса), дающему возможность теоретически обосновать закономерности существования фаз сплава в условиях равновесия. Данное правило дает возможность предсказать и проверить процессы, происходящие в сплавах при нагреве и охлаждении; показывает, происходит ли процесс кристаллизации при постоянной температуре или в интервале температур; указывает, какое число фаз может одновременно существовать в системе.

Сиб. ГТУ 4 Правило отрезков (правило рычага) Массовая доля твердой фазы определяется отношением длины плеча, примыкающего к составу жидкой фазы, к длине всего рычага, а массовая доля жидкой фазы – отношением длины рычага, примыкающего к составу твердой фазы, к длине всего рычага (коноды).

Сиб. ГТУ 4 Правило отрезков (правило рычага) Д. ф. р. неограниченных твердых растворов Qs/Ql = kl /ks Qs/Qs+l = kl /ks где Qs – массовая доля твердой фазы сплава, Ql – массовая доля жидкой фазы сплава, Qs+l – общая масса сплава.
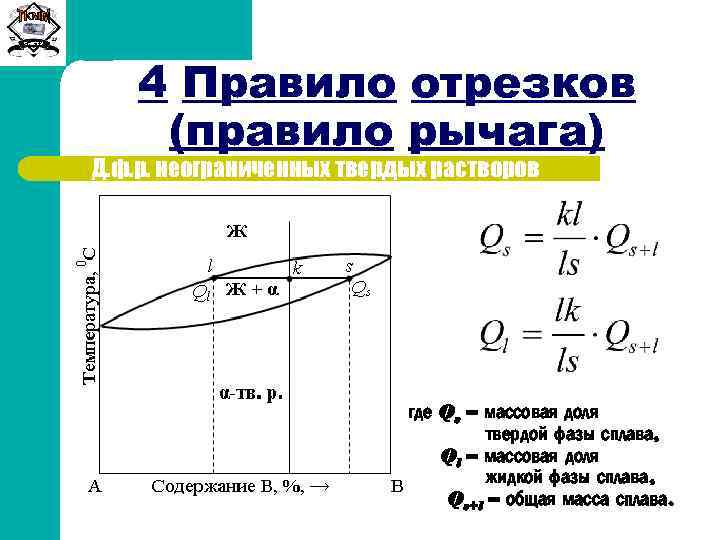
Сиб. ГТУ 4 Правило отрезков (правило рычага) Д. ф. р. неограниченных твердых растворов где Qs – массовая доля твердой фазы сплава, Ql – массовая доля жидкой фазы сплава, Qs+l – общая масса сплава.
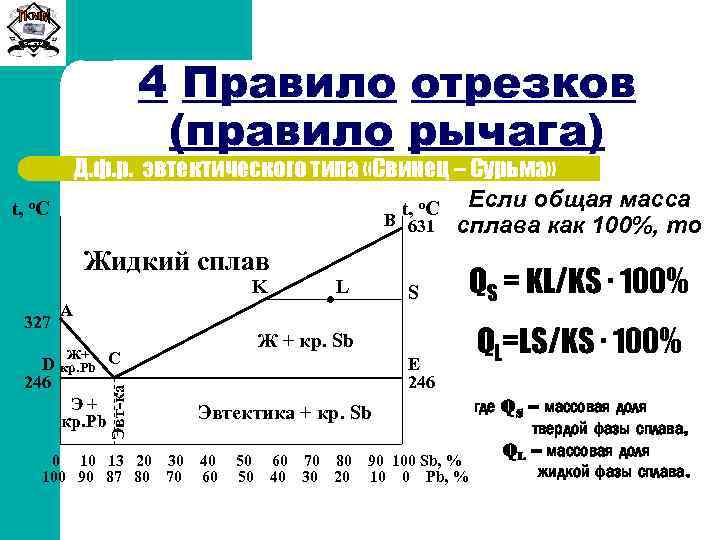
Сиб. ГТУ 4 Правило отрезков (правило рычага) Д. ф. р. эвтектического типа «Свинец – Сурьма» t, о. С Если общая масса В 631 сплава как 100%, то Жидкий сплав K А 0 10 13 20 30 100 90 87 80 70 S Ж + кр. Sb С Э+ кр. Pb D 246 Ж+ кр. Pb Эвт-ка 327 L E 246 QL=LS/KS ∙ 100% где QS – массовая доля твердой фазы сплава, QL – массовая доля 50 60 70 80 90 100 Sb, % жидкой фазы сплава. 50 40 30 20 10 0 Pb, % Эвтектика + кр. Sb 40 60 QS = KL/KS ∙ 100%

Сиб. ГТУ 5 Понятие ликвации в сплавах ЛИКВАЦИЯ – неоднородность химического состава и структуры сплава. В условиях реальных скоростей охлаждения при получении слитков (в земляной либо металлической форме, либо в кристаллизаторе) равновесные условия кристаллизации нарушаются, что приводит к получению химической неоднородности в конечной структуре литого сплава.

Сиб. ГТУ 5 Понятие ликвации в сплавах 5. 1 Ликвация по плотности – неоднородность химического состава и структуры сплава по объему слитка.

Сиб. ГТУ 5 Понятие ликвации в сплавах Ликвация по плотности возникает в том случае, когда процесс кристаллизации начинается с образования кристаллов, плотность которых значительно ниже плотности жидкого сплава. Ликвация по плотности – явление нежелательное. Ее можно уменьшить за счет увеличения скорости охлаждения и путем перемешивания сплава в процессе кристаллизации с помощью ультразвука.

Сиб. ГТУ 5 Понятие ликвации в сплавах Ликвация по плотности ярко выражена в заэвтектических сплавах Pb-Sb. Плотность сурьмы значительно ниже плотности свинца и, следовательно, жидкого сплава, в составе которого находится весь свинец. Поэтому при медленном охлаждении образующиеся кристаллы сурьмы всплывают вверх. В результате верхняя часть слитка состоит преимущественно из кристаллов сурьмы, а нижняя – эвтектики.

Сиб. ГТУ 5 Понятие ликвации в сплавах 5. 2 Дендритная (внутрикристаллитная) ликвация неоднородность химического состава сплава по сечению одного кристалла (дендрита).

Сиб. ГТУ 5 Понятие ликвации в сплавах При наличии постоянного теплоотвода от поверхности отливки в первую очередь кристаллизуются наиболее тугоплавкие и чистые по содержанию примесей участки жидкого сплава. Объемы жидкого сплава, легкоплавкие и наиболее загрязненные примесями, оттесняются в появившиеся впадинки на фронте кристаллизации и затвердевают в последнюю очередь. В результате этого слои кристалла, появившиеся в различные моменты кристаллизации, отличаются по химическому составу: центральная часть формируется наиболее тугоплавким и чистым металлом, а периферийные части наиболее сильно загрязнены примесями и богаче легкоплавкими металлами.

Сиб. ГТУ 5 Понятие ликвации в сплавах Например, в системе Cu – Ni образуются дендриты, у которых центральная часть богаче тугоплавким никелем, а периферийные части, наоборот, богаче медью.
Презентация Lection 2.ppt