Lektsiya_-Fermenti-Med-2012.ppt
- Количество слайдов: 45

Що таке біохімія? Раді надати відповідь! Огюст Роден “Мислитель” Кафедра біологічної та загальної хімії ВНМУ імені М. І. Пирогова http: //biochem. vsmu. edu. ua/

Ваша поведінка на лекції Вимкнути! Їжа – до лекції! За потребою – встати і тихо вийти! Бути вчасно! Допуск до модуля – рукопис лекцій!! 2
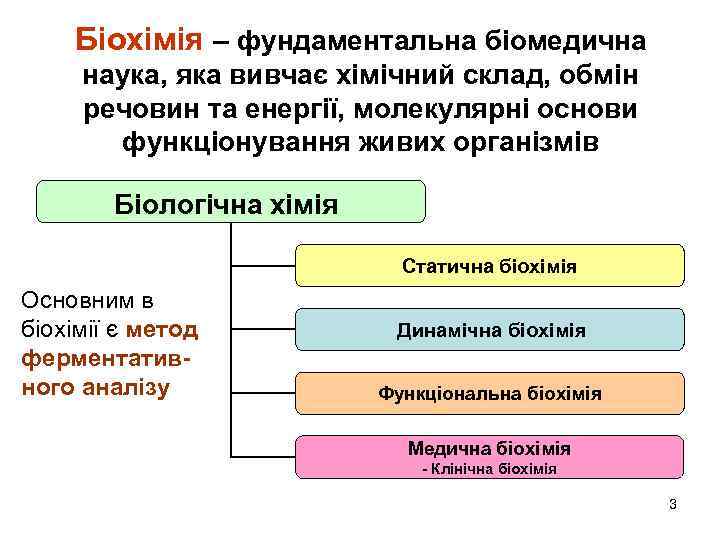
Біохімія – фундаментальна біомедична наука, яка вивчає хімічний склад, обмін речовин та енергії, молекулярні основи функціонування живих організмів Біологічна хімія Статична біохімія Основним в біохімії є метод ферментативного аналізу Динамічна біохімія Функціональна біохімія Медична біохімія - Клінічна біохімія 3

Медична біохімія - одна з провідних дисциплін медичного вузу, що формує світогляд майбутнього медика та його професійні знання ♥обмін речовин та його регуляція у здорової людини ♥зміни метаболізму в умовах патології ♥біохімічні методи діагностики захворювань та контролю за їх перебігом захворювань ♥створення нових лікарських засобів та методів лікування 2/8/2018 4
Лекція 1. Ферменти 1. 1. Номенклатура, класифікація, властивості ферментів 1. 2. Механізм дії ферментів, центри ферментів, 1. 3. Структура ферментів. 1. 4. Кінетика, енергетика ферм. реакції 1. 5. Активатори, інгібітори ферментів 1. 6. Ізоферменти, поліферментні системи 1. 7. Регуляція ферментативної активності 1. 8. Основи медичної ензимології Зав. каф. біологічної та загальної хімії, д. мед. н. Заічко Наталія Валентинівна 5

Ферменти (ензими) – це біокаталізатори переважно білкової природи та каталітичні молекули РНК (рибозими), які беруть участь в хімічних реакціях в організмі. • лат. «fermentatio» - бродіння ; грец. «en zyme» - у дріжджах, у заквасці. Ензимологія (ферментологія) – наука про ферменти 6

Умовні позначення в ензимології Е – фермент, ензим (“еnzуме”) S – субстрат - речовина, на яку діє фермент Р – продукт реакції - речовина, яка утворюється в результаті ферм. реакції 7
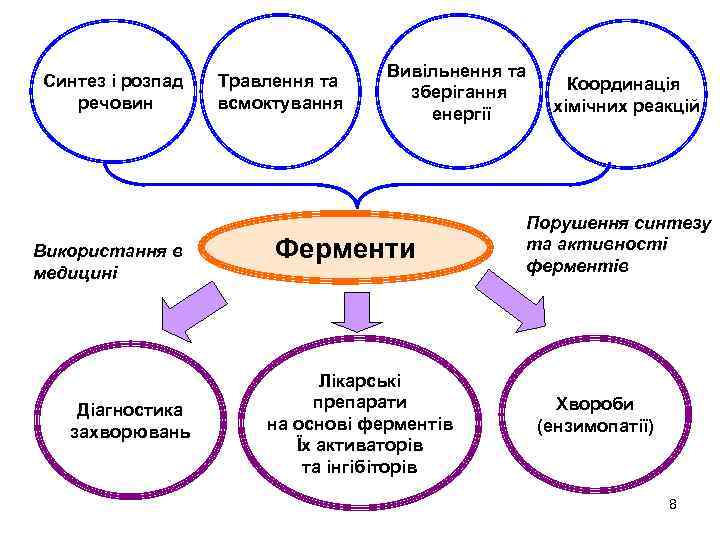
Синтез і розпад речовин Використання в медицині Діагностика захворювань Травлення та всмоктування Вивільнення та зберігання енергії Ферменти Лікарські препарати на основі ферментів Їх активаторів та інгібіторів Координація хімічних реакцій Порушення синтезу та активності ферментів Хвороби (ензимопатії) 8

Історія ензимології 17 ст. , Ван Гельмонт - термін «фермент» 1814 р. , Кірхгоф - солод ячменю викликає бродіння крохмалю. 1894 р. , Фішер - гіпотеза «ключа та замка» (специфічність дії ферментів) 1913 р. Ментен та Міхаеліс - теорія механізму дії ферментів та кінетика ферментативних реакцій 1926 р. Самнер - отримав фермент уреазу в кристалічній формі (рік народження ферментології як науки) 1969 р. Меррифільд - синтезував рибонуклеазу 80 -ті роки 20 ст. Томас Чек - відкрив каталітичні властивості у молекул РНК (рибозими). 9

Номенклатура ферментів 1. Робоча номенклатура (зручна для використання) Робоча назва ферменту = Ш хім. назва субстрату + «-аза» мальтоза + «-аза» = мальтаза Ш хім. назва субстрату + тип хім. реакції + «-аза» лактат + дегідрогенізація + «-аза» = лактатдегідрогеназа (ЛДГ) Ш історично усталена (тривіальна) назва пепсин, тромбін, трипсин, ренін 10

2. Систематична номенклатура (1961 р. Міжнародний союз біохімії та молекулярної біології) базується на класифікації ферментів (КФ), побудованої за типом хімічної реакції !!! Систематична назва ферменту = Сустрат 1 : Субстрат 2 (ко-субстрат) тип хім. реакції за КФ + «-аза» L-Лактат: НАД+ - оксидоредуктаза (систематична назва ЛДГ) 11
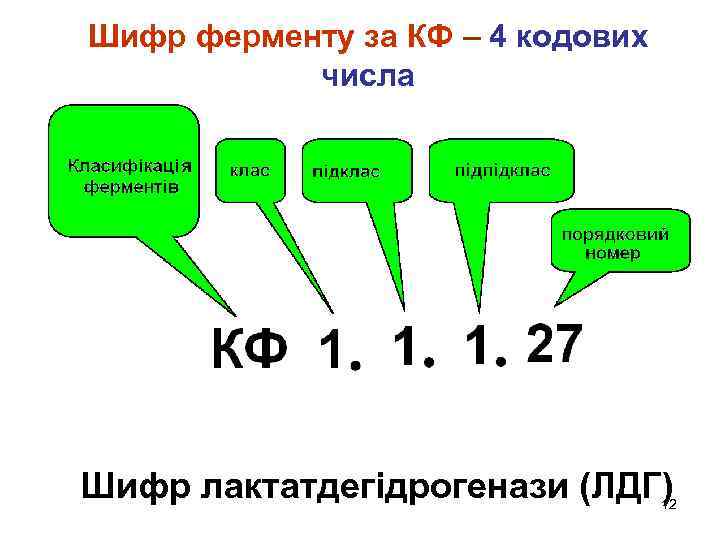
Шифр ферменту за КФ – 4 кодових числа Шифр лактатдегідрогенази (ЛДГ) 12

Класификація ферментів – 6 класів (КФ) КФ 1. Оксидоредуктази КФ 2. Трансферази КФ 3. Гідролази КФ 4. Ліази КФ 5. Ізомерази КФ 6. Лігази (синтетази) 13

КФ 1. Оксидоредуктази: переніс Н+, е-, Н Ш Дегідрогенази, оксидази, оксигенази (гідроксилази), цитохроми КФ 2. Трансферази: переніс хімічних груп Ш метил-, сульфо-, аміно-, фосфо-, ацил-, глікозил- трансферази Ш кінази (переніс фосфатного залишку з АТФ на субстрат) КФ 3. Гідролази: р-ції гідролізу - розщеплення субстрату за участі Н 2 О Ш пептидази, естерази, глікозидази, фосфатази 14

КФ 4. Ліази: розщеплення зв’язків між атомами C, O, N, S без участі Н 2 О Ш декарбоксилази, альдолази, дегідратази КФ 5. Ізомерази: реакції ізомерізації мутази, цис-транс-ізомерази, рацемази, епімерази КФ 6. Лігази (синтетази): з’єднання двох молекул з утворенням ковалентних зв’язків з використанням енергії АТФ або інших макроергів Ш синтетази (джерело енергії – АТФ) Ш синтази (джерело енергії інший макроерг) 15
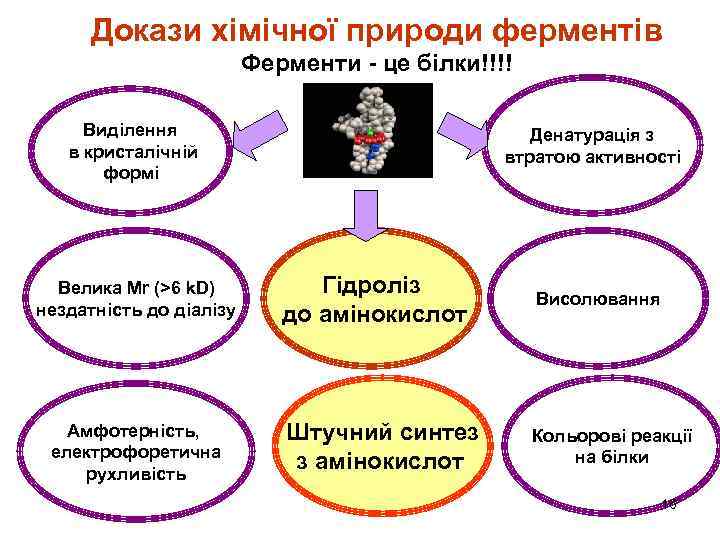
Докази хімічної природи ферментів Ферменти - це білки!!!! Виділення в кристалічній формі Велика Мr (>6 k. D) нездатність до діалізу Амфотерність, електрофоретична рухливість Денатурація з втратою активності Гідроліз до амінокислот Висолювання Штучний синтез з амінокислот Кольорові реакції на білки 16
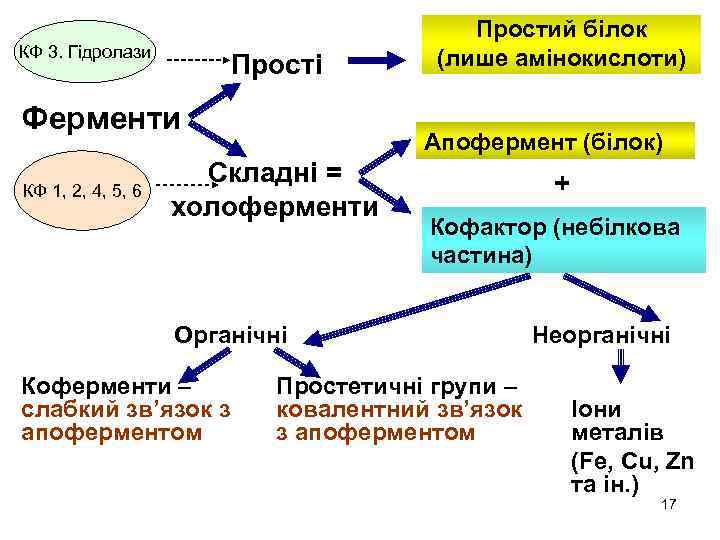
КФ 3. Гідролази Прості Ферменти КФ 1, 2, 4, 5, 6 Простий білок (лише амінокислоти) Апофермент (білок) Складні = холоферменти + Кофактор (небілкова частина) Органічні Коферменти – слабкий зв’язок з апоферментом Простетичні групи – ковалентний зв’язок з апоферментом Неорганічні Іони металів (Fe, Cu, Zn та ін. ) 17

Активний центр – ділянка молекули Е, у якій відбувається зв’язування і перетворення S. ь знаходиться в «просторовій ніші» ь містить 7 -15 амінокислот ь відповідає просторовій будові субстрату ь активних центрів може бути 2, 4, 6, 8 Активний центр хімотрипсину 18

19
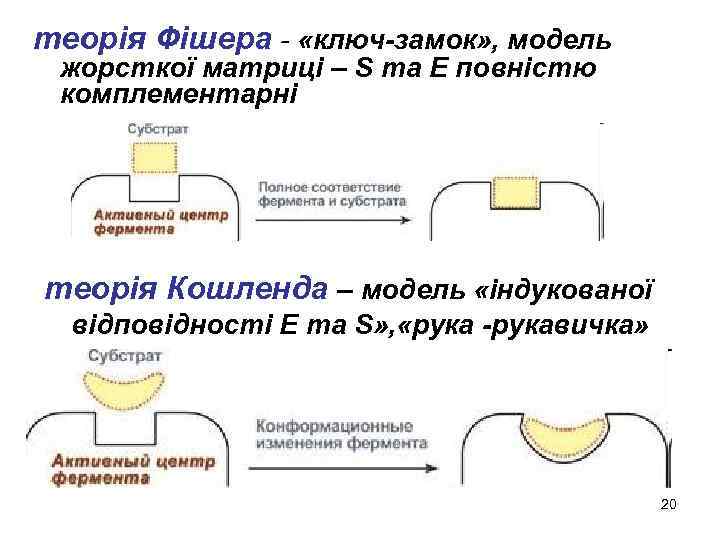
теорія Фішера - «ключ-замок» , модель жорсткої матриці – S та E повністю комплементарні теорія Кошленда – модель «індукованої відповідності E та S» , «рука -рукавичка» 20

Структура активного центру: • контактна (якірна) ділянка - зв’язує S • каталітична ділянка - перетворює S В акт. центр входять групи: - ОН (сер, тре, тир) - SН (цис) - NН (гіс) - СООН (глу, асп) - NН 2 (арг, ліз) У складних ферментів в каталітичній ділянці – ще й кофактори !!! 21
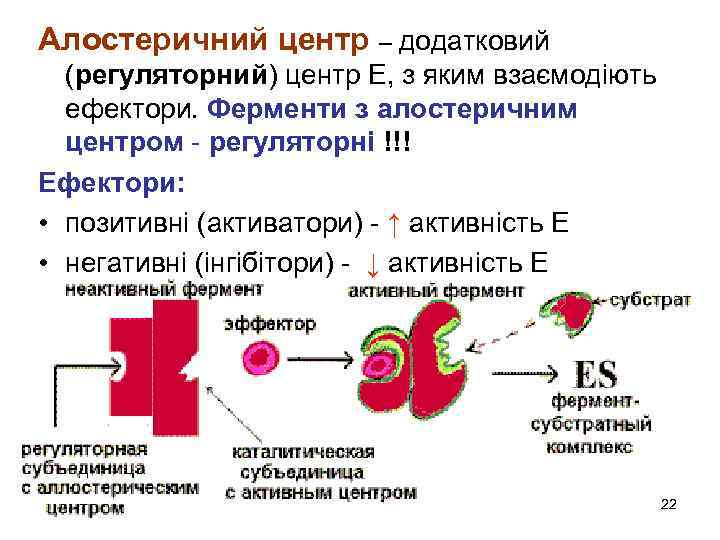
Алостеричний центр – додатковий (регуляторний) центр Е, з яким взаємодіють ефектори. Ферменти з алостеричним центром - регуляторні !!! Ефектори: • позитивні (активатори) - ↑ активність Е • негативні (інгібітори) - ↓ активність Е 22
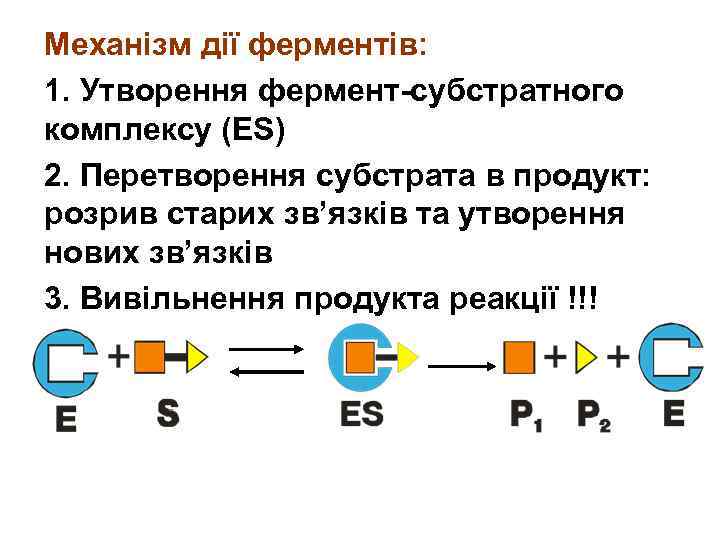
Механізм дії ферментів: 1. Утворення фермент-субстратного комплексу (ЕS) 2. Перетворення субстрата в продукт: розрив старих зв’язків та утворення нових зв’язків 3. Вивільнення продукта реакції !!!

Властивості ферментів як біокаталізаторів (!!!) 1. Специфічність - висока вибірковість дії а) абсолютна: один фермент – один субстрат (уреаза, аргіназа) б) стереоструктурна: дія на певний стереоізомер (ЛДГ -на L-лактат; оксидази D- та L-амінокислот) в) відносна: один фермент – один тип хімічного зв’язку (пептидази – пептидний зв’язок) 24
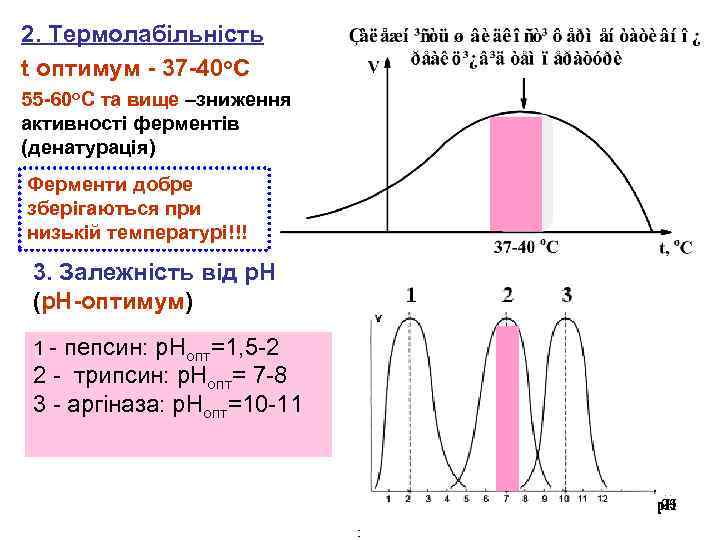
2. Термолабільність t оптимум - 37 -40 о. С 55 -60 о. С та вище –зниження активності ферментів (денатурація) Ферменти добре зберігаються при низькій температурі!!! 3. Залежність від р. Н (р. Н-оптимум) 1 - пепсин: р. Нопт=1, 5 -2 2 - трипсин: р. Нопт= 7 -8 3 - аргіназа: р. Нопт=10 -11 25

4) Прискорюють як пряму, так і зворотну реакцію 5) Регульованість дії 6) Висока ефективність, дія в дуже малих концентраціях 1 молекула карбангідрази розщеплює 36 млн молекул Н 2 СO 3 Як всі каталізатори ферменти: - каталізують лише термодинамічно можливі реакції - не змінюють напрямку реакцій 26 - не входять до складу продуктів реакції

Кінетика ферментативних реакцій (1913 р. – Міхаеліс та Ментен) Швидкість ферм. р-ції (V) визначається за зміною концентрації молекул реагуючих речовин за одиницю часу Залежить від: ь концентрації Е (ензиму) ь концентрації S (субстрату) ь t, р. Н та інших чинників 27
![Залежність швидкості ферментативної реакції від концентрації ферменту V = k∙[E] від концентрації субстрату V= Залежність швидкості ферментативної реакції від концентрації ферменту V = k∙[E] від концентрації субстрату V=](https://present5.com/presentation/-31213711_129715726/image-28.jpg)
Залежність швидкості ферментативної реакції від концентрації ферменту V = k∙[E] від концентрації субстрату V= Vmax___ 1+ Km / [S] Константа Міхаєліса (Km) – та концентрація S, при якій швидкість ферм. р-ції = ½ від максимальної.
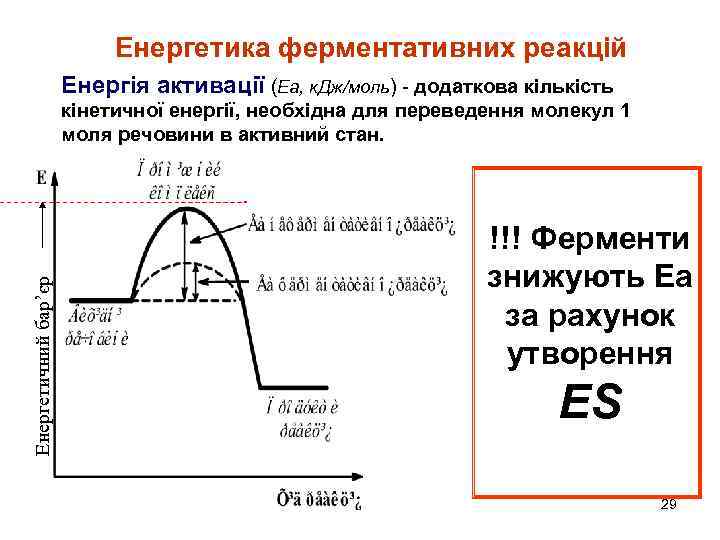
Енергетика ферментативних реакцій Енергія активації (Еа, к. Дж/моль) - додаткова кількість Енергетичний бар’єр кінетичної енергії, необхідна для переведення молекул 1 моля речовини в активний стан. !!! Ферменти знижують Еа за рахунок утворення ЕS 29

Активність ферменту – умовна величина, що відповідає швидкості біохімічної реакції, яку каталізує фермент Принципи визначення: Ш швидкістю зникнення S за Ш швидкістю накопичення Р за Одиниці активності ферментів: Міжнародна: Unit (Од. ). 1 U = 1 мкмоль/хв SI: Катал. 1 кат = 1 моль/с (1 кат = 6 ∙ 107 U) Питома активність: U / мг білка В медичній ензимології: U/л (мкмоль/хв·л) (Unit на 1 л плазми крові, сечі) 30

Активатори – збільшують активність Е органічні : жовчні кислоти, ентерокіназа, глутатіон, цистеїн, вітамін С та ін. неорганічні : HCl, іони металів (Na, K, Mg, Mn, Zn). Інгібітори – зменшують активність Е Види інгібування: Ш оборотне : Е+І ЕІ Ш необоротне : Е+І ЕІ Необоротне інгібування викликають денатуранти (висока to, конц. кислоти, луги, солі Hg, Pb, Cu), ФОС. За механізмом : Ш Конкурентне Ш Неконкурентне

Конкурентні інгібітори: ☻ структурно схожі на S ☻взаємодіють з контактною ділянкою активного центру ☻діють за високих концентрацій (І > S) ☻↑Km ☻інгібування завжди оборотне!!! Неконкурентні інгібітори: Mне схожі на S Mхімічно модифікують фермент в будь-якій ділянці Mдіють в малих концентраціях Mне змінюють Km Mінгібування частіше необоротне!!! Часто є клітинними отрутами !!!
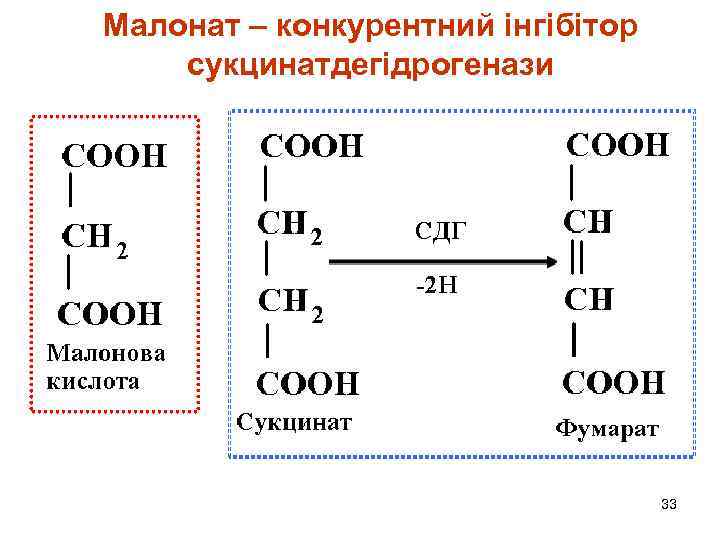
Малонат – конкурентний інгібітор сукцинатдегідрогенази 33

Конкурентні інгібітори в медицині: v сульфаніламіди - аналоги ПАБК (антимікробні) v метотрексат – аналог віт. В 9, блокує синтез ДНК (цитостатик) v дикумарини – аналоги віт. К, блокують синтез протромбіну (антизгортальні) v прозерин - аналог ацетилхоліну - інгібітор ацетилхолінестерази 34
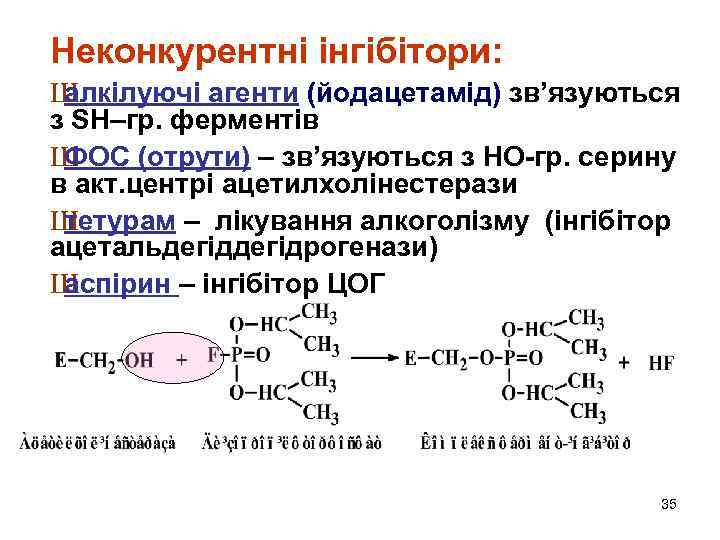
Неконкурентні інгібітори: Ш алкілуючі агенти (йодацетамід) зв’язуються з SН–гр. ферментів Ш ФОС (отрути) – зв’язуються з НО-гр. серину в акт. центрі ацетилхолінестерази Ш тетурам – лікування алкоголізму (інгібітор ацетальдегідрогенази) Ш аспірин – інгібітор ЦОГ 35
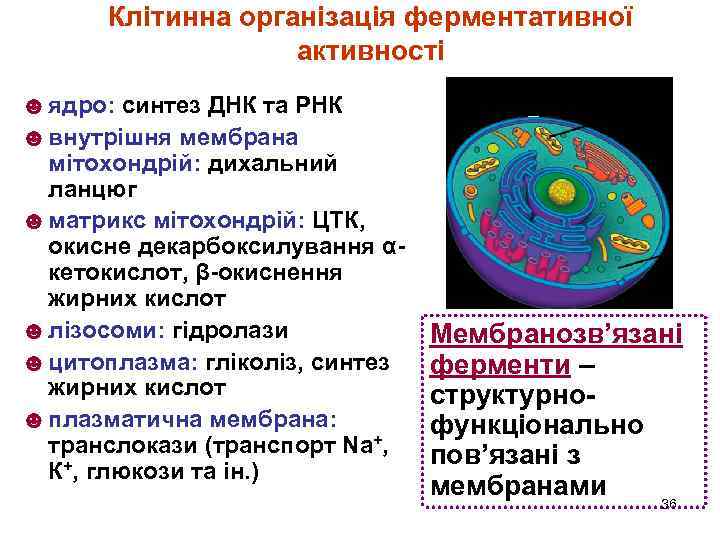
Клітинна організація ферментативної активності ☻ ядро: синтез ДНК та РНК ☻ внутрішня мембрана мітохондрій: дихальний ланцюг ☻ матрикс мітохондрій: ЦТК, окисне декарбоксилування αкетокислот, β-окиснення жирних кислот ☻ лізосоми: гідролази ☻ цитоплазма: гліколіз, синтез жирних кислот ☻ плазматична мембрана: транслокази (транспорт Nа+, К+, глюкози та ін. ) Мембранозв’язані ферменти – структурнофункціонально пов’язані з мембранами 36
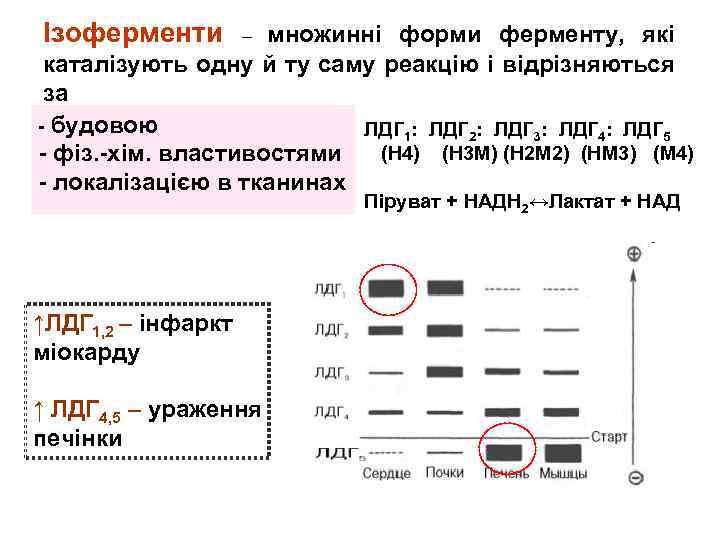
Ізоферменти множинні форми ферменту, які каталізують одну й ту саму реакцію і відрізняються за - будовою ЛДГ 1: ЛДГ 2: ЛДГ 3: ЛДГ 4: ЛДГ 5 (Н 4) (Н 3 М) (Н 2 М 2) (НМ 3) (М 4) - фіз. -хім. властивостями - локалізацією в тканинах – Піруват + НАДН 2↔Лактат + НАД ↑ЛДГ 1, 2 – інфаркт міокарду ↑ ЛДГ 4, 5 – ураження печінки
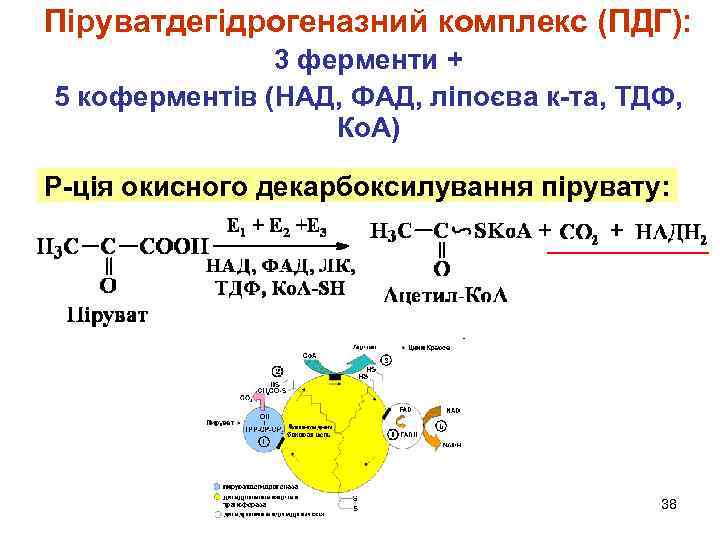
Піруватдегідрогеназний комплекс (ПДГ): 3 ферменти + 5 коферментів (НАД, ФАД, ліпоєва к-та, ТДФ, Ко. А) Р-ція окисного декарбоксилування пірувату: 38
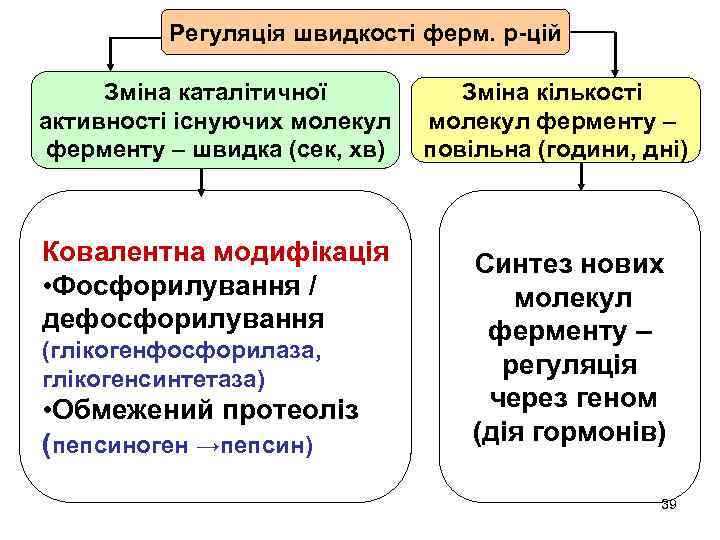
Регуляція швидкості ферм. р-цій Зміна каталітичної активності існуючих молекул ферменту – швидка (сек, хв) Ковалентна модифікація • Фосфорилування / дефосфорилування (глікогенфосфорилаза, глікогенсинтетаза) • Обмежений протеоліз (пепсиноген →пепсин) Зміна кількості молекул ферменту – повільна (години, дні) Синтез нових молекул ферменту – регуляція через геном (дія гормонів) 39

Медична ензимологія – розділ біохімії, що вивчає роль ферментів у - розвитку захворювань (ензимопатологія) - їх діагностиці (ензимодіагностика) - лікуванні (ензимотерапія) 40

Ензимопатологія (ензимопатії) – захворювання, зумовлені відсутністю ферментів або зниженням активності v Ензимопатії обміну фенілаланіну та тирозину: 1. Фенілпіровиноградна кетонурія та олігофренія 2. Альбінізм 41

Ензимодіагностика – використання ферментів для діагностики захворювань Ферменти – чутливі реагенти Глюкозооксидаза – для визначення глюкози в крові ІФА (імуноферментний аналіз) 42
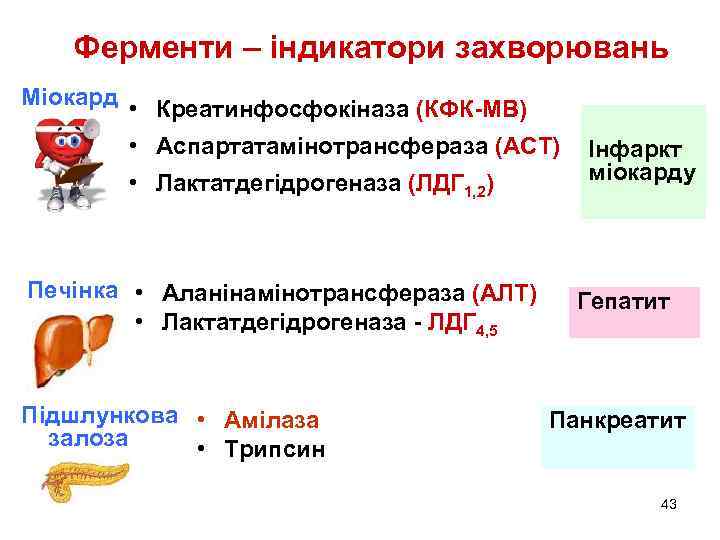
Ферменти – індикатори захворювань Міокард • Креатинфосфокіназа (КФК-МВ) • Аспартатамінотрансфераза (АСТ) • Лактатдегідрогеназа (ЛДГ 1, 2) Печінка • Аланінамінотрансфераза (АЛТ) • Лактатдегідрогеназа - ЛДГ 4, 5 Підшлункова • Амілаза залоза • Трипсин Інфаркт міокарду Гепатит Панкреатит 43

Ензимотерапія - використання ферментів, їх активаторів та інгібіторів для лікування захворювань рубці патологія ШКТ тромбози 44

Дякую за увагу! P. S. “Пам’ятай – наука безмежна, а життя коротке” Гіппократ 45
Lektsiya_-Fermenti-Med-2012.ppt