щелочные металлы.pptx
- Количество слайдов: 23
 Щелочные металлы Подготовила Васильева Алина АХ 12
Щелочные металлы Подготовила Васильева Алина АХ 12
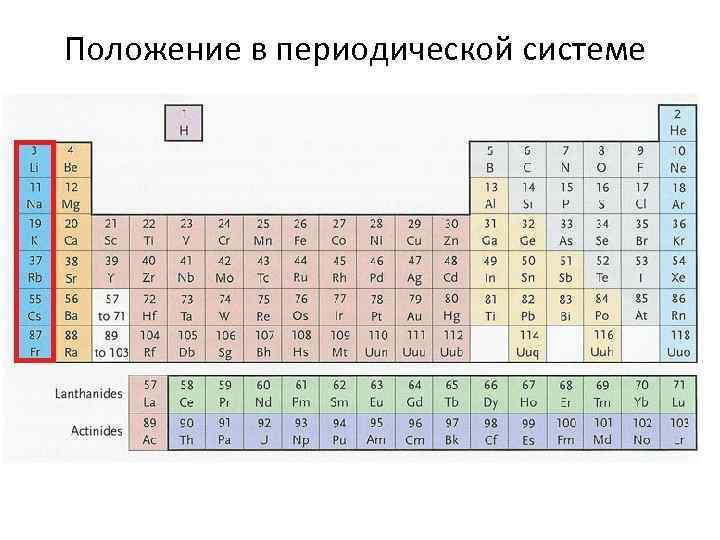 Положение в периодической системе
Положение в периодической системе
 Щелочные металлы Li (от греч. λίθος — камень) 1818 г. Г. Дэви Na (лат. Natrium «сода» ; лат. Sodium «головная боль» ) 1807 г. Г. Дэви K (от араб. аль кали — поташ). 1807 г. Г. Дэви Rb (от лат. Rubidium красный) 1863 г. Р. Бунзен Cs (от лат. Caesium — небесно голубой). 1860 г. Р. В. Бунзен и Г. Р. Кирхгоф Fr (от лат. Francium Франция) 1939 г. М. Пере Р. Бунзен Гемфри Дэви
Щелочные металлы Li (от греч. λίθος — камень) 1818 г. Г. Дэви Na (лат. Natrium «сода» ; лат. Sodium «головная боль» ) 1807 г. Г. Дэви K (от араб. аль кали — поташ). 1807 г. Г. Дэви Rb (от лат. Rubidium красный) 1863 г. Р. Бунзен Cs (от лат. Caesium — небесно голубой). 1860 г. Р. В. Бунзен и Г. Р. Кирхгоф Fr (от лат. Francium Франция) 1939 г. М. Пере Р. Бунзен Гемфри Дэви
 Нахождение в природе Содержание мас. % Li 1. 8 * 10 3 Na 2. 27 K 1. 84 Rb 7. 8 * 10 3 Cs 2. 6 * 10 4
Нахождение в природе Содержание мас. % Li 1. 8 * 10 3 Na 2. 27 K 1. 84 Rb 7. 8 * 10 3 Cs 2. 6 * 10 4
 Na 2 SO 4 • 10 H 2 O глауберова соль (мирабилит) Li 2 O • Al 2 O 3 • 4 Si. O 2 KCl • Na. Cl сильвинит сподумен KCl • Mg. Cl 2 • 6 H 2 O карналлит Na. NO 3 K 2 O • Al 2 O 3 • 6 Si. O 2 полевой Чилийская селитра шпат (ортоклаз)
Na 2 SO 4 • 10 H 2 O глауберова соль (мирабилит) Li 2 O • Al 2 O 3 • 4 Si. O 2 KCl • Na. Cl сильвинит сподумен KCl • Mg. Cl 2 • 6 H 2 O карналлит Na. NO 3 K 2 O • Al 2 O 3 • 6 Si. O 2 полевой Чилийская селитра шпат (ортоклаз)
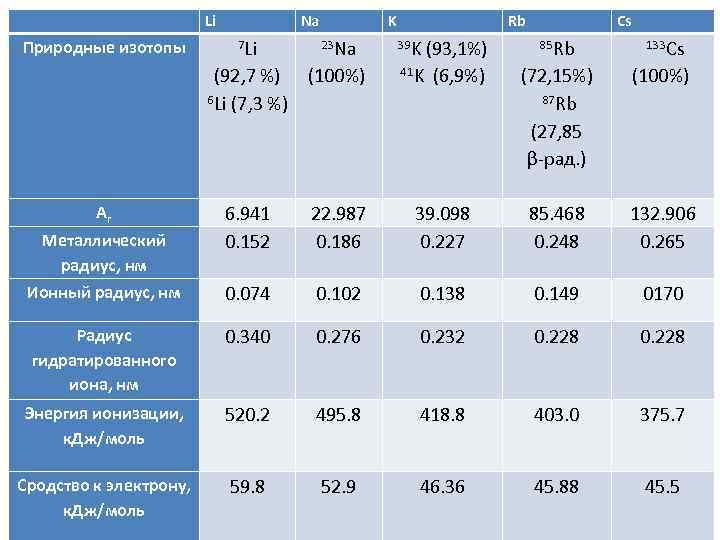 Природные изотопы Li Na 7 Li K 23 Na (92, 7 %) (100%) 6 Li (7, 3 %) Ar Rb Cs 39 K (93, 1%) 85 Rb 41 K (6, 9%) (72, 15%) 87 Rb (27, 85 β рад. ) 133 Cs (100%) 6. 941 0. 152 22. 987 0. 186 39. 098 0. 227 85. 468 0. 248 132. 906 0. 265 0. 074 0. 102 0. 138 0. 149 0170 Радиус гидратированного иона, нм 0. 340 0. 276 0. 232 0. 228 Энергия ионизации, к. Дж/моль 520. 2 495. 8 418. 8 403. 0 375. 7 Сродство к электрону, к. Дж/моль 59. 8 52. 9 46. 36 45. 88 45. 5 Металлический радиус, нм Ионный радиус, нм
Природные изотопы Li Na 7 Li K 23 Na (92, 7 %) (100%) 6 Li (7, 3 %) Ar Rb Cs 39 K (93, 1%) 85 Rb 41 K (6, 9%) (72, 15%) 87 Rb (27, 85 β рад. ) 133 Cs (100%) 6. 941 0. 152 22. 987 0. 186 39. 098 0. 227 85. 468 0. 248 132. 906 0. 265 0. 074 0. 102 0. 138 0. 149 0170 Радиус гидратированного иона, нм 0. 340 0. 276 0. 232 0. 228 Энергия ионизации, к. Дж/моль 520. 2 495. 8 418. 8 403. 0 375. 7 Сродство к электрону, к. Дж/моль 59. 8 52. 9 46. 36 45. 88 45. 5 Металлический радиус, нм Ионный радиус, нм
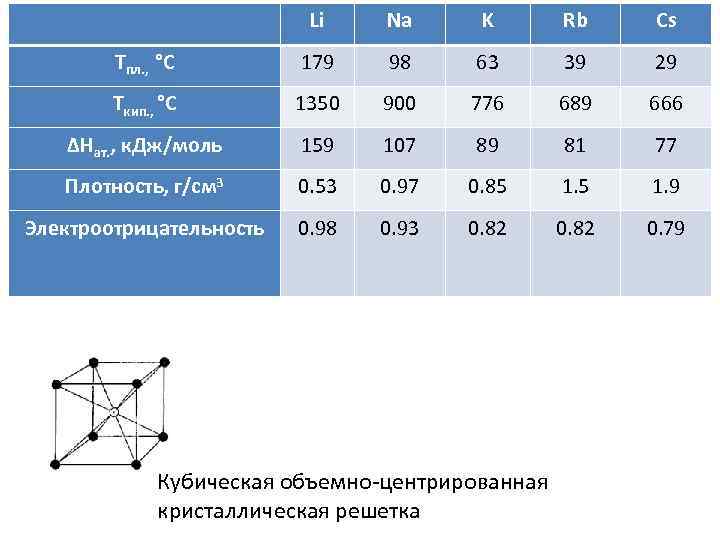 Li Na K Rb Cs Тпл. , °C 179 98 63 39 29 Ткип. , °C 1350 900 776 689 666 ΔHат. , к. Дж/моль 159 107 89 81 77 Плотность, г/см 3 0. 53 0. 97 0. 85 1. 9 Электроотрицательность 0. 98 0. 93 0. 82 0. 79 Кубическая объемно центрированная кристаллическая решетка
Li Na K Rb Cs Тпл. , °C 179 98 63 39 29 Ткип. , °C 1350 900 776 689 666 ΔHат. , к. Дж/моль 159 107 89 81 77 Плотность, г/см 3 0. 53 0. 97 0. 85 1. 9 Электроотрицательность 0. 98 0. 93 0. 82 0. 79 Кубическая объемно центрированная кристаллическая решетка
 Li Rb Na K Хранение в лаборатории Fr Cs
Li Rb Na K Хранение в лаборатории Fr Cs
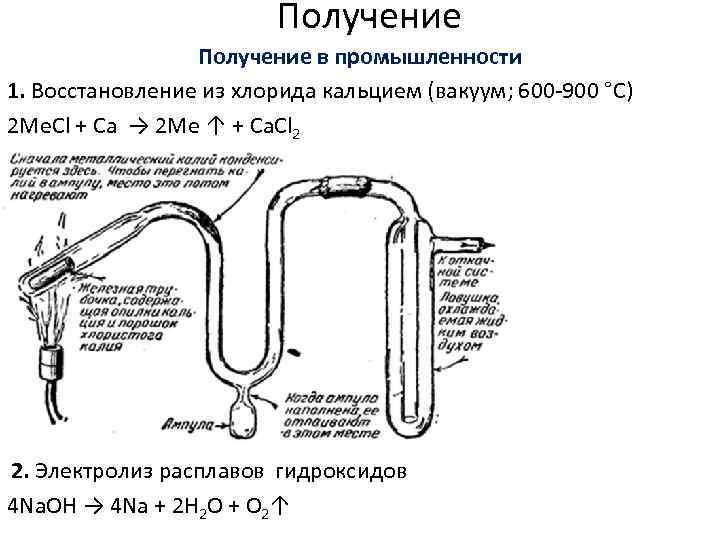 Получение в промышленности 1. Восстановление из хлорида кальцием (вакуум; 600 900 °C) 2 Me. Cl + Ca → 2 Me ↑ + Ca. Cl 2 2. Электролиз расплавов гидроксидов 4 Na. OH → 4 Na + 2 H 2 O + O 2↑
Получение в промышленности 1. Восстановление из хлорида кальцием (вакуум; 600 900 °C) 2 Me. Cl + Ca → 2 Me ↑ + Ca. Cl 2 2. Электролиз расплавов гидроксидов 4 Na. OH → 4 Na + 2 H 2 O + O 2↑
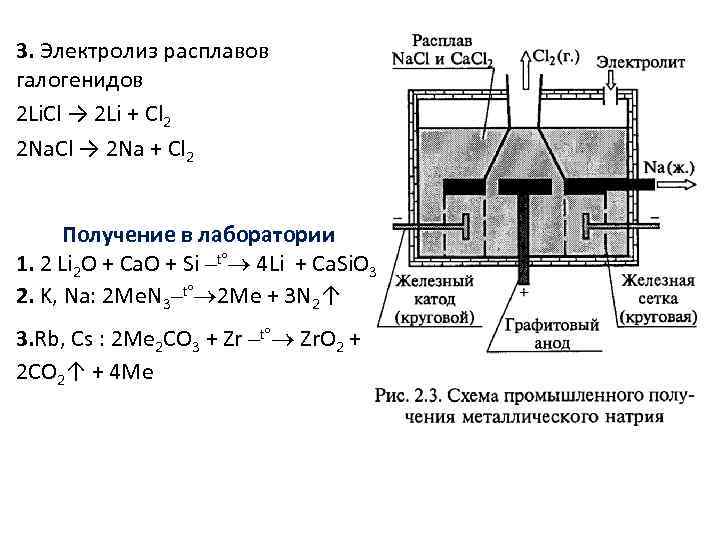 3. Электролиз расплавов галогенидов 2 Li. Cl → 2 Li + Cl 2 2 Na. Cl → 2 Na + Cl 2 Получение в лаборатории 1. 2 Li 2 O + Ca. O + Si –t°® 4 Li + Ca. Si. O 3 2. K, Na: 2 Me. N 3–t°® 2 Me + 3 N 2↑ 3. Rb, Cs : 2 Me 2 CO 3 + Zr –t°® Zr. O 2 + 2 CO 2↑ + 4 Me
3. Электролиз расплавов галогенидов 2 Li. Cl → 2 Li + Cl 2 2 Na. Cl → 2 Na + Cl 2 Получение в лаборатории 1. 2 Li 2 O + Ca. O + Si –t°® 4 Li + Ca. Si. O 3 2. K, Na: 2 Me. N 3–t°® 2 Me + 3 N 2↑ 3. Rb, Cs : 2 Me 2 CO 3 + Zr –t°® Zr. O 2 + 2 CO 2↑ + 4 Me
 Химические свойства • Li Na K Rb
Химические свойства • Li Na K Rb
 2. Взаимодействие с водой 2 Мe(тв. ) + 2 Н 2 О = 2 Мe (р. ) + 2 ОН (р. ) + Н 2 (г. )↑ 3. Взаимодействие с кислотами 2 Me + 2 HCl = 2 Me. Cl + H 2 4. Восстановители других металлов 5. Взаимодействие с неметаллами 2 Li + Cl 2 ® 2 Li. Cl(галогениды) 2 Na + S ® Na 2 S(сульфиды) 2 Na + H 2 ® 2 Na. H(гидриды) 6 Li + N 2 ® 2 Li 3 N(нитриды) 2 Li + 2 C ® 2 Li 2 C 2(карбиды) 2 Na + 2 NH 3 ® 2 Na. NH 2 + H 2 (амиды) 6. Амальгамы
2. Взаимодействие с водой 2 Мe(тв. ) + 2 Н 2 О = 2 Мe (р. ) + 2 ОН (р. ) + Н 2 (г. )↑ 3. Взаимодействие с кислотами 2 Me + 2 HCl = 2 Me. Cl + H 2 4. Восстановители других металлов 5. Взаимодействие с неметаллами 2 Li + Cl 2 ® 2 Li. Cl(галогениды) 2 Na + S ® Na 2 S(сульфиды) 2 Na + H 2 ® 2 Na. H(гидриды) 6 Li + N 2 ® 2 Li 3 N(нитриды) 2 Li + 2 C ® 2 Li 2 C 2(карбиды) 2 Na + 2 NH 3 ® 2 Na. NH 2 + H 2 (амиды) 6. Амальгамы
 Кислородные соединения 1. Способы получения 4 Li + O 2 ® 2 Li 2 O Na 2 O 2 + 2 Na ® 2 Na 2 O 5 Na. N 3 + Na. NO 3 ® 3 Na 2 O + 8 N 2 KO 2 + 3 K ® 2 K 2 O 2. Типичные основные оксиды Li 2 O + H 2 O ® 2 Li. OH Na 2 O + SO 3 ® Na 2 SO 4 K 2 O + 2 HNO 3 ® 2 KNO 3 + H 2 O
Кислородные соединения 1. Способы получения 4 Li + O 2 ® 2 Li 2 O Na 2 O 2 + 2 Na ® 2 Na 2 O 5 Na. N 3 + Na. NO 3 ® 3 Na 2 O + 8 N 2 KO 2 + 3 K ® 2 K 2 O 2. Типичные основные оксиды Li 2 O + H 2 O ® 2 Li. OH Na 2 O + SO 3 ® Na 2 SO 4 K 2 O + 2 HNO 3 ® 2 KNO 3 + H 2 O
 3. Пероксид натрия Na 2 O 2 2 Na. I + Na 2 O 2 + 2 H 2 SO 4 ® I 2 + 2 Na 2 SO 4 + 2 H 2 O 2 Na 2 O 2 + 2 CO 2 ® 2 Na 2 CO 3 + O 2 Na 2 O 2 + 2 H 2 O ® 2 Na. OH + H 2 O 2 4 Na 2 O 2 + Pb. S +4 H 2 SO 4 = Pb. SO 4↓ + 4 Na 2 SO 4 +4 H 2 O 4. Надпероксид калия KO 2 4 KO 2 + 2 CO 2 = 2 K 2 CO 3 + 3 O 2 (изолирующий противогаз) 2 KO 2 + 2 H 2 O = 2 KOH + H 2 O 2 + O 2
3. Пероксид натрия Na 2 O 2 2 Na. I + Na 2 O 2 + 2 H 2 SO 4 ® I 2 + 2 Na 2 SO 4 + 2 H 2 O 2 Na 2 O 2 + 2 CO 2 ® 2 Na 2 CO 3 + O 2 Na 2 O 2 + 2 H 2 O ® 2 Na. OH + H 2 O 2 4 Na 2 O 2 + Pb. S +4 H 2 SO 4 = Pb. SO 4↓ + 4 Na 2 SO 4 +4 H 2 O 4. Надпероксид калия KO 2 4 KO 2 + 2 CO 2 = 2 K 2 CO 3 + 3 O 2 (изолирующий противогаз) 2 KO 2 + 2 H 2 O = 2 KOH + H 2 O 2 + O 2
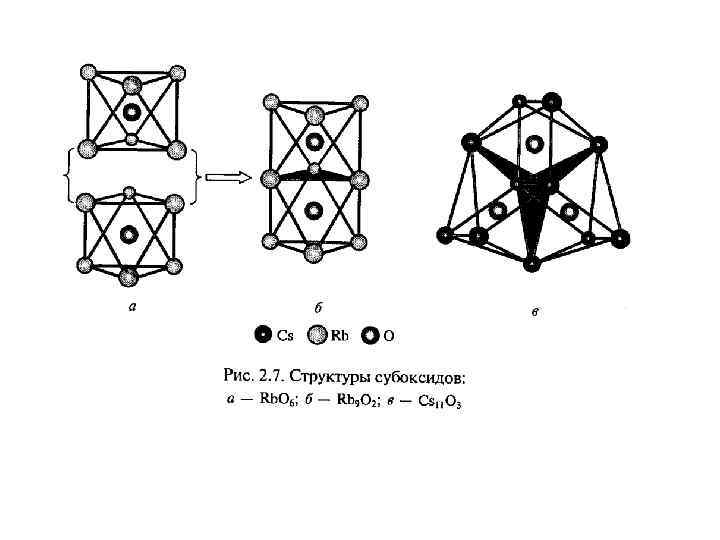
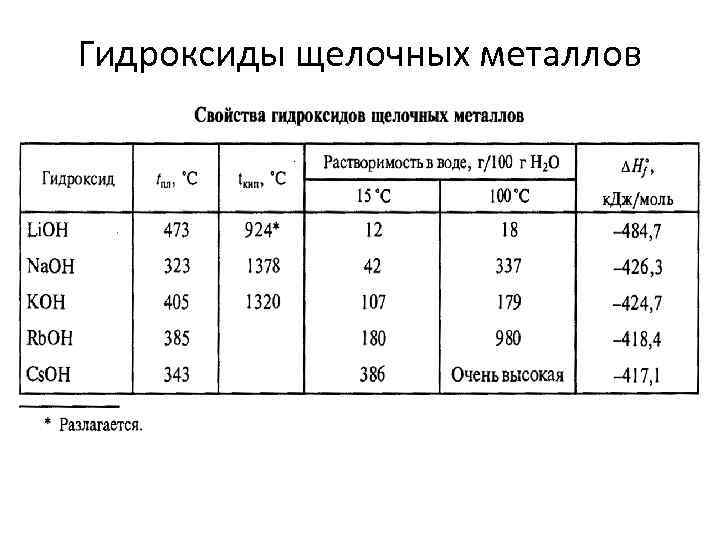 Гидроксиды щелочных металлов
Гидроксиды щелочных металлов
 1. Получение в промышленности 2 MCl (р-р) + 2 H 2 O ® 2 MOH + H 2 + Cl 2 (электролиз с диафрагмой) 2. Получение в лаборатории 2 KO 2 + 2 H 2 O ® 2 KOH + H 2 O 2 +O 2 Na 2 O 2 + 2 H 2 O ® 2 Na. OH + H 2 O 2 M 2 CO 3 + Ca(OH)2 ↔ Ca. CO 3 + 2 MOH (длительное кипячение) 3. Сильные основания 2 Na. OH + CO 2 ® Na 2 CO 3 + H 2 O Li. OH + HCl ® Li. Cl + H 2 O KOH + Al(OH)3 ® K[Al(OH)4] Na. OH + CH 3 COONa –t°® Na 2 CO 3 + CH 4 (сплавление)
1. Получение в промышленности 2 MCl (р-р) + 2 H 2 O ® 2 MOH + H 2 + Cl 2 (электролиз с диафрагмой) 2. Получение в лаборатории 2 KO 2 + 2 H 2 O ® 2 KOH + H 2 O 2 +O 2 Na 2 O 2 + 2 H 2 O ® 2 Na. OH + H 2 O 2 M 2 CO 3 + Ca(OH)2 ↔ Ca. CO 3 + 2 MOH (длительное кипячение) 3. Сильные основания 2 Na. OH + CO 2 ® Na 2 CO 3 + H 2 O Li. OH + HCl ® Li. Cl + H 2 O KOH + Al(OH)3 ® K[Al(OH)4] Na. OH + CH 3 COONa –t°® Na 2 CO 3 + CH 4 (сплавление)
 1. Получение Гидриды, нитриды 2 M + H 2 –t°® 2 MH (бесцветные «соли» ) 6 M + N 2 –t°® 2 M 3 N 2. Взаимодействие с водой MH + H 2 O –® MOH + H 2 M 3 N + 3 H 2 O –® 3 MOH + NH 3 3) Взаимодействие с солями
1. Получение Гидриды, нитриды 2 M + H 2 –t°® 2 MH (бесцветные «соли» ) 6 M + N 2 –t°® 2 M 3 N 2. Взаимодействие с водой MH + H 2 O –® MOH + H 2 M 3 N + 3 H 2 O –® 3 MOH + NH 3 3) Взаимодействие с солями
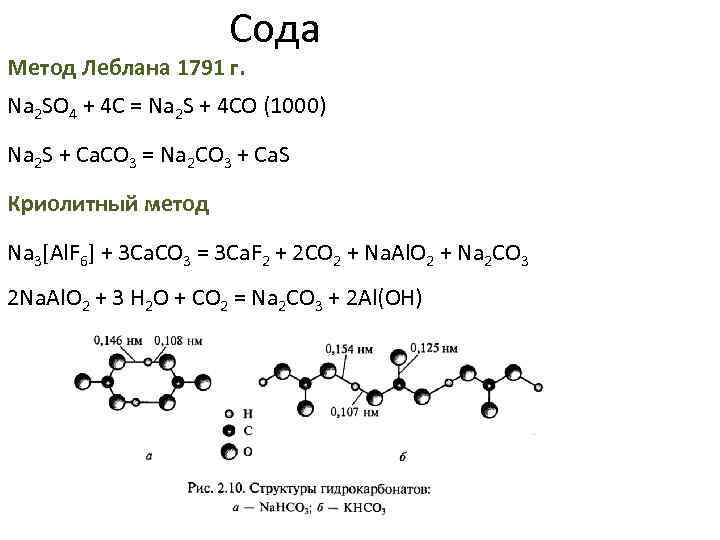 Сода Метод Леблана 1791 г. Na 2 SO 4 + 4 C = Na 2 S + 4 CO (1000) Na 2 S + Ca. CO 3 = Na 2 CO 3 + Ca. S Криолитный метод Na 3[Al. F 6] + 3 Ca. CO 3 = 3 Ca. F 2 + 2 CO 2 + Na. Al. O 2 + Na 2 CO 3 2 Na. Al. O 2 + 3 H 2 O + CO 2 = Na 2 CO 3 + 2 Al(OH)
Сода Метод Леблана 1791 г. Na 2 SO 4 + 4 C = Na 2 S + 4 CO (1000) Na 2 S + Ca. CO 3 = Na 2 CO 3 + Ca. S Криолитный метод Na 3[Al. F 6] + 3 Ca. CO 3 = 3 Ca. F 2 + 2 CO 2 + Na. Al. O 2 + Na 2 CO 3 2 Na. Al. O 2 + 3 H 2 O + CO 2 = Na 2 CO 3 + 2 Al(OH)
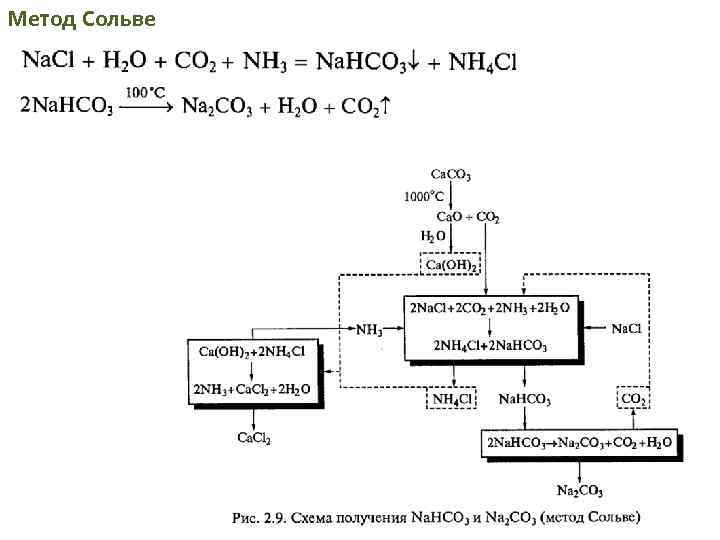 Метод Сольве
Метод Сольве
 Термоядерная бомба
Термоядерная бомба
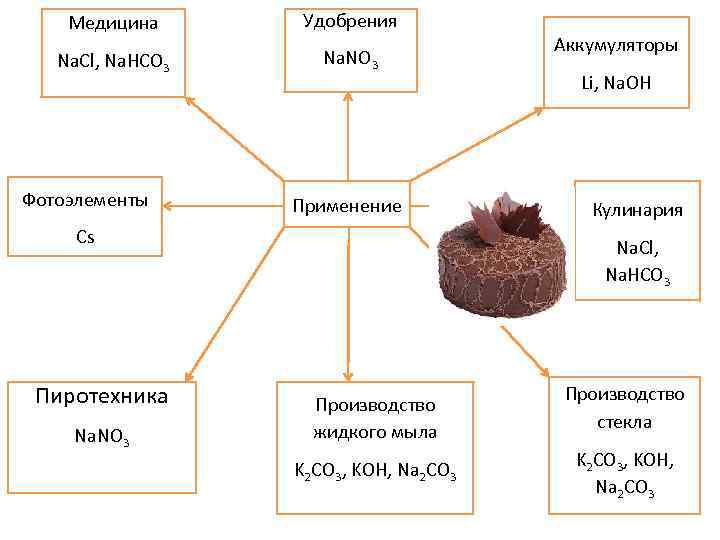 Медицина Удобрения Na. Cl, Na. HCO 3 Na. NO 3 Аккумуляторы Li, Na. OH Фотоэлементы Применение Cs Кулинария Na. Cl, Na. HCO 3 Пиротехника Na. NO 3 Производство жидкого мыла K 2 CO 3, KOH, Na 2 CO 3 Производство стекла K 2 CO 3, KOH, Na 2 CO 3
Медицина Удобрения Na. Cl, Na. HCO 3 Na. NO 3 Аккумуляторы Li, Na. OH Фотоэлементы Применение Cs Кулинария Na. Cl, Na. HCO 3 Пиротехника Na. NO 3 Производство жидкого мыла K 2 CO 3, KOH, Na 2 CO 3 Производство стекла K 2 CO 3, KOH, Na 2 CO 3



