Щелочные металлы к паре.pptx
- Количество слайдов: 18
 Щелочные металлы.
Щелочные металлы.
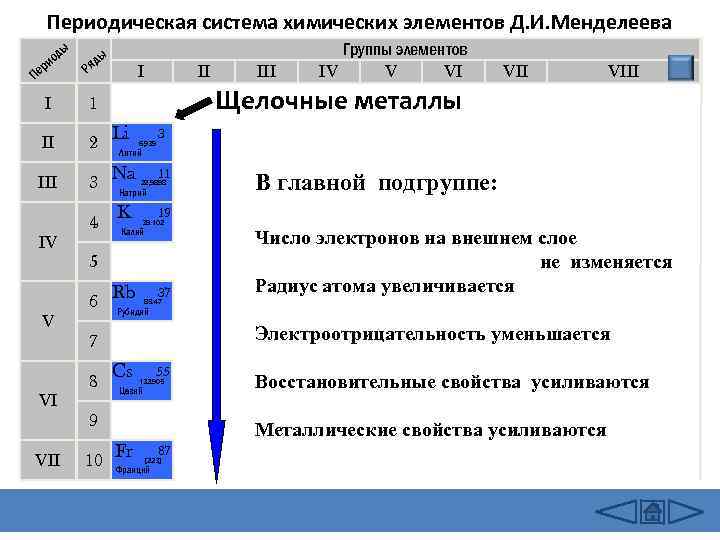 Периодическая система химических элементов Д. И. Менделеева ды ы яд о ри Р I 1 II 2 Li III 3 Na 4 K Пе IV V VI VII I II 6, 939 11 22, 9898 Натрий В главной подгруппе: 19 39. 102 Калий Rb 37 Число электронов на внешнем слое не изменяется Радиус атома увеличивается 85. 47 Рубидий Электроотрицательность уменьшается Cs 55 132. 905 Цезий 9 10 VIII Литий 7 8 Щелочные металлы VII 3 5 6 III Группы элементов IV V VI Fr Восстановительные свойства усиливаются Металлические свойства усиливаются 87 [223] Франций
Периодическая система химических элементов Д. И. Менделеева ды ы яд о ри Р I 1 II 2 Li III 3 Na 4 K Пе IV V VI VII I II 6, 939 11 22, 9898 Натрий В главной подгруппе: 19 39. 102 Калий Rb 37 Число электронов на внешнем слое не изменяется Радиус атома увеличивается 85. 47 Рубидий Электроотрицательность уменьшается Cs 55 132. 905 Цезий 9 10 VIII Литий 7 8 Щелочные металлы VII 3 5 6 III Группы элементов IV V VI Fr Восстановительные свойства усиливаются Металлические свойства усиливаются 87 [223] Франций
 Название металла Строение атома Li +3 ) ) 2 1 Na +11 ) ) ) 281 +19 ) ) 2881 +37 ) ) ) 2 8 18 8 1 +55 ) ) ) 2 8 18 18 8 1 +87 ) ) ) ) K Rb Cs Fr 2 8 18 32 18 8 1 Электронная формула 1 s 2|2 s 1 1 s 2|2 s 22 p 6|3 s 23 p 6|4 s 23 d 104 p 6|5 s 1 5 s 24 d 105 p 6|6 s 1 6 s 24 f 145 d 106 p 6|7 s 1
Название металла Строение атома Li +3 ) ) 2 1 Na +11 ) ) ) 281 +19 ) ) 2881 +37 ) ) ) 2 8 18 8 1 +55 ) ) ) 2 8 18 18 8 1 +87 ) ) ) ) K Rb Cs Fr 2 8 18 32 18 8 1 Электронная формула 1 s 2|2 s 1 1 s 2|2 s 22 p 6|3 s 23 p 6|4 s 23 d 104 p 6|5 s 1 5 s 24 d 105 p 6|6 s 1 6 s 24 f 145 d 106 p 6|7 s 1
 История открытия лития Арфведсон Юхан Август (12. 01. 1792 г. – 28. 10. 1841 г. ) Литий был открыт в 1817 г. А. Арфведсоном в минерале петалите. Берцелиус предложил назвать ее литионом (Lithion), поскольку эта щелочь впервые была найдена в "царстве минералов" (камней); название это произведено от греч. камень. Металлический Литий впервые получен в 1818 г. Г. Дэви путем злектролиза щелочи. В 1855 г. Бунзен и Маттессен разработали промышленный способ получения металлического лития злектролизом хлорида лития.
История открытия лития Арфведсон Юхан Август (12. 01. 1792 г. – 28. 10. 1841 г. ) Литий был открыт в 1817 г. А. Арфведсоном в минерале петалите. Берцелиус предложил назвать ее литионом (Lithion), поскольку эта щелочь впервые была найдена в "царстве минералов" (камней); название это произведено от греч. камень. Металлический Литий впервые получен в 1818 г. Г. Дэви путем злектролиза щелочи. В 1855 г. Бунзен и Маттессен разработали промышленный способ получения металлического лития злектролизом хлорида лития.
 История открытия натрия Гемфри Дэви (17. 12. 1778 г – 29. 05. 1829 г) Натрий (Natrium, от англ. и франц. Sodium, нем. Natrium от древнеевр. neter — бурлящее вещество. В 1807 г. Г. Дэви путем электролиза слегка увлажненных твердых щелочей получил свободный металл натрий, назвав его содий (Sodium). В следующем году Гильберт предложил именовать новый металл натронием (Natronium); Берцелиус сократил последнее название до "натрий" (Natrium).
История открытия натрия Гемфри Дэви (17. 12. 1778 г – 29. 05. 1829 г) Натрий (Natrium, от англ. и франц. Sodium, нем. Natrium от древнеевр. neter — бурлящее вещество. В 1807 г. Г. Дэви путем электролиза слегка увлажненных твердых щелочей получил свободный металл натрий, назвав его содий (Sodium). В следующем году Гильберт предложил именовать новый металл натронием (Natronium); Берцелиус сократил последнее название до "натрий" (Natrium).
 История открытия калия Калий (англ. Potassium, франц. Potassium, нем. Kalium) открыл в 1807 г. Г. Дэви, производивший электролиз твердого, слегка увлажненного едкого кали. Дэви именовал новый металл потассием (Potassium), но это название не прижилось. Крестным отцом металла оказался Гильберт, известный издатель журнала "Annalen deг Physik", предложивший название "калий"; оно было принято в Германии и России. Гемфри Дэви (17. 12. 1778 г – 29. 05. 1829 г)
История открытия калия Калий (англ. Potassium, франц. Potassium, нем. Kalium) открыл в 1807 г. Г. Дэви, производивший электролиз твердого, слегка увлажненного едкого кали. Дэви именовал новый металл потассием (Potassium), но это название не прижилось. Крестным отцом металла оказался Гильберт, известный издатель журнала "Annalen deг Physik", предложивший название "калий"; оно было принято в Германии и России. Гемфри Дэви (17. 12. 1778 г – 29. 05. 1829 г)
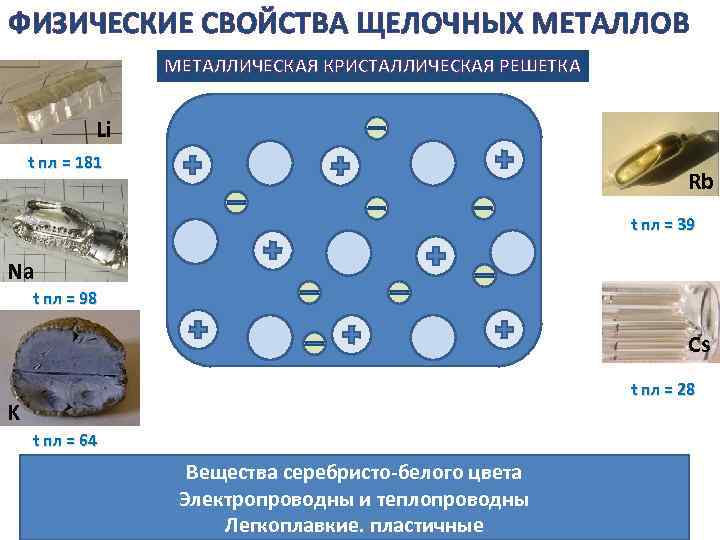 ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Li t пл = 181 Rb t пл = 39 Na t пл = 98 Cs t пл = 28 K t пл = 64 Вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные
ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Li t пл = 181 Rb t пл = 39 Na t пл = 98 Cs t пл = 28 K t пл = 64 Вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные
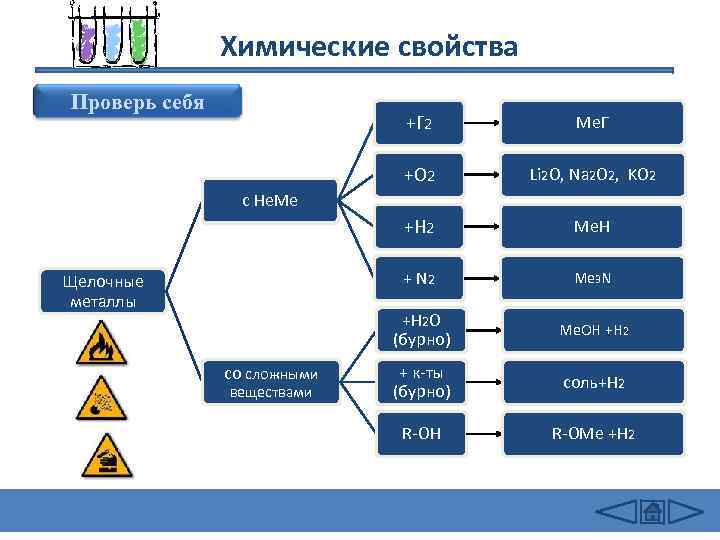 Химические свойства Проверь себя +Г 2 Me. Г +O 2 Li 2 O, Na 2 O 2, KO 2 +H 2 Ме. H + N 2 Me 3 N +H 2 O (бурно) Ме. OH +H 2 + к-ты (бурно) соль+H 2 R-OH R-OMe +H 2 с Не. Ме Щелочные металлы со сложными веществами
Химические свойства Проверь себя +Г 2 Me. Г +O 2 Li 2 O, Na 2 O 2, KO 2 +H 2 Ме. H + N 2 Me 3 N +H 2 O (бурно) Ме. OH +H 2 + к-ты (бурно) соль+H 2 R-OH R-OMe +H 2 с Не. Ме Щелочные металлы со сложными веществами
 Химические свойства 1) 2 Na + Cl 2 = 2 Na. Cl (в атмосфере F 2 и Cl 2 щелочные Me самовоспламеняются) 2) 4 Li + O 2 = 2 Li 2 O 2 Na + O 2 = Na 2 O 2 оксид Li 3) 2 Na + Н 2 = 2 Na. Н пероксид Na 2 K + 2 O 2 = K 2 O 4 надпероксид K (при нагревании 200 -400 o. C) 4) 6 Li + N 2 = 2 Li 3 N (Li - при комнатной T, остальные щелочные Me -при нагревании) 5) 2 Na + 2 Н 2 О = 2 Na. ОН + Н 2(Li - спокойно, Na - энергично, остальные – со взрывом – воспламеняется выделяющийся Н 2 Rb и Cs реагируют не только с жидкой Н 2 О, но и со льдом. ) 6) 2 Na+ Н 2 SО 4 = Na 2 SО 4 + Н 2 (протекают очень бурно) 7) 2 C 2 H 5 OH + 2 Na = 2 C 2 H 5 ONa + Н 2
Химические свойства 1) 2 Na + Cl 2 = 2 Na. Cl (в атмосфере F 2 и Cl 2 щелочные Me самовоспламеняются) 2) 4 Li + O 2 = 2 Li 2 O 2 Na + O 2 = Na 2 O 2 оксид Li 3) 2 Na + Н 2 = 2 Na. Н пероксид Na 2 K + 2 O 2 = K 2 O 4 надпероксид K (при нагревании 200 -400 o. C) 4) 6 Li + N 2 = 2 Li 3 N (Li - при комнатной T, остальные щелочные Me -при нагревании) 5) 2 Na + 2 Н 2 О = 2 Na. ОН + Н 2(Li - спокойно, Na - энергично, остальные – со взрывом – воспламеняется выделяющийся Н 2 Rb и Cs реагируют не только с жидкой Н 2 О, но и со льдом. ) 6) 2 Na+ Н 2 SО 4 = Na 2 SО 4 + Н 2 (протекают очень бурно) 7) 2 C 2 H 5 OH + 2 Na = 2 C 2 H 5 ONa + Н 2
 Взаимодействие щелочных металлов с водой.
Взаимодействие щелочных металлов с водой.
 Качественное определение щелочных металлов Для распознавания соединений щелочных металлов по окраске пламени исследуемое вещество вносится в пламя горелки на кончике железной проволоки. Li+ - карминово-красный K+ - фиолетовый Na+ - желтый Rb + - красный Li+ Na+ Cs+ - фиолетово-синий K+
Качественное определение щелочных металлов Для распознавания соединений щелочных металлов по окраске пламени исследуемое вещество вносится в пламя горелки на кончике железной проволоки. Li+ - карминово-красный K+ - фиолетовый Na+ - желтый Rb + - красный Li+ Na+ Cs+ - фиолетово-синий K+
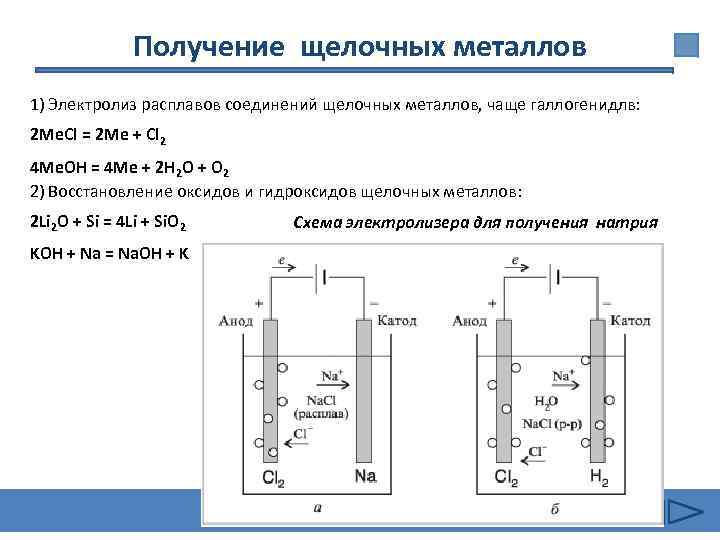 Получение щелочных металлов 1) Электролиз расплавов соединений щелочных металлов, чаще галлогенидлв: 2 Ме. Cl = 2 Ме + Cl 2 4 Ме. OH = 4 Ме + 2 Н 2 О + О 2 2) Восстановление оксидов и гидроксидов щелочных металлов: 2 Li 2 O + Si = 4 Li + Si. O 2 KOH + Na = Nа. OH + K Схема электролизера для получения натрия
Получение щелочных металлов 1) Электролиз расплавов соединений щелочных металлов, чаще галлогенидлв: 2 Ме. Cl = 2 Ме + Cl 2 4 Ме. OH = 4 Ме + 2 Н 2 О + О 2 2) Восстановление оксидов и гидроксидов щелочных металлов: 2 Li 2 O + Si = 4 Li + Si. O 2 KOH + Na = Nа. OH + K Схема электролизера для получения натрия
 Важнейшие соединения металлов Сульфат натрия Хлорид натрия
Важнейшие соединения металлов Сульфат натрия Хлорид натрия
 Оксиды • Оксиды щелочных металлов – соединения их с О вида Ме 2 О: О 2 О 2 Na+ Li+ • Оксиды основные, так как им соответсвуют гидроксиды Na. OH; Li. OH.
Оксиды • Оксиды щелочных металлов – соединения их с О вида Ме 2 О: О 2 О 2 Na+ Li+ • Оксиды основные, так как им соответсвуют гидроксиды Na. OH; Li. OH.
 Образование оксидов • Оксид лития образуется при реакции лития с кислородом: 4 Li + O 2=2 Li 2 O (t) Образование остальных оксидов рассмотрим на примере натрия: I 2 Na + O 2 = Na 2 O 2 (пероксид Na–O–О–Na) II 2 Na + Na 2 O 2 = 2 Na 2 O (t) I – активная стадия II – прокаливание Также образуются разложением солей (карбонатов и сульфитов) кислородосодержащих кислот с соответствующими металлами: K 2 CO 3 K 2 O + CO 2 Li 2 SO 3 Li 2 O + SO 2 (t)
Образование оксидов • Оксид лития образуется при реакции лития с кислородом: 4 Li + O 2=2 Li 2 O (t) Образование остальных оксидов рассмотрим на примере натрия: I 2 Na + O 2 = Na 2 O 2 (пероксид Na–O–О–Na) II 2 Na + Na 2 O 2 = 2 Na 2 O (t) I – активная стадия II – прокаливание Также образуются разложением солей (карбонатов и сульфитов) кислородосодержащих кислот с соответствующими металлами: K 2 CO 3 K 2 O + CO 2 Li 2 SO 3 Li 2 O + SO 2 (t)
 Гидроксиды • Гидроксиды щелочных металлов, кроме Li, термостойки и не разрушаются от температуры. • Гидроксиды реагируют с: Кислотами: 2 KOH + H 2 SO 4 = K 2 SO 4 + 2 H 2 O соль +вода Кислотными оксидами: 2 KOH + Si. O 2 = K 2 Si. O 3 + H 2 O соль + вода Солями, если образуется нерастворимое основание: 2 Na. OH + Cu. SO 4 Cu(OH)2 + Na 2 SO 4 нерастворимое основание + соль
Гидроксиды • Гидроксиды щелочных металлов, кроме Li, термостойки и не разрушаются от температуры. • Гидроксиды реагируют с: Кислотами: 2 KOH + H 2 SO 4 = K 2 SO 4 + 2 H 2 O соль +вода Кислотными оксидами: 2 KOH + Si. O 2 = K 2 Si. O 3 + H 2 O соль + вода Солями, если образуется нерастворимое основание: 2 Na. OH + Cu. SO 4 Cu(OH)2 + Na 2 SO 4 нерастворимое основание + соль
 Образование гидроксидов • Обратная реакция: оксид+вода=гидроксид K 2 O + H 2 O= 2 KOH Гидроксиды щелочных металлов – соединения их с группой ОН. Общая формула их: Ме. ОН; растворимы Na – O – H Li – O – H
Образование гидроксидов • Обратная реакция: оксид+вода=гидроксид K 2 O + H 2 O= 2 KOH Гидроксиды щелочных металлов – соединения их с группой ОН. Общая формула их: Ме. ОН; растворимы Na – O – H Li – O – H
 НЕКОТОРЫЕ СОЛИ КАЛИЯ И НАТРИЯ И ИХ ПРИМЕНЕНИЙ Сколько воды и хлорида натрия нужно Раствор хлорида натрия (0, 9%) взять в медицине. Такой применяется для приготовленияраствор физиологического раствора называется физиологическим массой 0, 5 кг? 4, 5 г соли ответ 495, 5 г воды Смесь хлорида применяется в кулинарии, Питьевая сода и гидрокарбоната натрия массойвыпечки кондитерских изделий. для 15 г обработали уксусной кислотой, при этом как добавка к пище Хлорид натрия - выделилось 2, 8 л (н. у. ) газа. Определите массовые доли в процентах компонентов смеси. 70% Na. HCO 3 ответ 30% Na. Cl Хлорид калия - очень ценное Тривиальные названия солей: Калийные удобрения играю важную минеральное удобрение. Рассчитайте роль в жизни растений. Na. Cl K 2 CO 3 массовую долю калия (%) в этом веществе. Поваренная соль поташ 52% ответ Кристалли. Na 2 CO 3*10 H 2 O ческая сода Na. HCO 3 Питьевая сода Калийная KNO селитра 3 Глауберова соль Na 2 SO 4*10 H 2 O
НЕКОТОРЫЕ СОЛИ КАЛИЯ И НАТРИЯ И ИХ ПРИМЕНЕНИЙ Сколько воды и хлорида натрия нужно Раствор хлорида натрия (0, 9%) взять в медицине. Такой применяется для приготовленияраствор физиологического раствора называется физиологическим массой 0, 5 кг? 4, 5 г соли ответ 495, 5 г воды Смесь хлорида применяется в кулинарии, Питьевая сода и гидрокарбоната натрия массойвыпечки кондитерских изделий. для 15 г обработали уксусной кислотой, при этом как добавка к пище Хлорид натрия - выделилось 2, 8 л (н. у. ) газа. Определите массовые доли в процентах компонентов смеси. 70% Na. HCO 3 ответ 30% Na. Cl Хлорид калия - очень ценное Тривиальные названия солей: Калийные удобрения играю важную минеральное удобрение. Рассчитайте роль в жизни растений. Na. Cl K 2 CO 3 массовую долю калия (%) в этом веществе. Поваренная соль поташ 52% ответ Кристалли. Na 2 CO 3*10 H 2 O ческая сода Na. HCO 3 Питьевая сода Калийная KNO селитра 3 Глауберова соль Na 2 SO 4*10 H 2 O


