презентация 2.pptx
- Количество слайдов: 11

Щелочные металлы
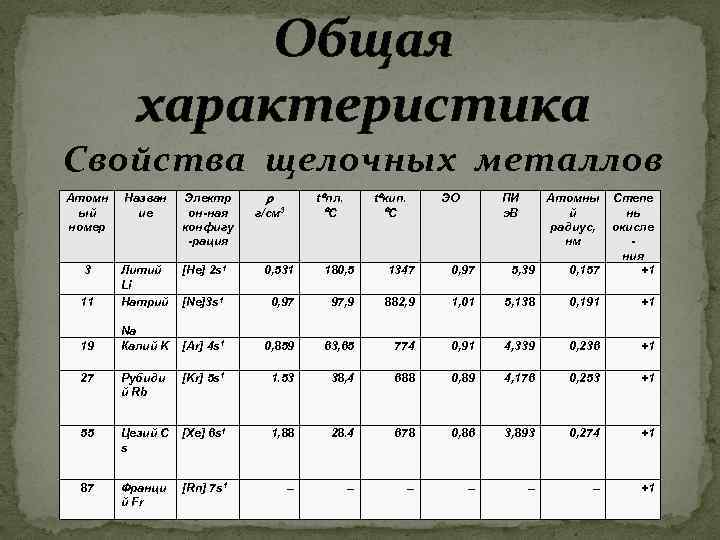
Общая характеристика Свойства щелочных металлов Атомн ый номер Назван ие 3 Литий Li Натрий Na Калий K 11 19 Электр он-ная конфигу -рация [He] 2 s 1 t°пл. °C r t°кип. °C 0, 531 180, 5 1347 0, 97 5, 39 0, 157 Степе нь окисле ния +1 [Ne]3 s 1 0, 97 97, 9 882, 9 1, 01 5, 138 0, 191 +1 [Ar] 4 s 1 0, 859 63, 65 774 0, 91 4, 339 0, 236 +1 г/см 3 ЭО ПИ э. В Атомны й радиус, нм 27 Рубиди й Rb [Kr] 5 s 1 1. 53 38, 4 688 0, 89 4, 176 0, 253 +1 55 Цезий C s [Xe] 6 s 1 1, 88 28. 4 678 0, 86 3, 893 0, 274 +1 87 Франци й Fr [Rn] 7 s 1 – – – +1

Физические свойства Низкие температуры плавления, малые значения плотностей, мягкие, режутся ножом. Низкий потенциал ионизации, который уменьшается с увеличением атомного номера.

Химические свойства Типичные металлы, очень сильные восстановители. В соединениях проявляют единственную степень окисления +1. Восстановительная способность увеличивается с ростом атомной массы. Все соединения имеют ионный характер, почти все растворимы в воде. Гидроксиды R–OH – щёлочи, сила их возрастает с увеличением атомной массы металла.

Воспламеняются на воздухе при умеренном нагревании. С водородом образуют солеобразные гидриды. Продукты сгорания чаще всего пероксиды.

Все щелочные металлы - очень сильные восстановители, в соединениях проявляют единственную степень окисления +1. Восстановительная способность увеличивается в ряду ––Li–Na–K–Rb–Cs®. Все соединения щелочных металлов имеют ионный характер.


1. Активно взаимодействуют с водой: 2 Na + 2 H 2 O ® 2 Na. OH + H 2 2 Li + 2 H 2 O ® 2 Li. OH + H 2 2. Реакция с кислотами: 2 Na + 2 HCl ® 2 Na. Cl + H 2 3. Реакция с кислородом: 4 Li + O 2 ® 2 Li 2 O(оксид лития) 2 Na + O 2 ® Na 2 O 2(пероксид натрия) K + O 2 ® KO 2(надпероксид калия) На воздухе щелочные металлы мгновенно окисляются. Поэтому их хранят под слоем органических растворителей (керосин и др. ).

4. В реакциях с другими неметаллами образуются бинарные соединения: 2 Li + Cl 2 ® 2 Li. Cl(галогениды) 2 Na + S ® Na 2 S(сульфиды) 2 Na + H 2 ® 2 Na. H(гидриды) 6 Li + N 2 ® 2 Li 3 N(нитриды) 2 Li + 2 C ® 2 Li 2 C 2(карбиды) Реагируют со спиртами и галогенопроизводными углеводородов (смотри "Органическую химию")

Нахождение в природе Li Li 2 O • Al 2 O 3 • 4 Si. O 2 – сподумен Na Na. Cl – каменная соль Na 2 SO 4 • 10 H 2 O – глауберова соль (мирабилит) Na. NO 3 – чилийская селитра K KCl • Na. Cl – сильвинит KCl • Mg. Cl 2 • 6 H 2 O – карналлит K 2 O • Al 2 O 3 • 6 Si. O 2 – полевой шпат (ортоклаз)

презентация 2.pptx