2011_inorg_medbiol_6.ppt
- Количество слайдов: 36
 Шестая лекция
Шестая лекция
 Полисульфиды Na 2 Sконц +(x-1)S = Na 2 Sx (получение) Na 2 Sx = 2 Na+ + Sx 2 - (диссоциация) Сульфаны Na 2 Sx + 2 HCl = H 2 Sx (получение) H 2 Sx - известны только для серы, Х=2 -6 выделены, Х=6 -9 в смесях. Более сильные кислоты, чем H 2 S 2: p. Ka 1 = 4; H 2 О 2: p. Ka 1 = 12 H 2 S: p. Ka 1 = 7; H 2 О: p. Ka 1 = 16 2
Полисульфиды Na 2 Sконц +(x-1)S = Na 2 Sx (получение) Na 2 Sx = 2 Na+ + Sx 2 - (диссоциация) Сульфаны Na 2 Sx + 2 HCl = H 2 Sx (получение) H 2 Sx - известны только для серы, Х=2 -6 выделены, Х=6 -9 в смесях. Более сильные кислоты, чем H 2 S 2: p. Ka 1 = 4; H 2 О 2: p. Ka 1 = 12 H 2 S: p. Ka 1 = 7; H 2 О: p. Ka 1 = 16 2
 SO 2 Tкип= -10 o. C, хорошо растворим в воде (10%) Получение. В промышленности – обжиг сульфидов: Zn. S + 3/2 O 2 = Zn. O + SO 2 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 (90% производства) В лаборатории: Na 2 SO 3 + 2 HCl = 2 Na. Cl + SO 2 + H 2 O Cu + 2 H 2 SO 4 конц = Cu. SO 4 + SO 2 + 2 H 2 O 3
SO 2 Tкип= -10 o. C, хорошо растворим в воде (10%) Получение. В промышленности – обжиг сульфидов: Zn. S + 3/2 O 2 = Zn. O + SO 2 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 (90% производства) В лаборатории: Na 2 SO 3 + 2 HCl = 2 Na. Cl + SO 2 + H 2 O Cu + 2 H 2 SO 4 конц = Cu. SO 4 + SO 2 + 2 H 2 O 3
 Кислородные соединения S 4+ Равновесия в воде: SO 2 газ + x. H 2 O = SO 2. x. H 2 O K 1 SO 2. x. H 2 O = H 2 SO 3 + (x-1)H 2 O K<<1 p. Ka 1 = 2; p. Ka 2 = 6 Взаимодействие со щелочью: 2 Na. OH + SO 2 = Na 2 SO 3 + H 2 O сульфит Na. OH + SO 2 = Na. HSO 3 гидросульфит, существует только в растворе 4
Кислородные соединения S 4+ Равновесия в воде: SO 2 газ + x. H 2 O = SO 2. x. H 2 O K 1 SO 2. x. H 2 O = H 2 SO 3 + (x-1)H 2 O K<<1 p. Ka 1 = 2; p. Ka 2 = 6 Взаимодействие со щелочью: 2 Na. OH + SO 2 = Na 2 SO 3 + H 2 O сульфит Na. OH + SO 2 = Na. HSO 3 гидросульфит, существует только в растворе 4
 Кислородные соединения S 4+ При упаривании раствора получают 2 Na. HSO 3 = Na 2 S 2 O 5 + H 2 O пиросульфит Кислота H 2 S 2 O 5 не известна Гидролиз сульфитов(p. H >7): SO 32 - + H 2 O = HSO 3 - + OH- Kh 10 -8 Гидролиз гидросульфитов(p. H <7): HSO 3 - + H 2 O = H 2 SO 3 + ОН- Kh 10 -12 HSO 3 - = SO 32 - + H+ Ka 2 10 -6 5
Кислородные соединения S 4+ При упаривании раствора получают 2 Na. HSO 3 = Na 2 S 2 O 5 + H 2 O пиросульфит Кислота H 2 S 2 O 5 не известна Гидролиз сульфитов(p. H >7): SO 32 - + H 2 O = HSO 3 - + OH- Kh 10 -8 Гидролиз гидросульфитов(p. H <7): HSO 3 - + H 2 O = H 2 SO 3 + ОН- Kh 10 -12 HSO 3 - = SO 32 - + H+ Ka 2 10 -6 5
 Кислородные соединения S 4+ • Диспропорционирование 4 SO 32 - = S 2 - + 3 SO 42 - (при нагревании) • Окисление (S 4+ S 6+) SO 2 + 1/2 O 2 = SO 3 (для синтеза H 2 SO 4) Na 2 SO 3 + 1/2 O 2 = Na 2 SO 4 (медленно) SO 2 + ОКИСЛИТЕЛЬ + H+ = SO 42(Mn. O 4 -, Cr 2 O 7 -, Cl. O 3 -, Cl 2, Br 2, I 2, H 2 O 2) • Восстановление SO 2 + 2 H 2 S = 3 S + 2 H 2 O 6
Кислородные соединения S 4+ • Диспропорционирование 4 SO 32 - = S 2 - + 3 SO 42 - (при нагревании) • Окисление (S 4+ S 6+) SO 2 + 1/2 O 2 = SO 3 (для синтеза H 2 SO 4) Na 2 SO 3 + 1/2 O 2 = Na 2 SO 4 (медленно) SO 2 + ОКИСЛИТЕЛЬ + H+ = SO 42(Mn. O 4 -, Cr 2 O 7 -, Cl. O 3 -, Cl 2, Br 2, I 2, H 2 O 2) • Восстановление SO 2 + 2 H 2 S = 3 S + 2 H 2 O 6
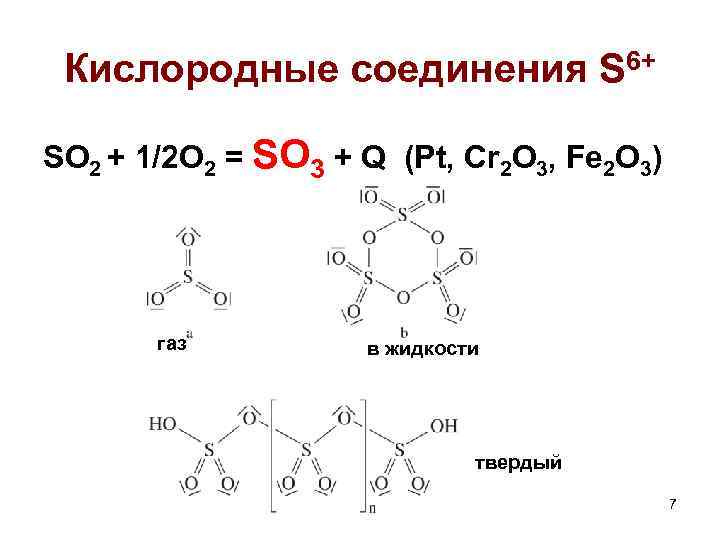 Кислородные соединения S 6+ SO 2 + 1/2 O 2 = SO 3 + Q (Pt, Cr 2 O 3, Fe 2 O 3) газ в жидкости твердый 7
Кислородные соединения S 6+ SO 2 + 1/2 O 2 = SO 3 + Q (Pt, Cr 2 O 3, Fe 2 O 3) газ в жидкости твердый 7
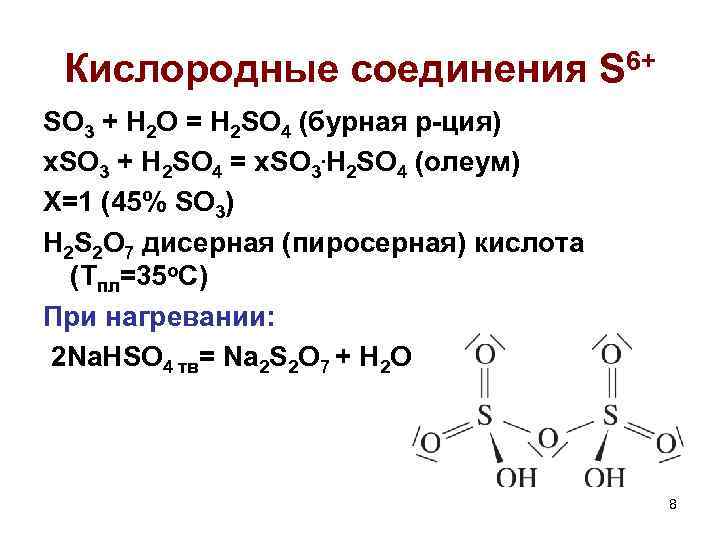 Кислородные соединения S 6+ SO 3 + H 2 O = H 2 SO 4 (бурная р-ция) x. SO 3 + H 2 SO 4 = x. SO 3. H 2 SO 4 (олеум) X=1 (45% SO 3) H 2 S 2 O 7 дисерная (пиросерная) кислота (Тпл=35 о. С) При нагревании: 2 Na. HSO 4 тв= Na 2 S 2 O 7 + H 2 O 8
Кислородные соединения S 6+ SO 3 + H 2 O = H 2 SO 4 (бурная р-ция) x. SO 3 + H 2 SO 4 = x. SO 3. H 2 SO 4 (олеум) X=1 (45% SO 3) H 2 S 2 O 7 дисерная (пиросерная) кислота (Тпл=35 о. С) При нагревании: 2 Na. HSO 4 тв= Na 2 S 2 O 7 + H 2 O 8
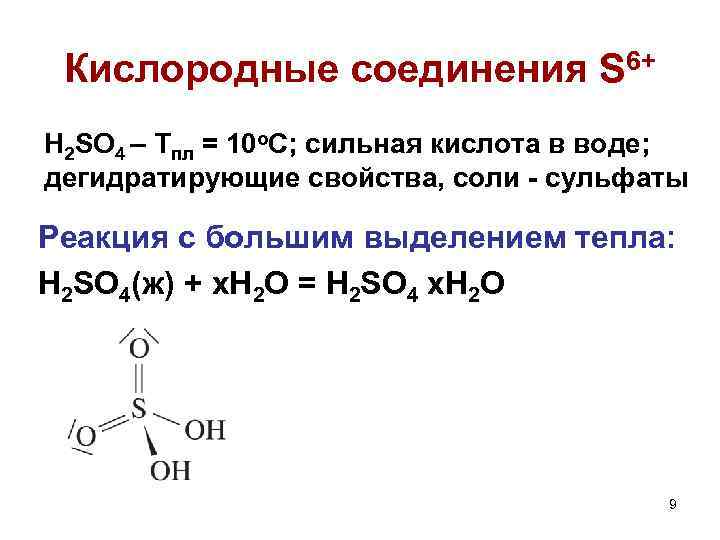 Кислородные соединения S 6+ H 2 SO 4 – Тпл = 10 о. С; сильная кислота в воде; дегидратирующие свойства, соли - сульфаты Реакция с большим выделением тепла: H 2 SO 4(ж) + x. H 2 O = H 2 SO 4 x. H 2 O 9
Кислородные соединения S 6+ H 2 SO 4 – Тпл = 10 о. С; сильная кислота в воде; дегидратирующие свойства, соли - сульфаты Реакция с большим выделением тепла: H 2 SO 4(ж) + x. H 2 O = H 2 SO 4 x. H 2 O 9
 H 2 SO 4 Конц. кислота – ОКИСЛИТЕЛЬ, обычно восстанавливается до SO 2 2 H 2 SO 4 + C = CO 2 + 2 SO 2 + 2 H 2 O Окисляет H 2 S, HBr, HJ, но не HCl H 2 Se. O 4 + 2 HCl = H 2 Se. O 3 + Cl 2 + H 2 O Отношение серной кислоты к металлам: E 0(Mn+/M 0) E 0<0 E 0>0 Au, Pt Разб. H 2 нет Конц. S, H 2 S SO 2 нет 10
H 2 SO 4 Конц. кислота – ОКИСЛИТЕЛЬ, обычно восстанавливается до SO 2 2 H 2 SO 4 + C = CO 2 + 2 SO 2 + 2 H 2 O Окисляет H 2 S, HBr, HJ, но не HCl H 2 Se. O 4 + 2 HCl = H 2 Se. O 3 + Cl 2 + H 2 O Отношение серной кислоты к металлам: E 0(Mn+/M 0) E 0<0 E 0>0 Au, Pt Разб. H 2 нет Конц. S, H 2 S SO 2 нет 10
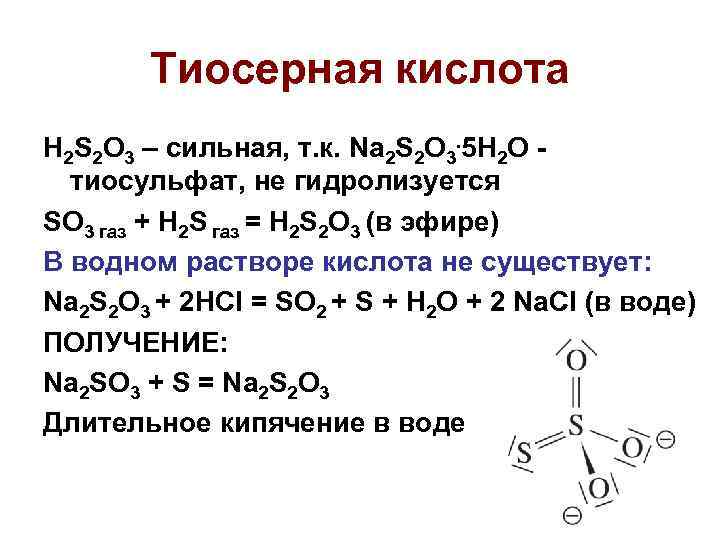 Тиосерная кислота H 2 S 2 O 3 – сильная, т. к. Na 2 S 2 O 3. 5 H 2 O тиосульфат, не гидролизуется SO 3 газ + H 2 S газ = H 2 S 2 O 3 (в эфире) В водном растворе кислота не существует: Na 2 S 2 O 3 + 2 HCl = SO 2 + S + H 2 O + 2 Na. Cl (в воде) ПОЛУЧЕНИЕ: Na 2 SO 3 + S = Na 2 S 2 O 3 Длительное кипячение в воде 11
Тиосерная кислота H 2 S 2 O 3 – сильная, т. к. Na 2 S 2 O 3. 5 H 2 O тиосульфат, не гидролизуется SO 3 газ + H 2 S газ = H 2 S 2 O 3 (в эфире) В водном растворе кислота не существует: Na 2 S 2 O 3 + 2 HCl = SO 2 + S + H 2 O + 2 Na. Cl (в воде) ПОЛУЧЕНИЕ: Na 2 SO 3 + S = Na 2 S 2 O 3 Длительное кипячение в воде 11
 Тиосульфаты Мягкий и удобный восстановитель S 2 O 32 - + 4 Cl 2 изб +5 H 2 O = 2 SO 42 - + 8 Cl- +10 H+ S 2 O 32 - + Br 2 +H 2 O = S + SO 42 - +2 Br- + 2 H+ ИОДОМЕТРИЯ: 2 S 2 O 32 - + J 2 = S 4 O 62 - + 2 J- КОЛИЧЕСТВЕННО! Комплексообразователь: Ag. Br↓ + 2 S 2 O 32 - = [Ag(S 2 O 3)2]3 - + Br- Донорный атом S используется в фотографии 12
Тиосульфаты Мягкий и удобный восстановитель S 2 O 32 - + 4 Cl 2 изб +5 H 2 O = 2 SO 42 - + 8 Cl- +10 H+ S 2 O 32 - + Br 2 +H 2 O = S + SO 42 - +2 Br- + 2 H+ ИОДОМЕТРИЯ: 2 S 2 O 32 - + J 2 = S 4 O 62 - + 2 J- КОЛИЧЕСТВЕННО! Комплексообразователь: Ag. Br↓ + 2 S 2 O 32 - = [Ag(S 2 O 3)2]3 - + Br- Донорный атом S используется в фотографии 12
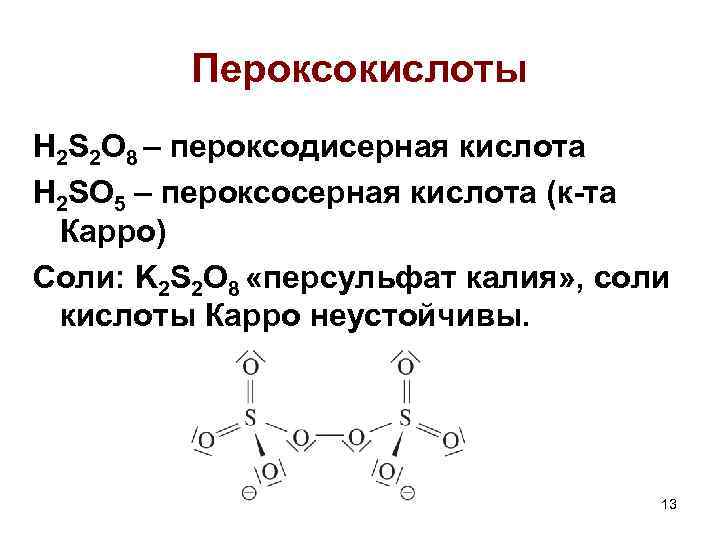 Пероксокислоты H 2 S 2 O 8 – пероксодисерная кислота H 2 SO 5 – пероксосерная кислота (к-та Карро) Соли: K 2 S 2 O 8 «персульфат калия» , соли кислоты Карро неустойчивы. 13
Пероксокислоты H 2 S 2 O 8 – пероксодисерная кислота H 2 SO 5 – пероксосерная кислота (к-та Карро) Соли: K 2 S 2 O 8 «персульфат калия» , соли кислоты Карро неустойчивы. 13
 Пероксокислоты E 0(S 2 O 82 -/2 SO 42 -) = +2, 01 В (сильный окислитель) 5 S 2 O 82 - + 2 Mn 2+ + 8 H 2 O = 10 SO 42 - + 2 Mn. O 4 - + 16 H+ 3 S 2 O 82 - + 2 Cr 3+ + 7 H 2 O = 6 SO 42 - + Cr 2 O 72 - + 14 H+ (реакции идут медленно, ускоряются Ag+) Электролиз 50% H 2 SO 4: Анод : 2 HSO 4 - -2 e = H 2 S 2 O 8 14
Пероксокислоты E 0(S 2 O 82 -/2 SO 42 -) = +2, 01 В (сильный окислитель) 5 S 2 O 82 - + 2 Mn 2+ + 8 H 2 O = 10 SO 42 - + 2 Mn. O 4 - + 16 H+ 3 S 2 O 82 - + 2 Cr 3+ + 7 H 2 O = 6 SO 42 - + Cr 2 O 72 - + 14 H+ (реакции идут медленно, ускоряются Ag+) Электролиз 50% H 2 SO 4: Анод : 2 HSO 4 - -2 e = H 2 S 2 O 8 14
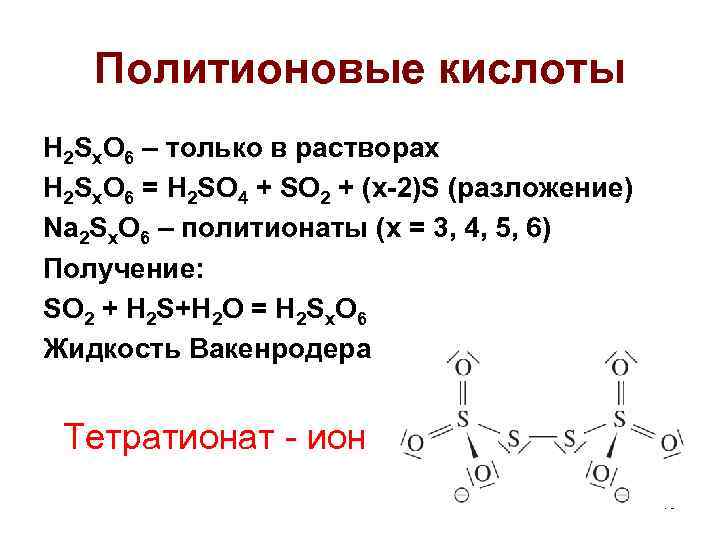 Политионовые кислоты H 2 Sx. O 6 – только в растворах H 2 Sx. O 6 = H 2 SO 4 + SO 2 + (x-2)S (разложение) Na 2 Sx. O 6 – политионаты (x = 3, 4, 5, 6) Получение: SO 2 + H 2 S+H 2 O = H 2 Sx. O 6 Жидкость Вакенродера Тетратионат - ион 15
Политионовые кислоты H 2 Sx. O 6 – только в растворах H 2 Sx. O 6 = H 2 SO 4 + SO 2 + (x-2)S (разложение) Na 2 Sx. O 6 – политионаты (x = 3, 4, 5, 6) Получение: SO 2 + H 2 S+H 2 O = H 2 Sx. O 6 Жидкость Вакенродера Тетратионат - ион 15
 Галогениды S S + F 2 = SF 4 или SF 6 SF 4 + 2 H 2 O = SO 2 + 4 HF SF 6 очень инертен 2 S + Cl 2 = S 2 Cl 2 (избыток серы) S + Cl 2 = SCl 2 (избыток хлора) Гидролиз протекает очень сложно S 2 Cl 2 + 2 H 2 O = H 2 S + SO 2 + 2 HCl 3 SCl 2 + 4 H 2 O = H 2 S + 2 SO 2 + 6 HCl 16
Галогениды S S + F 2 = SF 4 или SF 6 SF 4 + 2 H 2 O = SO 2 + 4 HF SF 6 очень инертен 2 S + Cl 2 = S 2 Cl 2 (избыток серы) S + Cl 2 = SCl 2 (избыток хлора) Гидролиз протекает очень сложно S 2 Cl 2 + 2 H 2 O = H 2 S + SO 2 + 2 HCl 3 SCl 2 + 4 H 2 O = H 2 S + 2 SO 2 + 6 HCl 16
 Оксогалогениды Хлорид тионила SO 2 + PCl 5 = SOCl 2 + PОCl 3 SO 3 + SCl 2 = SOCl 2 + SO 2 SOCl 2 + H 2 O = 2 HCl + SO 2 Хлорид сульфурила SO 2 + Cl 2 = SO 2 Cl 2 (катализатор актив. C) SO 2 Cl 2 + 2 H 2 O = H 2 SO 4 + 2 HCl 17
Оксогалогениды Хлорид тионила SO 2 + PCl 5 = SOCl 2 + PОCl 3 SO 3 + SCl 2 = SOCl 2 + SO 2 SOCl 2 + H 2 O = 2 HCl + SO 2 Хлорид сульфурила SO 2 + Cl 2 = SO 2 Cl 2 (катализатор актив. C) SO 2 Cl 2 + 2 H 2 O = H 2 SO 4 + 2 HCl 17
 Побочная подгруппа VI группы периодической системы 18
Побочная подгруппа VI группы периодической системы 18
 Содержание в земной коре и минералы • Cr – 20 местo Fe. Cr 2 O 4 – хромит, хромистый железняк • Mo – 37 место Mo. S 2 – молибденит Pb. Mo. O 4 - вульфенит • W – 39 место Ca. WO 4 - шеелит (Fe, Mn)WO 4 - вольфрамит 19
Содержание в земной коре и минералы • Cr – 20 местo Fe. Cr 2 O 4 – хромит, хромистый железняк • Mo – 37 место Mo. S 2 – молибденит Pb. Mo. O 4 - вульфенит • W – 39 место Ca. WO 4 - шеелит (Fe, Mn)WO 4 - вольфрамит 19
 Открытие элементов • Cr – в 1797 г. Француз Вокленд, греческое «хрома» –цвет; разнообразие окрасок в соединениях. • Mo – в 1817 г. Берцелиус, греческое «молюбдос» - свинец. • W – в 1781 г. Швед Шееле из минерала «тунгстен» . Вольфрам от немецкого Wolf Rahm. 20
Открытие элементов • Cr – в 1797 г. Француз Вокленд, греческое «хрома» –цвет; разнообразие окрасок в соединениях. • Mo – в 1817 г. Берцелиус, греческое «молюбдос» - свинец. • W – в 1781 г. Швед Шееле из минерала «тунгстен» . Вольфрам от немецкого Wolf Rahm. 20
 Cr Mo W Уменьшение активности металла: Cr + 2 HCl = Cr. Cl 2 + H 2 Mo и W не реагируют с «H+» Cr Mo W Увеличение устойчивости степени окисления 6+: Cr. O 3 Mo. O 3 и WO 3 Разлагается Устойчивы при 200 о. С до 1000 о. С 21
Cr Mo W Уменьшение активности металла: Cr + 2 HCl = Cr. Cl 2 + H 2 Mo и W не реагируют с «H+» Cr Mo W Увеличение устойчивости степени окисления 6+: Cr. O 3 Mo. O 3 и WO 3 Разлагается Устойчивы при 200 о. С до 1000 о. С 21
 Получение Cr Выплавка феррохрома: Fe. Cr 2 O 4 + 4 C = Fe + 2 Cr + 4 CO Получение чистого хрома: 4 Fe. Cr 2 O 4+ 8 Na 2 CO 3 +7 O 2 = 8 Na 2 Cr. O 4+2 Fe 2 O 3 +8 CO 2 2 Na 2 Cr. O 4 + 2 H 2 SO 4 = Na 2 Cr 2 O 7 + 2 Na. HSO 4 +H 2 O Na 2 Cr 2 O 7 + 2 C = Cr 2 O 3 +Na 2 CO 3 +CO Cr 2 O 3 +2 Al = Al 2 O 3 +2 Cr (алюмотермия) 22
Получение Cr Выплавка феррохрома: Fe. Cr 2 O 4 + 4 C = Fe + 2 Cr + 4 CO Получение чистого хрома: 4 Fe. Cr 2 O 4+ 8 Na 2 CO 3 +7 O 2 = 8 Na 2 Cr. O 4+2 Fe 2 O 3 +8 CO 2 2 Na 2 Cr. O 4 + 2 H 2 SO 4 = Na 2 Cr 2 O 7 + 2 Na. HSO 4 +H 2 O Na 2 Cr 2 O 7 + 2 C = Cr 2 O 3 +Na 2 CO 3 +CO Cr 2 O 3 +2 Al = Al 2 O 3 +2 Cr (алюмотермия) 22
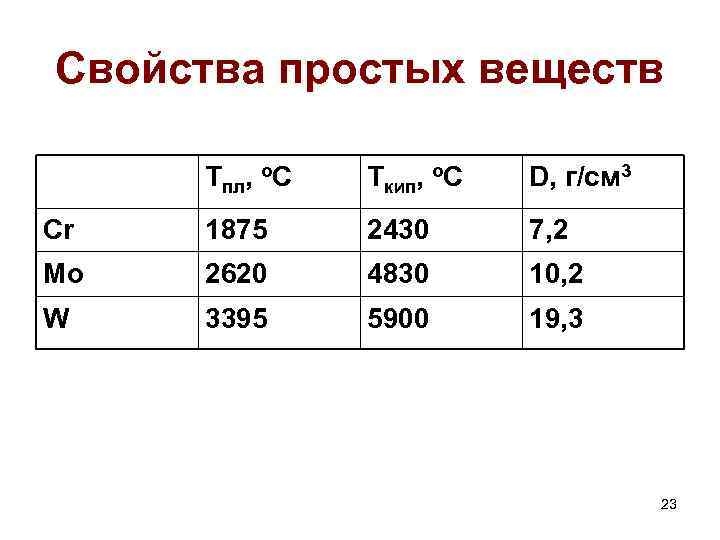 Свойства простых веществ Тпл, о. С Ткип, о. С D, г/см 3 Cr 1875 2430 7, 2 Mo 2620 4830 10, 2 W 3395 5900 19, 3 23
Свойства простых веществ Тпл, о. С Ткип, о. С D, г/см 3 Cr 1875 2430 7, 2 Mo 2620 4830 10, 2 W 3395 5900 19, 3 23
 Свойства простых веществ: Cr 1) Cr + 2 HCl = Cr. Cl 2 + H 2 Реакция в атм. Ar, голубой [Cr(H 2 O)6]2+ 2) 2 Cr +6 HCl + O 2 = 2 Cr. Cl 3 + H 2 +2 H 2 O Реакция на воздухе, зеленый [Cr(H 2 O)6]3+ 3) 2 Cr +6 H 2 SO 4 = Cr 2(SO 4)3 +3 SO 2 +6 H 2 O Конц. H 2 SO 4 окислитель 4) Конц. HNO 3 пассивирует поверхность 5) Щелочи пассивируют поверхность 24
Свойства простых веществ: Cr 1) Cr + 2 HCl = Cr. Cl 2 + H 2 Реакция в атм. Ar, голубой [Cr(H 2 O)6]2+ 2) 2 Cr +6 HCl + O 2 = 2 Cr. Cl 3 + H 2 +2 H 2 O Реакция на воздухе, зеленый [Cr(H 2 O)6]3+ 3) 2 Cr +6 H 2 SO 4 = Cr 2(SO 4)3 +3 SO 2 +6 H 2 O Конц. H 2 SO 4 окислитель 4) Конц. HNO 3 пассивирует поверхность 5) Щелочи пассивируют поверхность 24
 Свойства простых веществ: Mo, W Растворение металлов: W + 8 HF + 2 HNO 3 = H 2[WF 8] + 2 NO +4 H 2 O Mо + 3 Na. NO 3 + Na 2 CO 3 = Na 2 Mо. O 4 +3 Na. NO 2 +CO 2 2 W + 3 O 2 = 2 WO 3 Mo +2 S = Mo. S 2 25
Свойства простых веществ: Mo, W Растворение металлов: W + 8 HF + 2 HNO 3 = H 2[WF 8] + 2 NO +4 H 2 O Mо + 3 Na. NO 3 + Na 2 CO 3 = Na 2 Mо. O 4 +3 Na. NO 2 +CO 2 2 W + 3 O 2 = 2 WO 3 Mo +2 S = Mo. S 2 25
 Кислородные соединения Cr 6+ Cr. O 3 – темно-красный, разлагается выше 200 о. С, растворим в воде 4 Cr. O 3 = 2 Cr 2 O 3 + 3 O 2 Cr. O 3 + H 2 O = H 2 Cr. O 4 K 2 Cr 2 O 7 + 2 H 2 SO 4 конц= 2 Cr. O 3↓ + 2 KHSO 4 +H 2 O 26
Кислородные соединения Cr 6+ Cr. O 3 – темно-красный, разлагается выше 200 о. С, растворим в воде 4 Cr. O 3 = 2 Cr 2 O 3 + 3 O 2 Cr. O 3 + H 2 O = H 2 Cr. O 4 K 2 Cr 2 O 7 + 2 H 2 SO 4 конц= 2 Cr. O 3↓ + 2 KHSO 4 +H 2 O 26
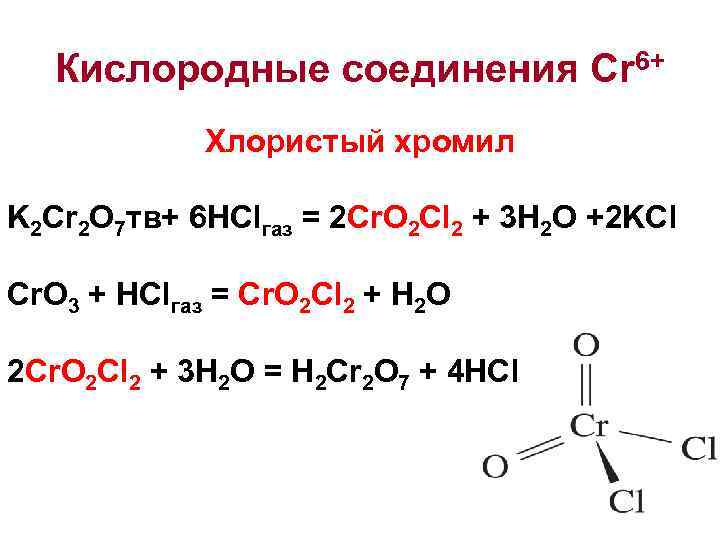 Кислородные соединения Cr 6+ Хлористый хромил K 2 Cr 2 O 7 тв+ 6 HClгаз = 2 Cr. O 2 Cl 2 + 3 H 2 O +2 KCl Cr. O 3 + HClгаз = Cr. O 2 Cl 2 + H 2 O 2 Cr. O 2 Cl 2 + 3 H 2 O = H 2 Cr 2 O 7 + 4 HCl 27
Кислородные соединения Cr 6+ Хлористый хромил K 2 Cr 2 O 7 тв+ 6 HClгаз = 2 Cr. O 2 Cl 2 + 3 H 2 O +2 KCl Cr. O 3 + HClгаз = Cr. O 2 Cl 2 + H 2 O 2 Cr. O 2 Cl 2 + 3 H 2 O = H 2 Cr 2 O 7 + 4 HCl 27
 Кислородные соединения Cr 6+ H 2 Cr. O 4 : Ka 1= 10 -1, Ka 2= 10 -7 H 2 Cr 2 O 7: Ka 2= 10 -2 Гидролиз солей: Cr. O 42 - - устойчив в щелочной среде (желтый) Cr 2 O 72 - устойчив в кислой среде (оранжевый) Cr 2 O 72 - + H 2 O = 2 Cr. O 42 - + 2 H+ 28
Кислородные соединения Cr 6+ H 2 Cr. O 4 : Ka 1= 10 -1, Ka 2= 10 -7 H 2 Cr 2 O 7: Ka 2= 10 -2 Гидролиз солей: Cr. O 42 - - устойчив в щелочной среде (желтый) Cr 2 O 72 - устойчив в кислой среде (оранжевый) Cr 2 O 72 - + H 2 O = 2 Cr. O 42 - + 2 H+ 28
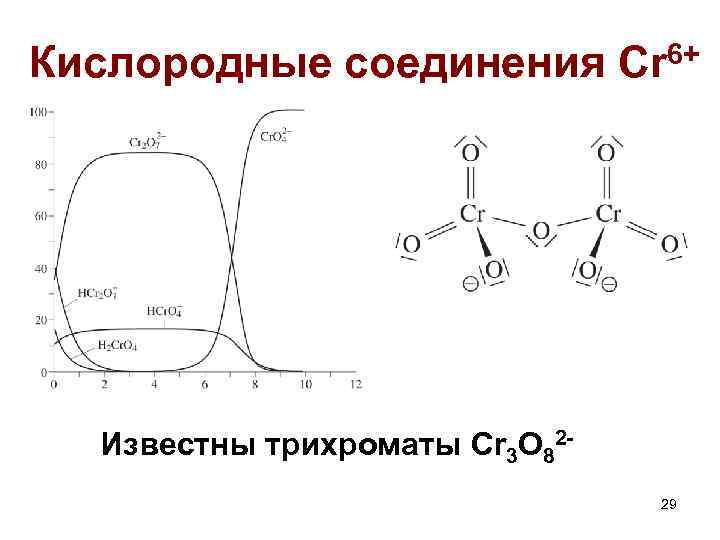 Кислородные соединения 6+ Cr Известны трихроматы Cr 3 O 8229
Кислородные соединения 6+ Cr Известны трихроматы Cr 3 O 8229
 Кислородные соединения 6+ Cr Соединения хрома(VI) гораздо более сильные окислители, чем соединения Mo и W 4 Cr. O 3 + C 2 H 5 OH = 2 Cr 2 O 3 + 2 CO 2 + 3 H 2 O (NH 4)2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4 H 2 O K 2 Cr 2 O 7 + 14 HClконц = 3 Cl 2 +2 Cr. Cl 3 + 7 H 2 O +2 KCl 30
Кислородные соединения 6+ Cr Соединения хрома(VI) гораздо более сильные окислители, чем соединения Mo и W 4 Cr. O 3 + C 2 H 5 OH = 2 Cr 2 O 3 + 2 CO 2 + 3 H 2 O (NH 4)2 Cr 2 O 7 = Cr 2 O 3 + N 2 + 4 H 2 O K 2 Cr 2 O 7 + 14 HClконц = 3 Cl 2 +2 Cr. Cl 3 + 7 H 2 O +2 KCl 30
 Кислородные соединения Cr 6+ В зависимости от p. H раствора Cr 2 O 72 - + 3 SO 32 - + 8 H+ = 2 Cr 3+ + 3 SO 42 - + 4 H 2 O 2 Cr. O 42 - + 3 SO 32 - + 5 H 2 O = 2 Cr(OH)3 + 3 SO 42 - + 4 OH 2 Cr. O 42 - + 3 Sn 2+ + 10 OH- + 8 H 2 O = 2[Cr(OH)4]- + 3[Sn(OH)6]2 - 31
Кислородные соединения Cr 6+ В зависимости от p. H раствора Cr 2 O 72 - + 3 SO 32 - + 8 H+ = 2 Cr 3+ + 3 SO 42 - + 4 H 2 O 2 Cr. O 42 - + 3 SO 32 - + 5 H 2 O = 2 Cr(OH)3 + 3 SO 42 - + 4 OH 2 Cr. O 42 - + 3 Sn 2+ + 10 OH- + 8 H 2 O = 2[Cr(OH)4]- + 3[Sn(OH)6]2 - 31
 Кислородные соединения +3 Cr Cr 2 O 3 – очень стабилен, зеленый пигмент в красках Не реагирует с водой, кислотами и р-рами щелочей Щелочной плавкой получают хромиты: Cr 2 O 3 + 2 Na. OHтв = 2 Na. Cr. O 2 + H 2 O Na. Cr. O 2 + 2 Na. OH + 2 H 2 O = Na 3[Cr(OH)6] 32
Кислородные соединения +3 Cr Cr 2 O 3 – очень стабилен, зеленый пигмент в красках Не реагирует с водой, кислотами и р-рами щелочей Щелочной плавкой получают хромиты: Cr 2 O 3 + 2 Na. OHтв = 2 Na. Cr. O 2 + H 2 O Na. Cr. O 2 + 2 Na. OH + 2 H 2 O = Na 3[Cr(OH)6] 32
 Гидрооксид Cr 3+ + 3 OH- = Cr(OH)3↓ - осторожное добавление щелочей или аммиака Стареет, свежеосажденный амфотерен: Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + Na. OH = Na[Cr(OH)4] 33
Гидрооксид Cr 3+ + 3 OH- = Cr(OH)3↓ - осторожное добавление щелочей или аммиака Стареет, свежеосажденный амфотерен: Cr(OH)3 + 3 HCl = Cr. Cl 3 + 3 H 2 O Cr(OH)3 + Na. OH = Na[Cr(OH)4] 33
 Соли Cr 3+ Хромовые квасцы KCr(SO 4)2. 12 H 2 O Многочисленные комплексы: Cr. Cl 3. 6 H 2 O – гидратная изомерия Соединение Цвет [Cr(H 2 O)6]Cl 3 фиолетовый [Cr(H 2 O)5 Cl]Cl 2. H 2 O Светло-зеленый [Cr(H 2 O)4 Cl 2]Cl. 2 H 2 O Темно-зеленый 34
Соли Cr 3+ Хромовые квасцы KCr(SO 4)2. 12 H 2 O Многочисленные комплексы: Cr. Cl 3. 6 H 2 O – гидратная изомерия Соединение Цвет [Cr(H 2 O)6]Cl 3 фиолетовый [Cr(H 2 O)5 Cl]Cl 2. H 2 O Светло-зеленый [Cr(H 2 O)4 Cl 2]Cl. 2 H 2 O Темно-зеленый 34
 Применение • Cr – коррозионностойкие стали, покрытия, инструменты • Mo – жаропрочные стали, нагреватели • W – нити накаливания, радиодетали 35
Применение • Cr – коррозионностойкие стали, покрытия, инструменты • Mo – жаропрочные стали, нагреватели • W – нити накаливания, радиодетали 35
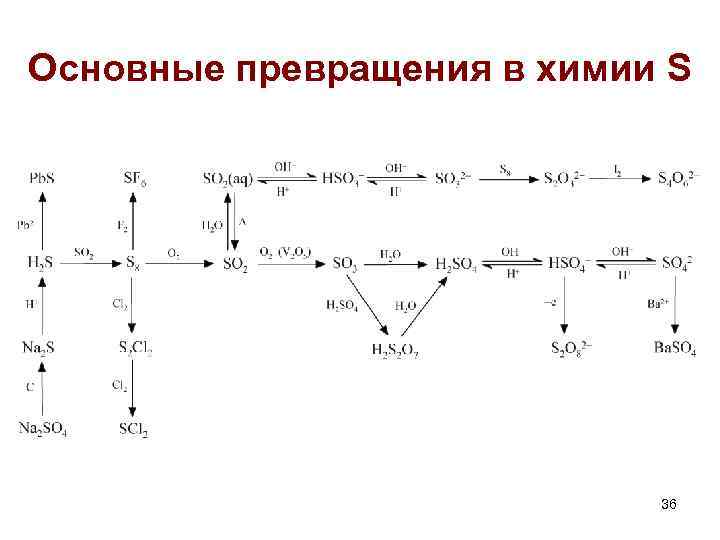 Основные превращения в химии S 36
Основные превращения в химии S 36


