 Сероводород. Сульфиды
Сероводород. Сульфиды
 Сероводород
Сероводород
 Сероводород в природе Входит в состав вулканических газов. Образуется при гниении белков. Встречается в минеральных источниках (Мацеста, Пятигорск, Кавказ).
Сероводород в природе Входит в состав вулканических газов. Образуется при гниении белков. Встречается в минеральных источниках (Мацеста, Пятигорск, Кавказ).
 Сероводород, сернистый водород (H 2 S) — бесцветный газ с резким запахом. Химическая формула H 2 S Отн. молек. масса 34. 082 а. е. м. Молярная масса 34. 082 г/моль Температура плавления -82. 30 °C Температура кипения -60. 28 °C Плотность вещества 1. 363 г/л г/см 3 Растворимость 0. 25 (40 °C) г/100 мл Состояние (ст. усл) бесцветный газ
Сероводород, сернистый водород (H 2 S) — бесцветный газ с резким запахом. Химическая формула H 2 S Отн. молек. масса 34. 082 а. е. м. Молярная масса 34. 082 г/моль Температура плавления -82. 30 °C Температура кипения -60. 28 °C Плотность вещества 1. 363 г/л г/см 3 Растворимость 0. 25 (40 °C) г/100 мл Состояние (ст. усл) бесцветный газ
 Физические свойства Газ, без цвета, с запахом тухлых яиц, ядовит (в больших концентрациях без запаха), тяжелее воздуха, растворим в воде (в 1 V H 2 O растворяется 2, 4 V H 2 S при н. у. ); t°пл = -86°C; t°кип = -60°С. Ядовит! Способен взаимодействовать с железом, входящим в гемоглобин крови. Работать с сероводородом в вытяжном шкафу и герметичных приборах!
Физические свойства Газ, без цвета, с запахом тухлых яиц, ядовит (в больших концентрациях без запаха), тяжелее воздуха, растворим в воде (в 1 V H 2 O растворяется 2, 4 V H 2 S при н. у. ); t°пл = -86°C; t°кип = -60°С. Ядовит! Способен взаимодействовать с железом, входящим в гемоглобин крови. Работать с сероводородом в вытяжном шкафу и герметичных приборах!
 Влияние сероводорода на организм Очень ядовит. Даже один вздох чистого сероводорода ведет к потере сознания из-за паралича дыхательного центра. Его коварство заключается в том, что после легкого отравления его запах перестает ощущаться. От сероводорода, выделяющегося при извержении Везувия, погиб в 79 г. до н. э. естествоиспытатель Плиний Старший.
Влияние сероводорода на организм Очень ядовит. Даже один вздох чистого сероводорода ведет к потере сознания из-за паралича дыхательного центра. Его коварство заключается в том, что после легкого отравления его запах перестает ощущаться. От сероводорода, выделяющегося при извержении Везувия, погиб в 79 г. до н. э. естествоиспытатель Плиний Старший.
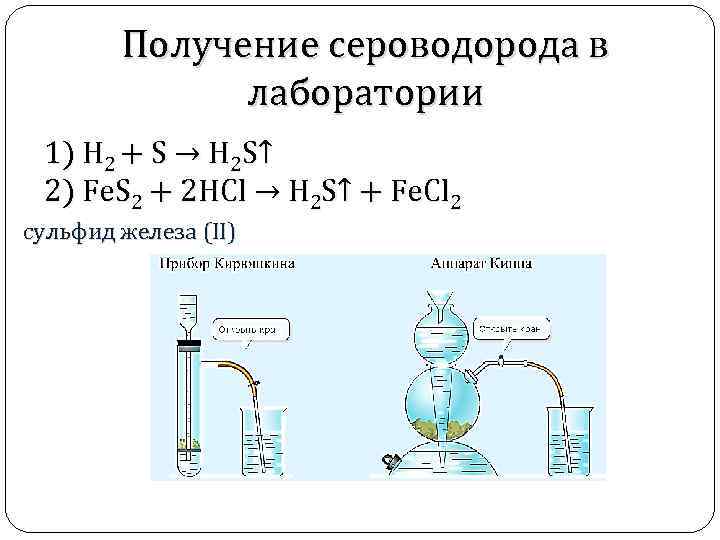 Получение сероводорода в лаборатории 1) H 2 + S → H 2 S↑ 2) Fe. S 2 + 2 HCl → H 2 S↑ + Fe. Cl 2 cульфид железа (II)
Получение сероводорода в лаборатории 1) H 2 + S → H 2 S↑ 2) Fe. S 2 + 2 HCl → H 2 S↑ + Fe. Cl 2 cульфид железа (II)
 Химические свойства сероводорода
Химические свойства сероводорода
 1) Горение сероводорода. Полное сгорание (при избытке O 2) 2 H 2 S-2 + 3 O 2 → 2 S+4 O 2 + 2 H 2 O Неполное сгорание (недостаток O 2) 2 H 2 S-2 + O 2 → 2 S 0 + 2 H 2 O
1) Горение сероводорода. Полное сгорание (при избытке O 2) 2 H 2 S-2 + 3 O 2 → 2 S+4 O 2 + 2 H 2 O Неполное сгорание (недостаток O 2) 2 H 2 S-2 + O 2 → 2 S 0 + 2 H 2 O
 2) Восстановительные свойства (с галогенами, солями, кислородом, кислотами). H 2 S-2 + Br 2 → S 0 + 2 HBr H 2 S-2 + 2 Fe. Cl 3 → 2 Fe. Cl 2 + S 0 + 2 HCl
2) Восстановительные свойства (с галогенами, солями, кислородом, кислотами). H 2 S-2 + Br 2 → S 0 + 2 HBr H 2 S-2 + 2 Fe. Cl 3 → 2 Fe. Cl 2 + S 0 + 2 HCl
 3) Взаимодействие с водой. Раствор H 2 S в воде – слабая двухосновная кислота (сероводородная кислота) Диссоциация происходит в две ступени: I ст. H 2 S⇄ H+ + HS- (гидросульфид - ион) II ст. HS- ⇄ H+ + S 2 - (сульфид-ион) Средние соли(сульфиды): Na 2 S – сульфид натрия Средние соли(сульфиды): Ca. S – сульфид кальция Кислые соли(гидросульфиды): Na. HS – гидросульфид натрия Ca(HS)2 – гидросульфид кальция
3) Взаимодействие с водой. Раствор H 2 S в воде – слабая двухосновная кислота (сероводородная кислота) Диссоциация происходит в две ступени: I ст. H 2 S⇄ H+ + HS- (гидросульфид - ион) II ст. HS- ⇄ H+ + S 2 - (сульфид-ион) Средние соли(сульфиды): Na 2 S – сульфид натрия Средние соли(сульфиды): Ca. S – сульфид кальция Кислые соли(гидросульфиды): Na. HS – гидросульфид натрия Ca(HS)2 – гидросульфид кальция
 4) Кислотные свойства. Взаимодействует с основаниями: H 2 S + 2 Na. OH изб. → Na 2 S + 2 H 2 O сульфид натрия H 2 S изб. + Na. OH → Na. HS + H 2 O гидросульфид натрия
4) Кислотные свойства. Взаимодействует с основаниями: H 2 S + 2 Na. OH изб. → Na 2 S + 2 H 2 O сульфид натрия H 2 S изб. + Na. OH → Na. HS + H 2 O гидросульфид натрия
 5) Качественная реакция на сероводородную кислоту и сульфиды. Н 2 S + Pb(NO 3)2 → Pb. S↓ + 2 HNO 3 Pb 2+ + S 2 - → Pb. S↓ черный H 2 S + Cu(NO 3)2 → Cu. S↓ + 2 HNO 3 Сu 2+ + S 2 - → Cu. S↓ черный
5) Качественная реакция на сероводородную кислоту и сульфиды. Н 2 S + Pb(NO 3)2 → Pb. S↓ + 2 HNO 3 Pb 2+ + S 2 - → Pb. S↓ черный H 2 S + Cu(NO 3)2 → Cu. S↓ + 2 HNO 3 Сu 2+ + S 2 - → Cu. S↓ черный
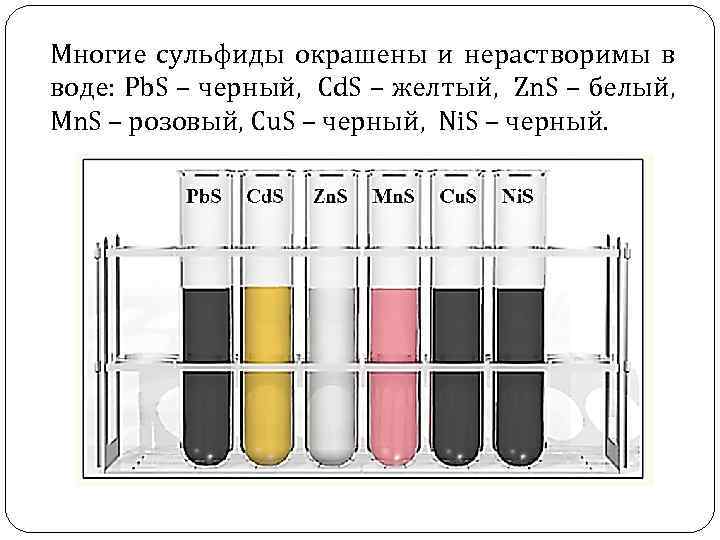 Многие сульфиды окрашены и нерастворимы в воде: Pb. S – черный, Cd. S – желтый, Zn. S – белый, Mn. S – розовый, Cu. S – черный, Ni. S – черный.
Многие сульфиды окрашены и нерастворимы в воде: Pb. S – черный, Cd. S – желтый, Zn. S – белый, Mn. S – розовый, Cu. S – черный, Ni. S – черный.
 Применение сероводорода Сероводород из-за своей токсичности находит ограниченное применение. Ø В медицине - в составе природных и искусственных сероводородных ванн (нормализует работу сердца и нервной системы, артериальное давление, используют при кожных заболеваниях. Ø Сероводород применяют для получения серной кислоты, серы, сульфидов.
Применение сероводорода Сероводород из-за своей токсичности находит ограниченное применение. Ø В медицине - в составе природных и искусственных сероводородных ванн (нормализует работу сердца и нервной системы, артериальное давление, используют при кожных заболеваниях. Ø Сероводород применяют для получения серной кислоты, серы, сульфидов.