 Сернистая кислота Н 2 SO 3 и Серная кислота Н 2 SO 4 Физические свойства и методы получения
Сернистая кислота Н 2 SO 3 и Серная кислота Н 2 SO 4 Физические свойства и методы получения
 Физические свойства Параметр сравнения Сернистая кислота Серная кислота Физические свойства Известна только в разбавленных водных растворах, растворы H 2 SO 3 всегда имеют резкий специфический запах Бесцветная, тяжелая, нелетучая маслянистая жидкость без запаха; при попадании на кожу, мгновенно разъедает её. Основность и сила кислоты Двухосновная кислота средней силы, ближе к слабым Двухосновная кислота сильная Диссоциация Ступенчатая, обратимая Ступенчатая, практически необратимая (по I ступени); обратимая (по II ступени); H 2 SO 3 ⇄ H 1+ + HSO 31– (I) K 1 = 1, 6∙ 10– 2 HSO 31– ⇄ H 1+ + SO 32– (II) K 2 = 6, 3∙ 10– 8 H 2 SO 4 → H 1+ + HSO 41– (I) K 1 = 1∙ 103 HSO 41– ⇄ H 1+ + SO 42– (II) К₂ = 1, 2∙ 10− 2
Физические свойства Параметр сравнения Сернистая кислота Серная кислота Физические свойства Известна только в разбавленных водных растворах, растворы H 2 SO 3 всегда имеют резкий специфический запах Бесцветная, тяжелая, нелетучая маслянистая жидкость без запаха; при попадании на кожу, мгновенно разъедает её. Основность и сила кислоты Двухосновная кислота средней силы, ближе к слабым Двухосновная кислота сильная Диссоциация Ступенчатая, обратимая Ступенчатая, практически необратимая (по I ступени); обратимая (по II ступени); H 2 SO 3 ⇄ H 1+ + HSO 31– (I) K 1 = 1, 6∙ 10– 2 HSO 31– ⇄ H 1+ + SO 32– (II) K 2 = 6, 3∙ 10– 8 H 2 SO 4 → H 1+ + HSO 41– (I) K 1 = 1∙ 103 HSO 41– ⇄ H 1+ + SO 42– (II) К₂ = 1, 2∙ 10− 2
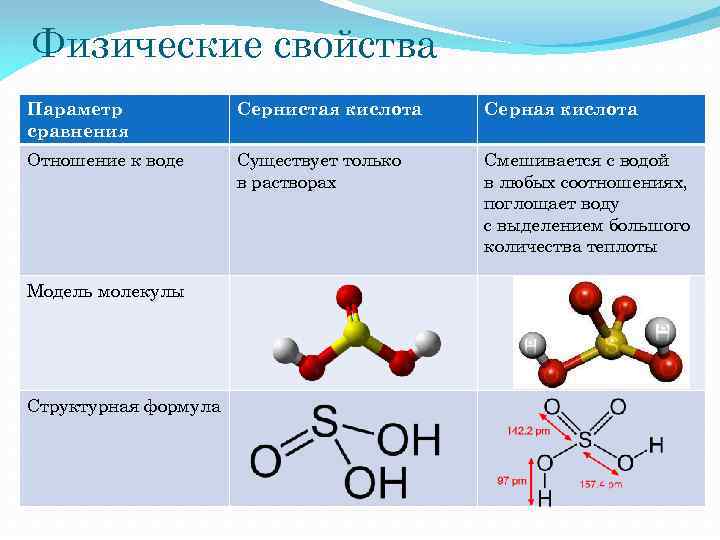 Физические свойства Параметр сравнения Сернистая кислота Серная кислота Отношение к воде Существует только в растворах Смешивается с водой в любых соотношениях, поглощает воду с выделением большого количества теплоты Модель молекулы Структурная формула
Физические свойства Параметр сравнения Сернистая кислота Серная кислота Отношение к воде Существует только в растворах Смешивается с водой в любых соотношениях, поглощает воду с выделением большого количества теплоты Модель молекулы Структурная формула
 Сопоставление силы сернистой и серной кислот Сернистая кислота Na 2 CO 3 + H 2 O + SO 2 → → Na 2 SO 3 + CO 2↑ + H 2 O Сернистая кислота – сильнее слабой угольной кислоты Na 2 SO 3 + 2 HCl → → 2 Na. Cl + SO 2↑ + H 2 O Na 2 SO 3 + H 2 SO 4 → → Na 2 SO 4 + SO 2↑ + H 2 O Сернистая кислота – слабее сильной соляной кислоты или серной кислоты Серная кислота Na 2 CO 3 + H 2 SO 4 → → Na 2 SO 4 + CO 2↑ + H 2 O Серная кислота – сильнее слабой угольной кислоты Ba. Cl 2 + H 2 SO 4 → → 2 HCl + Ba. SO 4↓ Ag 2 SO 4 + 2 HCl → → 2 Ag. Cl↓ + H 2 SO 4 Серная кислота – не слабее сильной соляной кислоты
Сопоставление силы сернистой и серной кислот Сернистая кислота Na 2 CO 3 + H 2 O + SO 2 → → Na 2 SO 3 + CO 2↑ + H 2 O Сернистая кислота – сильнее слабой угольной кислоты Na 2 SO 3 + 2 HCl → → 2 Na. Cl + SO 2↑ + H 2 O Na 2 SO 3 + H 2 SO 4 → → Na 2 SO 4 + SO 2↑ + H 2 O Сернистая кислота – слабее сильной соляной кислоты или серной кислоты Серная кислота Na 2 CO 3 + H 2 SO 4 → → Na 2 SO 4 + CO 2↑ + H 2 O Серная кислота – сильнее слабой угольной кислоты Ba. Cl 2 + H 2 SO 4 → → 2 HCl + Ba. SO 4↓ Ag 2 SO 4 + 2 HCl → → 2 Ag. Cl↓ + H 2 SO 4 Серная кислота – не слабее сильной соляной кислоты
 Методы получения Название метода Серная кислота Получение серной кислоты из железного купороса (1) термическое разложение сульфата железа 4 Fe. SO 4· 7 H 2 O → 2 Fe 2 O 3+ 4 SO 2 + 28 H 2 O+ O 2 (2) последующее охлаждение смеси 2 SO 2 + 2 H 2 O+ O 2 → 2 H 2 SO 4 Получение серной кислоты из сульфидов металлов (1) обжиг сульфидов 4 Fe. S + 7 O 2 → 2 Fe 2 O 3 + 4 SO 2 (t°C) (2) Каталитическое окисление сернистого газа кислородом воздуха 2 SO 2 + O 2 ⇄ 2 SO 3 (t°C, V 2 O 5 − катализатор) (3) Гидратация серного ангидрида – поглощение серного ангидрида раствором серной кислоты SO 3 + H 2 O → H 2 SO 4 Название метода Сернистая кислота Действие сильных кислот на сульфиты и гидросульфиты Практически сернистая кислота − раствор SO 2 в H 2 O Na 2 SO 3 + H 2 SO 4 → Na 2 SO 4 + H 2 O + SO 2↑
Методы получения Название метода Серная кислота Получение серной кислоты из железного купороса (1) термическое разложение сульфата железа 4 Fe. SO 4· 7 H 2 O → 2 Fe 2 O 3+ 4 SO 2 + 28 H 2 O+ O 2 (2) последующее охлаждение смеси 2 SO 2 + 2 H 2 O+ O 2 → 2 H 2 SO 4 Получение серной кислоты из сульфидов металлов (1) обжиг сульфидов 4 Fe. S + 7 O 2 → 2 Fe 2 O 3 + 4 SO 2 (t°C) (2) Каталитическое окисление сернистого газа кислородом воздуха 2 SO 2 + O 2 ⇄ 2 SO 3 (t°C, V 2 O 5 − катализатор) (3) Гидратация серного ангидрида – поглощение серного ангидрида раствором серной кислоты SO 3 + H 2 O → H 2 SO 4 Название метода Сернистая кислота Действие сильных кислот на сульфиты и гидросульфиты Практически сернистая кислота − раствор SO 2 в H 2 O Na 2 SO 3 + H 2 SO 4 → Na 2 SO 4 + H 2 O + SO 2↑
 Серная кислота – сильная кислота Взаимодействие разбавленной серной кислоты с металлами, основными и амфотерными оксидами, основаниями и амфотерными гидроксидами, солями
Серная кислота – сильная кислота Взаимодействие разбавленной серной кислоты с металлами, основными и амфотерными оксидами, основаниями и амфотерными гидроксидами, солями
 При взаимодействии с металлами серной кислоты разбавленной 1+ ионом-окислителем является протон Н , элементом-окислителем является Н+1. образуется сульфат металла и выделяется водород
При взаимодействии с металлами серной кислоты разбавленной 1+ ионом-окислителем является протон Н , элементом-окислителем является Н+1. образуется сульфат металла и выделяется водород
 Взаимодействие с металлами а) с активными металлами средней активности q Fe 0 + H+12 SO 4 разбавленная→ Fe+2 SO 4 + H 20↑ q Сr 0 + H+12 SO 4 разбавленная→ Cr+2 SO 4 + H 20↑ q Zn 0 + H+12 SO 4 разбавленная → Zn+2 SO₄ + H 20↑ q 2 H 1+ + Zn 0 → Zn 2+ + H 20↑ б) с неактивными металлами q H 2 SO 4 разб + Cu ≠
Взаимодействие с металлами а) с активными металлами средней активности q Fe 0 + H+12 SO 4 разбавленная→ Fe+2 SO 4 + H 20↑ q Сr 0 + H+12 SO 4 разбавленная→ Cr+2 SO 4 + H 20↑ q Zn 0 + H+12 SO 4 разбавленная → Zn+2 SO₄ + H 20↑ q 2 H 1+ + Zn 0 → Zn 2+ + H 20↑ б) с неактивными металлами q H 2 SO 4 разб + Cu ≠
 Взаимодействие с оксидами а) с основными оксидами q H 2 SO 4 разбавленная + Na₂O → H₂O + Na₂SO₄ q 2 H 1+ + Na₂O → 2 Na 1+ + H₂O б) с амфотерными оксидами q 3 H 2 SO 4 разбавленная + Al₂O₃ → 3 H₂O + Al₂(SO₄)₃ q 6 H 1+ + Al₂O₃ → 2 Al 3+ + 3 H₂O
Взаимодействие с оксидами а) с основными оксидами q H 2 SO 4 разбавленная + Na₂O → H₂O + Na₂SO₄ q 2 H 1+ + Na₂O → 2 Na 1+ + H₂O б) с амфотерными оксидами q 3 H 2 SO 4 разбавленная + Al₂O₃ → 3 H₂O + Al₂(SO₄)₃ q 6 H 1+ + Al₂O₃ → 2 Al 3+ + 3 H₂O
 Взаимодействие с гидроксидами а) со щелочами H 2 SO 4 разбавленная + 2 KOH → 2 H₂O + K₂SO₄ (избыток щелочи) H 1+ + OH 1− → H₂O H 2 SO 4 + KOH → KHSO 4 + H 2 O (избыток кислоты) 2 H 1+ + OH 1− → H₂O + HSO 41− б) с нерастворимыми основаниями H 2 SO 4 разбавленная + Cr(OH)2 → 2 H₂O + Cr. SO₄ 2 H 1+ + Cr(OH)2 → 2 H₂O + Cr 2+ в) с амфотерными гидроксидами 3 H 2 SO 4 разбавленная + 2 Cr(OH)₃ → 6 H₂O + Cr₂(SO₄)₃ 3 H 1+ + Cr(OH)₃ → 3 H₂O + Cr 3+
Взаимодействие с гидроксидами а) со щелочами H 2 SO 4 разбавленная + 2 KOH → 2 H₂O + K₂SO₄ (избыток щелочи) H 1+ + OH 1− → H₂O H 2 SO 4 + KOH → KHSO 4 + H 2 O (избыток кислоты) 2 H 1+ + OH 1− → H₂O + HSO 41− б) с нерастворимыми основаниями H 2 SO 4 разбавленная + Cr(OH)2 → 2 H₂O + Cr. SO₄ 2 H 1+ + Cr(OH)2 → 2 H₂O + Cr 2+ в) с амфотерными гидроксидами 3 H 2 SO 4 разбавленная + 2 Cr(OH)₃ → 6 H₂O + Cr₂(SO₄)₃ 3 H 1+ + Cr(OH)₃ → 3 H₂O + Cr 3+
 Взаимодействие с солями H 2 SO 4 разбавленная + Na 2 CO₃ → H₂O + CO₂↑ + Na₂SO₄ 2 H 1+ + CO 32− → H₂O + CO₂↑ H 2 SO 4 разбавленная + Fe. S → H₂S↑ + Fe. SO₄ 2 H 1+ + Fe. S → H₂S↑ + Fe 2+ H 2 SO 4 разбавленная + Ca. Si. O₃→ H 2 Si. O₃↓ + Ca. SO₄ 2 H 1+ + Ca. Si. O₃→ H 2 Si. O₃↓ + Ca 2+ H₂SO₄ разбавленная + Ba(NO₃)₂ → 2 HNO₃ + Ba. SO₄↓ SO₄2− + Ba 2+ → Ba. SO₄↓
Взаимодействие с солями H 2 SO 4 разбавленная + Na 2 CO₃ → H₂O + CO₂↑ + Na₂SO₄ 2 H 1+ + CO 32− → H₂O + CO₂↑ H 2 SO 4 разбавленная + Fe. S → H₂S↑ + Fe. SO₄ 2 H 1+ + Fe. S → H₂S↑ + Fe 2+ H 2 SO 4 разбавленная + Ca. Si. O₃→ H 2 Si. O₃↓ + Ca. SO₄ 2 H 1+ + Ca. Si. O₃→ H 2 Si. O₃↓ + Ca 2+ H₂SO₄ разбавленная + Ba(NO₃)₂ → 2 HNO₃ + Ba. SO₄↓ SO₄2− + Ba 2+ → Ba. SO₄↓
 Серная кислота – сильный окислитель Взаимодействие концентрированной серной кислоты с металлами, неметаллами ( S, P, C), сульфидами металлов Cu. S, Cu 2 S, Fe. S, пиритом Fe. S 2
Серная кислота – сильный окислитель Взаимодействие концентрированной серной кислоты с металлами, неметаллами ( S, P, C), сульфидами металлов Cu. S, Cu 2 S, Fe. S, пиритом Fe. S 2
 Отношение к металлам Взаимодействие концентрированной серной кислоты с металлами
Отношение к металлам Взаимодействие концентрированной серной кислоты с металлами
 При взаимодействии с металлами серной кислоты концентрированной ионом-окислителем является не протон Н 1+, а cульфат-анион 42–, элементом-окислителем SO является не Н+1, а S+6, образуется сульфат металла , продукты восстановления серы, вода водород не выделяется !
При взаимодействии с металлами серной кислоты концентрированной ионом-окислителем является не протон Н 1+, а cульфат-анион 42–, элементом-окислителем SO является не Н+1, а S+6, образуется сульфат металла , продукты восстановления серы, вода водород не выделяется !
 Отношениеконцентрированной серной кислоты к простым веществам-металлам а) металлы активныевосстанавливают серную кислоту до сероводорода : IA 8 Ме 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Me 2+1 SO 4 + H 2 S− 2↑ +4 H 2 O IA 8 Na 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Na 2+1 SO 4 + H 2 S− 2↑ +4 H 2 O IIA 4 Ме 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Me+2 SO 4 + H 2 S− 2↑ +4 H 2 O IIA 4 Мg 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Mg+2 SO 4 + H 2 S− 2↑ +4 H 2 O
Отношениеконцентрированной серной кислоты к простым веществам-металлам а) металлы активныевосстанавливают серную кислоту до сероводорода : IA 8 Ме 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Me 2+1 SO 4 + H 2 S− 2↑ +4 H 2 O IA 8 Na 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Na 2+1 SO 4 + H 2 S− 2↑ +4 H 2 O IIA 4 Ме 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Me+2 SO 4 + H 2 S− 2↑ +4 H 2 O IIA 4 Мg 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Mg+2 SO 4 + H 2 S− 2↑ +4 H 2 O
 Отношениеконцентрированной серной кислоты к простым веществам-металлам б) металлы средней активности восстанавливают серную кислоту до сернистого газа на холоду: Zn 0 + 2 H 2 S+6 O 4 концентрированная→ Zn+2 SO 4 + S+4 O 2↑ +2 H 2 O некоторые металлы средней активности пассивируются в холодной концентрированной серной кислоте Al 0 + H 2 S+6 O 4 концентрированная холодная ≠ Fe 0 + H 2 S+6 O 4 концентрированная холодная ≠ Cr 0 + H 2 S+6 O 4 концентрированная холодная ≠
Отношениеконцентрированной серной кислоты к простым веществам-металлам б) металлы средней активности восстанавливают серную кислоту до сернистого газа на холоду: Zn 0 + 2 H 2 S+6 O 4 концентрированная→ Zn+2 SO 4 + S+4 O 2↑ +2 H 2 O некоторые металлы средней активности пассивируются в холодной концентрированной серной кислоте Al 0 + H 2 S+6 O 4 концентрированная холодная ≠ Fe 0 + H 2 S+6 O 4 концентрированная холодная ≠ Cr 0 + H 2 S+6 O 4 концентрированная холодная ≠
 Отношениеконцентрированной серной кислоты к простым веществам-металлам б) металлы средней активности восстанавливают серную кислоту до сероводорода при нагревании: 4 Zn 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Zn+2 SO 4 + H 2 S− 2↑ +4 H 2 O некоторые металлы средней активности реагируют с горячей концентрированной серной кислотой 2 Al 0 + 6 H 2 S+6 O 4 концентрированная горячая → → Al+32(SO 4)3 + 3 S+4 O 2↑ +6 H 2 O 2 Fe 0 + 6 H 2 S+6 O 4 концентрированная горячая → → Fe+32(SO 4)3 + 3 S+4 O 2↑ +6 H 2 O 2 Cr 0 + 6 H 2 S+6 O 4 концентрированная горячая → → Cr+32(SO 4)3 + 3 S+4 O 2↑ +6 H 2 O
Отношениеконцентрированной серной кислоты к простым веществам-металлам б) металлы средней активности восстанавливают серную кислоту до сероводорода при нагревании: 4 Zn 0 + 5 H 2 S+6 O 4 концентрированная→ 4 Zn+2 SO 4 + H 2 S− 2↑ +4 H 2 O некоторые металлы средней активности реагируют с горячей концентрированной серной кислотой 2 Al 0 + 6 H 2 S+6 O 4 концентрированная горячая → → Al+32(SO 4)3 + 3 S+4 O 2↑ +6 H 2 O 2 Fe 0 + 6 H 2 S+6 O 4 концентрированная горячая → → Fe+32(SO 4)3 + 3 S+4 O 2↑ +6 H 2 O 2 Cr 0 + 6 H 2 S+6 O 4 концентрированная горячая → → Cr+32(SO 4)3 + 3 S+4 O 2↑ +6 H 2 O
 Отношениеконцентрированной серной кислоты к простым веществам-металлам в) некоторые неактивные металлы Hg, Ag) (Cu, восстанавливают серную кислоту до сернистого газа : Cu 0 + 2 H 2 S+6 O 4 концентрированная→ Cu+2 SO 4 + S+4 O 2↑ +2 H 2 O Hg 0 + 2 H 2 S+6 O 4 концентрированная→ Hg+2 SO 4 + S+4 O 2↑ +2 H 2 O 2 Ag 0 + 2 H 2 S+6 O 4 концентрированная→ Ag 2+1 SO 4 + S+4 O 2↑ +2 H 2 O другие неактивные металлы реагируют не с концентрированной серной кислотой ни на холоду, ни при нагревании Ме 0 + H 2 S+6 O 4 концентрированная ≠ Ме 0 = Au, Pt, Pd, Rh, Тa, Ir, W
Отношениеконцентрированной серной кислоты к простым веществам-металлам в) некоторые неактивные металлы Hg, Ag) (Cu, восстанавливают серную кислоту до сернистого газа : Cu 0 + 2 H 2 S+6 O 4 концентрированная→ Cu+2 SO 4 + S+4 O 2↑ +2 H 2 O Hg 0 + 2 H 2 S+6 O 4 концентрированная→ Hg+2 SO 4 + S+4 O 2↑ +2 H 2 O 2 Ag 0 + 2 H 2 S+6 O 4 концентрированная→ Ag 2+1 SO 4 + S+4 O 2↑ +2 H 2 O другие неактивные металлы реагируют не с концентрированной серной кислотой ни на холоду, ни при нагревании Ме 0 + H 2 S+6 O 4 концентрированная ≠ Ме 0 = Au, Pt, Pd, Rh, Тa, Ir, W
 Отношение к неметаллам Взаимодействие концентрированной и разбавленной серной кислоты с неметаллами S, P, C
Отношение к неметаллам Взаимодействие концентрированной и разбавленной серной кислоты с неметаллами S, P, C
 Взаимодействие разбавленной серной кислоты с неметаллами S, P, C S + H 2 SO 4 разбавленная ≠ C(тв. )+ H 2 SO 4 разбавленная ≠ P + H 2 SO 4 разбавленная ≠
Взаимодействие разбавленной серной кислоты с неметаллами S, P, C S + H 2 SO 4 разбавленная ≠ C(тв. )+ H 2 SO 4 разбавленная ≠ P + H 2 SO 4 разбавленная ≠
 Взаимодействие концентрированной серной кислоты с неметаллами S, P, C Окисление неметаллов: S 0(тв. )+ 2 H 2 S+6 O 4 (конц)→ 3 SO 2↑+2 H 2 O S 0 – восстановитель, H 2 SO 4 (конц) – окислитель восстановитель С 0 (тв. )+ 2 H 2 S+6 O 4 (конц) → 2 H 2 O + CO 2↑ + 2 SO 2↑ С 0 – восстановитель, H 2 SO 4 (конц) – окислитель восстановитель 2 P 0(тв. )+ 5 H 2 S+6 O 4 (конц) → 2 H 3 PO 4 + 5 SO 2↑+ 2 H 2 O P 0 – восстановитель, H 2 SO 4 (конц) - окислитель
Взаимодействие концентрированной серной кислоты с неметаллами S, P, C Окисление неметаллов: S 0(тв. )+ 2 H 2 S+6 O 4 (конц)→ 3 SO 2↑+2 H 2 O S 0 – восстановитель, H 2 SO 4 (конц) – окислитель восстановитель С 0 (тв. )+ 2 H 2 S+6 O 4 (конц) → 2 H 2 O + CO 2↑ + 2 SO 2↑ С 0 – восстановитель, H 2 SO 4 (конц) – окислитель восстановитель 2 P 0(тв. )+ 5 H 2 S+6 O 4 (конц) → 2 H 3 PO 4 + 5 SO 2↑+ 2 H 2 O P 0 – восстановитель, H 2 SO 4 (конц) - окислитель
 Взаимодействие серной кислоты разбавленной с сульфидами металлов Cu. S, Cu 2 S, Fe. S, пиритом Fe. S 2 Cu+12 S– 2 + H 2 SO 4(разб. )≠ Cu+2 S– 2 + H 2 SO 4(разб. )≠ Fe+2 S– 12 + H 2 SO 4(разб. )≠ Fe+2 S– 2 + H 2 SO 4(разб. ) → Fe+2 SO 4 + H 2 S– 2 ↑ − реакция обмена
Взаимодействие серной кислоты разбавленной с сульфидами металлов Cu. S, Cu 2 S, Fe. S, пиритом Fe. S 2 Cu+12 S– 2 + H 2 SO 4(разб. )≠ Cu+2 S– 2 + H 2 SO 4(разб. )≠ Fe+2 S– 12 + H 2 SO 4(разб. )≠ Fe+2 S– 2 + H 2 SO 4(разб. ) → Fe+2 SO 4 + H 2 S– 2 ↑ − реакция обмена
 Взаимодействие серной кислоты концентрированной с сульфидами металлов Cu. S, Cu 2 S, Fe. S, пиритом Fe. S 2 Cu+2 S– 2 + 4 H 2 S+6 O 4(конц. ) → Cu+2 SO 4 + 4 S+4 O 2↑ + 4 H 2 O (t ) Cu+12 S– 2 + 6 H 2 S+6 O 4(конц. )→ 2 Cu+2 SO 4 + 5 S+4 O 2↑ + 6 H 2 O (t ) 2 Fe+2 S– 2 +10 H 2 S+6 O 4(конц. )→ Fe 2+3(SO 4)3 + 9 S+4 O 2↑ +10 H 2 O 2 Fe+2 S– 12 + 14 H 2 S+6 O 4(конц. ) →Fe 2+3(SO 4)3 + 15 S+4 O 2↑ + 14 H 2 O В реакциях (3) и (4) не образуется Fe. SO 4 S– 2 − восстановитель, S+6 − окислитель (1) Cu+1, S– 2 − восстановители, S+6 − окислитель (2) Fe+2, S– 2− восстановители, S+6 − окислитель (3) Fe+2, S– 1 − восстановители, S+6 − окислитель (4) (1) (2) (3) (4)
Взаимодействие серной кислоты концентрированной с сульфидами металлов Cu. S, Cu 2 S, Fe. S, пиритом Fe. S 2 Cu+2 S– 2 + 4 H 2 S+6 O 4(конц. ) → Cu+2 SO 4 + 4 S+4 O 2↑ + 4 H 2 O (t ) Cu+12 S– 2 + 6 H 2 S+6 O 4(конц. )→ 2 Cu+2 SO 4 + 5 S+4 O 2↑ + 6 H 2 O (t ) 2 Fe+2 S– 2 +10 H 2 S+6 O 4(конц. )→ Fe 2+3(SO 4)3 + 9 S+4 O 2↑ +10 H 2 O 2 Fe+2 S– 12 + 14 H 2 S+6 O 4(конц. ) →Fe 2+3(SO 4)3 + 15 S+4 O 2↑ + 14 H 2 O В реакциях (3) и (4) не образуется Fe. SO 4 S– 2 − восстановитель, S+6 − окислитель (1) Cu+1, S– 2 − восстановители, S+6 − окислитель (2) Fe+2, S– 2− восстановители, S+6 − окислитель (3) Fe+2, S– 1 − восстановители, S+6 − окислитель (4) (1) (2) (3) (4)


