 Сера, селен и теллур
Сера, селен и теллур
 История открытия • Сера в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. Точно происхождение серы не установлено, этот элемент использовался до Рождества Христова, а значит знаком людям с давних времён. Впервые в литературе он описан у Агриколы. Элементарную природу серы установил А. Л. Лавуазье (1789) в своих опытах по сжиганию и включил ее в список неметаллических простых тел. В 1822 г. Э. Мичерлих обнаружил аллотропию серы. • Селен открыт Й. Я. Берцелиусом в 1817. рассказ самого Берцелиуса о том, как произошло это открытие: Я исследовал в содружестве с Готлибом Ганом метод, который применяют для производства серной кислоты в Грипсхольме. Мы обнаружили в серной кислоте осадок, частью красный, частью светло-коричневый. Этот осадок, опробованный с помощью паяльной трубки, издавал слабый редечный запах и образовывал свинцовый королёк. Согласно Клапроту, такой запах служит указанием на присутствие теллура. Ган заметил при этом, что на руднике в Фалуне, где собирается сера, необходимая для производства кислоты, также ощущается подобный запах, указывающий на присутствие теллура. Любопытство, вызванное надеждой обнаружить в этом коричневом осадке новый редкий металл, заставило меня исследовать осадок. Приняв намерение отделить теллур, я не смог, однако, открыть в осадке никакого теллура. Тогда я собрал всё, что образовалось при получении серной кислоты путём сжигания фалюнской серы за несколько месяцев, и подверг полученный в большом количестве осадок обстоятельному исследованию. Я нашёл, что масса (то есть осадок) содержит до сих пор неизвестный металл, очень похожий по своим свойствам на теллур. В соответствии с этой аналогией я назвал новое тело селеном (Selenium) от греческого σελήνη (луна), так как теллур назван по имени Tellus — нашей планеты • Теллур впервые был найден в 1782 году в золотоносных рудах Трансильвании горным инспектором Францом Иозефом Мюллером (впоследствии барон фон Рейхенштейн), на территории Австро-Венгрии. В 1798 году Мартин Генрих Клапрот выделил теллур и определил важнейшие его свойства.
История открытия • Сера в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. Точно происхождение серы не установлено, этот элемент использовался до Рождества Христова, а значит знаком людям с давних времён. Впервые в литературе он описан у Агриколы. Элементарную природу серы установил А. Л. Лавуазье (1789) в своих опытах по сжиганию и включил ее в список неметаллических простых тел. В 1822 г. Э. Мичерлих обнаружил аллотропию серы. • Селен открыт Й. Я. Берцелиусом в 1817. рассказ самого Берцелиуса о том, как произошло это открытие: Я исследовал в содружестве с Готлибом Ганом метод, который применяют для производства серной кислоты в Грипсхольме. Мы обнаружили в серной кислоте осадок, частью красный, частью светло-коричневый. Этот осадок, опробованный с помощью паяльной трубки, издавал слабый редечный запах и образовывал свинцовый королёк. Согласно Клапроту, такой запах служит указанием на присутствие теллура. Ган заметил при этом, что на руднике в Фалуне, где собирается сера, необходимая для производства кислоты, также ощущается подобный запах, указывающий на присутствие теллура. Любопытство, вызванное надеждой обнаружить в этом коричневом осадке новый редкий металл, заставило меня исследовать осадок. Приняв намерение отделить теллур, я не смог, однако, открыть в осадке никакого теллура. Тогда я собрал всё, что образовалось при получении серной кислоты путём сжигания фалюнской серы за несколько месяцев, и подверг полученный в большом количестве осадок обстоятельному исследованию. Я нашёл, что масса (то есть осадок) содержит до сих пор неизвестный металл, очень похожий по своим свойствам на теллур. В соответствии с этой аналогией я назвал новое тело селеном (Selenium) от греческого σελήνη (луна), так как теллур назван по имени Tellus — нашей планеты • Теллур впервые был найден в 1782 году в золотоносных рудах Трансильвании горным инспектором Францом Иозефом Мюллером (впоследствии барон фон Рейхенштейн), на территории Австро-Венгрии. В 1798 году Мартин Генрих Клапрот выделил теллур и определил важнейшие его свойства.

 Область применения • Сера применяется в первую очередь для получения серной кислоты: в бумажной промышленности (для получения сульфитцеллюлозы); в сельском хозяйстве (для борьбы с болезнями растений, главным образом винограда и хлопчатника); в резиновой промышленности (вулканизующий агент); в производстве красителей и светящихся составов; для получения чёрного (охотничьего) пороха; в производстве спичек. В медицинской практике применение Сера основано на её способности при взаимодействии с органическими веществами организма образовывать сульфиды и пентатионовую кислоту, от присутствия которых зависят кератолитические (растворяющие — от греч. kéras — рог и lytikós — растворяющий), противомикробные и противопаразитарные эффекты. • Селен потребляется главным образом при изготовлении выпрямителей переменного тока. • Теллур применяется в производстве свинцовых кабелей. Добавка его (до 0, 1%) к свинцу сильно повышает твердость и эластичность последнего Такой свинец оказывается также более стойким по отношению, к различным химическим воздействиям.
Область применения • Сера применяется в первую очередь для получения серной кислоты: в бумажной промышленности (для получения сульфитцеллюлозы); в сельском хозяйстве (для борьбы с болезнями растений, главным образом винограда и хлопчатника); в резиновой промышленности (вулканизующий агент); в производстве красителей и светящихся составов; для получения чёрного (охотничьего) пороха; в производстве спичек. В медицинской практике применение Сера основано на её способности при взаимодействии с органическими веществами организма образовывать сульфиды и пентатионовую кислоту, от присутствия которых зависят кератолитические (растворяющие — от греч. kéras — рог и lytikós — растворяющий), противомикробные и противопаразитарные эффекты. • Селен потребляется главным образом при изготовлении выпрямителей переменного тока. • Теллур применяется в производстве свинцовых кабелей. Добавка его (до 0, 1%) к свинцу сильно повышает твердость и эластичность последнего Такой свинец оказывается также более стойким по отношению, к различным химическим воздействиям.
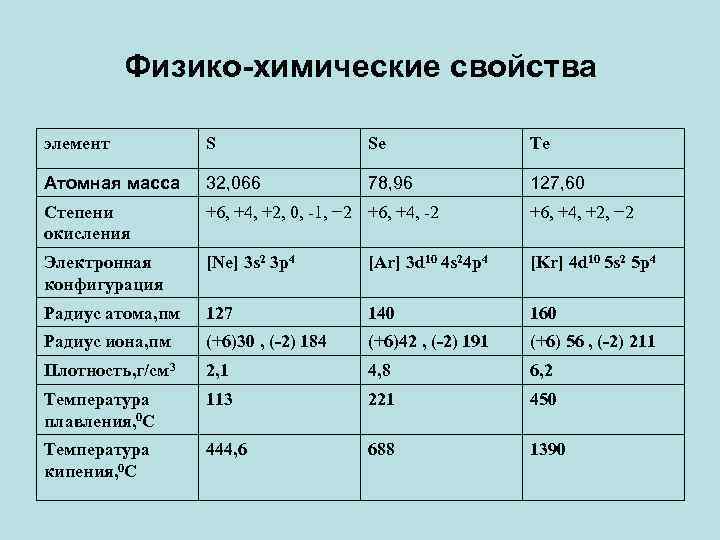 Физико-химические свойства элемент S Se Te Атомная масса 32, 066 78, 96 127, 60 Степени окисления +6, +4, +2, 0, -1, − 2 +6, +4, -2 +6, +4, +2, − 2 Электронная конфигурация [Ne] 3 s 2 3 p 4 [Ar] 3 d 10 4 s 24 p 4 [Kr] 4 d 10 5 s 2 5 p 4 Радиус атома, пм 127 140 160 Радиус иона, пм (+6)30 , (-2) 184 (+6)42 , (-2) 191 (+6) 56 , (-2) 211 Плотность, г/см 3 2, 1 4, 8 6, 2 Температура плавления, 0 С 113 221 450 Температура кипения, 0 С 444, 6 688 1390
Физико-химические свойства элемент S Se Te Атомная масса 32, 066 78, 96 127, 60 Степени окисления +6, +4, +2, 0, -1, − 2 +6, +4, -2 +6, +4, +2, − 2 Электронная конфигурация [Ne] 3 s 2 3 p 4 [Ar] 3 d 10 4 s 24 p 4 [Kr] 4 d 10 5 s 2 5 p 4 Радиус атома, пм 127 140 160 Радиус иона, пм (+6)30 , (-2) 184 (+6)42 , (-2) 191 (+6) 56 , (-2) 211 Плотность, г/см 3 2, 1 4, 8 6, 2 Температура плавления, 0 С 113 221 450 Температура кипения, 0 С 444, 6 688 1390
 • • • В обычных условиях сера c кислородом не взаимодействует. Лишь во влажной атмосфере она медленно окисляется кислородом с образованием следовых количеств SO 2. Температура воспламенения чистой серы в воздухе находится в пределах 280 -360°C. Примеси в сере значительно повышают температуру ее воспламенения. Пары серы, а также серная пыль в смеси с достаточным количеством воздуха, взрывоопасны. Сера горит голубоватым пламенем с образованием диоксида серы. Горение развивается по свободной поверхности при достижении температуры воспламенения. С водородом сера заметно взаимодействует уже при 150 -200°C с образованием H 2 S: S + H 2 = H 2 S. Сера взаимодействует почти со всеми металлами, образуя сульфиды. При комнатной температуре сера соединяется со щелочными и щелочноземельными (Mg, Ca, Sr, Ba) металлами, а также с Cu, Ag, Hg; при нагревании – с Fe, Pb, Sn, Ni, Co, Zn, Mn, Cr, Al. Тугоплавкие металлы и некоторые металлы платиновой группы взаимодействуют с серой при высокой температуре в мелкораздробленном состоянии; некоторые – с парами серы под давлением. Следует отметить, что с ростом температуры активность серы резко возрастает. И дело не только в том, что с ростом температуры возрастает количество молекул, способных преодолеть энергетический барьер реакции – энергию активации.
• • • В обычных условиях сера c кислородом не взаимодействует. Лишь во влажной атмосфере она медленно окисляется кислородом с образованием следовых количеств SO 2. Температура воспламенения чистой серы в воздухе находится в пределах 280 -360°C. Примеси в сере значительно повышают температуру ее воспламенения. Пары серы, а также серная пыль в смеси с достаточным количеством воздуха, взрывоопасны. Сера горит голубоватым пламенем с образованием диоксида серы. Горение развивается по свободной поверхности при достижении температуры воспламенения. С водородом сера заметно взаимодействует уже при 150 -200°C с образованием H 2 S: S + H 2 = H 2 S. Сера взаимодействует почти со всеми металлами, образуя сульфиды. При комнатной температуре сера соединяется со щелочными и щелочноземельными (Mg, Ca, Sr, Ba) металлами, а также с Cu, Ag, Hg; при нагревании – с Fe, Pb, Sn, Ni, Co, Zn, Mn, Cr, Al. Тугоплавкие металлы и некоторые металлы платиновой группы взаимодействуют с серой при высокой температуре в мелкораздробленном состоянии; некоторые – с парами серы под давлением. Следует отметить, что с ростом температуры активность серы резко возрастает. И дело не только в том, что с ростом температуры возрастает количество молекул, способных преодолеть энергетический барьер реакции – энергию активации.
 • • • Сульфаты и сульфиды являются обычными продуктами высокотемпературных эндогенных процессов, тогда как сульфиты в геологических обстановках, связанных с высокотемпературными эндогенными процессами, практически не встречаются. Скорее всего, это обусловлено тем, что сульфиты являются сильными восстановителями, при первой возможности окисляясь в сульфаты. Кроме того, в высокотемпературных условиях протекает реакция разложения сульфитов с одновременным образованием сульфидов и сульфатов. В состав природных сульфатов входят щелочные (Na, K) и щелочноземельные (Mg, Ca, Sr, Ba) металлы, а также Pb, Cu, Fe, Al. Значительная часть сульфатов – основные и водные соли. В тетраэдрическом анионе [SO 4]2– сера находится в высшей степени окисления. Для сульфатов характерен ионный тип связи. В основных и водных сульфатах велика роль водородных связей. Изовалентные и гетеровалентные замещения носят ограниченный характер. Совершенный изоморфизм установлен только между баритом Ba. SO 4 и целестином Sr. SO 4. В барите, кроме того, Ba 2+ нередко замещается ионами Pb 2+ и Ra 2+. Широкие замещения между катионами развиты в водных сульфатах Fe, Cu, Zn. Сера относится к халькофильным и биофильным элементам
• • • Сульфаты и сульфиды являются обычными продуктами высокотемпературных эндогенных процессов, тогда как сульфиты в геологических обстановках, связанных с высокотемпературными эндогенными процессами, практически не встречаются. Скорее всего, это обусловлено тем, что сульфиты являются сильными восстановителями, при первой возможности окисляясь в сульфаты. Кроме того, в высокотемпературных условиях протекает реакция разложения сульфитов с одновременным образованием сульфидов и сульфатов. В состав природных сульфатов входят щелочные (Na, K) и щелочноземельные (Mg, Ca, Sr, Ba) металлы, а также Pb, Cu, Fe, Al. Значительная часть сульфатов – основные и водные соли. В тетраэдрическом анионе [SO 4]2– сера находится в высшей степени окисления. Для сульфатов характерен ионный тип связи. В основных и водных сульфатах велика роль водородных связей. Изовалентные и гетеровалентные замещения носят ограниченный характер. Совершенный изоморфизм установлен только между баритом Ba. SO 4 и целестином Sr. SO 4. В барите, кроме того, Ba 2+ нередко замещается ионами Pb 2+ и Ra 2+. Широкие замещения между катионами развиты в водных сульфатах Fe, Cu, Zn. Сера относится к халькофильным и биофильным элементам
 Распространенность в земной коре Сера является шестнадцатым по химической распространённости элементом в земной коре. В свободном (самородном) состоянии встречается чаще всего сера а селен и теллур изредка. В виде соединении их встречаются на много больше чем в самородном виде.
Распространенность в земной коре Сера является шестнадцатым по химической распространённости элементом в земной коре. В свободном (самородном) состоянии встречается чаще всего сера а селен и теллур изредка. В виде соединении их встречаются на много больше чем в самородном виде.
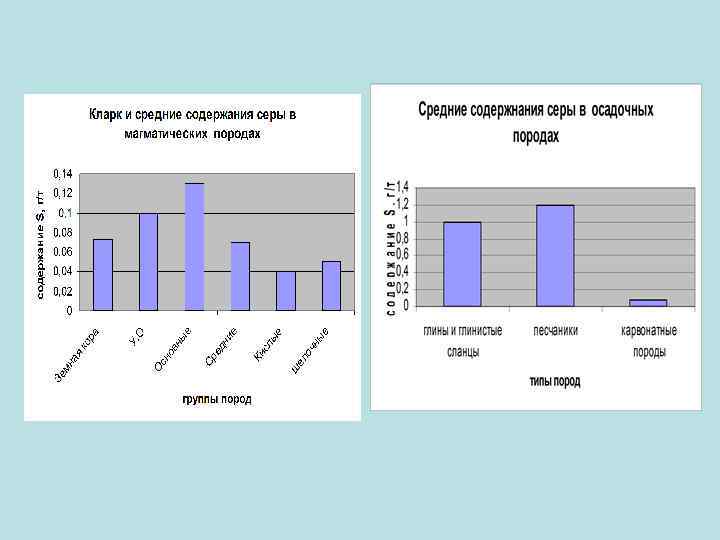
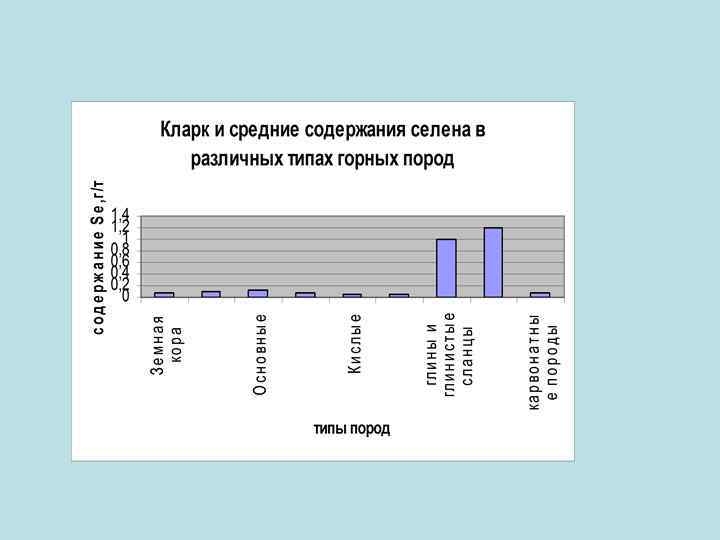
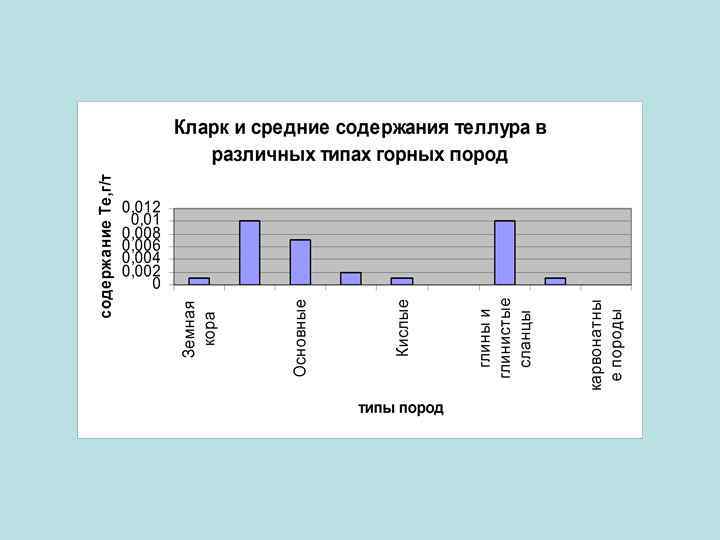
 Основные минералы-носители элемента Большие скопления самородной серы встречаются не так уж часто. Чаще она присутствует в минералах (сульфиды - 40 минералов и сульфаты): Fe. S 2 — железный колчедан или пирит, Zn. S — цинковая обманка или сфалерит (вюрцит), Pb. S — свинцовый блеск или галенит, Hg. S — киноварь, Sb 2 S 3 — антимонит(стибнит), Ca. SO 4 – ангидрит, Ba. SO 4 - барит, Sr. SO 4 целестин, Pb. SO 4 –англезит и т. д. • Селен образует 37 минералов, среди которых в первую очередь должны быть отмечены ашавалит Fe. Se, клаусталит Pb. Se, тиманнит Hg. Se, гуанахуатит Bi 2(Se, S)3, хастит Co. Se 2, платинит Pb. Bi 2(S, Se)3, ассоциирующие с различными сульфидами, а иногда также с касситеритом.
Основные минералы-носители элемента Большие скопления самородной серы встречаются не так уж часто. Чаще она присутствует в минералах (сульфиды - 40 минералов и сульфаты): Fe. S 2 — железный колчедан или пирит, Zn. S — цинковая обманка или сфалерит (вюрцит), Pb. S — свинцовый блеск или галенит, Hg. S — киноварь, Sb 2 S 3 — антимонит(стибнит), Ca. SO 4 – ангидрит, Ba. SO 4 - барит, Sr. SO 4 целестин, Pb. SO 4 –англезит и т. д. • Селен образует 37 минералов, среди которых в первую очередь должны быть отмечены ашавалит Fe. Se, клаусталит Pb. Se, тиманнит Hg. Se, гуанахуатит Bi 2(Se, S)3, хастит Co. Se 2, платинит Pb. Bi 2(S, Se)3, ассоциирующие с различными сульфидами, а иногда также с касситеритом.
 • Известно около 100 минералов теллура. Наиболее часты теллуриды меди, свинца, цинка, серебра и золота. Изоморфная примесь теллура наблюдается во многих сульфидах, однако изоморфизм Te — S выражен хуже, чем в ряду Se — S, и в сульфиды входит ограниченная примесь теллура. Среди минералов теллура особое значение имеют алтаит Pb. Te, сильванит Ag. Au. Te 4, калаверит Au. Te 2, гессит Ag 2 Te, креннерит (Au, Ag)Te, петцит Ag 2 Au. Te 2, мутманнит (Ag, Au)Te, монбрейит Au 2 Te 3, нагиагит [Pb 5 Au(Te, Sb)]4 S 5, тетрадимит Bi 2 Te 2 S. Встречаются кислородные соединения теллура, например Те. О 2 — теллуровая охра. Встречается самородный теллур и вместе с селеном и серой (японская теллуристая сера содержит 0, 17 % Те и 0, 06 % Se).
• Известно около 100 минералов теллура. Наиболее часты теллуриды меди, свинца, цинка, серебра и золота. Изоморфная примесь теллура наблюдается во многих сульфидах, однако изоморфизм Te — S выражен хуже, чем в ряду Se — S, и в сульфиды входит ограниченная примесь теллура. Среди минералов теллура особое значение имеют алтаит Pb. Te, сильванит Ag. Au. Te 4, калаверит Au. Te 2, гессит Ag 2 Te, креннерит (Au, Ag)Te, петцит Ag 2 Au. Te 2, мутманнит (Ag, Au)Te, монбрейит Au 2 Te 3, нагиагит [Pb 5 Au(Te, Sb)]4 S 5, тетрадимит Bi 2 Te 2 S. Встречаются кислородные соединения теллура, например Те. О 2 — теллуровая охра. Встречается самородный теллур и вместе с селеном и серой (японская теллуристая сера содержит 0, 17 % Те и 0, 06 % Se).
 Формы нахождения и поведение в водной и воздушной средах, участие в биологическом круговороте • • Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обуславливает «постоянную» жёсткость пресной воды. Сера — один из биогенных элементов. Сера входит в состав некоторых аминокислот (цистеин, метионин), витаминов (биотин, тиамин), ферментов. Сера участвует в образовании третичной структуры белка (формирование дисульфидных мостиков). Также сера участвует в бактериальном фотосинтезе (сера входит в состав бактериохлорофилла, а сероводород является источником водорода). Окислительно-восстановительные реакции серы — источник энергии в хемосинтезе. Человек содержит примерно 2 г серы на 1 кг своего веса. Концентрация селена в морской воде 4× 10 -4 мг/л. Входит в состав активных центров некоторых белков в форме аминокислоты селеноцистеина. Микроэлемент, но большинство соединений достаточно токсично (селеноводород, селеновая и селенистая кислота) даже в средних концентрациях. Микроколичества теллура всегда содержатся в живых организмах, его биологическая роль не выяснена. Теллур и его летучие соединения токсичны
Формы нахождения и поведение в водной и воздушной средах, участие в биологическом круговороте • • Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обуславливает «постоянную» жёсткость пресной воды. Сера — один из биогенных элементов. Сера входит в состав некоторых аминокислот (цистеин, метионин), витаминов (биотин, тиамин), ферментов. Сера участвует в образовании третичной структуры белка (формирование дисульфидных мостиков). Также сера участвует в бактериальном фотосинтезе (сера входит в состав бактериохлорофилла, а сероводород является источником водорода). Окислительно-восстановительные реакции серы — источник энергии в хемосинтезе. Человек содержит примерно 2 г серы на 1 кг своего веса. Концентрация селена в морской воде 4× 10 -4 мг/л. Входит в состав активных центров некоторых белков в форме аминокислоты селеноцистеина. Микроэлемент, но большинство соединений достаточно токсично (селеноводород, селеновая и селенистая кислота) даже в средних концентрациях. Микроколичества теллура всегда содержатся в живых организмах, его биологическая роль не выяснена. Теллур и его летучие соединения токсичны
 месторождение • • • Самородная сера встречается в верхней земной коры и на её поверхности при разложении сернистых соединении металлов и гипсоносных осадочных толщ. Главное промышленное значение на селен имеют сульфидные месторождения. Содержание селена в сульфидах колеблется от 7 до 110 г/т. Большая часть упомянутых минералов теллура развита в низкотемпературных золото-серебряных месторождениях, где они обычно выделяются после основной массы сульфидов совместно с самородным золотом, сульфосолями серебра, свинца, а также с минералами висмута. Несмотря на развитие большого числа теллуровых минералов, главная масса теллура, извлекаемого промышленностью, входит в состав сульфидов других металлов. В частности, теллур в несколько меньшей степени, чем селен, входит в состав халькопирита медно-никелевых месторождений магматического происхождения, а также халькопирита, развитого в медноколчеданных гидротермальных месторождениях. Теллур находится также в составе пирита, халькопирита, молибденита и галенита месторождений порфировых медных руд, полиметаллических месторождений алтайского типа, галенита свинцово-цинковых месторождений, связанных со скарнами, сульфидно-кобальтовых, сурьмяно-ртутных и некоторых других. Содержание теллура в молибдените колеблется в пределах 8 — 53 г/т, в халькопирите 9 — 31 г/т, в пирите до 70 г/т.
месторождение • • • Самородная сера встречается в верхней земной коры и на её поверхности при разложении сернистых соединении металлов и гипсоносных осадочных толщ. Главное промышленное значение на селен имеют сульфидные месторождения. Содержание селена в сульфидах колеблется от 7 до 110 г/т. Большая часть упомянутых минералов теллура развита в низкотемпературных золото-серебряных месторождениях, где они обычно выделяются после основной массы сульфидов совместно с самородным золотом, сульфосолями серебра, свинца, а также с минералами висмута. Несмотря на развитие большого числа теллуровых минералов, главная масса теллура, извлекаемого промышленностью, входит в состав сульфидов других металлов. В частности, теллур в несколько меньшей степени, чем селен, входит в состав халькопирита медно-никелевых месторождений магматического происхождения, а также халькопирита, развитого в медноколчеданных гидротермальных месторождениях. Теллур находится также в составе пирита, халькопирита, молибденита и галенита месторождений порфировых медных руд, полиметаллических месторождений алтайского типа, галенита свинцово-цинковых месторождений, связанных со скарнами, сульфидно-кобальтовых, сурьмяно-ртутных и некоторых других. Содержание теллура в молибдените колеблется в пределах 8 — 53 г/т, в халькопирите 9 — 31 г/т, в пирите до 70 г/т.

 Спасибо за внимание
Спасибо за внимание


