 Сера
Сера
 Цели урока ü Охарактеризовать серу в свете трёх форм существования элемента: в форме атомов, простых веществ (аллотропия), а также некоторых соединений серы. ü Химические свойства серы рассмотреть в свете ОВР.
Цели урока ü Охарактеризовать серу в свете трёх форм существования элемента: в форме атомов, простых веществ (аллотропия), а также некоторых соединений серы. ü Химические свойства серы рассмотреть в свете ОВР.
 План изучения 1. Положение серы в ПСХЭ 2. Строение атома, возможные степени окисления 3. Физические свойства серы 4. Нахождение в природе 5. Аллотропия серы 6. Химические свойства серы 7. Применение серы 8. Закрепление
План изучения 1. Положение серы в ПСХЭ 2. Строение атома, возможные степени окисления 3. Физические свойства серы 4. Нахождение в природе 5. Аллотропия серы 6. Химические свойства серы 7. Применение серы 8. Закрепление
 Положение серы в периодической системе химических элементов Д. И. Менделеева
Положение серы в периодической системе химических элементов Д. И. Менделеева
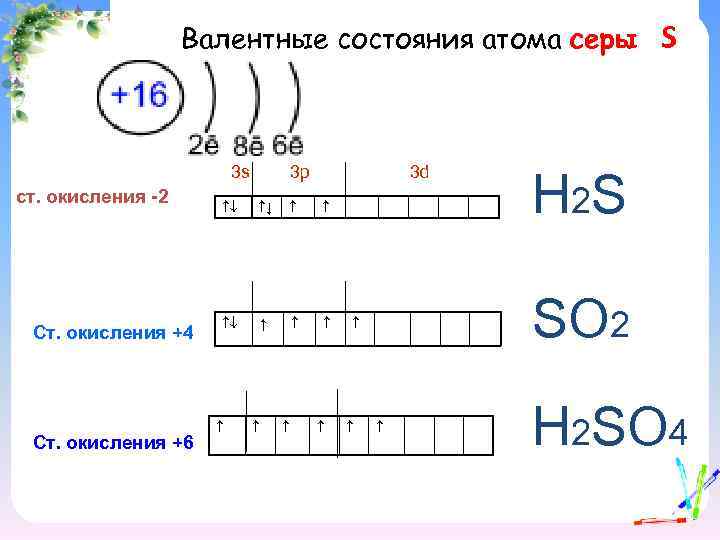 Валентные состояния атома серы 3 s ст. окисления -2 Ст. окисления +4 Ст. окисления +6 3 p 3 d ↓ ↑ Н 2 S SО 2 S Н 2 SО 4
Валентные состояния атома серы 3 s ст. окисления -2 Ст. окисления +4 Ст. окисления +6 3 p 3 d ↓ ↑ Н 2 S SО 2 S Н 2 SО 4
 Физические свойства серы • Твёрдое кристаллическое вещество желтого цвета, без запаха • Плохо проводит теплоту и не проводит электрический ток • Сера в воде практически не растворяется • Температура плавления 1200 С
Физические свойства серы • Твёрдое кристаллическое вещество желтого цвета, без запаха • Плохо проводит теплоту и не проводит электрический ток • Сера в воде практически не растворяется • Температура плавления 1200 С
 Нахождение серы в природе Сера является на 16 -м месте по распространённости в земной коре. Встречается в свободном (самородном) состоянии и связанном виде.
Нахождение серы в природе Сера является на 16 -м месте по распространённости в земной коре. Встречается в свободном (самородном) состоянии и связанном виде.
 Сера также встречается в виде сульфатов - солей серной кислоты мирабилит
Сера также встречается в виде сульфатов - солей серной кислоты мирабилит
 Пирит – «огненный камень» (соединение серы в природе)
Пирит – «огненный камень» (соединение серы в природе)
 Сера в природе Сера входит в состав белков. Особенно много серы в белках волос, рогов, шерсти. Кроме этого сера является составной частью биологически активных веществ: витаминов и гормонов. При недостатке серы в организме наблюдается хрупкость и ломкость костей, выпадение волос.
Сера в природе Сера входит в состав белков. Особенно много серы в белках волос, рогов, шерсти. Кроме этого сера является составной частью биологически активных веществ: витаминов и гормонов. При недостатке серы в организме наблюдается хрупкость и ломкость костей, выпадение волос.
 Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца
Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца
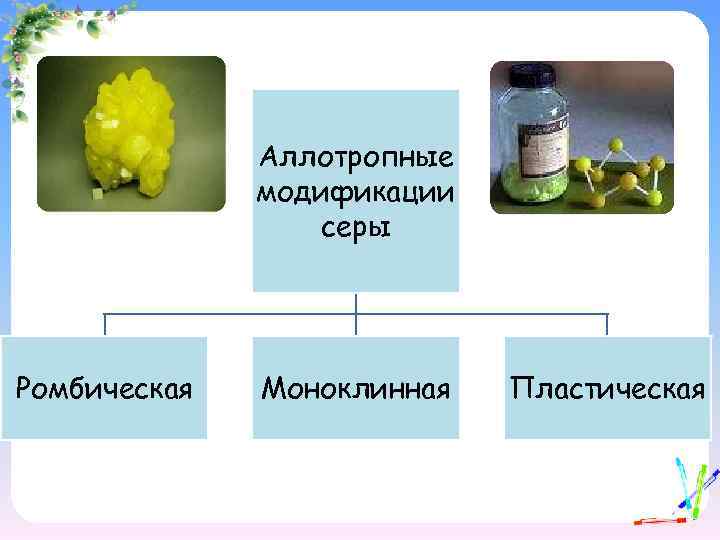 Аллотропные модификации серы Ромбическая Моноклинная Пластическая
Аллотропные модификации серы Ромбическая Моноклинная Пластическая
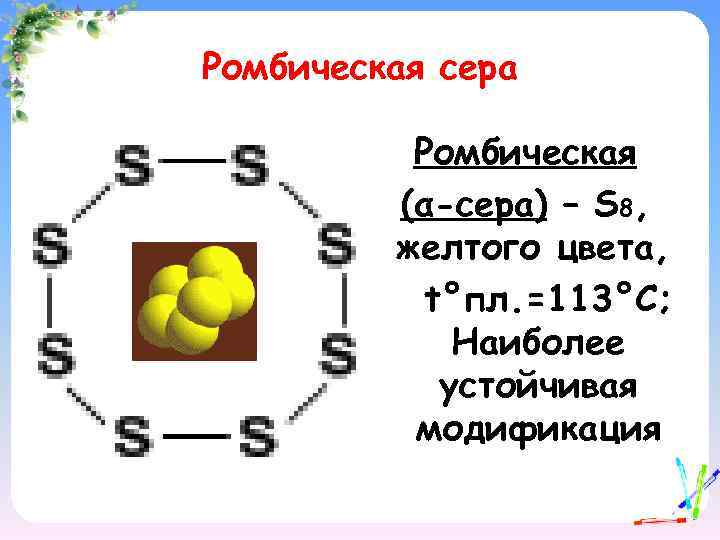 Ромбическая сера Ромбическая (α-сера) – S 8, желтого цвета, t°пл. =113°C; Наиболее устойчивая модификация
Ромбическая сера Ромбическая (α-сера) – S 8, желтого цвета, t°пл. =113°C; Наиболее устойчивая модификация
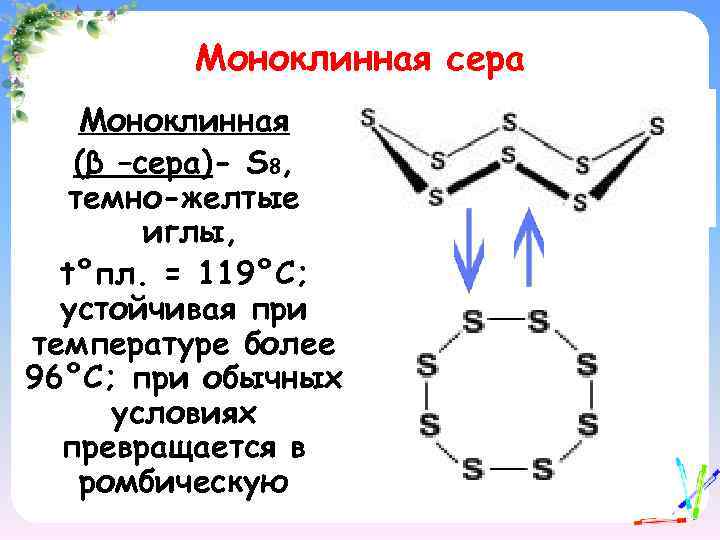 Моноклинная сера Моноклинная (β –сера)- S 8, темно-желтые иглы, t°пл. = 119°C; устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую
Моноклинная сера Моноклинная (β –сера)- S 8, темно-желтые иглы, t°пл. = 119°C; устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую
 Пластическая серакоричневая резиноподобная (аморфная) масса. Она неустойчива и через некоторое время становится хрупкой, приобретёт желтый цвет, т. е превращается в ромбическую серу
Пластическая серакоричневая резиноподобная (аморфная) масса. Она неустойчива и через некоторое время становится хрупкой, приобретёт желтый цвет, т. е превращается в ромбическую серу
 Химические свойства серы (восстановительные) Сера проявляет в реакциях с сильными окислителями: S - 2ē S+2; S - 4ē S+4; S - 6ē S+6 1) C кислородом: S + O 2 t S+4 O 2 2 S + 3 O 2 t ; Рt 2 S+6 O 3 2) С галогенами (кроме йода) S + Cl 2 S+2 Cl 2 3) С кислотами - окислителями: S + 2 H 2 SO 4(конц) 3 S+4 O 2 + 2 H 2 O S + 6 HNO 3(конц) H 2 S+6 O 4 + 6 NO 2 + 2 H 2 O
Химические свойства серы (восстановительные) Сера проявляет в реакциях с сильными окислителями: S - 2ē S+2; S - 4ē S+4; S - 6ē S+6 1) C кислородом: S + O 2 t S+4 O 2 2 S + 3 O 2 t ; Рt 2 S+6 O 3 2) С галогенами (кроме йода) S + Cl 2 S+2 Cl 2 3) С кислотами - окислителями: S + 2 H 2 SO 4(конц) 3 S+4 O 2 + 2 H 2 O S + 6 HNO 3(конц) H 2 S+6 O 4 + 6 NO 2 + 2 H 2 O
 Химические свойства серы (окислительные) S 0 + 2ē S-2 4) Сера реагирует со щелочными металлами без нагревания: 2 Na + S Na 2 S c остальными металлами (кроме Au, Pt) - при повышенной t : 2 Al + 3 S –t Al 2 S 3 Cu + S –t Cu. S 5) С некоторыми неметаллами сера образует бинарные соединения: H 2 + S H 2 S 2 P + 3 S P 2 S 3 C + 2 S CS 2
Химические свойства серы (окислительные) S 0 + 2ē S-2 4) Сера реагирует со щелочными металлами без нагревания: 2 Na + S Na 2 S c остальными металлами (кроме Au, Pt) - при повышенной t : 2 Al + 3 S –t Al 2 S 3 Cu + S –t Cu. S 5) С некоторыми неметаллами сера образует бинарные соединения: H 2 + S H 2 S 2 P + 3 S P 2 S 3 C + 2 S CS 2
 Применение серы Производство спичек Медицина Производство резины Сельское хозяйство Производство серной кислоты Производство взрывчатых веществ Красители
Применение серы Производство спичек Медицина Производство резины Сельское хозяйство Производство серной кислоты Производство взрывчатых веществ Красители
 Напишите уравнения реакций S → SO 2 → SO 3 → H 2 SO 4 →CASO 4
Напишите уравнения реакций S → SO 2 → SO 3 → H 2 SO 4 →CASO 4

 Домашнее задание § 22, упр. 1 -3
Домашнее задание § 22, упр. 1 -3


