Сепсис обзор.ppt
- Количество слайдов: 90

Сепсис новорождённых Шабалов Н. П. Военно-медицинская академия Кафедра детских болезней им. М. С. Маслова

Инфекции – распространенные причины заболеваемости и смертности новорождённых. До 2% новорожденных инфицируются внутриутробно (преимущественно в родах), 10% - на первом месяце жизни. Барбара Дж. Столл (Barbara J. Stoll) «Педиатрия по Нельсону» , 2009 (Nelson Textbook of Pediatrics, 2004) Частота первичного неонатального сепсиса составляет 1 – 5 на 1000 живорождённых. Заболеваемость гораздо выше у детей с ОНМТ с ранним началом сепсиса у 15 -19 на 1000 и поздним началом внутрибольничного сепсиса у 21% по данным Национального института развития ребенка США. Триция Гомелла (Tricia Gomella) и соавт. , 2015 По данным Г. А. Самсыгиной (2014) частота раннего неонатального сепсиса в разных регионах России в 2013 году составляла 1, 0 -3, 5‰, а позднего у детей со сроком гестации менее 25 недель - 46‰, 25 -28 недель - 29‰, 29 -32 недели - 10‰, а с гестационным возрастом более 32 недель – 2%. По нашим расчетам в Санкт-Петербурге в 2013 заболеваемость неонатальным сепсисом составила 1, 5 на

ИНФЕКЦИОННЫЕ БОЛЕЗНИ, СПЕЦИФИЧНЫЕ ДЛЯ ПЕРИНАТАЛЬНОГО ПЕРИОДА МКБ (P 35 -P 39) Включено: инфекции, приобретенные внутриутробно или во время родов • P 35 Врожденные вирусные инфекции • P 35. 0 Синдром врожденной краснухи • P 35. 1 Врожденная цитомегаловирусная инфекция • P 35. 2 Врожденная инфекция, вызванная вирусом простого герпеса [herpes simplex] • P 35. 3 Врожденный вирусный гепатит • P 35. 8 Другие врожденные вирусные инфекции • P 35. 9 Врожденная вирусная болезнь неуточненная

МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ БОЛЕЗНЕЙ 10 -го пересмотра • P 36 Бактериальный сепсис новорожденного Включено: врожденная септицемия • P 36. 0 Сепсис новорожденного, обусловленный стрептококком группы B • P 36. 1 Сепсис новорожденного, обусловленный другими и неуточненными стрептококками • P 36. 2 Сепсис новорожденного, обусловленный золотистым стафилококком [Staphylococcus aureus] • P 36. 3 Сепсис новорожденного, обусловленный другими и неуточненными стафилококками • P 36. 4 Сепсис новорожденного, обусловленный кишечной палочкой [Escherichia coli] • P 36. 5 Сепсис новорожденного, обусловленный анаэробными микроорганизмами • P 36. 8 Сепсис новорожденного, обусловленный другими бактериальными агентами

МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ БОЛЕЗНЕЙ 10 -го пересмотра • P 38 Омфалит новорожденного с небольшим кровотечением или без него • P 39 Другие инфекционные болезни, специфичные для перинатального периода • P 39. 0 Неонатальный инфекционный мастит • P 39. 1 Конъюнктивит и дакриоцистит у новорожденного Исключено: гонококковый конъюнктивит (A 54. 3) • P 39. 2 Внутриамниотическая инфекция плода, не классифицированная в других рубриках (ВАИ) • P 39. 3 Неонатальная инфекция мочевых путей • P 39. 4 Неонатальная инфекция кожных покровов Исключено: • – пузырчатка новорожденного (L 00) • – синдром стафилококкового ожога кожи в виде ожогоподобных пузырей (L 00) • P 39. 8 Другая уточненная инфекция, специфичная для перинатального периода • P 39. 9 Инфекция, специфичная для перинатального периода, не уточненная (ИСПП)

Терминология • Ранний неонатальный сепсис (РНС) (передающийся вертикальным путем) = ВАИ (Р 39. 2 по МКБ Х), ИСПП (Р 39. 8 по МКБ Х)? первые 72 ч. жизни; • Поздний неонатальный сепсис (ПНС, передающийся горизонтальным путем) = госпитальный? ! - >72 ч. ; • Очень поздний неонатальный сепсис = госпитальный или приобретенный в обществе – после второй недели жизни.

Всегда ли ПНС является следствием госпитального инфицирования, а РНС – материнского? Нет • Наиболее очевидные примеры: ПНС вследствие стрептококковой В инфекции и листериоза • РНС вследствие стафилококковой инфекции у детей с ОНМТ и ЭНМТ при эпидемиологическом неблагополучии в роддоме

«О сепсисе можно говорить Михаил Степанович Маслов (1885 – 1961) тогда, когда бактериемия интенсивная или длительная, когда прорывы в кровяное русло из очага происходят повторно, когда организм не в состоянии противодействовать прорывам, не в состоянии обезвреживать микробов и когда в организме создаются какие-то благоприятные условия для оседания и размножения микробов в определенных органах и тканях. Следовательно, развитие сепсиса возможно при наличии инфекционного очага, с одной стороны, и своеобразной реактивности детского организма, с другой стороны» .

• • Ипполит Васильевич Давыдовский (1887— 1968) «Громадная роль инфекта при сепсисе очевидна. Но в то же время ясно, что сепсис обуславливается не столько какими-нибудь особенностями микроба, сколько особенностями самой реакции организма. Если стрептококк, этот самый частый возбудитель сепсиса, вызывает еще чаще абсцесс, флегмону, рожу, скарлатину и т. д. , то это происходит, разумеется, не потому что существуют стрептококки септические, флегмонозные, рожистые, скарлатинозные, а потому, что реакции организма на стрептококк исключительно разнообразны. Таким образом, мы логически приходим к выводу, что ПРОБЛЕМА СЕПСИСА ЕСТЬ ПРОБЛЕМА ПРЕЖДЕ ВСЕГО МАКРОБИОЛОГИЧЕСКАЯ» ( И. В. Давыдовский, 1938)

Эдуард Кузьмич Цыбулькин 1938 -2001

Развитие взглядов на ведущее патогенетическое звено при сепсисе прошло несколько этапов (Цыбулькин Э. К. , 2001): 1. Начало века - патогенный микроорганизм. 2. С 20 -х годов - реакция Санарелли-Шварцмана. 3. 50 -е годы - эндотоксинемия. 4. 60 -х годов - реакция макроорганизма. 5. 70 -е годы - активация комплемента и нейтрофилов. 6. 80 -е годы - цитокины и метаболиты арахидоновой кислоты. 7. 90 -е годы - межклеточные взаимоотношения, регулируемые этапным включением медиаторов воспаления и иммуномодуляторов (синдром системного воспалительного ответа!).

Термин «синдром системного воспалительного ответа» (ССВО) – systemic inflammatory response syndrome (SIRS) введен в клиническую практику в 1991 году на конференция американской коллегии торакальных хирургов (АССР) и общества медицины критических состояний (SCCM). Критериями наличия ССВО у взрослых по предложению конференции являются: Температура тела выше 38 о. С или ниже 36 о. С Тахикардия выше 90 ударов в минуту Тахипноэ свыше 20 в минуту Количество лейкоцитов >12 х109/л, <4 х109/л, а число молодых форм превышает 10% Варианты течения сепсиса по мнению участников конференции: • Сепсис = SIRS (ССВО) + инфекция • Тяжелый сепсис = сепсис с органной дисфункцией, гипоперфузией или гипотензией • Септический шок = сепсис с артериальной гипотензией, несмотря на адекватной волемическое возмещение Целесообразность включения в определение сепсиса понятия ССВО была аргументирована обнаружением в крови больного сепсисом избытка провоспалительных цитокинов, хотя была также очевидна и неспецифичность ССВО. Последний может быть при любом экстремальном состоянии: анафилактическом шоке, ожогах, тяжелых гипоксии, гиповолемии, травмах и др. .
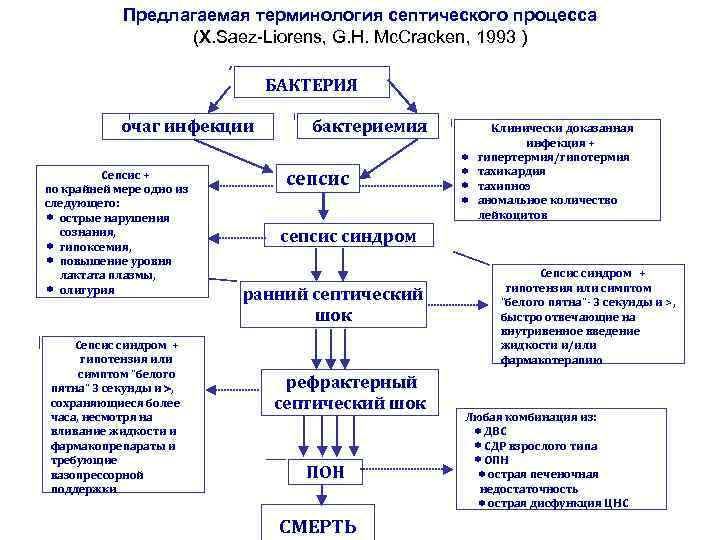
Предлагаемая терминология септического процесса (Х. Saez-Liorens, G. H. Mc. Cracken, 1993 ) БАКТЕРИЯ очаг инфекции Сепсис + по крайней мере одно из следующего: острые нарушения сознания, гипоксемия, повышение уровня лактата плазмы, олигурия Сепсис синдром + гипотензия или симптом “белого пятна” 3 секунды и , сохраняющиеся более часа, несмотря на вливание жидкости и фармакопрепараты и требующие вазопрессорной поддержки бактериемия сепсис Клинически доказанная инфекция + гипертермия/гипотермия тахикардия тахипноэ аномальное количество лейкоцитов сепсис синдром ранний септический шок рефрактерный септический шок ПОН СМЕРТЬ Сепсис синдром + гипотензия или симптом “белого пятна”- 3 секунды и >, быстро отвечающие на внутривенное введение жидкости и/или фармакотерапию Любая комбинация из: ДВС СДР взрослого типа ОПН острая печеночная недостаточность острая дисфункция ЦНС

Определение термина сепсис Сепсис – ациклическое инфекционное заболевание (т. е. без лечения приводящее к смерти), в основе которого лежит дисфункция фагоцитарномакрофагальной системы и неадекватный системный воспалительный ответ иммунокомпромиссного организма на бактериальную, как правило, условно патогенную (чаще госпитальную) инфекцию. Сепсис характеризуется генерализованным повреждением эндотелия сосудистого русла, интоксикацией, расстройствами гемостаза с обязательным рассеянным внутрисосудистым свертыванием крови или ДВС-синдромом и дальнейшей полиорганной недостаточностью.


Патогенез и фазовое течение сепсиса (А), причины дисциркуляции (Б) при септическом шоке ( «Сепсис» /Под ред. В. С. Савельева, Б. Р. Гельфанда, М. , МИА, 2010): м/о – микроорганизмы; ССВО – синдром системного воспалительного ответа; DO 2 – доставка кислорода; СВ – сердечный выброс; ССС – системное сосудистое сопротивление Sv. O 2; – насыщение венозной крови кислородом; O 2 ER – экстракция кислорода; ПОН – полиорганная недостаточность

Диагностические критерии сепсиса 2001 SCCM/ESICM/ACCP/ATS/SIS международная конференция по дефиниции сепсиса (Levy M. M. et al. , Crit. Care VTd. , 2003, vol. 31, № 4, p. 1250 -1256) Первостепенные консенсусные точки • Существующие концепции сепсиса, тяжелого сепсиса и септического шока выглядят здравыми и должны оставаться такими какими описаны 10 лет назад. • Существующие определения не позволяют точно выявлять стадии ответа макроорганизма на инфекцию. • Признаки и симптомы сепсиса значительно изменились по сравнению с теми что были первоначально установлены в 1991 году. • Будущее лежит в развитии системы стадийности, которая будет характеризовать прогрессирование сепсиса. Новая система PIRO предположительно будет характеризовать и определять стадии ответа хозяина на инфекцию.

Диагностические критерии сепсиса Инфекция документированная или предполагаемая и несколько из представленных ниже симптомов (Crit. Care Med. 2013; 41: 580 -637) Общие симптомы • Лихорадка (температура более 38, 3 С) • Гипотермия (температура менее 36, 5 С). • Частота сердечных сокращений более 2 квадратичных отклонений от нормы • Тахипное более 2 квадратичных отклонений от нормы • Изменение ментального статуса (оценка по шкале ком Глазго < 11) • Значительный отек или задержка жидкости более 20 мл/кг в течение 24 часов • Гипергликемия (глюкоза плазмы крови более 120 мг/дл. или 7, 7 ммоль/л) в отсутствии диабета Показатели воспаления • Лейкоцитоз (число лейкоцитов более 12 000/мкл) • Лейкопения (число лейкоцитов менее 4 000/мкл) • Более чем 10% лейкоцитов представлены незрелыми клетками • С-реактивный белок плазмы крови превышает нормальные значения на 2 квадратичных отклонения Прокальциотонин плазмы крови превышает нормальные значения на 2 квадратичных отклонения Гемодинамические показатели • Артериальная гипотензия АД на 2 квадратичных отклонения от возрастной нормы Признаки органной дисфункции • Артериальная гипоксемия (Pa. O 2/Fi. O 2 <300) • Острая олигурия (диурез менее 0, 5 мл/кг в час или мочевина более 45 ммоль/л в течение по крайней мере 4 часов креатинин крови выше 2 квадратичных отклонений от нормы ) • Коагуляционные нарушения (МНО > 1, 5, а АЧТВ > 60 с)) • Парез кишечника • Тромбоцитопения (число тромбоцитов менее 100 000/мкл) • Гипербилирубинемия (общий билирубин более 4 мг/дл. или 70 ммоль/л) • Признаки нарушения тканевой перфузии • Гиперлактатемия (более 4 ммоль/л в артериальной крови) • Уменьшение капиллярного наполнения или появление симптома белого пятна более 5 секунд

Диагностические критерии сепсиса у детей (Crit. Care Med. 2013; 41: 580 -637) Наличие инфекционного процесса с с системными проявлениями воспаления в сочетании: • с гипер- или гипотермией; • тахикардией + не менее одного из проявлений органных дисфункций; • нарушение сознания; • гипоксемия; • повышение сывороточного лактата; • вариабельный пульс.

Концепция PIRO • Predisposition (предрасположенность) • Infection (инфекция) • Response (реакция) • Возраст, генетические факторы, сопутствующие заболевания, иммуносупрессивная терапия и др. • Локализация очага инфекции, возбудитель инфекции • Клинические проявления инфекционного процесса (температура тела, ЧСС, уровень лейкоцитоза, концентрация С-реактивного белка, прокальцитонина и др. ) • Organ dysfunction (органная • Для оценки степени органной дисфункции используют разные дисфункция) шкалы, например, SOFA

Наиболее существенные факторы высокого риска РНС: 1. Смерть предыдущих детей в семье от системных бактериальных инфекций в возрасте до 3 -х месяцев (подозрение на наследственный иммунодефицит) 1. Смерть предыдущего ребенка от стрептококковой В инфекции 2. Многочисленные аборты в анамнезе* 3. Хориоамнионит*, многоводие, наличие околоплодных вод с запахом*, околоплодные воды в виде «горохового супа» 4. Хронические очаги инфекции, прежде всего в урогенитальной сфере*, желудочно-кишечном тракте 5. Клинически выраженные бактериальные инфекционные процессы у матери непосредственно до родов и в родах* 6. Клинически выявленный бактериальный вагиноз у матери* 7. Обнаружение у матери в родовых путях стрептококка В или его антигенов* 9. Безводный промежуток более 12 часов* 10. Рождение ребенка с очень низкой и особенно экстремально низкой массой тела * Факторы высокого риска ВАИ

Наиболее существенные факторы высокого риска ПНС: 1. Рождение с ОНМТ и особенно с ЭНМТ) 2. Асфиксия при рождении или другая патология потребовавшая реанимационных пособий и длительного воздержания от энтерального питания 3. Хирургические операции особенно с обширным травмированием тканей 4. Врожденные пороки развития с поврежденными кожными покровами ожоги 5. Многодневные катетеризации пупочной и центральных вен, дефицитное питание 6. Внутриутробные инфекции (ВУИ) 7. Множественные пороки развития или более 5 стигм дизэмбриогенеза 8. Длительные и массивные курсы антибактериальной терапии у новорождённых. 9. Использование схем де-эскалационной терапии в первую неделю жизни

При международной неопределённости критериев диагностики раннего неонатального сепсиса A. L. Anderson-Berry et all. (2010) пишут, что 7 -13% новорождённых США получают антибиотики в связи с предположительным диагнозом неонатальный сепсис, но подтверждение диагноза происходит лишь у 3 -8% детей. Установлено, что один документированный случай сепсиса приходится на 11 -23 случаев, когда новорожденным назначают лечение, исходя из подозрения на наличие сепсиса (Gerdes J. S. , 1991).

Инфекционная заболеваемость новорожденных в ОРИТН ДГБ № 1 (2013) (Хрусталева Н. М. ) • Сепсис 40 (~ 3%) • Внутриутробная инфекция 50 бактериальная— код МКБ — Р 37. 8 -9 2 вирусная — код МКБ — 35. 1 -. . . 8 48 • ВАИ код МКБ Р. 39. 2 291 • ИТПП код МКБ — Р 39. 9, Р 39. 8 101 • ИТОГО: 405 (~ 30%)

Клинические критерии SIRS у новорожденных: 1. Расстройство температурного гомеостата (гипертермия или гипотермия) 2. Одышка или тахипное более 50 в 1 минуту (у детей на ИВЛ – р. СО 2 менее 32 мм. рт. ст. ) 3. Тахикардия более 180 в 1 минуту или брадикардия менее 100 в 1 минуту 4. Утрата коммуникабельности анорексия угнетение и/или судороги 5. Олигурия (диурез менее 0, 5 мл/кг/час в сутки или в течение 6 часов менее 1, 0 мл/кг/час на фоне адекватной инфузионной терапии)

Посев крови • Чувствительность при сепсисе 25 -48% и отрицательные результаты не могут гарантировать отсутствие бактериемии • Причины: повреждение бактерий антибиотиками или факторами иммунной защиты, при бактериальной транслокации – гепатоэнтерогенная циркуляция бактерий без проникновения их в системный кровоток. • Посев не позволяет выявить концентрацию химических субстанций бактериального происхождения, а именно они играют решающую роль в запуске воспалительного каскада (Н. В. Белобородова, 2006). • Согласно Marshall J. , Sweeney D. (Arch. Surg. , 1990, 121, 1, 17 -22) у больных с хирургическим сепсисом при отрицательной гемокультуре летальность была выше, чем у больных с доказанной бактериемией.

Лабораторные признаки SIRS у новорожденных: 1. Внезапно возникший тяжелый метаболический лактат-ацидоз с гипокапнией (последнее при отсутствии поражения легких) 2. Лейкоцитоз (кол-во лейкоцитов у детей первого дня жизни >30000, 2 -7 дней >20000 и старше >15000 в 1 мкл капиллярной крови) или лейкопения (кол-во лейкоцитов в 1 мкл крови в 1 -ый день жизни <6000 и далее <5000) с нейтрофилезом (количество нейтрофилов в 1 мкл капиллярной крови у детей первого дня жизни >20000 2 -7 дней >10000 и 8 дней и старше >7000) или нейтропения (соответственно в указанные выше дни число нейтрофилов <5000 2000, и 1500)

Лабораторные признаки SIRS у новорожденных: 3. Регенераторный или регенераторнодегенеративный сдвиг лейкоцитарной формулы при числе палочкоядерных и более молодых форм >500. в мкл (в первый день жизни >2000 в мкл) 4. Токсическая зернистость нейтрофилов 5. Лимфоцитопения (менее 3000 в первую неделю жизни и менее 2000 в дальнейшем) 6. Тромбоцитопения 7. Анемия

Лабораторные признаки SIRS у новорожденных: 8. Внезапно возникшее укорочение или удлинение активированного частичного тромбопластинового времени (АЧТВ) или протромбинового времени (ПТВ) 9. Повышение уровня ПКТ, СR-протеина или других острофазовых белков 10. Увеличение СОЭ более 10 мм в час 11. Бактериемия 12. Гипергликемия более 7, 5 ммоль/л на фоне адекватной инфузионной терапии (глюкоза 5 -6 мг/кг/мин)

Прокальцитонин (ПСТ) • • • ПСТ – полипептид с молекулярной массой 14, 5 к. Да, состоит из 116 аминокислотных остатков, предшественник кальцитонина, лишенный гормональной активности, синтезируемый в С-клетках щитовидной железы и практически не поступающий в кровь. Повышение концентрации ПСТ в крови происходит при бактериальных инфекциях и сепсисе даже у больных перенесших тотальную резекцию щитовидной железы (Assicot M. et al. , Lancet, 1993, 341 (8844), 515 -518). Период полужизни ПСТ ~ 24 часа. ПСТ при бактериальных инфекциях синтезируется в лейкоцитах, нейроэндокринных клетках кишечника, легких и печени. У здоровых добровольцев после инъекции бактериального эндотоксина уровень ПСТ в крови повышается в 1700 раз (начало через 2 -3 часа, плато через 6 -8 часов) вслед за подъемом уровня провоспалительных цитокитнов IL-6, TNF -α (через 90 и 180 минут). Снижение уровня ПСТ на 30% - признак уменьшения тяжести инфекционного процесса. Измерение уровня ПСТ в крови является специфическим маркером тяжести бактериальных инфекций и он не повышается при вирусных инфекциях и аутоиммунных процессах.
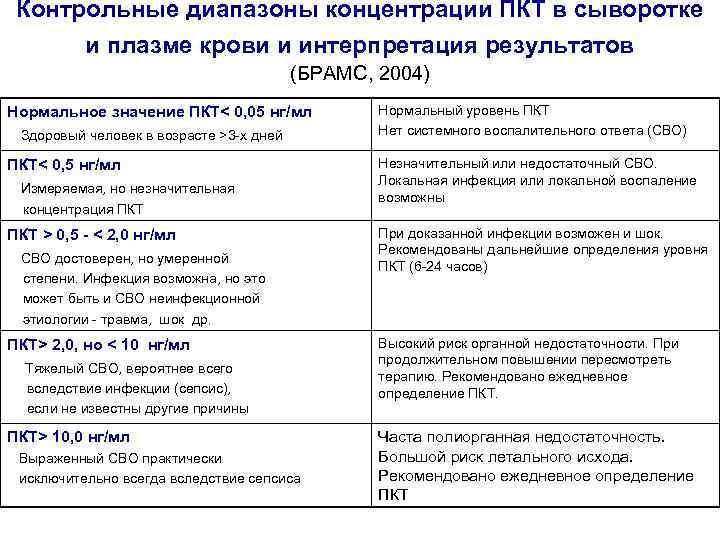
Контрольные диапазоны концентрации ПКТ в сыворотке и плазме крови и интерпретация результатов (БРАМС, 2004) Нормальное значение ПКТ< 0, 05 нг/мл Здоровый человек в возрасте >3 -х дней Нормальный уровень ПКТ Нет системного воспалительного ответа (СВО) ПКТ< 0, 5 нг/мл Измеряемая, но незначительная Незначительный или недостаточный СВО. Локальная инфекция или локальной воспаление возможны концентрация ПКТ > 0, 5 - < 2, 0 нг/мл СВО достоверен, но умеренной степени. Инфекция возможна, но это может быть и СВО неинфекционной этиологии - травма, шок др. ПКТ> 2, 0, но < 10 нг/мл Тяжелый СВО, вероятнее всего вследствие инфекции (сепсис), если не известны другие причины ПКТ> 10, 0 нг/мл Выраженный СВО практически исключительно всегда вследствие сепсиса При доказанной инфекции возможен и шок. Рекомендованы дальнейшие определения уровня ПКТ (6 -24 часов) Высокий риск органной недостаточности. При продолжительном повышении пересмотреть терапию. Рекомендовано ежедневное определение ПКТ. Часта полиорганная недостаточность. Большой риск летального исхода. Рекомендовано ежедневное определение ПКТ
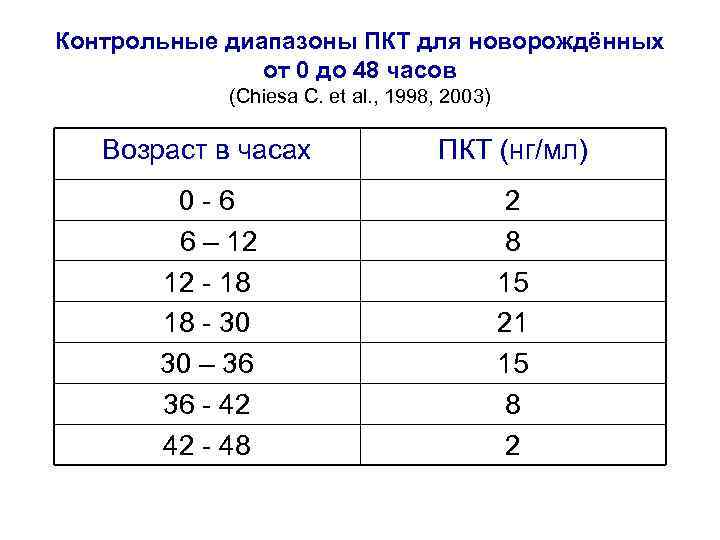
Контрольные диапазоны ПКТ для новорождённых от 0 до 48 часов (Chiesa C. et al. , 1998, 2003) Возраст в часах ПКТ (нг/мл) 0 - 6 6 – 12 12 - 18 18 - 30 30 – 36 36 - 42 42 - 48 2 8 15 21 15 8 2

Сепсис следует диагностировать у детей с факторами высокого риска + 4 клинических и 4 лабораторных признака SIRS инфекционного генеза. Если у ребенка имеется клинически очевидный очаг инфекции то для диагностики сепсиса достаточно 4 клинических и трех лабораторных признаков SIRS инфекционного генеза

Когда и где ставить диагноз сепсис новорождённых. • ВАИ и ИСПП – диагнозы роддомов при наличии у ребенка хотя бы 3 -4 х факторов риска РНС, ИСПП и 3 -4 х признаков СВО инфекционного генеза, но отсутствии первых признаков системной дисфункции эндотелия (метаболический ацидоз [лактат-ацидоз], необъяснимая гипергликемия, гипоксемия при отсутствии данных за поражения сердца и лёгких, олигурия, необходимость инотропной поддержки при отсутствии очевидных не инфекционных причин для этого). • В принципе диагноз сепсиса и ИСПП (Р 39. 9 ), как правило, должен ставиться на основе динамических наблюдения и результатов обследования, ответа ребёнка на адекватную терапию. • Из лабораторных критериев диагностики ПНС наиболее общепринятыми являются: 1) высев одинаковых бактерий из 2 -3 -х локусов и особенно крови, 2) ПКТ более 10 нг/мл.

Инфекции специфичные для перинатального периода (ИСПП - Р 39. 9 по МКБ Х) • По времени возникновения ИСПП могут быть антеили интранатальными. Подавляющее большинство ИСПП вызывают оппортунистические возбудители (от лат. opportunis – выгодный, удобный) которые у детей старше года и взрослых могут вызывать заболевание лишь на фоне наследственных или приобретенных иммунодефицитов (примером может служить течение ВИЧ-инфекции на стадии СПИДа). • Частота распространения ИСПП не известна, но в 2005 году по данным И. С. Сидоровой 2005 году в РФ родилось 32 255 детей с ВУИ (~0, 02%). Частота диагностики ВУИ как основного диагноза у больных новорождённых в 9 и 10 отделениях ДГБ № 1 ~ 3, 5%. • Диагноз ВУИ и ИСПП основан на учете факторов риска, клинической картине и совокупности лабораторных данных.

ИСПП • Диагноз ИСПП (Р 39. 9 по МКБ Х) должен быть очень редким (как окончательный диагноз), лишь после исключения ВУИ по совокупности бактериологической, ПЦР и иммунологической диагностики инфекции. • ИСПП (Р 39. 9) – диагноз роддома, а в отделении патологии ДГБ диагноз должен быть уточнён – либо ВУИ (P 35. 1 -9), либо ИСПП (P 39. 8 другая уточненная инфекция, специфичная для перинатального периода) при достоверной при повторных исследованиях диагностике инфекционного процесса и высеве условно патогенной флоры, типичной для патологии перинатального периода.

Течение сепсиса • «В 2002 г. возникло международное движение специалистов «Переживем сепсис» , поставившее задачу 25%-го снижения летальности в течение ближайших лет, однако к 2009 г. летальность осталась на прежнем уровне» ( «Сепсис» /Под ред. В. С. Савельева, Б. Р. Гельфанда, М. , МИА, 2010, стр. 20) • «Хотя сепсис является одной из ведущих причин смертности у детей, летальность от сепсиса среди педиатрических пациентов существенно ниже в сравнении со взрослыми. К 2002 году смертность при тяжелом сепсисе у детей и новорождённых была снижена с 97 до 9%, в то время как у взрослых она составляла 28%» ( «Сепсис» /Под ред. В. С. Савельева, Б. Р. Гельфанда, М. , МИА, 2010, стр. 240).

Возможности терапии • • • Инфекционный контроль Антибактериальная терапия Иммунотерапия Трофический статус Поддержание гомеостаза и сопутствующая терапия

Инфекционный контроль: Система организационных, профилактических и противоэпидемических мероприятий, направленных на предупреждение возникновения и распространения нозокомиальных инфекций, базирующаяся на результатах систематической высококачественной бактериологической и эпидемиологической диагностики. В каждом неонатальном стационаре должен быть разработана схема обязательного бактериологического обследования с учетом местных условий и регулярного систематического анализа результатов бактериологического обследования!!! Медицинская сестра отделения по инфекционному контролю – «сестра учитель» !!! Локальные «мануалы» по выполнению всех манипуляций с описанием всех этапов от А до Я.

Инфекционный контроль • Перчатки пластиковые • Жидкое бактерицидное мыло • Бумажные полотенца • Бактерицидные растворы для обработки рук • Мойте руки! • Мойте руки!

Инфекционный контроль • Рациональная обработка аппаратов для ИВЛ и кувезов, использование одноразовых ЭТТ и катетеров, смена контуров аппарата после каждого больного, • Локальные «мануалы» по выполнению всех манипуляций. • При любых манипуляциях с повреждением кожных покровов интубациях установке зонда необходимо надеть одноразовые перчатки. Медицинским сестрам это по первоначалу кажется не удобным но надо внушать мысль – перчатки это не только защита ребенка от микробов взрослого но и защита медицинского работника от инфекционных агентов ребенка (что при наличии достаточно широкого распространения вирусов гепатита и ВИЧ – быстро усваивается персоналом). • В отделениях патологии новорожденных ДГБ № 1 Санкт-Петербурга над кроваткой больного гнойно-воспалительным заболеванием когда то висел транспарант: «Осторожно!!! Я инфицирован! Пожалуйста оденьте перчатки!» .

Инфекционный контроль Централизованное приготовление инфузионных растворов • Нет разноса инфекции • Меньше трагических для больного ошибок в дозировке лекарств • Значительный экономический эффект • Персональная ответственность за хранение и расход медикаментов

Опасности длительной инфузионной терапии • Микробная колонизация инфузионных сред происходит в 5, 8% случаев, дистального конца инфузионной системы – в 13, 7%, участка кожи рядом с катетером - 20% случаев. • Инородные частицы (кристаллы антибиотиков и сочетания лекарств, выпадающих в осадок, частицы стекла, пластмассы, полимеров, бумаги). • Эндотоксины (образуются через 24 часа от инфицирования). • Фильтры Pall Intravenous Set Saver (ELD 96), Pall DUO Set. Saver (DUO) с мембраной 0, 2 мкм предназначены для задержки бактерий, эндотоксинов, инородных частиц и воздуха при постоянной инфузионной терапии (подключение к конечному звену системы для инфузии) в течение 96 часов. • Фильтр Pall Totall Admixture Filter (TNA 1 B) с мембраной 1, 2 мкм используют при инфузии липидов

Мероприятия по снижению колонизации и инфицированности MRSA и ESBLs-GN В ОИТН (Philip Toltzis «Гематология, иммунология и инфекционные болезни (Проблемы и противоречия в неонатологии), 2013» • Эндемические Профилактика инфекций Постоянное соблюдение гигиены рук Применение надежной механической защиты (перчатки, халаты, маски персонала; особенно при контакте с больными MRSA) Изоляция инфицированных детей Дезинфекция оборудования и деконтаминация поверхностей Разработка стратегии применения антибиотиков Контроли профилактических мер

Мероприятия по снижению колонизации и инфицированности MRSA и ESBLs-GN В ОИТН (Philip Toltzis «Гематология, иммунология и инфекционные болезни (Проблемы и противоречия в неонатологии), 2013» • Эпидемические Постоянное соблюдение гигиены рук Когортная идентификация детей Изоляция инфицированных детей Разделение медицинского оборудования на применяемого только для пациентов с колонизацией и только для пациентов, свободных от колонизации Скрининг сотрудников клиники на MRSA и лечение инфицированных Выделение культур с поверхностей предметов окружающих пациентов Ограничения применения антибиотиков Закрытие ОИТН на санитарную обработку

«Особого внимания заслуживает организация профилактики сепсиса и септических состояний. Профилактика сепсиса у новорожденных и недоношенных детей является делом очень сложным. Она не дает эффекта, если применяют какое-либо одно новое мероприятие» . Маслов М. С. (1959)
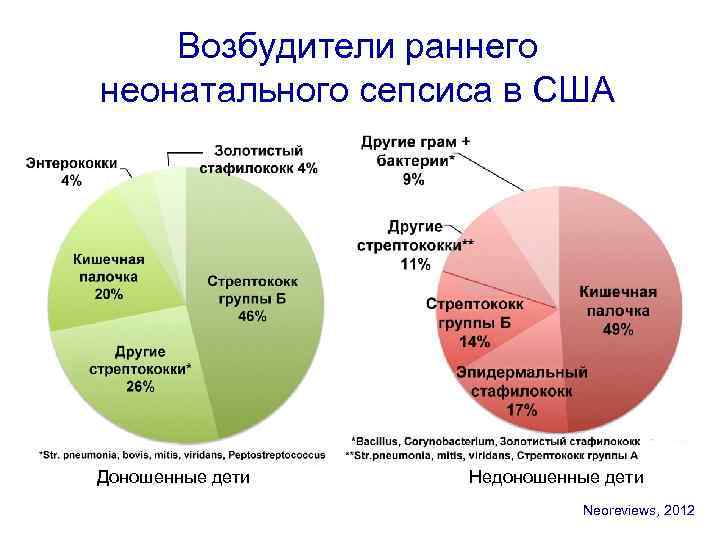
Возбудители раннего неонатального сепсиса в США Доношенные дети Недоношенные дети Neoreviews, 2012

Эмпирическое назначение антибиотиков для лечения РНС • Самое частое сочетание АБ для лечения РНС: – ампициллин + гентамицин (амикацин) или пенициллин + гентамицин (амикацин)); • Не рекомендуется начинать эмпирическое лечение РНС с цефалоспоринов третьего поколения или других антибиотиков широкого спектра действия: – Больше побочного действия; – Быстрее появляются антибиотикоустойчивые штаммы бактерий; – Увеличивает риск фунгемии; – Увеличивается смертность недоношенных новорожденных детей; Felciglia G. et al, Neoreviews, 2012

Эмпирическое назначение антибиотиков для лечения раннего неонатального сепсиса (РНС) • Колонизация новорожденных бактериями, устойчивыми к антибиотикам, увеличивалась 18 раз, когда детям в отделении ИТН назначали амоксациллин с цефотаксимом по сравнению с теми детьми, которых лечили пенициллином и тобрамицином; • Ретроспективный анализ более 100 000 случаев показал, что эмпирическое назначение ампициллина с цефотаксимом для лечения РНС значительно (1. 5 раза!) увеличивает смертность среди новорожденных, по сравнению с теми детьми, которым назначались ампициллин с гентамицином; • Вывод: нецелесообразна комбинация аминопенициллинов и цефалоспоринов. Clark et al, Pediatrics, 2006; 117 De Man P et al Lancet 2000; 355

Рекомендации Center for Disease Control USA - CDC (1997, пересмотр 2002, 2010) по профилактике стрептококковой В инфекции у новорожденных • • Универсальный скрининг на 35 -37 неделе беременности с однократным комбинированным посевом из вагино-аноректальной области и антибиотикопрофилактика всем носителям СГВ в родах. Если результаты посева неизвестны, антибиотикопрофилактика в родах назначается всем женщинам с факторами риска: – Роды до 37 недель беременности – Лихорадка у матери более 38 о. С – Бактериурия СГБ во время беременности – Безводный промежуток более 18 часов – В анамнезе рождение ребенка с СГБ во время беременности независимо от статуса колонизации матери при данной беременности При таком подходе 28% рожениц получают антибиотикопрофилактику (пенициллин, а при аллергии к нему – эритромицин ил др. ). Антибиотикопрофилактика у новорожденных менее 2000 г – не эффективна (Red Book, 2015). Однако, если антибиоткопрофилактику проводили матери и у нее есть хориоамнионит, то её всё же надо продолжить у детей с ОНМТ, по крайней мере, в течение 48 часов.

Рекомендации Center for Disease Control USA - CDC (1997, пересмотр 2010) по профилактике стрептококковой В инфекции у новорожденных Пенициллин G в/в в дозе 5 млн. ЕД (или 2 гр. ампициллина) и далее по 2, 5 млн. ЕД (или по 1 гр. ампициллина) каждые 4 часа в течение 48 часов. При аллергии к пенициллинам: Цефазолин 2 гр. и далее по 1 гр. каждые 8 часов или Клинадамицин (900 мг в/в каждые 8 часов), Эритромицин (500 мг в/в каждые 6 часов), Ванкомицин (1000 мг каждые 12 часов) Согласно Red Book, 2015, 15 -30% стрептококков групп В резистентны к эритромицину и назначенная внутрь антибиотикопрофилактика не снижает частоту инфекционных поражений мозга у новорожденных.


Назначение антибиотиков роженице • Эффективность профилактики β-стрептококкового сепсиса при назначении пенициллина или ампициллина не менее чем за 4 часа до рождения ребенка составляет: – Для доношенных детей 91%, – Для недоношенных – 86%; • При назначении клиндамицина – всего 22%; • Эффективность пенициллинов резко снижается при их назначении матери за 2 -3 часа до рождения ребенка: соответственно 47 и 38% Fairlie T еt al. Obstet Gynecol 2013; 121
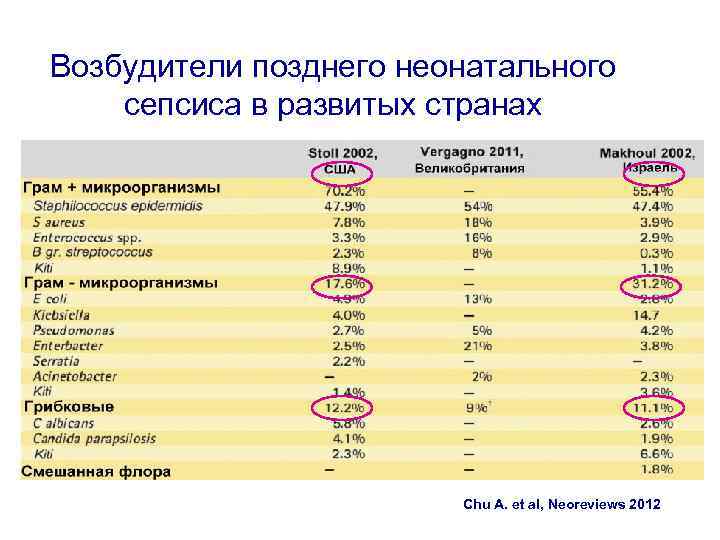
Возбудители позднего неонатального сепсиса в развитых странах Chu A. et al, Neoreviews 2012
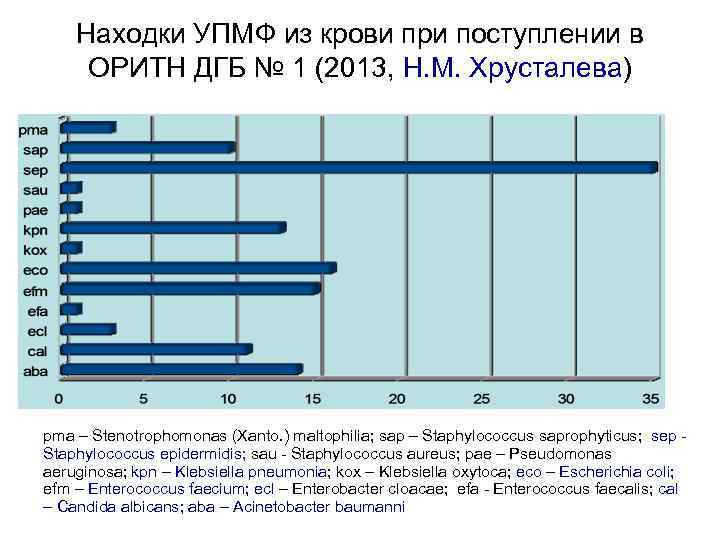
Находки УПМФ из крови при поступлении в ОРИТН ДГБ № 1 (2013, Н. М. Хрусталева) pma – Stenotrophomonas (Xanto. ) maltophilia; sap – Staphylococcus saprophyticus; sep - Staphylococcus epidermidis; sau - Staphylococcus aureus; pae – Pseudomonas aeruginosa; kpn – Klebsiella pneumonia; kox – Klebsiella oxytoca; eco – Escherichia coli; efm – Enterococcus faecium; ecl – Enterobacter cloacae; efa - Enterococcus faecalis; cal – Candida albicans; aba – Acinetobacter baumanni
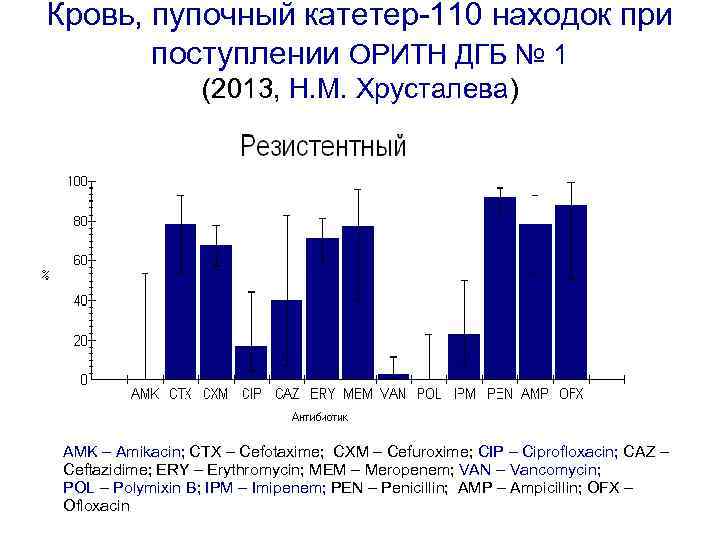
Кровь, пупочный катетер-110 находок при поступлении ОРИТН ДГБ № 1 (2013, Н. М. Хрусталева) AMK – Amikacin; CTX – Cefotaxime; CXM – Cefuroxime; CIP – Ciprofloxacin; CAZ – Ceftazidime; ERY – Erythromycin; MEM – Meropenem; VAN – Vancomycin; POL – Polymixin B; IPM – Imipenem; PEN – Penicillin; AMP – Ampicillin; OFX – Ofloxacin
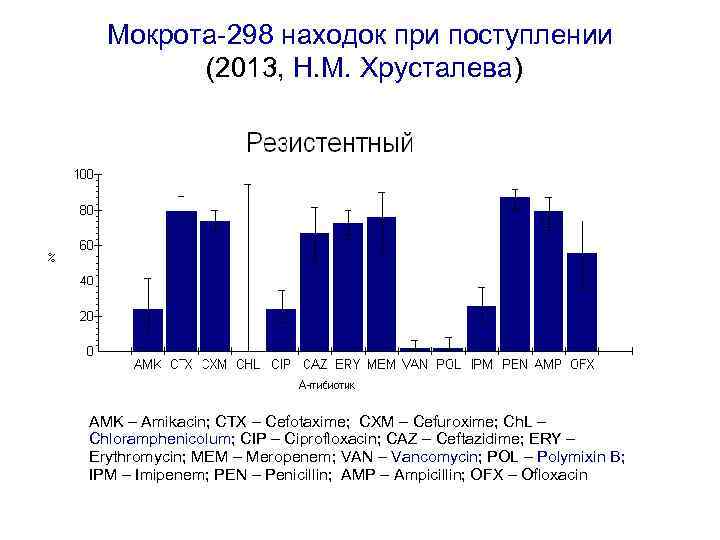
Мокрота-298 находок при поступлении (2013, Н. М. Хрусталева) AMK – Amikacin; CTX – Cefotaxime; CXM – Cefuroxime; Ch. L – Chloramphenicolum; CIP – Ciprofloxacin; CAZ – Ceftazidime; ERY – Erythromycin; MEM – Meropenem; VAN – Vancomycin; POL – Polymixin B; IPM – Imipenem; PEN – Penicillin; AMP – Ampicillin; OFX – Ofloxacin
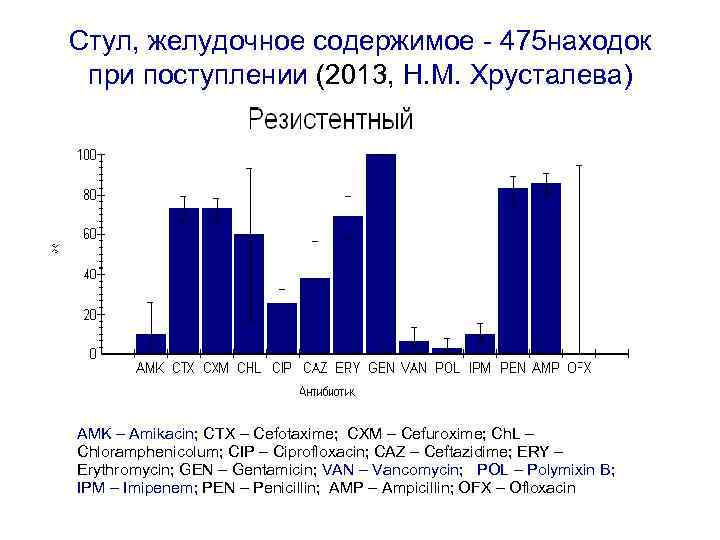
Стул, желудочное содержимое - 475 находок при поступлении (2013, Н. М. Хрусталева) AMK – Amikacin; CTX – Cefotaxime; CXM – Cefuroxime; Ch. L – Chloramphenicolum; CIP – Ciprofloxacin; CAZ – Ceftazidime; ERY – Erythromycin; GEN – Gentamicin; VAN – Vancomycin; POL – Polymixin B; IPM – Imipenem; PEN – Penicillin; AMP – Ampicillin; OFX – Ofloxacin
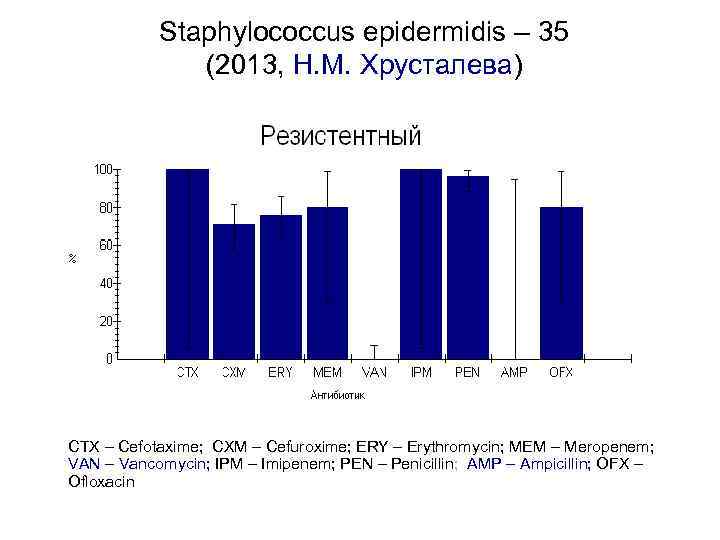
Staphylococcus epidermidis – 35 (2013, Н. М. Хрусталева) CTX – Cefotaxime; CXM – Cefuroxime; ERY – Erythromycin; MEM – Meropenem; VAN – Vancomycin; IPM – Imipenem; PEN – Penicillin; AMP – Ampicillin; OFX – Ofloxacin
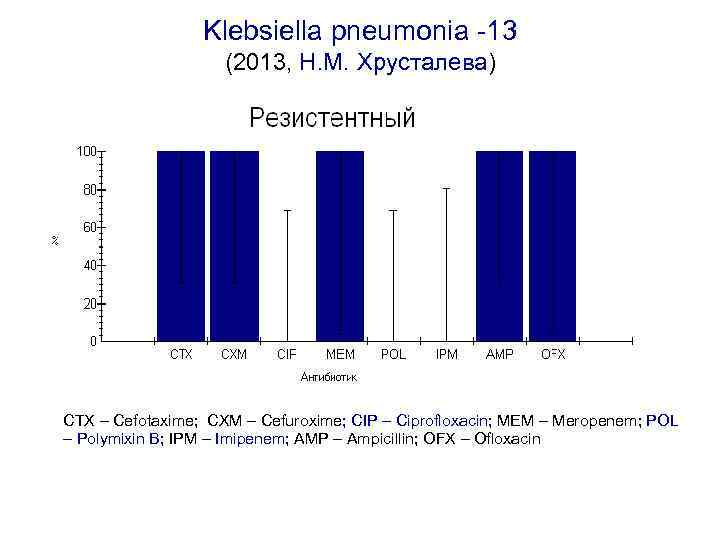
Klebsiella pneumonia -13 (2013, Н. М. Хрусталева) CTX – Cefotaxime; CXM – Cefuroxime; CIP – Ciprofloxacin; MEM – Meropenem; POL – Polymixin B; IPM – Imipenem; AMP – Ampicillin; OFX – Ofloxacin
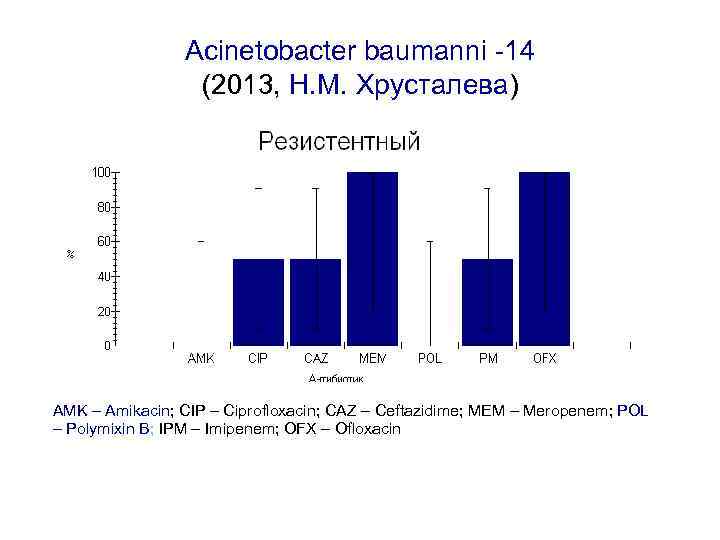
Acinetobacter baumanni -14 (2013, Н. М. Хрусталева) AMK – Amikacin; CIP – Ciprofloxacin; CAZ – Ceftazidime; MEM – Meropenem; POL – Polymixin B; IPM – Imipenem; OFX – Ofloxacin

Всегда ли ПНС – следствие госпитальной инфекции? • Нередко ПНС развивается у новорожденных с установленной ВАИ вследствие суперинфекции. • Суперинфекция возникает как результат последовательно развивающихся событий: подавление антибиотиком чувствительно к нему микрофлоры, нарушение микробного баланса (биоценоза), «неконтролируемое» размножение микроорганизма (микроорганизмов), устойчивого к антибиотику, накопление биомассы микроба, достаточной для болезнетворного воздействия на ткани человека, возникновение и развитие инфекционного процесса (М. С. Поляк, 2010)

По мнению М. С. Поляк (2010) термин суперинфекция подразумевает: • осложнение должно иметь очевидную клиническую составляющую; • осложнение должно напрямую связано с предшествующей или продолжающейся антибиотикотерапией; • возбудитель суперинфекции должен быть микроорганизмом, относящимся к резидентной (чаще минорной) или транзиторной микрофлоре человека (C. difficile, Candida spp. , S. aureus, P. aeruginosa, K. pneumoniae, E. coli, Proteus vulgaris, S. maltophilia, Aspergillis spp. , энтерококки и др. ). ; • возбудитель осложнения в большинстве случаев должен быть устойчивым к применяемым для лечения больного противомикробным препаратам (последнее не может быть обязательным в силу условности понятий «чувствительный» , «резистентный» ).

Патогенез бактериемии при неонатальном сепсисе • Как известно, среди пограничных состояний новорождённых выделяют «транзиторный дисбактериоз» , обусловленный заселением кишечника и кожи флорой родовых путей матери и окружающей среды. • При гипоксемии, ишемии кишечника, расстройствах микроциркуляции, отсутствии энтерального питания (!!!) проницаемость кишечного барьера повышается и происходит транслокация бактериальной флоры кишечника в кровь (смена лидеров при сепсисе по С. Я. Долецкому). • Существует афоризм: «Кишечник – не дренированный абсцесс при полиорганной недостаточности» . • М. С. Маслов (1946) подчеркивал: “кишечная стенка ребенка проходима для бактерий. Возможна не только энтерогенная бактериемия, но и токсемия и аутоинтоксикация”.
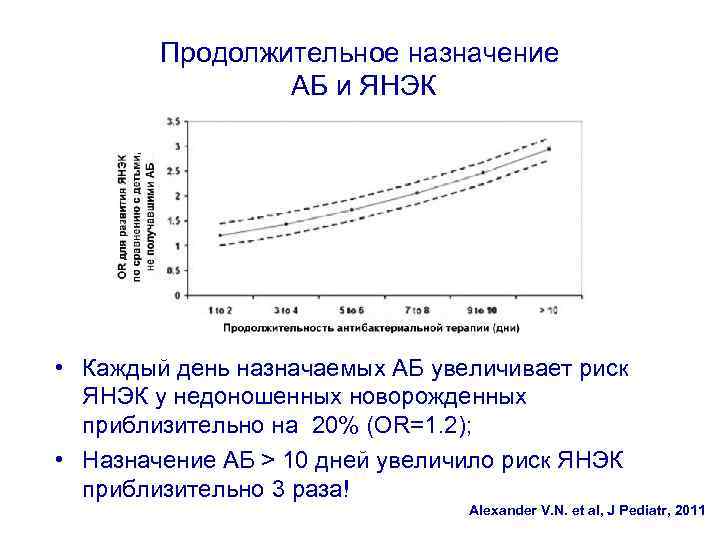
Продолжительное назначение АБ и ЯНЭК • Каждый день назначаемых АБ увеличивает риск ЯНЭК у недоношенных новорожденных приблизительно на 20% (OR=1. 2); • Назначение АБ > 10 дней увеличило риск ЯНЭК приблизительно 3 раза! Alexander V. N. et al, J Pediatr, 2011

Лечение сепсиса, вызванного полирезистентными бактериями • Сепсис, вызванный грам «+» устойчивыми микроорганизмами: – Чаще всего устойчивые к АБ группы лактамамов – оксациллину, нафциллину, нередко – аминогликозидам; – Ванкомицин чаще всего хорошо действует против Staph. Aureus и epidermidis, – Линезолид в том числе к ванкомицину устойчивых бактерий. Bhatti M. et al, Neoreviews, 2012

Лечение сепсиса, вызванного полирезистентными бактериями • Сепсис, вызванный грам «-» устойчивыми микроорганизмами: – Ципрофлоксацин обладает бактерицидным действием против большинства грамотрицательных бактерий, в том числе и против Pseudomonas aeruginosa; – Имипенем и Mеропенем обладает широким спектром действия против большинства грам «-» и грам «+» бактерий в том числе – против анаэробов; – Возвращение к “старым и забытым” АБ: Колистин (колимицин, полимиксин E), Фосфомицин – к ним часто чувствительны полирезистентные бактерии (Kl. pleumonia, Serratia, Ps. aeruginosa, E. Coli и др. ). Bhatti M. et al, Neoreviews, 2012 Falagas M. E. et al, Lancet, 2010

β-лактамные антибиотики 1. Пенициллины: • природные – бензилпенициллин и др. ; • аминопенициллины – ампициллин, амоксициллин и др. ; • антистафилококковые (пенициллины резистентные к пенициллиназе) – оксациллин, нафциллин, метициллин и др. ; • карбоксипенициллины (антисинегнойные) – карбенициллин, тикарциллин; • уреидопенициллины (антисинегнойные и антиклебиселлезные) – пиперациллин, азлоциллин, мезлоциллин 2. Ингибиторы β-лактамаз (клавулановая кислота, сульбактам, тазобактам) 3. Цефалоспорины 4. Карбапенициллины (карбапенемы) – имипенем (тиенам), меронем и др. 5. Монобактамы (моноциклические β-лактамы) - азтреонам 6. Комбинированные препараты – Аугментин (амоксициллин + калия клавуланат), Уназин (ампициллин + сульбактам), Амписид (сультамициллин: ампициллин + сульбактам), Тиментин (тикарциллин + клавулановая кислота), Тазоцин (пиперациллин + тазобактам), Сульперазон (цефоперазон + сульбактам)
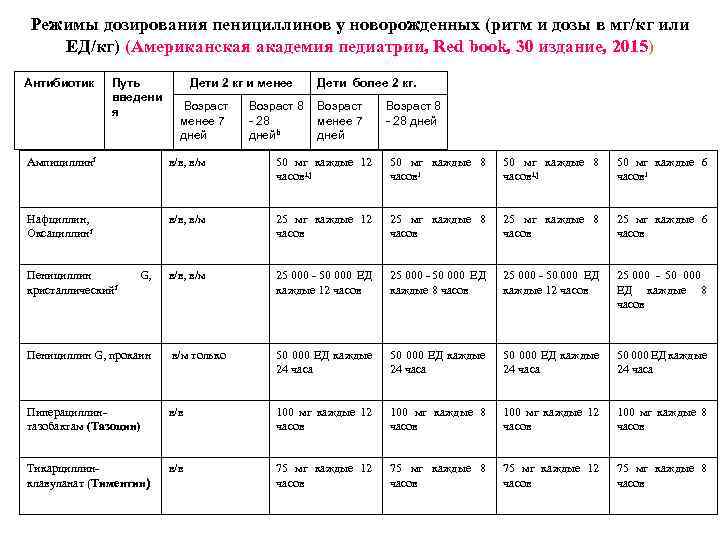
Режимы дозирования пенициллинов у новорожденных (ритм и дозы в мг/кг или ЕД/кг) (Американская академия педиатрии Red book 30 издание 2015) Антибиотик Путь введени я Дети 2 кг и менее Возраст менее 7 дней Дети более 2 кг. Возраст 8 Возраст - 28 менее 7 днейb дней Возраст 8 - 28 дней Ампициллинf в/в в/м 50 мг каждые 12 часовi, j 50 мг каждые 8 часовi, j 50 мг каждые 6 часовi Нафциллин, Оксациллинf в/в в/м 25 мг каждые 12 часов 25 мг каждые 8 часов 25 мг каждые 6 часов в/м 25 000 - 50 000 ЕД каждые 12 часов 25 000 - 50 000 ЕД каждые 8 часов 25 000 - 50 000 ЕД каждые 12 часов 25 000 - 50 000 ЕД каждые 8 часов Пенициллин G прокаин в/м только 50 000 ЕД каждые 24 часа Пиперациллинтазобактам (Тазоцин) в/в 100 мг каждые 12 часов 100 мг каждые 8 часов Тикарциллинклавуланат (Тиментин) в/в 75 мг каждые 12 часов 75 мг каждые 8 часов Пенициллин кристаллическийf G
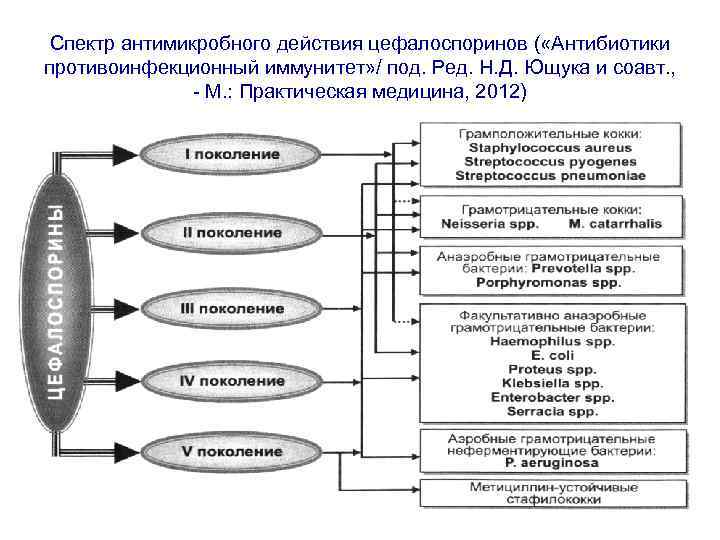
Спектр антимикробного действия цефалоспоринов ( «Антибиотики противоинфекционный иммунитет» / под. Ред. Н. Д. Ющука и соавт. , - М. : Практическая медицина, 2012)

Эмпирическое назначение АБ для лечения ПНС • Невозможно предвидеть единую тактику эмпирической АБ терапии при подозрении ПНС. • Каждое отделение должно иметь свой протокол АБ лечения, основанный на наиболее часто встречающихся возбудителях госпитальной инфекции и их чувствительности к антибиотикам. • Протокол должен быть гибким и регулярно пересматриваться в зависимости от эпидемиологической ситуации. • Целесообразно знать сан. -эпид. обстановку в других учреждениях, из которых поступают дети.

Основные наши проблемы антибактериальной терапии: • • Адекватное и современное бактериологическое обследование. Когда заканчивать, чем руководствуясь? - результатами бактериологического обследования? - клиническим анализом крови? - показателями острофазового ответа ( СRP, ПКТ и др. )? - локализацией процесса и данными лучевых методов? - как ребёночек себя чувствует (!) и как выглядит, коммуникабелен (? - !) (искусство врача!!!)
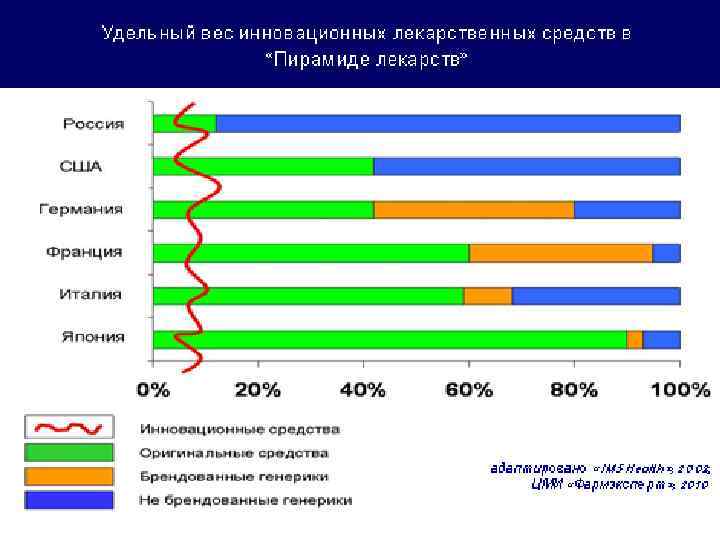

Неонатальный кандидоз (НК) • Группа высокого риска НК: - дети с ЭНМТ (5 -20%) - дети с наследственными дефектами фагоцитоаа, Длительно получающие парентеральное питание, цефалоспорины III-IV генерации, карбопенемы, ванкомицин, с длительным стоянием в/в катетеров. • Профилактика: - детям с ЭНМТ, начиная через 48 -72 часа после рождения (в СПб детям с ОНМТ), другим детям группы высокого риска по показаниям в/в введение флуконазола (дифлюкана) 3 мг/кг массы дважды в неделю до 4 -6 недель или до окончания стояния в/в катетера.

Иммунотерапия «Можно ли одними антибиотиками вылечить ребенка от сепсиса? На это можно дать совершенно четкий ответ - нельзя. Сепсис - это заболевание, вызванное микробом, но в организме с измененной реактивностью. Поэтому совершенно необходимо применение средств и мероприятий, повышающих естественную резистентность организма, вызывающих к жизни защитные силы» . Маслов М. С. (1959)
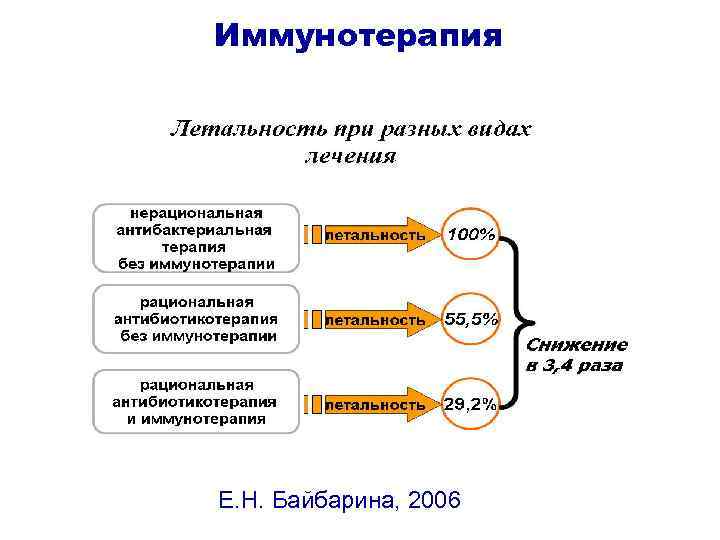
Иммунотерапия Е. Н. Байбарина, 2006
![Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of](https://present5.com/presentation/3/65859928_437218811.pdf-img/65859928_437218811.pdf-77.jpg)
Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of Systematic Reviews 000062. dx. doi. org/10. 1002/1465182013; 7: ED 58. ED 000062 • Частота внутрибольничных инфекций среди детей с ЭНМТ и ОНМТ снизилась в период 2000 до 2011 годов с 21, 4% до 13, 7% за счет совершенствования качества медицинской помощи, включая инициативы по улучшению качества мытья рук, установки центральных венозных катетеров и ухода. Тем не менее, и сейчас неонатальные инфекции являются серьезными осложнениями ассоциирующимися с плохим неврологическим исходом и смертностью. • Учитывая то, что внутриутробно Ig. G проникает к плоду главным образом после 32 недель гестации и дети с ОНМТ и ЭНМТ имеют его дефицит, а эндогенный синтез Ig. G начинается с 24 недель после рождения идея введения поливалентного внутривенного иммуноглобулина (ВВИГ) для профилактики и лечения неонатальных инфекций у них достаточно обоснована.
![Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of](https://present5.com/presentation/3/65859928_437218811.pdf-img/65859928_437218811.pdf-78.jpg)
Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of Systematic Reviews 2013; 7: ED 000062. dx. doi. org/10. 1002/14651858. ED 000062 • Олссон А. и Лейси Дж. Б. (июль 2013) проанализировали результаты 19 рандомизированных, контролируемых исследований применения ВВИГ для профилактики и лечения неонатальных инфекций у 5000 детей с ОНМТ и ЭНМТ. Действительно при профилактическом введении ВВИГ частота сепсиса снижается и для предотвращения внутрибольничной инфекции у одного ребенка надо пролечить 33. При этом, помимо снижения частоты сепсиса, нет другой пользы, включая смертность, частоту НЭК, БЛД и длительность госпитализации. • Применение ВВИГ при доказанной инфекции не снижает смертность, длительность госпитализации. Возможно это связано с дефицитом специфических антител, но применение антистафилококкового ВВИГ не приводит к снижению смертности при стафилококковом сепсисе.
![Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of](https://present5.com/presentation/3/65859928_437218811.pdf-img/65859928_437218811.pdf-79.jpg)
Soll RF. Calling time on intravenous immunoglobulin for preterm infants? [editorial]. Cochrane Database of Systematic Reviews 2013; 7: ED 000062. dx. doi. org/10. 1002/14651858. ED 000062 Заключение • Не опубликовано ни одного руководства Неонатального центра с рекомендациями по профилактическому введению ВВИГ детям с ЭНМТ и ОНМТ. • Нет необходимости дальнейших клинических испытаний и обобщений по использованию ВВИГ для профилактики и лечения сепсиса у детей с ОНМТ. • В для достижения этой цели в практической деятельности целесообразнее сосредоточиться на совершенствовании гигиены рук, питания, ухода за кожей, сосудистым доступом и катетерами.

Ситуация после проведения курса лечения Пентаглобином • • • Согласно Bellanti J. A. et al. (Avery Neonatology, 2012) уровень Ig. M у доношенных новорождённых ~ 8 -10% от уровня взрослых (при сроке гестации 30 недель вдвое ниже) и соответственно у доношенного новорожденного в крови содержится примерно 20 мг Ig. M (при сроке 30 недель гестации ~ 6 -7 мг), и при трехдневном курсе Пентаглобина соответственно поступает 72 мг Ig. M – доношенному и около 20 -24 мг ребенку со сроком гестации 30 недель, т. е. создается принципиально новая ситуация в иммунной системе ребенка. Ig. M – типичный представитель мембранных иммуноглобулинов и вероятно избыточное его количество в крови оседает на В-лимфоцитах и макрофагах, тормозя их избыточную активацию при системном воспалительном ответе, блокируя синтез провоспалительных цитокинов (ИЛ-1, ИЛ-2, ИЛ-6, ФНО, гаммаинтерферон – down-регуляция гиперактивных клеток) и стимулирует синтез антагонистов рецептора к ИЛ-1, растворимых рецепторов ИЛ-2 и ФНО, синтез антивоспалительных цитокинов ИЛ-8, МЛ-10. Кроме того, Ig. M связывает эндотоксин грамотрицательных бактерий, суперантиген (экзотоксин) стафилококков, С 4 b и C 3 b-компоненты комплемента и тем самым усиливает последующий фагоцитоз.
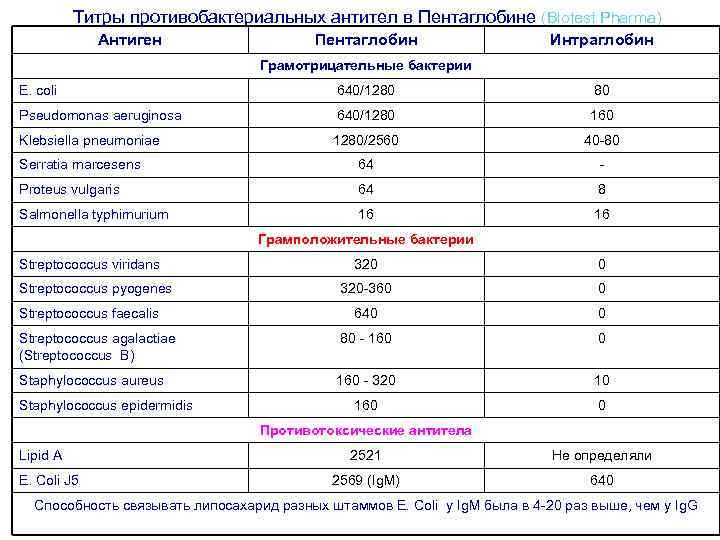
Титры противобактериальных антител в Пентаглобине (Biotest Pharma) Антиген Пентаглобин Интраглобин Грамотрицательные бактерии E. coli 640/1280 80 Pseudomonas aeruginosa 640/1280 160 Klebsiella pneumoniae 1280/2560 40 -80 Serratia marcesens 64 - Proteus vulgaris 64 8 Salmonella typhimurium 16 16 Грамположительные бактерии Streptococcus viridans 320 0 320 -360 0 640 0 Streptococcus agalactiae (Streptococcus B) 80 - 160 0 Staphylococcus aureus 160 - 320 10 160 0 Streptococcus pyogenes Streptococcus faecalis Staphylococcus epidermidis Противотоксические антитела Lipid A E. Coli J 5 2521 Не определяли 2569 (Ig. M) 640 Способность связывать липосахарид разных штаммов E. Coli у Ig. M была в 4 -20 раз выше, чем у Ig. G

Пентаглобин – золотой стандарт лечения при неонатальном сепсисе Пентаглобин является единственным ВВИГ, эффективность которого в плане снижения летальности при сепсисе и септическом шоке подтверждена с позиций доказательной медицины (надежность доказательств – категория Ia, рекомендации – категория А). Обоснованность включения Пентаглобина в комплексную терапию пациентов с сепсисом и септическим шоком подтверждена данными мета-анализа, проведенного группой независимых ученых Соchrane Infection Disease Group, указавшей что это снижает летальность в 2, 1 раза. (Alejandria M. M. et al. The Cochrane Library, 2005, Issure 3, Oxfort Update Software; Haque KN. , 2010; Resch E. et Resch B. , 2013)


Иммунотерапия В конце прошлого и начале нынешнего века появилось много иммуностимуляторов различного происхождения и механизма действия. В отечественной литературе есть работы, в которых сообщается о применении препаратов тимического происхождения, различных цитокинов при лечении новорожденных с инфекционной патологией. Например, о лечении отечественным рекомбинантным человеческим интерлейкином-2 ( «Ронколекин» ) новорожденных с сепсисом и лимфоцитопенией. Подчеркнем, что в зарубежной литературе таких работ нет.

Иммунотерапия Интерферонотерапия Учитывая нередкость при сепсисе сочетания с вирусной инфекцией показано применение рекомбинантного интерферона α 2β человека (Виферон), назначаемого по 1 свече (150 000 МЕ) 2 раза в день в прямую кишку в течение 7 -14 дней. Показатель летальности в группе детей с ВУИ бактериально-вирусной этиологии, получивших терапию Вифероном, составил 4, 9% (4/81), а в группе детей, получивших только базисную терапию, - 18, 4%. Эффективность Виферона определяется снижением показателя летальности, сокращением сроков санации очагов инфекции, нормализацией показателей гемограммы и иммунного статуса, у детей, получившими иммунотерапию Вифероном, по сравнению с детьми, получившими только базисную терапию (категория доказательств 2 В). ( «Сепсис» /Под ред. В. С. Савельева, Б. Р. Гельфанда, М. , МИА, 2010)

Трофический статус • Неадекватное (дефицитное) питание в перинатальном периоде приводит и к снижению гомеостатических возможностей новорождённого (прежде всего - ЦНС и иммунитета), и к отдаленным последствиям в виде задержек и/или нарушений развития. • Общепринятым мнением является необходимость обеспечения с самого рождения достаточного количества энергии и основных пищевых ингредиентов энтерально или парэнтерально.

Поддержание гомеостаза и сопутствующая терапия • • Восстановление ОЦК Обеспечение легочной вентиляции Коррекция ацидоза Восстановление адекватных: гемостаза, гемореологии и микроциркуляции • Подержание сердечной деятельности • Восстановление функции почек • Энергообеспечение

Заключение • Эпидемиологический контроль: введение постоянного инфекционного контроля (внутренний противоинфекционный аудит) • Мытье рук с использованием антисептических средств, одноразовые перчатки при работе с внутривенными линиями, интубационными трубками, катетерами • Рациональная обработка аппаратов для ИВЛ и кувезов, использование одноразовых ЭТТ и катетеров, смена контуров аппарата после каждого больного • Рациональное применение антибиотиков (в том числе – ротация антибиотиков первого ряда и резерва в отделении) • Рациональная иммунотерапия • Как можно более раннее начало энтерального питания!!! • Обучение персонала (сестра-учитель!) • С целью уменьшения иатрогенных осложнений создание местных неонатальных формуляров, централизованное приготовление неонатальных инфузионных растворов и применение их с использованием бактериальных фильтров. • Разработка единого «Неонатального формуляра» и компьютерная оценка врачебных назначений новорождённому «на входе» .

И всё таки, и всё таки и всё же Когда же российские неонатологи будут иметь возможность использовать в лечении: • Растворы декстрозы (р. Н 10% раствора глюкозы – 3, 0, ибо для стабилизации используют HCL) • Витамин К 1 (фитоменадион, Конакион), а не К 3 (викасол) • Coffeinum citrate, а не Coffeinum-natrii benzoas (токсичен для мозга!) • Витамино-микроэлементные препараты для внутривенного введения • Натрия глицерофосфат для внутривенного введения для лечения недоношенных особенно с ОНМТ и ЭНМТ.

Сепсис обзор.ppt