6fddc0dd740d64aca190ef3b2eb9fa98.ppt
- Количество слайдов: 23

Семинар «Основы надлежащей практики фармаконадзора. Организация работы уполномоченного лица» 18 мая 2016 г. Понятия системы менеджмента качества. Разработка и внедрение системы менеджмента качества Источники информации: - ISO 9000: 2015 (ГОСТ Р ИСО 9000 -2015). Системы менеджмента качества. Основные положения и словарь. - ISO 9001: 2015 (ГОСТ Р ИСО 9001 -2015). Системы менеджмента качества. Требования. - Правила надлежащей практики фармаконадзора для ЕС, ЕАЭС (2015) Вельц Наталья Юрьевна, м. н. с. , к. б. н. , доцент

СИСТЕМА МЕНЕДЖМЕНТА КАЧЕСТВА (СМК – это то, как организована работа персонала) Основные термины и определения в области качества – см. пункт 3 ГОСТ Р ИСО 9000 -2015 Системы менеджмента качества. Требования. (вступил в силу в России с 01. 11. 2015, идентичен (IDT) ISO 9000: 2015): 3. 7. 1. цель (objective): Результат, который должен быть достигнут. 3. 6. 2. качество (quality): Степень соответствия совокупности присущих характеристик объекта требованиям. 3. 5. 4. система менеджмента качества (quality management system) : Часть системы мененджмента применительно к качеству. 3. 6. 4. требование (requirement): Потребность или ожидание, которое установлено, обычно предполагается или является обязательным. 3. 6. 11. соответствие (conformity): Выполнение требования. 3. 6. 9. несоответствие (nonconformity): 2 Невыполнение требования.

Деятельность по фармаконадзору должна осуществляться КАЧЕСТВЕННО Она должна соответствовать какой-либо (любой из. . ) системе стандартов качества - национальной (ГОСТ Р – это > 30 тыс. стандартов, ОСТ, ТУ, СТП, СТО), региональной или международной (напр. Международной организации по стандартизации ISO – это > 20 тыс. стандартов). Система качества ISO (от греч. ISOS, т. е. «равный» , на всех языках мира всегда звучит как ИСО) – используется чаще всего. Организация сама решает (Приказом) – будет ли ее система фармаконадзора элементом общей системы менеджмента качества этой организации (ISO 9000, или иная), или она просто осуществляется надлежащим образом на основании Правил GVP. 3
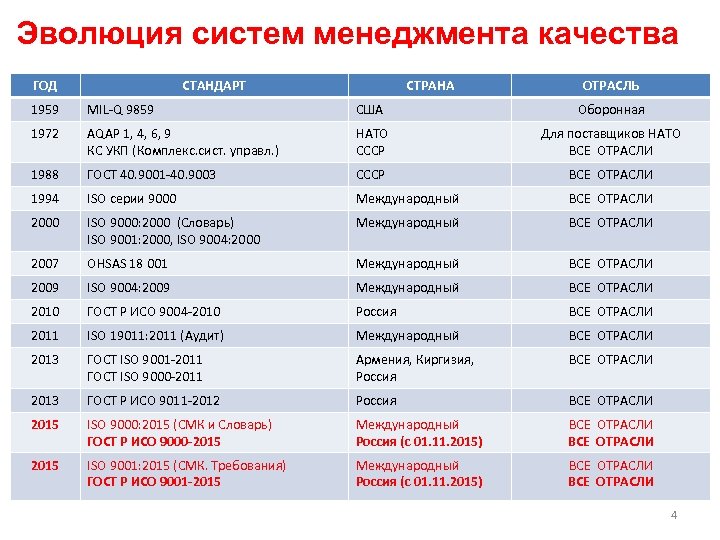
Эволюция систем менеджмента качества ГОД СТАНДАРТ СТРАНА ОТРАСЛЬ 1959 MIL-Q 9859 США Оборонная 1972 AQAP 1, 4, 6, 9 КС УКП (Комплекс. сист. управл. ) НАТО СССР Для поставщиков НАТО ВСЕ ОТРАСЛИ 1988 ГОСТ 40. 9001 -40. 9003 CCCР ВСЕ ОТРАСЛИ 1994 ISO серии 9000 Международный ВСЕ ОТРАСЛИ 2000 ISO 9000: 2000 (Словарь) ISO 9001: 2000, ISO 9004: 2000 Международный ВСЕ ОТРАСЛИ 2007 OHSAS 18 001 Международный ВСЕ ОТРАСЛИ 2009 ISO 9004: 2009 Международный ВСЕ ОТРАСЛИ 2010 ГОСТ Р ИСО 9004 -2010 Россия ВСЕ ОТРАСЛИ 2011 ISO 19011: 2011 (Аудит) Международный ВСЕ ОТРАСЛИ 2013 ГОСТ ISO 9001 -2011 ГОСТ ISO 9000 -2011 Армения, Киргизия, Россия ВСЕ ОТРАСЛИ 2013 ГОСТ Р ИСО 9011 -2012 Россия ВСЕ ОТРАСЛИ 2015 ISO 9000: 2015 (СМК и Словарь) ГОСТ Р ИСО 9000 -2015 Международный Россия (с 01. 11. 2015) ВСЕ ОТРАСЛИ 2015 ISO 9001: 2015 (СМК. Требования) ГОСТ Р ИСО 9001 -2015 Международный Россия (с 01. 11. 2015) ВСЕ ОТРАСЛИ 4
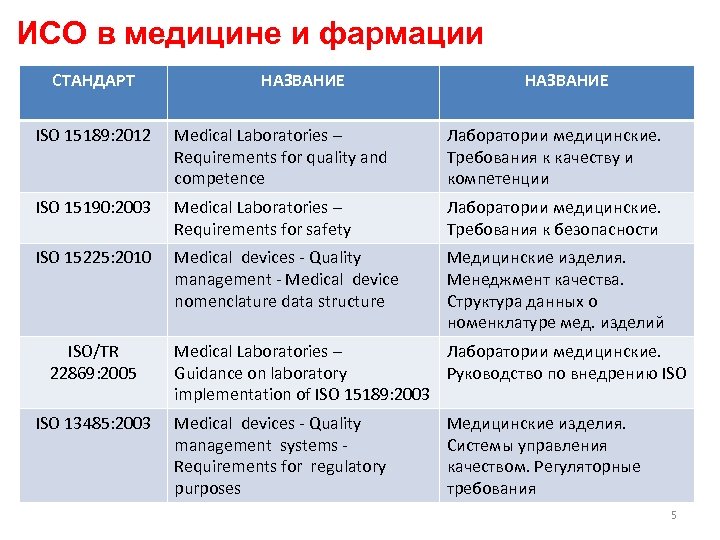
ИСО в медицине и фармации СТАНДАРТ НАЗВАНИЕ ISO 15189: 2012 Medical Laboratories – Requirements for quality and competence Лаборатории медицинские. Требования к качеству и компетенции ISO 15190: 2003 Medical Laboratories – Requirements for safety Лаборатории медицинские. Требования к безопасности ISO 15225: 2010 Medical devices - Quality management - Medical device nomenclature data structure Медицинские изделия. Менеджмент качества. Структура данных о номенклатуре мед. изделий ISO/TR 22869: 2005 ISO 13485: 2003 Medical Laboratories – Лаборатории медицинские. Guidance on laboratory Руководство по внедрению ISO implementation of ISO 15189: 2003 Medical devices - Quality management systems Requirements for regulatory purposes Медицинские изделия. Системы управления качеством. Регуляторные требования 5

Внедрение системы качества Первый этап - анализ существующей ситуации в организации и обучение персонала; Второй этап - разработка документации и изменение работы сотрудников; Третий этап - проведение внутреннего аудита системы качества. 6

Анализ существующей ситуации в организации и обучение персонала 1. Издается приказ по предприятию о начале работ по системе качества; 2. Проводится обучение участников рабочей группы менеджменту качества и требованиям стандартов ИСО серии 9000; 3. Осуществляется анализ текущей ситуации. 7

Разработка документации и изменение работы сотрудников 1. Проводится планирование по организации системы качества; 2. Осуществляется определение и документирование процессов организации; 3. Проводится документирование и внедрение процедур системы менеджмента качества. 8

Проведение внутреннего аудита системы качества 1. Назначается команда аудиторов, подготавливается план и программа проведения аудита в подразделениях, вопросники для проведения аудита, издается приказ о проведении аудита; 2. Проведение аудитных бесед; 3. Осуществляется подготовка отчета об аудите и плана корректирующих действий. 9
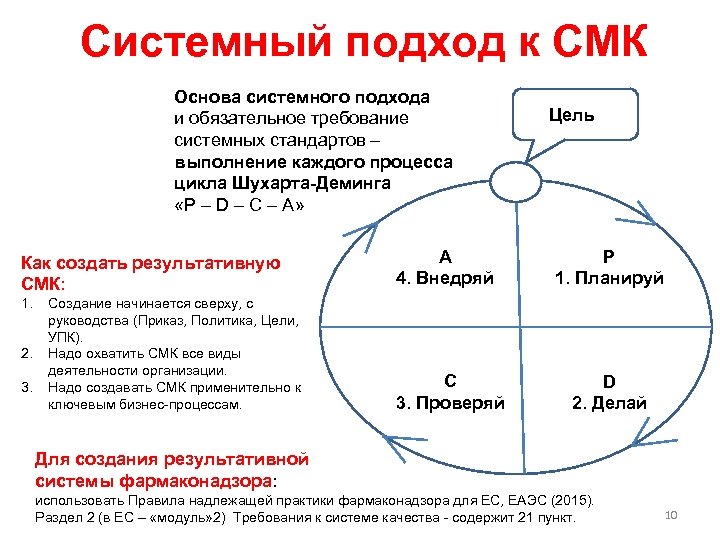
Системный подход к СМК Основа системного подхода и обязательное требование системных стандартов – выполнение каждого процесса цикла Шухарта-Деминга «P – D – C – A» Как создать результативную СМК: 1. 2. 3. Создание начинается сверху, с руководства (Приказ, Политика, Цели, УПК). Надо охватить СМК все виды деятельности организации. Надо создавать СМК применительно к ключевым бизнес-процессам. А 4. Внедряй С 3. Проверяй Цель Р 1. Планируй D 2. Делай Для создания результативной системы фармаконадзора: использовать Правила надлежащей практики фармаконадзора для ЕС, ЕАЭС (2015). Раздел 2 (в ЕС – «модуль» 2) Требования к системе качества - содержит 21 пункт. 10
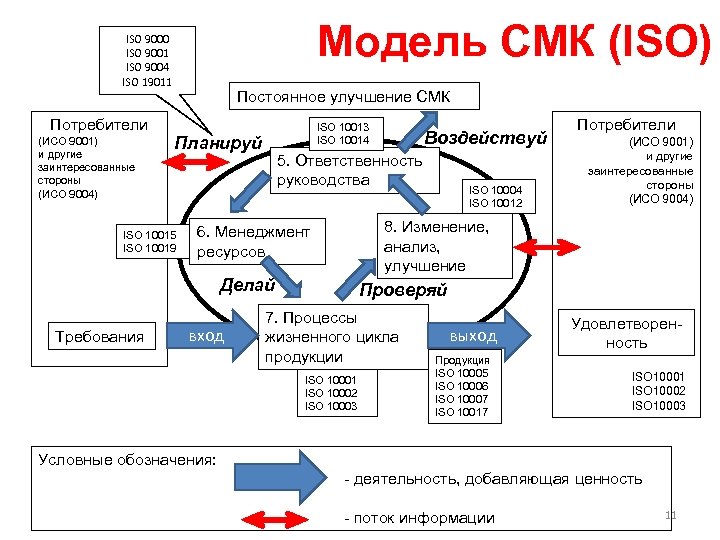
Модель СМК (ISO) ISO 9000 ISO 9001 ISO 9004 ISO 19011 Потребители (ИСО 9001) и другие заинтересованные стороны (ИСО 9004) Постоянное улучшение СМК ISO 10013 ISO 10014 Планируй ISO 10015 ISO 10019 5. Ответственность руководства вход ISO 10004 ISO 10012 Потребители (ИСО 9001) и другие заинтересованные стороны (ИСО 9004) 8. Изменение, анализ, улучшение 6. Менеджмент ресурсов Делай Требования Воздействуй Проверяй 7. Процессы жизненного цикла продукции ISO 10001 ISO 10002 ISO 10003 выход Продукция ISO 10005 ISO 10006 ISO 10007 ISO 10017 Удовлетворенность ISO 10001 ISO 10002 ISO 10003 Условные обозначения: - деятельность, добавляющая ценность - поток информации 11

2. Требования к системе качества (в этом разделе 21 пункт) 2. 1. Система качества должна включать надлежащее управление ресурсами, контроль соответствия нормативным требованиям и управление документацией. 2. 1. 2 Система качества предусматривает: а) создание структуры системы и планирование интегрированных и согласованных процессов (планирование качества); б) выполнение задач и обязанностей системы качества (контроль качества); в) контроль и оценку эффективности работы структур и процессов системы качества (обеспечение качества); г) корректировку и улучшение структуры и процессов системы качества (улучшение качества). 2. 1. 3. Общими целями системы качества в системе фармаконадзора являются: а) выполнение нормативных требований (норм регулирования)и обязанностей по фармаконадзору; б) предотвращение нежелательных последствий применения зарегистрированных лекарственных препаратов; в) обеспечение применения лекарственных препаратов при превышении пользы над риском; г) содействие защите здоровья пациентов и общественного здоровья. 12

2. 2. Принципы надлежащей практики фармаконадзора 2. 2. 1. Для выполнения общих целей качества, изложенных в пункте 2. 1. 3, следует придерживаться следующих принципов : а) обеспечение удовлетворения требований пациентов, медицинских работников и общества в целом в отношении безопасности лекарственных препаратов; б) обеспечение эффективного руководства по внедрению системы качества и мотивации персонала; в) вовлечение всех сотрудников организации (предприятия) в процесс поддержки системы фармаконадзора на уровне возложенных на них обязанностей; г) вовлечение всех сотрудников организации в постоянный процесс повышения качества системы фармаконадзора; д) организация ресурсной базы и поставленных перед системой фармаконадзора задач в форме структур и процессов таким образом, чтобы обеспечивать активную, соответствующую уровню риска, непрерывную работу по фармаконадзору; е) необходимо учитывать и оценивать все имеющиеся доказательные данные по соотношению польза-риск и все данные, которые могут оказать влияние на данное соотношение и применение лекарственного препарата, должны рассматриваться и оцениваться для принятия дальнейших решений; ж) содействие развитию эффективного сотрудничества между разработчиками, держателями регистрационных удостоверений, регуляторными органами, учреждениями здравоохранения, пациентами, медицинскими работниками, научными организациями и другими заинтересованными сторонами в соответствии с условиями действующего законодательства. 13

2. 3. Ответственные за систему качества 2. 3. 1. Обеспечение работы системы фармаконадзора в соответствии с требованиями к системе качества является ответственностью всех специалистов, выполняющих работу по организации системы качества Необходимо обеспечить системный подход по внедрению и поддержанию системы качества на надлежащем уровне. Организация должна обеспечить достаточное количество компетентных и обученных специалистов, имеющих соответствующую профессиональную подготовку, для выполнения требуемого объема работ по фармаконадзору на надлежащем уровне. 14

Обеспечение соответствия нормативным требованиям (нормам регулирования) регуляторными органами 2. 7. 1. Регуляторные органы должны иметь соответствующую систему обеспечения качества процессов с целью обеспечения: а) оценки качества представляемых данных по фармаконадзору; б) оценки и обработки данных по фармаконадзору в соответствии с действующими законодательными требованиями; в) гарантированной независимости в выполнении деятельности по фармаконадзору; г) эффективного информирования пациентов, медицинских работников, держателей регистрационных удостоверений и общества в целом; д) проведения инспекций, включая дорегистрационное инспектирование. 2. 7. 2. Независимость в выполнении деятельности по фармаконадзору определяется принятием всех регуляторных решений только в интересах здоровья пациента и общественного здоровья. 15

2. 8. Управление документацией 2. 8. 1. Система управления документацией является частью системы качества, распространяется на все документы системы фармаконадзора и обеспечивает возможность поиска данных и прослеживаемость выполняемых процедур, включая процедуры по оценке новых данных по безопасности в отношении времени выполнения оценки и принятых решений. 2. 8. 2. Система управления документацией должна обеспечивать: а) качество данных по фармаконадзору, включая полноту, точность и целостность; б) эффективную внутреннюю и внешнюю передачу данных; в) сохранение документов, имеющих отношение к системам фармаконадзора и осуществления фармаконадзора по каждому из лекарственных препаратов, согласно применимым срокам хранения. 2. 8. 3. Держатель регистрационного удостоверения должен обеспечить надлежащее документирование, обращение и хранение всей информации по фармаконадзору с целью выполнения процедур точного репортирования, интерпретации и верификации данных. Держателем регистрационного удостоверения должна быть обеспечена система прослеживаемости и последующей оценки сообщений о нежелательных реакциях. 2. 8. 4. Система управления документацией должна включать комплекс мер по обеспечению безопасности и конфиденциальности данных в целях выполнения требований по защите персональных данных пациентов в соответствии с требованиями законодательства. Указанные меры должны включать строгое ограничение доступа к документации и базам данных только уполномоченных лиц. 2. 8. 5. Система управления документацией должна включать в себя процессы 16 обеспечения защиты информации по фармаконадзору от потери и разрушения.

2. 9. Документация системы качества 2. 9. 1. Все элементы, требования и положения системы качества должны быть документированы и систематизированы соответствующим образом в форме письменных руководств и процедур, таких как план по качеству, руководство по качеству и отчеты по качеству. 2. 9. 2. План по качеству определяет основные цели системы качества и процессы, которые должны быть внедрены для достижения поставленных целей. Процедуры по качеству представляют собой описание установленного порядка выполнения процессов и могут иметь форму стандартных операционных процедур и других форм рабочих инструкций или руководств. Руководство по качеству определяет область распространения системы качества, процессы системы качества и их взаимосвязь. Отчеты по качеству включают полученные результаты работы системы либо подтверждения выполняемой деятельности. 17

2. 9. Документация системы качества 2. 9. 3. Система качества должна быть отражена в следующих документах: а) документация по организационной структуре и обязанностям персонала; б) план обучения и отчеты по проведенному обучению; в) инструкции по соответствию процессов управления; г) инструкции по критическим процессам фармаконадзора, включая обеспечение непрерывности процесса; д) индикаторы выполнения процессов, которые используются для постоянного мониторирования надлежащего выполнения функций по фармаконадзору; е) отчеты по аудиту и последующему аудиту системы качества, включая полученные данные и результаты. 2. 9. 4. Документация по системе качества должна также включать: а) методы мониторирования эффективности функционирования системы качества и, в частности, ее способность выполнения задач системы качества; б) отчеты по результатам выполненных процедур по фармаконадзору, подтверждающие выполнение всех предусмотренных этапов и действий; в) документы и отчеты по средствам и оборудованию, включая проверку функциональных свойств, деятельность по квалификации и валидации, которые подтверждают выполнение всех стадий соответствующих требований, протоколов и процедур; г) отчеты, подтверждающие контроль отклонений от установленной системы качества, принятие предупредительных и корректирующих мероприятий, оценку 18 эффективности принятых мер.

2. 11. Дополнительная документация по системе качества регуляторных органов В дополнение к требуемой документации по системе качества, регуляторный орган должен документировать организационную структуру, распределение задач и ответственности всего персонала, а также определить контактные лица для обеспечения взаимодействия между регуляторными органами, держателями регистрационных удостоверений и лицами, представляющими информацию по рискам, связанным с лекарственными препаратами. 19

2. 19. Общие обязанности по фармаконадзору в рамках международных договоров и актов, составляющих право СОЮЗА 2. 19. 1 Уполномоченные органы государств-членов несут ответственность за выполнение задач по фармаконадзору, возлагаемых на них законодательством государства-члена, международными договорами и актами, составляющими право Союза. С этой целью каждый уполномоченный орган государства-члена обеспечивает функционирование системы фармаконадзора, создает и применяет надлежащую эффективную систему качества осуществляемой деятельности по фармаконадзору. 2. 19. 2. Государства-члены сотрудничают с целью постоянного совершенствования систем фармаконадзора по достижению высоких стандартов защиты здоровья общественности, включая использование объединенных ресурсов в целях оптимизации использования имеющейся ресурсной базы в рамках Союза. 2. 19. 3. Государства-члены определяют контактные точки с целью упрощения взаимодействия уполномоченных органов государств-членов, держателей регистрационных удостоверений и лиц, представляющих информацию по фармаконадзору. 20

2. 20. Функции регуляторных органов государств-членов 2. 20. 1. Каждое государство-член должно назначить уполномоченный орган, ответственный за осуществление фармаконадзора. 2. 20. 2. Каждый уполномоченный орган государства-члена должен внедрить и обеспечить эффективное функционирование системы фармаконадзора при выполнении своих задач и участии в деятельности по фармаконадзору в рамках Союза. В данном контексте уполномоченный орган государства-члена отвечает за контроль безопасности каждого лекарственного препарата, зарегистрированного на территории государства-члена. 2. 20. 3. Задачи и обязанности уполномоченных органов по фармаконадзору включают в себя сотрудничество при обнаружении сигналов и применение мер минимизации риска принятии соответствующих решений. 2. 20. 4. Уполномоченные органы государств-членов отвечают за проверку осуществления держателями регистрационных удостоверений фармаконадзора лекарственных препаратов на своей территории, включая выполнение инспекций систем фармаконадзора держателей регистрационных удостоверений. Уполномоченный орган каждого государства-члена обеспечивает представление всех данных по каждой из процедур по фармаконадзору в уполномоченные органы других государств-членов в соответствии с законодательством государства-члена, международными договорами и актами, составляющими право Союза. 21

2. 21. Планирование готовности к фармаконадзору при возникновении экстренных ситуаций в общественном здравоохранении 2. 21. 1. Системы фармаконадзора держателей регистрационных удостоверений и уполномоченных органов государств-членов должны быть адаптированы к экстренным ситуациям в общественном здравоохранении. По мере необходимости должны быть разработаны планы готовности. Экстренная ситуация в общественном здравоохранении представляет собой угрозу общественному здоровью, признанную Всемирной Организацией Здравоохранения (ВОЗ) либо уполномоченными органами государств-членов. Требования фармаконадзора к экстренным ситуациям в общественном здравоохранении оцениваются уполномоченными органами государств-членов на индивидуальной основе. О требованиях фармаконадзора сообщается держателям регистрационных удостоверений и общественности. Уполномоченные органы государств-членов публикуют уведомления об экстренных ситуациях на своих официальных сайтах. 22

Спасибо за внимание! 23
6fddc0dd740d64aca190ef3b2eb9fa98.ppt