Лекция_19.ppt
- Количество слайдов: 31

СЕМЕЙСТВО МАКРОМОЛЕКУЛ В ЕДИНИЧНОМ ОБЪЕМЕ 1. Средние молекулярные массы полимеров. ММР. Полидисперсность. Фракционирование полимеров. Физико-химические основы фракционирования. 2. Структурообразование в полимерном теле и структурная организация аморфных полимеров. Надмолекулярные структуры аморфных полимерных тел. Примеры организации упорядоченного состояния. Сравнение с низкомолекулярными телами. ПОЛИМЕРНОЕ ТЕЛО 1. Агрегатные, фазовые и физические состояния полимерных тел. Деформация полимеров. Термомеханический метод изучения механических свойств физических тел. Три физических состояния аморфных полимерных тел. Характеристика стеклообразного состояния. Вынужденная высокоэластичность. Хрупкость полимерных тел. Характеристика высокоэластического состояния. Термодинамика и молекулярный механизм высокоэластической деформации. Вязко-текучее состояние полимеров. Механизм и закон вязкого течения. Зависимость вязкого течения от молекулярной массы. 2. Условия кристаллизации полимеров. Термомеханическая кривая кристаллического тела. Изотермы растяжения. Рекристаллизация полимерного тела. Ориентированные структуры полимеров. Физико-механические свойства аморфных и кристаллических полимерных тел. Пластификация полимеров. 3. Релаксационные явления в твердых полимерных телах (крип, упругий гистерезис). 4. Композиционная неоднородность. Микроструктурная неоднородность. Лекция 22 1
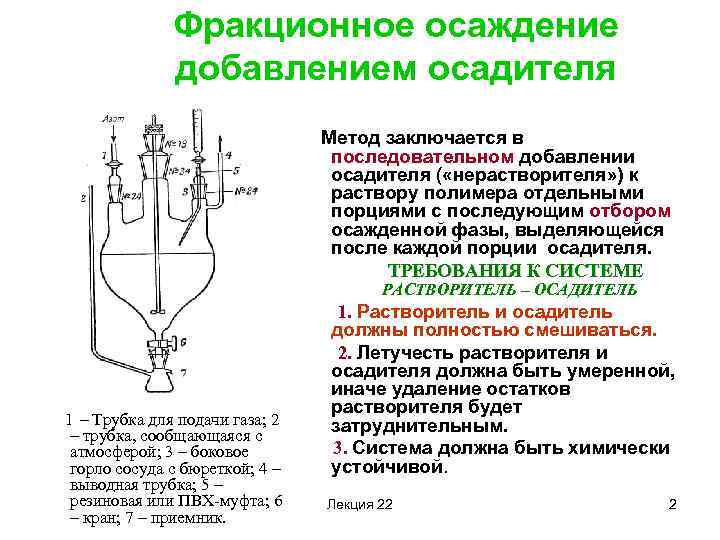
Фракционное осаждение добавлением осадителя Метод заключается в последовательном добавлении осадителя ( «нерастворителя» ) к раствору полимера отдельными порциями с последующим отбором осажденной фазы, выделяющейся после каждой порции осадителя. ТРЕБОВАНИЯ К СИСТЕМЕ РАСТВОРИТЕЛЬ – ОСАДИТЕЛЬ 1 – Трубка для подачи газа; 2 – трубка, сообщающаяся с атмосферой; 3 – боковое горло сосуда с бюреткой; 4 – выводная трубка; 5 – резиновая или ПВХ-муфта; 6 – кран; 7 – приемник. 1. Растворитель и осадитель должны полностью смешиваться. 2. Летучесть растворителя и осадителя должна быть умеренной, иначе удаление остатков растворителя будет затруднительным. 3. Система должна быть химически устойчивой. Лекция 22 2

Средние молекулярные массы fn = fm = Массовые (fm) и численные (fn) доли Лекция 22 3

Полидисперсность полимеров fm = F fn = Образец любого синтетического полимера является полидисперсным. Полидисперсность описывается с помощью функции распределения по ММ (f (Mi)), M Пример. Пусть образец состоит из десяти равных по массе фракций с ММ 1000: 10, 20, 30, 40, 50, 60, 70, 80, 90 и 100. Посчитаем средние ММ: =M 1 f 1+M 2 f 2+M 3 f 3+…+Mxfx=0. 1 (10000+20000+30000+ +100000) =55000 и =1/( = fi. Мi )= 1/ [0. 1 ( и + =1/( fi/Мi). + Лекция 22 + …+ )]=34000. 55000: 34000=1. 62 4
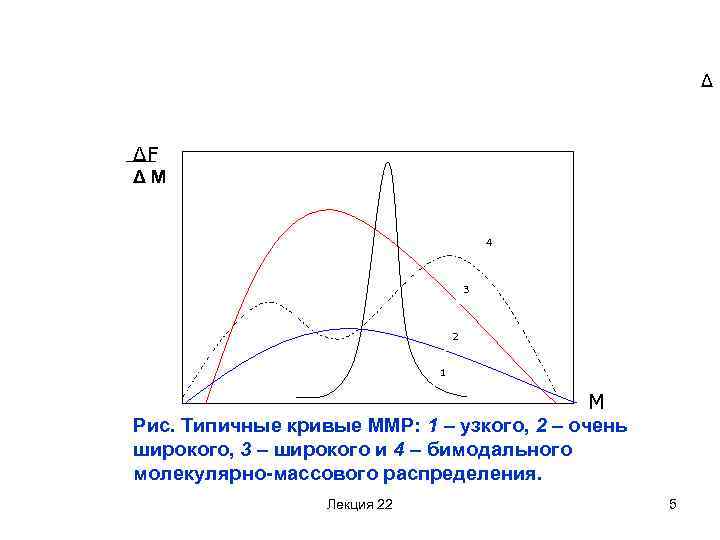
Δ ΔF ΔM 4 3 2 1 M Рис. Типичные кривые ММР: 1 – узкого, 2 – очень широкого, 3 – широкого и 4 – бимодального молекулярно-массового распределения. Лекция 22 5
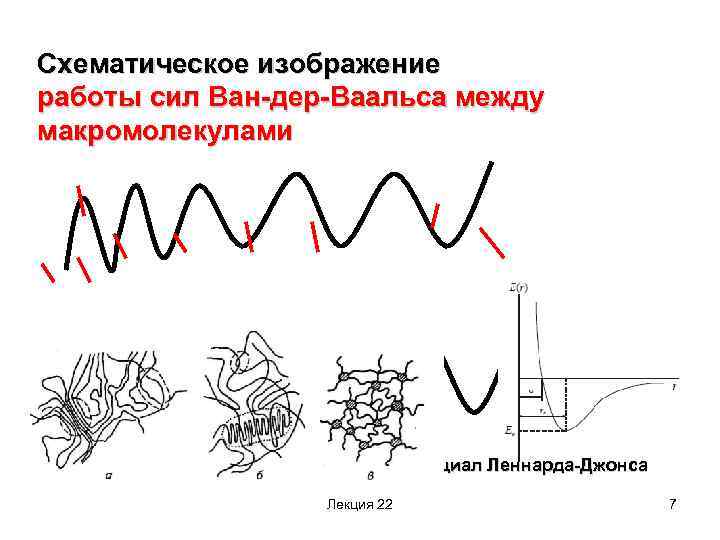
Схематическое изображение работы сил Ван-дер-Ваальса между макромолекулами Потенциал Леннарда-Джонса Лекция 22 7
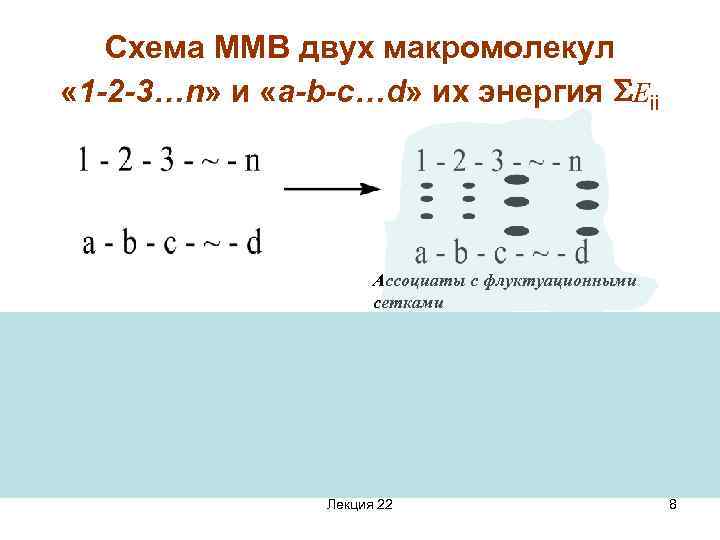
Схема ММВ двух макромолекул « 1 -2 -3…n» и «a-b-c…d» их энергия Еii Ассоциаты с флуктуационными сетками Евзаим пропорциональна числу повторяющихся звеньев, т. е ~ ММ Лекция 22 8

Макромолекулы вступают в интенсивную ассоциацию за счет работы межмолекулярных сил, образуя сначала надмолекулярные структуры, затем полимерное тело. Тела могут находиться в двух агрегатных и двух фазовых состояниях: твердом и жидком. Высокомолекулярные соединения не могут образовать газовую фазу. При анализе фазовых и агрегатных переходов высокомолекулярных веществ следует учитывать особое свойство макромолекул – их гибкость. Лекция 22 9
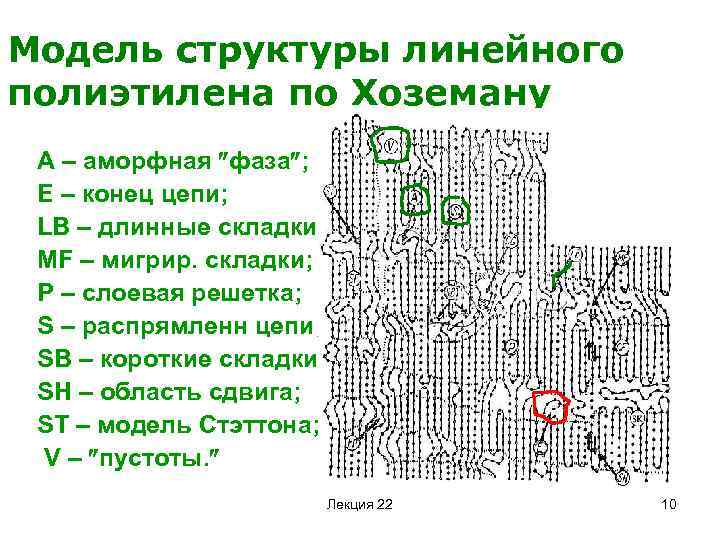
Модель структуры линейного полиэтилена по Хоземану A – аморфная фаза ; E – конец цепи; LB – длинные складки; MF – мигрир. складки; P – слоевая решетка; S – распрямленн цепи; SB – короткие складки; SH – область сдвига; ST – модель Стэттона; V – пустоты. Лекция 22 10

Схема строения флуктуационных сеток а – ассоциат с параллельной укладкой сегментов; б – ассоциат складчатый; в – схема флуктуационной сетки с проходными молекулами, соединяющими узлы сетки Лекция 22 11
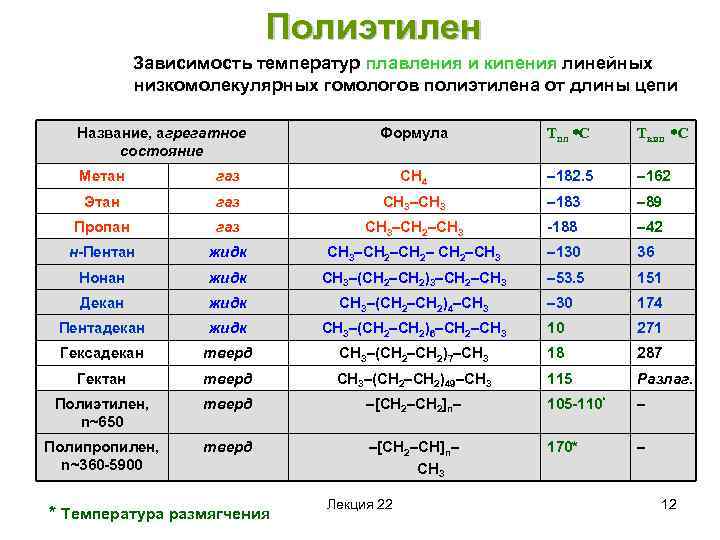
Полиэтилен Зависимость температур плавления и кипения линейных низкомолекулярных гомологов полиэтилена от длины цепи Название, агрегатное состояние Формула Тпл ºС Ткип ºС – 182. 5 – 162 Метан газ СН 4 Этан газ СН 3–СН 3 – 183 – 89 Пропан газ СН 3–СН 2–СН 3 -188 – 42 н-Пентан жидк СН 3–СН 2–СН 3 – 130 36 Нонан жидк СН 3–(СН 2–СН 2)3–СН 2–СН 3 – 53. 5 151 Декан жидк СН 3–(СН 2–СН 2)4–СН 3 – 30 174 Пентадекан жидк СН 3–(СН 2–СН 2)6–СН 2–СН 3 10 271 Гексадекан тверд СН 3–(СН 2–СН 2)7–СН 3 18 287 Гектан тверд СН 3–(СН 2–СН 2)49–СН 3 115 Разлаг. Полиэтилен, n~650 тверд –[CH 2–CH 2]n– 105 -110* – Полипропилен, n~360 -5900 тверд –[CH 2–CH]n– СН 3 170* – * Температура размягчения Лекция 22 12
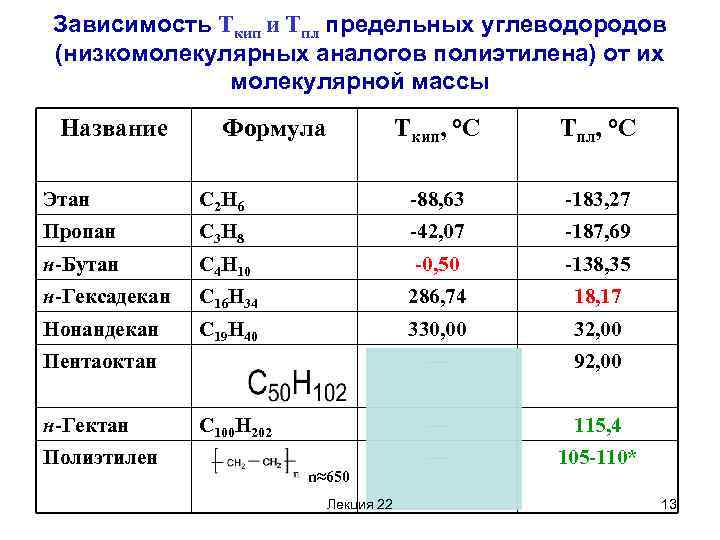
Зависимость Ткип и Тпл предельных углеводородов (низкомолекулярных аналогов полиэтилена) от их молекулярной массы Название Формула Ткип, °C Тпл, °C Этан С 2 Н 6 -88, 63 -183, 27 Пропан С 3 Н 8 -42, 07 -187, 69 н-Бутан С 4 Н 10 -0, 50 -138, 35 н-Гексадекан С 16 Н 34 286, 74 18, 17 Нонандекан С 19 Н 40 330, 00 32, 00 — 92, 00 — 115, 4 — 105 -110* Пентаоктан н-Гектан Полиэтилен С 100 Н 202 n≈650 Лекция 22 13

Генезис и морфология полимерного тела Макромолекулы, вступая в интенсивную ассоциацию за счет работы межмолекулярных сил, образуют полимерные тела, которые могут находиться только в двух агрегатных и только в двух фазовых состояниях: твердом и жидком. При анализе фазовых и агрегатных переходов высокомолекулярных веществ следует учитывать особое свойство макромолекул – их гибкость. Лекция 22 14

Условия перехода вещества из одного агрегатного состояния в другое Кинетическая энергия частицы: Е = 3/2 k. T Агрегатное состояние ↓ газообразное жидкое твердое Лекция 22 15
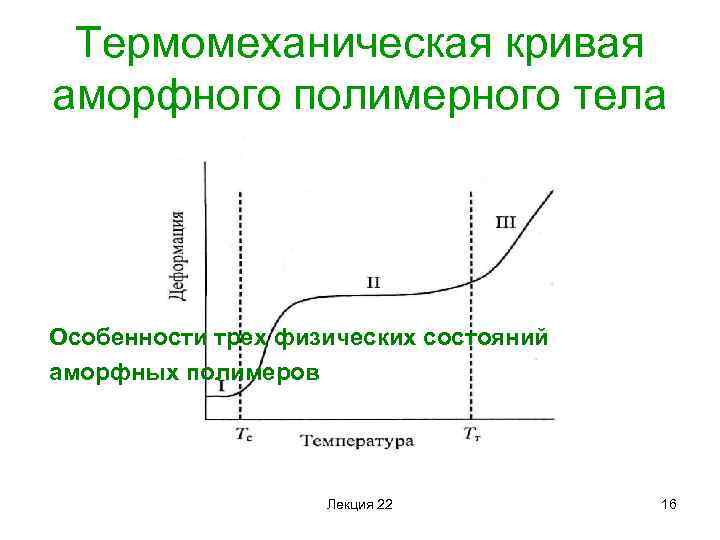
Термомеханическая кривая аморфного полимерного тела Особенности трех физических состояний аморфных полимеров Лекция 22 16
Деформация полимерного тела при постоянном объеме Лекция 22 17

ТРИ ФИЗИЧЕСКИХ СОСТОЯНИЯ ПОЛИМЕРНОГО ТЕЛА 1. СТЕКЛООБРАЗНОЕ СОСТОЯНИЕ 2. ВЫСОКОЭЛАСТИЧЕСКОЕ СОСТОЯНИЕ 3. ВЯЗКОТЕКУЧЕЕ СОСТОЯНИЕ Лекция 22 18
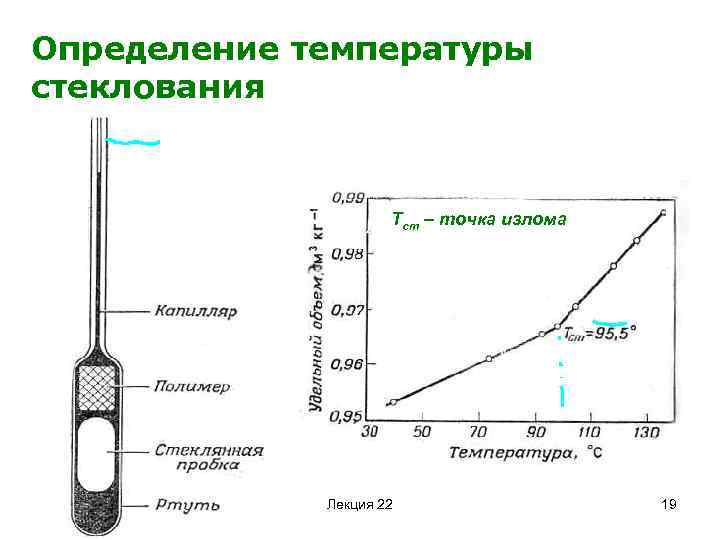
Определение температуры стеклования Тст – точка излома Лекция 22 19

Надмолекулярные структуры или надмолекулярные образования • это ассоциаты макромолекул, взаимоупорядоченных в 3 -х мерном пространстве. • Размеры этих надмолекулярных структур соизмеримы с размерами макромолекул, хотя и превосходят их на порядки. Ассоциаты образованы из макромолекул, формирующих только ближний порядок. • Они имеют самые разнообразные и причудливые геометрические формы и размеры - пачки, фибриллы, сферолиты, дендриты и др. Лекция 22 20
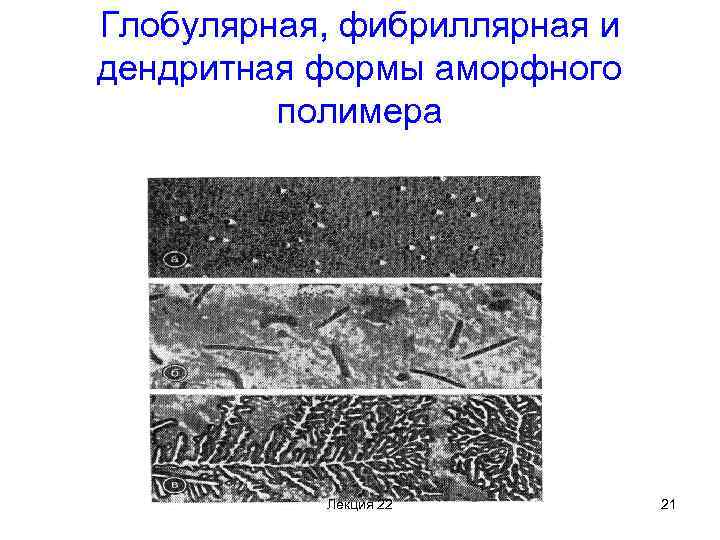
Глобулярная, фибриллярная и дендритная формы аморфного полимера Лекция 22 21

Надмолекулярные структуры аморфных полимерных тел Сферолиты Лекция 22 22

Сферолиты и кристаллы изотактического полибутадиена Лекция 22 23

Различные надмолекулярные структуры изотактического полипропилена Лекция 22 24

Кристаллизация полимерного тела • • • Увеличение упорядоченности: S 0 Выделение тепла: Н >0 F= Н - T S 0 Образование зародышей (ассоциатов) Их дальнейший рост благодаря гибкости цепей и балансу энергий: Лекция 22 25

Кристаллические полимерные тела Модель с чередующимися областями порядка и беспорядка Монокристалл полиэтилена Лекция 22 Глобулярный монокристалл вируса некроза табака 26
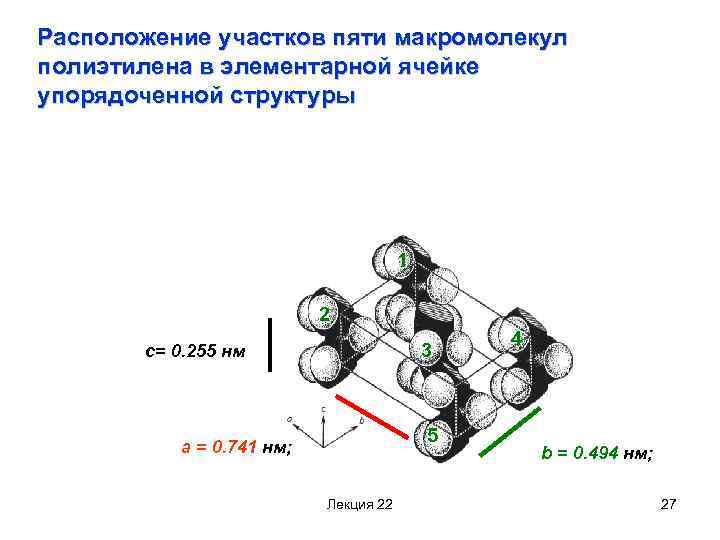
Расположение участков пяти макромолекул полиэтилена в элементарной ячейке упорядоченной структурыa = 0. 741 нм; b = 0. 494 нм; c= 0. 255 нм структуры 1 2 3 c= 0. 255 нм 5 a = 0. 741 нм; Лекция 22 4 b = 0. 494 нм; 27
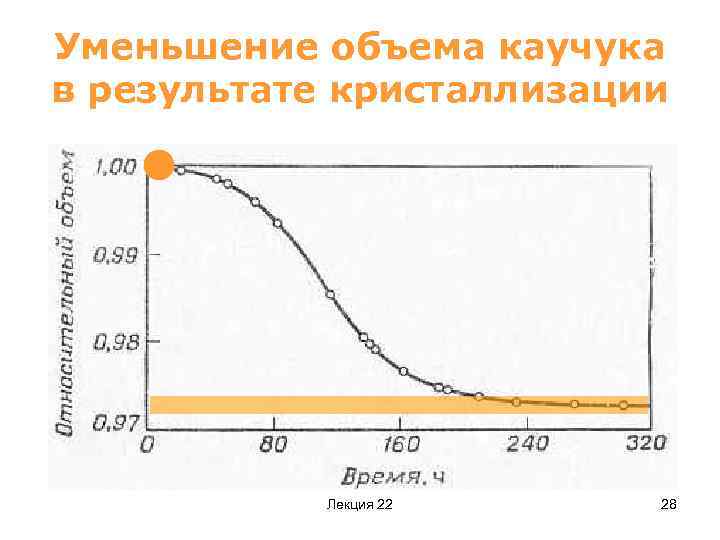
Уменьшение объема каучука в результате кристаллизации Лекция 22 28
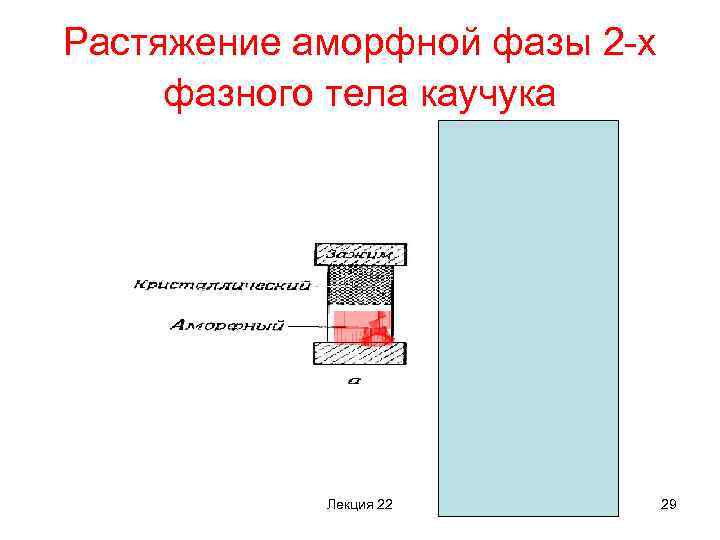
Растяжение аморфной фазы 2 -х фазного тела каучука Лекция 22 29
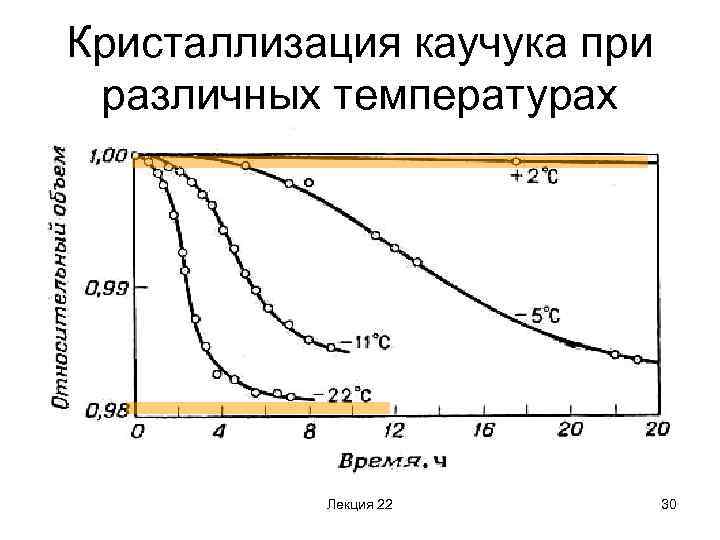
Кристаллизация каучука при различных температурах Лекция 22 30
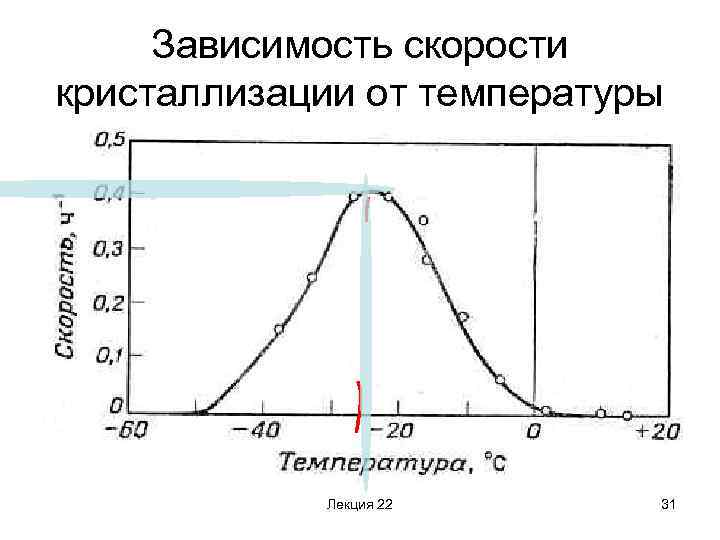
Зависимость скорости кристаллизации от температуры Лекция 22 31

Рекристаллизация полимерного тела Лекция 22 32
Лекция_19.ppt