лекция 13.ppt
- Количество слайдов: 60

Сельскохозяйственная биотехнология

Биологические методы и препараты для борьбы с вредителями и болезнями сельскохозяйственных растений и животных Наиболее распространенные инсектопатогенные бактерии и инфицируемые ими насекомые Бактерии Насекомые Pseudomonas aeruginosa Саранчи Pseudomonas septica Жук-навозник, жук-древесинник Vibrio leonardia Огневка пчелиная большая, мотылек кукурузный Enterobacter aerogenes Бабочка-голубянка, бабочка-толстоголовка Proteus vulgaris Саранчи Salmonella enteritidis Огневка пчелиная большая Diplococcus spp. Майский хрущ, шелкопряд тутовый, шелкопряд непарный, шелкопряд дубовый походный Bacillus thuringiensis Различные бабочки, моли B. popilliae Жук-навозник B. sphaericus Комары B. moritai Мухи 2

Бактерию впервые выделили из погибших шелковичных червей в начале XX века в Японии. Bacillus thuringiensis — грамположительная, спорообразующая почвенная бактерия. Клетки и специфический кристаллический белковый δэндотоксин проявляют инсектицидное действие по отношению к гусеницам многих представителей насекомых отрядов Чешуекрылые и Жёсткокрылые, личинкам москитов, мошек, нематод. Используется в биозащите растений, при помощи гена эндотоксина (Cry-токсина) осуществлена трансформация растений и получены ГМ растения, устойчивые к поеданию вредителями. Характерной морфологической особенностью является наличие кристаллов токсинов в цитоплазме, окрашиваемых красителем анилиновым чёрным.

Биологические методы и препараты для борьбы с вредителями и болезнями сельскохозяйственных растений и животных Бактериальные препараты • Энтобактерин – на основе Bac. thuringiensis var. Dalleriae; эффективен против чешуекрылых насекомых. • Дендробациллин – препарат для защиты леса от сибирского шелкопряда на основе Bac. thuringiensis var. dendrolimus. • Инсектин – предназначен для борьбы с сибирским шелкопрядом. Получен на основе Bac. thuringiensis var. insectus. • БИП – на основе Bac. thuringiensis var. darmstadiensis; эффективен против вредителей плодовых (молей, пядениц, листоверток, шелкопрядов) и овощных культур (белянок, молей). • Бактулоцид – бактерия, на основе которой выпускается данный препарат, выделена из водоема и отнесена к группе Bt H 14. 4

Технология получения δ-эндотоксина • Температуру культивирования на всех стадиях поддерживают постоянной (28 -30 о. С), продолжительность ферментации составляет 35 -40 часов. Используют дрожже-полисахаридную среду, содержащую в процентах: кормовые дрожжи - 2 -3; кукурузную муку - 1 -1. 5; кашалотовый жир - 1. р. Н составляет около 6. 3. , Культивирование заканчивают при степени споруляции 90 -95% и титре спор не менее 109 в 1 мл. После сепарации культуральной жидкости получают пасту влажностью 85% с выходом около 100 кг в 1 кубометре культуральной жидкости и титром порядка 20*109 спор в 1 грамме.

Биологические методы и препараты для борьбы с вредителями и болезнями сельскохозяйственных растений и животных Грибные препараты • Metarhizium anisopliae – наиболее известный энтомопатогенный гриб, описанный более 100 лет назад как зеленый мускаридный гриб. • Verticilium lecanii является единственным грибным энтомопатогеном, на основе которого на западе успешно выпускают препараты в промышленных масштабах. • Hirsutella thompsonii использовали некоторое время в США для производства препарата «Микар» с целью контроля численности цитрусовых клещей. • Боверин является отечественным грибным препаратом, который изготавливают на основе конидиоспор Beauveria bassiana Vuill. 6

Борьбы с грызунами • Интенсивно и в значительных масштабах бактерии используются в защите растений для борьбы с грызунами. Широко известный препарат – бактороденцид – готовится на основе вида Salmonella intepiditis, патогенного для мышей и водяных крыс. Его дусты содержат 1 млрд жизнеспособных бактериальных клеток на 1 г препарата. На практике препараты смешивают с приманкой в зависимости от объекта – с зерном или мелконарезанным картофелем, которая раскладывается в местах скопления грызунов. Норма расхода составляет 2 -5 кг/га против водяных крыс и 1 -2 кг/га против мышей.
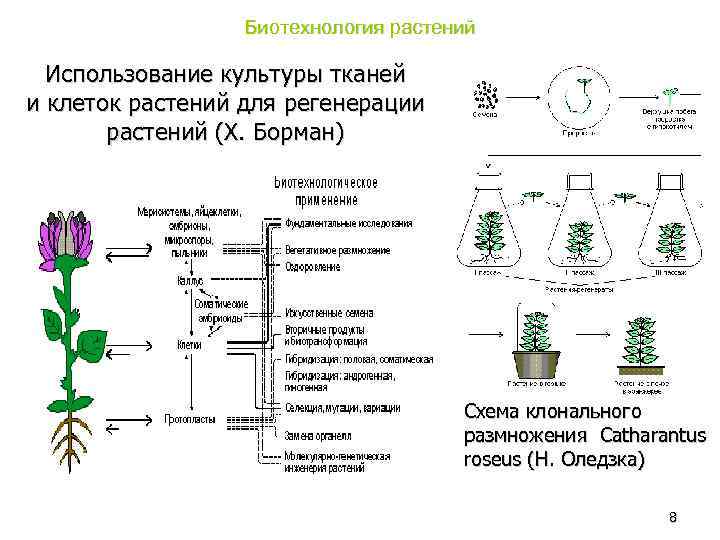
Биотехнология растений Использование культуры тканей и клеток растений для регенерации растений (Х. Борман) Схема клонального размножения Catharantus roseus (Н. Оледзка) 8
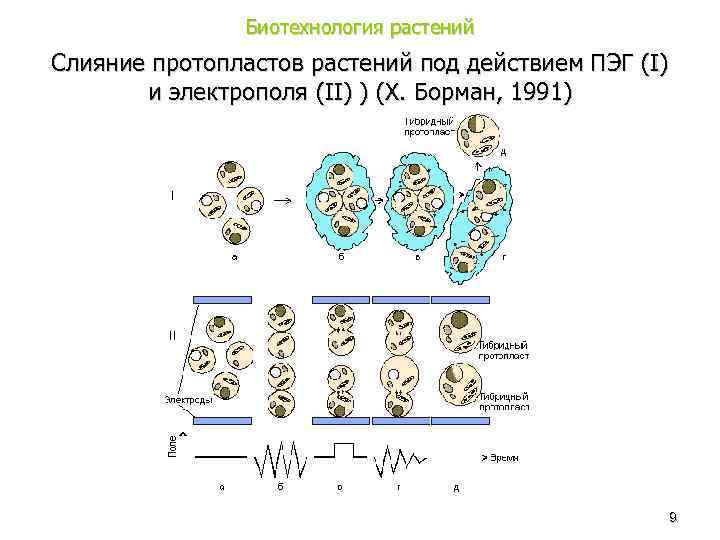
Биотехнология растений Слияние протопластов растений под действием ПЭГ (I) и электрополя (II) ) (Х. Борман, 1991) 9
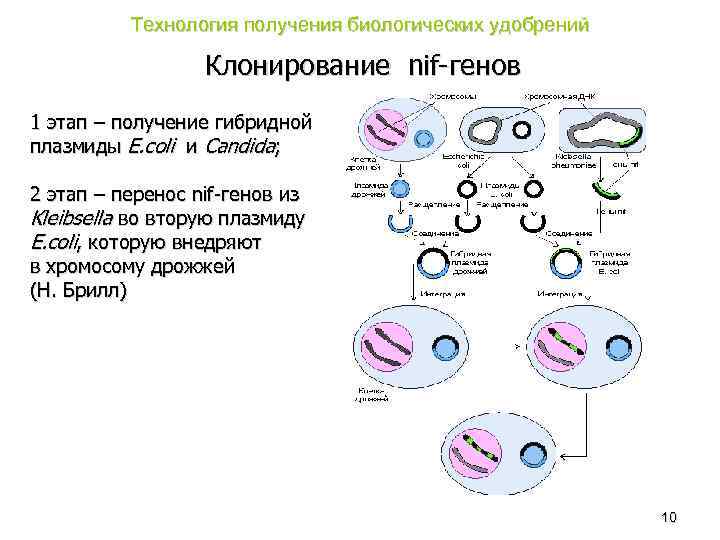
Технология получения биологических удобрений Клонирование nif-генов 1 этап – получение гибридной плазмиды E. coli и Candida; 2 этап – перенос nif-генов из Kleibsella во вторую плазмиду E. coli, которую внедряют в хромосому дрожжей (Н. Брилл) 10

Биологические методы и препараты для борьбы с вредителями и болезнями сельскохозяйственных растений и животных Вирусные препараты • «Вирин-ГЯП» (против гусеницы яблоневой плодожорки); • «Вирин-КШ» (против кольчатого шелкопряда); • «Вирин-ЭНШ» (против непарного шелкопряда); • «Вирин-ЭКС» (против капустной совки); • В США усовершенствован процесс производства нескольких вирусных препаратов для защиты лесов ( «ТМ-Биоконтрол» и «Циптек» ). 11

ПОСТГЕНОМНЫЕ ТЕХНОЛОГИИ ЭТО ТЕХНОЛОГИИ, КОТОРЫЕ ВОЗНИКЛИ НА ОСНОВЕ НАШИХ ЗНАНИЙ О ГЕНОМАХ ЖИВЫХ СИСТЕМ И, В ПЕРВУЮ ОЧЕРЕДЬ, ГЕНОМА ЧЕЛОВЕКА. ОНИ НЕ ПРИШЛИ НА СМЕНУ СУЩЕСТВОВАВШИМ ГЕНОМНЫМ ТЕХНОЛОГИЯМ, А ЯВЛЯЮТСЯ ИХ ДАЛЬНЕЙШИМ РАЗВИТИЕМ. КАКИЕ ПОСТГЕНОМНЫЕ ТЕХНОЛОГИИ В ПЕРВУЮ ОЧЕРЕДЬ ВАЖНЫ ДЛЯ МЕДИЦИНЫ? 1. ТЕХНОЛОГИИ ОПРЕДЕЛЕНИЯ ГЕНОМНОГО ПОЛИМОРФИЗМА. 2. IN SILICO ТЕХНОЛОГИИ СОЗДАНИЯ НОВЫХ ЛЕКАРСТВ. 3. ПРОТЕОМНЫЕ ТЕХНОЛОГИИ РАННЕЙ ДИАГНОСТИКИ РАКА. 4. НАНОБИОТЕХНОЛОГИИ. Выражение "in silico" используют для обозначения биологических экспериментов полностью осуществленных на компьютере

ИНДИВИДУАЛЬНОСТЬ ГЕНОМА • ОДИН ЧЕЛОВЕК ОТЛИЧАЕТСЯ ОТ ДРУГОГО НА 0. 1% ГЕНОМА • ЭТО ВСЕГО ЛИШЬ 30 ГЕНОВ ИЗ 30 ТЫСЯЧ ИЛИ 3 МЛН. ОСНОВАНИЙ ИЗ 3 МЛРД. • ***** • ВОЗМОЖНО 3 • 106 ВАРИАНТОВ ГЕНОМА • 10 2 000 КОМБИНАЦИЙ ИЗ ВАРИАНТОВ • ***** • НАСЕЛЕНИЕ ЗЕМНОГО ШАРА 6 • 109 • ЧИСЛО АТОМОВ ВО ВСЕЛЕННОЙ 1080

ОСНОВНЫЕ ЗАДАЧИ ПОСТГЕНОМНЫХ ТЕХНОЛОГИЙ 1. ГЕНОТИПИРОВАНИЕ 2000 ЧЕЛОВЕК ПО 400 000 SNP ЗА 10 000$ ИЛИ МЕНЬШЕ. 2. ВОЗМОЖНОСТЬ СЕКВЕНИРОВАТЬ ДНК СО СТОИМОСТЬЮ НА 4 -5 ПОРЯДКОВ НИЖЕ, ЧЕМ В НАСТОЯЩЕЕ ВРЕМЯ, Т. Е. ЧЕЛОВЕЧЕСКИЙ ГЕНОМ ДОЛЖЕН СТОИТЬ НЕ БОЛЕЕ 1000$. 3. НЕОБХОДИМО СОЗДАТЬ ТЕХНОЛОГИИ, ПОЗВОЛЯЮЩИЕ СИНТЕЗИРОВАТЬ ДЛИННЫЕ МОЛЕКУЛЫ ДНК ПО ЦЕНЕ НЕ БОЛЕЕ 10 ЦЕНТОВ ЗА ОСНОВАНИЕ. СТОИМОСТЬ СИНТЕЗА ОДНОГО ГЕНА ДОЛЖНА БЫТЬ НЕ ВЫШЕ 10 000 $. 4. НЕОБХОДИМО СОЗДАТЬ МЕТОДЫ ОПРЕДЕЛЕНИЯ МЕТИЛИРОВАНИЯ ВСЕЙ ДНК В ОДНОЙ КЛЕТКЕ. 5. НЕОБХОДИМЫ ТЕХНОЛОГИИ, ОБЕСПЕЧИВАЮЩИЕ ОДНОМОМЕНТНЫЙ МОНИТОРИНГ ВСЕХ БЕЛКОВ В ОДНОЙ КЛЕТКЕ.

ТЕХНОЛОГИИ ОПРЕДЕЛЕНИЯ ГЕНОМНОГО ПОЛИМОРФИЗМА Каждый вариант генома может содержать в себе сигналы, указывающие на предрасположенность конкретного индивидуума к развитию определенного рода заболеваний. Сигналы эти зачастую очень незначительны и заключаются в замене одного нуклеотида в цепочке ДНК на другой Эти замены получили название однонуклеотидных - Single Nucleotide Polymorphism (SNP).

• Вывод: зная заранее о SNP, можно, повлияв на факторы внешней среды, снизить вероятность развития заболевания, если провести соответствующие индивидуальные профилактические мероприятия.

Задачи генотипирования • выявление SNP, ассоциированных с заболеваниями • выявление SNP, ответственных за фармакокинетику и фармакодинамику лекарств. • создание индивидуального "геномного паспорта". Геномный паспорт позволит выбрать для каждого индивидуума соответствующий образ жизни. На его основе можно будет определять персонифицированное лечение, воплощая в жизнь золотой стандарт современной медицины: каждому больному - свое лекарство в нужное время и в нужной дозе. • Проведение масштабной геномной паспортизации, хотя бы в рамках мегаполиса.

Компьютерные технологии создания новых лекарств (IN SILICO ТЕХНОЛОГИИ) Ежегодно в США около 100 тыс. пациентов умирают от побочного действия лекарств. Побочные эффекты увеличивают срок пребывания в стационаре в среднем на два дня и затраты на 2500 долл. в расчете на одного пациента. Таким образом, задача создания новых, более эффективных и безопасных лекарств не только актуальна, но и одна из основных в медицине. среди востребованных медициной постгеномных технологий на первое место выдвигаются вычислительные платформы "от геномов к лекарству" Основные понятия, используемые в драг-дизайне — это мишень и лекарство. Мишенью называют макромолекулярную биологическую структуру, предположительно связанную с определенной функцией, нарушение которой приводит к заболеванию. Корректно спланированное воздействие на мишень способно улучшить течение заболевания или вылечить его. Наиболее часто встречающиеся мишени — это рецепторы и ферменты. Лекарство — это химическое соединение (как правило, низкомолекулярное), специфически взаимодействующее с мишенью и тем или иным образом модифицирующее воздействие, оказываемое ей на клетку.

этапы разработки лекарства IN SILICO • • сканирование геномов в поисках наиболее перспективных молекулярных мишеней для действия лекарств (например, ферментов или рецепторов, а также комплексов белковых молекул); получение информации о пространственной структуре отобранных макромолекул мишеней и их комплексов; поиск в базах данных лигандов, способных связываться с отобранными мишенями и путем связывания препятствовать реализации естественной функции макромолекулы, при этом высокие требования предъявляются как к алгоритмическим средствам моделирования взаимодействия между макромолекулой и лигандом, так и к мощностям вычислительных систем; экспериментальное тестирование биологической активности обнаруженных лигандов: необходимо убедится, что найденные in silico лиганды действительно работают, как в системах in vitro, так и in vivo; оптимизация фармакодинамических и фармакокинетических характеристик базовых структур: если вещество планируется как лекарство, то следует оценить его возможную токсичность, канцерогенность, способность к всасыванию и многое другое. Перспективным направлением конструирования лекарств является создание ингибиторов белок-белковых взаимодействий.

ПРОТЕОМИКА - ЭТО НОВАЯ НАУЧНАЯ ДИСЦИПЛИНА, КОТОРАЯ ЗАНИМАЕТСЯ ИНВЕНТАРИЗАЦИЕЙ БЕЛКОВ И ВЫЯВЛЯЕТ БЕЛКИ, ОТВЕТСТВЕННЫЕ ЗА ТЕ ИЛИ ИНЫЕ ПАТОЛОГИЧЕСКИЕ ПРОЦЕССЫ. - наука, основным предметом изучения которой являются белки и их взаимодействия в живых организмах, в том числе — в человеческом. Учёные, работающие в области протеомики, исследуют «производство» белков, их декомпозицию и замену белков внутри тела. Они также изучают как белки модифицируются после их синтеза в организме ПРОТЕОМИКА УСТАНАВЛИВАЕТ КОРРЕЛЯЦИЮ МЕЖДУ НАБОРОМ БЕЛКОВ, НАРАБАТЫВАЕМЫХ В ТКАНИ ИЛИ КЛЕТКЕ, И НАЧАЛОМ ИЛИ РАЗВИТИЕМ БОЛЕЗНИ. Первоочередные задачи проекта "Протеом человека" - составление протеомных карт плазмы крови, печени и мозга

ОСНОВНЫЕ ПРОБЛЕМЫ ПРОТЕОМИКИ 1. ОГРОМНОЕ РАЗНООБРАЗИЕ БЕЛКОВ: 30000 ГЕНОВ Х 200 ВОЗМОЖНЫХ МОДИФИКАЦИЙ = 6 000 БЕЛКОВ. (Задача сходна с геномикой, где определяется зависимость между болезнью и геномом, но на порядок сложнее. Дело в том, что белков намного больше, чем генов. Количество генов оценивается в 30 -40 тыс. , однако каждый ген может считываться во множестве (до 200) альтернативных вариантов, а значит, белков может быть значительно больше - до 6 -8 млн. в одной клетке. 2. ОГРОМНЫЙ ДИАПАЗОН КОНЦЕНТРАЦИЙ – ОТ НЕСКОЛЬКИХ МОЛЕКУЛ ДО СОТЕН МИЛЛИОНОВ. Каждый конкретный белок может быть экспрессирован как в виде единичных молекулярных копий, так и в огромном количестве - налицо широкий диапазон концентраций белков в клетке и биологических жидкостях. 3. ОТСУТСТВИЕ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ, Т. Е. НЕВОЗМОЖНОСТЬ РАЗМНОЖАТЬ БЕЛКИ И ТАКИМ ОБРАЗОМ РЕШИТЬ ПРОБЛЕМУ НИЗКИХ КОНЦЕНТРАЦИЙ. методической основой протеомики должен быть подход, при котором чувствительность приборов позволяет регистрировать отдельные молекулы.

Схема проведения протеомного анализа

Протеомный анализ • Использование роботизированных конвейерных линий: • устройство для сканирования двумерных электрофореграмм, сопряженное с роботом, который вырезает отмеченные оператором пятна. • Они переносятся в ячейки планшета, где происходит ферментативное расщепление белков на пептидные фрагменты. • Содержимое каждой ячейки переносится на фиксированную позицию мишени, которая помещается в масс-спектрометр. За один цикл работы масс-спектрометр снимает спектры со всех позиций мишени. Снятые масс-спектры передаются в программу идентификации белков.

Дифференциальная диагностика онкологических заболеваний с помощью протеомного подхода • Для анализа были отобраны пять групп людей: контрольная, куда вошли условно здоровые добровольцы, пациенты с доброкачественной опухолью, пациенты, страдающие раком молочной железы, пациенты с раком яичника и пациенты с раком матки. • В каждой группе было по 10 человек, у каждого проводили забор крови, согласно стандартному протоколу. Сравнительный анализ двумерных электрофореграмм выявил 18 белковых пятен, совокупность которых позволяет статистически значимо различать наличие и природу онкопатологии. После массспектрометрической идентификации пятен результаты были сведены в таблицу.
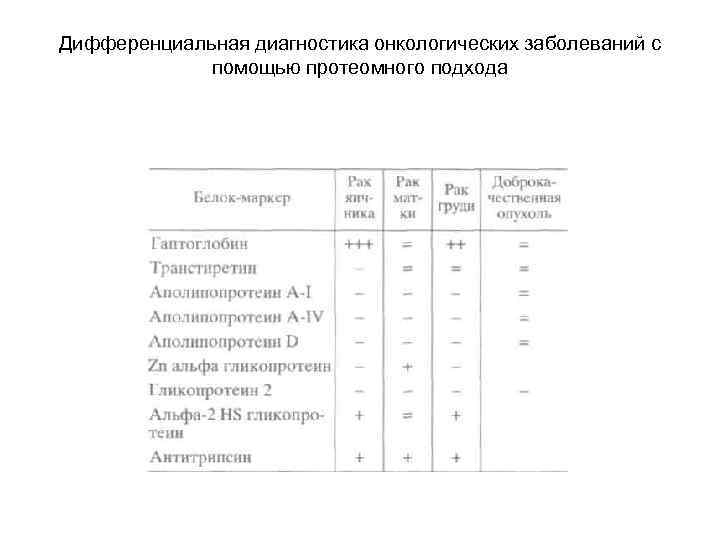
Дифференциальная диагностика онкологических заболеваний с помощью протеомного подхода

Нанобиотехнологии

МИРОВОЙ РЫНОК НАНОТЕХНОЛОГИЙ В 2015 г. ОБЩИЙ ОБЪЕМ РЫНКА- 1 ТРИЛ. $ ОСНОВНЫЕ ПРОДУКТЫ НА РЫНКЕ: А НАНОМАТЕРИАЛЫ; БНАНОБИОТЕХНОЛОГИЯ; В НАНОЭЛЕКТРОНИКА

НАНОТЕХНОЛОГИИ ЭТО ТЕХНОЛОГИИ, КОТОРЫЕ а) ИМЕЮТ ДЕЛО С ОБЪЕКТАМИ РАЗМЕРОМ НЕ БОЛЕЕ 100 nm б) ИСПОЛЬЗУЮТ ИХ УНИКАЛЬНЫЕ СВОЙСТВА , ВОЗНИКАЮЩИЕ ВСЛЕДСТВИЕ ТОГО, ЧТО В НАНОЧАСТИЦАХ, БЛАГОДАРЯ ИХ МАЛЫМ РАЗМЕРАМ, СУЩЕСТВЕННО ИЗМЕНЯЮТСЯ ФИЗИКОХИМИЧЕСКИЕ СВОЙСТВА ВЕЩЕСТВА • К арсеналу нанобиотехнологии относятся такие методы, как атомносиловая микроскопия, криомассдетекторы, спектроскопия единичных молекул и т. д. Интересным представляется подход, в котором для детекции отдельных молекул используется стандартный привод персонального компьютера для чтения компакт-дисков, превращенных в биочипы. Перспективно также создание биочипов на основе атомносиловой микроскопии.

Нанобиотехнологии • – мультимеждисциплинарная область, в которой применяются нанотехнологические методы и подходы в создании наноустройств для изучения биосистем. А так же изучаются возможности использования живых систем для создания таких устройств. в наноматериалах, в связи с мелким размером частиц все атомы и молекулы находятся на поверхности структуры, придавая ей реакционоспособость. А в обычных материалах они в основном располагаются внутри.

НАНО(БИО)ТЕХНОЛОГИИ В МЕДИЦИНЕ - НАНОМЕДИЦИНА 1. НАНОДИАГНОСТИКУМЫ. 2. НАНОЧАСТИЦЫ КАК КОНТЕЙНЕРЫ ДЛЯ ДОСТАВКИ ЛЕКАРСТВ. 3. НАНОЧАСТИЦЫ КАК ЛЕКАРСТВА. 4. СИНТЕТИЧЕСКИЕ ГЕНОМЫ В КАЧЕСТВЕ САМОРАЗМНОЖАЮЩИХСЯ СИСТЕМ. 5. НАНОРОБОТЫ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ. 6. НАНОМАТЕРИАЛЫ В РЕГЕНЕРАТИВНОЙ МЕДИЦИНЕ
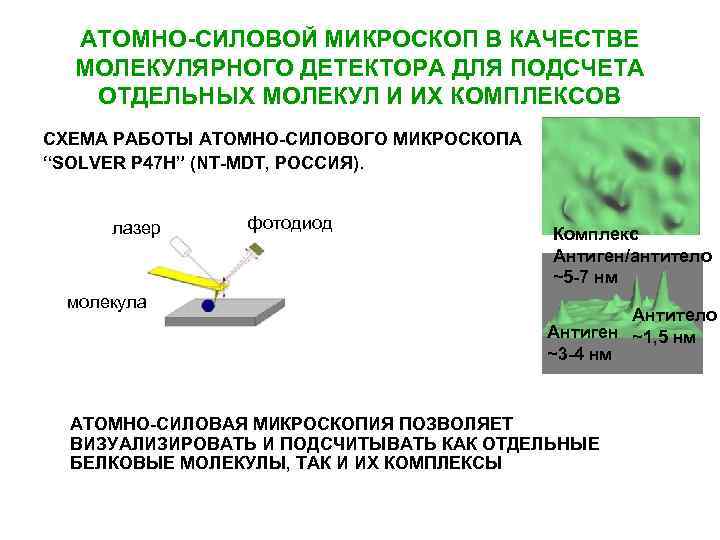
АТОМНО-СИЛОВОЙ МИКРОСКОП В КАЧЕСТВЕ МОЛЕКУЛЯРНОГО ДЕТЕКТОРА ДЛЯ ПОДСЧЕТА ОТДЕЛЬНЫХ МОЛЕКУЛ И ИХ КОМПЛЕКСОВ СХЕМА РАБОТЫ АТОМНО-СИЛОВОГО МИКРОСКОПА “SOLVER P 47 H” (NT-MDT, РОССИЯ). лазер молекула фотодиод Комплекс Антиген/антитело ~5 -7 нм Антитело Антиген ~1, 5 нм ~3 -4 нм АТОМНО-СИЛОВАЯ МИКРОСКОПИЯ ПОЗВОЛЯЕТ ВИЗУАЛИЗИРОВАТЬ И ПОДСЧИТЫВАТЬ КАК ОТДЕЛЬНЫЕ БЕЛКОВЫЕ МОЛЕКУЛЫ, ТАК И ИХ КОМПЛЕКСЫ

НАНОТЕХНОЛОГИИ В ЛЕЧЕНИИ 1. НАНОЧАСТИЦЫ КАК КОНТЕЙНЕРЫ ДЛЯ ЛЕКАРСТВ И ВАКЦИН. 2. НАНОЧАСТИЦЫ КАК ЛЕКАРСТВА 3. СИНТЕТИЧЕСКИЕ САМОРАЗМНОЖАЮЩИЕСЯ ГЕНОМЫ. 4. НАНОРОБОТЫ – НАНОУСТРОЙСТВА, РАЗЫСКИВАЮЩИЕ ВНУТРИ ОРГАНИЗМА ОЧАГИ ЗАБОЛЕВАНИЙ И УСТРАНЯЮЩИЕ ИХ. 5. НАНОУСТРОЙСТВА ВЫПОЛНЯЮЩИЕ ФУНКЦИИ ЭРИТРОЦИТОВ, ТРОМБОЦИТОВ И МАКРОФАГОВ.

Наночастицы, используемые для доставки терапевтических молекул. 1 — липосома и аденовирус; 2 — полимерная наноструктура; 3 — дендример; 4 — углеродная нанотрубка

НАНОЧАСТИЦЫ В КАЧЕСТВЕ КОНТЕЙНЕРОВ ДЛЯ ТРАНСПОРТА ЛЕКАРСТВ ИИЛИ КАК ЛЕКАРСТВА ПРЕИМУЩЕСТВА СИСТЕМ ДОСТАВКИ ЛЕКАРСТВ ПО СРАВНЕНИЮ СО СВОБОДНЫМИ ЛЕКАРСТВАМИ 1. ПОВЫШАЕТСЯ РАСТВОРИМОСТЬ МНОГИХ ЛЕКАРСТВ. . 2. УЛУЧШАЕТСЯ ИХ ПРОНИКНОВЕНИЕ В КЛЕТКИ. 3. УЛУЧШАЕТСЯ ФАРМАКОКИНЕТИКА. 4. У МНОГИХ ЛЕКАРСТВ ПОЯВЛЯЕТСЯ СПОСОБНОСТЬ ПЕРЕСЕКАТЬ МЕМБРАННЫЕ И ГЕМАТО-ЭНЦЕФАЛИЧЕСКИЙ БАРЬЕРЫ. 5. УМЕНЬШАЕТСЯ ТОКСИЧНОСТЬ
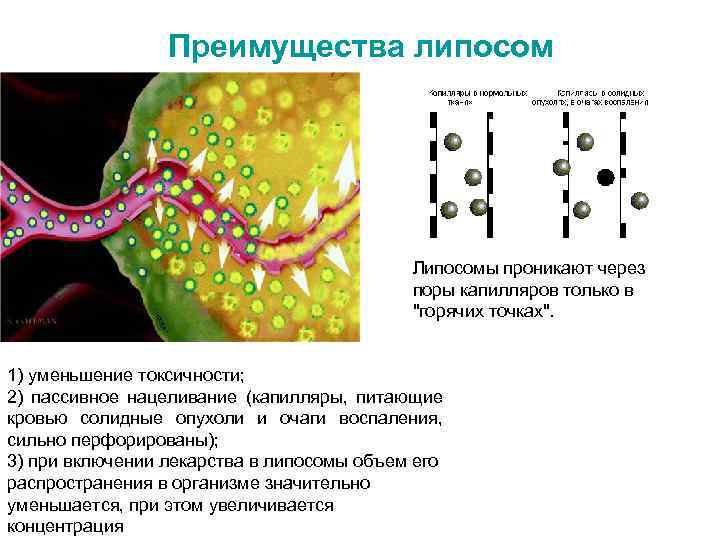
Преимущества липосом Липосомы проникают через поры капилляров только в "горячих точках". 1) уменьшение токсичности; 2) пассивное нацеливание (капилляры, питающие кровью солидные опухоли и очаги воспаления, сильно перфорированы); 3) при включении лекарства в липосомы объем его распространения в организме значительно уменьшается, при этом увеличивается концентрация
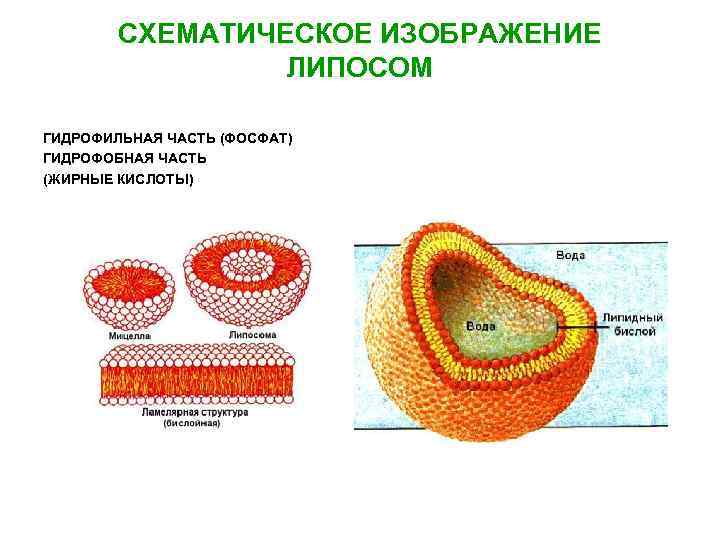
СХЕМАТИЧЕСКОЕ ИЗОБРАЖЕНИЕ ЛИПОСОМ ГИДРОФИЛЬНАЯ ЧАСТЬ (ФОСФАТ) ГИДРОФОБНАЯ ЧАСТЬ (ЖИРНЫЕ КИСЛОТЫ)

Стерически стабилизированные липосомы (Stealth liposomes). Фосфатидилэтаноламин, конъюгированный с ПЭГ, используемый для получения стерически стабилизированных липосом

Липосомы, попадая в кровоток, как правило, становятся добычей макрофагов и не доходят до цели. Но если они соединены с антителами к белкам-адресатам, то большая их часть успевает прибыть в место назначения раньше, чем произойдет встреча с макрофагом. Еще лучше результаты будут, если вперед пустить липосомы без груза, а следом – с лекарством, тогда первые попадутся макрофагам, а вторые без помех дойдут до цели.

Углеродные нанотрубки протяжённые цилиндрические структуры диаметром от одного до нескольких десятков нанометров и длиной до нескольких сантиметров состоят из одной или нескольких свёрнутых в трубку гексагональных графитовых плоскостей (графенов) и заканчиваются обычно полусферической головкой.

Возможные применения нанотрубок • • Механические применения: сверхпрочные нити, композитные материалы, нановесы Медицина. Могут легко поглощаться клетками и поэтому могут выступать в роли средств доставки различных молекул, необходимых для лечения и диагностики. Возможная токсичность этих материалов очень активно обсуждается. Применения в микроэлектронике: транзисторы, нанопровода, прозрачные проводящие поверхности, топливные элементы Для создания соединений между биологическими нейронами и электронными устройствами в новейших нейрокомпьютерных разработках Капиллярные применения: капсулы для активных молекул, хранение металлов и газов, нанопипетки Оптические применения: дисплеи, светодиоды Одностенные нанотрубки (индивидуальные, в небольших сборках или в сетях) являются миниатюрными датчиками для обнаружения молекул в газовой среде или в растворах с ультравысокой чувствительностью — при адсорбции на поверхности нанотрубки молекул её электросопротивление, а также характеристики нанотранзистора могут изменяться. Такие нанодатчики могут использоваться для мониторинга окружающей среды, в военных, медицинских и биотехнологических применениях. Ученым из лаборатории IBM удалось, на основе нанотрубок, создать микросхему, которая в 500 раз меньше аналогичной кремниевой. Исследования ведущих специалистов в данной области показывают, что потенциал кремния, как основы интегральных схем будет исчерпан в течение ближайших 10– 20 лет. Материалы из нанотрубок способны обеспечить новому поколению компьютеров практически неограниченные память и быстродействие.

Получение углеродных нанотрубок В настоящее время наиболее распространенным является метод термического распыления графитовых электродов в плазме дугового разряда. Процесс синтеза осуществляется в камере, заполненной гелием под давлением около 500 торр. При горении плазмы происходит интенсивное термическое испарение анода, при этом на торцевой поверхности катода образуется осадок, в котором формируются нанотрубки углерода. Наибольшее количество нанотрубок образуется тогда, когда ток плазмы минимален и его плотность составляет около 100 А/см 2. В экспериментальных установках напряжение между электродами обычно составляет около 15 -25 В, ток разряда несколько десятков ампер, расстояние между концами графитовых электродов 1 -2 мм. В процессе синтеза около 90% массы анода осаждается на катоде. Атомная структура поверхности углеродной нанотрубки

Типы исследованных in vivo нанотрубок: Исходные нанотрубки, плохо растворимы в водных растворах и имеют сильную склонность к агрегации (а); нанотрубки с нанесенными на поверхность амфифильными макромолекулами, например, коньюгатом липид-ПЭГ(b), сополимеров, ПАВ (с) и даже односпиральной ДНК (d), растворимость существенно повышена. Ковалентно модифицированные нанотрубки изготовлены из исходного материала с поверхностью, модифицированной либо по реакции циклоприсоединения для пришивания аммонийных групп (е), либо обработкой сильной кислотой для образования карбоксильных групп (f). Оба способа химической обработки существенно улучшают растворимость в воде.

ТРИ АЛЛОТРОПНЫХ СОСТОЯНИЯ УГЛЕРОДА • ГРАФИТ • АЛМАЗ • НАНОЧАСТИЦЫ НАНОТРУБОЧКИ, НАНОШАРИКИ (ФУЛЛЕРЕНЫ) И ДЕНДРИМЕРЫ

Фуллерены (наиболее изучена молекула С 60, имеющая в своей конструкции 60 взаимосвязанных атомов углерода) восстанавливают клеточные повреждения от активных форм кислорода, обладают антибактериальными и антивирусными свойствами. В ряде экспериментов на модельных объектах они показали противоопухолевую активность. Дендримеры ( от греч. dendron– дерево) – относятся к классу полимерных соединений. Их молекулы имеют большое число разветвлений, что позволяет прикреплять к ним лекарственные соединения для доставки в биомишени, в том числе, в раковые клетки.

ФУЛЛЕРЕНЫ И ДЕНДРИМЕРЫ ДЛЯ ТРАНСПОРТА ЛЕКАРСТВ И В КАЧЕСТВЕ ЛЕКАРСТВ СТРУКТУРЫ МОДИФИЦИРОВАННЫХ ФУЛЛЕРЕНОВ

ТРЕХМЕРНОЕ ИЗОБРАЖЕНИЕ ЧАСТИЦ ФОСФОГЛИВА НА СЛЮДЕ

НАНОЧАСТИЦЫ В КАЧЕСТВЕ БИОРОБОТОВ 1. ЭРИТРОЦИТАРНЫЕ НАНОРОБОТЫ –РЕСПИРОЦИТЫ-1 мкм СФЕРИЧЕСКИЕ ЧАСТИЧКИ АЛМАЗА. 18 МИЛЛИАРДОВ АТОМОВ УГЛЕРОДА НЕСУТ 3 МИЛЛИАРДА АТОМОВ КИСЛОРОДА И УГЛЕКИСЛОГО ГАЗА. ОНИ В 250 РАЗ ЭФФЕКТИВНЕЕ ЭРИТРОЦИТОВ. 5 МЛ РЕСПИРОЦИТОВ(5 ТРИЛЛИОНОВ НАНОРОБОТОВ ) УДВАИВАЕТ КИСЛОРОД ПЕРЕНОСЯЩИЕ ВОЗМОЖНОСТИ 5 Л КРОВИ. 2. ТРОМБОЦИТАРНЫЕ НАНОРОБОТЫ –КЛОТТОЦИТЫ. 3. ФАГОЦИТАРНЫЕ НАНОРОБОТЫ-МИКРОБИВОРСЫСФЕРИЧЕСКИЕ ЧАСТИЦЫ С ДИАМЕТРОМ 3. 4 мкм, СОДЕРЖАЩИЕ 610 МИЛЛИАРДОВ СТРОГО СТРУКТУРИРОВАННЫХ АТОМОВ. ОНИ В 80 РАЗ БОЛЕЕ ЭФФЕКТИВНЫ ПО СРАВНЕНИЮ С МАКРОФАГАМИ НА ЕДИНИЦУ ОБЪЕМА. 4. СИНТЕТИЧЕСКИЕ ГЕНОМЫ В КАЧЕСТВЕ САМОВОСПРОИЗВОДЯЩИХ СЕБЯ СТРУКТУР. МИНИМАЛЬНЫЙ ПО РАЗМЕРАМ САМОВОСПРОИЗВОДЯЩИЙСЯ ГЕНОМ (5. 4 к. В) БАКТЕРИОФАГА БЫЛ СИНТЕЗИРОВАН ЗА 14 ДНЕЙ. МИНИМАЛЬНРЫЙ РАЗМЕР МИКРОБНОГО ГЕНОМА-300 ГЕНОВ ДЛИНОЙ 150 к. В.

Искусственные клетки крови нанометрических размеров «респироциты»
Механический фагоцит - способен полностью уничтожать бактерии, вирусы и микропаразиты размером менее 2 мкм, что позволит быстро очистить кровь животного или человека от заражения.

Биосинтез магнитных наночастиц магниточувствительные бактерии – бактерии, способные ориентироваться по силовым линиям магнитного поля Земли (магнитотаксис). Эти бактерии содержат частицы магнетита Fe 3 O 4 толщиной около 150 нм. Грамотрицательные, подвижные. Electron micrographs of magnetosomes in cells of M. gryphiswaldense. (A) Chain of magnetosomes from a cell grown in the presence of a steady concentration of 30 µM Fe. Cl 3. Mature crystals, which are prevalently located in the middle of the chain, are cubo-octahedral and 45 nm in diameter. (a) Magnetospirillum magneticum с цепочками магнитосом внутри; (b) нанокристаллы магнетита, соединенные фосфолипидной мембраной. Обратите внимание на разницу в шкалах (ПЭМ). белок mms 6 можно использовать для синтеза in vitro Magnetobacterium bavaricum частиц магнетита при комнатной температуре из гидроксида железа(II).

Модели полярности магниточувствительных бактерий
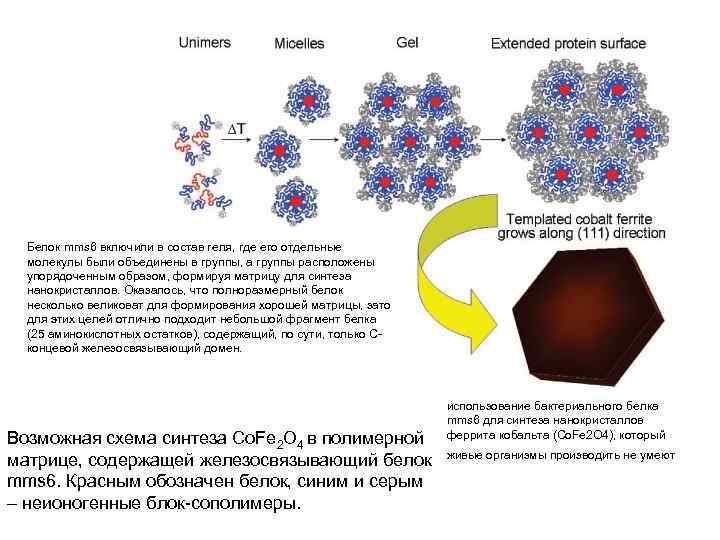
Белок mms 6 включили в состав геля, где его отдельные молекулы были объединены в группы, а группы расположены упорядоченным образом, формируя матрицу для синтеза нанокристаллов. Оказалось, что полноразмерный белок несколько великоват для формирования хорошей матрицы, зато для этих целей отлично подходит небольшой фрагмент белка (25 аминокислотных остатков), содержащий, по сути, только Сконцевой железосвязывающий домен. Возможная схема синтеза Co. Fe 2 O 4 в полимерной матрице, содержащей железосвязывающий белок mms 6. Красным обозначен белок, синим и серым – неионогенные блок-сополимеры. использование бактериального белка mms 6 для синтеза нанокристаллов феррита кобальта (Co. Fe 2 O 4), который живые организмы производить не умеют
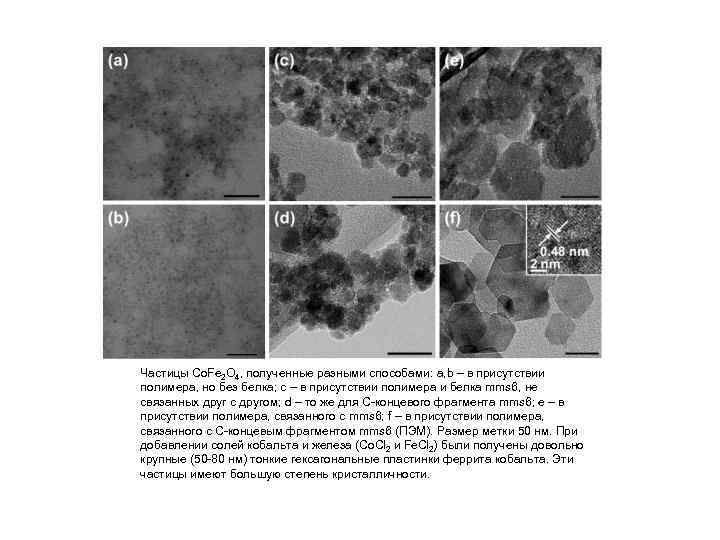
Частицы Co. Fe 2 O 4, полученные разными способами: a, b – в присутствии полимера, но без белка; c – в присутствии полимера и белка mms 6, не связанных друг с другом; d – то же для C-концевого фрагмента mms 6; e – в присутствии полимера, связанного с mms 6; f – в присутствии полимера, связанного с C-концевым фрагментом mms 6 (ПЭМ). Размер метки 50 нм. При добавлении солей кобальта и железа (Co. Cl 2 и Fe. Cl 2) были получены довольно крупные (50 -80 нм) тонкие гексагональные пластинки феррита кобальта. Эти частицы имеют большую степень кристалличности.

microaerophilic magnetic bacterium Magnetospirillum gryphiswaldense Variations of magnetism in a culture of M. gryphiswaldense during growth monitored by changes in differential light scattering (Cmag). Magnetic cells were inoculated into a medium which was constantly agitated and contained 30 µM ferric citrate. , Magnetism (M); , optical density (OD). 2 to 7 µM O 2 at 30°C. 2% iron as magnetite crystals in intracytoplasmic vesicles

Карта плазмиды p. BTN 11. Сайты рестрикции: B - Bam. HI, Bg - Bgl. II, C - Cla. I, E - Eco. RI, H - Hind. III, Hp - Hpa. I, N - Not. I, Ps - Pst. I, Pv - Pvu. II, Ss - Sst. I. Экспрессия cry 3 A-гена находится под контролем собственного промотора и двух гетерологичных промоторов: Pm и Pc (промо-тор cry 1 Ab-гена). Репликон (rep) и mob-гены принадлежат плазмиде p. NM 185

• С развитием нанотехнологий появились устройства, благодаря которым мы можем осуществлять целенаправленное манипулирование отдельными атомами, молекулами, вирусами, микроорганизмами другими частицами: видеть их, считать, диагностировать по ним состояние организма. Это другой мир. И совершенно другие возможности. Кроме того, отличительной особенностью некоторых наноструктур является их способность к самосборке и вполне вероятно в ближайшем будущем к самовоспроизведению, что заполнит ту пропасть, которая существует между живыми и неживыми системами. Даже сейчас для большинства ученых она кажется непреодолимой. А такие геномные самовоспроизводящиеся структуры уже синтезированы.

• Такие технологии лежат в основе многих новейших медицинских методов. Они применимы в диагностике для производства и транспорта лекарств; в разработке наноматериалов; для создания нанороботов. Это определило появление новой отрасли – наномедицины. Ее развитие позволит контролировать биологические системы человека на молекулярном уровне, вносить в них исправления, восстанавливать повреждения с помощью наноматериалов и наноустройств. Например, в нанодиагностике задействованы высокоточные аналитические технологии, позволяющие с помощью атомно-силовых, сканирующих электронных микроскопов, биосенсоров выявлять единичные молекулы в биоматериале, концентрировать и идентифицировать функционально значимые из них, регистрировать единичные иммунные комплексы. В ближайшем будущем эти методы станут мощным инструментом диагностики онкологических, сердечнососудистых, инфекционных, , эндокринных заболеваний, и, в первую очередь, ВИЧ-инфекций, вирусных гепатитов на самых ранних стадиях.

• Как известно, именно работа белков определяет функции, жизнедеятельность и болезни организма. Протеомный анализ позволяет диагностировать развитие патологий в организме на ранних стадиях и регистрировать новые белкимишени (биомаркеры), которые могут иметь важное диагностическое и терапевтическое значение. Особенно это важно для онкологии, потому что ранняя диагностика рака одна из основных проблем современной медицины. И здесь определенные надежды возлагаются на нанотехнологии. Если говорить о лечении, то уже появились наноматериалы, из которых делают нанолекарства - препараты нового поколения. Получены данные о возможности использования наночастиц для создания эффективных вакцин. Разработаны новые транспортные наносистемы (контейнеры) для доставки лекарств в органы -мишени. Эти разработки позволяют повысить растворимость, биодоступность, терапевтические возможности препаратов, снизить дозы и побочные эффекты, значительно уменьшив лекарственные нагрузки на организм. Перспективными для терапии, хирургии, травматологии является создание биосовместимых наноматериалов широкого спектра применения (от стоматологии до восстановления костных тканей), обладающих заместительными свойствами. То есть, технологии есть. Есть много заделов, которые разрабатываются. Необходимо, чтобы научное и медицинское сообщество повернулось к ним лицом.
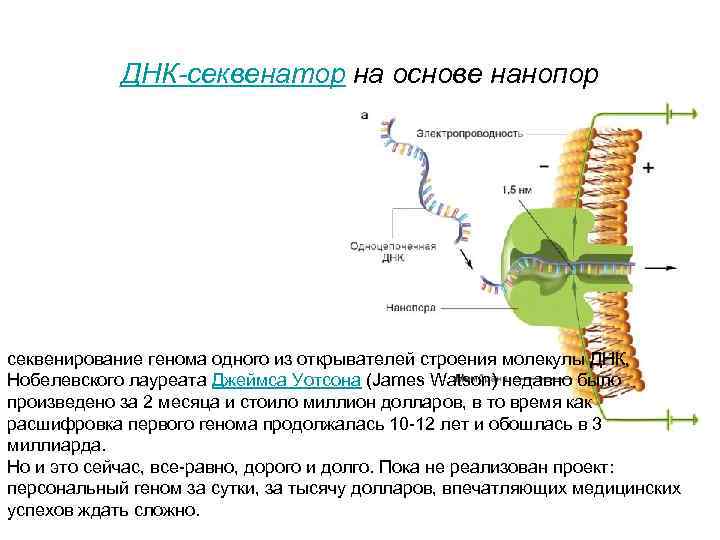
ДНК-секвенатор на основе нанопор секвенирование генома одного из открывателей строения молекулы ДНК, Нобелевского лауреата Джеймса Уотсона (James Watson) недавно было произведено за 2 месяца и стоило миллион долларов, в то время как расшифровка первого генома продолжалась 10 -12 лет и обошлась в 3 миллиарда. Но и это сейчас, все-равно, дорого и долго. Пока не реализован проект: персональный геном за сутки, за тысячу долларов, впечатляющих медицинских успехов ждать сложно.

Приоритетные технологии • развитие ранней диагностики рака, инфекционных болезней и др. , создавать биосовместимые наноматериалы, нанолекарства, нанотранспорные системы для лекарств. Надо формировать федеральные базы криобиоматериалов в медицине. Без них использование нанотехнологий не будет эффективным. Вот сейчас во всем мире, с появлением нанотехнологий возникла проблема их безопасности. Требуется развивать систему тестирования. Чтобы не оказаться в решении этой проблемы на отшибе - надо входить с мировое сообщество. Является ли наша страна членом этого сообщества, планирует ли им стать – я об этом не слышал. На повестке дня проект : “ПРОТЕОМ ЧЕЛОВЕКА“. А ведь именно при его выполнении НАНОТЕХНОЛОГИИ могут играть решающую роль.
лекция 13.ppt