анисимова замятина.ppt
- Количество слайдов: 16
 Селективная недостаточность Ig. A. Выполнили ст. гр. М-04(I)-08 Анисимова А. С. , Замятина С. И.
Селективная недостаточность Ig. A. Выполнили ст. гр. М-04(I)-08 Анисимова А. С. , Замятина С. И.
 n Иммунная недостаточность подразумевает дефицит способности распознавать, элиминировать из внутренней среды и запоминать агенты чужеродной генетической природы, прежде всего микробные. Иммунная недостаточность имеет важное значение в объяснении повышенной восприимчивости к инфекциям и некоторым другим иммунопатологическим проявлениям (аллергии, аутоиммунитету, неоплазиям).
n Иммунная недостаточность подразумевает дефицит способности распознавать, элиминировать из внутренней среды и запоминать агенты чужеродной генетической природы, прежде всего микробные. Иммунная недостаточность имеет важное значение в объяснении повышенной восприимчивости к инфекциям и некоторым другим иммунопатологическим проявлениям (аллергии, аутоиммунитету, неоплазиям).
 Клинические проявления иммунодефицитов n n n 1. Повышенная чувствительность к инфекциям: Необъяснимые хронические рецидивирующие инфекции Инфекции, вызываемые низковирулентными возбудителями или редкими возбудителями Чрезвычайно тяжелое течение инфекций 2. Аутоиммунные или воспалительные заболевания 3. В составе синдромокомплекса
Клинические проявления иммунодефицитов n n n 1. Повышенная чувствительность к инфекциям: Необъяснимые хронические рецидивирующие инфекции Инфекции, вызываемые низковирулентными возбудителями или редкими возбудителями Чрезвычайно тяжелое течение инфекций 2. Аутоиммунные или воспалительные заболевания 3. В составе синдромокомплекса
 Иммуноглобулины А (Ig. A) n n Иммуноглобулины А (Ig. A) циркулируют в сыворотке крови (составляет 15 -20% от всех Ig), а также секретируются на поверхность зпителия. Присутствуют в слюне, слёзной жидкости, молоке и на поверхности слизистых оболочек. Молекулы Ig. A участвуют в реакциях нейтрализации и агглютинации возбудителей. Кроме того, после образования комплекса Аг. АТ они участвуют в активации комплемента по альтернативному пути.
Иммуноглобулины А (Ig. A) n n Иммуноглобулины А (Ig. A) циркулируют в сыворотке крови (составляет 15 -20% от всех Ig), а также секретируются на поверхность зпителия. Присутствуют в слюне, слёзной жидкости, молоке и на поверхности слизистых оболочек. Молекулы Ig. A участвуют в реакциях нейтрализации и агглютинации возбудителей. Кроме того, после образования комплекса Аг. АТ они участвуют в активации комплемента по альтернативному пути.
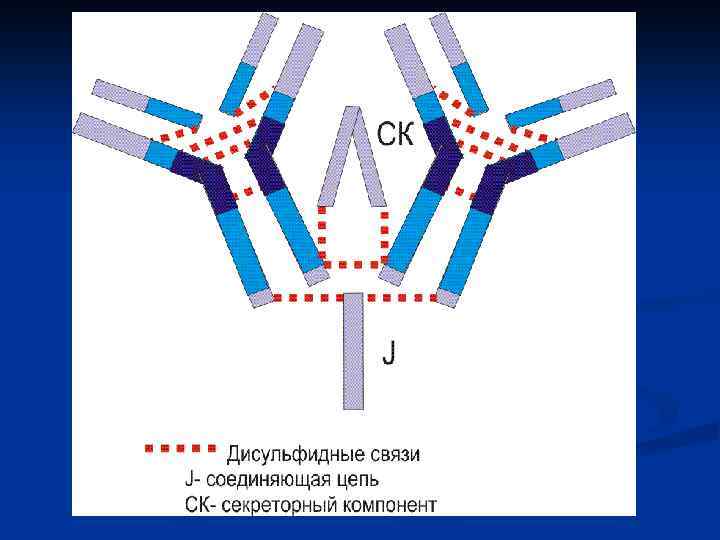
 Функция Ig. A n Основной функцией сывороточного Ig. A является нейтрализация вирусов. Его главная роль - защита дыхательных, мочеполовых путей и желудочно-кишечного тракта от инфекции. Секреторные антитела обладают выраженным антиадсорбционным действием: они препятствуют прикреплению бактерий к поверхности эпителиальных клеток, предотвращают адгезию, без которой бактериальное повреждение клетки становится невозможным. Вместе с неспецифическими факторами они обеспечивают защиту слизистых оболочек от микробов и вирусов. Ig. A не проходит через плацентарный барьер, уровень его у новорожденных около 1% от концентрации у взрослых (к году жизни этот показатель составляет всего 20% от уровня взрослых). Поэтому новорожденным в первые дни жизни секреторные Ig. A поступают с молозивом матери, защищая их дыхательные пути и желудочно-кишечный тракт до тех пор, пока не сформируются механизмы его синтеза в собственном организме. Возраст 3 мес. многими авторами определяется как критический период; этот период особенно важен для диагностики врождённой или транзиторной недостаточности местного иммунитета. Уровня, характерного для взрослого человека, достигает примерно к 5 -летнему возрасту.
Функция Ig. A n Основной функцией сывороточного Ig. A является нейтрализация вирусов. Его главная роль - защита дыхательных, мочеполовых путей и желудочно-кишечного тракта от инфекции. Секреторные антитела обладают выраженным антиадсорбционным действием: они препятствуют прикреплению бактерий к поверхности эпителиальных клеток, предотвращают адгезию, без которой бактериальное повреждение клетки становится невозможным. Вместе с неспецифическими факторами они обеспечивают защиту слизистых оболочек от микробов и вирусов. Ig. A не проходит через плацентарный барьер, уровень его у новорожденных около 1% от концентрации у взрослых (к году жизни этот показатель составляет всего 20% от уровня взрослых). Поэтому новорожденным в первые дни жизни секреторные Ig. A поступают с молозивом матери, защищая их дыхательные пути и желудочно-кишечный тракт до тех пор, пока не сформируются механизмы его синтеза в собственном организме. Возраст 3 мес. многими авторами определяется как критический период; этот период особенно важен для диагностики врождённой или транзиторной недостаточности местного иммунитета. Уровня, характерного для взрослого человека, достигает примерно к 5 -летнему возрасту.
 Селективный дефицит Ig. A • Среди больных с дефицитом Ig. A: 30% парциальный дефицит, 70% -полный. • Генетический дефект – не определен. Детерминированность на уров не. HLA-системы (гаплотип А 1, В 8, DR 3). • Патогенез: нарушение терминальной диффер енцировки Вклеток(возможен дефицит CD 40 на Влимфоцитах).
Селективный дефицит Ig. A • Среди больных с дефицитом Ig. A: 30% парциальный дефицит, 70% -полный. • Генетический дефект – не определен. Детерминированность на уров не. HLA-системы (гаплотип А 1, В 8, DR 3). • Патогенез: нарушение терминальной диффер енцировки Вклеток(возможен дефицит CD 40 на Влимфоцитах).
 • Варианты течения : 1)без клинических проявлений, по крайней мере, длительно 2)с клиническими проявлениями в виде рекуррентных инфекци й 3) в составе синдромокомплекса (атаксия-телеангиэктазия) 4)в сочетании с гипер- Ig. М • Основные клинические проявления: 1)рецидивирующие инфекции дыхательных путей и ЖКТ( цели акия, неспецифический язвенный колит, болезнь Крона). 2)иммунокомплексная патология • Лабораторная диагностика – Ig. А < 0, 05 г/л, Ig. М, Ig. G, Ig. E – N; Т и В – N. Пролиферация В ↓
• Варианты течения : 1)без клинических проявлений, по крайней мере, длительно 2)с клиническими проявлениями в виде рекуррентных инфекци й 3) в составе синдромокомплекса (атаксия-телеангиэктазия) 4)в сочетании с гипер- Ig. М • Основные клинические проявления: 1)рецидивирующие инфекции дыхательных путей и ЖКТ( цели акия, неспецифический язвенный колит, болезнь Крона). 2)иммунокомплексная патология • Лабораторная диагностика – Ig. А < 0, 05 г/л, Ig. М, Ig. G, Ig. E – N; Т и В – N. Пролиферация В ↓
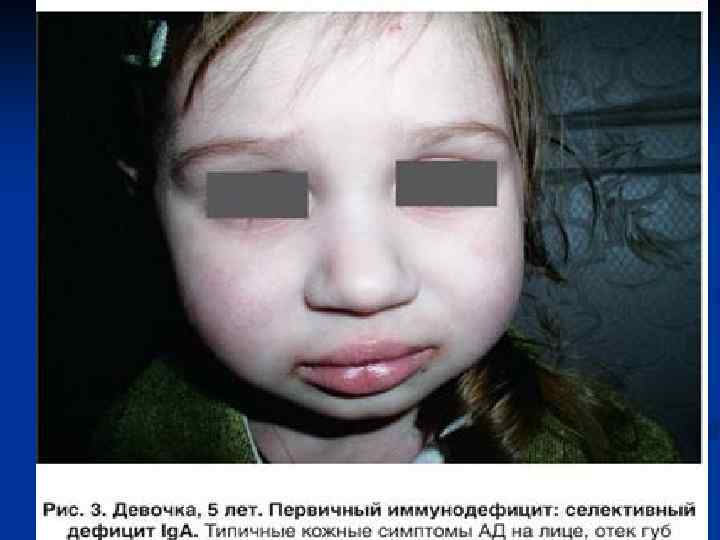
 n Основные осложнения при этом состоянии связаны с секреторным Ig. A как основным иммуноглобулином, защищающим дыхательные пути и желудочно-кишечный тракт, а также другие секреторные участки организма. Следствием его недостаточности являются рецидивирующие респираторные инфекции и различные синдромы, сопровождающиеся хронической диареей. Отмечена выраженная связь этого вида иммунологической недостаточности с аутоиммунными заболеваниями, особенно с системной красной волчанкой и ревматоидным артритом.
n Основные осложнения при этом состоянии связаны с секреторным Ig. A как основным иммуноглобулином, защищающим дыхательные пути и желудочно-кишечный тракт, а также другие секреторные участки организма. Следствием его недостаточности являются рецидивирующие респираторные инфекции и различные синдромы, сопровождающиеся хронической диареей. Отмечена выраженная связь этого вида иммунологической недостаточности с аутоиммунными заболеваниями, особенно с системной красной волчанкой и ревматоидным артритом.
 n Считается, что аутоиммунное состояние обусловлено бесконтрольным поступлением в лимфоидную систему антигенов из желудочно-кишечного тракта, вызывающим его чрезмерную стимуляцию и формирование комплексов антиген — антитело. Другой причиной такой связи может служить выраженная зависимость выработки Ig. A от сохранности функции вилочковой железы. Вероятно, о недостаточности ее функции можно судить по сниженной продукции этого иммуноглобулина. Отсутствие или недостаточность в вилочковой железе супрессорных Т-клеток могут предрасполагать к развитию аутоиммунного состояния.
n Считается, что аутоиммунное состояние обусловлено бесконтрольным поступлением в лимфоидную систему антигенов из желудочно-кишечного тракта, вызывающим его чрезмерную стимуляцию и формирование комплексов антиген — антитело. Другой причиной такой связи может служить выраженная зависимость выработки Ig. A от сохранности функции вилочковой железы. Вероятно, о недостаточности ее функции можно судить по сниженной продукции этого иммуноглобулина. Отсутствие или недостаточность в вилочковой железе супрессорных Т-клеток могут предрасполагать к развитию аутоиммунного состояния.
 n n У некоторых больных с избирательной недостаточностью Ig. A может наступить спонтанное выздоровление. Так, у двух больных с этим видом иммунологической недостаточности уровень Ig. A постепенно нормализовался в течение 3— 5 лет без какоголибо специфического лечения. Это предположение основано на том, что, во-первых, у всех обследованных до настоящего времени больных число несекретирующих лимфоцитов, несущих на своей поверхности молекулы Ig. A, находилось в пределах нормы и, во-вторых, как свидетельствуют результаты одного из исследований, эти клетки после стимуляции in vitro начинают секретировать Ig. A. Можно поэтому предположить, что возможно спонтанное выздоровление всех больных. Избирательная недостаточность Ig. A может быть спровоцирована внешними факторами, например введением фенитоина (дифенин).
n n У некоторых больных с избирательной недостаточностью Ig. A может наступить спонтанное выздоровление. Так, у двух больных с этим видом иммунологической недостаточности уровень Ig. A постепенно нормализовался в течение 3— 5 лет без какоголибо специфического лечения. Это предположение основано на том, что, во-первых, у всех обследованных до настоящего времени больных число несекретирующих лимфоцитов, несущих на своей поверхности молекулы Ig. A, находилось в пределах нормы и, во-вторых, как свидетельствуют результаты одного из исследований, эти клетки после стимуляции in vitro начинают секретировать Ig. A. Можно поэтому предположить, что возможно спонтанное выздоровление всех больных. Избирательная недостаточность Ig. A может быть спровоцирована внешними факторами, например введением фенитоина (дифенин).
 n У больных с селективной тотальной недостаточностю Ig. A сохраняется способность синтеза Ig. G-антител, а В-клетки активно отвечают на большинство антигенов. При введении больным Ig. A любого происхождения весьма вероятна выработка к нему антител, поскольку их иммунная система распознает его как чужеродный белок. Часто источником Ig. A служит иммунный сывороточный гамма-глобулин. Это обусловлено распространенной и, по нашему мнению, неоправданной практикой эмпирического введения иммунного сывороточного гамма-глобулина в качестве профилактического средства детям, страдающим частыми респираторными инфекциями, что характерно для больных с тотальным отсутствием Ig. A. В иммунном сывороточном гамма-глобулине содержатся следовые количества Ig. A, которых оказывается достаточно для сенсибилизации ребенка с тотальной недостаточностью Ig. A, но недостаточно для создания защиты от микроорганизмов, вызывающих респираторные инфекции. Если в последующем больному переливают кровь или ее продукты, содержащие значительное количество Ig. A, у него может развиться анафилактическая реакция с летальным исходом.
n У больных с селективной тотальной недостаточностю Ig. A сохраняется способность синтеза Ig. G-антител, а В-клетки активно отвечают на большинство антигенов. При введении больным Ig. A любого происхождения весьма вероятна выработка к нему антител, поскольку их иммунная система распознает его как чужеродный белок. Часто источником Ig. A служит иммунный сывороточный гамма-глобулин. Это обусловлено распространенной и, по нашему мнению, неоправданной практикой эмпирического введения иммунного сывороточного гамма-глобулина в качестве профилактического средства детям, страдающим частыми респираторными инфекциями, что характерно для больных с тотальным отсутствием Ig. A. В иммунном сывороточном гамма-глобулине содержатся следовые количества Ig. A, которых оказывается достаточно для сенсибилизации ребенка с тотальной недостаточностью Ig. A, но недостаточно для создания защиты от микроорганизмов, вызывающих респираторные инфекции. Если в последующем больному переливают кровь или ее продукты, содержащие значительное количество Ig. A, у него может развиться анафилактическая реакция с летальным исходом.
 n Избирательная недостаточность Ig. A может наследоваться по аутосомно-рецессивному или аутосомно-доминантному типу. Сибсы больных с пангипогаммаглобулинемией часто страдают избирательной недостаточностью Ig. A. Интересно, хотя до сих пор и необъяснимо, сочетание этого вида избирательной недостаточности с аномалией хромосомы 18; на ней, по-видимому, не локализуются структурные гены иммуноглобулинов.
n Избирательная недостаточность Ig. A может наследоваться по аутосомно-рецессивному или аутосомно-доминантному типу. Сибсы больных с пангипогаммаглобулинемией часто страдают избирательной недостаточностью Ig. A. Интересно, хотя до сих пор и необъяснимо, сочетание этого вида избирательной недостаточности с аномалией хромосомы 18; на ней, по-видимому, не локализуются структурные гены иммуноглобулинов.
 n Выработка сывороточного и секреторного Ig. A контролируется, вероятно, разными генами, однако практически у всех больных с недостаточностью сывороточного отмечается недостаточность и секреторного Ig. A. Иногда при недостаточности сывороточного Ig. A в кишечнике удавалось обнаружить плазматические клетки, несущие этот иммуноглобулин. Поскольку при этом не была проведена полная оценка способности вырабатывать секреторный. Ig. A в желудочнокишечном тракте и дыхательных путях, остается невыясненным, соответствовало ли норме количество Ig. A продуцирующих клеток во всей секреторной системе организма и был ли уровень синтеза этими клетками секреторного Ig. A достаточным для создания защиты. Таким образом, следует признать, что наибольшее значение имеет нормальная функция Ig. A в различных секретах; с практической же точки зрения в большинстве случаев определение его содержания в сыворотке позволяет достоверно судить о выработке секреторного Ig. A. Его недостаточность при нормальном уровне в сыворотке связана с недостаточностью секреторного компонента. Таким образом, можно считать, что при соответствующей симптоматике уровень секреторного Ig. A необходимо определять независимо от его уровня в сыворотке.
n Выработка сывороточного и секреторного Ig. A контролируется, вероятно, разными генами, однако практически у всех больных с недостаточностью сывороточного отмечается недостаточность и секреторного Ig. A. Иногда при недостаточности сывороточного Ig. A в кишечнике удавалось обнаружить плазматические клетки, несущие этот иммуноглобулин. Поскольку при этом не была проведена полная оценка способности вырабатывать секреторный. Ig. A в желудочнокишечном тракте и дыхательных путях, остается невыясненным, соответствовало ли норме количество Ig. A продуцирующих клеток во всей секреторной системе организма и был ли уровень синтеза этими клетками секреторного Ig. A достаточным для создания защиты. Таким образом, следует признать, что наибольшее значение имеет нормальная функция Ig. A в различных секретах; с практической же точки зрения в большинстве случаев определение его содержания в сыворотке позволяет достоверно судить о выработке секреторного Ig. A. Его недостаточность при нормальном уровне в сыворотке связана с недостаточностью секреторного компонента. Таким образом, можно считать, что при соответствующей симптоматике уровень секреторного Ig. A необходимо определять независимо от его уровня в сыворотке.
 СПАСИБО ЗА ВНИМАНИЕ!!!
СПАСИБО ЗА ВНИМАНИЕ!!!


