1c76d76f3f0fda48360455867a2d2376.ppt
- Количество слайдов: 53

СБЕРЕГАЮЩИЕ ТЕХНОЛОГИИ ЛЕКЦИЯ 10.

Технологии для предотвращения загрязнения атмосферы Предотвратить загрязнение атмосферы можно двумя способами: предотвратить образование загрязнителя в источнике; улавливать загрязнитель из отходящих газов. Ключевой задачей является первое – предотвращение образования загрязнителя внутри химико-технологического процесса. 1. 2. Очень часто забывают о том, что сами системы очистки являются технологическими процессами, которые расходуют энергию и могут эмитировать вторичные загрязнения в атмосферу. Источниками загрязнения атмосферы являются теплоэлектростанции, автомобильный, морской и авиационный транспорт, крупные предприятия и т. д. 2

Основные загрязнители атмосферы Пыль Диоксид серы SO 2 Оксиды азота NОx Летучие органические соединения VOC (volitile organic compounds) Запахи Традиционные методы очистки отходящих газов - абсорбция, адсорбция, термическая и каталитическая очистка. 3

Современные, новые методы и процессы предотвращения загрязнения атмосферы: Биофильтрация органических паров Сорбционные методы для улавливания диоксинов/фуранов и тяжелых металлов Использование электронного излучения для очистки дымовых газов от SO 2 и NОx Мембранные методы (для удаления VOC) Методы выделения (sequestration - секвестрации) СО 2. 4

Абсорбция SO 2, NOx, VOC из отходящих газов При абсорбционном процессе нежелательные примеси поглощают из газов подходящей жидкостью или раствором (вода, щелочной раствор, органический растворитель). 5
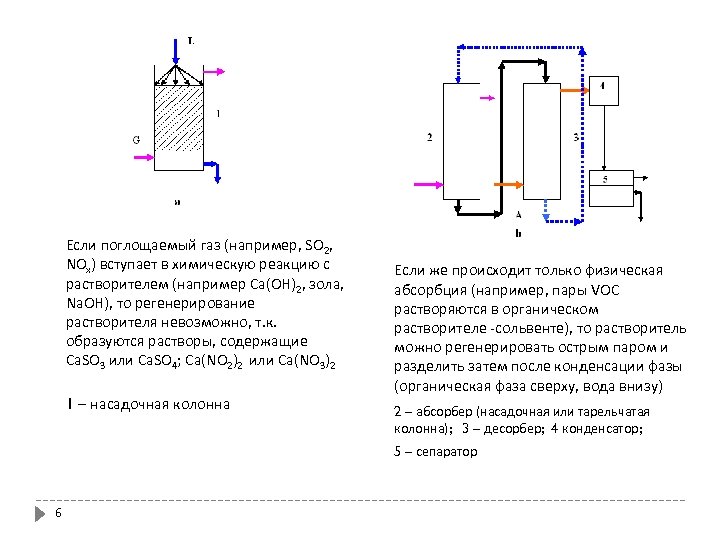
Если поглощаемый газ (например, SO 2, NOx) вступает в химическую реакцию с растворителем (например Са(ОН)2, зола, Na. OH), то регенерирование растворителя невозможно, т. к. образуются растворы, содержащие Ca. SO 3 или Ca. SO 4; Ca(NO 2)2 или Ca(NO 3)2 1 – насадочная колонна Если же происходит только физическая абсорбция (например, пары VOC растворяются в органическом растворителе -сольвенте), то растворитель можно регенерировать острым паром и разделить затем после конденсации фазы (органическая фаза сверху, вода внизу) 2 – абсорбер (насадочная или тарельчатая колонна); 3 – десорбер; 4 конденсатор; 5 – сепаратор 6

Выделение SO 2 из отходящих газов (1) Методы для улавливания SO 2 разделяются на мокрые, полусухие и сухие в зависимости от концентрации химически активного компонента в водном растворе. Применяют следующие поглотители: Ca. O, Na. OH, Na 2 CO 3, NH 4 OH, Ca(OH)2, Ca. CO 3, Ca. CO 3∙Mg. CO 3. Некоторые реакции: SO 2 + Са. О → Ca. SO 3 2 Ca. SO 3 + О 2 → 2 Ca. SO 4 Са. СО 3 + SO 2 → Ca. SO 3 + СО 2 Результатом очистки является шлам сульфитов/сульфатов, который требует осаждения и обезвоживания. Степень очистки газа от SO 2 до 90 %. При применении вместо Са. О или Ca(OH)2 известняка Ca. CO 3 или доломита Ca. CO 3∙Mg. CO 3 эффективность очистки ниже 90 %, т. к. ниже химическая активность поглотителя. 7

Выделение SO 2 из отходящих газов (2) Процесс Vellman-Lord, где SO 2 абсорбируют раствором сульфита: SO 32 - + SO 2 → SO 42 - + SO 2 + Н 2 О → 2 НSO 3 При кипячении раствора бисульфита SO 2 регенерируется: НSO 3 - → 2 SO 3 -+ Н 2 О + SO 2 8
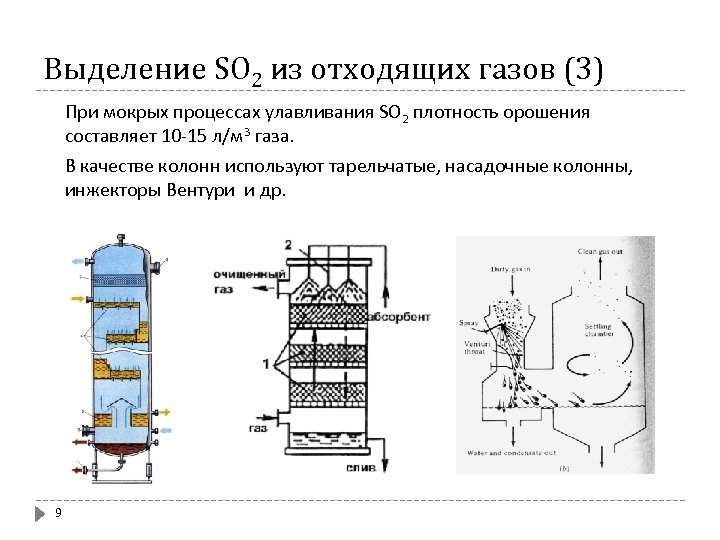
Выделение SO 2 из отходящих газов (3) При мокрых процессах улавливания SO 2 плотность орошения составляет 10 -15 л/м 3 газа. В качестве колонн используют тарельчатые, насадочные колонны, инжекторы Вентури и др. 9

Выделение SO 2 из отходящих газов (4) При полусухих и сухих методах отходящий газ контактирует с суспензией с очень малым содержанием воды За счет тепла газа вода испаряется и реакционные продукты выделяются в виде сухой золы. При сухих процессах орошение составляется только 0, 03 -0, 05 л/м 3 газа. На рис. показана схема полусухой очистки газа. Сухой метод практически относится уже к процессам адсорбции. 10

Адсорбция при очистке газов (1) Процесс абсорбции можно называть предочисткой газа, за которой следует доочистка методом адсорбции. Самые известные адсорбенты – это активированный уголь синтетические ионообменные смолы (цеолиты) и алюмосиликаты, содержащие оксиды Al 2 O 3; Fe 2 O 3; Mn. O 2; Si. O 2. В зависимости от свойств адсорбируемого материала максимальная (равновесная) поглотительная способность адсорбентов составляет: активированные угли синтетические смолы неорганические оксиды 0, 1 -0, 9 г/г 0, 1 -0, 25 г/г Реальная поглотительная способность в динамической обстановке зависит от гидродинамического режима в аппарате и может составлять 50 -90 % от теоретической. 11
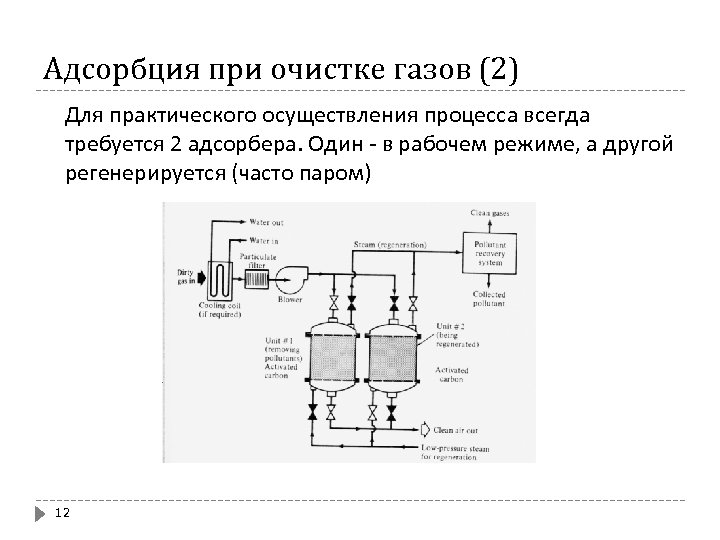
Адсорбция при очистке газов (2) Для практического осуществления процесса всегда требуется 2 адсорбера. Один - в рабочем режиме, а другой регенерируется (часто паром) 12
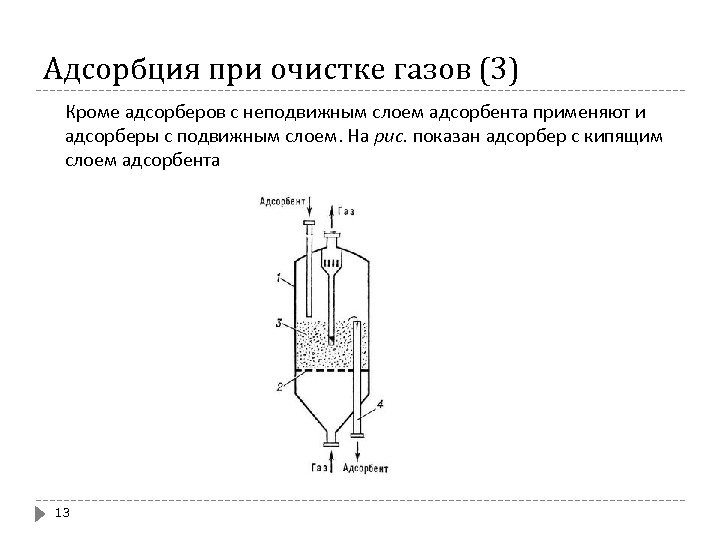
Адсорбция при очистке газов (3) Кроме адсорберов с неподвижным слоем адсорбента применяют и адсорберы с подвижным слоем. На рис. показан адсорбер с кипящим слоем адсорбента 13
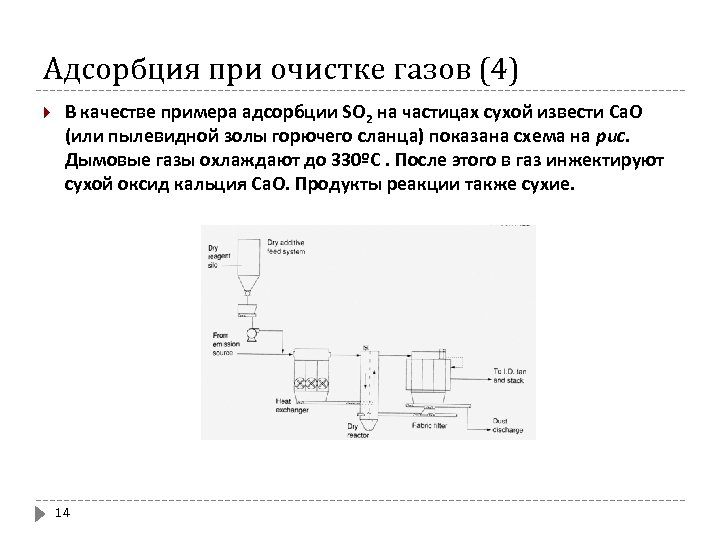
Адсорбция при очистке газов (4) В качестве примера адсорбции SO 2 на частицах сухой извести Са. О (или пылевидной золы горючего сланца) показана схема на рис. Дымовые газы охлаждают до 330ºС. После этого в газ инжектируют сухой оксид кальция Са. О. Продукты реакции также сухие. 14

Методы удаления NOx из газов (1) NОx – это смесь NO 2 + NO NO практически не растворяется в воде NO 2 хорошо растворяется в воде Поэтому вначале перед применением абсорбционных методов следует окислить NO до растворимой NO 2. Для этого применяют растворы KMn. O 4, H 2 O 2, O 3, O 2. В качестве катализаторов могут применяться диспергированные в жидкой фазе алюмогель, силикагель и Mn. O 2. Можно достичь 90 %-ной степени улавливания. 15

Методы удаления NOx из газов (2) Наиболее широко распространены методы восстановления. Добавлением аммиака в газовую фазу переводят NO в N 2 и Н 2 О в присутствии кислорода: NO + NH 3 + ½ O 2 → N 2 + 3/2 H 2 O NH 3 + 5/4 O 2 → NO + 3/2 H 2 O Кроме NH 3 можно для восстановления в газовой фазе применять еще CH 4, СО, H 2 и др. Температура процесса зависит от температуры зажигания катализатора (Pt, Pd, Rh, Ru и др. ) и от восстановителя. Для CH 4 требуется 450480ºС, для пропана/бутана 350ºС, для H 2 и СО – 150 -200ºС. 4 NO + CH 4 → 2 N 2 + СО 2 + 2 Н 2 О 2 NO 2 + CH 4 → N 2 + СО 2 + 2 Н 2 О 2 NO + 2 H 2 → N 2 + 2 Н 2 О 2 NО 2 + 4 H 2 → N 2 + 4 Н 2 О 16

Методы удаления NOx из газов (3) Селективное каталитическое восстановление (selective catalytic reduction, SCR). Здесь используют в качестве восстановителя аммиак, который в присутствии катализатора реагирует только с NOx и практически не реагирует с кислородом, содержащимся в нитрозных газах. Температура процесса относительно низкая (300 -450ºС). В качестве катализаторов используют Cu. O, Fe 2 O 3, V 2 O 5, Cr 2 O 3 и др. 6 NO + 4 NH 3 → 5 N 2 + 6 Н 2 О 6 NO 2 + 8 NH 3 → 7 N 2 + 12 Н 2 О Свыше 95 % NOx восстанавливаются до N 2. 17

Методы удаления ЛОС (VOC) Пары органических веществ (VOC) встречаются практически везде из-за широкого применения в промышленности бензола, толуола, ксилола, эфиров, метанола, этанола, бутанола, хлорированных углеродов (метилхлорид, хлороформ, три- и тетрахлорэтилен). Кроме того, при переработке фруктов и овощей освобождаются большие количества низкомолекулярных спиртов, кетонов, альдегидов и др. Для удаления VOC применяют: сжигание каталитическое окисление адсорбцию абсорбцию сольвентами Указанные методы хорошо развиты, но они имеют целый ряд недостатков. Например, сжигание и каталитическое окисление дороги и образуют газы, которые сами являются загрязнителями. При сжигании ТСЕ (трихлорэтилена) образуются токсичные продукты типа ДДТ. Адсорбция и абсорбция не решают проблему полностью, т. к. при их использовании загрязнитель транспортируется из газовой фазы в твердую или в жидкую. Однако, самый большой недостаток этих методов состоит в их низкой эффективности при малых концентрациях загрязнителя. 18
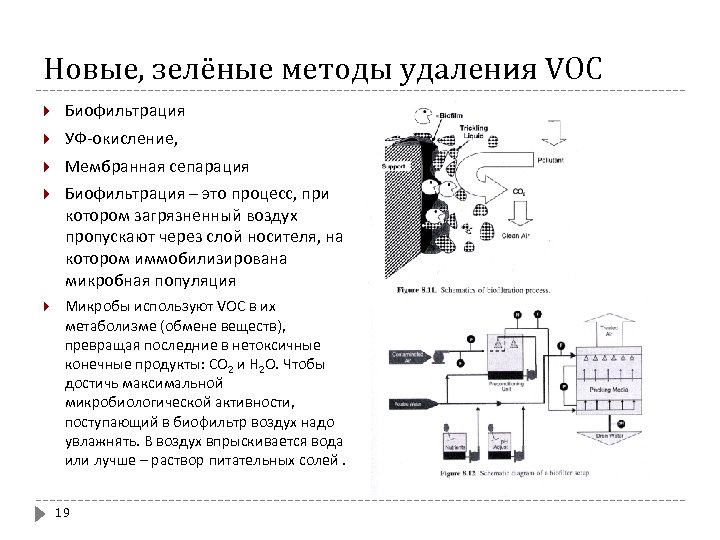
Новые, зелёные методы удаления VOC Биофильтрация УФ-окисление, Мембранная сепарация Биофильтрация – это процесс, при котором загрязненный воздух пропускают через слой носителя, на котором иммобилизирована микробная популяция Микробы используют VOC в их метаболизме (обмене веществ), превращая последние в нетоксичные конечные продукты: СО 2 и Н 2 О. Чтобы достичь максимальной микробиологической активности, поступающий в биофильтр воздух надо увлажнять. В воздух впрыскивается вода или лучше – раствор питательных солей. 19

Биофильтрация не является новым методом. В Индии накрывают навозную кучу сухим сеном, периодически орошаемым водой. Микробы растут на увлажненном сене и очищают воздух от запаха. В Европе также используют биофильтрацию для дезодорирования воздуха от хранилищ шлама сточной воды и т. п. Однако, использование биологической фильтрации для удаления промышленных VOC - относительно новое направление. Первые такие примитивные системы были установлены в Германии и в США уже в 60 -тых годах 20 века. Усовершенствованные системы начали распространяться в США и Европе в 90 тые годы. В начале 21 -го века в США работало свыше 4000 биофильтрационных установок. 20

Популярность биофильтров объясняется следующими причинами: 21 VOC окисляются при обычных температурах; отсутствуют высокая температура сжигания и продукты горения процесс полностью безопасен низкие эксплуатационные расходы (энергия расходуется только на увлажнение и на продувку газа через слой носителя) низкое гидравлическое сопротивление низкая стоимость обслуживания (мало вращающихся деталей) зеленая технология (нет эмиссий NOx, SO 2; эмиссия СО 2 низкая, т. к. часть углерода переходит в биомассу)

Несмотря на кажущуюся простоту биофильтрации, проектирование этого процесса сложно, т. к. надо оптимизировать ряд параметров: 22 микроорганизмы и носитель кислород и питательные вещества влажность и температура гидравлическое сопротивление материалы насадки кинетика процесса

Микроорганизмы и носитель Основные микроорганизмы в этом процессе – это прокариоты (prokaryotes). Установлено, что грибы (fungi) и плесневые грибки помогают процессу. В качестве носителя можно использовать торф с деревянными стружками, пластмассу в виде деталей разной конфигурации. Кислород и питательные вещества Процесс биофильтрации по-существу аэробный. Равномерное распределение кислорода в насадке имеет существенное значение. Нужны также фосфор (P) и азот (N). Если применяют торф или кору древесины, то они уже содержат N и P, если же применять синтетические полимеры, надо добавлять питательные вещества. 23

Влажность и температура Исследования показали, что биофильтры работают нормально, если 50 % от объема пор в насадке наполнены водой. При высоких скоростях воздуха насадка быстро высушивается, поэтому воздух увлажняется до поступления в биофильтр. Кроме того, все коммерческие установки снабжены автоматическими разбрызгивателями воды. Оптимальная температура работы биофильтра 5÷ 50ºС. Установлено, что эффективность удаления паров стирола повышается в 2 раза при увеличении температуры на 7ºС. Однако, влияние температуры двустороннее, при ее повышении скорость биологического разложения повышается, а адсорбция VOC на насадке ухудшается. Гидравлическое сопротивление Типичное сопротивление порядка 2, 5÷ 5, 0 см вод. ст. на 1 м насадки. 24

Материалы насадки Четыре критических параметра для материала: пористость способность удерживания влаги содержание P и N длительность работы Испытаны различные материалы и их комбинации: навоз с деревянными стружками и частицами коры садовый компост + кора Bio Strata (черные листы PVC) Bio Fill (белые ленты и пленки PVC) полипропиленовые подушки (ПП) Siporax (стекло) 25

Кинетика процесса Если концентрация компонента в газе мала, то общая скорость процесса лимитируется скоростью диффузии компонента через пленку воды до биопленки. Если биопленка полностью активная, пленка воды тонкая и концентрация компонента выше, то процесс лимитируется скоростью биологического окисления. 26
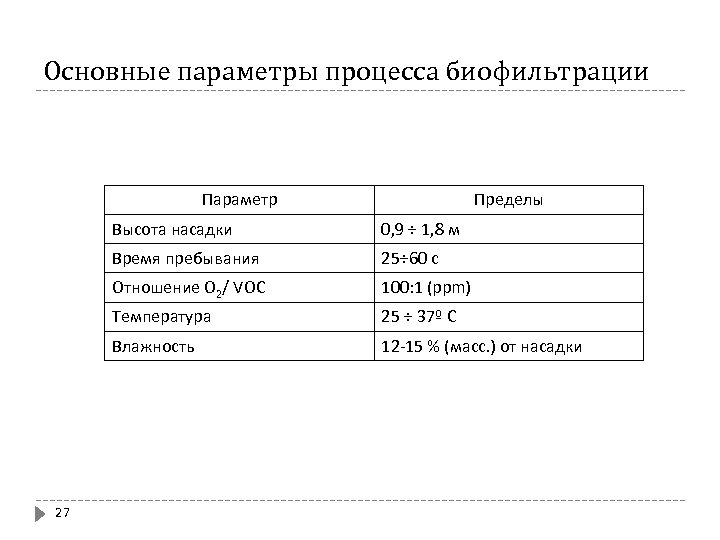
Основные параметры процесса биофильтрации Параметр Пределы Высота насадки Время пребывания 25÷ 60 с Отношение О 2/ VOC 100: 1 (ppm) Температура 25 ÷ 37º С Влажность 27 0, 9 ÷ 1, 8 м 12 -15 % (масс. ) от насадки
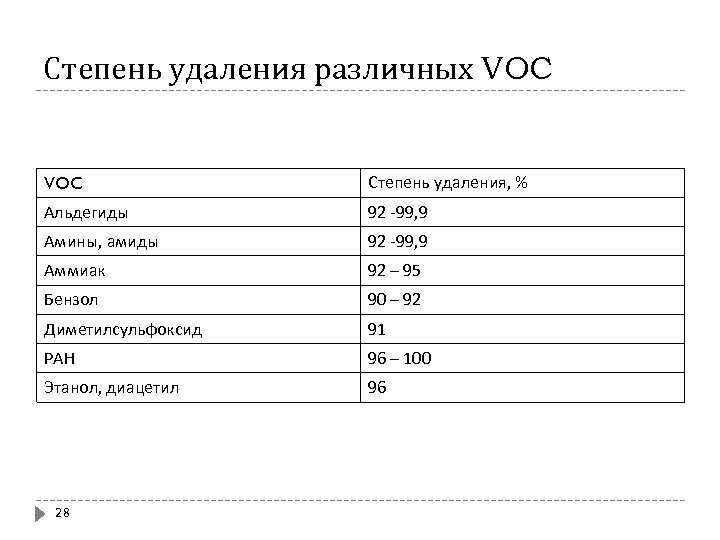
Степень удаления различных VOC Степень удаления, % Альдегиды 92 -99, 9 Амины, амиды 92 -99, 9 Аммиак 92 – 95 Бензол 90 – 92 Диметилсульфоксид 91 PAH 96 – 100 Этанол, диацетил 96 28
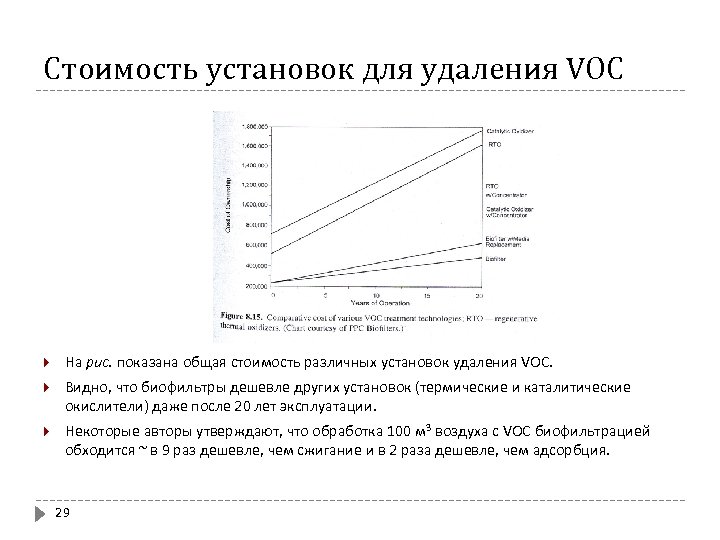
Стоимость установок для удаления VOC На рис. показана общая стоимость различных установок удаления VOC. Видно, что биофильтры дешевле других установок (термические и каталитические окислители) даже после 20 лет эксплуатации. Некоторые авторы утверждают, что обработка 100 м 3 воздуха с VOC биофильтрацией обходится ~ в 9 раз дешевле, чем сжигание и в 2 раза дешевле, чем адсорбция. 29

Использование сорбентов для удаления из газов диоксинов/фуранов и тяжёлых металлов Супертоксины: полихлорированные дибензо-пара-диоксины (PCDDs = polychlorinated dibenzo-p-dioxins) и полихлорированные дибензофураны (PCDFs = polychlorinated dibenzofurans) Это группа трехциклических соединений содержащих от 1 до 8 атомов хлора Известны 210 различных соединений – 75 PCDDs и 135 PCDFs Из них 17 соединений являются более токсичными, чем остальные. В них атомы хлора располагаются в позициях 2, 3, 7 и 8 PCDDs и PCDFs являются очень стабильными соединениями, с большим временем пребывания как в природе, так и в организме человека. Они по характеру гидрофобные, т. е. накапливаются с осадках и в организмах. 30

Источники PCDDs и PCDFs Основным источником PCDDs и PCDFs являются дымовые газы и зола процессов сжигания отходов (flue gases and fly/bottom ash from waste incineration). Эти токсичные компоненты, которые не образуются при температурах > 1500ºС, но образуются в зоне догорания (дожигания), где газы прохладнее, при температурах 300600ºС. Некоторые металлы, в частности медь, являются катализаторами формирования PCDDs и PCDFs образуются также в качестве нежелательных побочных продуктов в производстве целлюлозы, бумаги, пестицидов и др. Подводя итог: PCDDs и PCDFs эмитируются установками сжигания коммунальных отходов, медицинских отходов, шламов, древесины, отработанных масел и др. Установлено, что PCDDs и PCDFs вызывают риск заболевания раком при ингаляции, при поступлении в организм с пищей и при кожном контакте. PCDDs и PCDFs были впервые обнаружены в летучей золе и в дымовых газах печи сжигания коммунальных отходов в 1977 г. В настоящее время существует мнение, что они не являются продуктами чисто газообразных реакций, а металлы и летучая зола сама являются здесь сильными катализаторами. Для объяснения их формирования предложено два механизма: De-Noro синтез и реакция Deacon 31

De-Noro синтез Реакция Deacon Предполагают, что PCDDs и PCDFs образуются из всех углеводородов и хлора в присутствии металлических катализаторов, в частности на базе бензола, фенолов, нафталенов и бифенолов. Ионы Сu 2+ являются сильнейшими катализаторами, в то время как ионы Fe 3+, Pb 2+ и Zn 2+ имеют очень слабый эффект. Важными параметрами процесса. Являются содержание в газе кислорода, температура, размеры частиц золы Полагают, что определяющей является реакция окисления HCl в присутствии металлических катализаторов с образованием Cl 2 и Н 2 О. Основными источниками HCl являются хлорированные пластики (PVC): Cu. O 2 HCl + ½ O 2 → Cl 2 + Н 2 О (<900ºC) Эта реакция называется реакцией Deacon. Далее происходит образование хлорированной ароматики: Bz (г) + Cl 2 → Cl 2 Bz Катализатор Cu. O в реакции Deacon образуется: Сu. Cl 2 + ½ O 2 → Cu. O + Cl 2 32 Хлорированные ароматические соединения (Cl 2 Bz) являются промежуточными продуктами образования диоксинов и фуранов. Исследования показали, что, если летучая зола была нагрета до ~ 230ºC, количество диоксинов и фуранов увеличивалось. Интересным является факт, что присутствие серы в твердых отходах снижает образование диоксинов и фуранов. Объясняется это тем, что при горении серы образуется SO 2 + SO 3, которые расщепляют молекулярный хлор (Cl 2).

В настоящее время разработаны два коммерческих решения этой проблемы улавливания диоксинов и фуранов: инжекция минерального сорбента инжекция порошкообразного активированного угля 33
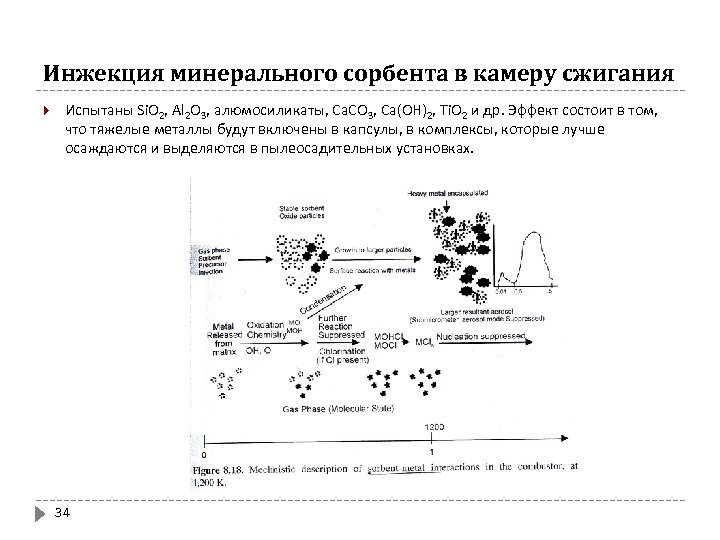
Инжекция минерального сорбента в камеру сжигания Испытаны Si. O 2, Al 2 O 3, алюмосиликаты, Ca. CO 3, Ca(OH)2, Ti. O 2 и др. Эффект состоит в том, что тяжелые металлы будут включены в капсулы, в комплексы, которые лучше осаждаются и выделяются в пылеосадительных установках. 34
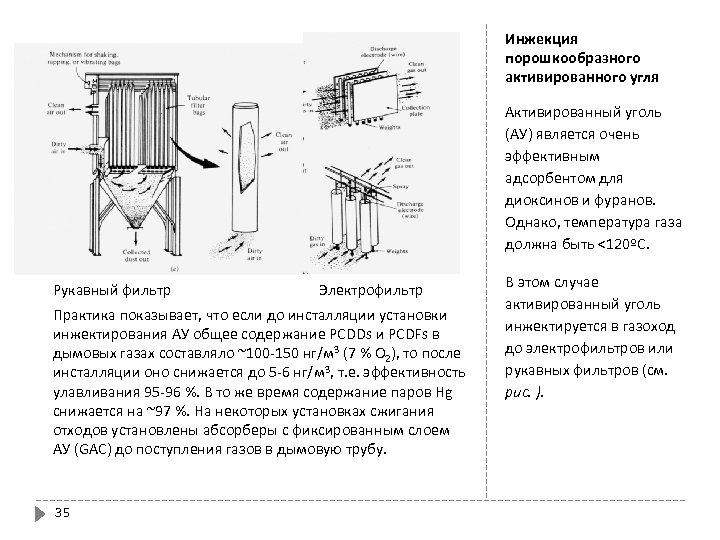
Инжекция порошкообразного активированного угля Активированный уголь (АУ) является очень эффективным адсорбентом для диоксинов и фуранов. Однако, температура газа должна быть <120ºC. Рукавный фильтр Электрофильтр Практика показывает, что если до инсталляции установки инжектирования АУ общее содержание PCDDs и PCDFs в дымовых газах составляло ~100 -150 нг/м 3 (7 % О 2), то после инсталляции оно снижается до 5 -6 нг/м 3, т. е. эффективность улавливания 95 -96 %. В то же время содержание паров Hg снижается на ~97 %. На некоторых установках сжигания отходов установлены абсорберы с фиксированным слоем АУ (GAC) до поступления газов в дымовую трубу. 35 В этом случае активированный уголь инжектируется в газоход до электрофильтров или рукавных фильтров (см. рис. ).

Плазменный метод (1) Это одна из новейших технологий контроля атмосферы для предотвращения загрязнения ее с VOC, NOx, SO 2, Hg, CO 2 и другими парниковыми газами от сжигания каменного угля. Каменный уголь как топливо критикуют из-за того, что при его горении образуются разные загрязнители воздуха (NOx, SOх, Hg). Наряду с развитой адсорбционной техникой разрабатываются новые методы для улавливания газообразных оксидов и паров Hg. Сущность плазменного метода заключается в том, что в результате электрохимического разряда образуются электроны, которые при столкновении с молекулами газа вызывают их активацию, ионизацию и образование метастабильных компонентов. В 1972 г. проводили первые эксперименты с оксидами азота в University College, в Лондоне. Затем, в 80 -90 -тые годы исследовали «коронный» разряд для эмиссий NOx и SO 2, а также влияние пульсации и электронного излучения (e-beam). 36

Плазменный метод (2) Под действием электрического разряда происходит конверсия (превращение) NO в N 2 В плазме образуется и озон, который окисляет ртуть Hg + О 3 → Hg. О + О 2 Плазменный метод на практике применяют во многих компаниях США. Примером является ТЭЦ с каменным углем (125 МW). Дымовой газ содержит NOx 240 -400 ррm, SO 2 1700 -1800 ррm. Температура газа 300ºC. Достигнуты следующие степени улавливания: соответственно 97, 90 и 80 % для ртути. Станция очистки пропускает 185000 м 3/с газа и состоит из 6000 реакционных труб. 37

Метод электронного излучения для очистки дымовых газов от NОx и SO 2 e-beam treatment Электронная радиация нашла применение для обработки дымовых газов, с целью окисления NOx и SO 2. После обработки электронным излучением продукты окисления реагируют с аммиаком с образованием аммонийных солей. Электронная радиация создает пары ионов, свободные радикалы и активированные молекулы в газе. В качестве источников радиации наиболее часто применяют Со 60 и Сs 37 , которые эмитируют γ-лучи, а также ускорители электронов, выделяющие пучок электронов (electron beam). Мощность последних находится в интервале от 5 до 300 к. Вт и энергия 0, 15 -10 Ме. В (Me. V). Электронная радиация хорошо подходит для обработки газов, т. к. энергию электронов можно выбирать таким образом, что практически вся энергия абсорбируется газом. γ-радиация для газов менее эффективна. 38

Метод электронного излучения для очистки дымовых газов от NОx и SO 2 Что происходит с газом при радиации? Образуются очень активные, но с коротким временем жизни частицы: электроны, положительные ионы, активированные атомы и молекулы и свободные радикалы. Многочисленные исследования радиации дымовых газов показали, что образуются частицы, которые облегчают удаление оксидов NOx, SO 2. Основные компоненты дымового газа: N 2, О 2, Н 2 О, СО 2, NOx, SO 2. При абсорбции электронов образуются вторичные электроны и смесь активированных частиц и свободных радикалов: е-, N 2+, N+, О 2+, О+, Н 2 О+, ОН+, СО 2+, СО+, N 2*, N, О, Н, ОН, СО и др. Между ними протекают различные реакции. Конечными продуктами являются азотная и серная кислоты. 39
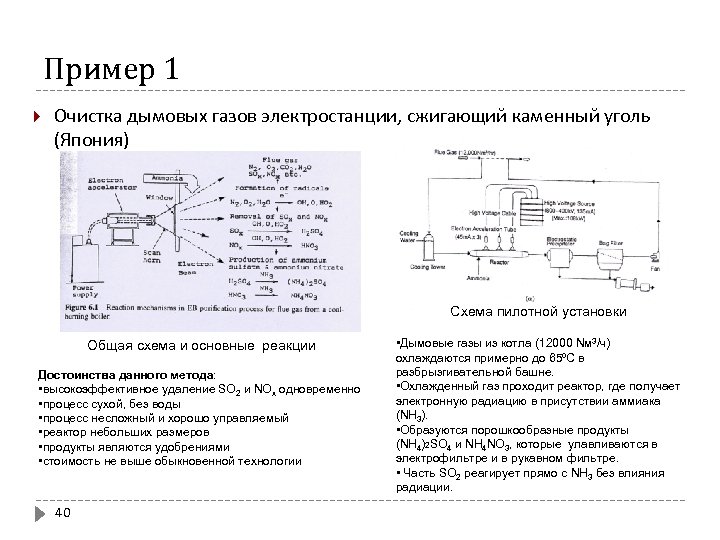
Пример 1 Очистка дымовых газов электростанции, сжигающий каменный уголь (Япония) Схема пилотной установки Общая схема и основные реакции Достоинства данного метода: • высокоэффективное удаление SO 2 и NOx одновременно • процесс сухой, без воды • процесс несложный и хорошо управляемый • реактор небольших размеров • продукты являются удобрениями • стоимость не выше обыкновенной технологии 40 • Дымовые газы из котла (12000 Nм 3/ч) охлаждаются примерно до 65ºC в разбрызгивательной башне. • Охлажденный газ проходит реактор, где получает электронную радиацию в присутствии аммиака (NH 3). • Образуются порошкообразные продукты (NH 4)2 SO 4 и NH 4 NO 3, которые улавливаются в электрофильтре и в рукавном фильтре. • Часть SO 2 реагирует прямо с NH 3 без влияния радиации.
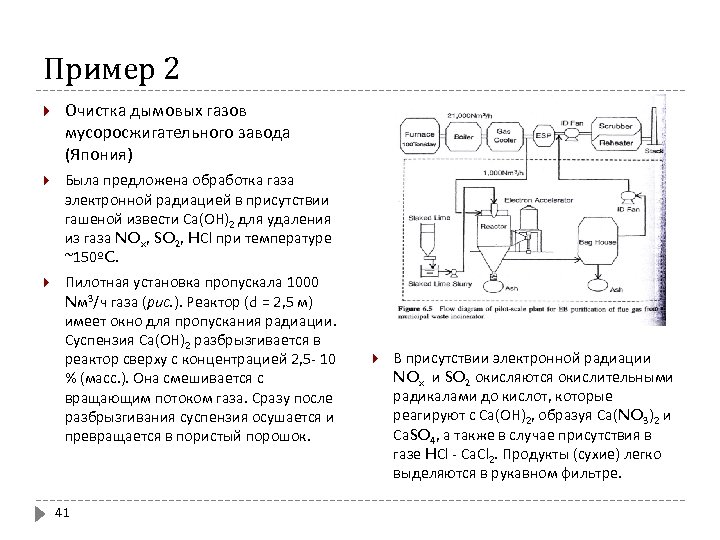
Пример 2 Очистка дымовых газов мусоросжигательного завода (Япония) Была предложена обработка газа электронной радиацией в присутствии гашеной извести Са(ОН)2 для удаления из газа NOx, SO 2, HСl при температуре ~150ºC. Пилотная установка пропускала 1000 Nм 3/ч газа (рис. ). Реактор (d = 2, 5 м) имеет окно для пропускания радиации. Суспензия Са(ОН)2 разбрызгивается в реактор сверху с концентрацией 2, 5 - 10 % (масс. ). Она смешивается с вращающим потоком газа. Сразу после разбрызгивания суспензия осушается и превращается в пористый порошок. 41 В присутствии электронной радиации NOx и SO 2 окисляются окислительными радикалами до кислот, которые реагируют с Са(ОН)2, образуя Са(NO 3)2 и Са. SO 4, а также в случае присутствия в газе HСl - Са. Сl 2. Продукты (сухие) легко выделяются в рукавном фильтре.

Пример 3 Выделение NOх из вентиляционных выбросов туннеля автомобильной дороги. Обычная технология выделения NOх из вентиляционных выбросов туннелей не оказалась экономически эффективной, т. к. концентрация NOх обычно невысокая (< 10 ppm). В Японии разработана технология с применением электронного излучения. Пилотная установка пропускает 50000 Nм 3/час загрязненного воздуха. В присутствии аммиака NOх превращается в порошкообразное удобрение NН 4 NO 3. Перед выходом газ проходит через фильтр с активированным углем для улавливания озона, который образуется при электронной радиации. Задача была достичь 80 %-ного улавливания NOх при исходной концентрации 3 ppm. 42
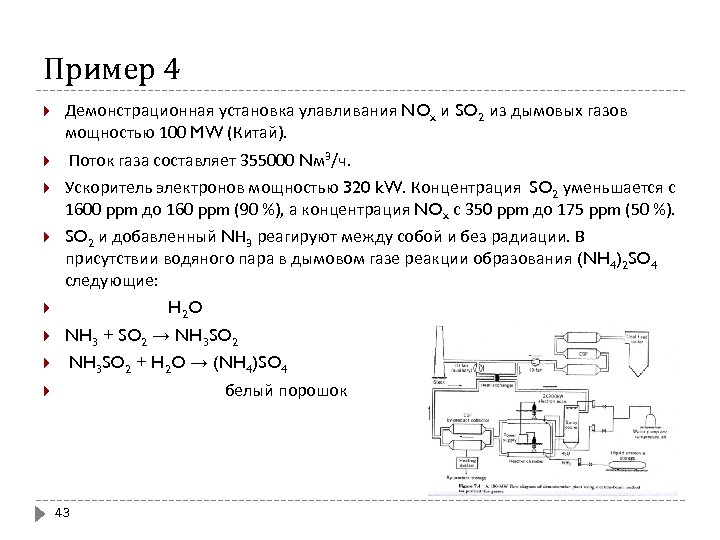
Пример 4 Демонстрационная установка улавливания NOx и SO 2 из дымовых газов мощностью 100 MW (Китай). Поток газа составляет 355000 Nм 3/ч. Ускоритель электронов мощностью 320 k. W. Концентрация SO 2 уменьшается с 1600 ppm до 160 ppm (90 %), а концентрация NOx с 350 ppm до 175 ppm (50 %). SO 2 и добавленный NН 3 реагируют между собой и без радиации. В присутствии водяного пара в дымовом газе реакции образования (NH 4)2 SO 4 следующие: NH 3 + SO 2 → NH 3 SO 2 + H 2 O → (NH 4)SO 4 H 2 O белый порошок 43
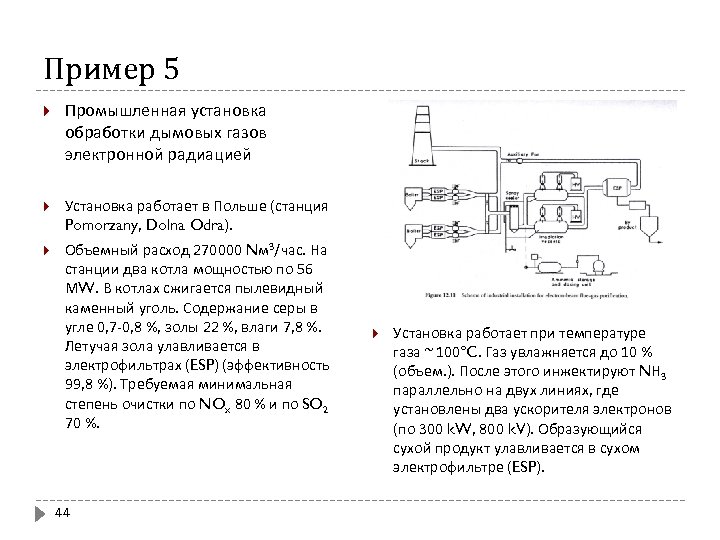
Пример 5 Промышленная установка обработки дымовых газов электронной радиацией Установка работает в Польше (станция Pomorzany, Dolna Odra). Объемный расход 270000 Nм 3/час. На станции два котла мощностью по 56 МW. В котлах сжигается пылевидный каменный уголь. Содержание серы в угле 0, 7 -0, 8 %, золы 22 %, влаги 7, 8 %. Летучая зола улавливается в электрофильтрах (ESP) (эффективность 99, 8 %). Требуемая минимальная степень очистки по NOx 80 % и по SO 2 70 %. 44 Установка работает при температуре газа ~ 100ºC. Газ увлажняется до 10 % (объем. ). После этого инжектируют NН 3 параллельно на двух линиях, где установлены два ускорителя электронов (по 300 k. W, 800 k. V). Образующийся сухой продукт улавливается в сухом электрофильтре (ESP).

Мембранные технологии при защите ОС Будущее в технологии защиты окружающей среды принадлежит двум процессам – мембранным процессам разделения и процессам глубокого окисления (AOP = advanced oxidation processes). Мембранные процессы основываются на явлении обратного осмоса (RO = reverse osmosis) (рис. ). Если разделить сосуд с водой при помощи полупроницаемой мембраны, например, ацетатцеллюлозы, и в левую часть влить чистую, несоленую воду, а в правую часть соленую (раствор Na. Cl) и оставить стоять на некоторое время, то скоро увидим, что чистая вода проникла через мембрану в соленую воду и выдавила в пьезометрической трубке столбик соленой воды определенной высоты (мера осмотического давления). Если же теперь поступить обратно этому явлению, то есть оказывать давление на этот столбик соленой воды, то происходит обратное явление – чистая вода проникает обратно через мембрану в левую часть сосуда, оставляя соли за мембраной. Для проведения обратного осмоса (RO) надо применять давление выше осмотического. 45

Осмотическое давление выражается: π = θ∙N∙Cs∙RT, атм где θ – коэффициент осмотического давления (θ < 1) N – число ионов растворенного вещества Cs – концентрация, моль/л R = 0, 082 атм∙л/моль∙К T - температура, К Пример Определить осмотическое давление для раствора Na. Cl с концентрацией 23, 4 г/л при температуре 25ºС, если θ = 0, 82. Решение N =2; (Na+ + Cl-); М = 58, 45 С s = 23, 4/58, 45 = 0, 4 моль/л; Т = 298 К π =0, 92 ∙ 0, 4 ∙ 0, 082 ∙ 298 = 18 атм Это значит, что для производства чистой воды из этого раствора требуется давление выше 18 атм. Каждые 1000 мг/л растворенного ионизированного вещества повышают осмотическое давление примерно на 0, 07 МПа. 46
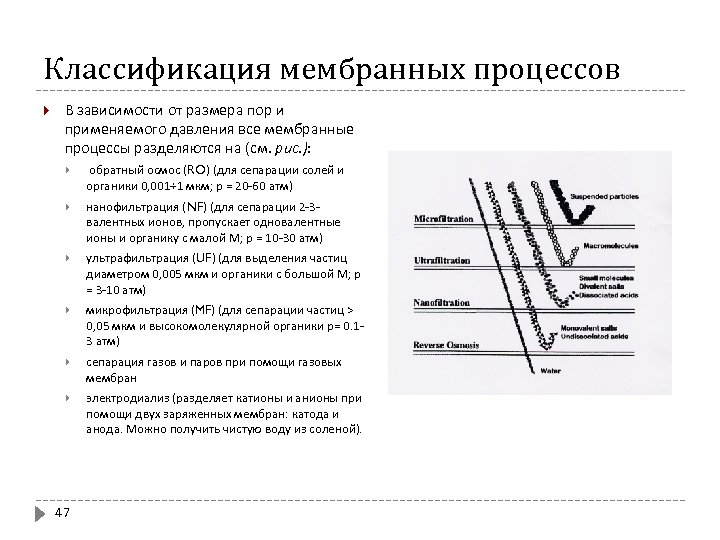
Классификация мембранных процессов В зависимости от размера пор и применяемого давления все мембранные процессы разделяются на (см. рис. ): обратный осмос (RO) (для сепарации солей и органики 0, 001÷ 1 мкм; р = 20 -60 атм) нанофильтрация (NF) (для сепарации 2 -3 - валентных ионов, пропускает одновалентные ионы и органику с малой М; р = 10 -30 атм) ультрафильтрация (UF) (для выделения частиц диаметром 0, 005 мкм и органики с большой М; р = 3 -10 атм) микрофильтрация (MF) (для сепарации частиц > 0, 05 мкм и высокомолекулярной органики р= 0. 13 атм) сепарация газов и паров при помощи газовых мембран электродиализ (разделяет катионы и анионы при помощи двух заряженных мембран: катода и анода. Можно получить чистую воду из соленой). 47

Мембраны Мембраны известны уже свыше 100 лет, но внедрения промышленного масштаба появились только в течение последних 50 лет. В 1940 г. пористые фторуглероды были применены для разделения изотопа 235 UF 6 от 238 UF 6. Первые мембранные аппараты с ацетатцеллюлозной мембраной были разработаны в США Рейдом, Бретоном и Соурираяном в 50 -тые годы. В 1960 г. обратный осмос с ацетатцеллюлозой был применен для обессолевания морской воды, чтобы получить питьевую воду с солесодержанием до 500 мг/л. Затем последовали коммерческие ультрафильтрационные мембраны. В 1979 г. компания Monsanto Chemical внедрила процесс обогащения водород- или СО 2 -содержащего газа при помощи полисульфоновых мембран. 48

Мембраны могут быть 3 различных типов (рис. ): Гомогенные Они имеют поры одинакового диаметра по всей толщине. Из-за малой пропускной способности мало применяются (за исключением для микрофильтрации). Асимметричные Имеют на поверхности мелкие поры, которые по толщине увеличиваются. Они имеют поверхностный слой (кожа, skin) с толщиной 1 -2 мкм, который опирается на пористый носитель толщиной ~ 100 мкм. Композиционные Такие же как и асимметричные, но поверхностный слой и носитель изготовлены из разных материалов (например, поверхностный слой из неорганического материала). 49
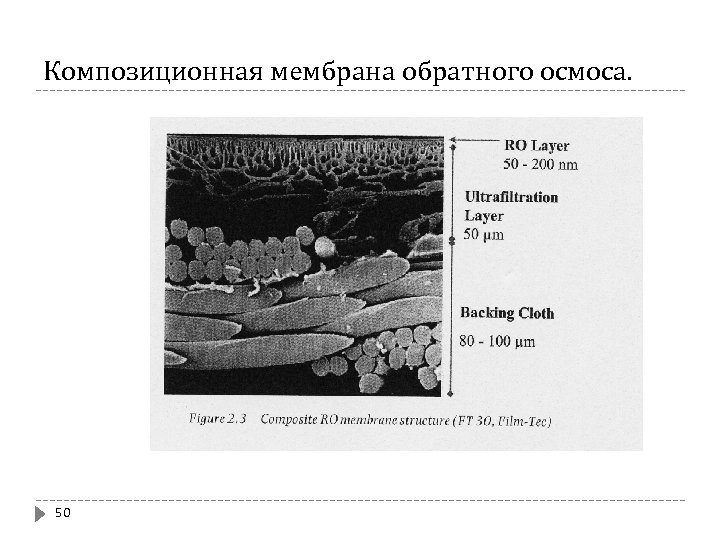
Композиционная мембрана обратного осмоса. 50

Мембранная фильтрация в общих чертах аналогична обычной фильтрации с той лишь разницей, что здесь несколько другая терминология. Фильтрат называется «пермеат» (permeate), а остаточный раствор за мембраной – «ретентат» (retentate). Скорость мембранной фильтрации обычно выражается через объем пермеата в л/м 2∙ч. Как и при обычной фильтрации, при увеличении сопротивления (толщина осадка на мембране) скорость мембранной фильтрации падает по кривой 2 (рис. ). Если же осадок одновременно срезается (удаляется), то наступает псевдоравновесие и падение скорости замедляется (кривая 1 на рис. ). 51

Газовые мембраны При мембранном разделении газов исходный газ обычно, имея высокое давление Р 1, содержит некоторые примеси с малой молярной массой (M<50). В этом случае другая сторона мембраны находится при значительно меньшем давлении P 2 (P 2<<Р 1). Мембрана обычно пропускает примеси с малой молярной массой А и В (рис. ). Если молярные массы компонентов А и В близки, то хорошего разделения не получается. pi. F pi 0 GAS pi. L 52 pip

Начиная с 80 -тых годов были внедрены следующие процессы разделения: 53 водород от метана регулирование соотношения Н 2/СО в синтез-газе обогащение воздуха кислородом О 2 обогащение воздуха азотом N 2 выделение из газа СО 2 выделение Не осушение газа и воздуха выделение паров VOC.
1c76d76f3f0fda48360455867a2d2376.ppt