Рак тела матки 2011.ppt
- Количество слайдов: 71
 Саратовский государственный медицинский университет Кафедра хирургии и онкологии ФПК ППС Рак тела матки (клиника, диагностика, лечение) Ассистент, канд. мед. наук Селезнева Т. Д.
Саратовский государственный медицинский университет Кафедра хирургии и онкологии ФПК ППС Рак тела матки (клиника, диагностика, лечение) Ассистент, канд. мед. наук Селезнева Т. Д.
 8, 0 на 100. 000 - стандартизированный показатель заболеваемости РТМ женского населения в мире, на 2008 г. 11, 0 на 100. 000 - стандартизированный показатель заболеваемости РТМ женского населения в Европе, на 2008 г.
8, 0 на 100. 000 - стандартизированный показатель заболеваемости РТМ женского населения в мире, на 2008 г. 11, 0 на 100. 000 - стандартизированный показатель заболеваемости РТМ женского населения в Европе, на 2008 г.
 13, 2 на 100. 000 - стандартизированный показатель заболеваемости РТМ женского населения в России, на 2008 г. Увеличение заболеваемости за последнее 5 лет до 12, 4%
13, 2 на 100. 000 - стандартизированный показатель заболеваемости РТМ женского населения в России, на 2008 г. Увеличение заболеваемости за последнее 5 лет до 12, 4%
 Факторы риска РТМ: - ановуляция и ановуляторные маточные кровотечения в пременопаузе, -поздняя менопауза (после 50 лет), -эстрогенный тип кольпоцитологической реакции в постменопаузе, -миома матки и генитальный эндометриоз -гиперпластический процесс эндометрия и гормонозависимые опухоли в анамнезе, -прием эстрогенов в постменопаузе, -отягощенная наследственность по раку органов репродуктивной системы, -ожирение, -гиперлипидемия, -сахарный диабет, -гипертоническая болезнь.
Факторы риска РТМ: - ановуляция и ановуляторные маточные кровотечения в пременопаузе, -поздняя менопауза (после 50 лет), -эстрогенный тип кольпоцитологической реакции в постменопаузе, -миома матки и генитальный эндометриоз -гиперпластический процесс эндометрия и гормонозависимые опухоли в анамнезе, -прием эстрогенов в постменопаузе, -отягощенная наследственность по раку органов репродуктивной системы, -ожирение, -гиперлипидемия, -сахарный диабет, -гипертоническая болезнь.
 Следует отметить, что имеет значение не количество факторов, сколько сочетание нарушений в двух системах: репродуктивной и энергетической. При сочетании 3 факторов и более в различных гомеостатических системах риск развития РТМ увеличивается в 9 раз.
Следует отметить, что имеет значение не количество факторов, сколько сочетание нарушений в двух системах: репродуктивной и энергетической. При сочетании 3 факторов и более в различных гомеостатических системах риск развития РТМ увеличивается в 9 раз.
 Для выявления РТМ на ранних стадиях женщинам до 40 лет обследование следует проводить при наличии жалоб; после 40 -46 лет – при наличии факторов риска, даже при отсутствии жалоб.
Для выявления РТМ на ранних стадиях женщинам до 40 лет обследование следует проводить при наличии жалоб; после 40 -46 лет – при наличии факторов риска, даже при отсутствии жалоб.
 У большинства больных РТМ вследствие повышения активности гипоталамуса наблюдаются нарушения в репродуктивной и энергетической системах, поэтому у них часто встречаются ожирение, сахарный диабет и гипертоническая болезнь.
У большинства больных РТМ вследствие повышения активности гипоталамуса наблюдаются нарушения в репродуктивной и энергетической системах, поэтому у них часто встречаются ожирение, сахарный диабет и гипертоническая болезнь.
 Первый патогенетический вариант гиперпластических процессов и рака эндометрия характеризуются многообразием и глубиной гиперэстрогении в сочетании с нарушением мирового и углеводного обмена. Клинический симптомокомплекс проявляется в ановуляторных маточных кровотечениях, бесплодии, позднем наступлении менопаузы, гиперплазии тека-ткани яичников в сочетании с синдромом Штейна-Левенталя; в гиперпластических процессах эндометрия, окружающего полипы, очаги атипической гиперплазии или рака; в миоме матки. Обменные нарушения при 1 -м патогенетическом варианте сводятся к ожирению, гиперлипидемии и сахарному диабету. Первый патогенетический вариант встречается у 60 -70% больных раком эндометрия. У больных данного типа чаще встречается опухоль высокой дифференцировки и обладает меньшей степенью злокачественности. Клиническое течение заболевания у этих больных более благоприятно.
Первый патогенетический вариант гиперпластических процессов и рака эндометрия характеризуются многообразием и глубиной гиперэстрогении в сочетании с нарушением мирового и углеводного обмена. Клинический симптомокомплекс проявляется в ановуляторных маточных кровотечениях, бесплодии, позднем наступлении менопаузы, гиперплазии тека-ткани яичников в сочетании с синдромом Штейна-Левенталя; в гиперпластических процессах эндометрия, окружающего полипы, очаги атипической гиперплазии или рака; в миоме матки. Обменные нарушения при 1 -м патогенетическом варианте сводятся к ожирению, гиперлипидемии и сахарному диабету. Первый патогенетический вариант встречается у 60 -70% больных раком эндометрия. У больных данного типа чаще встречается опухоль высокой дифференцировки и обладает меньшей степенью злокачественности. Клиническое течение заболевания у этих больных более благоприятно.
 При втором патогенетическом варианте, встречающемся у 30 -40% больных, указанные эндокринно-обменные нарушения выражены нечетко или совсем отсутствуют. Характерно сочетание фиброза стромы яичников и атрофии эндометрия на фоне которой возникают полипы, атипическая гиперплазия и рак. У больных этой группы опухоль развивается на фоне атрофичного эндометрия, чаще выявляются железисто-солидные и солидные формы. Клиническое течение заболевания менее благоприятно.
При втором патогенетическом варианте, встречающемся у 30 -40% больных, указанные эндокринно-обменные нарушения выражены нечетко или совсем отсутствуют. Характерно сочетание фиброза стромы яичников и атрофии эндометрия на фоне которой возникают полипы, атипическая гиперплазия и рак. У больных этой группы опухоль развивается на фоне атрофичного эндометрия, чаще выявляются железисто-солидные и солидные формы. Клиническое течение заболевания менее благоприятно.
 Этапы онкогенеза при РЭ I. III. IV. - функциональных нарушений (ановуляция, гиперэстрогения); - формирование морфологических нарушений, расцениваемых как фоновые (диффузная и очаговая гиперплазия эндометрия); - формирование морфологических изменений, расцениваемых как предраковые (слабо и умеренно выраженные формы атипической гиперплазии); - развитие злокачественной опухоли (фаза преинвазивного рака - выраженная форма атипической гиперплазии, рак в пределах слизистой, рак с минимальной инвазией, выраженные формы рака эндометрия).
Этапы онкогенеза при РЭ I. III. IV. - функциональных нарушений (ановуляция, гиперэстрогения); - формирование морфологических нарушений, расцениваемых как фоновые (диффузная и очаговая гиперплазия эндометрия); - формирование морфологических изменений, расцениваемых как предраковые (слабо и умеренно выраженные формы атипической гиперплазии); - развитие злокачественной опухоли (фаза преинвазивного рака - выраженная форма атипической гиперплазии, рак в пределах слизистой, рак с минимальной инвазией, выраженные формы рака эндометрия).
 Риск рака тела матки снижают: u комбинированные оральные контрацептивы: vриск рака тела матки снижается на 11, 7 % в год; vснижение риска сохраняется в течение более 15 лет после прекращения приема оральных контрацептивов; u прием β-каротина, мононенасыщенных жирных кислот, фруктов и овощей; u физическая активность; u умеренное потребление алкоголя (по некоторым данным); u курение.
Риск рака тела матки снижают: u комбинированные оральные контрацептивы: vриск рака тела матки снижается на 11, 7 % в год; vснижение риска сохраняется в течение более 15 лет после прекращения приема оральных контрацептивов; u прием β-каротина, мононенасыщенных жирных кислот, фруктов и овощей; u физическая активность; u умеренное потребление алкоголя (по некоторым данным); u курение.
 Клинико-морфологическая классификация патологических состояний тела матки. Фоновые процессы: -железистая гиперплазия, -эндометриальные полипы. Предраковые заболевания: -атипическая гиперплазия. Рак: -аденокарцинома, -аденоакантома (аденокарцинома с доброкачественными -плоскоклеточными включениями), -светлоклеточная мезонефроидная аденокарцинома, -железисто-плоскоклеточный рак, -недифференцированный рак.
Клинико-морфологическая классификация патологических состояний тела матки. Фоновые процессы: -железистая гиперплазия, -эндометриальные полипы. Предраковые заболевания: -атипическая гиперплазия. Рак: -аденокарцинома, -аденоакантома (аденокарцинома с доброкачественными -плоскоклеточными включениями), -светлоклеточная мезонефроидная аденокарцинома, -железисто-плоскоклеточный рак, -недифференцированный рак.
 Фоновые заболевания тела матки. Полипы эндометрия развиваются вследствие пролиферации желез базального слоя эндометрия. Непременное анатомическое свойство полипов – наличие ножки, состоящей из фиброзной и гладкомышечной ткани. Признак «органоидности» отличает полип от полиповидной формы железистой гиперплазии эндометрия, которую иногда неточно обозначают как «полипоз эндометрия» . Полипы чаще располагаются в области дна и трубных углов матки. Эндометриальные полипы малигнизируются так же редко (2 -5%), как и железистая гиперплазия эндометрия, но в постменопаузе указанная частота достигает 10%.
Фоновые заболевания тела матки. Полипы эндометрия развиваются вследствие пролиферации желез базального слоя эндометрия. Непременное анатомическое свойство полипов – наличие ножки, состоящей из фиброзной и гладкомышечной ткани. Признак «органоидности» отличает полип от полиповидной формы железистой гиперплазии эндометрия, которую иногда неточно обозначают как «полипоз эндометрия» . Полипы чаще располагаются в области дна и трубных углов матки. Эндометриальные полипы малигнизируются так же редко (2 -5%), как и железистая гиперплазия эндометрия, но в постменопаузе указанная частота достигает 10%.
 Предраковые заболевания тела матки Макроскопическая картина атипической гиперплазии эндометрия (АГЭ) нехарактерна: она может быть обнаружена как в утолщенном (гиперплазированном), так и в истонченном (атрофическом) эндометрии и полипах. Выделяют 3 формы АГЭ: слабую, умеренную и тяжелую. Дискуссионным остается вопрос о правомерности диагноза «Ca in situ эндометрия» . С точки зрения биологического поведения, тяжелая АГЭ эквивалентна современным представлениям о преинвазивном раке. Но гистологический диагноз «Ca in situ» при исследовании соскобов проблематичен, так как тяжелую АГЭ иногда трудно отличить от высокодифференцированной аденокарциномы.
Предраковые заболевания тела матки Макроскопическая картина атипической гиперплазии эндометрия (АГЭ) нехарактерна: она может быть обнаружена как в утолщенном (гиперплазированном), так и в истонченном (атрофическом) эндометрии и полипах. Выделяют 3 формы АГЭ: слабую, умеренную и тяжелую. Дискуссионным остается вопрос о правомерности диагноза «Ca in situ эндометрия» . С точки зрения биологического поведения, тяжелая АГЭ эквивалентна современным представлениям о преинвазивном раке. Но гистологический диагноз «Ca in situ» при исследовании соскобов проблематичен, так как тяжелую АГЭ иногда трудно отличить от высокодифференцированной аденокарциномы.
 Гиперплазия эндометрия 1. u ТИПИЧНАЯ ГИПЕРПЛАЗИЯ (фоновый процесс): – Простая гиперплазия без атипии – Сложная гиперплазия без атипии u АТИПИЧЕСКАЯ ГИПЕРПЛАЗИЯ: – Простая атипическая гиперплазия (встречается крайне редко) – Сложная атипическая гиперплазия (истинный предрак)
Гиперплазия эндометрия 1. u ТИПИЧНАЯ ГИПЕРПЛАЗИЯ (фоновый процесс): – Простая гиперплазия без атипии – Сложная гиперплазия без атипии u АТИПИЧЕСКАЯ ГИПЕРПЛАЗИЯ: – Простая атипическая гиперплазия (встречается крайне редко) – Сложная атипическая гиперплазия (истинный предрак)
 2. u ПРОСТАЯ ТИПИЧНАЯ ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ повышение количества как железистых, так и стромальных элементов, при некотором преобладании последних; отсутствует заметное тесное расположение желез u СЛОЖНАЯ ТИПИЧНАЯ ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ без атипии (аденоматоз без атипии) наличие тесного расположения желез с утратой стромы между ними; в железах больше выражена многоядерность эпителия, чем при простой железистой гиперплазии
2. u ПРОСТАЯ ТИПИЧНАЯ ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ повышение количества как железистых, так и стромальных элементов, при некотором преобладании последних; отсутствует заметное тесное расположение желез u СЛОЖНАЯ ТИПИЧНАЯ ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ без атипии (аденоматоз без атипии) наличие тесного расположения желез с утратой стромы между ними; в железах больше выражена многоядерность эпителия, чем при простой железистой гиперплазии
 u ПРОСТАЯ АТИПИЧЕСКАЯ 3. ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ атипия клеток с утратой полярности расположения и необычная форма ядер; u СЛОЖНАЯ АТИПИЧЕСКАЯ ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ (аденоматоз с атипией) выраженная пролиферация эпителиального компонента, сочетающаяся с атипией на тканевом и клеточном уровнях без инвазии базальной мембраны железистых структур и преобладанием железистых элементов над стромальными. Трудно отличить от высокодифференцированного рака.
u ПРОСТАЯ АТИПИЧЕСКАЯ 3. ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ атипия клеток с утратой полярности расположения и необычная форма ядер; u СЛОЖНАЯ АТИПИЧЕСКАЯ ЖЕЛЕЗИСТАЯ ГИПЕРПЛАЗИЯ (аденоматоз с атипией) выраженная пролиферация эпителиального компонента, сочетающаяся с атипией на тканевом и клеточном уровнях без инвазии базальной мембраны железистых структур и преобладанием железистых элементов над стромальными. Трудно отличить от высокодифференцированного рака.
 Общие противопоказания к назначению гормонального лечения. 1. 2. 3. 4. Злокачественные новообразования женских половых и других органов. Увеличение яичников неясного генеза. Миома матки более 12 нед. беременности или субмукозные узлы миомы. Острые воспалительные заболевания гениталий.
Общие противопоказания к назначению гормонального лечения. 1. 2. 3. 4. Злокачественные новообразования женских половых и других органов. Увеличение яичников неясного генеза. Миома матки более 12 нед. беременности или субмукозные узлы миомы. Острые воспалительные заболевания гениталий.
 Противопоказания к гормонотерапии Эстрогенами u злокачественные опухоли u увеличение придатков u миома матки u острые заболевания внутренних половых органов u хронический гепатит, холецистит, панкреатит, цирроз u нефрит, нефроз с отечным синдромом u нарушение гемостаза u варикозное расширение вен u сосудистые нарушения сетчатки глаз при гепертонической болезни и сахарном диабете
Противопоказания к гормонотерапии Эстрогенами u злокачественные опухоли u увеличение придатков u миома матки u острые заболевания внутренних половых органов u хронический гепатит, холецистит, панкреатит, цирроз u нефрит, нефроз с отечным синдромом u нарушение гемостаза u варикозное расширение вен u сосудистые нарушения сетчатки глаз при гепертонической болезни и сахарном диабете
 Противопоказания к гормонотерапии Гестагенами u тромбэмболические заболевания u варикоз u хронический гепатит u хронический холецистит
Противопоказания к гормонотерапии Гестагенами u тромбэмболические заболевания u варикоз u хронический гепатит u хронический холецистит
 1. Комбинированные стероидные половые гормоны: Монофазные эстроген-гестагены (НОН-ОВЛОН, ОВИДОН, РИГЕВИДОН, МАРВЕЛОН, ФЕМОДЕН, АНОВЛАР, ДЕМУЛЕН, ДУОЛУТОН, ФЕМОВАН, АН-НА и др. ). Лечебный эффект синтетических прогестинов объясняется их многообразным воздействием на различные звенья репродуктивной системы, с преимущественным ингибирующим влиянием на гипоталамо-гипофизарную систему, что вызывает в последующем регресс гиперпластических процессов в эндометрии.
1. Комбинированные стероидные половые гормоны: Монофазные эстроген-гестагены (НОН-ОВЛОН, ОВИДОН, РИГЕВИДОН, МАРВЕЛОН, ФЕМОДЕН, АНОВЛАР, ДЕМУЛЕН, ДУОЛУТОН, ФЕМОВАН, АН-НА и др. ). Лечебный эффект синтетических прогестинов объясняется их многообразным воздействием на различные звенья репродуктивной системы, с преимущественным ингибирующим влиянием на гипоталамо-гипофизарную систему, что вызывает в последующем регресс гиперпластических процессов в эндометрии.
 2. Прогестагены: а) гормоны желтого тела - ПРОГЕСТЕРОН, ПРЕГНИН, 17 ОПК. Последний обладает наиболее выраженной гестагенной активностью. Применение данных препаратов основано на их способности вызывать секреторную трансформацию эндометрия, стимулировать ЛГ; б) норстероиды - производные тестостерона: НОРКОЛУТ, ОРГАМЕТРИЛ, ТУРИНАЛ, ГЕСТРИНОН - обладающие высокой гестагенной активностью, в несколько раз превосходящей активность прогестерона; в) производные норстероида-ацетата (природного гормона желтого тела) - ДЮФАСТОН, ПРИМОЛЮТ-НОР, ПРОВЕРА, ДЕПО-ПРОВЕРА, ДЕПОСТАТ. Эти лекарственные средства наиболее эффективны при рецидивирующих гиперпластических заболеваниях, неэффективности лечения «чистыми» гестагенами, отсутствии условий для оперативного лечения.
2. Прогестагены: а) гормоны желтого тела - ПРОГЕСТЕРОН, ПРЕГНИН, 17 ОПК. Последний обладает наиболее выраженной гестагенной активностью. Применение данных препаратов основано на их способности вызывать секреторную трансформацию эндометрия, стимулировать ЛГ; б) норстероиды - производные тестостерона: НОРКОЛУТ, ОРГАМЕТРИЛ, ТУРИНАЛ, ГЕСТРИНОН - обладающие высокой гестагенной активностью, в несколько раз превосходящей активность прогестерона; в) производные норстероида-ацетата (природного гормона желтого тела) - ДЮФАСТОН, ПРИМОЛЮТ-НОР, ПРОВЕРА, ДЕПО-ПРОВЕРА, ДЕПОСТАТ. Эти лекарственные средства наиболее эффективны при рецидивирующих гиперпластических заболеваниях, неэффективности лечения «чистыми» гестагенами, отсутствии условий для оперативного лечения.
 3. Препараты – антагонисты гонадотропинов: ДАНАЗОЛ, ДАНОВАЛ и их аналоги, обладающие преимущественно антигонадотропным действием. Прямая антипрогестероновая активность Даназола и его аналогов обусловлена способностью препаратов занимать прогестероновые рецепторы. 4. Агонисты рилизинг-факторов гонадотропных гормонов: ЗОЛАДЕКС, ДЕКАПЕПТИЛ-ДЕПО, СИНАРЕЛ, НАФЕРЕЛИН, БУСЕРЕЛИН, ТРИПТОРЕЛИН и др.
3. Препараты – антагонисты гонадотропинов: ДАНАЗОЛ, ДАНОВАЛ и их аналоги, обладающие преимущественно антигонадотропным действием. Прямая антипрогестероновая активность Даназола и его аналогов обусловлена способностью препаратов занимать прогестероновые рецепторы. 4. Агонисты рилизинг-факторов гонадотропных гормонов: ЗОЛАДЕКС, ДЕКАПЕПТИЛ-ДЕПО, СИНАРЕЛ, НАФЕРЕЛИН, БУСЕРЕЛИН, ТРИПТОРЕЛИН и др.
 Лечебная тактика при гиперплазии эндометрия В пубертатном периоде на первом этапе лечения необходимо использовать монофазные эстроген-гестагеновые препараты (РИГЕВИДОН, МАРВЕЛОН, ФЕМОДЕН, ДИАНЕ-35 и др. ) по контрацептивной схеме от 3 до 6 месяцев или гестагены с 16 по 25 день менструального цикла на 6 месяцев. При неэффективности лечения показано назначение гестагенов во вторую фазу менструального цикла не менее чем на 4 -6 месяцев.
Лечебная тактика при гиперплазии эндометрия В пубертатном периоде на первом этапе лечения необходимо использовать монофазные эстроген-гестагеновые препараты (РИГЕВИДОН, МАРВЕЛОН, ФЕМОДЕН, ДИАНЕ-35 и др. ) по контрацептивной схеме от 3 до 6 месяцев или гестагены с 16 по 25 день менструального цикла на 6 месяцев. При неэффективности лечения показано назначение гестагенов во вторую фазу менструального цикла не менее чем на 4 -6 месяцев.
 Лечение ЖГЭ в репродуктивном периоде I. – – II. – – Гемостаз хирургический раздельное лечебно-диагностическое выскабливание цервикального канала и полости матки; параллельная симптоматическая и физиотерапия. Регуляция цикла, профилактика рецидива КОК по контрацептивной схеме, 6 месяцев; гестагены 6 месяцев; циклическая витамино-физио-гормонотерапия 3 месяца; клостильбегит 50 -150 мг в день, 5 -9 дни цикла, 3 -6 месяцев у молодых женщин с целью формирования овуляторного менструального цикла и стимуляции овуляции;
Лечение ЖГЭ в репродуктивном периоде I. – – II. – – Гемостаз хирургический раздельное лечебно-диагностическое выскабливание цервикального канала и полости матки; параллельная симптоматическая и физиотерапия. Регуляция цикла, профилактика рецидива КОК по контрацептивной схеме, 6 месяцев; гестагены 6 месяцев; циклическая витамино-физио-гормонотерапия 3 месяца; клостильбегит 50 -150 мг в день, 5 -9 дни цикла, 3 -6 месяцев у молодых женщин с целью формирования овуляторного менструального цикла и стимуляции овуляции;
 Лечение ЖГЭ в репродуктивном периоде III. Диспансеризация и контроль за эффективностью лечения – УЗИ малого таза через 3 -6 -12 месяцев; – аспирационная цитология через 6 месяцев или abrasio cavi uteri и гистероскопия через 6 месяцев; – не менее 1 года после стойкой нормализации менструального цикла или наступление беременности
Лечение ЖГЭ в репродуктивном периоде III. Диспансеризация и контроль за эффективностью лечения – УЗИ малого таза через 3 -6 -12 месяцев; – аспирационная цитология через 6 месяцев или abrasio cavi uteri и гистероскопия через 6 месяцев; – не менее 1 года после стойкой нормализации менструального цикла или наступление беременности
 Лечение ЖГЭ в пременопаузальном периоде I. – II. – – Гемостаз хирургический раздельное, тщательное лечебно-диагностическое выскабливание цервикального канала и полости матки. Профилактика рецидива гестагены; ингибиторы гонадотропинов (данол, неместран); агонисты гонадолиберина (золадекс); при противопоказаниях к гормоногтерапии, рецидивах, противопоказаниях к оперативному лечению: - электро- или лазерная аблация эндометрия, - криодеструкция эндометрия, - химическая деструкция эндометрия йодом (по Грамматикати);
Лечение ЖГЭ в пременопаузальном периоде I. – II. – – Гемостаз хирургический раздельное, тщательное лечебно-диагностическое выскабливание цервикального канала и полости матки. Профилактика рецидива гестагены; ингибиторы гонадотропинов (данол, неместран); агонисты гонадолиберина (золадекс); при противопоказаниях к гормоногтерапии, рецидивах, противопоказаниях к оперативному лечению: - электро- или лазерная аблация эндометрия, - криодеструкция эндометрия, - химическая деструкция эндометрия йодом (по Грамматикати);
 Лечение ЖГЭ в пременопаузальном периоде III. Диспансеризация и контроль за эффективностью лечения – УЗИ малого таза через 3 -6 -12 месяцев; – аспирационная цитология через 3 месяца; – раздельное диагностическое выскабливание или гистероскопия через 6 месяцев; ; – диспансерный учет не менее года стойкой постменопаузы.
Лечение ЖГЭ в пременопаузальном периоде III. Диспансеризация и контроль за эффективностью лечения – УЗИ малого таза через 3 -6 -12 месяцев; – аспирационная цитология через 3 месяца; – раздельное диагностическое выскабливание или гистероскопия через 6 месяцев; ; – диспансерный учет не менее года стойкой постменопаузы.
 Рак эндометрия. Начальные формы РТМ возникают в области дна и трубных углов матки. В дальнейшем рост опухоли затушевывает место ее возникновения. Начальный РЭ не имеет патогномоничной макроструктуры, а выявляется при цитологическом и гистологическом исследованиях. Клинически развитые формы РЭ представлены в виде экзофитных разрастаний, реже полиповидных. Эндофитная форма роста РЭ- редкое исключение, она отмечается менее чем в 5% наблюдений. Различают локальные и диффузные формы РЭ.
Рак эндометрия. Начальные формы РТМ возникают в области дна и трубных углов матки. В дальнейшем рост опухоли затушевывает место ее возникновения. Начальный РЭ не имеет патогномоничной макроструктуры, а выявляется при цитологическом и гистологическом исследованиях. Клинически развитые формы РЭ представлены в виде экзофитных разрастаний, реже полиповидных. Эндофитная форма роста РЭ- редкое исключение, она отмечается менее чем в 5% наблюдений. Различают локальные и диффузные формы РЭ.
 Важное влияние на клиническое течение РЭ оказывает глубина инвазии в миометрий, в 8% случаев она отсутствует. Такие опухоли могут быть полностью удалены при диагностическом выскабливании. В этом случае ставится диагноз «РЭ I стадии» . Глубина инвазии в миометрий может быть поверхностной и глубокой, проникать до серозной оболочки матки и прорастать ее.
Важное влияние на клиническое течение РЭ оказывает глубина инвазии в миометрий, в 8% случаев она отсутствует. Такие опухоли могут быть полностью удалены при диагностическом выскабливании. В этом случае ставится диагноз «РЭ I стадии» . Глубина инвазии в миометрий может быть поверхностной и глубокой, проникать до серозной оболочки матки и прорастать ее.
 Морфологическая классификация До данным Международной гистологической классификации (ВОЗ) выделены следующие морфологические формы рака эндометрия: -аденокарцинома -светлоклеточная (мезонефроидная) аденокарцинома -плоскоклеточный рак - железистоплоскоклеточный рак - недифференцированный рак.
Морфологическая классификация До данным Международной гистологической классификации (ВОЗ) выделены следующие морфологические формы рака эндометрия: -аденокарцинома -светлоклеточная (мезонефроидная) аденокарцинома -плоскоклеточный рак - железистоплоскоклеточный рак - недифференцированный рак.
 Аденокарциномы эндометрия в зависимости от степени гистологической дифференцировки делят на: -высокодифференцированные, -умереннодифференцированные, -низкодифференцированные.
Аденокарциномы эндометрия в зависимости от степени гистологической дифференцировки делят на: -высокодифференцированные, -умереннодифференцированные, -низкодифференцированные.
 Плоскоклеточный рак эндометрия в виде первичной опухоли встречается крайне редко. Чаще он является результатом разрастания плоскоклеточного рака шейки матки.
Плоскоклеточный рак эндометрия в виде первичной опухоли встречается крайне редко. Чаще он является результатом разрастания плоскоклеточного рака шейки матки.
 Железисто-плоскоклеточный рак эндометрия морфологически представляет собой как бы сочетание аденокарциномы и плоскоклеточного рака. Степень дифференцировки каждого из компонентов может варьировать, определяя прогноз заболевания.
Железисто-плоскоклеточный рак эндометрия морфологически представляет собой как бы сочетание аденокарциномы и плоскоклеточного рака. Степень дифференцировки каждого из компонентов может варьировать, определяя прогноз заболевания.
 Недифференцированный рак – редко встречающаяся форма опухоли эндометрия, представленная недифференцированными клетками.
Недифференцированный рак – редко встречающаяся форма опухоли эндометрия, представленная недифференцированными клетками.
 Клиническая классификация РТМ I стадия подразделяется на: Ia - опухоль ограничена эндометрием. Iб - инвазия опухоли до 1 см в миометрий. Iв - инвазия опухолью более 1 см, но не доходит до серозной оболочки. II стадия - опухоль распространяется на шейку матки. III стадия также подразделяется на: IIIa - рак тела матки с метастазами в регионарные лимфатические узлы, в придатки, во влагалище. IIIб - рак тела матки с инфильтрацией параметрия на одной или на обеих сторонах, перешедших на стенку малого таза, но без вовлечения близлежащих органов. IV стадия: IVa - рак тела матки с прорастанием брюшины к с переходом на мочевой пузырь или прямую кишку, или на подпаянные другие отделы кишечника. IVб - рак тела матки с отдаленными метастазами (в легкие, печень, кости)
Клиническая классификация РТМ I стадия подразделяется на: Ia - опухоль ограничена эндометрием. Iб - инвазия опухоли до 1 см в миометрий. Iв - инвазия опухолью более 1 см, но не доходит до серозной оболочки. II стадия - опухоль распространяется на шейку матки. III стадия также подразделяется на: IIIa - рак тела матки с метастазами в регионарные лимфатические узлы, в придатки, во влагалище. IIIб - рак тела матки с инфильтрацией параметрия на одной или на обеих сторонах, перешедших на стенку малого таза, но без вовлечения близлежащих органов. IV стадия: IVa - рак тела матки с прорастанием брюшины к с переходом на мочевой пузырь или прямую кишку, или на подпаянные другие отделы кишечника. IVб - рак тела матки с отдаленными метастазами (в легкие, печень, кости)
 Классификация по системе TNM Т - первичная опухоль. Тх - недостаточно данных для оценки первичной опухоли. То - первичная опухоль не определяется. Тis- преинвазивная карцинома (carcinoma in situ), атипическая гиперплазия эндометрия. Т 1 - опухоль ограничена телом матки Т 2 - опухоль распространяется на шейку матки, но не за пределы матки. ТЗ - опухоль распространяется за пределы матки, но остается в пределах малого таза. Т 4 - опухоль распространяется из слизистую мочевого пузыря или прямой кишки и/или выходит за пределы малого таза.
Классификация по системе TNM Т - первичная опухоль. Тх - недостаточно данных для оценки первичной опухоли. То - первичная опухоль не определяется. Тis- преинвазивная карцинома (carcinoma in situ), атипическая гиперплазия эндометрия. Т 1 - опухоль ограничена телом матки Т 2 - опухоль распространяется на шейку матки, но не за пределы матки. ТЗ - опухоль распространяется за пределы матки, но остается в пределах малого таза. Т 4 - опухоль распространяется из слизистую мочевого пузыря или прямой кишки и/или выходит за пределы малого таза.
 Классификация по системе TNM N - регионарные (тазовые) лимфатические узлы. Для рака тела матки регионарными лимфатическими узлами являются подчревные (обтураторные), подвздошные (общие, внутренние и наружные), расположенные около матки и сакральные. Nx - состояние регионарных лимфатических узлов оценить невозможно. Nо - нет признаков поражения метастазами регионарных лимфоузлов. N 1 - метастазы в регионарных лимфатических узлах. М - отдаленные метастазы. Мх -недостаточно данных для определения отдаленных метастазов. М 0 - нет признаков отдаленных метастазов. М 1 - имеются отдаленные метастазы.
Классификация по системе TNM N - регионарные (тазовые) лимфатические узлы. Для рака тела матки регионарными лимфатическими узлами являются подчревные (обтураторные), подвздошные (общие, внутренние и наружные), расположенные около матки и сакральные. Nx - состояние регионарных лимфатических узлов оценить невозможно. Nо - нет признаков поражения метастазами регионарных лимфоузлов. N 1 - метастазы в регионарных лимфатических узлах. М - отдаленные метастазы. Мх -недостаточно данных для определения отдаленных метастазов. М 0 - нет признаков отдаленных метастазов. М 1 - имеются отдаленные метастазы.
 Группировка по стадиям Стадия 0 Тis. No. Mо Стадия 1 а Т 1 a. Nо. Мо Стадия 1 б Т 1 в. Nо. Mо Стадия II Т 2 No. Mo Стадия III Т 1 N 1 Mo T 2 N 1 Mo Т 3 любая N Мо Стадия IVа T 4 любая N Мо Стадия IVв Любая Т любая N М 1.
Группировка по стадиям Стадия 0 Тis. No. Mо Стадия 1 а Т 1 a. Nо. Мо Стадия 1 б Т 1 в. Nо. Mо Стадия II Т 2 No. Mo Стадия III Т 1 N 1 Mo T 2 N 1 Mo Т 3 любая N Мо Стадия IVа T 4 любая N Мо Стадия IVв Любая Т любая N М 1.
 Клиническое течение РТМ Основное проявление РТМ – маточное кровотечение. Этот симптом наблюдается у 70 -90% больных. В репродуктивном возрасте кровотечение происходит по типу мено- и метроррагии, в пременопаузе – по ациклическому типу, в постменопаузе – в виде кровянистых выделений мажущего характера. Лейкорея и боли, которые при этой патологии появляются раньше, чем при РШМ, менее постоянны, имеют схваткообразный характер и сопровождаются усилением выделений.
Клиническое течение РТМ Основное проявление РТМ – маточное кровотечение. Этот симптом наблюдается у 70 -90% больных. В репродуктивном возрасте кровотечение происходит по типу мено- и метроррагии, в пременопаузе – по ациклическому типу, в постменопаузе – в виде кровянистых выделений мажущего характера. Лейкорея и боли, которые при этой патологии появляются раньше, чем при РШМ, менее постоянны, имеют схваткообразный характер и сопровождаются усилением выделений.
 Этапы клинического течения РТМ I этап клинического течения РТМ охватывает период от возникновения инвазивного рака до момента его глубокого прорастания в миометрий. II этап клинического течения характеризуется местно-регионарным распространением. III этап клинического течения диссеминация процесса
Этапы клинического течения РТМ I этап клинического течения РТМ охватывает период от возникновения инвазивного рака до момента его глубокого прорастания в миометрий. II этап клинического течения характеризуется местно-регионарным распространением. III этап клинического течения диссеминация процесса
 Диагностика РТМ -Общий гинекологический осмотр -УЗИ -Цитология аспирата эндометрия -Гистероскопия с прицельной биопсией -Раздельное диагностическое выскабливание матки -Ректороманоскопия -Цистоскопия -УЗИ почек, экскреторная урография -Рентгенография грудной клетки -УЗИ печени -УЗИ забрюшинных лимфатических узлов -Сканирование и рентгенография костей скелета -Компьютерная томография -Магнитно-резонансная томография
Диагностика РТМ -Общий гинекологический осмотр -УЗИ -Цитология аспирата эндометрия -Гистероскопия с прицельной биопсией -Раздельное диагностическое выскабливание матки -Ректороманоскопия -Цистоскопия -УЗИ почек, экскреторная урография -Рентгенография грудной клетки -УЗИ печени -УЗИ забрюшинных лимфатических узлов -Сканирование и рентгенография костей скелета -Компьютерная томография -Магнитно-резонансная томография
 Двуручное ректовагинальноабдоминальное исследование в ряде случаев может подтвердить подозрение на рак тела матки (разномерное увеличение матки, приобретение ею округлой формы и неравномерной консистенции с участками размягчения и уплотнения за счет растяжения полости скопившимися в ней продуктами распада опухоли).
Двуручное ректовагинальноабдоминальное исследование в ряде случаев может подтвердить подозрение на рак тела матки (разномерное увеличение матки, приобретение ею округлой формы и неравномерной консистенции с участками размягчения и уплотнения за счет растяжения полости скопившимися в ней продуктами распада опухоли).
 Особое место в диагностике рака тела матки занимает гистероскопия с прицельной биопсией, которую пока применяют, в основном в стационаре. Вместе с тем высокая эффективность выявления заболевания даже в начальных его стадиях (информативность метода при начальных формах рака эндометрия достигает 94, 4%) определяет перспективность использования этого метода на ранних этапах диагностики.
Особое место в диагностике рака тела матки занимает гистероскопия с прицельной биопсией, которую пока применяют, в основном в стационаре. Вместе с тем высокая эффективность выявления заболевания даже в начальных его стадиях (информативность метода при начальных формах рака эндометрия достигает 94, 4%) определяет перспективность использования этого метода на ранних этапах диагностики.
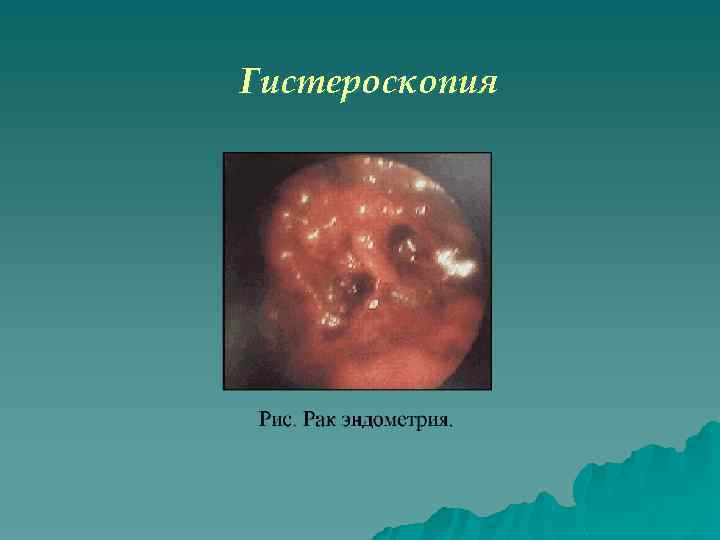 Гистероскопия
Гистероскопия
 Общеизвестна информативность метода гистеросальпингографии в плане первичного установления опухолевого очага в полости матки, которая при распространенном раке эндометрия достигает почти 90%), а при начальном опухолевом процессе не превышает 46%).
Общеизвестна информативность метода гистеросальпингографии в плане первичного установления опухолевого очага в полости матки, которая при распространенном раке эндометрия достигает почти 90%), а при начальном опухолевом процессе не превышает 46%).
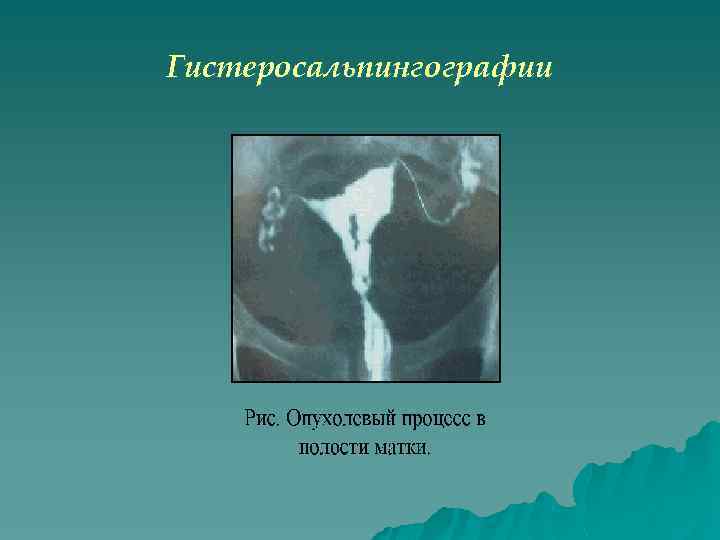 Гистеросальпингографии
Гистеросальпингографии
 За последние годы значительно возросла роль ультразвукового метода, позволяющего установить параметры первичного опухолевого очага и получить данные о состоянии эндометрия, придатков матки, взаимоотношениях органов малого таза с другими антомическими структурами, планировать лучевую терапию. Особое внимание следует обратить на то, что с помощью этого метода можно получить информацию о глубине инфильтрации опухолью миометрия - одном из основных критериев прогноза. Информативность данного метода приближается к 80%.
За последние годы значительно возросла роль ультразвукового метода, позволяющего установить параметры первичного опухолевого очага и получить данные о состоянии эндометрия, придатков матки, взаимоотношениях органов малого таза с другими антомическими структурами, планировать лучевую терапию. Особое внимание следует обратить на то, что с помощью этого метода можно получить информацию о глубине инфильтрации опухолью миометрия - одном из основных критериев прогноза. Информативность данного метода приближается к 80%.
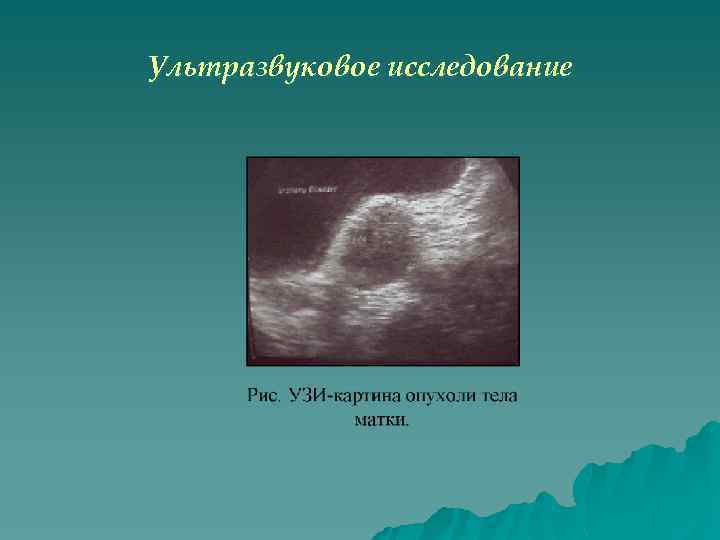 Ультразвуковое исследование
Ультразвуковое исследование
 Для лечения больных раком тела матки в настоящее время применяются различные методы: хирургический, комбинированный, сочетанная лучевая терапия, гормоно- и химиотерапия.
Для лечения больных раком тела матки в настоящее время применяются различные методы: хирургический, комбинированный, сочетанная лучевая терапия, гормоно- и химиотерапия.
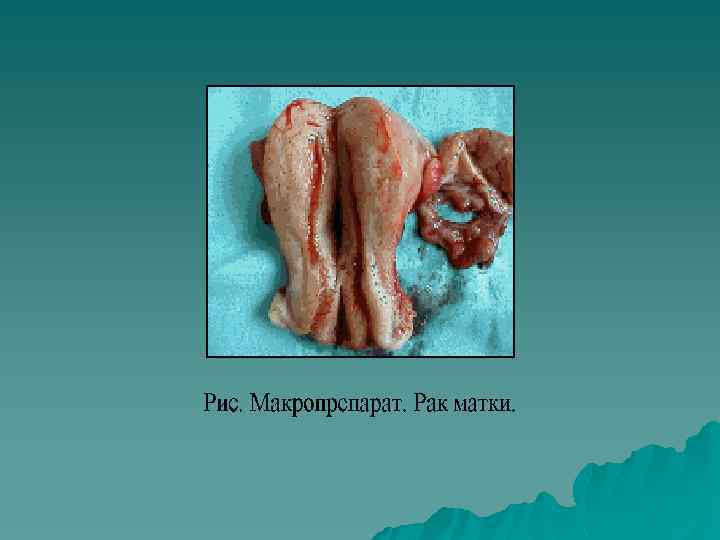
 Оперативное лечение включает: экстирпацию матки с придатками расширенную экстирпацию матки с придатками (лимфаденэктомия, резекция большого сальника)
Оперативное лечение включает: экстирпацию матки с придатками расширенную экстирпацию матки с придатками (лимфаденэктомия, резекция большого сальника)
 Лучевое лечение, включающее лучевое воздействие в пред - или послеоперационном периоде, применяемое при соответствующих показаниах, заметно повышает эффективность лечения. Предоперационную лучевую терапию используют редко. Показания к дистанционной лучевой терапии после операции определяются расположением опухоли в области дна, трубных углов и боковых стенок без перехода на нижнюю треть матки; глубиной инвазии опухоли в миометрий на 1/3 и более; умеренной степенью дифференцировки опухоли.
Лучевое лечение, включающее лучевое воздействие в пред - или послеоперационном периоде, применяемое при соответствующих показаниах, заметно повышает эффективность лечения. Предоперационную лучевую терапию используют редко. Показания к дистанционной лучевой терапии после операции определяются расположением опухоли в области дна, трубных углов и боковых стенок без перехода на нижнюю треть матки; глубиной инвазии опухоли в миометрий на 1/3 и более; умеренной степенью дифференцировки опухоли.
 У больных с повышенным риском метастазирования рака эндометрия во влагалище (поражение нижнего сегмента матки, канала шейки матки, низкой степени дифференцировки опухоли) целесообразно в послеоперационном периоде провести сочетанную лучевую терапию. При выполнении сочетанного лучевого лечения облучение начинают с дистанционной гамма-терапии на область малого таза и путей метастазирования в статическом или подвижном режиме до очаговой дозы в точке А 20 Гр. Далее дистанционную гамма-терапию продолжают только на зоны регионарного метастазирования, чередуя с внутриполостной гамматерапией на влагалищную трубку. Разовая доза 2 Гр в точке В до суммарной очаговой дозы 40 -42 Гр. Внутриполостное облучение влагалищной трубки проводят путем автоматизированного последовательного введения кольпостатов и источников высокой активности ("АГАТ-Б") по 3 Гр за 7 -8 фракций до суммарной дозы 21 -24 Гр на глубине 0, 5 см от слизистой оболочки влагалища.
У больных с повышенным риском метастазирования рака эндометрия во влагалище (поражение нижнего сегмента матки, канала шейки матки, низкой степени дифференцировки опухоли) целесообразно в послеоперационном периоде провести сочетанную лучевую терапию. При выполнении сочетанного лучевого лечения облучение начинают с дистанционной гамма-терапии на область малого таза и путей метастазирования в статическом или подвижном режиме до очаговой дозы в точке А 20 Гр. Далее дистанционную гамма-терапию продолжают только на зоны регионарного метастазирования, чередуя с внутриполостной гамматерапией на влагалищную трубку. Разовая доза 2 Гр в точке В до суммарной очаговой дозы 40 -42 Гр. Внутриполостное облучение влагалищной трубки проводят путем автоматизированного последовательного введения кольпостатов и источников высокой активности ("АГАТ-Б") по 3 Гр за 7 -8 фракций до суммарной дозы 21 -24 Гр на глубине 0, 5 см от слизистой оболочки влагалища.
 Химиотерапия показана при низкодифференцированных аденокарциномах и серозно-папиллярном раке. Обычно используют комбинации таких препаратов, как производные платины I поколения (цисплатин) или II поколения (карбоплатин), адриамицин, циклофосфан, метотрексат, фторурацил и т. д. В числе наиболее эффективных препаратов, дающих полный и частичный эффект более чем в 20% случаев, следует назвать адриамицин, фармарубицин, препараты платины I и II поколения (схемы САР, СР).
Химиотерапия показана при низкодифференцированных аденокарциномах и серозно-папиллярном раке. Обычно используют комбинации таких препаратов, как производные платины I поколения (цисплатин) или II поколения (карбоплатин), адриамицин, циклофосфан, метотрексат, фторурацил и т. д. В числе наиболее эффективных препаратов, дающих полный и частичный эффект более чем в 20% случаев, следует назвать адриамицин, фармарубицин, препараты платины I и II поколения (схемы САР, СР).
 Базисные препараты для лекарственной терапии РТМ u Антранциклины доксорубицин, эпирубицин(фармарубицин), липосомальный доксорубицин (келикс) Алкилирующие агенты: препараты платины (цисплатин, карбоплатин, оксалиплатин) u Ингибиторы митоза: таксаны (паклитаксел) винкаалкалоиды (винорельбин) u Антиэстрогены ( тамоксифен, фазлодекс) u Прогестины (мегестрол, провера) u Ингибиторы ароматазы (фемара, аримидекс) u Герцептин u
Базисные препараты для лекарственной терапии РТМ u Антранциклины доксорубицин, эпирубицин(фармарубицин), липосомальный доксорубицин (келикс) Алкилирующие агенты: препараты платины (цисплатин, карбоплатин, оксалиплатин) u Ингибиторы митоза: таксаны (паклитаксел) винкаалкалоиды (винорельбин) u Антиэстрогены ( тамоксифен, фазлодекс) u Прогестины (мегестрол, провера) u Ингибиторы ароматазы (фемара, аримидекс) u Герцептин u
 Показания для адъювантной химиотерапии – папиллярный серозный, светлоклеточный и анеуплоидный РТМ, не зависимо от инвазии и размеров опухоли. – РТМ III—IV морфологических стадий (преимущества перед ЛТ, GOG 122, 2006) – РТМ ранних стадий при наличии по крайней мере двух из следующих факторов риска u низкая степень дифференцировки u глубокая инвазия миометрия u поражение стромы шейки матки u опухолевые эмболы в лимфатических и кровеносных сосудах (Fleming J. et al. , ASCO 2006) Необходимо помнить, что светлоклеточная аденокарцинома эндометрия связана с повышенным риском венозных тромбозов. (Carret L. , abs. 5597, ASCO 2007)
Показания для адъювантной химиотерапии – папиллярный серозный, светлоклеточный и анеуплоидный РТМ, не зависимо от инвазии и размеров опухоли. – РТМ III—IV морфологических стадий (преимущества перед ЛТ, GOG 122, 2006) – РТМ ранних стадий при наличии по крайней мере двух из следующих факторов риска u низкая степень дифференцировки u глубокая инвазия миометрия u поражение стромы шейки матки u опухолевые эмболы в лимфатических и кровеносных сосудах (Fleming J. et al. , ASCO 2006) Необходимо помнить, что светлоклеточная аденокарцинома эндометрия связана с повышенным риском венозных тромбозов. (Carret L. , abs. 5597, ASCO 2007)
 п и я 2 Цисплатин 50 мг/м в/в капельно р Эпирубицин 60 мг/м 2 в/в а к Циклофосфан 600 мг/м 2 в/в а в 1 и 21 день одновременно с облучением малого таза до СОД э 45 -50 Гр. и зоны параортальных лимфоузлов н д о
п и я 2 Цисплатин 50 мг/м в/в капельно р Эпирубицин 60 мг/м 2 в/в а к Циклофосфан 600 мг/м 2 в/в а в 1 и 21 день одновременно с облучением малого таза до СОД э 45 -50 Гр. и зоны параортальных лимфоузлов н д о
 Для проведения адъювантного гормонального лечения чаще всего используют прогестагены: 17 -ОПК, депо-провера, фарлутал, депостат, мегейс в сочетании с тамоксифеном или без него. Начинать лечение в этих случаях следует при наличии положительных рецепторов прогестерона и эстрогенов в опухоли.
Для проведения адъювантного гормонального лечения чаще всего используют прогестагены: 17 -ОПК, депо-провера, фарлутал, депостат, мегейс в сочетании с тамоксифеном или без него. Начинать лечение в этих случаях следует при наличии положительных рецепторов прогестерона и эстрогенов в опухоли.
 Схемы адъювантной гормонотерапии: Депо-провера 500 мг 2 раза в неделю 2 месяца, затем 1 раз в неделю; Депостат 200 мг 2 раза в неделю 2 месяца, затем 1 раз в неделю; Провера 500 мг 3 раза в неделю, 2 месяца, затем 2 раза в неделю; Мегейс 160 мг 3 раза в неделю 2 месяца, затем 2 раза в неделю; 17 ОПК 500 мг 3 раза в неделю 2 месяца, затем 2 раза в неделю. Гормонотерапия в монорежиме при невыполнимости оперативного лечения назначантся в более высоких дозировках (17 ОПК 500 мг ежедневно 2 месяца, затем 500 мг через день 2 месяца, затем 2 -3 раза в неделю) в сочетании с тамоксифеном (20 -40 мг) или без него.
Схемы адъювантной гормонотерапии: Депо-провера 500 мг 2 раза в неделю 2 месяца, затем 1 раз в неделю; Депостат 200 мг 2 раза в неделю 2 месяца, затем 1 раз в неделю; Провера 500 мг 3 раза в неделю, 2 месяца, затем 2 раза в неделю; Мегейс 160 мг 3 раза в неделю 2 месяца, затем 2 раза в неделю; 17 ОПК 500 мг 3 раза в неделю 2 месяца, затем 2 раза в неделю. Гормонотерапия в монорежиме при невыполнимости оперативного лечения назначантся в более высоких дозировках (17 ОПК 500 мг ежедневно 2 месяца, затем 500 мг через день 2 месяца, затем 2 -3 раза в неделю) в сочетании с тамоксифеном (20 -40 мг) или без него.
 Пятилетняя выживаемость больных раком тела матки составляет при I стадии – 86 -98%, при II стадии – 70 -71%, при III стадии – 32, 5%, при IV стадии – менее 5%.
Пятилетняя выживаемость больных раком тела матки составляет при I стадии – 86 -98%, при II стадии – 70 -71%, при III стадии – 32, 5%, при IV стадии – менее 5%.
 Группы риска в зависимости от показателей рецидива и выживаемости: (i) риск: стадия Ia/Ib, степень дифференцировки 1 или 2 эндометриоидный вариант; u (ii) умеренный риск: стадия Iс, степень дифференцировки 1 или 2 эндометриоидный вариант, стадия Ia/Ib, степень дифференцировки 3, эндометриоидный вариант; u (iii) высокий риск: стадия Iс, степень дифференцировки З, эндометриоидный вариант; стадия Iа или Ib, или Ic, серозный, светлоклеточный, мелкоклеточный или недифференцированный вариант. u
Группы риска в зависимости от показателей рецидива и выживаемости: (i) риск: стадия Ia/Ib, степень дифференцировки 1 или 2 эндометриоидный вариант; u (ii) умеренный риск: стадия Iс, степень дифференцировки 1 или 2 эндометриоидный вариант, стадия Ia/Ib, степень дифференцировки 3, эндометриоидный вариант; u (iii) высокий риск: стадия Iс, степень дифференцировки З, эндометриоидный вариант; стадия Iа или Ib, или Ic, серозный, светлоклеточный, мелкоклеточный или недифференцированный вариант. u
 Стадия I Группа низкого риска: адъювантное лечение не проводится. u Группа умеренного риска: адъювантная лучевая терапия на область таза значительно сокращает риск тазовых влагалищных рецидивов, но не оказывает влияния на общую выживаемость (ОВ). У пациентов из группы умеренного риска, имеющих два из трех основных факторов риска (возраст >60 лет, глубокая инвазия или степень дифференцировки G 3) частота локорегионарных рецидивов составляет >15%; им может быть рекомендована тазовая и/или внутривлагалищная адъювантная лучевая терапия. u
Стадия I Группа низкого риска: адъювантное лечение не проводится. u Группа умеренного риска: адъювантная лучевая терапия на область таза значительно сокращает риск тазовых влагалищных рецидивов, но не оказывает влияния на общую выживаемость (ОВ). У пациентов из группы умеренного риска, имеющих два из трех основных факторов риска (возраст >60 лет, глубокая инвазия или степень дифференцировки G 3) частота локорегионарных рецидивов составляет >15%; им может быть рекомендована тазовая и/или внутривлагалищная адъювантная лучевая терапия. u
 u Группа высокого риска: рекомендуется проведение лучевой терапии для уменьшения локорегионарного метастазирования. В связи с высокой частотой отдаленного метастазирования требуются новые стратегии адъювантной терапии с целью увеличения выживаемости пациентов этой группы. Последние данные свидетельствуют об эффективности адъювантной химиотерапии.
u Группа высокого риска: рекомендуется проведение лучевой терапии для уменьшения локорегионарного метастазирования. В связи с высокой частотой отдаленного метастазирования требуются новые стратегии адъювантной терапии с целью увеличения выживаемости пациентов этой группы. Последние данные свидетельствуют об эффективности адъювантной химиотерапии.
 Стадия II u Стадия IIa: лечение как в стадии Iа. u Стадия. IIb: расширенная радикальная гистерэктомия, двусторонняя сальпингоофорэктомия с лимфодиссекцией. Пациентам, перенесшим экстрафасциальную гистерэктомию матки или входящим в группу высокого риска (те же критерии, что и при стадии I) показана адъювантная лучевая терапия на область таза с/или без интравагинального облучения.
Стадия II u Стадия IIa: лечение как в стадии Iа. u Стадия. IIb: расширенная радикальная гистерэктомия, двусторонняя сальпингоофорэктомия с лимфодиссекцией. Пациентам, перенесшим экстрафасциальную гистерэктомию матки или входящим в группу высокого риска (те же критерии, что и при стадии I) показана адъювантная лучевая терапия на область таза с/или без интравагинального облучения.
 Стадия III и IV u У пациентов в хорошем общем состоянии рассматривается возможность выполнения циторедуктивной операции в максимальном объеме. u Пациентов с III стадией заболевания, имеющих только положительные результаты перитонеального цитологического исследования, лечат, как пациентов с I или II стадиями заболевания с учетом других клиникоморфологических данных.
Стадия III и IV u У пациентов в хорошем общем состоянии рассматривается возможность выполнения циторедуктивной операции в максимальном объеме. u Пациентов с III стадией заболевания, имеющих только положительные результаты перитонеального цитологического исследования, лечат, как пациентов с I или II стадиями заболевания с учетом других клиникоморфологических данных.
 u Лучевая терапия на область малого таза снижает риск распространения процесса в пределах таза. u В режиме монотерапии выраженный объективный эффект дают цисплатин, карбоплатин, антрациклины и паклитаксел.
u Лучевая терапия на область малого таза снижает риск распространения процесса в пределах таза. u В режиме монотерапии выраженный объективный эффект дают цисплатин, карбоплатин, антрациклины и паклитаксел.
 u Комбинация доксорубицина с цисплатином и паклитакселом (с поддержкой костномозгового кроветворения) значительно увеличивает выживаемость без прогрессирования (ВБП) и общую выживаемость в сравнении с комбинацией цисплатин и доксорубицин, но обладает крайне высокой токсичностью и потому не может быть признана в качестве стандарта.
u Комбинация доксорубицина с цисплатином и паклитакселом (с поддержкой костномозгового кроветворения) значительно увеличивает выживаемость без прогрессирования (ВБП) и общую выживаемость в сравнении с комбинацией цисплатин и доксорубицин, но обладает крайне высокой токсичностью и потому не может быть признана в качестве стандарта.
 u Комбинация цисплатина и доксорубицина существенно улучшает время до прогрессирования и общую выживаемость у пациентов с III и IV стадиями после циторедуктивной операции в оптимальном объеме в сравнении с облучением всего живота (WAR — Whole Abdominal Radiation) и дополнительным облучением на малый таз.
u Комбинация цисплатина и доксорубицина существенно улучшает время до прогрессирования и общую выживаемость у пациентов с III и IV стадиями после циторедуктивной операции в оптимальном объеме в сравнении с облучением всего живота (WAR — Whole Abdominal Radiation) и дополнительным облучением на малый таз.
 Наблюдение u Большинство рецидивов происходят в течение первых 3 -х лет после лечения. Контрольное клиническое обследование, включающее сбор анамнеза, физикальное и гинекологическое обследования, рекомендуется проводить каждые 3 -4 месяца. На четвертом и пятом годах наблюдения рекомендуемый интервал между обследованиями - 6 месяцев, далее ежегодно.
Наблюдение u Большинство рецидивов происходят в течение первых 3 -х лет после лечения. Контрольное клиническое обследование, включающее сбор анамнеза, физикальное и гинекологическое обследования, рекомендуется проводить каждые 3 -4 месяца. На четвертом и пятом годах наблюдения рекомендуемый интервал между обследованиями - 6 месяцев, далее ежегодно.
 Благодарим за внимание!
Благодарим за внимание!


