Рак толстой кишки (презентация).ppt
- Количество слайдов: 122
 Саратовский государственный медицинский университет Кафедра онкологии ФПК ППС
Саратовский государственный медицинский университет Кафедра онкологии ФПК ППС
 РАК ТОЛСТОЙ КИШКИ Зав. кафедрой онкологии ФПК ППС, доктор мед. наук Т. Н. Попова
РАК ТОЛСТОЙ КИШКИ Зав. кафедрой онкологии ФПК ППС, доктор мед. наук Т. Н. Попова
 ЕЖЕГОДНО В МИРЕ РЕГИСТРИРУЕТСЯ ОКОЛО 800 ТЫС. ВНОВЬ ВЫЯВЛЕННЫХ СЛУЧАЕВ РАКА ТОЛСТОЙ КИШКИ НАКОПЛЕННЫЙ КОНТИНГЕНТ СОСТАВЛЯЕТ БОЛЕЕ 3, 5 МЛН. ЧЕЛОВЕК
ЕЖЕГОДНО В МИРЕ РЕГИСТРИРУЕТСЯ ОКОЛО 800 ТЫС. ВНОВЬ ВЫЯВЛЕННЫХ СЛУЧАЕВ РАКА ТОЛСТОЙ КИШКИ НАКОПЛЕННЫЙ КОНТИНГЕНТ СОСТАВЛЯЕТ БОЛЕЕ 3, 5 МЛН. ЧЕЛОВЕК
 Наиболее низкие показатели Наиболее высокие показатели 1, 6 -5, 9 на 100 тыс. 46, 3 -51, 7 на 100 тыс. АФРИКА ЗАПАДНАЯ ЕВРОПА СЕВЕРНАЯ АМЕРИКА Средние показатели 23, 6 -33, 8 на 100 тыс. ЮЖНАЯ и ВОСТОЧНАЯ ЕВРОПА
Наиболее низкие показатели Наиболее высокие показатели 1, 6 -5, 9 на 100 тыс. 46, 3 -51, 7 на 100 тыс. АФРИКА ЗАПАДНАЯ ЕВРОПА СЕВЕРНАЯ АМЕРИКА Средние показатели 23, 6 -33, 8 на 100 тыс. ЮЖНАЯ и ВОСТОЧНАЯ ЕВРОПА
 2 МЕСТО В РАЗВИТЫХ СТРАНАХ 8 МЕСТО В РАЗВИВАЮЩИХСЯ СТРАНАХ 3 МЕСТО В РОССИИ
2 МЕСТО В РАЗВИТЫХ СТРАНАХ 8 МЕСТО В РАЗВИВАЮЩИХСЯ СТРАНАХ 3 МЕСТО В РОССИИ
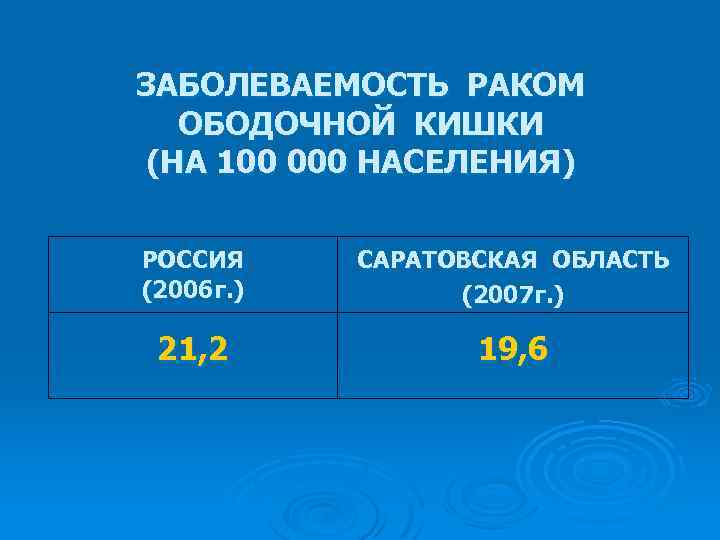 ЗАБОЛЕВАЕМОСТЬ РАКОМ ОБОДОЧНОЙ КИШКИ (НА 100 000 НАСЕЛЕНИЯ) РОССИЯ (2006 г. ) САРАТОВСКАЯ ОБЛАСТЬ (2007 г. ) 21, 2 1 9 , 6
ЗАБОЛЕВАЕМОСТЬ РАКОМ ОБОДОЧНОЙ КИШКИ (НА 100 000 НАСЕЛЕНИЯ) РОССИЯ (2006 г. ) САРАТОВСКАЯ ОБЛАСТЬ (2007 г. ) 21, 2 1 9 , 6
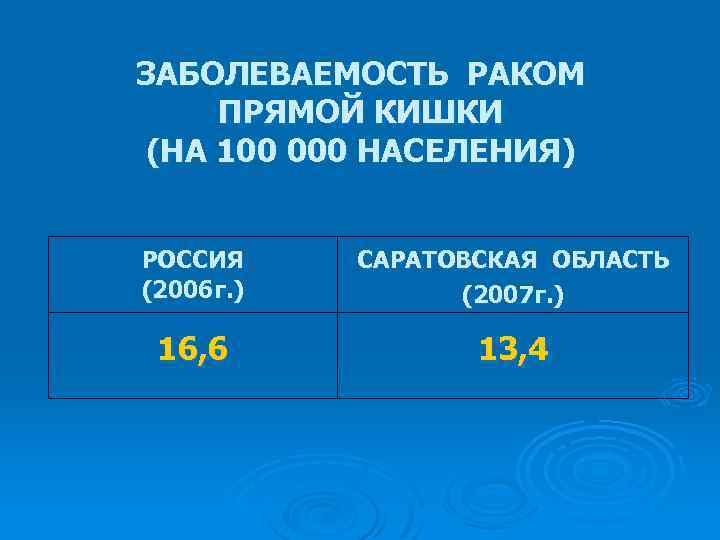 ЗАБОЛЕВАЕМОСТЬ РАКОМ ПРЯМОЙ КИШКИ (НА 100 000 НАСЕЛЕНИЯ) РОССИЯ (2006 г. ) САРАТОВСКАЯ ОБЛАСТЬ (2007 г. ) 16, 6 13, 4
ЗАБОЛЕВАЕМОСТЬ РАКОМ ПРЯМОЙ КИШКИ (НА 100 000 НАСЕЛЕНИЯ) РОССИЯ (2006 г. ) САРАТОВСКАЯ ОБЛАСТЬ (2007 г. ) 16, 6 13, 4
 30% 5 -ЛЕТНЯЯ ВЫЖИВАЕМОСТЬ НА ВСЮ ГРУППУ ПЕРВИЧНО ЗАРЕГЕСТРИРОВАННЫХ БОЛЬНЫХ РАКОМ ТОЛСТОЙ КИШКИ
30% 5 -ЛЕТНЯЯ ВЫЖИВАЕМОСТЬ НА ВСЮ ГРУППУ ПЕРВИЧНО ЗАРЕГЕСТРИРОВАННЫХ БОЛЬНЫХ РАКОМ ТОЛСТОЙ КИШКИ
 У 70 – 90% БОЛЬНЫХ РАКОМ ПРЯМОЙ КИШКИ ОТМЕЧАЮТСЯ КРОВЯНИСТЫЕ ВЫДЕЛЕНИЯ У 85% ВПЕРВЫЕ ОБРАТИВШИХСЯ БОЛЬНЫХ С СИМПТОМАМИ КРОВЯНИСТЫХ ВЫДЕЛЕНИЙ ИЗ ПРЯМОЙ КИШКИ ПЕРВОНАЧАЛЬНО БЫЛ ПОСТАВЛЕН ДИАГНОЗ ГЕМОРРОЯ В ПОЛИКЛИНИКЕ 35% ПАЦИЕНТАМ, ОБРАТИВШИМСЯ С ЖАЛОБАМИ, ВЫПОЛНЯЕТСЯ ПАЛЬЦЕВОЕ ИССЛЕДОВАНИЕ ПРЯМОЙ КИШКИ; 3% БОЛЬНЫМ ПРОИЗВОДИТСЯ РЕКТОРОМАНОСКОПИЯ
У 70 – 90% БОЛЬНЫХ РАКОМ ПРЯМОЙ КИШКИ ОТМЕЧАЮТСЯ КРОВЯНИСТЫЕ ВЫДЕЛЕНИЯ У 85% ВПЕРВЫЕ ОБРАТИВШИХСЯ БОЛЬНЫХ С СИМПТОМАМИ КРОВЯНИСТЫХ ВЫДЕЛЕНИЙ ИЗ ПРЯМОЙ КИШКИ ПЕРВОНАЧАЛЬНО БЫЛ ПОСТАВЛЕН ДИАГНОЗ ГЕМОРРОЯ В ПОЛИКЛИНИКЕ 35% ПАЦИЕНТАМ, ОБРАТИВШИМСЯ С ЖАЛОБАМИ, ВЫПОЛНЯЕТСЯ ПАЛЬЦЕВОЕ ИССЛЕДОВАНИЕ ПРЯМОЙ КИШКИ; 3% БОЛЬНЫМ ПРОИЗВОДИТСЯ РЕКТОРОМАНОСКОПИЯ
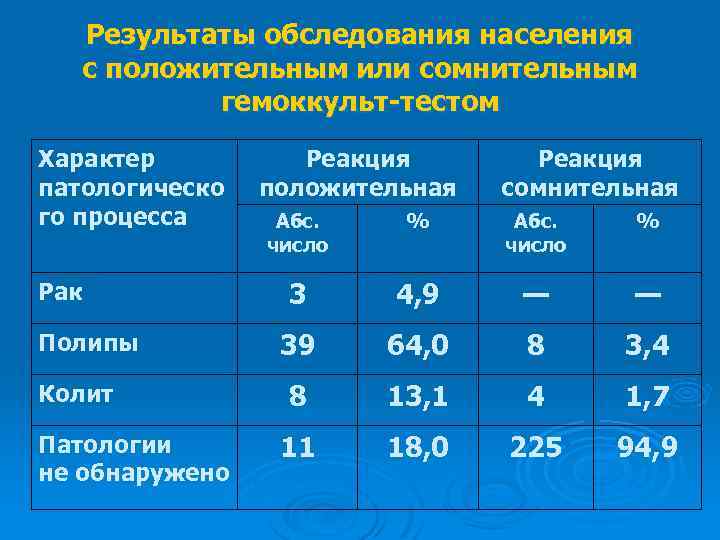 Результаты обследования населения с положительным или сомнительным гемоккульт-тестом Характер патологическо го процесса Рак Полипы Колит Патологии не обнаружено Реакция положительная Реакция сомнительная Абс. число % 3 4, 9 — — 39 64, 0 8 3, 4 8 13, 1 4 1, 7 11 18, 0 225 94, 9
Результаты обследования населения с положительным или сомнительным гемоккульт-тестом Характер патологическо го процесса Рак Полипы Колит Патологии не обнаружено Реакция положительная Реакция сомнительная Абс. число % 3 4, 9 — — 39 64, 0 8 3, 4 8 13, 1 4 1, 7 11 18, 0 225 94, 9
 Гемоккульт-тест широко используется в Европе и США, а также странах Юго. Восточной Азии и Японии. В странах Западной Европы была создана программа скрининговых исследований колоректального рака. На 3 -й международной конференции в Дублине (Ирландия, 2001) были приведены итоги этой программы. При сравнении показатели смертности от колоректального рака между исследуемой и контрольной группами выявлено, что в тестируемой группе она на 14 - 18% ниже, чем в контрольной.
Гемоккульт-тест широко используется в Европе и США, а также странах Юго. Восточной Азии и Японии. В странах Западной Европы была создана программа скрининговых исследований колоректального рака. На 3 -й международной конференции в Дублине (Ирландия, 2001) были приведены итоги этой программы. При сравнении показатели смертности от колоректального рака между исследуемой и контрольной группами выявлено, что в тестируемой группе она на 14 - 18% ниже, чем в контрольной.
 Проведение скрининга колоректального рака должно осуществляться не менее одного раза в 2 года с использованием нерегидратированного гемоккульт-теста, который в литературе обозначается как гемоккульт-тест II. В настоящее время это единственный тест, который может быть распространен на популяционном уровне среди взрослых лиц в возрасте от 50 до 74 лет при отсутствии симптомов, указывающих на патологию со стороны толстой кишки.
Проведение скрининга колоректального рака должно осуществляться не менее одного раза в 2 года с использованием нерегидратированного гемоккульт-теста, который в литературе обозначается как гемоккульт-тест II. В настоящее время это единственный тест, который может быть распространен на популяционном уровне среди взрослых лиц в возрасте от 50 до 74 лет при отсутствии симптомов, указывающих на патологию со стороны толстой кишки.
 Ø Эти положения были одобрены Европейским комитетом по борьбе со злокачественными опухолями. Согласие пациентов на это исследование должно быть не менее чем у 50%; при этом колоноскопию необходимо провести у каждого пациента с положительным гемоккульт-тестом.
Ø Эти положения были одобрены Европейским комитетом по борьбе со злокачественными опухолями. Согласие пациентов на это исследование должно быть не менее чем у 50%; при этом колоноскопию необходимо провести у каждого пациента с положительным гемоккульт-тестом.
 Ø При первичном скрининге колоректального рака число положительных ответов с гемоккульттестом II без соблюдения диеты составляет 2%, при последующем скрининге 1 -1, 5%. Специфичность теста составляет 98%, чувствительность 5060%. Ø Европейский комитет по борьбе со злокачественными опухолями считает, что позитивная прогностическая ценность скрининга колоректального рака с использованием гемоккульт-теста II составляет 10% для рака и 30 -40% для аденом толстой кишки.
Ø При первичном скрининге колоректального рака число положительных ответов с гемоккульттестом II без соблюдения диеты составляет 2%, при последующем скрининге 1 -1, 5%. Специфичность теста составляет 98%, чувствительность 5060%. Ø Европейский комитет по борьбе со злокачественными опухолями считает, что позитивная прогностическая ценность скрининга колоректального рака с использованием гемоккульт-теста II составляет 10% для рака и 30 -40% для аденом толстой кишки.
 Ø Таким образом, гемоккульт-тест является эффективным способом выявления опухолей толстой кишки профилактических осмотрах населения. Поскольку рак толстой кишки развивается преимущественно из полипов, которые также можно выявлять с помощью гемоккульт-теста, то этот метод можно рассматривать не только как способ раннего выявления рака, но и как способ профилактики. Выявление и лечение полипов толстой кишки является важным профилактическим мероприятием в снижении рака прямой и ободочной кишки.
Ø Таким образом, гемоккульт-тест является эффективным способом выявления опухолей толстой кишки профилактических осмотрах населения. Поскольку рак толстой кишки развивается преимущественно из полипов, которые также можно выявлять с помощью гемоккульт-теста, то этот метод можно рассматривать не только как способ раннего выявления рака, но и как способ профилактики. Выявление и лечение полипов толстой кишки является важным профилактическим мероприятием в снижении рака прямой и ободочной кишки.
 ØВ США предложен еще один скрининговый тест для раннего выявления рака прямой и ободочной кишок. Метод основан на анализе слизи, взятой из прямой кишки. Окрашенная реагентом Шиффа слизь при наличии неоплазии в толстой кишке меняет свой цвет. Метод прост, дешев, быстр и не дает большого процента ложноположительных и ложноотрицательных результатов.
ØВ США предложен еще один скрининговый тест для раннего выявления рака прямой и ободочной кишок. Метод основан на анализе слизи, взятой из прямой кишки. Окрашенная реагентом Шиффа слизь при наличии неоплазии в толстой кишке меняет свой цвет. Метод прост, дешев, быстр и не дает большого процента ложноположительных и ложноотрицательных результатов.
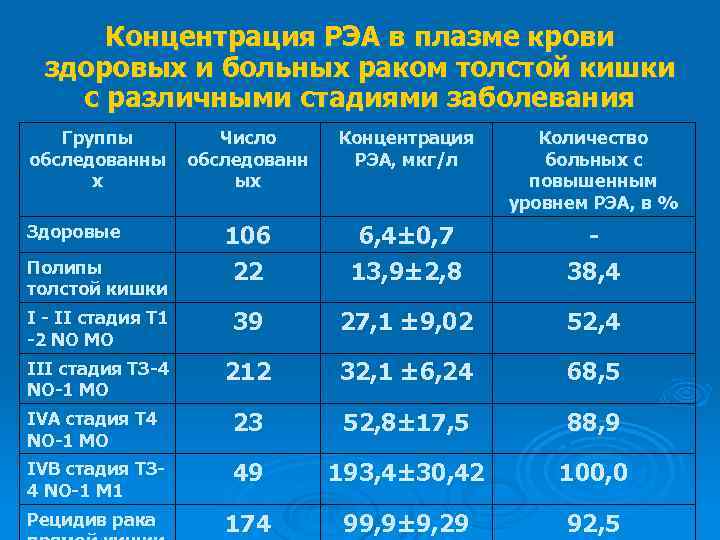 Концентрация РЭА в плазме крови здоровых и больных раком толстой кишки с различными стадиями заболевания Группы обследованны х Число обследованн ых Концентрация РЭА, мкг/л Количество больных с повышенным уровнем РЭА, в % 106 6, 4± 0, 7 - Полипы толстой кишки 22 13, 9± 2, 8 38, 4 I - II стадия Т 1 -2 NО МО 39 27, 1 ± 9, 02 52, 4 III стадия ТЗ-4 NО-1 МО 212 32, 1 ± 6, 24 68, 5 IVА стадия Т 4 NО-1 МО 23 52, 8± 17, 5 88, 9 IVВ стадия ТЗ 4 NО-1 М 1 49 193, 4± 30, 42 100, 0 Рецидив рака 174 99, 9± 9, 29 92, 5 Здоровые
Концентрация РЭА в плазме крови здоровых и больных раком толстой кишки с различными стадиями заболевания Группы обследованны х Число обследованн ых Концентрация РЭА, мкг/л Количество больных с повышенным уровнем РЭА, в % 106 6, 4± 0, 7 - Полипы толстой кишки 22 13, 9± 2, 8 38, 4 I - II стадия Т 1 -2 NО МО 39 27, 1 ± 9, 02 52, 4 III стадия ТЗ-4 NО-1 МО 212 32, 1 ± 6, 24 68, 5 IVА стадия Т 4 NО-1 МО 23 52, 8± 17, 5 88, 9 IVВ стадия ТЗ 4 NО-1 М 1 49 193, 4± 30, 42 100, 0 Рецидив рака 174 99, 9± 9, 29 92, 5 Здоровые
 Ø Диагностика рака прямой Ø Рак прямой кишки - это кишки в принципе не визуализируемая опухоль и представляет каких-либо порой достаточно только трудностей. Как справедливо пальцевого обследования отметил Р. Dеуhlе, если врач прямой кишки, что позволяет или просто медицинский в значительном проценте работник или сам больной случаев установить диагноз. подумают об опухолевой Использование ректоскопии патологии, то в 30% случаев позволяет полностью обеспечено безусловное подтвердить или отвергнуть установление диагноза, тем предполагаемый диагноз. более рака прямой кишки. Это простые истины, но, зачастую пренебрегая этими двумя методами обследования больных раком прямой кишки, первичный диагноз устанавливается в запущенной стадии.
Ø Диагностика рака прямой Ø Рак прямой кишки - это кишки в принципе не визуализируемая опухоль и представляет каких-либо порой достаточно только трудностей. Как справедливо пальцевого обследования отметил Р. Dеуhlе, если врач прямой кишки, что позволяет или просто медицинский в значительном проценте работник или сам больной случаев установить диагноз. подумают об опухолевой Использование ректоскопии патологии, то в 30% случаев позволяет полностью обеспечено безусловное подтвердить или отвергнуть установление диагноза, тем предполагаемый диагноз. более рака прямой кишки. Это простые истины, но, зачастую пренебрегая этими двумя методами обследования больных раком прямой кишки, первичный диагноз устанавливается в запущенной стадии.
 Ø В последнее время значительный интерес вызывают последние разработки отечественных и зарубежных исследователей, позволяющие проведение генетического скрининга колоректального рака. Клетки колоректального рака выделяются с калом, обеспечивая потенциальную возможность раннего выявления заболевания неинвазивной методикой. Метод основывается на выявлении мутантных генов ТР 53, ВАТ 26, К-КА 5 в выделенной из кала и умноженной с помощью полимеразной цепной реакции (РСR) ДНК клеток колоректальных опухолей. Данная методика находится в стадии разработки, однако, при достижении приемлемой чувствительности и специфичности, а также стоимости, перспективы ее весьма многообещающи.
Ø В последнее время значительный интерес вызывают последние разработки отечественных и зарубежных исследователей, позволяющие проведение генетического скрининга колоректального рака. Клетки колоректального рака выделяются с калом, обеспечивая потенциальную возможность раннего выявления заболевания неинвазивной методикой. Метод основывается на выявлении мутантных генов ТР 53, ВАТ 26, К-КА 5 в выделенной из кала и умноженной с помощью полимеразной цепной реакции (РСR) ДНК клеток колоректальных опухолей. Данная методика находится в стадии разработки, однако, при достижении приемлемой чувствительности и специфичности, а также стоимости, перспективы ее весьма многообещающи.
 Для улучшения диагностики онкологических больных необходимо: помимо общегосударственных усилий (организация смотровых кабинетов и обеспечение их соответствующей аппаратурой, укомплектованность врачами специалистами и т. д. ), также проведение целенаправленных скрининговых мероприятий; Ø необходима дальнейшая научная разработка критериев, позволяющих формировать группу повышенного риска; Ø внедрение в клиническую практику массовых обследований, анализа кала на скрытую кровь, последующее углубленное обследование с применением рентгенологических и эндоскопических методов. Ø
Для улучшения диагностики онкологических больных необходимо: помимо общегосударственных усилий (организация смотровых кабинетов и обеспечение их соответствующей аппаратурой, укомплектованность врачами специалистами и т. д. ), также проведение целенаправленных скрининговых мероприятий; Ø необходима дальнейшая научная разработка критериев, позволяющих формировать группу повышенного риска; Ø внедрение в клиническую практику массовых обследований, анализа кала на скрытую кровь, последующее углубленное обследование с применением рентгенологических и эндоскопических методов. Ø
 ФАКТОРЫ РИСКА ДЛЯ КОЛОРЕКТАЛЬНОГО РАКА Ø Ø Ø Ø Ø диета с высоким содержанием жира и низким содержанием растительных волокон, возраст старше 40 лет, колоректальный рак у родственников, наследственный аденоматозный полипоз, наследственный неполипозный колоректальный рак, ранее перенесенный колоректальный рак или аденома, неспецифический язвенный колит, болезнь Крона, гамартомы, полипы и полипозные синдромы (Гарднера, Пейтца-Егерса-Турена и Туркота, семейный ювенильный полипоз).
ФАКТОРЫ РИСКА ДЛЯ КОЛОРЕКТАЛЬНОГО РАКА Ø Ø Ø Ø Ø диета с высоким содержанием жира и низким содержанием растительных волокон, возраст старше 40 лет, колоректальный рак у родственников, наследственный аденоматозный полипоз, наследственный неполипозный колоректальный рак, ранее перенесенный колоректальный рак или аденома, неспецифический язвенный колит, болезнь Крона, гамартомы, полипы и полипозные синдромы (Гарднера, Пейтца-Егерса-Турена и Туркота, семейный ювенильный полипоз).
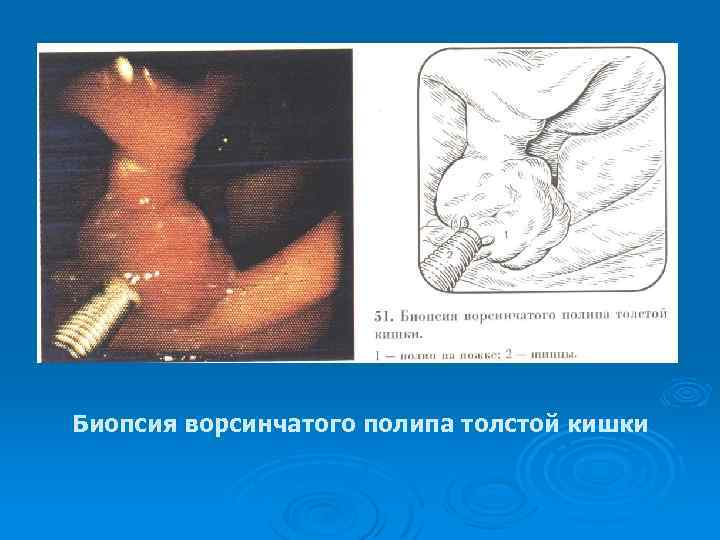 Биопсия ворсинчатого полипа толстой кишки
Биопсия ворсинчатого полипа толстой кишки
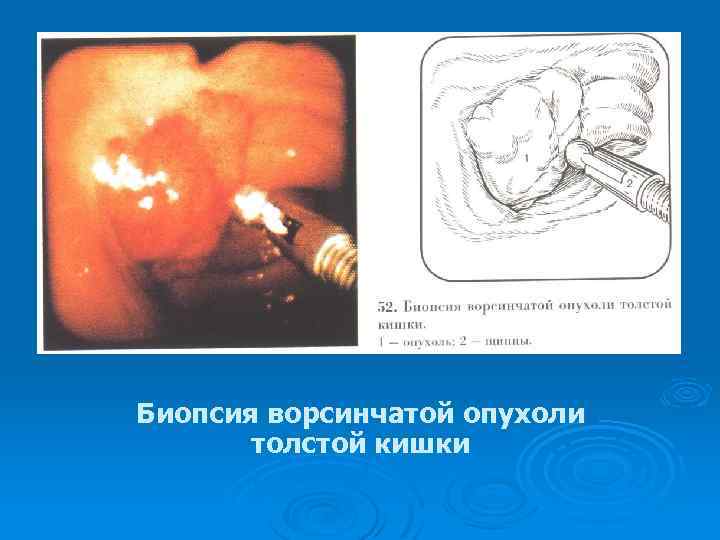 Биопсия ворсинчатой опухоли толстой кишки
Биопсия ворсинчатой опухоли толстой кишки
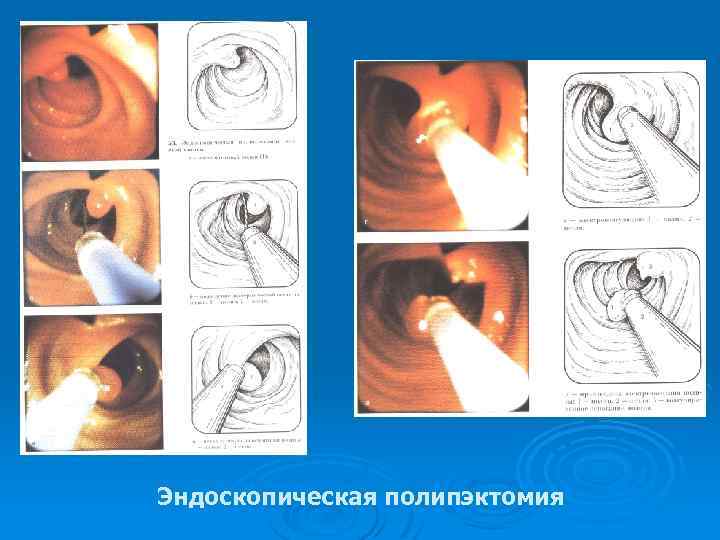 Эндоскопическая полипэктомия
Эндоскопическая полипэктомия
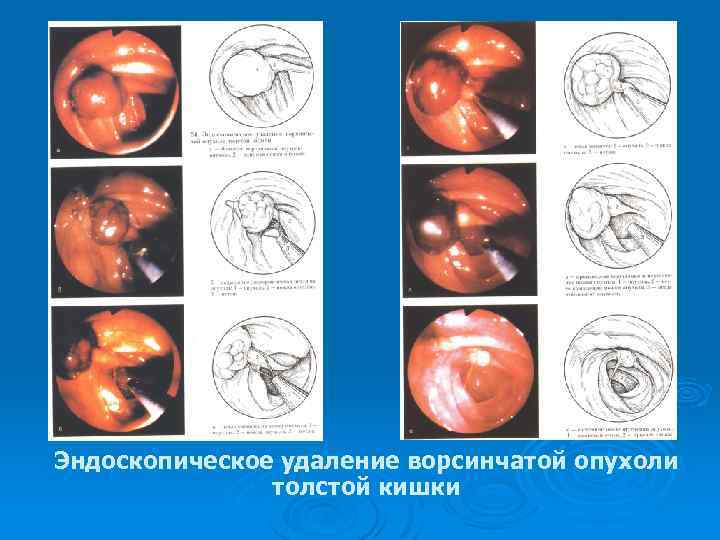 Эндоскопическое удаление ворсинчатой опухоли толстой кишки
Эндоскопическое удаление ворсинчатой опухоли толстой кишки
 Препарат удаленной ворсинчатой опухоли
Препарат удаленной ворсинчатой опухоли
 ЛОКАЛИЗАЦИЯ РАКА В ТОЛСТОЙ КИШКЕ в сигмовидной кишке (50%), Ø слепой (15%), Ø восходящая ободочная кишка – 12%, Ø правый изгиб – 8%, Ø поперечная ободочная кишка – 5%, Ø левый изгиб - 5%, Ø нисходящая ободочная кишка - 5%. Ø
ЛОКАЛИЗАЦИЯ РАКА В ТОЛСТОЙ КИШКЕ в сигмовидной кишке (50%), Ø слепой (15%), Ø восходящая ободочная кишка – 12%, Ø правый изгиб – 8%, Ø поперечная ободочная кишка – 5%, Ø левый изгиб - 5%, Ø нисходящая ободочная кишка - 5%. Ø
 Особенности анатомического строения рака правой и левой половины ободочной кишки Правая половина Левая половина Экзофитные формы рака: Эндофитные формы рака: узловые, Ø полипообразные, Ø ворсинчатопапиллярные Ø блюдцеобразные, Ø диффузноинфильтративные Ø
Особенности анатомического строения рака правой и левой половины ободочной кишки Правая половина Левая половина Экзофитные формы рака: Эндофитные формы рака: узловые, Ø полипообразные, Ø ворсинчатопапиллярные Ø блюдцеобразные, Ø диффузноинфильтративные Ø
 Международная гистологическая классификация опухолей толстой кишки (1981 г. ) Ø Ø Ø Ø аденокарцинома с выделением трех степеней дифференцировки; слизистая аденокарцинома (синонимы — слизистый, или коллоидный, рак); перстневидно-клеточный (слизеобразующий) рак, характеризующийся преобладанием изолированных клеток, растянутых слизистым содержимым; плоскоклеточный рак без выделения ороговевающего или неороговевающего; железисто-плоскоклеточный рак. Аденокарциному с небольшими участками плоскоклеточной дифференцировки следует относить к группе аденокарцином; недифференцированный рак. Для обозначения этих опухолей можно пользоваться терминами «карцинома simplex (простая)» , «медуллярный рак» , «трабекулярный рак» ; неклассифицируемый рак. К этой группе относят опухоли, которые не могут быть отнесены ни к одной из указанных выше категорий опухолей. Выделявшийся ранее солидный рак, или скирр, входит в группу недифференцированного рака.
Международная гистологическая классификация опухолей толстой кишки (1981 г. ) Ø Ø Ø Ø аденокарцинома с выделением трех степеней дифференцировки; слизистая аденокарцинома (синонимы — слизистый, или коллоидный, рак); перстневидно-клеточный (слизеобразующий) рак, характеризующийся преобладанием изолированных клеток, растянутых слизистым содержимым; плоскоклеточный рак без выделения ороговевающего или неороговевающего; железисто-плоскоклеточный рак. Аденокарциному с небольшими участками плоскоклеточной дифференцировки следует относить к группе аденокарцином; недифференцированный рак. Для обозначения этих опухолей можно пользоваться терминами «карцинома simplex (простая)» , «медуллярный рак» , «трабекулярный рак» ; неклассифицируемый рак. К этой группе относят опухоли, которые не могут быть отнесены ни к одной из указанных выше категорий опухолей. Выделявшийся ранее солидный рак, или скирр, входит в группу недифференцированного рака.
 Метастазирование происходит следующими путями: Ø Лимфогенным (30%) Ø Гематогенным (50%) Ø Имплантационным (20%)
Метастазирование происходит следующими путями: Ø Лимфогенным (30%) Ø Гематогенным (50%) Ø Имплантационным (20%)
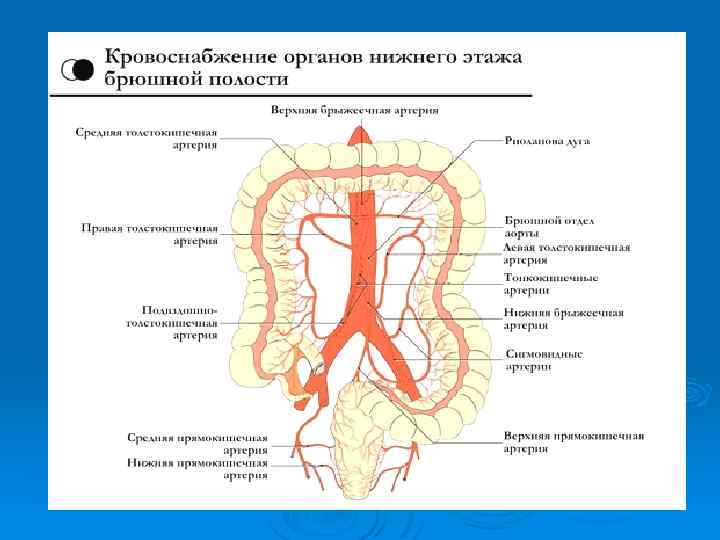
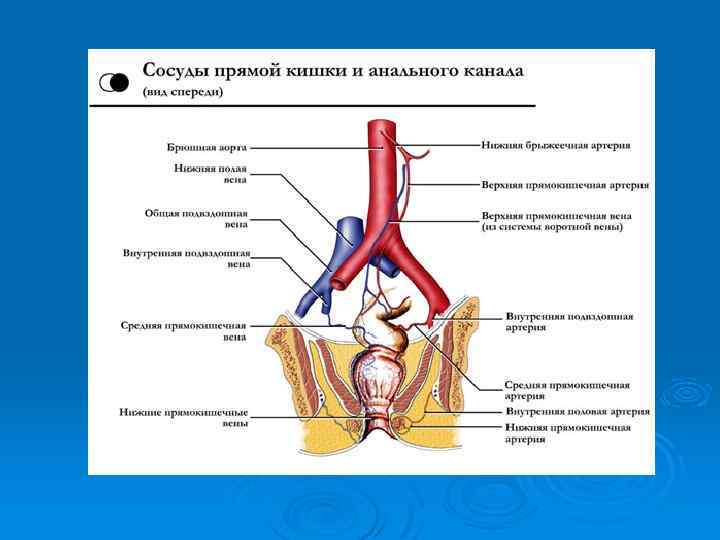
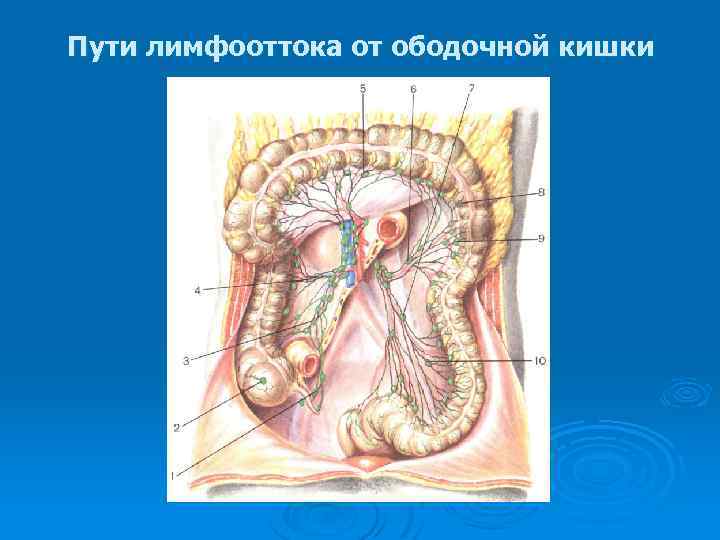 Пути лимфооттока от ободочной кишки
Пути лимфооттока от ободочной кишки
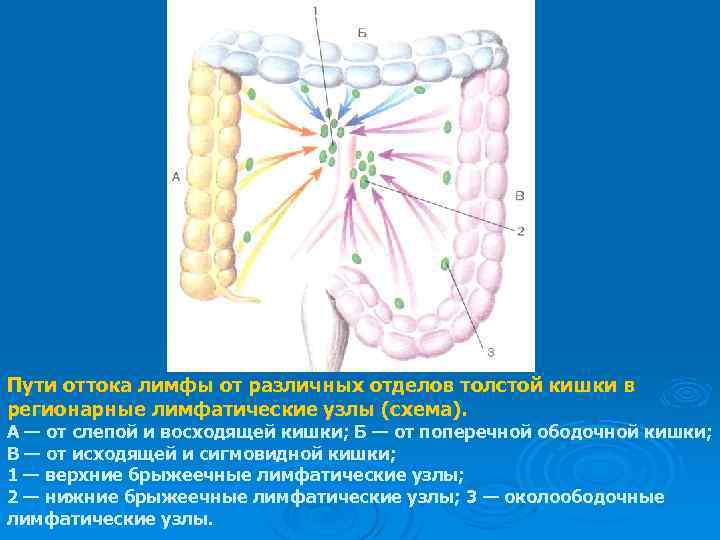 Пути оттока лимфы от различных отделов толстой кишки в регионарные лимфатические узлы (схема). А — от слепой и восходящей кишки; Б — от поперечной ободочной кишки; В — от исходящей и сигмовидной кишки; 1 — верхние брыжеечные лимфатические узлы; 2 — нижние брыжеечные лимфатические узлы; 3 — околоободочные лимфатические узлы.
Пути оттока лимфы от различных отделов толстой кишки в регионарные лимфатические узлы (схема). А — от слепой и восходящей кишки; Б — от поперечной ободочной кишки; В — от исходящей и сигмовидной кишки; 1 — верхние брыжеечные лимфатические узлы; 2 — нижние брыжеечные лимфатические узлы; 3 — околоободочные лимфатические узлы.
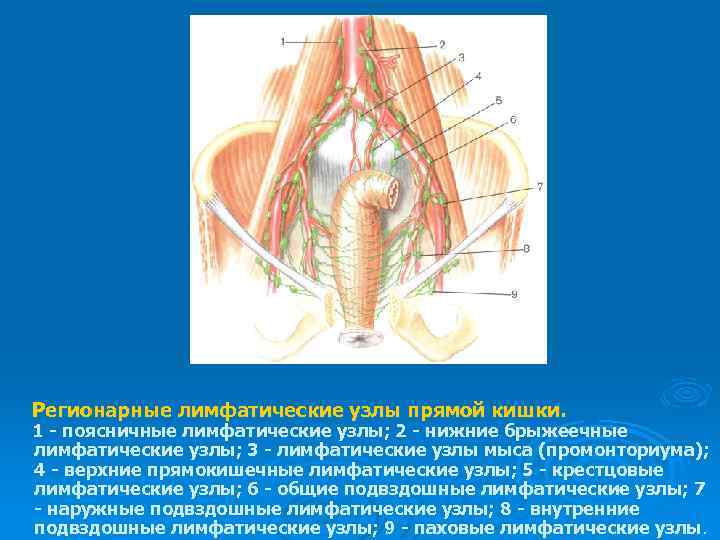 Регионарные лимфатические узлы прямой кишки. 1 - поясничные лимфатические узлы; 2 - нижние брыжеечные лимфатические узлы; 3 - лимфатические узлы мыса (промонториума); 4 - верхние прямокишечные лимфатические узлы; 5 - крестцовые лимфатические узлы; 6 - общие подвздошные лимфатические узлы; 7 - наружные подвздошные лимфатические узлы; 8 - внутренние подвздошные лимфатические узлы; 9 - паховые лимфатические узлы.
Регионарные лимфатические узлы прямой кишки. 1 - поясничные лимфатические узлы; 2 - нижние брыжеечные лимфатические узлы; 3 - лимфатические узлы мыса (промонториума); 4 - верхние прямокишечные лимфатические узлы; 5 - крестцовые лимфатические узлы; 6 - общие подвздошные лимфатические узлы; 7 - наружные подвздошные лимфатические узлы; 8 - внутренние подвздошные лимфатические узлы; 9 - паховые лимфатические узлы.
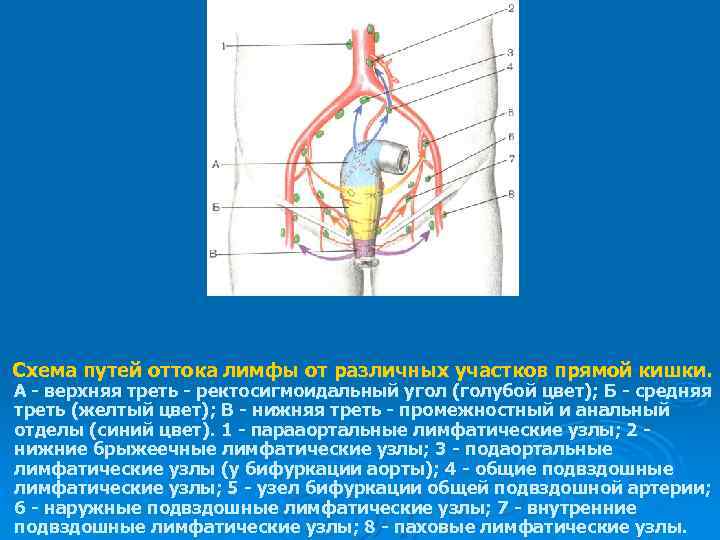 Схема путей оттока лимфы от различных участков прямой кишки. А - верхняя треть - ректосигмоидальный угол (голубой цвет); Б - средняя треть (желтый цвет); В - нижняя треть - промежностный и анальный отделы (синий цвет). 1 - парааортальные лимфатические узлы; 2 нижние брыжеечные лимфатические узлы; 3 - подаортальные лимфатические узлы (у бифуркации аорты); 4 - общие подвздошные лимфатические узлы; 5 - узел бифуркации общей подвздошной артерии; 6 - наружные подвздошные лимфатические узлы; 7 - внутренние подвздошные лимфатические узлы; 8 - паховые лимфатические узлы.
Схема путей оттока лимфы от различных участков прямой кишки. А - верхняя треть - ректосигмоидальный угол (голубой цвет); Б - средняя треть (желтый цвет); В - нижняя треть - промежностный и анальный отделы (синий цвет). 1 - парааортальные лимфатические узлы; 2 нижние брыжеечные лимфатические узлы; 3 - подаортальные лимфатические узлы (у бифуркации аорты); 4 - общие подвздошные лимфатические узлы; 5 - узел бифуркации общей подвздошной артерии; 6 - наружные подвздошные лимфатические узлы; 7 - внутренние подвздошные лимфатические узлы; 8 - паховые лимфатические узлы.
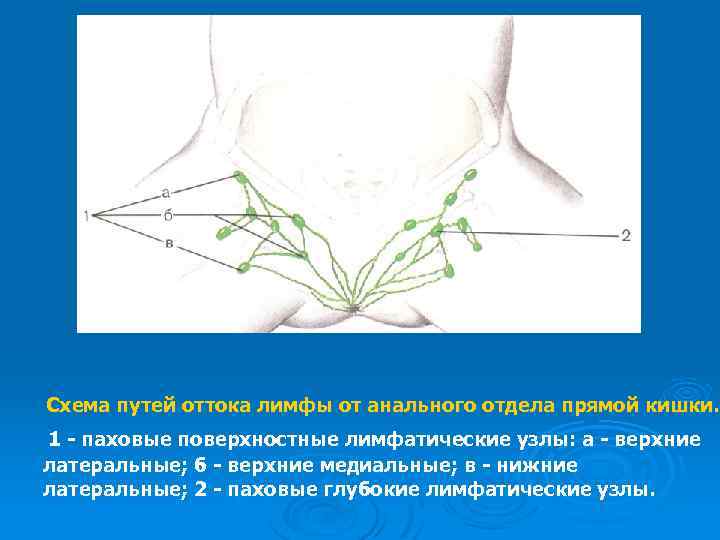 Схема путей оттока лимфы от анального отдела прямой кишки. 1 - паховые поверхностные лимфатические узлы: а - верхние латеральные; б - верхние медиальные; в - нижние латеральные; 2 - паховые глубокие лимфатические узлы.
Схема путей оттока лимфы от анального отдела прямой кишки. 1 - паховые поверхностные лимфатические узлы: а - верхние латеральные; б - верхние медиальные; в - нижние латеральные; 2 - паховые глубокие лимфатические узлы.
 Гематогенное метастазирование Ø печень, Ø легкие, Ø кости скелета, Ø в головной мозг.
Гематогенное метастазирование Ø печень, Ø легкие, Ø кости скелета, Ø в головной мозг.
 Классификация рака ободочной и прямой кишки по системе TNM (6 изд. ) Ø Ø Ø Ø Тх -недостаточно данных для оценки первичной опухоли Т 0 - первичная опухоль не определяется Тis - интраэпителиальная или с инвазией слизистой оболочки Т 1 - опухоль инфильтрирует стенку кишки до подслизистой Т 2 - опухоль инфильтрирует мышечный слой стенки кишки Т 3 - опухоль инфильтрирует субсерозу или ткань неперитонизированных участков ободочной и прямой кишки Т 4 - опухоль прорастает висцеральную брюшину или непосредственно распространяется на соседние органы и структуры
Классификация рака ободочной и прямой кишки по системе TNM (6 изд. ) Ø Ø Ø Ø Тх -недостаточно данных для оценки первичной опухоли Т 0 - первичная опухоль не определяется Тis - интраэпителиальная или с инвазией слизистой оболочки Т 1 - опухоль инфильтрирует стенку кишки до подслизистой Т 2 - опухоль инфильтрирует мышечный слой стенки кишки Т 3 - опухоль инфильтрирует субсерозу или ткань неперитонизированных участков ободочной и прямой кишки Т 4 - опухоль прорастает висцеральную брюшину или непосредственно распространяется на соседние органы и структуры
 Nх – недостаточно данных для оценки регионарных лимфатических узлов Ø N 0 - нет признаков метастатического поражения регионарных лимфатических узлов Ø N 1 - метастазы в 1 -3 регионарных лимфатических узлах Ø N 2 - метастазы в 4 и более регионарных лимфатических узлах Ø Мх - недостаточно данных для определения отдаленных метастазов Ø М 0 - нет признаков отдаленных метастазов Ø М 1 - имеются отдаленные метастазы Ø
Nх – недостаточно данных для оценки регионарных лимфатических узлов Ø N 0 - нет признаков метастатического поражения регионарных лимфатических узлов Ø N 1 - метастазы в 1 -3 регионарных лимфатических узлах Ø N 2 - метастазы в 4 и более регионарных лимфатических узлах Ø Мх - недостаточно данных для определения отдаленных метастазов Ø М 0 - нет признаков отдаленных метастазов Ø М 1 - имеются отдаленные метастазы Ø
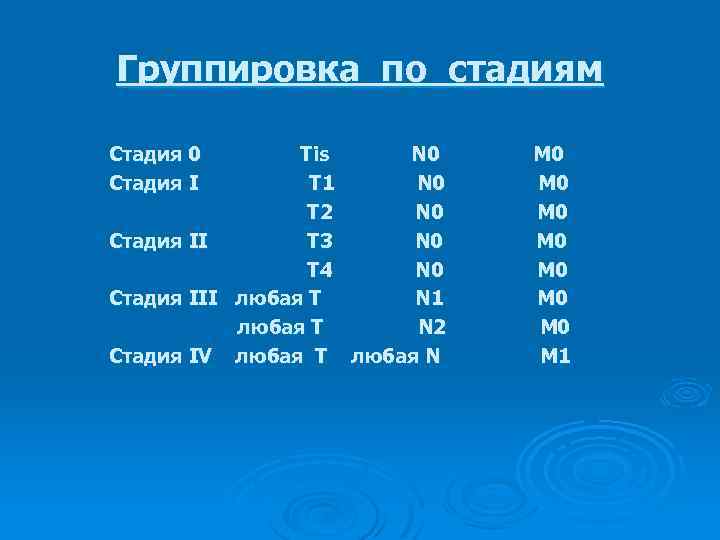 Группировка по стадиям Стадия 0 Стадия I Тis N 0 Т 1 N 0 Т 2 N 0 Стадия II Т 3 N 0 Т 4 N 0 Стадия III любая Т N 1 любая Т N 2 Стадия IV любая Т любая N М 0 М 0 М 1
Группировка по стадиям Стадия 0 Стадия I Тis N 0 Т 1 N 0 Т 2 N 0 Стадия II Т 3 N 0 Т 4 N 0 Стадия III любая Т N 1 любая Т N 2 Стадия IV любая Т любая N М 0 М 0 М 1
 Классификация рака анального канала по системе TNM (6 изд. ) Ø Ø Ø Ø Тх - недостаточно данных для оценки первичной опухоли Т 0 - первичная опухоль не определяется Тis - преинвазивная карцинома Т 1 - опухоль до 2 см в наибольшем измерении Т 2 - опухоль до 5 см в наибольшем измерении Т 3 - опухоль более 5 см в наибольшем измерении Т 4 - опухоль любого размера, прорастающая соседние органы: влагалище, мочеиспускательный канал, мочевой пузырь (вовлечение одного мышечного сфинктера не классифицируется как Т 4)
Классификация рака анального канала по системе TNM (6 изд. ) Ø Ø Ø Ø Тх - недостаточно данных для оценки первичной опухоли Т 0 - первичная опухоль не определяется Тis - преинвазивная карцинома Т 1 - опухоль до 2 см в наибольшем измерении Т 2 - опухоль до 5 см в наибольшем измерении Т 3 - опухоль более 5 см в наибольшем измерении Т 4 - опухоль любого размера, прорастающая соседние органы: влагалище, мочеиспускательный канал, мочевой пузырь (вовлечение одного мышечного сфинктера не классифицируется как Т 4)
 Ø Ø Ø Nх - недостаточно данных для оценки регионарных лимфатических узлов N 0 - нет признаков метастатического поражения регионарных лимфатических узлов (е) N 1 - метастазы в околопрямокишечных лимфатических узлах N 2 - метастазы в подвздошных или паховых лимфатических узлах (е) с одной стороны N 3 - метастазы в околопрямокишечных и паховых лимфатических узлах и/или в подвздошных и/или паховых с обеих сторон Мх - недостаточно данных для определения отдаленных метастазов Ø М 0 - нет признаков отдаленных метастазов Ø М 1 - имеются отдаленные метастазы Ø
Ø Ø Ø Nх - недостаточно данных для оценки регионарных лимфатических узлов N 0 - нет признаков метастатического поражения регионарных лимфатических узлов (е) N 1 - метастазы в околопрямокишечных лимфатических узлах N 2 - метастазы в подвздошных или паховых лимфатических узлах (е) с одной стороны N 3 - метастазы в околопрямокишечных и паховых лимфатических узлах и/или в подвздошных и/или паховых с обеих сторон Мх - недостаточно данных для определения отдаленных метастазов Ø М 0 - нет признаков отдаленных метастазов Ø М 1 - имеются отдаленные метастазы Ø
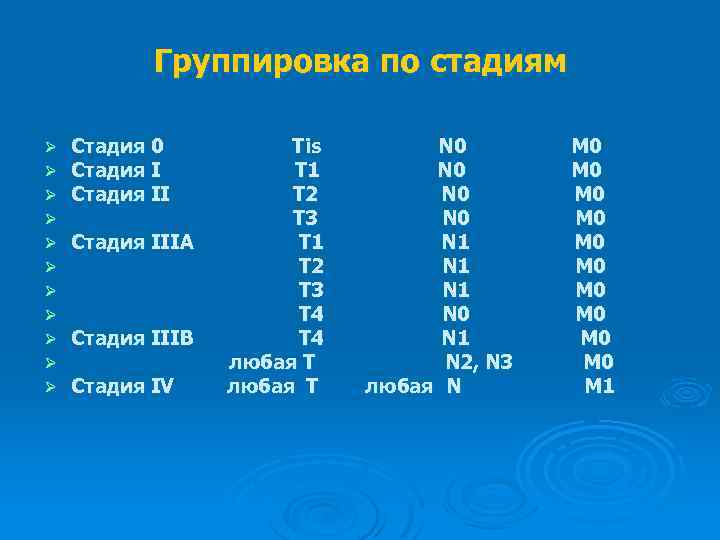 Группировка по стадиям Ø Ø Ø Стадия 0 Стадия IIIА Стадия IIIВ Стадия IV Тis Т 1 Т 2 Т 3 Т 4 любая Т N 0 N 0 N 1 N 1 N 0 N 1 N 2, N 3 любая N М 0 М 0 М 0 М 1
Группировка по стадиям Ø Ø Ø Стадия 0 Стадия IIIА Стадия IIIВ Стадия IV Тis Т 1 Т 2 Т 3 Т 4 любая Т N 0 N 0 N 1 N 1 N 0 N 1 N 2, N 3 любая N М 0 М 0 М 0 М 1
 Стадирование по классификации ТNМ и в модификации Дюкса (Dukes stage): ТNМ Стадия Тis N 0 М 0 0 Т 1 N 0 М 0 Распространеннос ть Модифицированн ая стадия Дюкс 5 -летняя общая выживаемость Саrcinoma in situ — ~ 100% I Слизистая или подслизистая А > 90 % Т 2 N 0 М 0 I Собственная мышечная оболочка В 1 85 % ТЗ N 0 М 0 II Брюшина/ ткани вокруг кишки В 2 70 - 80 % Т 4 N 0 М 0 II Перфорация или инвазия в другие органы ВЗ Т 2 N 1 -2 М 0 III Т 2, N 1: 1 -3/N 2: > 4 лимфоузла С 1 ТЗ N 1 -2 М 0 III ТЗ, N 1: 1 -3/N 2: > 4 лимфоузла С 2 Т 4 N 1 -2 М 0 III Т 4, N 1: 1 -3/N 2: 4 лимфоузла СЗ Любые IV Отдаленные D 25 - 60 % 5 -30 %
Стадирование по классификации ТNМ и в модификации Дюкса (Dukes stage): ТNМ Стадия Тis N 0 М 0 0 Т 1 N 0 М 0 Распространеннос ть Модифицированн ая стадия Дюкс 5 -летняя общая выживаемость Саrcinoma in situ — ~ 100% I Слизистая или подслизистая А > 90 % Т 2 N 0 М 0 I Собственная мышечная оболочка В 1 85 % ТЗ N 0 М 0 II Брюшина/ ткани вокруг кишки В 2 70 - 80 % Т 4 N 0 М 0 II Перфорация или инвазия в другие органы ВЗ Т 2 N 1 -2 М 0 III Т 2, N 1: 1 -3/N 2: > 4 лимфоузла С 1 ТЗ N 1 -2 М 0 III ТЗ, N 1: 1 -3/N 2: > 4 лимфоузла С 2 Т 4 N 1 -2 М 0 III Т 4, N 1: 1 -3/N 2: 4 лимфоузла СЗ Любые IV Отдаленные D 25 - 60 % 5 -30 %
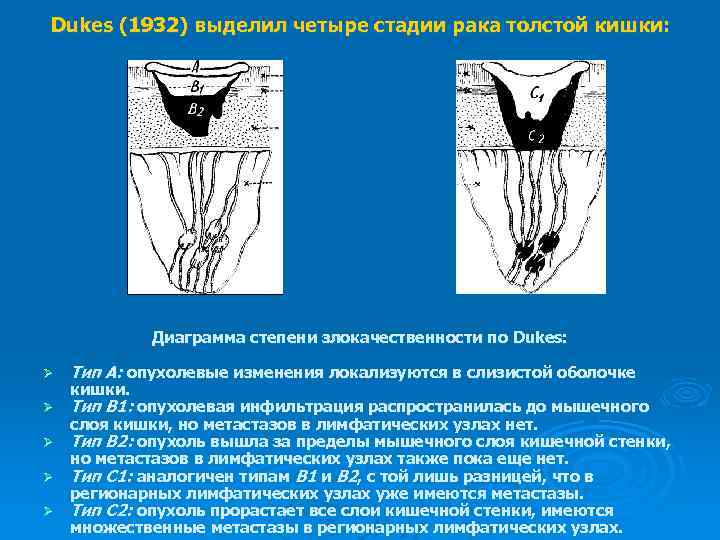 Dukes (1932) выделил четыре стадии рака толстой кишки: Диаграмма степени злокачественности по Dukes: Ø Тип А: опухолевые изменения локализуются в слизистой оболочке Ø Тип В 1: опухолевая инфильтрация распространилась до мышечного кишки. слоя кишки, но метастазов в лимфатических узлах нет. Ø Тип В 2: опухоль вышла за пределы мышечного слоя кишечной стенки, но метастазов в лимфатических узлах также пока еще нет. Ø Тип С 1: аналогичен типам В 1 и В 2, с той лишь разницей, что в регионарных лимфатических узлах уже имеются метастазы. Ø Тип С 2: опухоль прорастает все слои кишечной стенки, имеются множественные метастазы в регионарных лимфатических узлах.
Dukes (1932) выделил четыре стадии рака толстой кишки: Диаграмма степени злокачественности по Dukes: Ø Тип А: опухолевые изменения локализуются в слизистой оболочке Ø Тип В 1: опухолевая инфильтрация распространилась до мышечного кишки. слоя кишки, но метастазов в лимфатических узлах нет. Ø Тип В 2: опухоль вышла за пределы мышечного слоя кишечной стенки, но метастазов в лимфатических узлах также пока еще нет. Ø Тип С 1: аналогичен типам В 1 и В 2, с той лишь разницей, что в регионарных лимфатических узлах уже имеются метастазы. Ø Тип С 2: опухоль прорастает все слои кишечной стенки, имеются множественные метастазы в регионарных лимфатических узлах.
 3 фазы развития рака толстой кишки: Ø бессимптомная (10 лет), Ø бессимптомных узлов (несколько лет), Ø клинического проявления (длится несколько месяцев).
3 фазы развития рака толстой кишки: Ø бессимптомная (10 лет), Ø бессимптомных узлов (несколько лет), Ø клинического проявления (длится несколько месяцев).
 Клиническая картина рака толстой кишки Ø функциональные признаки без кишечных расстройств, Ø кишечные расстройства, Ø кишечная непроходимость, Ø патологические выделения из заднего прохода, Ø прощупываемая опухолъ.
Клиническая картина рака толстой кишки Ø функциональные признаки без кишечных расстройств, Ø кишечные расстройства, Ø кишечная непроходимость, Ø патологические выделения из заднего прохода, Ø прощупываемая опухолъ.
 Функциональные признаки без кишечных расстройств Ø Боли в животе Болевой синдром как начальный признак при раке правой половины в 3 раза чаще, чем при раке левой половины толстой кишки Ø Кишечный дискомфорт потеря аппетита, тошнота, отрыжка, неприятные ощущения во рту, однократная рвота, вздутие и чувство тяжести в эпигастральной области
Функциональные признаки без кишечных расстройств Ø Боли в животе Болевой синдром как начальный признак при раке правой половины в 3 раза чаще, чем при раке левой половины толстой кишки Ø Кишечный дискомфорт потеря аппетита, тошнота, отрыжка, неприятные ощущения во рту, однократная рвота, вздутие и чувство тяжести в эпигастральной области
 Кишечные расстройства Ø запоры, Ø поносы, Ø смена запоров поносами, Ø вздутие, Ø урчание в животе
Кишечные расстройства Ø запоры, Ø поносы, Ø смена запоров поносами, Ø вздутие, Ø урчание в животе
 Осложнения рака толстой кишки Ø кишечная непроходимость (у 1015% больных), Ø воспаление в окружающих опухоль тканях (у 12 -35% больных), Ø перфорацией кишечной стенки (у 2 -5% больных), Ø переход рака на соседние органы (у 15 -20% больных).
Осложнения рака толстой кишки Ø кишечная непроходимость (у 1015% больных), Ø воспаление в окружающих опухоль тканях (у 12 -35% больных), Ø перфорацией кишечной стенки (у 2 -5% больных), Ø переход рака на соседние органы (у 15 -20% больных).
 Клинические формы рака толстой кишки (А. М. Ганичкин, 1970) Ø Ø Ø Токсико-анемическая форма Энтероколитическая форма Диспептическая форма Обтурационная форма Псевдовоспалительная форма Опухолевая атипичная форма
Клинические формы рака толстой кишки (А. М. Ганичкин, 1970) Ø Ø Ø Токсико-анемическая форма Энтероколитическая форма Диспептическая форма Обтурационная форма Псевдовоспалительная форма Опухолевая атипичная форма
 Диагностика Пальцевое исследование (70%) Ø Ректороманоскопия с биопсией Ø Ирригоскопия Ø Колоноскопия Ø
Диагностика Пальцевое исследование (70%) Ø Ректороманоскопия с биопсией Ø Ирригоскопия Ø Колоноскопия Ø
 С 18. 00. РАК ОБОДОЧНОЙ КИШКИ С 18. 00. 1. ОБСЛЕДОВАНИЕ ДЛЯ ВСЕХ СТАДИЙ С 18. 00. 1. 1. Обязательные процедуры С 18. 00. 1. 1. 1. Пальцевое исследование анального канала, прямой кишки и перианальной области С 18. 00. 1. 1. 2. Пальпация паховых лимфатических узлов С 18. 00. 1. 1. 3. Ректороманоскопия (при определении опухолибиопсия) С 18. 00. 1. 1. 4. Фиброколоноскопия с биопсией С 18. 00. 1. 1. 5. Ирригоскопия С 18. 00. 1. 1. 6. Ультразвуковое исследование печени и забрюшинных лимфоузлов С 18. 00. 1. 1. 7. Ренгенологическое исследование органов грудной полости С 18. 00. 1. 1. 8. ЭКГ стандартная С 18. 00. 1. 1. 9. Консультация заведующего отделением С 18. 00. 1. 1. 10. Консилиум хирурга, радиолога, химиотерапевта С 18. 00. 1. 1. 11. Консультация терапевта С 18. 00. 1. 1. 12. Консультация анестезиолога С 18. 00. 1. 1. 13. Врачебный осмотр в приемном отделении (в случаях госпитализации)
С 18. 00. РАК ОБОДОЧНОЙ КИШКИ С 18. 00. 1. ОБСЛЕДОВАНИЕ ДЛЯ ВСЕХ СТАДИЙ С 18. 00. 1. 1. Обязательные процедуры С 18. 00. 1. 1. 1. Пальцевое исследование анального канала, прямой кишки и перианальной области С 18. 00. 1. 1. 2. Пальпация паховых лимфатических узлов С 18. 00. 1. 1. 3. Ректороманоскопия (при определении опухолибиопсия) С 18. 00. 1. 1. 4. Фиброколоноскопия с биопсией С 18. 00. 1. 1. 5. Ирригоскопия С 18. 00. 1. 1. 6. Ультразвуковое исследование печени и забрюшинных лимфоузлов С 18. 00. 1. 1. 7. Ренгенологическое исследование органов грудной полости С 18. 00. 1. 1. 8. ЭКГ стандартная С 18. 00. 1. 1. 9. Консультация заведующего отделением С 18. 00. 1. 1. 10. Консилиум хирурга, радиолога, химиотерапевта С 18. 00. 1. 1. 11. Консультация терапевта С 18. 00. 1. 1. 12. Консультация анестезиолога С 18. 00. 1. 1. 13. Врачебный осмотр в приемном отделении (в случаях госпитализации)
 С 18. 00. 1. 2. Дополнительные процедуры С 18. 00. 1. 2. 1. Консультация специалистов (уролога, гинеколога, эндокринолога и др. ) С 18. 00. 1. 2. 2. Компьютерная томография брюшной полости С 18. 00. 1. 3. Лабораторные исследования
С 18. 00. 1. 2. Дополнительные процедуры С 18. 00. 1. 2. 1. Консультация специалистов (уролога, гинеколога, эндокринолога и др. ) С 18. 00. 1. 2. 2. Компьютерная томография брюшной полости С 18. 00. 1. 3. Лабораторные исследования
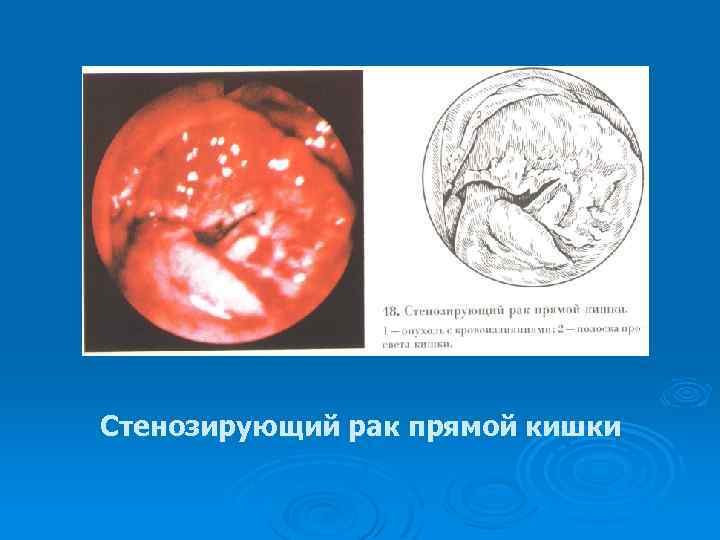 Стенозирующий рак прямой кишки
Стенозирующий рак прямой кишки
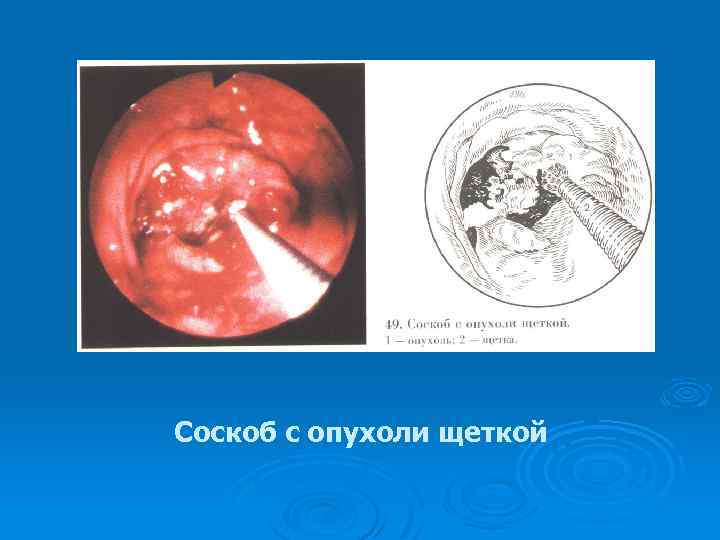 Соскоб с опухоли щеткой
Соскоб с опухоли щеткой
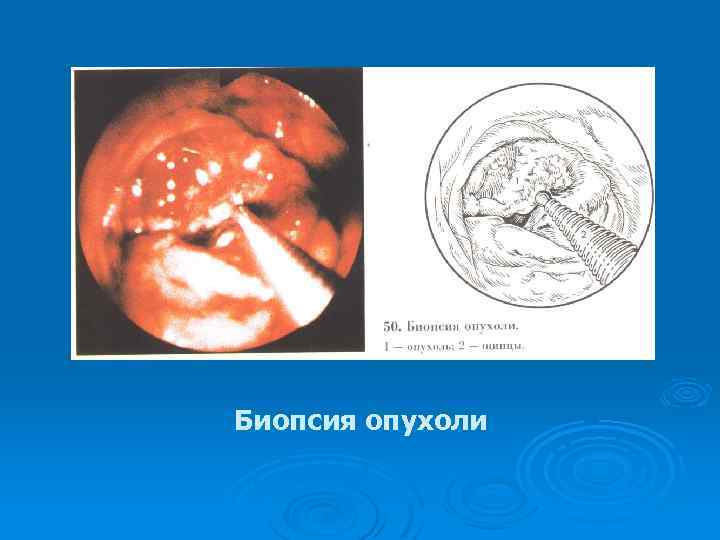 Биопсия опухоли
Биопсия опухоли
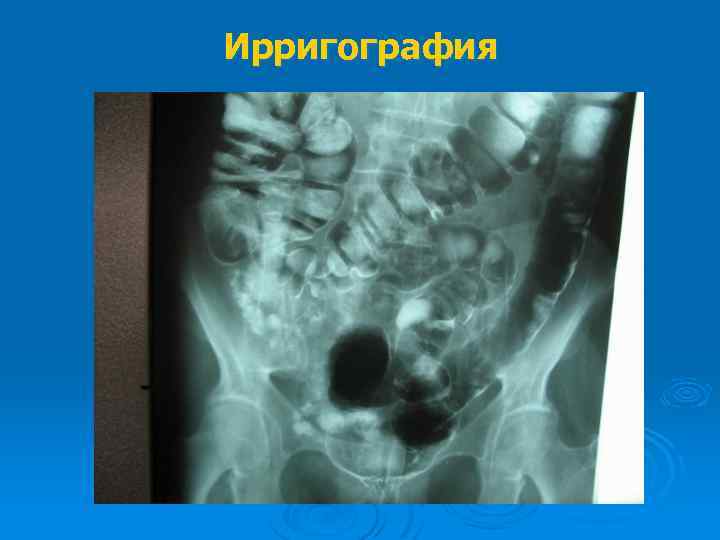 Ирригография
Ирригография
 Стадирование Ультразвуковая колоноскопия Обнаружение и оценка на основании известной эндоскопической семиотики различных новообразований толстой кишки, определение их характера, размеров, типа роста, получение фрагментов ткани для морфологического изучения. Ø Определение отсутствия или наличия опухолевой инвазии (в том числе оценка ее глубины) обнаруженного новообразования в толщу стенки толстой кишки. Ø Определение местной распространенности обнаруженных злокачественных новообразований, вовлечение в них прилежащих к пораженному участку кишечной стенки органов и тканей, регионарных околокишечных лимфатических узлов. Ø
Стадирование Ультразвуковая колоноскопия Обнаружение и оценка на основании известной эндоскопической семиотики различных новообразований толстой кишки, определение их характера, размеров, типа роста, получение фрагментов ткани для морфологического изучения. Ø Определение отсутствия или наличия опухолевой инвазии (в том числе оценка ее глубины) обнаруженного новообразования в толщу стенки толстой кишки. Ø Определение местной распространенности обнаруженных злокачественных новообразований, вовлечение в них прилежащих к пораженному участку кишечной стенки органов и тканей, регионарных околокишечных лимфатических узлов. Ø
 Чувствительность ультразвуковой колоноскопии в дифференциальной диагностике эпителиальных новообразований толстой кишки составила 96, 7%, специфичность - 82, 4%. Ø Точность ультразвуковой колоноскопии в определении наличия или отсутствия опухолевой инвазии в стенку толстой кишки составила 91, 6%. Ø Правильное определение глубины опухолевой инвазии стенки толстой кишки возможно в 75, 4%, при этом наилучшие результаты получены при установлении инвазии ТЗ и Т 4, где точность диагностики составила 88, 2 и 100%, соответственно. Ø
Чувствительность ультразвуковой колоноскопии в дифференциальной диагностике эпителиальных новообразований толстой кишки составила 96, 7%, специфичность - 82, 4%. Ø Точность ультразвуковой колоноскопии в определении наличия или отсутствия опухолевой инвазии в стенку толстой кишки составила 91, 6%. Ø Правильное определение глубины опухолевой инвазии стенки толстой кишки возможно в 75, 4%, при этом наилучшие результаты получены при установлении инвазии ТЗ и Т 4, где точность диагностики составила 88, 2 и 100%, соответственно. Ø
 Факторы, влияющие на точность ультразвуковой оценки глубины инвазии кишечной стенки опухолью При опухолях ободочной кишки показатель точности (81%) выше, чем при опухолях прямой кишки (72, 5%). Это объясняется тем, что параректальная клетчатка больше чем серозная оболочка подвержена воздействию воспалительной инфильтрации, которую при ультразвуковой колоноскопии можно ложно принять за опухолевую. Ø При опухолях размерами менее 2 и более 5 см показатель точности составил 85, 7 и 88, 2%, соответственно, в то время, как при размерах опухоли от 2 до 5 см - 66, 7%. Новообразования размером более 5 см чаще прорастают всю стенку кишки и за ее пределы, поэтому граница инвазии хорошо видна и точность диагностики высока. При опухоли до 2 см во время исследования на срез датчика попадает весь ее массив, она редко кровоточит и позволяет прицельно подвести аппарат, что также позволяет получать наилучшие результаты. Ø При опухолях блюдцеобразной формы показатель точности 100%, в то время как при полиповидной - 75% и инфильтративной - 68, 8%. Высокая точность при блюдцеобразных опухолях связана с тем, что происходит не только инфильтрация слоев кишечной стенки опухолью, но и их разрыв, обусловленный наличием язвенного дефекта. Ø
Факторы, влияющие на точность ультразвуковой оценки глубины инвазии кишечной стенки опухолью При опухолях ободочной кишки показатель точности (81%) выше, чем при опухолях прямой кишки (72, 5%). Это объясняется тем, что параректальная клетчатка больше чем серозная оболочка подвержена воздействию воспалительной инфильтрации, которую при ультразвуковой колоноскопии можно ложно принять за опухолевую. Ø При опухолях размерами менее 2 и более 5 см показатель точности составил 85, 7 и 88, 2%, соответственно, в то время, как при размерах опухоли от 2 до 5 см - 66, 7%. Новообразования размером более 5 см чаще прорастают всю стенку кишки и за ее пределы, поэтому граница инвазии хорошо видна и точность диагностики высока. При опухоли до 2 см во время исследования на срез датчика попадает весь ее массив, она редко кровоточит и позволяет прицельно подвести аппарат, что также позволяет получать наилучшие результаты. Ø При опухолях блюдцеобразной формы показатель точности 100%, в то время как при полиповидной - 75% и инфильтративной - 68, 8%. Высокая точность при блюдцеобразных опухолях связана с тем, что происходит не только инфильтрация слоев кишечной стенки опухолью, но и их разрыв, обусловленный наличием язвенного дефекта. Ø
 Визуализация регионарных лимфатических узлов при ультразвуковой колоноскопии - точность 80, 3%, - чувствительность - 90, 9%, - специфичность - 74, 4%. В оценке характера визуализированных околокишечных лимфатических узлов по ультразвуковым признакам точность диагностики составила 63, 6%. В этой связи, несмотря на высокую точность в определении метастатического характера поражения лимфатических узлов (81, 8%), говорить о высокой эффективности ультразвуковой колоноскопии в дифференциальной диагностике опухолевых и воспалительных изменений регионарных лимфатических узлов не представляется возможным.
Визуализация регионарных лимфатических узлов при ультразвуковой колоноскопии - точность 80, 3%, - чувствительность - 90, 9%, - специфичность - 74, 4%. В оценке характера визуализированных околокишечных лимфатических узлов по ультразвуковым признакам точность диагностики составила 63, 6%. В этой связи, несмотря на высокую точность в определении метастатического характера поражения лимфатических узлов (81, 8%), говорить о высокой эффективности ультразвуковой колоноскопии в дифференциальной диагностике опухолевых и воспалительных изменений регионарных лимфатических узлов не представляется возможным.
 Разрешающая возможность ультразвуковой колоноскопии и других инструментальных методов диагностики Критерии оценки Колоноскоп Ирригоскоп ия ия Точность ниже на 9, 5% ниже на 6, 7% Чувствител ьность ниже на 8, 2% ниже на 20, 0% Специфичн ость ниже на 11, 8% ниже на 10, 0%
Разрешающая возможность ультразвуковой колоноскопии и других инструментальных методов диагностики Критерии оценки Колоноскоп Ирригоскоп ия ия Точность ниже на 9, 5% ниже на 6, 7% Чувствител ьность ниже на 8, 2% ниже на 20, 0% Специфичн ость ниже на 11, 8% ниже на 10, 0%
 Компьютерная томография Ø Ядерно-магнитная резонансная томография Возможность КТ Ø ЯМР не может оценивать определить наличие опухолевую прорастания опухоли инфильтрацию стенки через стенку кишки прямой кишки с высокой весьма ограничена по точностью, но подобно КТ сравнению с ЭУЗИ. дает хорошее Действительно, представление о хорошая вовлеченности чувствительность КТ (82 окружающих тканей и -89%) при этом структур и в 81 -82% соседствует с низкой предсказывает специфичностью (51%). поражение метастазами регионарных лимфоузлов.
Компьютерная томография Ø Ядерно-магнитная резонансная томография Возможность КТ Ø ЯМР не может оценивать определить наличие опухолевую прорастания опухоли инфильтрацию стенки через стенку кишки прямой кишки с высокой весьма ограничена по точностью, но подобно КТ сравнению с ЭУЗИ. дает хорошее Действительно, представление о хорошая вовлеченности чувствительность КТ (82 окружающих тканей и -89%) при этом структур и в 81 -82% соседствует с низкой предсказывает специфичностью (51%). поражение метастазами регионарных лимфоузлов.
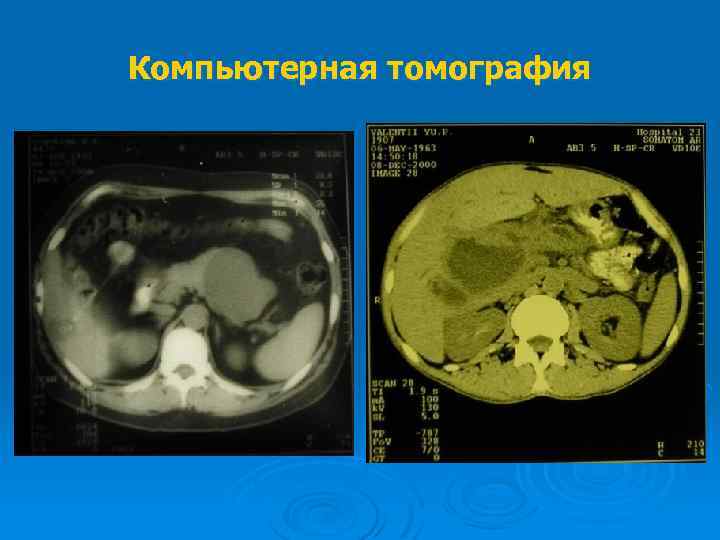 Компьютерная томография
Компьютерная томография
 Оценки критерия N Определенная информация может быть получена при: Ø Ø Ø ЭУЗИ, КТ таза ЯМР. Более специфичные исследования: лимфангиография, внутритканевая лимфосцинтиграфия (с Тс 99 m трехсернистой сурьмой коллоидного раствора, вводимого на глубину 4 см в каждую седалищно-прямокишечную ямку), Ø прямокишечная лимфосцинтиграфия (с Тс 99 m - коллоидного раствора сернистого олова, вводимого в подслизистый слой прямой кишки с использованием иглы Gabriala через ректоскоп) Ø иммунолимфосцинтиграфия прямой кишки с моноклональными антителами использовались с целью повышения точности диагностики поражения лимфоузлов метастазами в дооперациронной дифференциальной диагностики между стадиями Dukes'а В и С или N 0 и N 1. Ø Ø
Оценки критерия N Определенная информация может быть получена при: Ø Ø Ø ЭУЗИ, КТ таза ЯМР. Более специфичные исследования: лимфангиография, внутритканевая лимфосцинтиграфия (с Тс 99 m трехсернистой сурьмой коллоидного раствора, вводимого на глубину 4 см в каждую седалищно-прямокишечную ямку), Ø прямокишечная лимфосцинтиграфия (с Тс 99 m - коллоидного раствора сернистого олова, вводимого в подслизистый слой прямой кишки с использованием иглы Gabriala через ректоскоп) Ø иммунолимфосцинтиграфия прямой кишки с моноклональными антителами использовались с целью повышения точности диагностики поражения лимфоузлов метастазами в дооперациронной дифференциальной диагностики между стадиями Dukes'а В и С или N 0 и N 1. Ø Ø
 Оценка критерия М Ø клиническое обследование, Ø эхотомография печени (УЗИ), Ø КТ, Ø ЯМР, Ø дооперационная чрезкожная игловая биопсия
Оценка критерия М Ø клиническое обследование, Ø эхотомография печени (УЗИ), Ø КТ, Ø ЯМР, Ø дооперационная чрезкожная игловая биопсия
 Компьютерная томография органов брюшной полости
Компьютерная томография органов брюшной полости
 Определение биологической агрессивности опухолей РЭА, Ø степень дифференцировки, Ø индексы клеточной пролиферации, Ø плоидность ДНК. Ø
Определение биологической агрессивности опухолей РЭА, Ø степень дифференцировки, Ø индексы клеточной пролиферации, Ø плоидность ДНК. Ø
 Раковоэмбриональный антиген (РЭА) Имеется четкая корреляция между дооперационным уровнем РЭА, дифференцировкой и стадией заболевания. Повышение РЭА: Ø при высокодифференцированных опухолях - в 61% случаев, Ø при низкодифференцированных - у 3, 5% опухолей. Ø стадия I - РЭА 1, 63 ng/ml, Ø стадия II -РЭА 7, 22 ng/ml, Ø стадия Ш - РЭА 13, 93 ng/ml Ø стадия IV - РЭА 47, 76 ng/ml
Раковоэмбриональный антиген (РЭА) Имеется четкая корреляция между дооперационным уровнем РЭА, дифференцировкой и стадией заболевания. Повышение РЭА: Ø при высокодифференцированных опухолях - в 61% случаев, Ø при низкодифференцированных - у 3, 5% опухолей. Ø стадия I - РЭА 1, 63 ng/ml, Ø стадия II -РЭА 7, 22 ng/ml, Ø стадия Ш - РЭА 13, 93 ng/ml Ø стадия IV - РЭА 47, 76 ng/ml
 Степень дифференцировки опухолевых клеток (G) Ø Ø G 1 - высокодифференцированные опухоли (20%), G 2 - опухоли средней дифференцировки (50%), G 3 - низкодифференцированные опухоли (30%) , G 4 - недифференцированные опухоли. Метастазы в лимфоузлах: Ø Ø Ø G 1 – 25% G 2 – 50% G 3 -4 - 80%
Степень дифференцировки опухолевых клеток (G) Ø Ø G 1 - высокодифференцированные опухоли (20%), G 2 - опухоли средней дифференцировки (50%), G 3 - низкодифференцированные опухоли (30%) , G 4 - недифференцированные опухоли. Метастазы в лимфоузлах: Ø Ø Ø G 1 – 25% G 2 – 50% G 3 -4 - 80%
 Кинетические индексы клеточной пролиферации Индекс меченного тимидина (TLI) соответствует числу клеток, меченных «puls labelling» с [Н 3]тимидин, измеряющим процент клеток при активном синтезе ДНК. Коррелирует с безрецидивной выживаемостью и длительностью выживаемости после появления рецидива. Ø Индекс первичной зависимости альфа - ДНК полимераз пробы (РДР-LI), позволяющий лучше определять тканевую пролиферацию - как установлено фракцию истинноциклических клеток в общей популяции (фактор роста GF). РДР -LI показала выраженную корреляцию со стадиями Dukes'а, более четко при С стадии (стадия III по ТNМ), чем при А стадии (стадия I, ТNМ) и В (стадия II ТNМ) (р < 0, 05). Ø
Кинетические индексы клеточной пролиферации Индекс меченного тимидина (TLI) соответствует числу клеток, меченных «puls labelling» с [Н 3]тимидин, измеряющим процент клеток при активном синтезе ДНК. Коррелирует с безрецидивной выживаемостью и длительностью выживаемости после появления рецидива. Ø Индекс первичной зависимости альфа - ДНК полимераз пробы (РДР-LI), позволяющий лучше определять тканевую пролиферацию - как установлено фракцию истинноциклических клеток в общей популяции (фактор роста GF). РДР -LI показала выраженную корреляцию со стадиями Dukes'а, более четко при С стадии (стадия III по ТNМ), чем при А стадии (стадия I, ТNМ) и В (стадия II ТNМ) (р < 0, 05). Ø
 Плоидность ДНК при исследовании диплоидности ДНК в опухолях статистически хуже (р = 0, 017) прогноз был при недиплоидной ДНК, по сравнению с диплоидной ДНК, но наиболее плохой прогноз при наличии в опухолевых клетках тетраплоидной ДНК. Ø при определении прогностической связи образцов - ДНК было установлено, что пятилетняя выживаемость больных колоректальным раком, имеющих Dukes', С 1 (поражено метастазами от 1 до 4 лимфоузлов согласно модификации классификации Dukes' Gastrointestinal Tumor Study Group), имеющих диплоидную ДНК в опухолевых клетках, составила 74%, а недиплоидную ДНК - лишь 44% (р = 0, 047). Ø
Плоидность ДНК при исследовании диплоидности ДНК в опухолях статистически хуже (р = 0, 017) прогноз был при недиплоидной ДНК, по сравнению с диплоидной ДНК, но наиболее плохой прогноз при наличии в опухолевых клетках тетраплоидной ДНК. Ø при определении прогностической связи образцов - ДНК было установлено, что пятилетняя выживаемость больных колоректальным раком, имеющих Dukes', С 1 (поражено метастазами от 1 до 4 лимфоузлов согласно модификации классификации Dukes' Gastrointestinal Tumor Study Group), имеющих диплоидную ДНК в опухолевых клетках, составила 74%, а недиплоидную ДНК - лишь 44% (р = 0, 047). Ø
 Схема диагностики колоректалыюго рака Развитые страны Пальцевое обследование Ø Ректосигмоидоскопия Ø Ирригоскопия с двойным контрастированием и/или колоноскопия Ø Гистологическое исследование Ø Развивающиеся страны Пальцевое обследование Ø Ректосигмоидоскопия Ø Ирригоскопия с двойным контрастированием и/или колоноскопия Ø Гистологическое исследование Ø
Схема диагностики колоректалыюго рака Развитые страны Пальцевое обследование Ø Ректосигмоидоскопия Ø Ирригоскопия с двойным контрастированием и/или колоноскопия Ø Гистологическое исследование Ø Развивающиеся страны Пальцевое обследование Ø Ректосигмоидоскопия Ø Ирригоскопия с двойным контрастированием и/или колоноскопия Ø Гистологическое исследование Ø
 Схема стадирования колоректального рака Развитые страны Ø Ø Ø Ø Трансректальное ЭУЗИ КТ или ЯМР В/в урография УЗИ печени КТ печени или ЯМР Ro-графия грудной клетки Тест РЭА Развивающиеся страны Ø Ø УЗИ печени Ro-графия грудной клетки
Схема стадирования колоректального рака Развитые страны Ø Ø Ø Ø Трансректальное ЭУЗИ КТ или ЯМР В/в урография УЗИ печени КТ печени или ЯМР Ro-графия грудной клетки Тест РЭА Развивающиеся страны Ø Ø УЗИ печени Ro-графия грудной клетки
 Лечение рака толстой кишки Предоперационная подготовка толстой кишки перорально фортранс, растворенный в 3 л воды; Ø ортоградное промывание кишечника путем введения 6— 8 л изотонического раствора через зонд, установленный в двенадцатиперстной кишке; Ø бесшлаковая диета и очистительные клизмы. Ø
Лечение рака толстой кишки Предоперационная подготовка толстой кишки перорально фортранс, растворенный в 3 л воды; Ø ортоградное промывание кишечника путем введения 6— 8 л изотонического раствора через зонд, установленный в двенадцатиперстной кишке; Ø бесшлаковая диета и очистительные клизмы. Ø
 Выбор метода хирургического вмешательства зависит Ø от локализации опухоли, Ø наличия или отсутствия осложнений и метастазов, Ø общего состояния больного
Выбор метода хирургического вмешательства зависит Ø от локализации опухоли, Ø наличия или отсутствия осложнений и метастазов, Ø общего состояния больного
 Правосторонняя гемиколэктомия
Правосторонняя гемиколэктомия
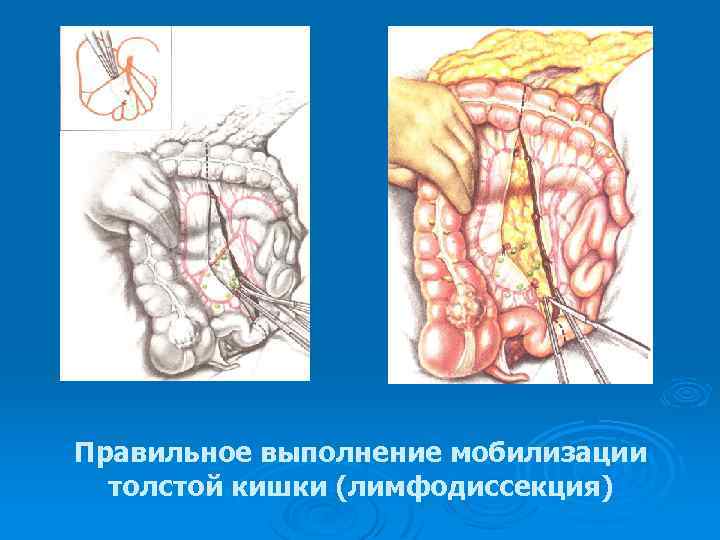 Правильное выполнение мобилизации толстой кишки (лимфодиссекция)
Правильное выполнение мобилизации толстой кишки (лимфодиссекция)
 Левосторонняя гемиколэктомия
Левосторонняя гемиколэктомия
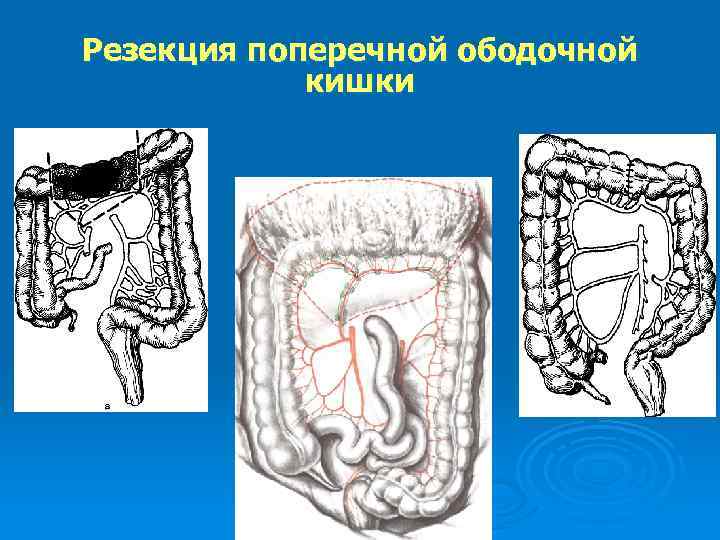 Резекция поперечной ободочной кишки
Резекция поперечной ободочной кишки
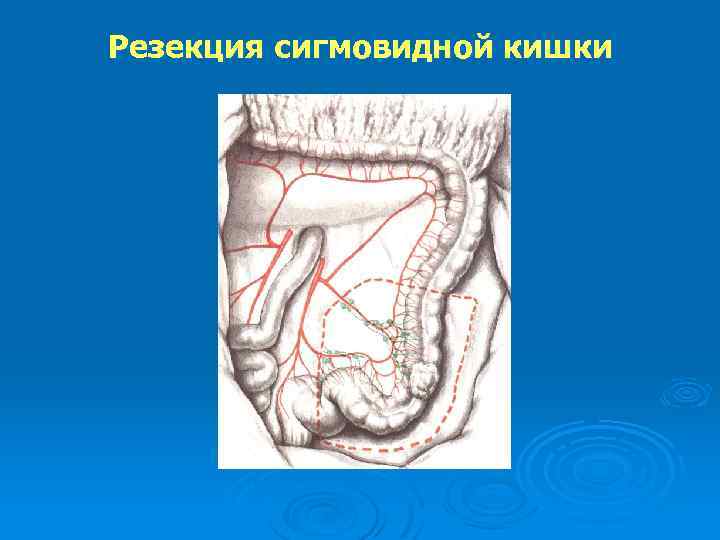 Резекция сигмовидной кишки
Резекция сигмовидной кишки
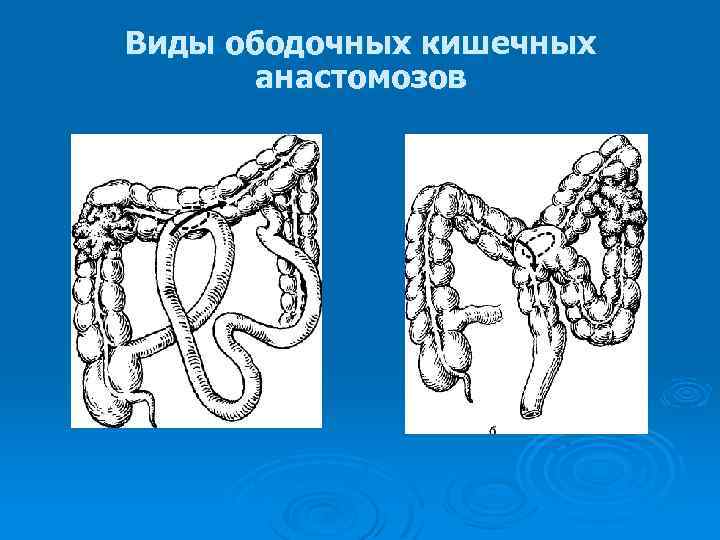 Виды ободочных кишечных анастомозов
Виды ободочных кишечных анастомозов
 Лечебная тактика при колоректальном раке определена: на Всероссийской конференции «Современные возможности хирургического, комбинированного и комплексного лечения колоректального рака» (Пермь, 2003 г. ) Ø На 1 -м Всероссийском съезде колопроктологов (Самара, 2003 г. ) Ø
Лечебная тактика при колоректальном раке определена: на Всероссийской конференции «Современные возможности хирургического, комбинированного и комплексного лечения колоректального рака» (Пермь, 2003 г. ) Ø На 1 -м Всероссийском съезде колопроктологов (Самара, 2003 г. ) Ø
 Современные принципы хирургического лечения колоректального рака удаление пораженной части кишки в едином блоке с клетчаткой и сосудисто-нервным пучком, с высокой перевязкой сосудов и отступлением на 10 см выше опухоли и на 5 см ниже опухоли для ободочной кишки и не менее 2 см для прямой кишки; Ø тотальная мезоректумэктомия (удаление прямой кишки с окружающей клетчаткой, сосудисто-нервными структурами и лимфатическими узлами, ограниченными висцеральной фасцией) должна быть выполнена острым путем; Ø для обеспечения латеральной границы резекции при раке прямой кишки необходимо удаление мезоректум без повреждения вегетативных нервов таза (гипогастральных, сакральных нервов и тазового сплетения). Удаление опухолей средне - и нижнеампулярного отдела прямой кишки должно сопровождаться тотальной мезоректумэктомией, тогда как при раке верхнеампулярного отдела достаточно ограничиться резекцией мезоректум на протяжении 5 см дистальнее опухоли; Ø при локализованном раке дистальных отделов прямой кишки (Т 1 -2 N 0 M 0), расположенном выше 2 см от зубчатой линии, допустимо выполнение сфинктеросохраняющих вмешательств при обязательном морфологическом контроле краев резекции. Ø
Современные принципы хирургического лечения колоректального рака удаление пораженной части кишки в едином блоке с клетчаткой и сосудисто-нервным пучком, с высокой перевязкой сосудов и отступлением на 10 см выше опухоли и на 5 см ниже опухоли для ободочной кишки и не менее 2 см для прямой кишки; Ø тотальная мезоректумэктомия (удаление прямой кишки с окружающей клетчаткой, сосудисто-нервными структурами и лимфатическими узлами, ограниченными висцеральной фасцией) должна быть выполнена острым путем; Ø для обеспечения латеральной границы резекции при раке прямой кишки необходимо удаление мезоректум без повреждения вегетативных нервов таза (гипогастральных, сакральных нервов и тазового сплетения). Удаление опухолей средне - и нижнеампулярного отдела прямой кишки должно сопровождаться тотальной мезоректумэктомией, тогда как при раке верхнеампулярного отдела достаточно ограничиться резекцией мезоректум на протяжении 5 см дистальнее опухоли; Ø при локализованном раке дистальных отделов прямой кишки (Т 1 -2 N 0 M 0), расположенном выше 2 см от зубчатой линии, допустимо выполнение сфинктеросохраняющих вмешательств при обязательном морфологическом контроле краев резекции. Ø
 При раке прямой кишки наиболее часто используют: брюшно-промежностную экстирпацию прямой кишки, Ø переднюю резекцию прямой кишки, Ø брюшно-анальную резекцию прямой кишки с низведением сигмовидной кишки, Ø обструктивную резекцию (операцию Гартмана). Ø
При раке прямой кишки наиболее часто используют: брюшно-промежностную экстирпацию прямой кишки, Ø переднюю резекцию прямой кишки, Ø брюшно-анальную резекцию прямой кишки с низведением сигмовидной кишки, Ø обструктивную резекцию (операцию Гартмана). Ø
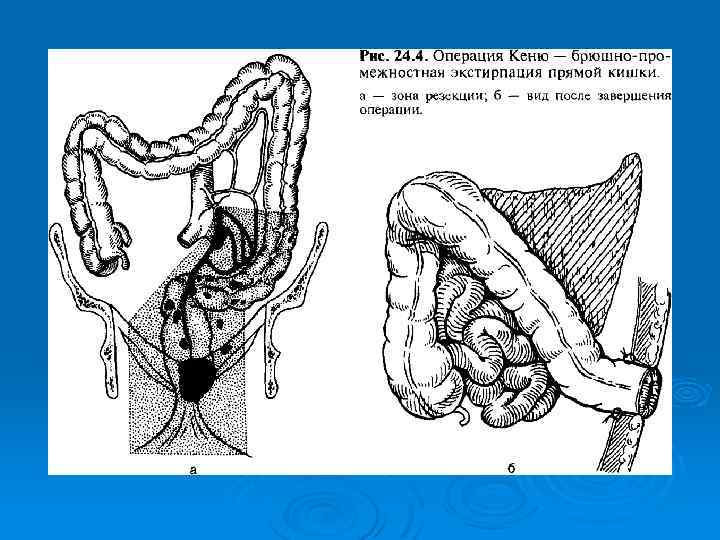
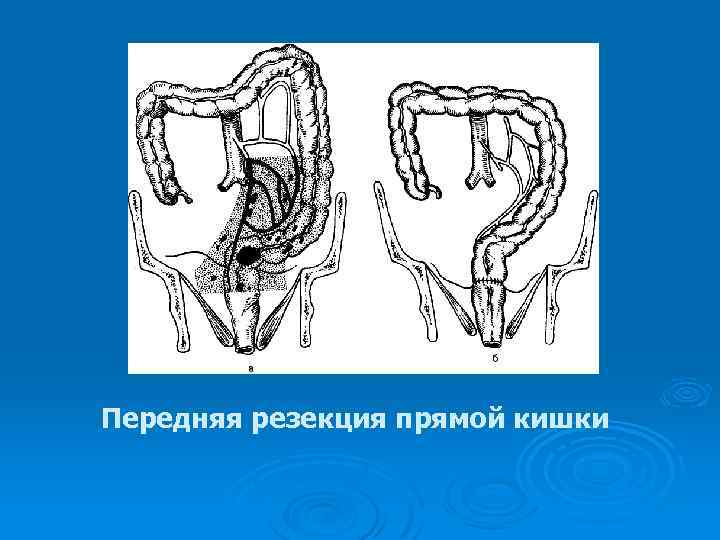 Передняя резекция прямой кишки
Передняя резекция прямой кишки
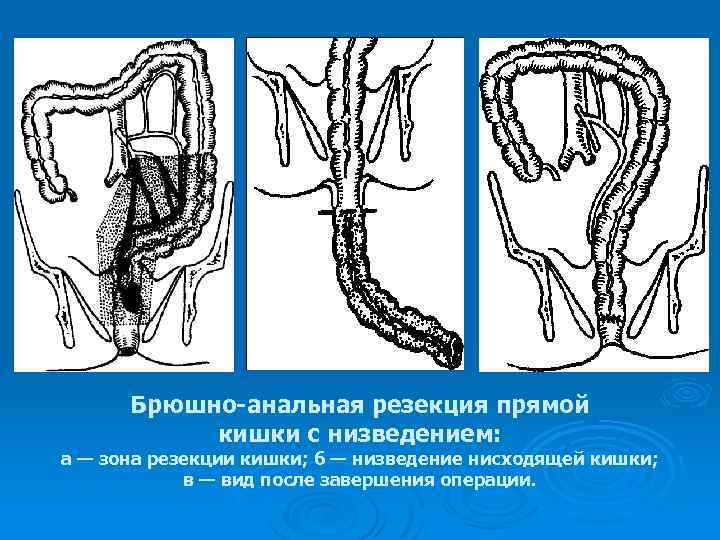 Брюшно-анальная резекция прямой кишки с низведением: а — зона резекции кишки; б — низведение нисходящей кишки; в — вид после завершения операции.
Брюшно-анальная резекция прямой кишки с низведением: а — зона резекции кишки; б — низведение нисходящей кишки; в — вид после завершения операции.
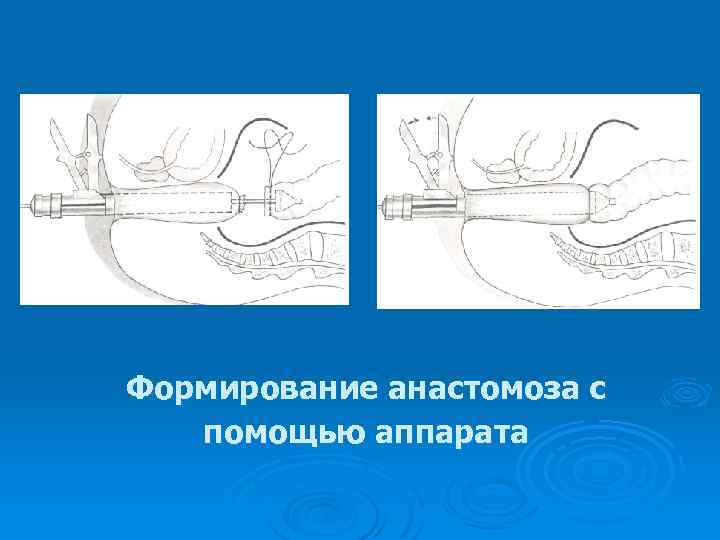 Формирование анастомоза с помощью аппарата
Формирование анастомоза с помощью аппарата
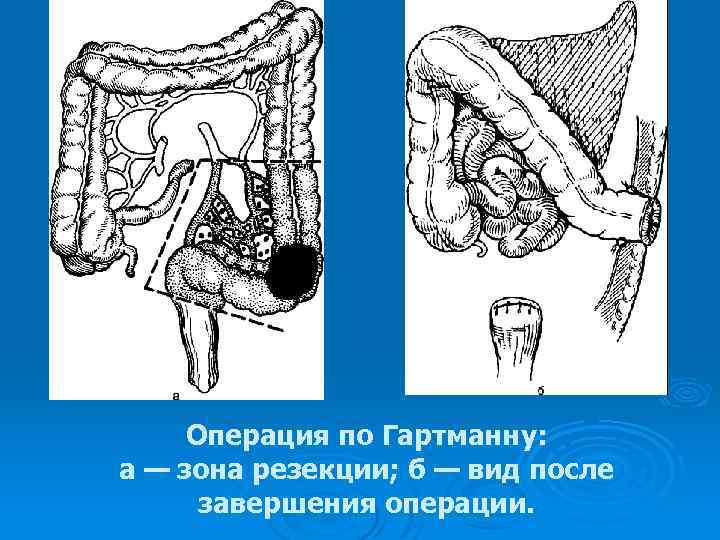 Операция по Гартманну: а — зона резекции; б — вид после завершения операции.
Операция по Гартманну: а — зона резекции; б — вид после завершения операции.
 «Синдром низкой передней резекции» частые (до 6 раз в сутки) акты дефекации, многомоментное, длительное и неполное опорожнение кишечника, Ø императивные позывы на дефекацию, Ø различной степени выраженности явления анальной инконтиненции. Ø Ø
«Синдром низкой передней резекции» частые (до 6 раз в сутки) акты дефекации, многомоментное, длительное и неполное опорожнение кишечника, Ø императивные позывы на дефекацию, Ø различной степени выраженности явления анальной инконтиненции. Ø Ø
 Общий вид толстокишечного J-резервуара
Общий вид толстокишечного J-резервуара
 Аорто-подвздошная лимфаденэктомия направлена на предотвращение метастазирования по восходящему пути Производится высокая перевязка нижней брыжеечной артерии (у места отхождения от аорты), после чего отсепаровывается париетальная фасция с клетчаткой и лимфатическими сосудами от аорты, нижней полой вены и общих подвздошных сосудов. Ø Вопрос о способах удаления латеральных лимфатических коллекторов до сих пор является не решенным. Исторически сложившиеся школы западных и японских хирургов придерживаются двух противоположных точек зрения: если в Японии расширенная лимфаденэктомия с латеральной лимфодиссекцией активно практикуется вот уже несколько десятилетий, то в Европе и США от нее практически отказались. Ø
Аорто-подвздошная лимфаденэктомия направлена на предотвращение метастазирования по восходящему пути Производится высокая перевязка нижней брыжеечной артерии (у места отхождения от аорты), после чего отсепаровывается париетальная фасция с клетчаткой и лимфатическими сосудами от аорты, нижней полой вены и общих подвздошных сосудов. Ø Вопрос о способах удаления латеральных лимфатических коллекторов до сих пор является не решенным. Исторически сложившиеся школы западных и японских хирургов придерживаются двух противоположных точек зрения: если в Японии расширенная лимфаденэктомия с латеральной лимфодиссекцией активно практикуется вот уже несколько десятилетий, то в Европе и США от нее практически отказались. Ø
 Варианты лимфаденэктомии (T. Takahashi) Ø ограниченная лимфаденэктомия, Ø стандартная лимфаденэктомия, Ø расширенная лимфаденэктомия.
Варианты лимфаденэктомии (T. Takahashi) Ø ограниченная лимфаденэктомия, Ø стандартная лимфаденэктомия, Ø расширенная лимфаденэктомия.
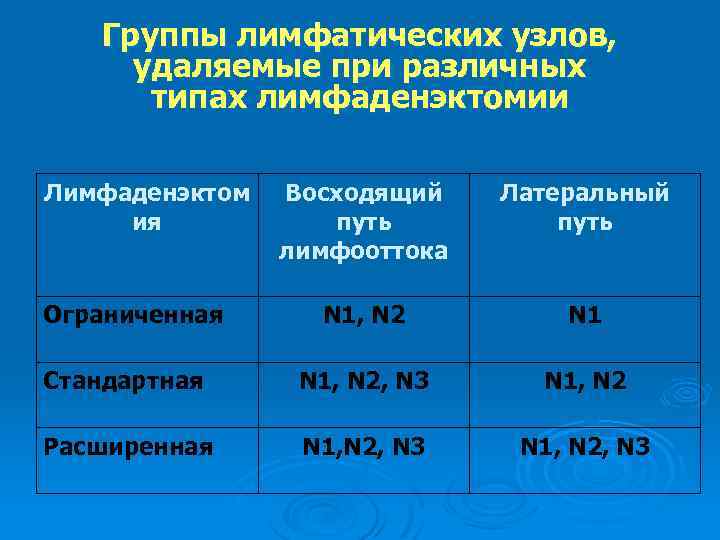 Группы лимфатических узлов, удаляемые при различных типах лимфаденэктомии Лимфаденэктом ия Восходящий путь лимфооттока Латеральный путь N 1, N 2 N 1 Стандартная N 1, N 2, N 3 N 1, N 2 Расширенная N 1, N 2, N 3 Ограниченная
Группы лимфатических узлов, удаляемые при различных типах лимфаденэктомии Лимфаденэктом ия Восходящий путь лимфооттока Латеральный путь N 1, N 2 N 1 Стандартная N 1, N 2, N 3 N 1, N 2 Расширенная N 1, N 2, N 3 Ограниченная
 По мнению японских хирургов: ограниченная лимфаденэктомия показана при ранних стадиях рака прямой кишки, Ø стандартная - при распространенном раке верхних, Ø расширенная - при распространенном раке нижних отделов. Ø Расширенная лимфаденэктомия включает в себя: - тотальную мезоректумэктомию, - высокую перевязку нижней брыжеечной артерии, - а также латеральную лимфодиссекцию, при которой удаляются узлы по ходу подвздошных сосудов и в запирательном пространстве.
По мнению японских хирургов: ограниченная лимфаденэктомия показана при ранних стадиях рака прямой кишки, Ø стандартная - при распространенном раке верхних, Ø расширенная - при распространенном раке нижних отделов. Ø Расширенная лимфаденэктомия включает в себя: - тотальную мезоректумэктомию, - высокую перевязку нижней брыжеечной артерии, - а также латеральную лимфодиссекцию, при которой удаляются узлы по ходу подвздошных сосудов и в запирательном пространстве.
 Пятилетняя выживаемость у больных с раком Dukes В Автор, год Стандартная Расширенная лимфаденэктом ия (%) Takahashi T. et al. , 19741983 84, 1 80, 6 Коуаmа Y. еt аl, . 1984 62, 7 83, 2 Takahashi T. et al. , 19841988 100 87 74 88 - 79 Hojo K. et al. , 1989 Moriya. , 1997
Пятилетняя выживаемость у больных с раком Dukes В Автор, год Стандартная Расширенная лимфаденэктом ия (%) Takahashi T. et al. , 19741983 84, 1 80, 6 Коуаmа Y. еt аl, . 1984 62, 7 83, 2 Takahashi T. et al. , 19841988 100 87 74 88 - 79 Hojo K. et al. , 1989 Moriya. , 1997
 Пятилетняя выживаемость у больных с раком Dukes С Автор, год Стандартная лимфаденэктомия (%) Расширенная лимфаденэктомия (%) Takahashi T. et al. , 1974 -1983 64, 7 51, 1 Коуаmа Y. еt аl, . 1984 30, 8 52, 5 Takahashi T. et al. , 1984 -1988 70, 5 55, 3 Hojo K. et al. , 1989 43 61 Moriya. , 1997 - 55
Пятилетняя выживаемость у больных с раком Dukes С Автор, год Стандартная лимфаденэктомия (%) Расширенная лимфаденэктомия (%) Takahashi T. et al. , 1974 -1983 64, 7 51, 1 Коуаmа Y. еt аl, . 1984 30, 8 52, 5 Takahashi T. et al. , 1984 -1988 70, 5 55, 3 Hojo K. et al. , 1989 43 61 Moriya. , 1997 - 55
 Западные хирурги считают, что эффект расширенной лимфаденэктомии весьма сомнителен и редко выполняют ее, в то же время японские хирурги полагают, что расширенная лимодиссекция высокоэффективна и должна рутинно выполняться при операциях по поводу рака прямой кишки
Западные хирурги считают, что эффект расширенной лимфаденэктомии весьма сомнителен и редко выполняют ее, в то же время японские хирурги полагают, что расширенная лимодиссекция высокоэффективна и должна рутинно выполняться при операциях по поводу рака прямой кишки
 Общепризнано, что основными недостатками расширенной лимфаденэктомии являются нарушения мочевой и половой функций. Мочевая дисфункция возникает на протяжении первого года: у 8% пациентов после обычной сфинктеросохраняющей резекции, Ø у 10% - после стандартной брюшнопромежностной экстирпации прямой кишки, Ø у 45% и 40% пациентов соответственно после дополнения этих операций расширенной лимфаденэктомией. Ø
Общепризнано, что основными недостатками расширенной лимфаденэктомии являются нарушения мочевой и половой функций. Мочевая дисфункция возникает на протяжении первого года: у 8% пациентов после обычной сфинктеросохраняющей резекции, Ø у 10% - после стандартной брюшнопромежностной экстирпации прямой кишки, Ø у 45% и 40% пациентов соответственно после дополнения этих операций расширенной лимфаденэктомией. Ø
 В последних работах описывается техника сохранения автономных нервов (nerve-sparing surgery) с целью предотвращения развития мочевой и половой дисфункций. Предлагается несколько вариантов этой методики: Ø Ø Ø полное сохранение автономных нервов, полное сохранение тазовых нервов, частичное сохранение тазовых нервов. По мнению Y. Moriya и соавт. , полное сохранение автономных нервов целесообразно применять при распространенной опухоли, соответствующей Т 2, полное сохранение тазовых нервов - при ТЗ, а частичное сохранение тазовых нервов - при ТЗ с поражением регионарных лимфатических узлов.
В последних работах описывается техника сохранения автономных нервов (nerve-sparing surgery) с целью предотвращения развития мочевой и половой дисфункций. Предлагается несколько вариантов этой методики: Ø Ø Ø полное сохранение автономных нервов, полное сохранение тазовых нервов, частичное сохранение тазовых нервов. По мнению Y. Moriya и соавт. , полное сохранение автономных нервов целесообразно применять при распространенной опухоли, соответствующей Т 2, полное сохранение тазовых нервов - при ТЗ, а частичное сохранение тазовых нервов - при ТЗ с поражением регионарных лимфатических узлов.
 Ø Ø Несмотря на кажущуюся целесообразность выполнения латеральной лимфодиссекции у больных нижнеампулярным раком, такая операция не получила широкого распространения. Причин подобного негативного отношения несколько. Противоречивые данные о показателях 5 -летней выживаемости после выполнения такого рода вмешательств. Однако в ряде случаев (особенно при включении в исследование только больных с распространенностью опухоли Dukes В и Dukes С) было показано увеличение показателей 5 -летней выживаемости по сравнению со стандартной лимфаденэктомией. Следует отметить, что все исследования носили ретроспективный характер. Усложнение и удлинение времени вмешательства наряду с увеличением кровопотери и объема перелитой крови, без увеличения госпитальной летальности по сравнению со стандартной хирургией. Высокая частота мочеполовых расстройств, которые отмечаются всеми авторами. Наконец, для западных хирургов - трудности выполнения латеральной лимфодиссекции у пациентов с избыточной массой тела среди лиц европеоидной расы.
Ø Ø Несмотря на кажущуюся целесообразность выполнения латеральной лимфодиссекции у больных нижнеампулярным раком, такая операция не получила широкого распространения. Причин подобного негативного отношения несколько. Противоречивые данные о показателях 5 -летней выживаемости после выполнения такого рода вмешательств. Однако в ряде случаев (особенно при включении в исследование только больных с распространенностью опухоли Dukes В и Dukes С) было показано увеличение показателей 5 -летней выживаемости по сравнению со стандартной лимфаденэктомией. Следует отметить, что все исследования носили ретроспективный характер. Усложнение и удлинение времени вмешательства наряду с увеличением кровопотери и объема перелитой крови, без увеличения госпитальной летальности по сравнению со стандартной хирургией. Высокая частота мочеполовых расстройств, которые отмечаются всеми авторами. Наконец, для западных хирургов - трудности выполнения латеральной лимфодиссекции у пациентов с избыточной массой тела среди лиц европеоидной расы.
 Комбинированные методы лечения Применяются при раке дистальных отделов прямой кишки III стадии, т. е. при прорастании опухолью всех слоев стенки кишки и врастании в жировую клетчатку, а также при метастатическом поражении регионарных лимфатических узлов
Комбинированные методы лечения Применяются при раке дистальных отделов прямой кишки III стадии, т. е. при прорастании опухолью всех слоев стенки кишки и врастании в жировую клетчатку, а также при метастатическом поражении регионарных лимфатических узлов
 В 1995 г. опубликованы окончательные результаты крупного многоцентрового рандомизированного исследования SCCSG (Stockholm Colorectal Cancer Study Group) по использованию предоперационной ЛТ коротким курсом при лечении операбельного рака прямой кишки. Исследование проводилось в период с 1980 по 1987 гг. и включало 849 больных. В группе, получавшей комбинированное лечение, в предоперационном периоде проводилась ЛТ в суммарной очаговой дозе (СОД) 25 Гр за 5 -7 фракций, после чего в течение недели осуществлялось оперативное вмешательство. Зона облучения включала анус, прямую кишку, промежность, зоны регионарного метастазирования, паховые лимфатические узлы, область запирательных отверстий и паравертебральные лимфатические узлы.
В 1995 г. опубликованы окончательные результаты крупного многоцентрового рандомизированного исследования SCCSG (Stockholm Colorectal Cancer Study Group) по использованию предоперационной ЛТ коротким курсом при лечении операбельного рака прямой кишки. Исследование проводилось в период с 1980 по 1987 гг. и включало 849 больных. В группе, получавшей комбинированное лечение, в предоперационном периоде проводилась ЛТ в суммарной очаговой дозе (СОД) 25 Гр за 5 -7 фракций, после чего в течение недели осуществлялось оперативное вмешательство. Зона облучения включала анус, прямую кишку, промежность, зоны регионарного метастазирования, паховые лимфатические узлы, область запирательных отверстий и паравертебральные лимфатические узлы.
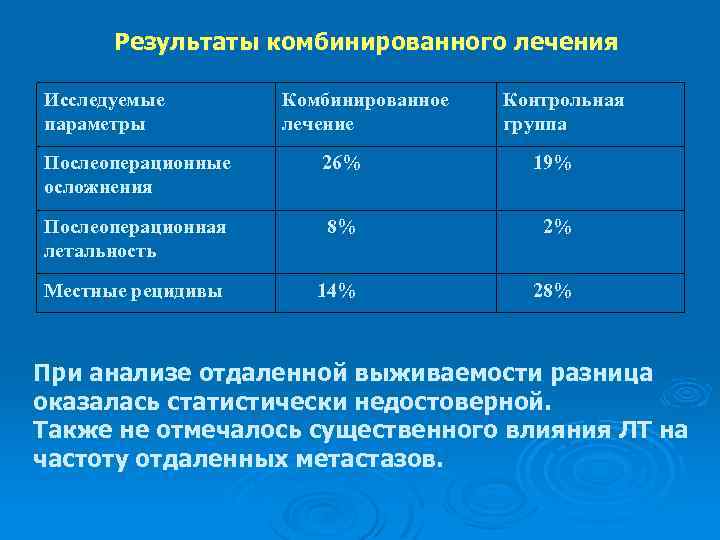 Результаты комбинированного лечения Исследуемые параметры Комбинированное лечение Контрольная группа Послеоперационные осложнения 26% 19% Послеоперационная летальность 8% 2% Местные рецидивы 14% 28% При анализе отдаленной выживаемости разница оказалась статистически недостоверной. Также не отмечалось существенного влияния ЛТ на частоту отдаленных метастазов.
Результаты комбинированного лечения Исследуемые параметры Комбинированное лечение Контрольная группа Послеоперационные осложнения 26% 19% Послеоперационная летальность 8% 2% Местные рецидивы 14% 28% При анализе отдаленной выживаемости разница оказалась статистически недостоверной. Также не отмечалось существенного влияния ЛТ на частоту отдаленных метастазов.
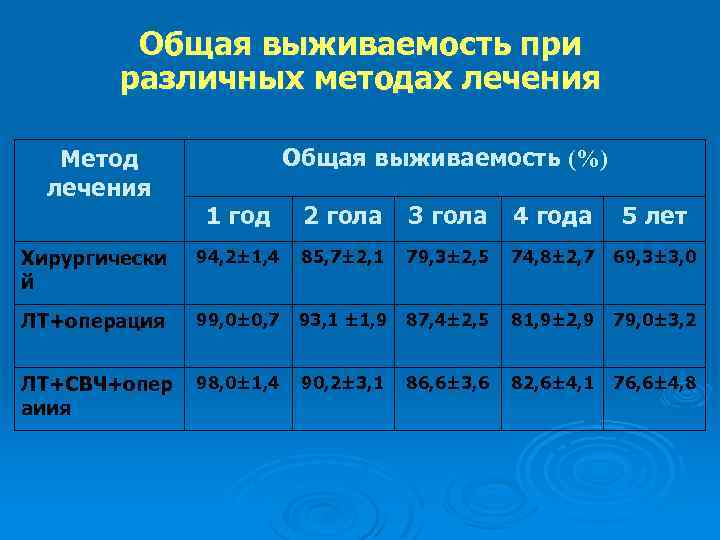 Общая выживаемость при различных методах лечения Метод лечения Общая выживаемость (%) 1 год 2 гола 3 гола 4 года 5 лет Хирургически й 94, 2± 1, 4 85, 7± 2, 1 79, 3± 2, 5 74, 8± 2, 7 69, 3± 3, 0 ЛТ+операция 99, 0± 0, 7 93, 1 ± 1, 9 87, 4± 2, 5 81, 9± 2, 9 79, 0± 3, 2 ЛТ+СВЧ+опер аиия 98, 0± 1, 4 90, 2± 3, 1 86, 6± 3, 6 82, 6± 4, 1 76, 6± 4, 8
Общая выживаемость при различных методах лечения Метод лечения Общая выживаемость (%) 1 год 2 гола 3 гола 4 года 5 лет Хирургически й 94, 2± 1, 4 85, 7± 2, 1 79, 3± 2, 5 74, 8± 2, 7 69, 3± 3, 0 ЛТ+операция 99, 0± 0, 7 93, 1 ± 1, 9 87, 4± 2, 5 81, 9± 2, 9 79, 0± 3, 2 ЛТ+СВЧ+опер аиия 98, 0± 1, 4 90, 2± 3, 1 86, 6± 3, 6 82, 6± 4, 1 76, 6± 4, 8
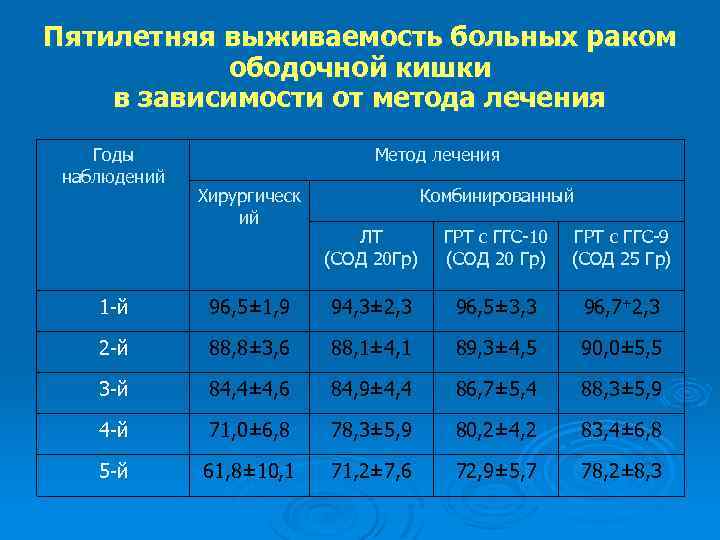 Пятилетняя выживаемость больных раком ободочной кишки в зависимости от метода лечения Годы наблюдений Метод лечения Хирургическ ий Комбинированный ЛТ (СОД 20 Гр) ГРТ с ГГС-10 (СОД 20 Гр) ГРТ с ГГС-9 (СОД 25 Гр) 1 -й 96, 5± 1, 9 94, 3± 2, 3 96, 5± 3, 3 96, 7+2, 3 2 -й 88, 8± 3, 6 88, 1± 4, 1 89, 3± 4, 5 90, 0± 5, 5 3 -й 84, 4± 4, 6 84, 9± 4, 4 86, 7± 5, 4 88, 3± 5, 9 4 -й 71, 0± 6, 8 78, 3± 5, 9 80, 2± 4, 2 83, 4± 6, 8 5 -й 61, 8± 10, 1 71, 2± 7, 6 72, 9± 5, 7 78, 2± 8, 3
Пятилетняя выживаемость больных раком ободочной кишки в зависимости от метода лечения Годы наблюдений Метод лечения Хирургическ ий Комбинированный ЛТ (СОД 20 Гр) ГРТ с ГГС-10 (СОД 20 Гр) ГРТ с ГГС-9 (СОД 25 Гр) 1 -й 96, 5± 1, 9 94, 3± 2, 3 96, 5± 3, 3 96, 7+2, 3 2 -й 88, 8± 3, 6 88, 1± 4, 1 89, 3± 4, 5 90, 0± 5, 5 3 -й 84, 4± 4, 6 84, 9± 4, 4 86, 7± 5, 4 88, 3± 5, 9 4 -й 71, 0± 6, 8 78, 3± 5, 9 80, 2± 4, 2 83, 4± 6, 8 5 -й 61, 8± 10, 1 71, 2± 7, 6 72, 9± 5, 7 78, 2± 8, 3
 Основные потенциальные взаимодействия между ионизирующей радиацией и цитостатиками Изменения в выживаемости клеток Задержка репарации (сублетальное или потенциально летальное повреждение) Цитокинетический эффект Селективная токсичность, зависящая от фазы клеточного цикла Селективная токсичность для гипоксических клеток Задержка клеточной репопуляции Уменьшение опухолевой массы и увеличение оксигенации Увеличение апоптоза Пространственное взаимодействие Фармакомодуляция внутриклеточной концентрации цитостатика ионизирующей радиацией
Основные потенциальные взаимодействия между ионизирующей радиацией и цитостатиками Изменения в выживаемости клеток Задержка репарации (сублетальное или потенциально летальное повреждение) Цитокинетический эффект Селективная токсичность, зависящая от фазы клеточного цикла Селективная токсичность для гипоксических клеток Задержка клеточной репопуляции Уменьшение опухолевой массы и увеличение оксигенации Увеличение апоптоза Пространственное взаимодействие Фармакомодуляция внутриклеточной концентрации цитостатика ионизирующей радиацией
 Схема клиники Мейо внутривенные инъекции 5 -ФУ и лейковорина в низкой дозе 5 дней с интервалами в 45 нед. Новые цитостатики Ø таксаны, Ø гемцитабин, Ø ингибиторы топомеразы I, Ø тирапазамин, Ø ЮФТ и др.
Схема клиники Мейо внутривенные инъекции 5 -ФУ и лейковорина в низкой дозе 5 дней с интервалами в 45 нед. Новые цитостатики Ø таксаны, Ø гемцитабин, Ø ингибиторы топомеразы I, Ø тирапазамин, Ø ЮФТ и др.
 Недостатки послеоперационного химиолучевого лечения: Ø Ø происходит задержка начала адъювантного лечения; уменьшается радиочувствительность резидуальных опухолевых клеток, ибо до операции оксигенация значительно лучше и клетки рака прямой кишки имеют, примерно, в 3 раза большую чувствительность к радиации, чем гипоксические клетки из-за развития фиброза после хирургического вмешательства; увеличивается токсичность облучения из-за фиксации петель тонкой кишки в тазу; такой вариант лечения не может способствовать увеличению резектабельности локально нерезектабельных опухолей. Лечение фактически разделяется на две фазы: совместное использование химиотерапии (чаще всего фторурацила) и ионизирующей радиации для оптимизации локального контроля путем суммирования эффекта этих методов и затем добавочные курсы химиотерапии с целью уменьшения рецидивирования.
Недостатки послеоперационного химиолучевого лечения: Ø Ø происходит задержка начала адъювантного лечения; уменьшается радиочувствительность резидуальных опухолевых клеток, ибо до операции оксигенация значительно лучше и клетки рака прямой кишки имеют, примерно, в 3 раза большую чувствительность к радиации, чем гипоксические клетки из-за развития фиброза после хирургического вмешательства; увеличивается токсичность облучения из-за фиксации петель тонкой кишки в тазу; такой вариант лечения не может способствовать увеличению резектабельности локально нерезектабельных опухолей. Лечение фактически разделяется на две фазы: совместное использование химиотерапии (чаще всего фторурацила) и ионизирующей радиации для оптимизации локального контроля путем суммирования эффекта этих методов и затем добавочные курсы химиотерапии с целью уменьшения рецидивирования.
 Преимущества послеоперационного химиолучевого лечения Ø Ø Ø Ø Благодаря хирургическому вмешательству достоверно определяются степень распространенности опухолевого процесса и прогностические факторы: глубина инвазии опухоли в стенку кишки с или без распространения на соседние структуры, промежностная инвазия, число пораженных лимфатических узлов, наличие или отсутствие опухолевых клеток в хирургических краях раны, выраженность сосудистой и лимфатической инвазии, степень гистологической дифференцировки плоидности опухолевых клеток.
Преимущества послеоперационного химиолучевого лечения Ø Ø Ø Ø Благодаря хирургическому вмешательству достоверно определяются степень распространенности опухолевого процесса и прогностические факторы: глубина инвазии опухоли в стенку кишки с или без распространения на соседние структуры, промежностная инвазия, число пораженных лимфатических узлов, наличие или отсутствие опухолевых клеток в хирургических краях раны, выраженность сосудистой и лимфатической инвазии, степень гистологической дифференцировки плоидности опухолевых клеток.
 Преимущества предоперационного химиолучевого лечения Ø Ø Ø сокращается размер опухоли и улучшается резектабельность; падает жизнеспособность опухолевых клеток, что, в частности, способствует уменьшению имплантационного метастазирования; существенно снижается токсичность для желудочно-кишечного тракта ввиду отсутствия выраженной фиксации петель тонкой кишки в тазу.
Преимущества предоперационного химиолучевого лечения Ø Ø Ø сокращается размер опухоли и улучшается резектабельность; падает жизнеспособность опухолевых клеток, что, в частности, способствует уменьшению имплантационного метастазирования; существенно снижается токсичность для желудочно-кишечного тракта ввиду отсутствия выраженной фиксации петель тонкой кишки в тазу.
 Недостатки предоперационного химиолучевого лечения Ø Ø происходит задержка в выполнении хирургического вмешательства на 4— 8 нед. ; добавочные технические трудности во время операции; проблемы, связанные с заживлением послеоперационной раны; неточность в стадировании опухолевого процесса.
Недостатки предоперационного химиолучевого лечения Ø Ø происходит задержка в выполнении хирургического вмешательства на 4— 8 нед. ; добавочные технические трудности во время операции; проблемы, связанные с заживлением послеоперационной раны; неточность в стадировании опухолевого процесса.
 Радикальной называется операция, если при значительном местно—регионарном распространении рака толстой кишки удается удалить все опухолевые очаги. Ø Ø Циторедуктивные операции заключаются в удалении первичного или рецидивного опухолевого очага и одновременном полном или частичном удалении отдаленных метастазов. Можно различать 4 вида циторедуктивных операций. 100% визуальная опухолевая редукция - когда удаляется путем типичной или комбинированной операции первичный опухолевый очаг и удаляются все отдаленные метастазы. Частичная опухолевая циторедукция - когда удаляется первичный опухолевый очаг и производится частичное удаление отдаленных метастазов. Частичная опухолевая циторедукция - когда удаляется первичный опухолевый очаг, а отдаленные метастазы не удаляются. Удаление отдаленных метастазов в различные сроки после ранее выполненной радикальной или циторедуктивной операции.
Радикальной называется операция, если при значительном местно—регионарном распространении рака толстой кишки удается удалить все опухолевые очаги. Ø Ø Циторедуктивные операции заключаются в удалении первичного или рецидивного опухолевого очага и одновременном полном или частичном удалении отдаленных метастазов. Можно различать 4 вида циторедуктивных операций. 100% визуальная опухолевая редукция - когда удаляется путем типичной или комбинированной операции первичный опухолевый очаг и удаляются все отдаленные метастазы. Частичная опухолевая циторедукция - когда удаляется первичный опухолевый очаг и производится частичное удаление отдаленных метастазов. Частичная опухолевая циторедукция - когда удаляется первичный опухолевый очаг, а отдаленные метастазы не удаляются. Удаление отдаленных метастазов в различные сроки после ранее выполненной радикальной или циторедуктивной операции.
 Противопоказания к выполнению циторедуктивных операций тяжелое общее состояние больного, Ø наличие множественных метастазов сразу в нескольких органах, Ø наличие асцита и тотального канцероматоза брюшины. Ø
Противопоказания к выполнению циторедуктивных операций тяжелое общее состояние больного, Ø наличие множественных метастазов сразу в нескольких органах, Ø наличие асцита и тотального канцероматоза брюшины. Ø
 Ø При циторедуктивной операции с удалением всех визуально определяемых отдаленных метастазов 3 - и 5 -летняя выживаемость выше, чем при удалении только первичного опухолевого очага и составляет соответственно 26% и 15%. При симптоматических операциях результаты значительно хуже. Ø Одновременное удаление первичного опухолевого очага и метастазов в печени позволяет обеспечить до 1427% 5 -летней выживаемости. Резекция печени по поводу отдаленных метастазов, возникших в различные сроки после радикальных операций, также приносят достаточно удовлетворительный лечебный эффект - от 27% до 43% 5 -летней выживаемости. Важно подчеркнуть, что летальность при этих операциях не превышает 9%.
Ø При циторедуктивной операции с удалением всех визуально определяемых отдаленных метастазов 3 - и 5 -летняя выживаемость выше, чем при удалении только первичного опухолевого очага и составляет соответственно 26% и 15%. При симптоматических операциях результаты значительно хуже. Ø Одновременное удаление первичного опухолевого очага и метастазов в печени позволяет обеспечить до 1427% 5 -летней выживаемости. Резекция печени по поводу отдаленных метастазов, возникших в различные сроки после радикальных операций, также приносят достаточно удовлетворительный лечебный эффект - от 27% до 43% 5 -летней выживаемости. Важно подчеркнуть, что летальность при этих операциях не превышает 9%.
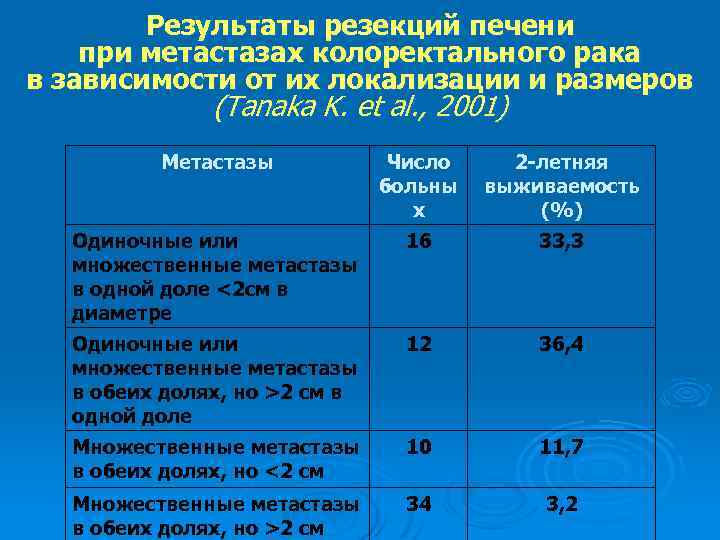 Результаты резекций печени при метастазах колоректального рака в зависимости от их локализации и размеров (Tanaka K. et al. , 2001) Метастазы Число больны х 2 -летняя выживаемость (%) Одиночные или множественные метастазы в одной доле <2 см в диаметре 16 33, 3 Одиночные или множественные метастазы в обеих долях, но >2 см в одной доле 12 36, 4 Множественные метастазы в обеих долях, но <2 см 10 11, 7 Множественные метастазы в обеих долях, но >2 см 34 3, 2
Результаты резекций печени при метастазах колоректального рака в зависимости от их локализации и размеров (Tanaka K. et al. , 2001) Метастазы Число больны х 2 -летняя выживаемость (%) Одиночные или множественные метастазы в одной доле <2 см в диаметре 16 33, 3 Одиночные или множественные метастазы в обеих долях, но >2 см в одной доле 12 36, 4 Множественные метастазы в обеих долях, но <2 см 10 11, 7 Множественные метастазы в обеих долях, но >2 см 34 3, 2
 Повторные операции при вновь возникших метастазах также могут быть рекомендованы и во многих случаях существенно продлевают жизнь пациентам. Ø Противопоказанием к выполнению таких операций признается одновременное наличие множественных метастазов в лимфатических узлах брюшной полости. Ø Результаты хирургического лечения одиночных метастазов рака прямой кишки в легкие также вполне удовлетворительны.
Повторные операции при вновь возникших метастазах также могут быть рекомендованы и во многих случаях существенно продлевают жизнь пациентам. Ø Противопоказанием к выполнению таких операций признается одновременное наличие множественных метастазов в лимфатических узлах брюшной полости. Ø Результаты хирургического лечения одиночных метастазов рака прямой кишки в легкие также вполне удовлетворительны.
 Прогноз Пятилетняя выживаемость после радикального хирургического лечения при раке прямой кишки составляет около 40— 50%. Ø Ø При использовании одного хирургического метода 5 -летняя выживаемость больных раком прямой кишки, по данным французских авторов, составила при I стадии - 85%, II стадии - 60%, III стадии - 40%. Ø Ø Ø По мнению онкологов из клиники Мауо, эти показатели находятся в пределах I стадия 85 - 90%, II стадия - 70 -75%, III стадия - 35 -40%, а при IV стадии ниже 5%.
Прогноз Пятилетняя выживаемость после радикального хирургического лечения при раке прямой кишки составляет около 40— 50%. Ø Ø При использовании одного хирургического метода 5 -летняя выживаемость больных раком прямой кишки, по данным французских авторов, составила при I стадии - 85%, II стадии - 60%, III стадии - 40%. Ø Ø Ø По мнению онкологов из клиники Мауо, эти показатели находятся в пределах I стадия 85 - 90%, II стадия - 70 -75%, III стадия - 35 -40%, а при IV стадии ниже 5%.
 Благодарю за внимание !
Благодарю за внимание !


