ген связь орг соед.ppt
- Количество слайдов: 31

Санкт-Петербургский государственный университет Генетическая связь между основными классами органических соединений профессор СПб. ГУ, доктор химических наук Карцова Анна Алексеевна Санкт-Петербург 2011

Алиса (в Стране Чудес Чеширскому коту): – Скажите, а куда мне отсюда идти? Чеширский кот: – Это зависит от того, куда Вы хотите придти? 2
От простого – к сложному Состав Строение Свойства 3
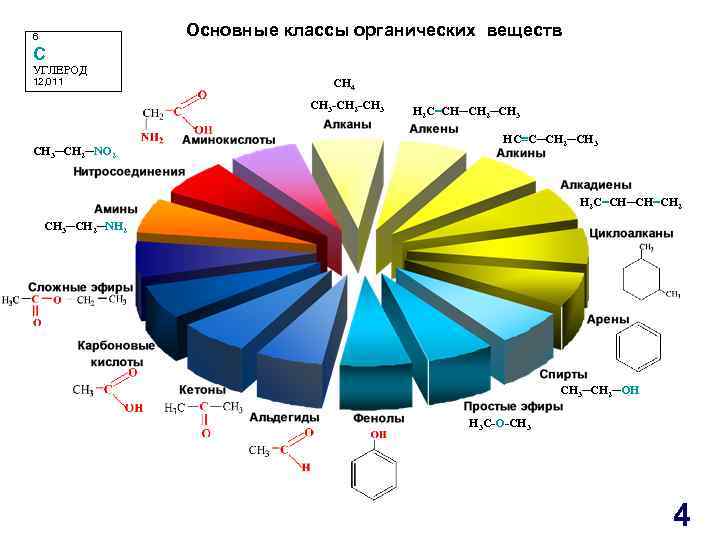
Основные классы органических веществ 6 C УГЛЕРОД 12, 011 CH 4 CH 3 -CH 2 -CH 3─CH 2─NO 2 H 2 C=CH─CH 2─CH 3 HC≡C─CH 2─CH 3 H 2 C=CH─CH=CH 2 CH 3─CH 2─NH 2 CH 3─CH 2─OH H 3 C-O-CH 3 4

Стратегия синтеза Выбор исходного сырья Построение углеродного остова молекулы Введение, удаление или замена функциональной группы Защита группы Стереоселективность «Я хочу воспеть хвалу сотворению молекул – химическому синтезу… …Я глубоко убежден, что он и есть искусство. И в то же время синтез – это логика» . Роальд Хоффман (Нобелевская премия по химии 1981 г) 5
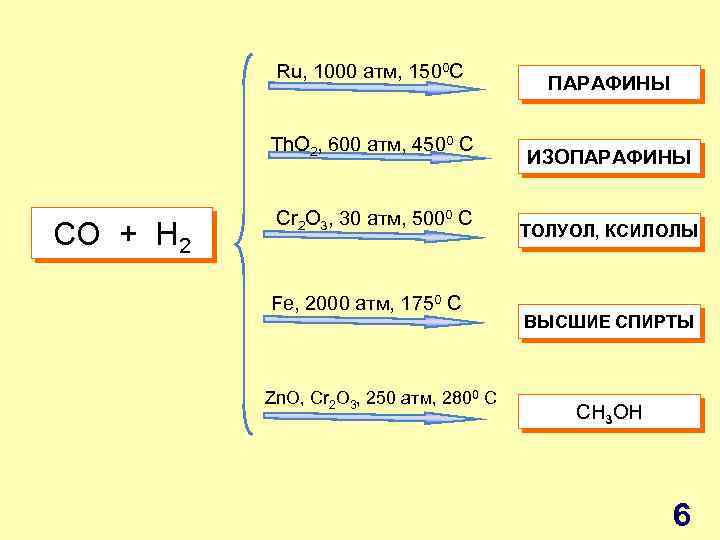
Ru, 1000 атм, 1500 C Th. O 2, 600 атм, 4500 C СO + H 2 Cr 2 O 3, 30 атм, 5000 C Fe, 2000 атм, 1750 C Zn. O, Cr 2 O 3, 250 атм, 2800 C ПАРАФИНЫ ИЗОПАРАФИНЫ ТОЛУОЛ, КСИЛОЛЫ ВЫСШИЕ СПИРТЫ СH 3 OH 6
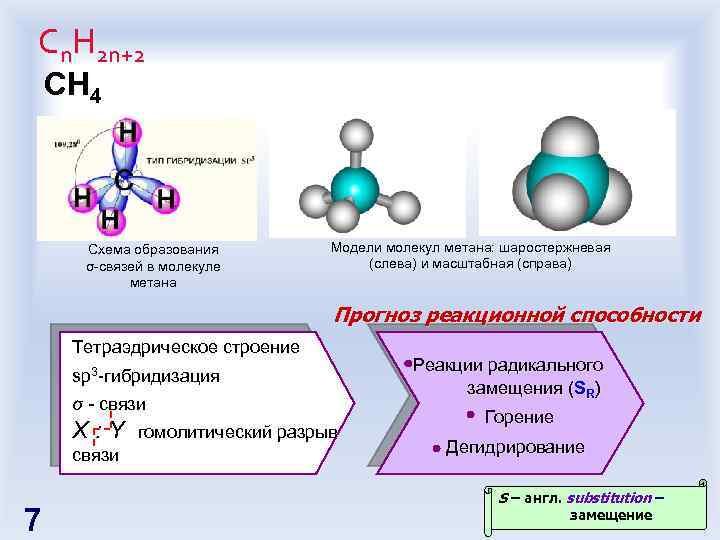
Сn. H 2 n+2 СH 4 Схема образования σ-связей в молекуле метана Модели молекул метана: шаростержневая (слева) и масштабная (справа) Прогноз реакционной способности Тетраэдрическое строение sp 3 -гибридизация σ - связи X : Y гомолитический разрыв связи 7 Реакции радикального замещения (SR) Горение Дегидрирование S – англ. substitution – замещение
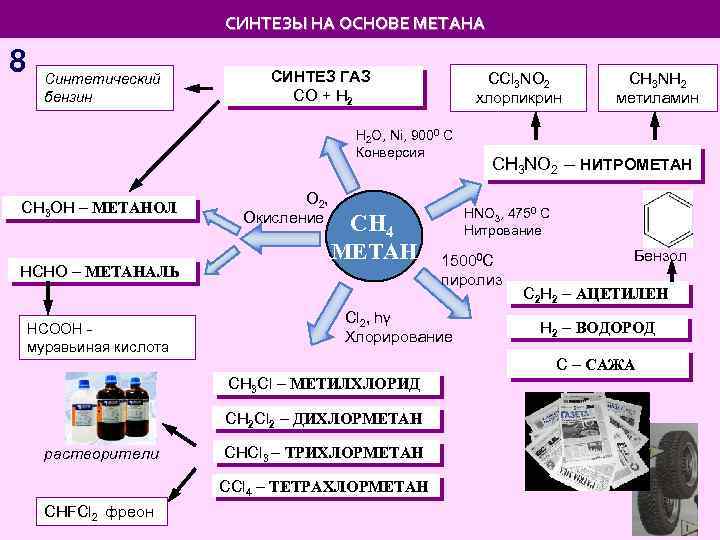
СИНТЕЗЫ НА ОСНОВЕ МЕТАНА 8 Синтетический бензин СИНТЕЗ ГАЗ СO + H 2 СCl 3 NO 2 хлорпикрин Н 2 О, Ni, 9000 C Конверсия СH 3 OH – МЕТАНОЛ HCHO – МЕТАНАЛЬ HCOOH муравьиная кислота О 2, Окисление CH 4 МЕТАН СH 3 NH 2 метиламин СH 3 NO 2 – НИТРОМЕТАН HNO 3, 4750 C Нитрование 15000 С пиролиз Сl 2, hγ Хлорирование Бензол С 2 Н 2 – АЦЕТИЛЕН Н 2 – ВОДОРОД С – САЖА СH 3 Cl – МЕТИЛХЛОРИД СH 2 Cl 2 – ДИХЛОРМЕТАН растворители СHCl 3 – ТРИХЛОРМЕТАН СCl 4 – ТЕТРАХЛОРМЕТАН СHFCl 2 фреон
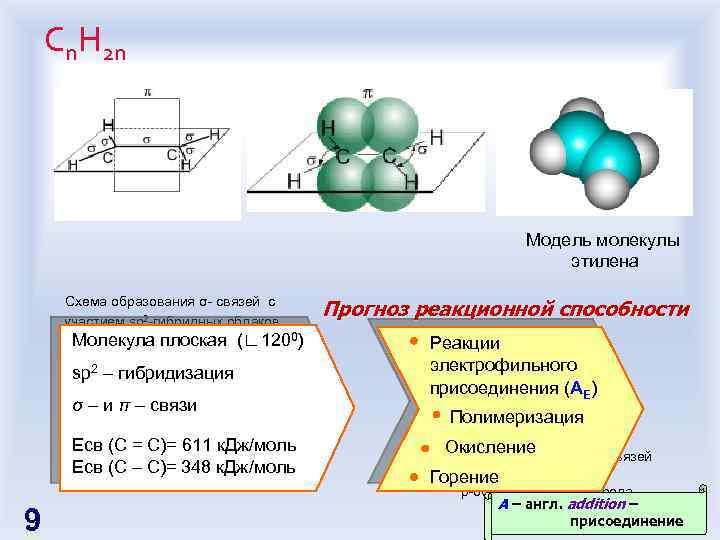
Сn. H 2 n Модель молекулы этилена Схема образования σ- связей с участием sp 2 -гибридных облаков атома углерода Молекула плоская (∟ 1200) sp 2 – гибридизация σ – и π – связи Есв (С = С)= 611 к. Дж/моль Есв (С – С)= 348 к. Дж/моль 9 Прогноз реакционной способности Реакции электрофильного присоединения (AE) Полимеризация Окисление Схема образования π – связей Горение с участием p-облаков атома углерода A – англ. addition – присоединение
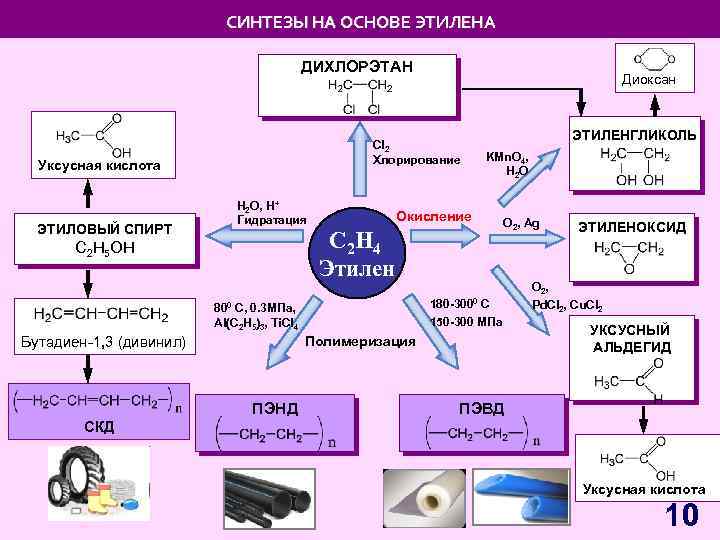
СИНТЕЗЫ НА ОСНОВЕ ЭТИЛЕНА ДИХЛОРЭТАН Cl 2 Хлорирование Уксусная кислота ЭТИЛОВЫЙ СПИРТ Диоксан H 2 O, H+ Гидратация ЭТИЛЕНГЛИКОЛЬ KMn. O 4, H 2 O Окисление C 2 H 4 Этилен С 2 Н 5 OH 150 -300 МПа Полимеризация ПЭНД ЭТИЛЕНОКСИД O 2, 180 -3000 С 800 С, 0. 3 МПа, Al(C 2 H 5)3, Ti. Cl 4 Бутадиен-1, 3 (дивинил) O 2, Ag Pd. Cl 2, Cu. Cl 2 УКСУСНЫЙ АЛЬДЕГИД ПЭВД СКД Уксусная кислота 10
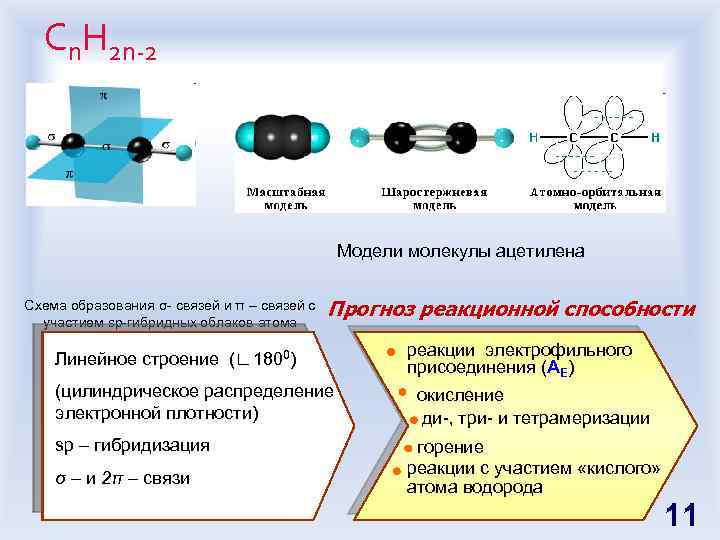
Сn. H 2 n-2 Модели молекулы ацетилена Схема образования σ- связей и π – связей с участием sp-гибридных облаков атома углерода Прогноз реакционной способности Линейное строение (∟ 1800) (цилиндрическое распределение электронной плотности) sp – гибридизация σ – и 2π – связи 2 реакции электрофильного присоединения (AE) окисление ди-, три- и тетрамеризации горение реакции с участием «кислого» атома водорода 11
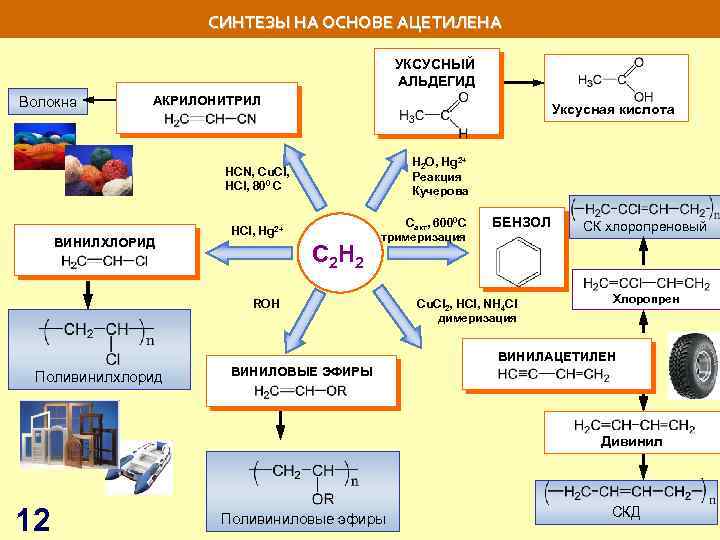
СИНТЕЗЫ НА ОСНОВЕ АЦЕТИЛЕНА УКСУСНЫЙ АЛЬДЕГИД Волокна АКРИЛОНИТРИЛ Уксусная кислота H 2 O, Hg 2+ Реакция Кучерова HCN, Сu. Cl, HCl, 800 C ВИНИЛХЛОРИД HСl, Hg 2+ C 2 H 2 Сакт, 6000 С тримеризация ROH БЕНЗОЛ Сu. Cl 2, HCl, NH 4 Cl димеризация СК хлоропреновый Хлоропрен ВИНИЛАЦЕТИЛЕН Поливинилхлорид ВИНИЛОВЫЕ ЭФИРЫ Дивинил 12 Поливиниловые эфиры СКД
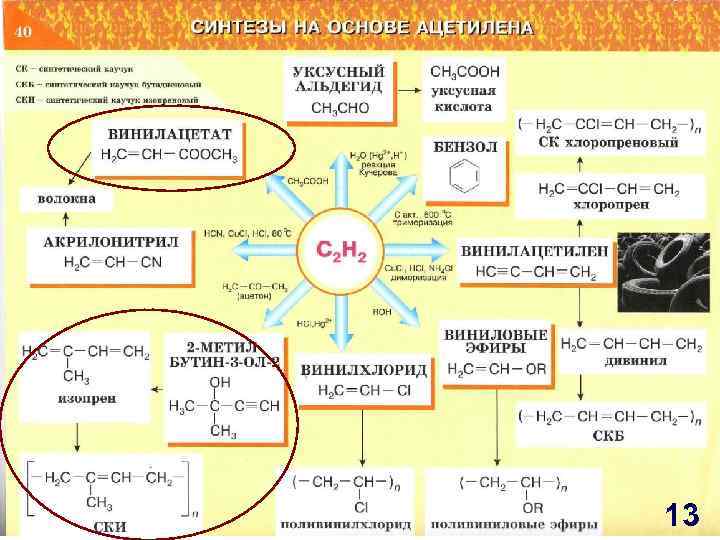
13
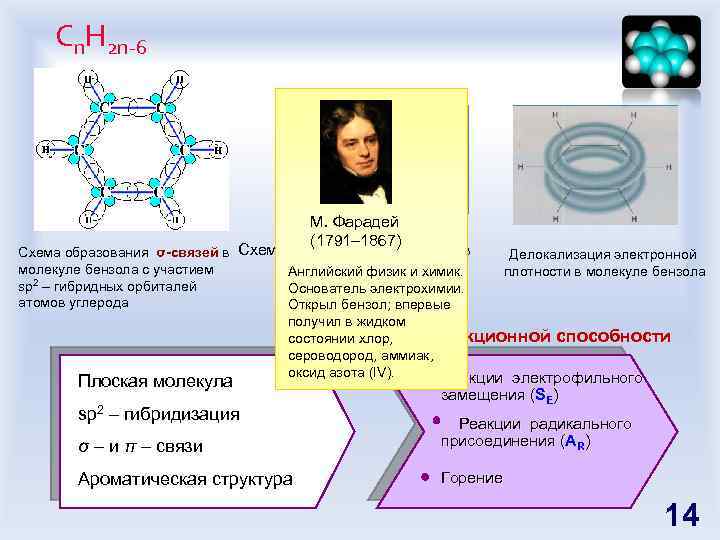
Сn. H 2 n-6 М. Фарадей (1791– 1867) Схема образования σ-связей в Схема образования π-связей в молекуле бензола с участием молекуле бензолахимик. Английский физик и sp 2 – гибридных орбиталей атомов углерода Плоская молекула Делокализация электронной плотности в молекуле бензола Основатель электрохимии. Открыл бензол; впервые получил в жидком состоянии Прогноз реакционной способности хлор, сероводород, аммиак, оксид азота (IV). Реакции электрофильного sp 2 – гибридизация Реакции электрофильного замещения (SE) σ – и π – связи Реакции радикального присоединения (АR) Ароматическая структура Горение 14
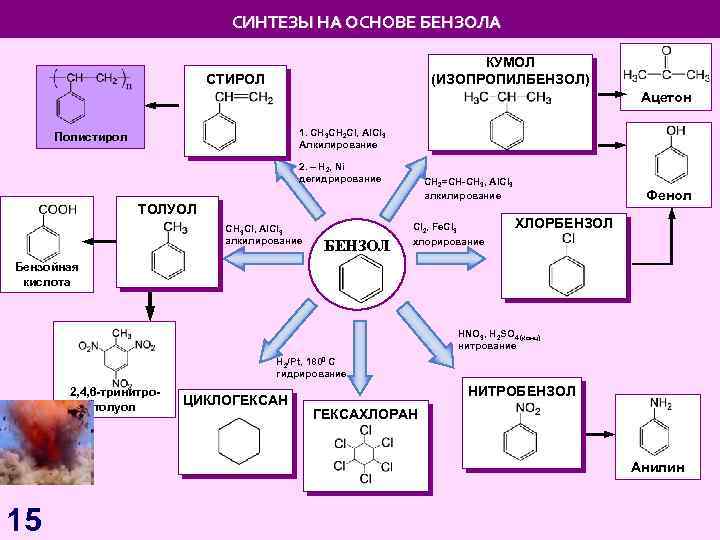
СИНТЕЗЫ НА ОСНОВЕ БЕНЗОЛА КУМОЛ (ИЗОПРОПИЛБЕНЗОЛ) СТИРОЛ Ацетон 1. СH 3 CH 2 Cl, Al. Cl 3 Алкилирование Полистирол 2. – H 2, Ni дегидрирование СH 2=CH-CH 3, Al. Cl 3 алкилирование ТОЛУОЛ CH 3 Cl, Al. Cl 3 алкилирование БЕНЗОЛ Сl 2, Fe. Cl 3 хлорирование Фенол ХЛОРБЕНЗОЛ Бензойная кислота HNO 3, H 2 SO 4 (конц) нитрование H 2/Pt, 1800 C гидрирование 2, 4, 6 -тринитротолуол ЦИКЛОГЕКСАН НИТРОБЕНЗОЛ ГЕКСАХЛОРАН Анилин 15
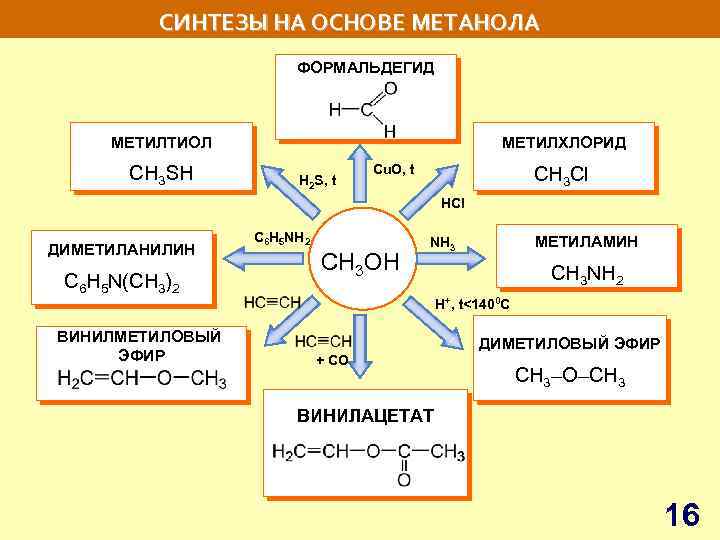
СИНТЕЗЫ НА ОСНОВЕ МЕТАНОЛА ФОРМАЛЬДЕГИД МЕТИЛТИОЛ СН 3 SH МЕТИЛХЛОРИД H 2 S, t Сu. O, t СН 3 Сl HCl ДИМЕТИЛАНИЛИН C 6 H 5 N(CH 3)2 С 6 H 5 NH 2 СH 3 OH МЕТИЛАМИН NH 3 СН 3 NH 2 H+, t<1400 C ВИНИЛМЕТИЛОВЫЙ ЭФИР + CO ДИМЕТИЛОВЫЙ ЭФИР CH 3–O–CH 3 ВИНИЛАЦЕТАТ 16
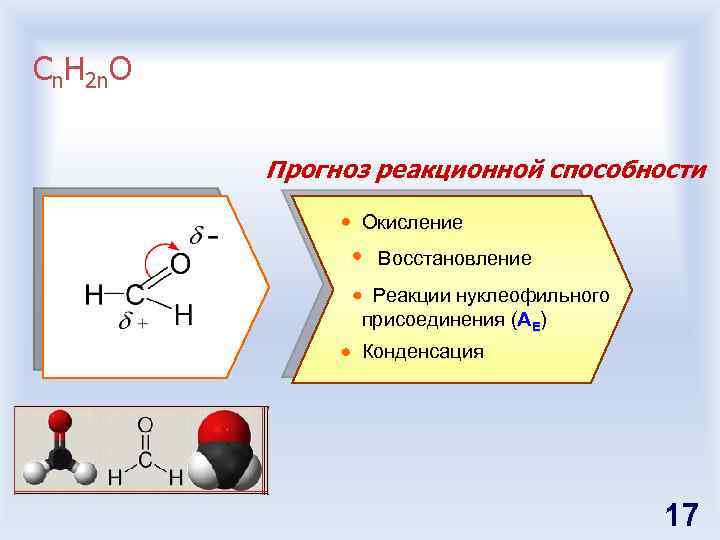
Сn. H 2 n. O Прогноз реакционной способности Окисление Восстановление Реакции нуклеофильного присоединения (AE) Конденсация 17
![СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДА КАРБАМИДНЫЕ СМОЛЫ ФЕНОЛФОРМАЛЬДЕГИДНЫЕ СМОЛЫ МУРАВЬИНАЯ КИСЛОТА [O] ПЕРВИЧНЫЕ СПИРТЫ ПАРАФОРМ СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДА КАРБАМИДНЫЕ СМОЛЫ ФЕНОЛФОРМАЛЬДЕГИДНЫЕ СМОЛЫ МУРАВЬИНАЯ КИСЛОТА [O] ПЕРВИЧНЫЕ СПИРТЫ ПАРАФОРМ](https://present5.com/presentation/-57355521_233358604/image-18.jpg)
СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДА КАРБАМИДНЫЕ СМОЛЫ ФЕНОЛФОРМАЛЬДЕГИДНЫЕ СМОЛЫ МУРАВЬИНАЯ КИСЛОТА [O] ПЕРВИЧНЫЕ СПИРТЫ ПАРАФОРМ [H] ТРИОКСАН МЕТАНОЛ СH 3 OH УРОТРОПИН (ГЕКСМЕТИЛЕНТЕТРАМИН) Гексоген 1861 г. А. М. Бутлеров 18
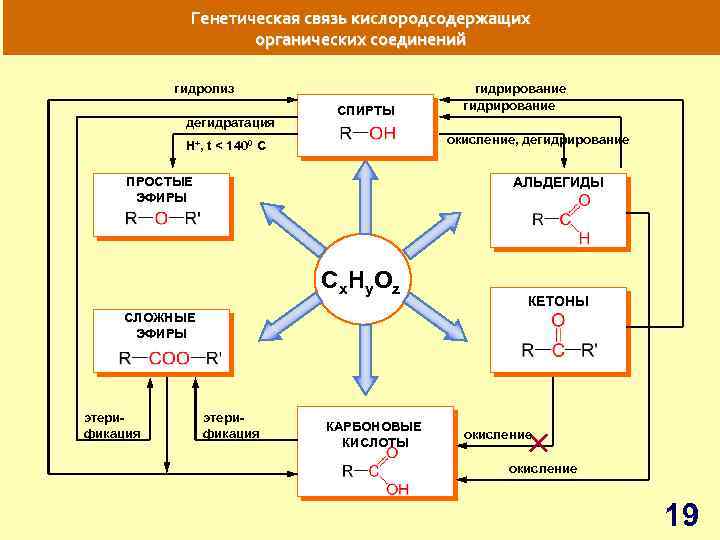
Генетическая связь кислородсодержащих органических соединений гидролиз дегидратация СПИРТЫ гидрирование окисление, дегидрирование H+, t < 1400 C АЛЬДЕГИДЫ ПРОСТЫЕ ЭФИРЫ C x. H y. O z КЕТОНЫ СЛОЖНЫЕ ЭФИРЫ этерификация КАРБОНОВЫЕ КИСЛОТЫ окисление 19

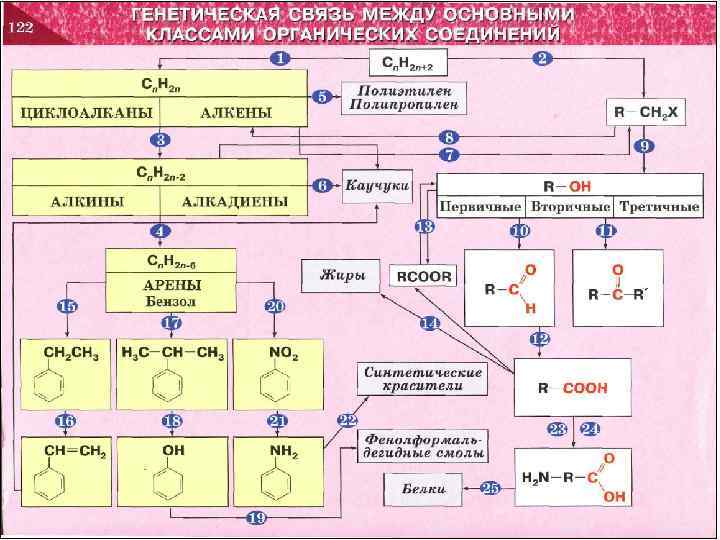
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ ОСНОВНЫМИ КЛАССАМИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
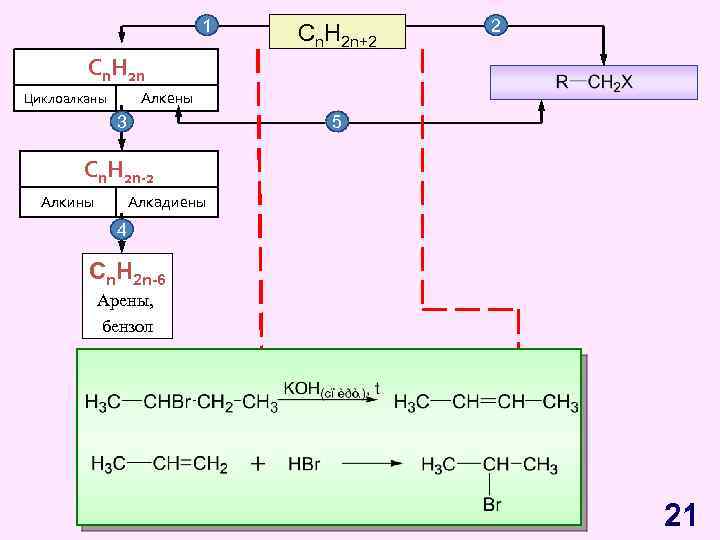
1 Cn. H 2 n+2 2 Cn. H 2 n Алкены Циклоалканы 3 5 Cn. H 2 n-2 Алкины Алкадиены 4 Cn. H 2 n-6 Арены, бензол 21
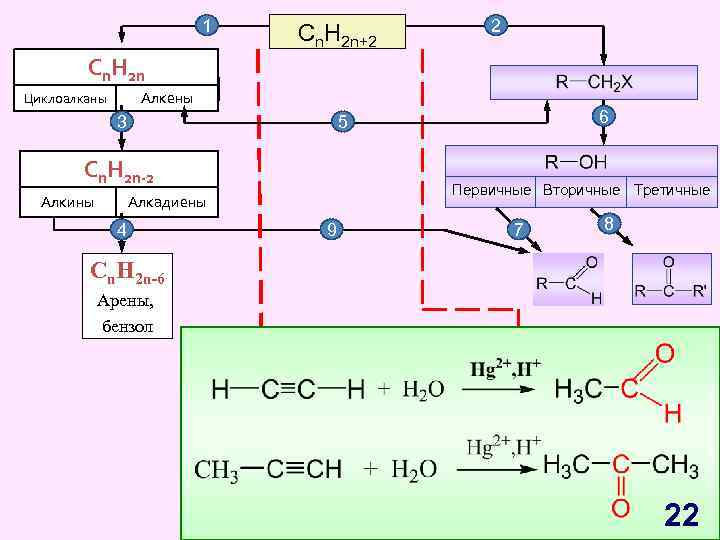
1 Cn H Cn. H 2 n 2 n Циклоалканы Cn. H 2 n+2 2 Алкены Циклоалканы 3 CH Cnn. H 2 n-2 -2 2 n Алкины 6 5 Первичные Вторичные Третичные Алкадиены 4 9 7 8 Cn. H 2 n-6 Арены, бензол 22
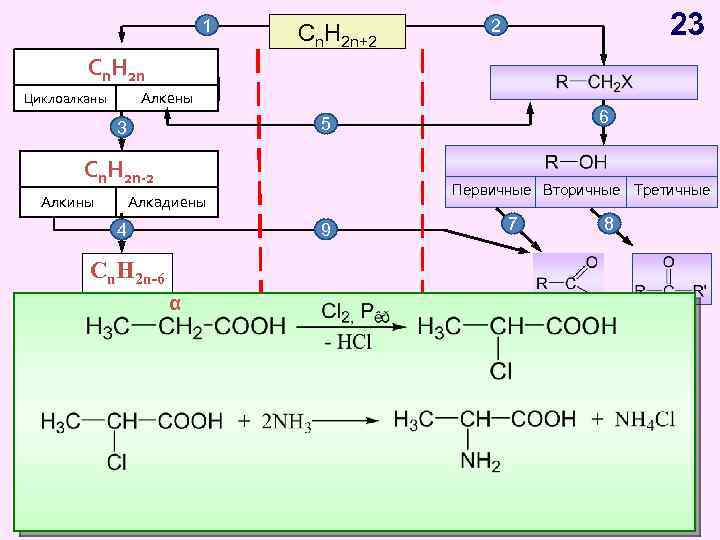
1 Cn H Cn. H 2 n 2 n Циклоалканы Cn. H 2 n+2 23 2 Алкены Циклоалканы CH Cnn. H 2 n-2 -2 2 n Алкины 6 5 3 Первичные Вторичные Третичные Алкадиены 4 9 7 8 Cn. H 2 n-6 Арены, α бензол 10 11
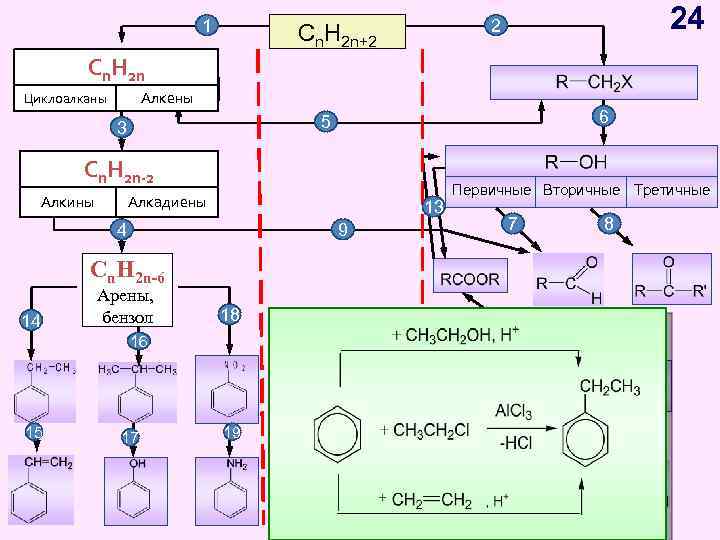
1 Cn H Cn. H 2 n 2 n Циклоалканы 24 2 Cn. H 2 n+2 Алкены Циклоалканы 6 5 3 CH Cnn. H 2 n-2 -2 2 n Алкины Алкадиены 13 4 9 Первичные Вторичные Третичные 7 8 Cn. H 2 n-6 14 Арены, бензол 18 16 15 17 19 12 10 11
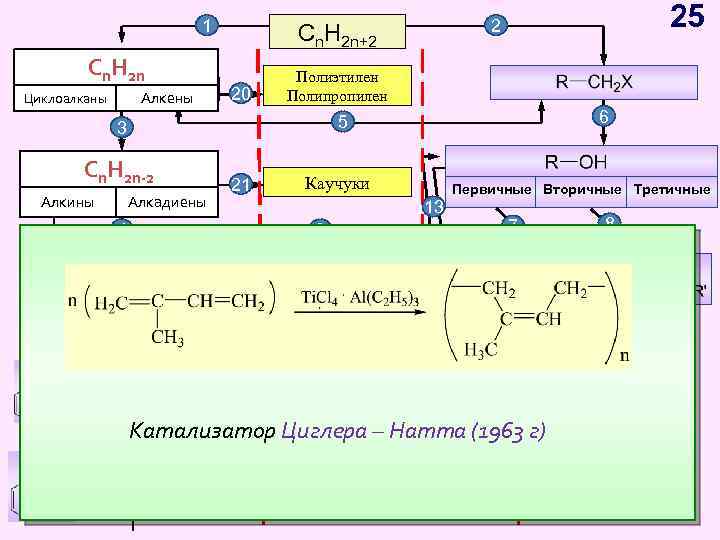
1 Cn H Cn. H 2 n 2 n Циклоалканы Алкены Циклоалканы Cn. H 2 n+2 20 Полиэтилен Полипропилен 6 5 3 CH Cnn. H 2 n-2 -2 2 n Алкины 25 2 Алкадиены 21 Каучуки Первичные Вторичные Третичные 13 4 9 8 7 Cn. H 2 n-6 14 Арены, бензол 18 16 15 17 19 Катализатор 12 Циглера – Натта (1963 г) 10 11
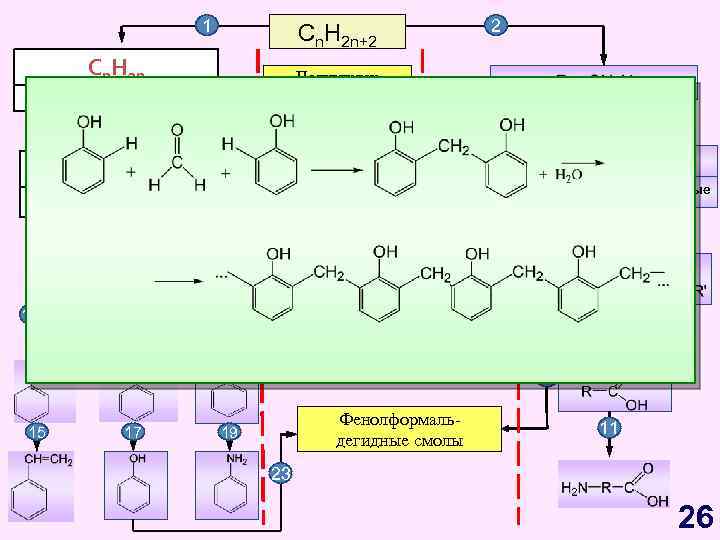
1 Cn H Cn. H 2 n 2 n Циклоалканы Алкены Циклоалканы 20 Полиэтилен Полипропилен CH Cnn. H 2 n-2 -2 2 n Алкадиены Каучуки 21 Первичные Вторичные 13 4 Арены, бензол Третичные 8 7 9 Cn. H 2 n-6 14 6 5 3 Алкины 2 Cn. H 2 n+2 Жиры 18 22 16 12 10 23 15 17 Фенолформальдегидные смолы 19 11 23 26
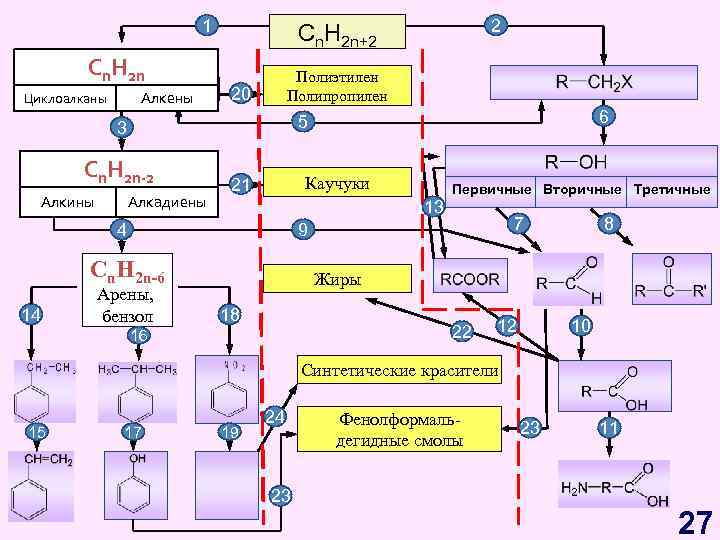
1 Cn H Cn. H 2 n 2 n Циклоалканы Алкены Циклоалканы Полиэтилен Полипропилен 20 CH Cnn. H 2 n-2 -2 2 n Алкадиены Каучуки 21 Первичные Вторичные Третичные 13 4 7 9 Cn. H 2 n-6 14 6 5 3 Алкины 2 Cn. H 2 n+2 Арены, бензол 8 Жиры 18 22 16 12 10 Синтетические красители 15 17 19 24 23 Фенолформальдегидные смолы 23 11 27
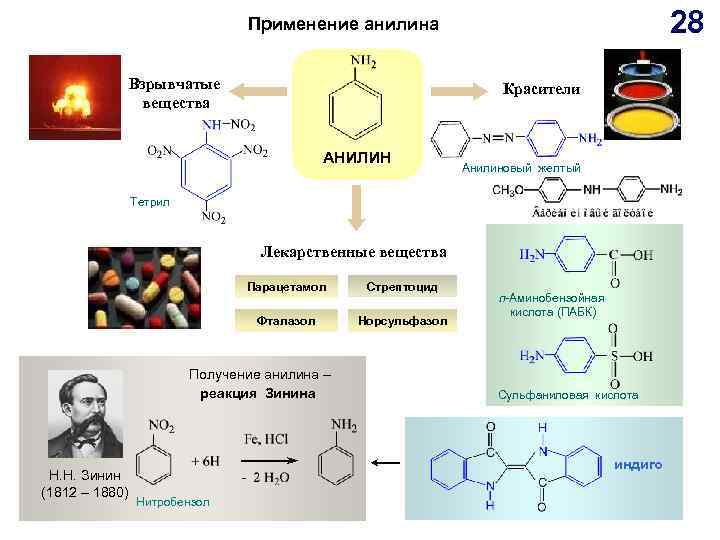
28 Применение анилина Взрывчатые вещества Красители АНИЛИН Анилиновый желтый Тетрил Лекарственные вещества Парацетамол Cтрептоцид Фталазол Норсульфазол Получение анилина – реакция Зинина Н. Н. Зинин (1812 – 1880) п-Аминобензойная кислота (ПАБК) Сульфаниловая кислота индиго Нитробензол
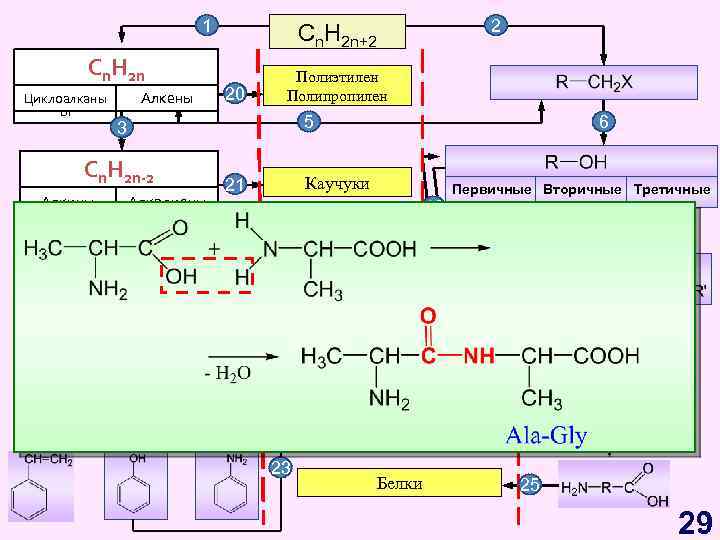
1 Cn. H 2 n Циклоалканы ы Алкены 20 Полиэтилен Полипропилен 5 3 Cn. H 2 n-2 Алкины Алкадиены 6 Каучуки 21 Первичные Вторичные Третичные 13 4 7 9 Cn. H 2 n-6 14 2 Cn. H 2 n+2 Арены, бензол 16 Жиры 18 22 12 Синтетические красители 24 15 17 8 19 23 10 23 Фенолформальдегидные смолы Белки 11 25 29

ген связь орг соед.ppt