Практика 1.ppt
- Количество слайдов: 30

Санкт-Петербургский Государственный Университет Биолого-почвенный факультет Кафедра биохимии Физико-химические свойства аминокислот и белков. Количественные (колориметрические) методы определения концентрации белка Практическое занятие № 1 Санкт-Петербург 2012
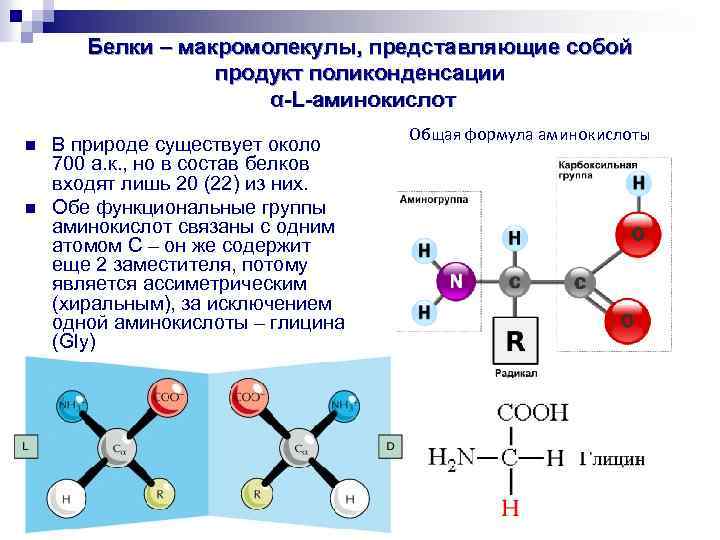
Белки – макромолекулы, представляющие собой продукт поликонденсации α-L-аминокислот n n В природе существует около 700 а. к. , но в состав белков входят лишь 20 (22) из них. Обе функциональные группы аминокислот связаны с одним атомом С – он же содержит еще 2 заместителя, потому является ассиметрическим (хиральным), за исключением одной аминокислоты – глицина (Gly) Общая формула аминокислоты
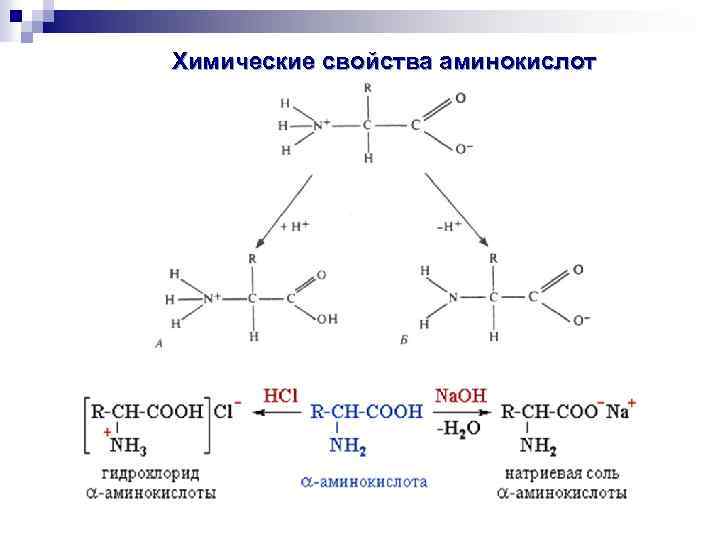
Химические свойства аминокислот
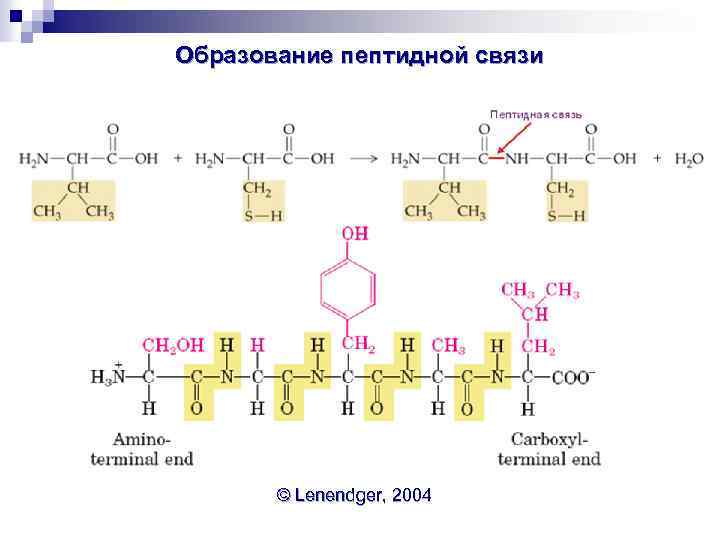
Образование пептидной связи © Lenendger, 2004
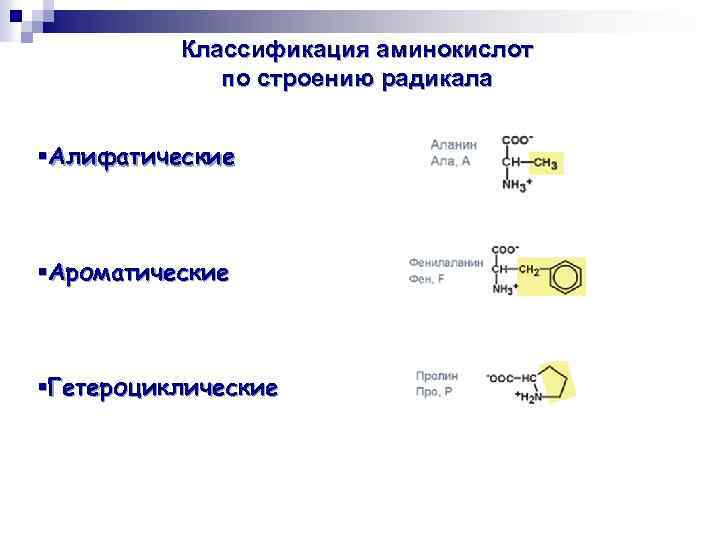
Классификация аминокислот по строению радикала §Алифатические §Ароматические §Гетероциклические
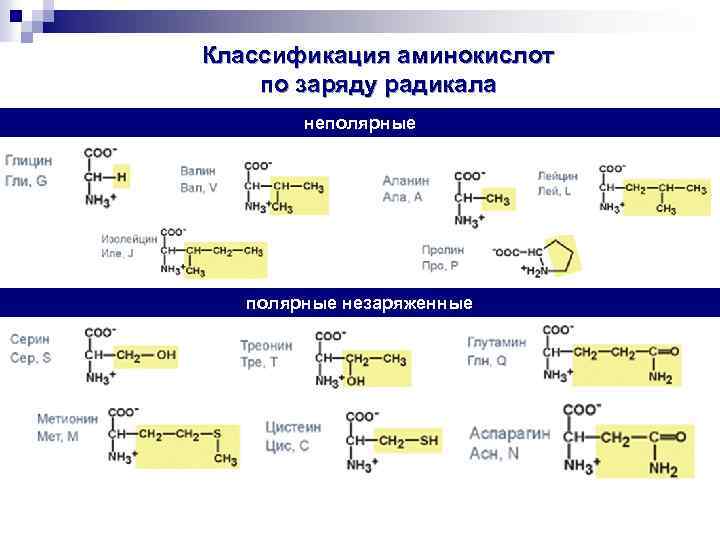
Классификация аминокислот по заряду радикала неполярные незаряженные
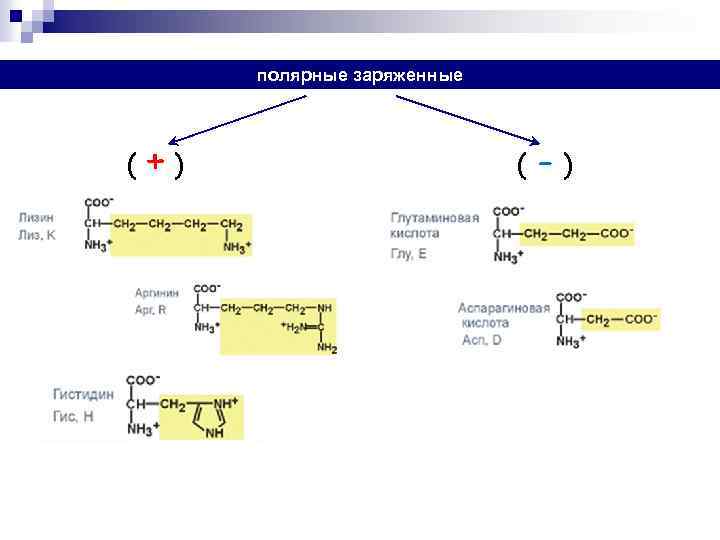
полярные заряженные (+) ( -)

Функциональные группы боковых радикалов §карбоксильная -СООН §амино -NH 2 §тиольная -SH §амидная -CO-NH 2 §гидроксильная -ОН §гуанидиновая -(NH-C(NH 2)=NH)
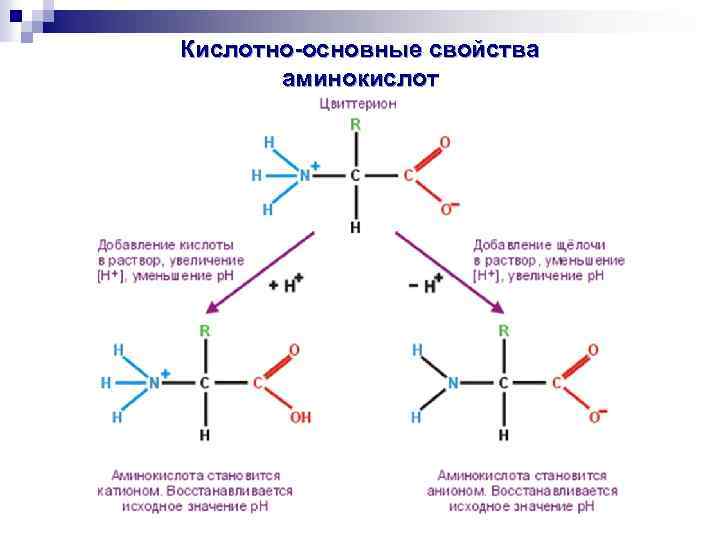
Кислотно-основные свойства аминокислот
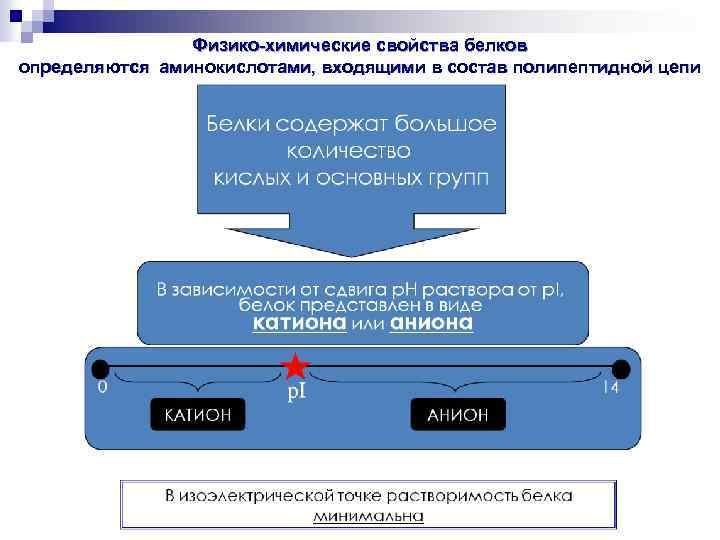
Физико-химические свойства белков определяются аминокислотами, входящими в состав полипептидной цепи

§ изоэлектрическая точка p. I - p. H раствора, при котором суммарный заряд аминокислоты равен 0 § в изоэлектрической точке наблюдается агрегация белковых молекул, выпадение белка в осадок § среднее арифметическое двух величин p. K’:
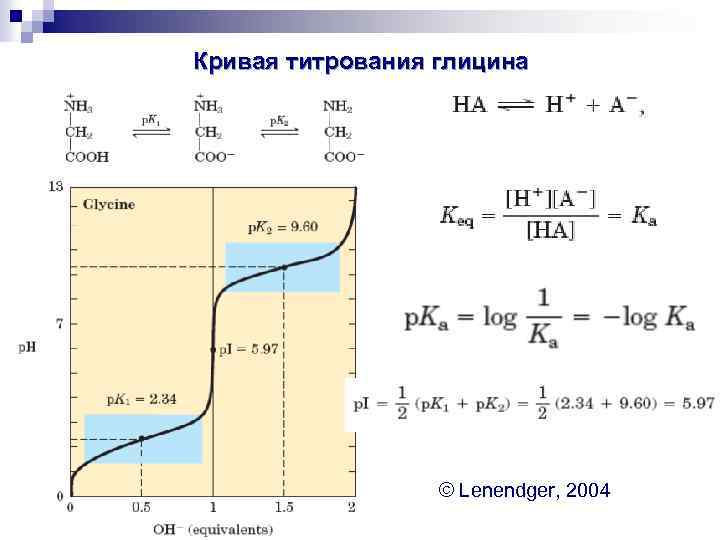
Кривая титрования глицина © Lenendger, 2004
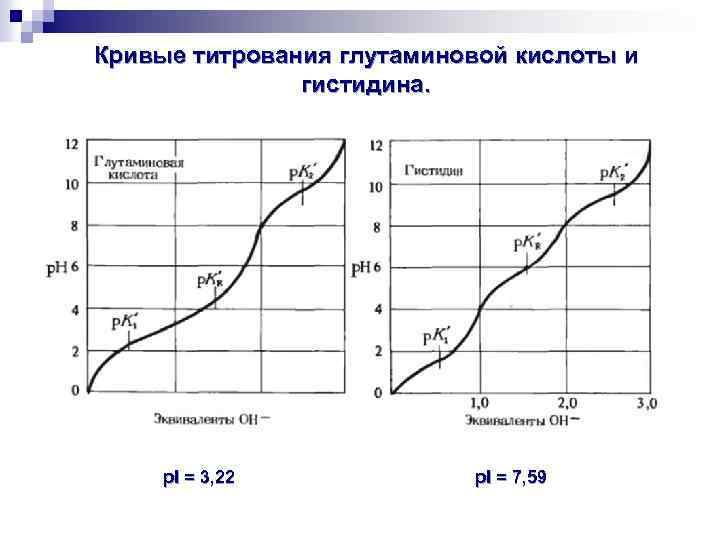
Кривые титрования глутаминовой кислоты и гистидина. p. I = 3, 22 p. I = 7, 59
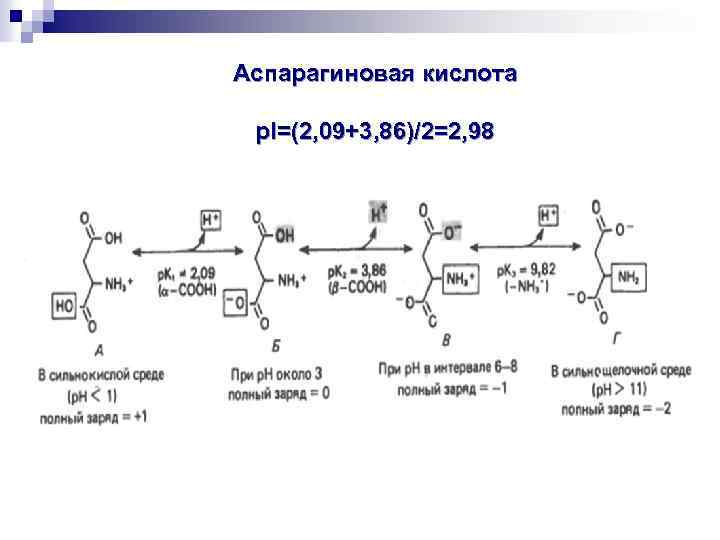
Аспарагиновая кислота р. I=(2, 09+3, 86)/2=2, 98

Денатурация белков (от лат. de- —, обратимая необратимая удаление и лат. nature — природа) — потеря белками их естественных свойств (растворимости, гидрофильности и др. ) вследствие нарушения пространственной структуры их молекул. Денатурация часто приводит к тому, что в коллоидном растворе белковых молекул происходит процесс агрегации частиц белка в более крупные. Ренатурация - восстановление нативной (биологически активной) пространственной структуры белка.
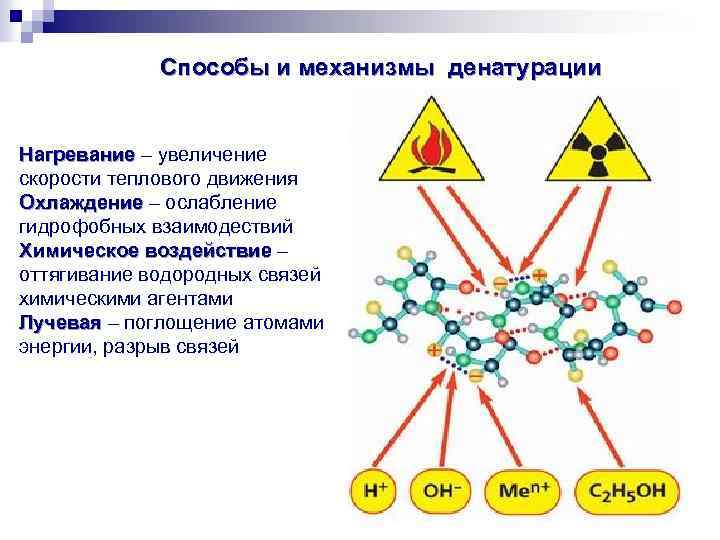
Способы и механизмы денатурации Нагревание – увеличение Нагревание скорости теплового движения Охлаждение – ослабление Охлаждение гидрофобных взаимодествий Химическое воздействие – оттягивание водородных связей химическими агентами Лучевая – поглощение атомами Лучевая энергии, разрыв связей
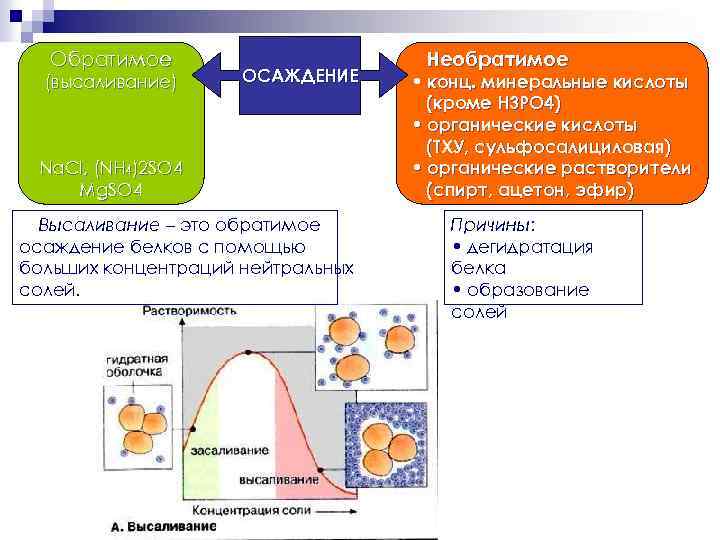
Обратимое (высаливание) ОСАЖДЕНИЕ Na. Cl, (NH 4)2 SO 4 Mg. SO 4 Высаливание – это обратимое осаждение белков с помощью больших концентраций нейтральных солей. Необратимое • конц. минеральные кислоты (кроме H 3 PO 4) • органические кислоты (ТХУ, сульфосалициловая) • органические растворители (спирт, ацетон, эфир) Причины: • дегидратация белка • образование солей
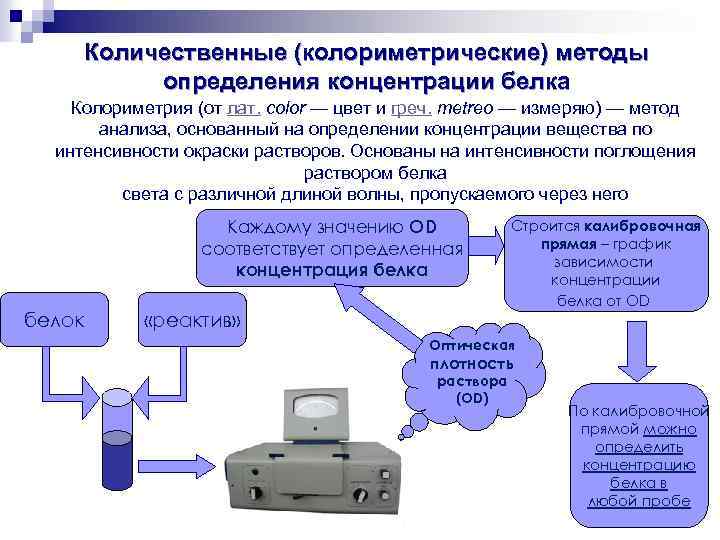
Количественные (колориметрические) методы определения концентрации белка Колориметрия (от лат. color — цвет и греч. metreo — измеряю) — метод анализа, основанный на определении концентрации вещества по интенсивности окраски растворов. Основаны на интенсивности поглощения раствором белка света с различной длиной волны, пропускаемого через него Каждому значению OD соответствует определенная концентрация белка белок «реактив» Строится калибровочная прямая – график зависимости концентрации белка от OD Оптическая плотность раствора (OD) По калибровочной прямой можно определить концентрацию белка в любой пробе

Принцип работы спектрофотометра (Лампа накаливания/ дейтериевая) СФ - 46
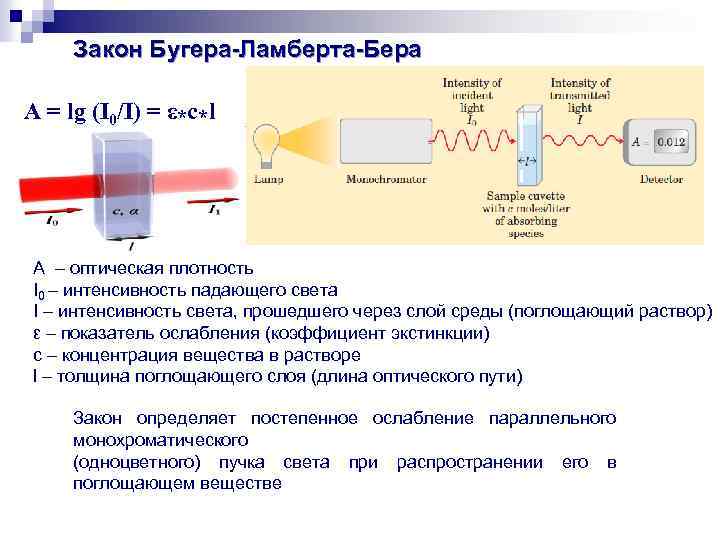
Закон Бугера-Ламберта-Бера А = lg (I 0/I) = ε*c*l A – оптическая плотность I 0 – интенсивность падающего света I – интенсивность света, прошедшего через слой среды (поглощающий раствор) ε – показатель ослабления (коэффициент экстинкции) c – концентрация вещества в растворе l – толщина поглощающего слоя (длина оптического пути) Закон определяет постепенное ослабление параллельного монохроматического (одноцветного) пучка света при распространении его в поглощающем веществе

Фотометрические методы Спектрофотометрические Колориметрические Основаны на поглощении света в определенных участках спектра отдельными химическими группами, входящими в их структуру. Для большинства природных белков характерны два пика поглощения в видимой и ближней ультрафиолетовой части спектра Основаны на образовании окрашенных комплексов с белком, интенсивность окраски прямо пропорциональна концентрации белка в растворе. Спектры поглощения находятся в ультрафиолетовой (200— 400 нм), видимой (400— 760 нм) и инфракрасной (>760 нм) областях спектра.

Колориметрические методы Взаимодействие белка и ионами меди в щелочной среде (биуретовый метод, метод Лоури). Концентрация окрашенных комплексов (интенсивность окраски) пропорциональны числу пептидных связей Взаимодействие положительно заряженных групп аминокислотных остатков белков с разнообразными по структуре кислыми красителями (метод Бредфорд, метод Флореса)

Колориметрические методы по сравнению со спектрофотометрическими более трудоемки и требуют значительных затрат времени, но в целом обладают большей чувствительностью и помехоустойчивостью, т. к. при взаимодействии с белками образуются специфические комплексы с очень интенсивным окрашиванием

Цветные реакции на белки и аминокислоты n n n Ксантопротеиновая (нитрование концентрированной HNO 3 ароматических аминокислотных остатков) Биуретовая (комплексное соединение пептидных групп с ионами меди) Диазореакция Паули (гистидин и тирозин реагируют с диазобензолсульфоновой кислотой) Реакция Эрлиха на серусодержащие аминокислоты Нингидриновая реакция на свободные аминокислоты
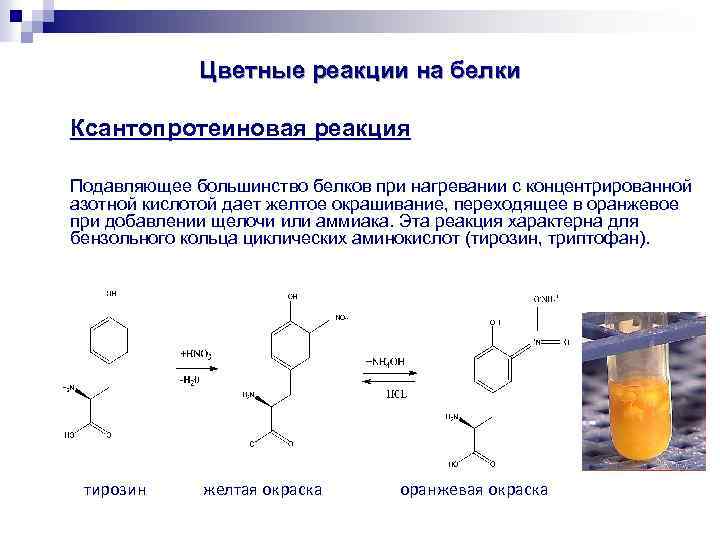
Цветные реакции на белки Ксантопротеиновая реакция Подавляющее большинство белков при нагревании с концентрированной азотной кислотой дает желтое окрашивание, переходящее в оранжевое при добавлении щелочи или аммиака. Эта реакция характерна для бензольного кольца циклических аминокислот (тирозин, триптофан). тирозин желтая окраска оранжевая окраска

Биуретовый метод Метод основан на образовании в щелочной среде окрашенного в фиолетовый цвет комплекса пептидных связей белков с ионами двухвалентной меди. 1 –енолизация пептида в щелочной среде 2 – образование сине-фиолетового комплекса

Метод Лоури Белки с реактивом Фолина-Чокальтеу (кислый фосфорномолибденово-фосфорновольфрамовый реактив, взаимодействует с остатками ароматических аминокислот Tyr, Trp) в присутствии сернокислой меди и щелочи дают комплексное соединение синего цвета.
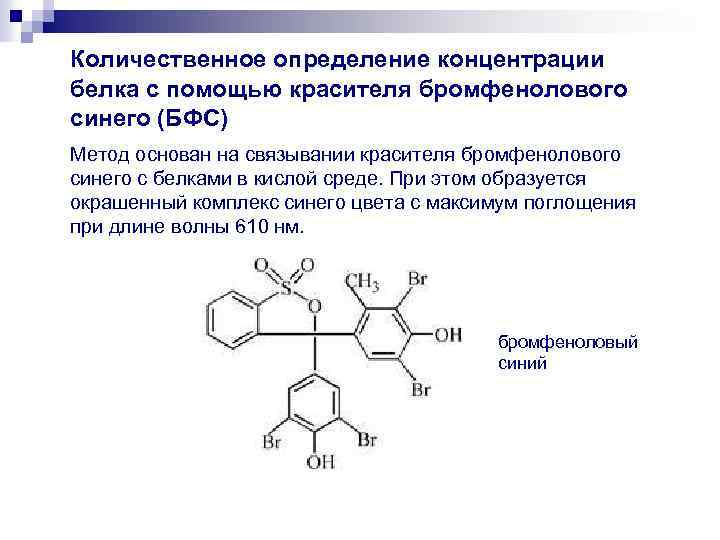
Количественное определение концентрации белка с помощью красителя бромфенолового синего (БФС) Метод основан на связывании красителя бромфенолового синего с белками в кислой среде. При этом образуется окрашенный комплекс синего цвета с максимум поглощения при длине волны 610 нм. бромфеноловый синий

Форма отчетности Внимание! Все, что делается, следует конспектировать. Записывать концентрации, разведения, данные с фотоколориметра. Все пробирки с растворами следует подписывать. Это значительно упростит работу После выполнения всех заданий нужно оформить отчет и подписать его у преподавателя Отчет должен содержать: -Описание метода, его принцип -Результаты эксперимента (наблюдаемые явления, полученные данные, графики) -Выводы ***Также для получения зачета необходимо знать теоретические основы***

Счастливой практики)
Практика 1.ppt