Санкт-Петербургский государственный университет


Санкт-Петербургский государственный университет НЕЙРОИММУНОЛОГИЯ NEUROIMMUNOLOGY Проф. д. б. н. Обухов Д. К. Академик Российской и Европейской Академии Естествознания Санкт-Петербург
Санкт-Петербургский государственный университет Биологический факультет НЕЙРОИММУНОЛОГИЯ Лекция 2 Иннервация лимфоидной системы. Нервы и иммунитет
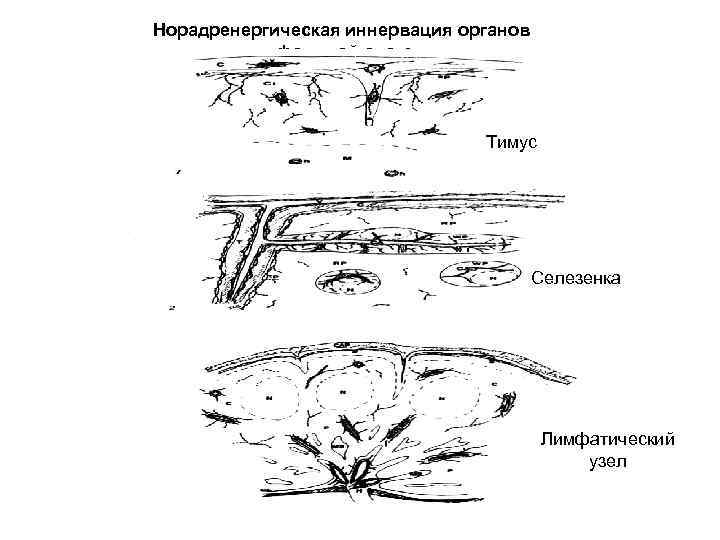
Норадренергическая иннервация органов лимфоидной системы Тимус Селезенка Лимфатический узел

Иннервация тимуса Основными источниками симпатической иннервации тимуса являются симпатические нервы, связанные с верхним шейным и звездчатыми ганглиями. Катехоламинэргические постганглионарные волокна проникают в орган по ходу кровеносных сосудов, основная их концентрация наблюдается в корковой зоне, в мозговом веществе их концентрация намного ниже. Тем не менее, норадренергическая иннервация является преобладающей. Парасимпатическая иннервация (холинэргическая) тимуса связана с системой блуждающего нерва и шейными сегментами спинного мозга. Основная масса волокон расположена вдоль сосудов, в паренхиме органа их намного меньше. Важно отметить, что гистохимическое и иммуннногистохимическое выявление АХЭ- азы и АХТ-азы показало, что они находятся не только в волокнах парасимпатической природы, но и клеточных элементах самого тимуса (тимоцитах, эпителиальных клетках). это говорит о возможности синтеза АХ непосредственно клетками иммунной системы, на которых, кроме того были обнаружены рецепторы к НА и АХ. Пептидэргическая иннервация тимуса чрезвычайно богата. Она преобладает в капсуле, субкапсуллярной зоне, междольковых септах и вокруг сосудов коры и паракортикальной зоны. Очень часто наблюдается сочетанное присутствие нескольких нейропептидов в одной терминали. Часть пептидов обнаруживается в элементах ткани тимуса и системой клеток АПУД-систмы и не связаны с нервными волокнами.
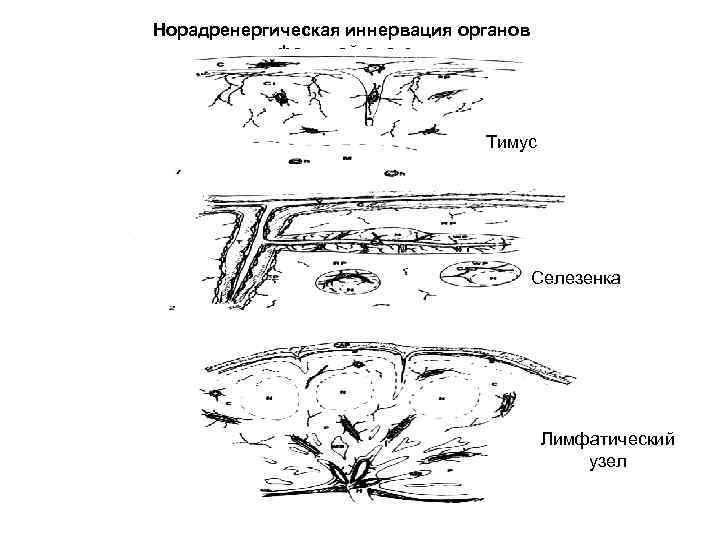
Норадренергическая иннервация органов лимфоидной системы Тимус Селезенка Лимфатический узел

Иннервация селезенки Симпатическая (норадренергическая) иннервация селезенки происходит из симпатического верхнего брыжеечного ганглия. Основная масса волокон распространяется вдоль кровеносных сосудов и по трабекулам. Большинство волокон находится в белой пульпе, тогда как в красной менее 1 % В В-зону проникают только отдельные волокна, в паракортикальной зоне они выявляются чаще. Электронно-микроскопические исследования показали, что адренергические волокна находятся в тесном контакте не только с гл. мускулатурой сосудов, но и непосредственно с паренхимой селезенки (макрофагами, ретикулярными клетками) и лимфоцита (Рис. ) Некоторые волокна образуют даже впячивания в лимфоциты. Такой тесный контакт волокон с клетками селезенки (до 6 нм) предполагает синаптический или паракринный характер их взаимодействия. Холинэргическая , парасимпатическая иннервация селезенки практически отсутствует, т. е. влияние вагуса и парасимпатической нервной системы минимально. Neuroanatomical and neurochemical evidence demonstrates that neural innervation of the spleen is entirely sympathetic in origin, and indicates further that there is no evidence for parasympatheticor sensory input to the spleen (Nance, Sanders 2007)
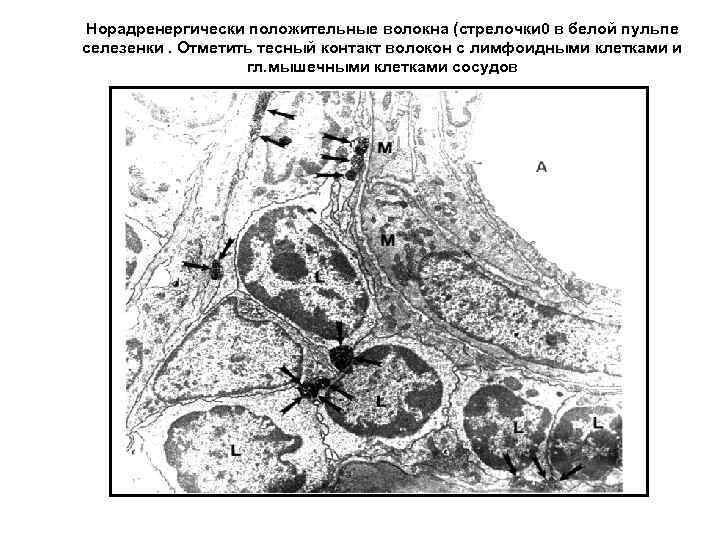
Норадренергически положительные волокна (стрелочки 0 в белой пульпе селезенки. Отметить тесный контакт волокон с лимфоидными клетками и гл. мышечными клетками сосудов
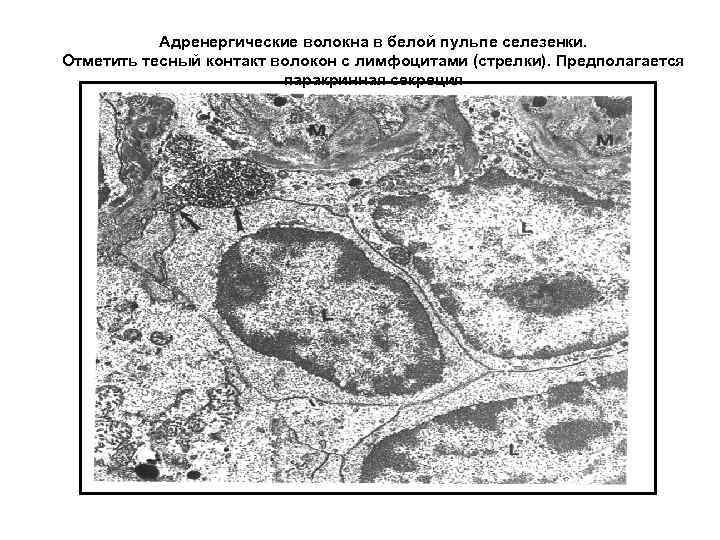
Адренергические волокна в белой пульпе селезенки. Отметить тесный контакт волокон с лимфоцитами (стрелки). Предполагается паракринная секреция
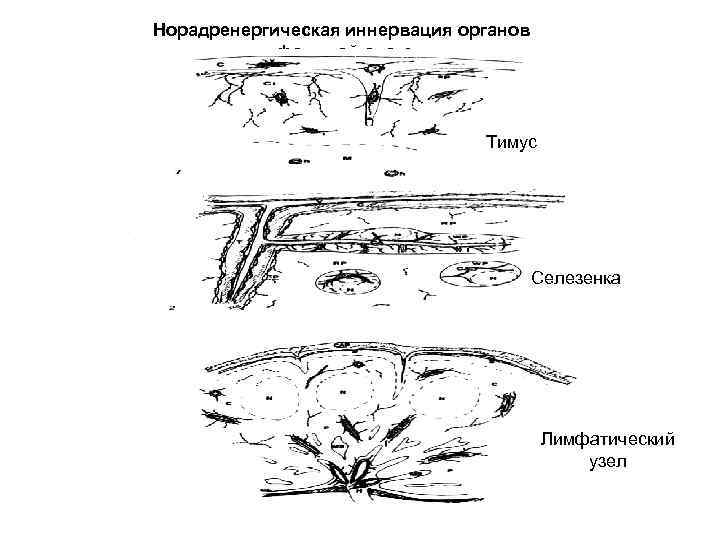
Норадренергическая иннервация органов лимфоидной системы Тимус Селезенка Лимфатический узел

Иннервация лимфатических узлов. Норадренергические волокна проникают в лимфатические узлы вдоль кровеносных сосудов, распределяясь затем, в основном, в мозговой зоне узла Часть нервных волокон проникает в кортикальную и паракортикальную зоны узла и только отдельные волокна проникают в паренхиму узла. Интересно, что в зоны реактивного центра лимфатических фолликулов волокна, как правило, не проникают. Электронномикроскопические исследования показали тесную связь адренергических окончаний с гл. мышечными клетками сосудов, ретикулярными клетками стромы, плазматическими клетками и лимфоцитами (как в селезенке). Парасимпатическая, холинэргическая иннервация лимфоузлов осуществляется через систему блуждающего нерва. Она изучена очень плохо Это связано, в частности с тем, что холинэргическую активность показывают многие тканевые элементы лимфоидной ткани и показать точно распределение холинэргических волокон внутри ткани узла очень трудно In contrast to the thymus and spleen, there is some neuroanatomical evidence that lymph nodes may receive a neural afferent supply
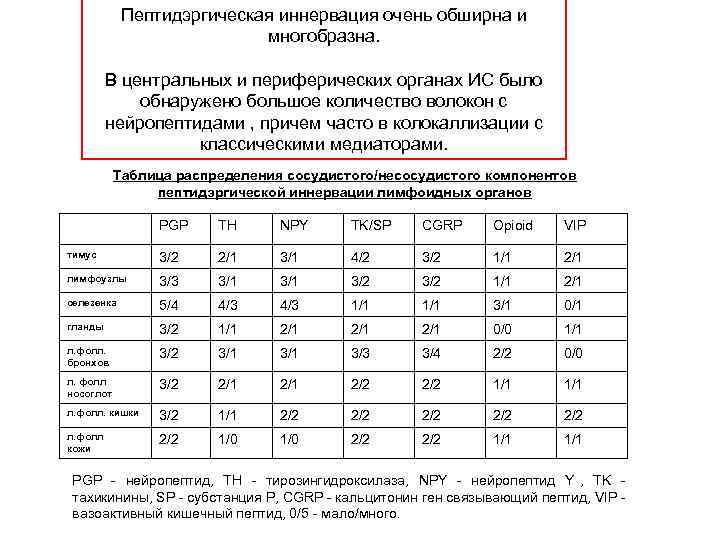
Пептидэргическая иннервация очень обширна и многобразна. В центральных и периферических органах ИС было обнаружено большое количество волокон с нейропептидами , причем часто в колокаллизации с классическими медиаторами. Таблица распределения сосудистого/несосудистого компонентов пептидэргической иннервации лимфоидных органов PGP TH NPY TK/SP CGRP Opioid VIP тимус 3/2 2/1 3/1 4/2 3/2 1/1 2/1 лимфоузлы 3/3 3/1 3/2 1/1 2/1 селезенка 5/4 4/3 1/1 3/1 0/1 гланды 3/2 1/1 2/1 2/1 0/0 1/1 л. фолл. 3/2 3/1 3/3 3/4 2/2 0/0 бронхов л. фолл 3/2 2/1 2/2 1/1 носоглот л. фолл. кишки 3/2 1/1 2/2 2/2 л. фолл 2/2 1/0 2/2 1/1 кожи PGP - нейропептид, TH - тирозингидроксилаза, NPY - нейропептид Y , TK - тахикинины, SP - субстанция Р, CGRP - кальцитонин ген связывающий пептид, VIP - вазоактивный кишечный пептид, 0/5 - мало/много.
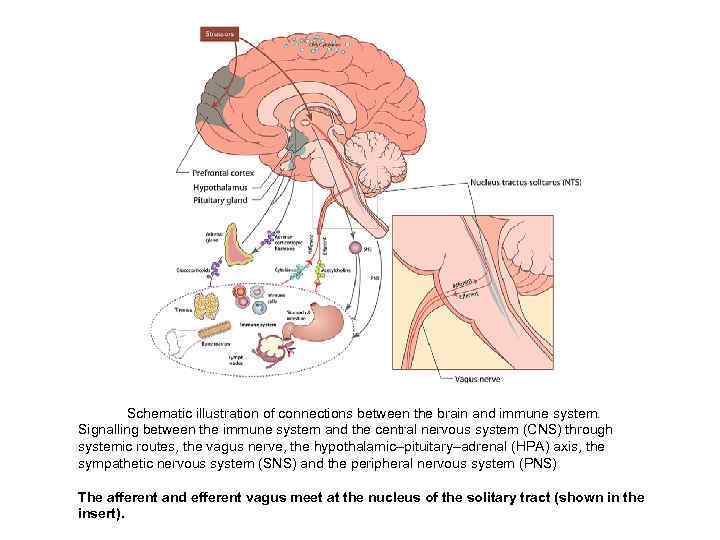
Schematic illustration of connections between the brain and immune system. Signalling between the immune system and the central nervous system (CNS) through systemic routes, the vagus nerve, the hypothalamic–pituitary–adrenal (HPA) axis, the sympathetic nervous system (SNS) and the peripheral nervous system (PNS) The afferent and efferent vagus meet at the nucleus of the solitary tract (shown in the insert).

ДОПАМИНЕРГИЧЕСКАЯ СИСТЕМА Где допамин нервной системы может взаимодействовать с иммунными клетками 1. Brain – Dopamine is produced in the brain. Since activated T cells regularly transmigrate into the CNS across the blood brain barrier (BBB), upon entry of such T cells into the brain they will most probably encounter dopamine. 2. The lymphoid organs – The secondary lymphoid tissues are highly innervated by sympathetic nerve fibers that store dopamine at high contents. Lymphocytes and other immune cells are capable of active synthesis and release of dopamine 3. Blood – Under physiological conditions dopamine is present in the plasma in relatively low conc. . Immune cells that are present regularly in the circulation will thus encounter dopamine at this low conc. In the blood yet not necessarily respond to it, since the optimal dopamine conc. for affecting immune cells is higher: ~10 8 M and above 4. In other dopamine-containing peripheral organs – Dopaminergic neurons innervate human peripheral tissues among them the kidney and the hepatic vasculature. Immune cells may enter such tissues and encounter dopamine in them.

Dopamine plays a very important role in the immune system and thus can be re-named a “Neuro- Immuno-Transmitter” since three major criteria are fulfilled: 1. Most, if not all, immune cells express DRs The most abundant are D 2 R, D 3 R, D 4 R and D 5 R, but some immune cells like Tregs, macrophages and microglia also express D 1 R. The DRs expression in immune cells is very sensitive to the activation state of the cell, and often modified sharply after antigenic or mitogenic stimulation. 2. Dopamine and/or to its selective agonists and antagonists induce direct and potent effects on immune cells, primarily T cells and dendritic cells (DC’s), resulting in either augmented or suppressed immune functions and features, depending on the context. 3. Many immune cells produce endogenous dopamine (~10 17– 10 20 M per cell, see Table 1. 1). The immune-derived dopamine may induce autocrine and paracrine immune effects. 4. Dopamine usually stimulates naı¨ve T cells. but inhibits activated T cells, i. e. T cells that havе already been activated by either antigen, mitogen, CD 3 and CD 28 antibodiescytokines etc. , or cells that are being activated simultaneously with dopamine and any of these otherstimuli 5 Activation of different DRs expressed in the same immune cell, or within a given immune cell population, often leads to very different effects. 6. Dopamine seems to activate naı¨ve Teffs mainly via the D 2 R and D 3 R, but suppress Tregs via the D 1 R. Dopamine-induced inhibition of Tregs is evident in many features and functions of тhese cells
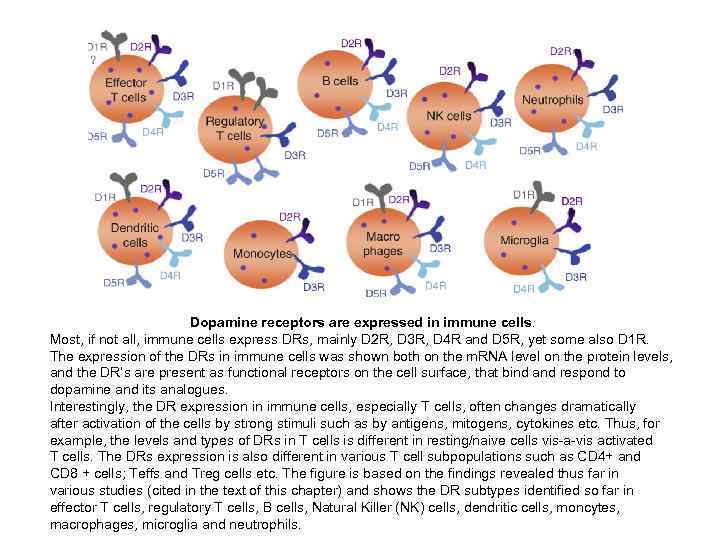
Dopamine receptors are expressed in immune cells. Most, if not all, immune cells express DRs, mainly D 2 R, D 3 R, D 4 R and D 5 R, yet some also D 1 R. The expression of the DRs in immune cells was shown both on the m. RNA level on the protein levels, and the DR’s are present as functional receptors on the cell surface, that bind and respond to dopamine and its analogues. Interestingly, the DR expression in immune cells, especially T cells, often changes dramatically after activation of the cells by strong stimuli such as by antigens, mitogens, cytokines etc. Thus, for example, the levels and types of DRs in T cells is different in resting/naive cells vis-a-vis activated T cells. The DRs expression is also different in various T cell subpopulations such as CD 4+ and CD 8 + cells; Teffs and Treg cells etc. The figure is based on the findings revealed thus far in various studies (cited in the text of this chapter) and shows the DR subtypes identified so far in effector T cells, regulatory T cells, B cells, Natural Killer (NK) cells, dendritic cells, moncytes, macrophages, microglia and neutrophils.
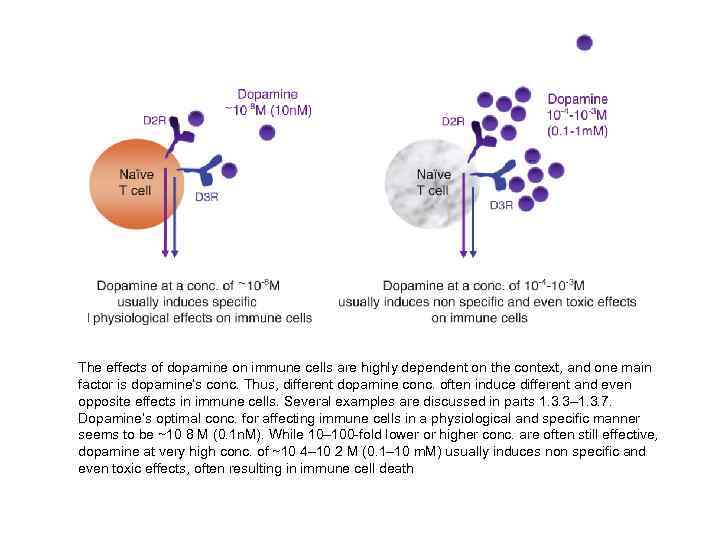
The effects of dopamine on immune cells are highly dependent on the context, and one main factor is dopamine’s conc. Thus, different dopamine conc. often induce different and even opposite effects in immune cells. Several examples are discussed in parts 1. 3. 3– 1. 3. 7. Dopamine’s optimal conc. for affecting immune cells in a physiological and specific manner seems to be ~10 8 M (0. 1 n. M). While 10– 100 -fold lower or higher conc. are often still effective, dopamine at very high conc. of ~10 4– 10 2 M (0. 1– 10 m. M) usually induces non specific and even toxic effects, often resulting in immune cell death
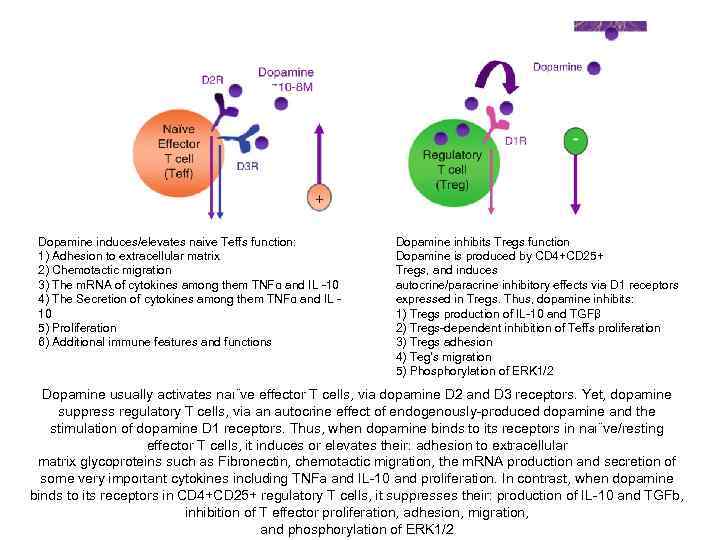
Dopamine induces/elevates naive Teffs function: Dopamine inhibits Tregs function 1) Adhesion to extracellular matrix Dopamine is produced by CD 4+CD 25+ 2) Chemotactic migration Tregs, and induces 3) The m. RNA of cytokines among them TNFα and IL -10 autocrine/paracrine inhibitory effects via D 1 receptors 4) The Secretion of cytokines among them TNFα and IL - expressed in Tregs. Thus, dopamine inhibits: 10 1) Tregs production of IL-10 and TGFβ 5) Proliferation 2) Tregs-dependent inhibition of Teffs proliferation 6) Additional immune features and functions 3) Tregs adhesion 4) Teg’s migration 5) Phosphorylation of ERK 1/2 Dopamine usually activates naı¨ve effector T cells, via dopamine D 2 and D 3 receptors. Yet, dopamine suppress regulatory T cells, via an autocrine effect of endogenously-produced dopamine and the stimulation of dopamine D 1 receptors. Thus, when dopamine binds to its receptors in naı¨ve/resting effector T cells, it induces or elevates their: adhesion to extracellular matrix glycoproteins such as Fibronectin, chemotactic migration, the m. RNA production and secretion of some very important cytokines including TNFa and IL-10 and proliferation. In contrast, when dopamine binds to its receptors in CD 4+CD 25+ regulatory T cells, it suppresses their: production of IL-10 and TGFb, inhibition of T effector proliferation, adhesion, migration, and phosphorylation of ERK 1/2
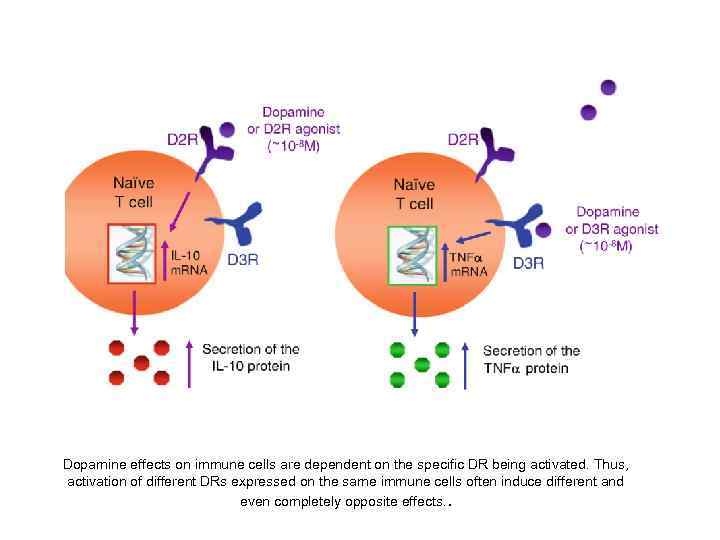
Dopamine effects on immune cells are dependent on the specific DR being activated. Thus, activation of different DRs expressed on the same immune cells often induce different and even completely opposite effects. .
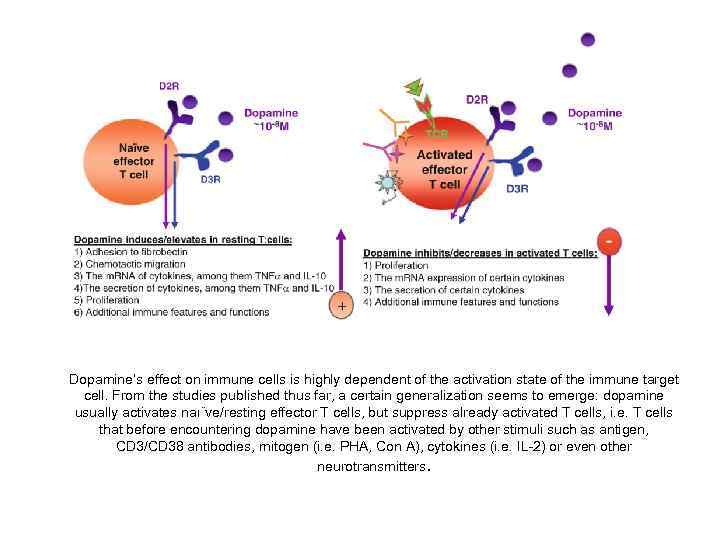
Dopamine’s effect on immune cells is highly dependent of the activation state of the immune target cell. From the studies published thus far, a certain generalization seems to emerge: dopamine usually activates naı¨ve/resting effector T cells, but suppress already activated T cells, i. e. T cells that before encountering dopamine have been activated by other stimuli such as antigen, CD 3/CD 38 antibodies, mitogen (i. e. PHA, Con A), cytokines (i. e. IL-2) or even other neurotransmitters.
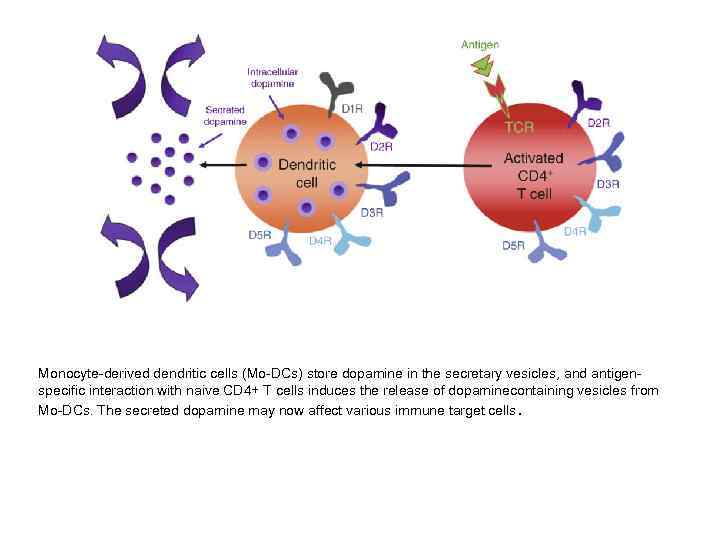
Monocyte-derived dendritic cells (Mo-DCs) store dopamine in the secretary vesicles, and antigen- specific interaction with naive CD 4+ T cells induces the release of dopaminecontaining vesicles from Mo-DCs. The secreted dopamine may now affect various immune target cells.
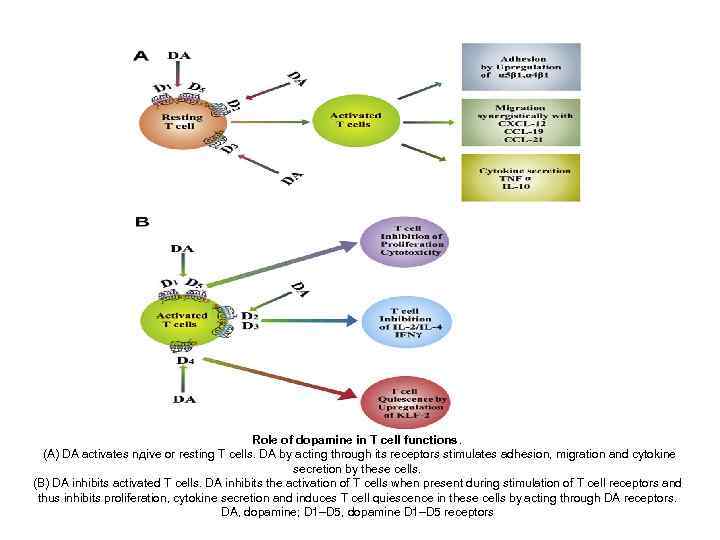
Role of dopamine in T cell functions. (A) DA activates nдive or resting T cells. DA by acting through its receptors stimulates adhesion, migration and cytokine secretion by these cells. (B) DA inhibits activated T cells. DA inhibits the activation of T cells when present during stimulation of T cell receptors and thus inhibits proliferation, cytokine secretion and induces T cell quiescence in these cells by acting through DA receptors. DA, dopamine; D 1–D 5, dopamine D 1–D 5 receptors
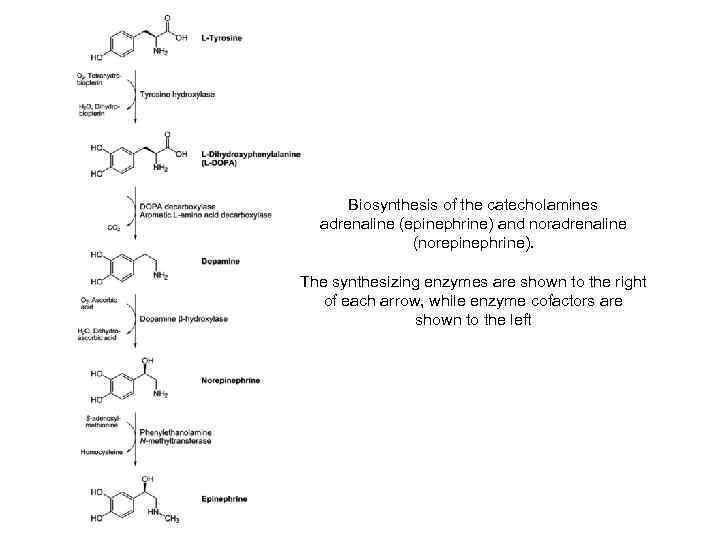
Biosynthesis of the catecholamines adrenaline (epinephrine) and noradrenaline (norepinephrine). The synthesizing enzymes are shown to the right of each arrow, while enzyme cofactors are shown to the left

Норадреналин (НА), выделяемый из варикозностей симпатических нервов, взаимодействует с а и β-адренорецепторами на мембранах Т-лимфоцитов, проявляя выраженный иммунорегуляторный эффект: Подавляет митотическую активность тимоцитов Повышает экспрессию дифференцировочных антигенов на мембране тимоцитов Подавляет активность комплемента и активность макрофагов при уничтожении вирус (герпес) - инфицированных клеток Симпатоэктомия приводила к ослаблению первичного иммунного ответа в селезенке при системной иммунизации Подавлялась активность Тк на аллогенные клетки и резко ослаблялись реакции гиперчувствительности В лимфатических узлах падала митотическая активность В-лимфоцитов Подавляли активность NK-лимфоцитов путем модификации рецепторов НК к клеткам мишеням и блокады секреции НК цитокинов, необходимых для их созревания и дифференцировки Агонисты НА подавляют активность НК клеток путем регуляции продукции перфоринов, гранзима В и интерферона –γ Центральное подавление синтеза катехоламинов путем введения ингибитора синтеза КА – 6 -гидроксидопамина (6 -OHDA) приводило у крыс через 7 дней подавление пролиферации лимфоцитов ККМ и селезенки.
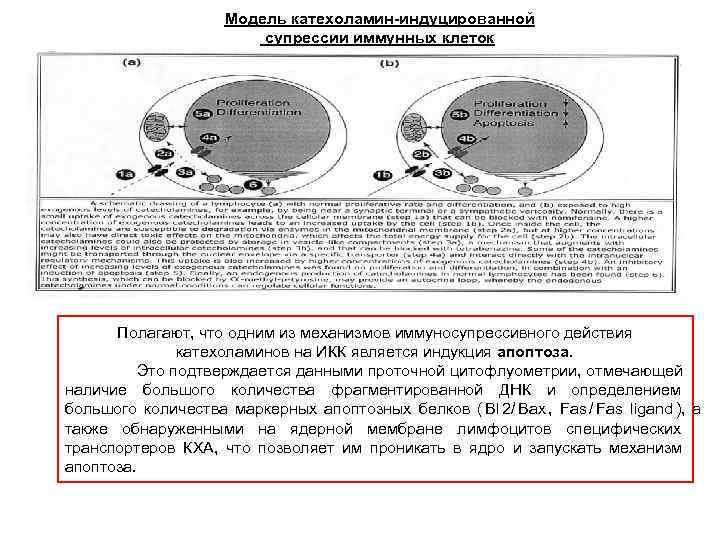
Модель катехоламин-индуцированной супрессии иммунных клеток Полагают, что одним из механизмов иммуносупрессивного действия катехоламинов на ИКК является индукция апоптоза. Это подтверждается данными проточной цитофлуометрии, отмечающей наличие большого количества фрагментированной ДНК и определением большого количества маркерных апоптозных белков ( Bl 2/ Bax , Fas / Fas ligand ), а также обнаруженными на ядерной мембране лимфоцитов специфических транспортеров КХА, что позволяет им проникать в ядро и запускать механизм апоптоза.
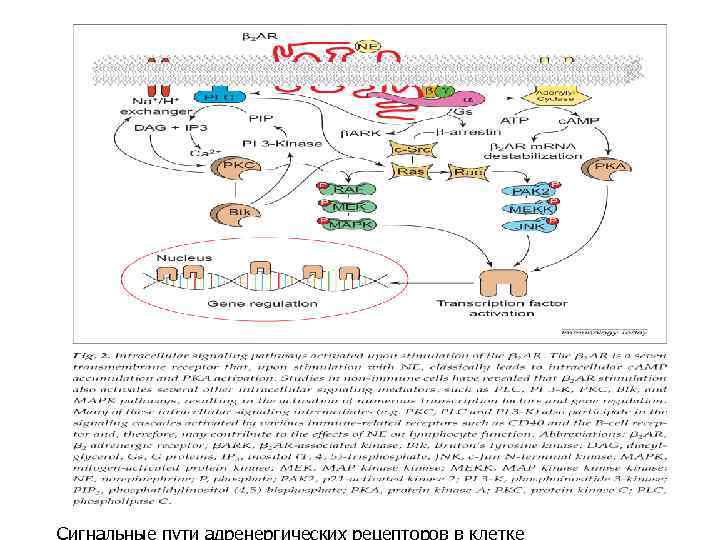
Сигнальные пути адренергических рецепторов в клетке
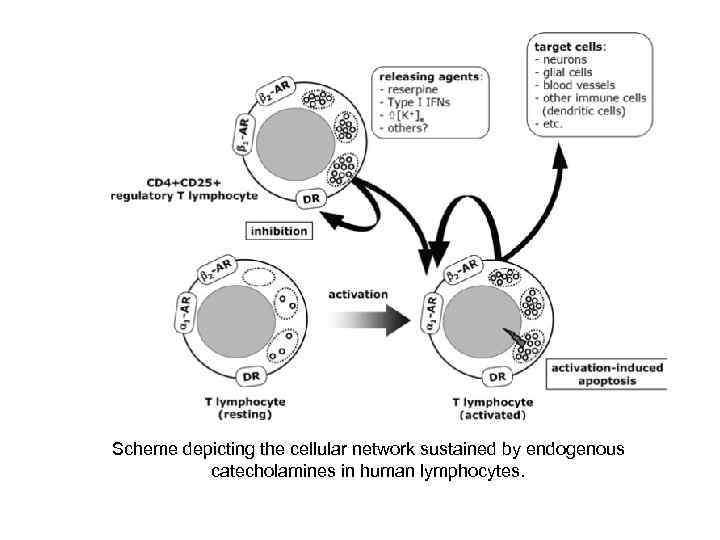
Scheme depicting the cellular network sustained by endogenous catecholamines in human lymphocytes.

Холинэргическая система На клетках иммунной системы обнаружены М и N холинорецепторы, что предполагает участие холинэргической (парасимпатической) системы в регуляции функций ИС. В целом действие холинэргической системы противоположно катехоламинэргической, но есть ряд важных моментов, которые надо учитывать: на разных популяциях ИКК отмечена разная плотность рецепторов на T лимфоцитах обнаружено присутствие обоих типов рецепторов к Ах Ах-система парасимпатических нервов (блуждающий нерв) подавляет воспалительный процесс Это действие получило наименование «холинэргический антивоспалительный путь» действие холинопрепаратов на разных этапах иммуногенеза различное блокирует активность эндотелиальных клеток и циркуляцию лимфоцитов во время воспаления Роль холинэргических факторов состоит главным образом в стимуляции пролиферации и дифференцировки лимфоцитов в начале иммунного ответа, причем это действие не прямое, а опосредованное через действие на холинорецепторы иммуносупрессоров.
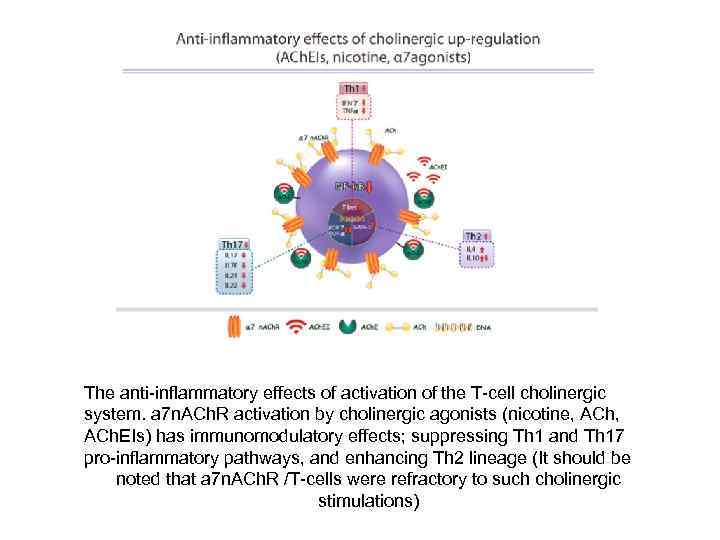
The anti-inflammatory effects of activation of the T-cell cholinergic system. a 7 n. ACh. R activation by cholinergic agonists (nicotine, ACh. EIs) has immunomodulatory effects; suppressing Th 1 and Th 17 pro-inflammatory pathways, and enhancing Th 2 lineage (It should be noted that a 7 n. ACh. R /T-cells were refractory to such cholinergic stimulations)
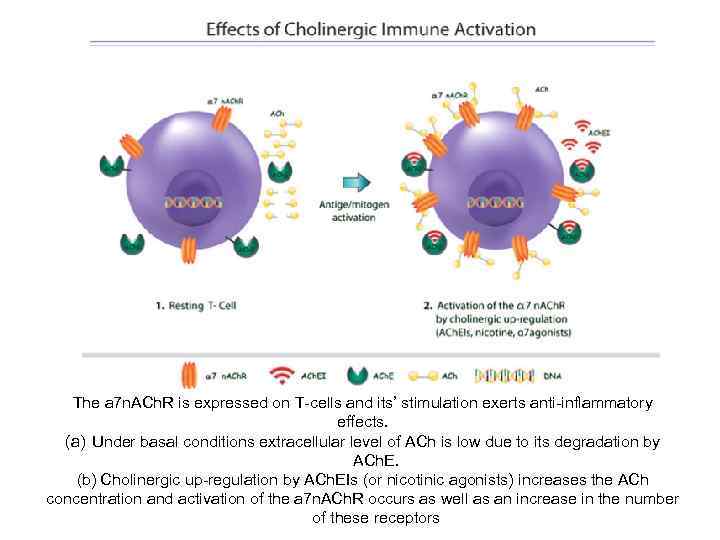
The a 7 n. ACh. R is expressed on T-cells and its’ stimulation exerts anti-inflammatory effects. (a) Under basal conditions extracellular level of ACh is low due to its degradation by ACh. E. (b) Cholinergic up-regulation by ACh. EIs (or nicotinic agonists) increases the ACh concentration and activation of the a 7 n. ACh. R occurs as well as an increase in the number of these receptors
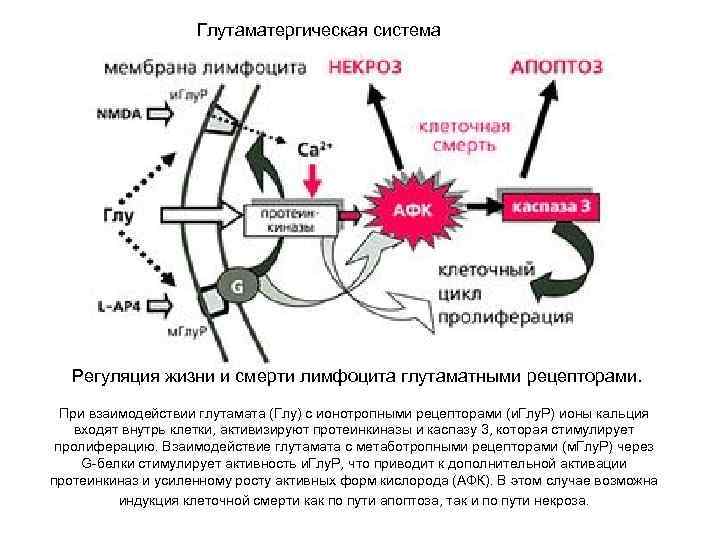
Глутаматергическая система Регуляция жизни и смерти лимфоцита глутаматными рецепторами. При взаимодействии глутамата (Глу) с ионотропными рецепторами (и. Глу. Р) ионы кальция входят внутрь клетки, активизируют протеинкиназы и каспазу 3, которая стимулирует пролиферацию. Взаимодействие глутамата с метаботропными рецепторами (м. Глу. Р) через G-белки стимулирует активность и. Глу. Р, что приводит к дополнительной активации протеинкиназ и усиленному росту активных форм кислорода (АФК). В этом случае возможна индукция клеточной смерти как по пути апоптоза, так и по пути некроза.
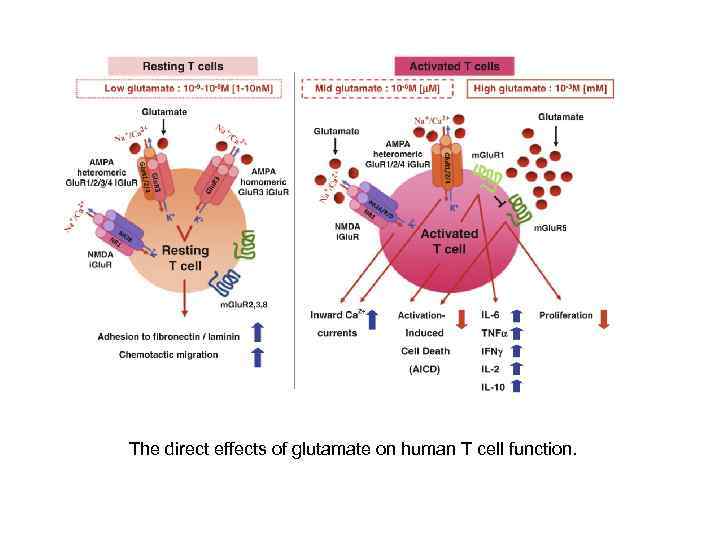
The direct effects of glutamate on human T cell function.

ГАМК-эргическая система. ГАМК - важный тормозный медиатор в нервной системе высших животных, контролирующий работу интернейронов в нервных центрах разного уровня (от вегетативных ганглиев, до коры головного мозга). Экспериментальные работы по действию агонистов ГАМК на ГАМК-рецепторы показали неоднозначность ее действия на модуляцию иммунного ответа. Во первых обнаружен дозо-зависимый эффект (при увеличении дозы происходит изменение иммунной реакции от стимуляции до угнетения). Действие ГАМК тесно связано с иммунным "фоном" - только при определенной активации иммунной системы проявляется эффект ГАМК и ее агонистов. Механизм активации или угнетения иммунной реакции осуществляется, по- видимому, не путем активации каждой клетки ИМС, а путем перераспределения ИКК, несущих определенную функцию между центральными и периферическими органами ИС
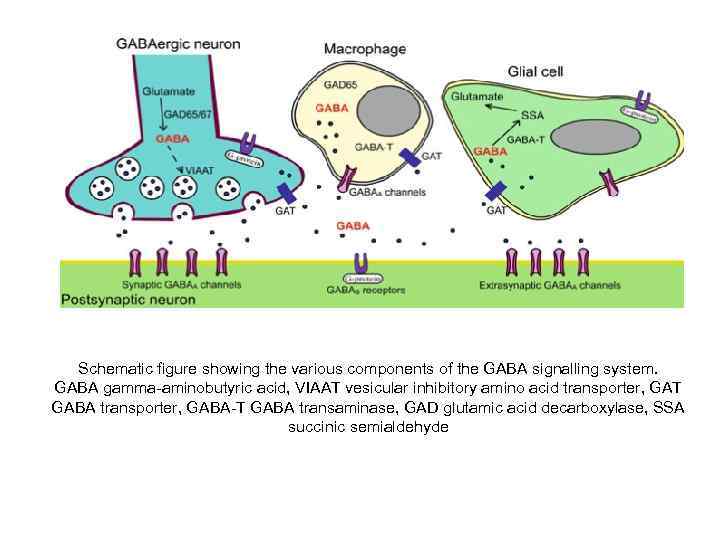
Schematic figure showing the various components of the GABA signalling system. GABA gamma-aminobutyric acid, VIAAT vesicular inhibitory amino acid transporter, GAT GABA transporter, GABA-T GABA transaminase, GAD glutamic acid decarboxylase, SSA succinic semialdehyde

Серотонинэргическая система Серотонинэргическая. В настоящее время накапливаются факты иммуносупрессивного действия серотонина и его аналогов на функции иммунной системы. Угнетение иммунного ответа серотонином было получено в отношении разных звеньев иммунной реакции: выработки АТ, числа эффекторных клеток, иммунологической памяти, времени латентного периода развития иммунной реакции (удлиняют). Интересно, что экспериментальное введение веществ, блокирующих синтез серотонина и снижающих его уровень - усиливает иммунный ответ. Показано, что повышение активности 5 -НТергической системы, достигнутое фармакологическими воздействиями на синтез, метаболизм и пост- или пре- синпатические рецепторы, приводит к иммуносупрессии, эффект реализуется через гипоталамо-гипофизарно-надпочечниковую систему. Психоэмоциональное напряжение прииммобилизационном или социальном стрессах, при которых наблюдается изменение нейро- химического паттерна мозга с преобладанием 5 -НТергической системы, также сопровождаются угнетением иммунного ответа. Отмечается сходство процессов клеточного перераспределения субпопуляций Т-лимфоцитов (CD 8+ и CD 4+) при повышении или снижении активности 5 -НТергической системы, полученное фармакологическим путем или экспериментальным моделированием подчиненного, депрессивно-подобного или агрессивного состояния. (Идова и др, 2008)

Для усиления/ослабления процесса психонейроиммуномодуляции наиболее важным представляется активность именно центральной 5 -НТергической системы. В этом случае происходит не локальное изменение функции одной или нескольких клеток, а генерализованное изменение иммунологической реактивности организма, что, главным образом, определяется перераспределением Т-лимфоцитов с различным фенотипом и включением в защитное реагирование и центральных, и периферических иммунокомпетентных органов Повышение активности 5 -НТергической системы, достигнутое фармакологическими воздействиями на синтез, метаболизм и пост- или пресинпатические рецепторы, приводит к иммуносупрессии, эффект реализуется через гипоталамо-гипофизарно-надпочечниковую систему. Психоэмоциональное напряжение при иммобилизационном или социальном стрессах, при которых наблюдается изменение нейрохимического паттерна мозга с преобладанием 5 -НТергической системы, также сопровождаются угнетением иммунного ответа. Отмечается сходство процессов клеточного перераспределения субпопуляций Т-лимфоцитов (CD 8+ и CD 4+) при повышении или снижении активности 5 -НТергической системы, полученное фармакологическим путем или экспериментальным моделированием подчиненного, депрессивно-подобного или агрессивного состояния.
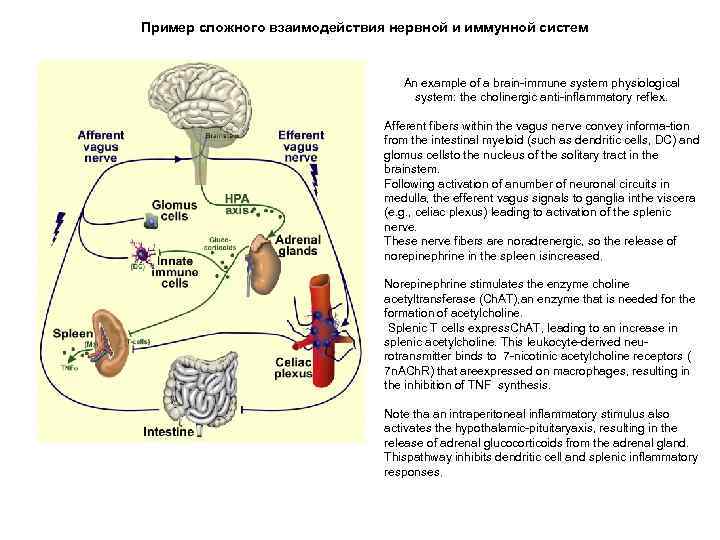
Пример сложного взаимодействия нервной и иммунной систем An example of a brain-immune system physiological system: the cholinergic anti-inflammatory reflex. Afferent fibers within the vagus nerve convey informa-tion from the intestinal myeloid (such as dendritic cells, DC) and glomus cellsto the nucleus of the solitary tract in the brainstem. Following activation of anumber of neuronal circuits in medulla, the efferent vagus signals to ganglia inthe viscera (e. g. , celiac plexus) leading to activation of the splenic nerve. These nerve fibers are noradrenergic, so the release of norepinephrine in the spleen isincreased. Norepinephrine stimulates the enzyme choline acetyltransferase (Ch. AT), an enzyme that is needed for the formation of acetylcholine. Splenic T cells express. Ch. AT, leading to an increase in splenic acetylcholine. This leukocyte-derived neu- rotransmitter binds to 7 -nicotinic acetylcholine receptors ( 7 n. ACh. R) that areexpressed on macrophages, resulting in the inhibition of TNF synthesis. Note tha an intraperitoneal inflammatory stimulus also activates the hypothalamic-pituitaryaxis, resulting in the release of adrenal glucocorticoids from the adrenal gland. Thispathway inhibits dendritic cell and splenic inflammatory responses.

Regulatory factors of the cytokine balance that affect the CNS functions. In “normal” healthy brain the pro-inflammatory cytokine expressionis low and the homeostasis is maintained by the counterregulatory effect of anti-inflmmatory cytokines. One of the most important survival factors isthe insulin-like growth factor-1 (IGF-1) that recruits and phosporylates the tyrosine residues of various cytosolic molecules and ultimately results inthe activation of phosphatydil-inositol-39 -kinase (PI 3 kinase). IGF-1 receptor also activates mitogen-activated kinase and the expression of transcriptionregulatory genes, for example, Fos and Jun. These regulatory events initiate further signaling mechanisms that play important roles in controlling cellgrowth, differentiation, and survival. Enhancements in nerve growth factor (NGF) synthesis are also neuroprotective. Neurotransmitters that increaseintracellular c. AMP level, the CREB phosphorylation, and the activation of the anti-apoptotic BCL-2 gene family shifts the balance also to the directionof protection and survival. Inflammation, ischemia, or other brain injuries enhance the production of pro- inflammatory cytokines and mediators, like. NO and other free radicals. In these pathological situations the SOSS signaling is interrupted, resulting in the activation of stress-activated protein

В целом анализ влияния нейромедиаторных препаратов на функции иммунокомпетентных (ИКК) клеток позволили выявить общую закономерность, касающуюся роли адрено- и холинэргических факторов в эффекторной фазе иммунного ответа 1. Популяции клеток эффекторов находятся под реципрокным влиянием адрено- и холинэргических стимулов благодаря наличию обоих видов рецепторов на мембранах клеток. 2. Наличие рецепторов на многих видах клеток иммунной системы говорит о том, что нейромедиаторы оказывают влияние на все звенья иммуного процесса 3. Нейромедиаторные факторы, как правило, действуют реципрокно. Адреноэргические стимулы, как правило, снижают функциональную активность ИКК, холинэргические стимулы - усиливают функции. 4. Разные звенья иммуногенеза обладают разной чувствительностью и направленностью по отношению действия одних и тех же нейромедиаторов Складывается впечатление, что адрено-влияния способствуют стимуляции иммуноцитопоэза и подавляют этапы эффекторного ответа, холино-влияния наоборот - стимулируют эффекторные ИКК и тормозит процессы иммуноцитопоэза 5. Способность самих клеток лимфоидной системы синтезировать и секретировать катехоламины вносит дополнительную сложность в схемы действия нейромедиаторов на иммунную систему, поскольку регуляторный эффект может быть вызван как экзогенными нейромедиаторами (нервной природы), так и эндогенными (синтезируемыми самими ИКК) по типу аутокринной или паракринной стимуляции

Центральные нервные механизмы, вовлеченные в нейро-иммунные взаимодействия
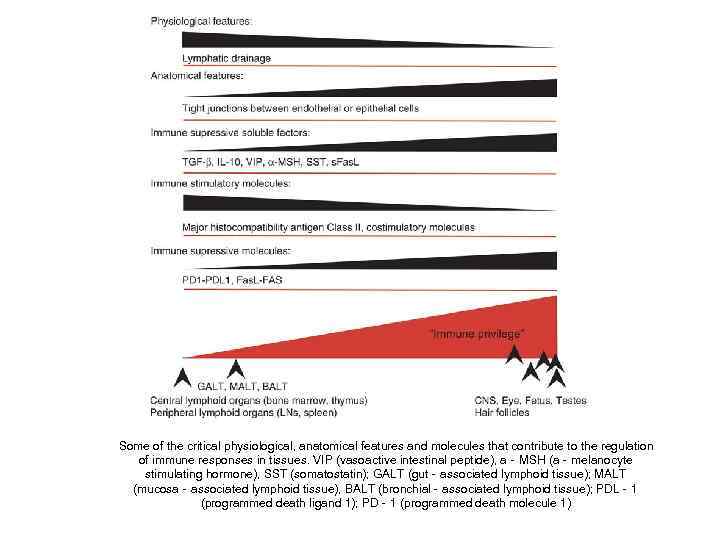
Some of the critical physiological, anatomical features and molecules that contribute to the regulation of immune responses in tissues. VIP (vasoactive intestinal peptide), a‐MSH (a‐melanocyte stimulating hormone), SST (somatostatin); GALT (gut‐associated lymphoid tissue); MALT (mucosa‐associated lymphoid tissue), BALT (bronchial‐associated lymphoid tissue); PDL‐ 1 (programmed death ligand 1); PD‐ 1 (programmed death molecule 1)
Лекция Медиаторы и имм клетки.ppt
- Количество слайдов: 40

