Курсовая работа на тему.pptx
- Количество слайдов: 24

Санкт-Петербургский Государственный Технологический Институт (Технический Университет) Курсовая работа на тему: Антибиотики макролиды Выполнила: Павлова Е. В. Проверил: Островский В. А.

Антибиотики (от др. -греч. ἀντί — против + βίος — жизнь) — вещества природного или полусинтетического происхождения, подавляющие рост живых клеток, чаще всего прокариотических или простейших По ГОСТ 21507 -81 (СТ СЭВ 1740 -79): Антибиотик — вещество микробного, животного или растительного происхождения, способное подавлять рост микроорганизмов или вызывать их гибель.

Спектр применения антибиотиков • Некоторые антибиотики оказывают сильное подавляющее действие на рост и размножение бактерий • Некоторые антибиотики используются в качестве цитостатических (противоопухолевых) препаратов при лечении онкологических заболеваний • Антибиотики не воздействуют на вирусы, и поэтому бесполезны при лечении заболеваний, вызываемых вирусами (например, грипп, гепатиты А, В, С, ветряная оспа, герпес, краснуха, корь).

Классификация антибиотиков по механизму действия • Ингибиторы синтеза клеточной стенки. • Ингибиторы синтеза белка на рибосомах. • Ингибиторы синтеза нуклеиновых кислот • Нарушающие функцию мембран клетки
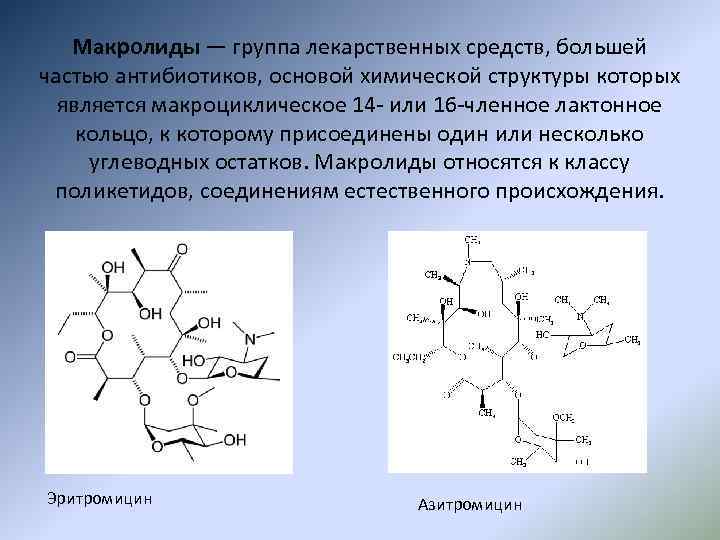
Макролиды — группа лекарственных средств, большей частью антибиотиков, основой химической структуры которых является макроциклическое 14 - или 16 -членное лактонное кольцо, к которому присоединены один или несколько углеводных остатков. Макролиды относятся к классу поликетидов, соединениям естественного происхождения. Эритромицин Азитромицин

МЕХАНИЗМ ДЕЙСТВИЯ МАКРОЛИДОВ Антимикробное действие макролидов обусловлено нарушением синтеза белка на этапе трансляции в клетках чувствительных микроорганизмов. Макролиды обратимо связываются с 50 S субъединицей рибосом. В результате приостанавливается процесс формирования и наращивания пептидной цепи. Связывание макролидов с 50 S-субъединицей возможно на любой стадии рибосомального цикла
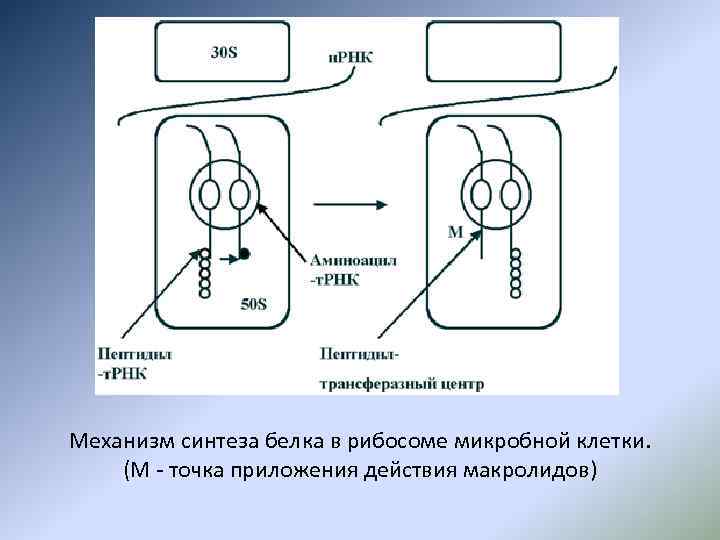
Механизм синтеза белка в рибосоме микробной клетки. (M - точка приложения действия макролидов)

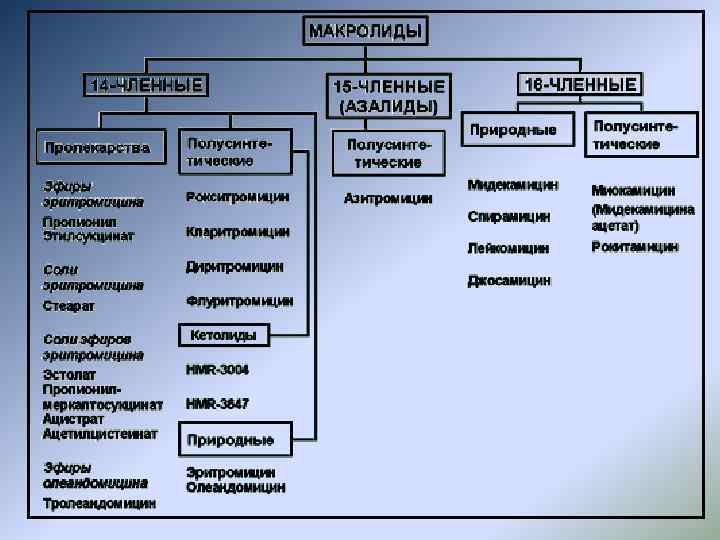
Классификация макролидов В настоящее время группа макролидов насчитывает более десяти различных антибиотиков. Все они имеют определенное структурное сходство с эритромицином, отличаясь от него по количеству атомов углерода в лактонном кольце и характеру боковых цепей. Макролиды можно классифицировать по химической структуре и по происхождению. Химическая классификация предполагает разделение препаратов на 3 группы, в зависимости от числа атомов углерода в лактонном кольце - 14 -, 15 - и 16 -членные, причем 15 -членные препараты правильнее называть не макролидами, а азалидами, так как в кольцо включен атом азота

Показания к применению макролидов Традиционные показания • Коклюш • Дифтерия • Скарлатина • Инфекции ВДП и ЛОР-органов (тонзиллофарингит, синусит, отит) • Инфекции НДП (особенно "атипичная" пневмония) • Инфекции кожи и мягких тканей, тяжелая угревая сыпь • Ородентальные инфекции (периодонтит, периостит) • Инфекции, передаваемые половым путем • Воспалительные заболевания органов малого таза (связанные с инфекцией) • Кишечные инфекции Профилактическое применение • Профилактика коклюша у контактных лиц • Профилактика дифтерии у контактных • Профилактика инфекционных осложнений при стоматологических процедурах Противопоказания • Беременность, период лактации • Гиперчувствительность • Тяжелая печеночная недостаточность
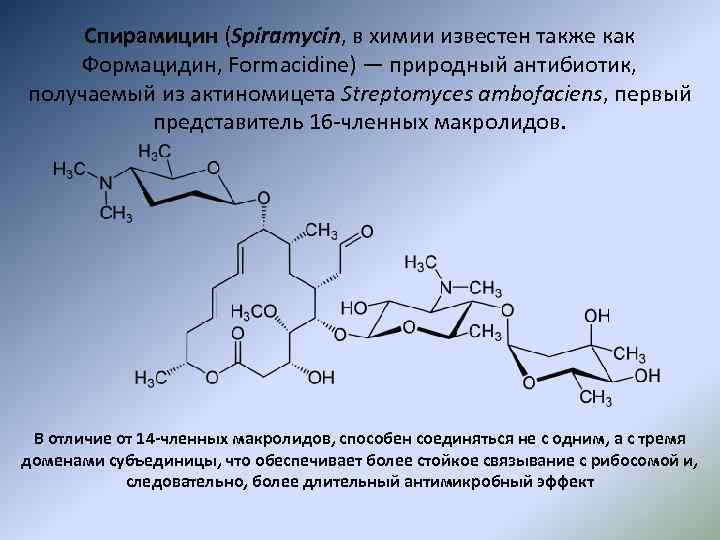
Спирамицин (Spiramycin, в химии известен также как Формацидин, Formacidine) — природный антибиотик, получаемый из актиномицета Streptomyces ambofaciens, первый представитель 16 -членных макролидов. В отличие от 14 -членных макролидов, способен соединяться не с одним, а с тремя доменами субъединицы, что обеспечивает более стойкое связывание с рибосомой и, следовательно, более длительный антимикробный эффект
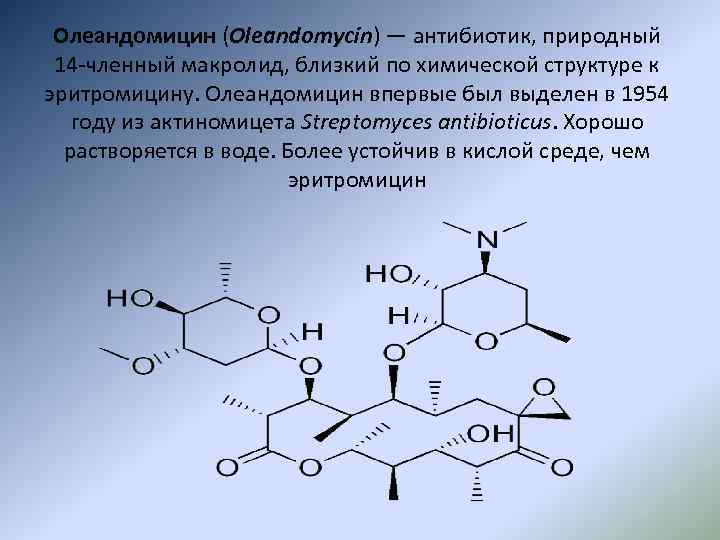
Олеандомицин (Oleandomycin) — антибиотик, природный 14 -членный макролид, близкий по химической структуре к эритромицину. Олеандомицин впервые был выделен в 1954 году из актиномицета Streptomyces antibioticus. Хорошо растворяется в воде. Более устойчив в кислой среде, чем эритромицин
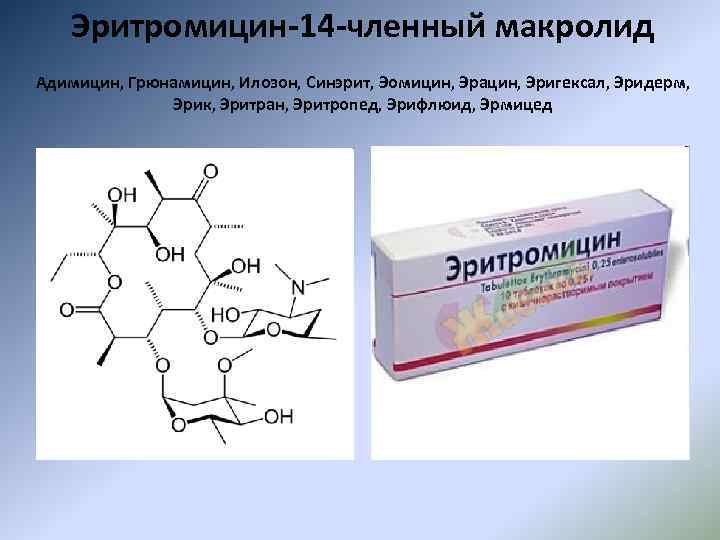
Эритромицин-14 -членный макролид Адимицин, Грюнамицин, Илозон, Синэрит, Эомицин, Эрацин, Эригексал, Эридерм, Эрик, Эритран, Эритропед, Эрифлюид, Эрмицед
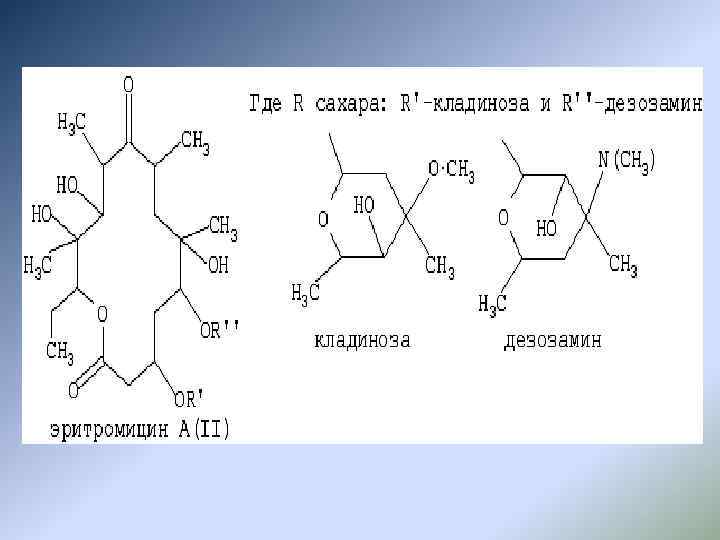

Рокситромицин (Roxithromycin) — антибиотик, первый полусинтетический 14 -членный макролид. Является производным эритромицина А, в химическом отношении представляет собой эритромицин-9 -О-2 -метоксиэтокси-метил оксим. Структурные особенности рокситромицина, отличающие его от эритромицина, придают ему более высокую кислотоустойчивость, улучшенные фармакокинетические и микробиологические параметры.
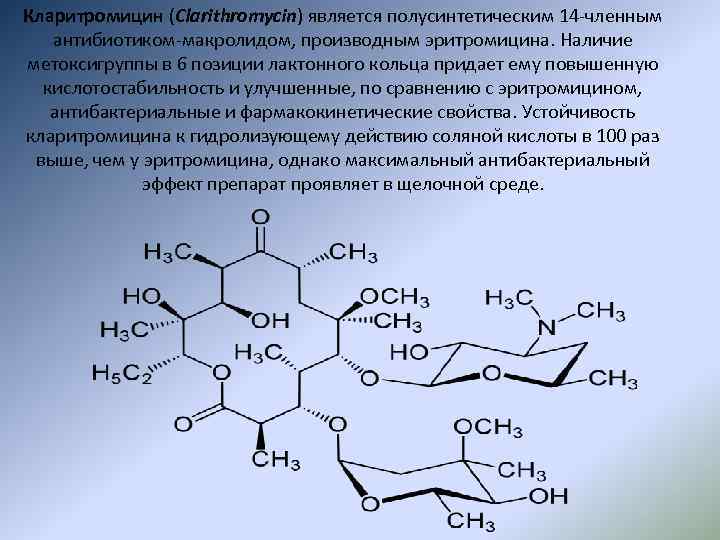
Кларитромицин (Clarithromycin) является полусинтетическим 14 -членным антибиотиком-макролидом, производным эритромицина. Наличие метоксигруппы в 6 позиции лактонного кольца придает ему повышенную кислотостабильность и улучшенные, по сравнению с эритромицином, антибактериальные и фармакокинетические свойства. Устойчивость кларитромицина к гидролизующему действию соляной кислоты в 100 раз выше, чем у эритромицина, однако максимальный антибактериальный эффект препарат проявляет в щелочной среде.
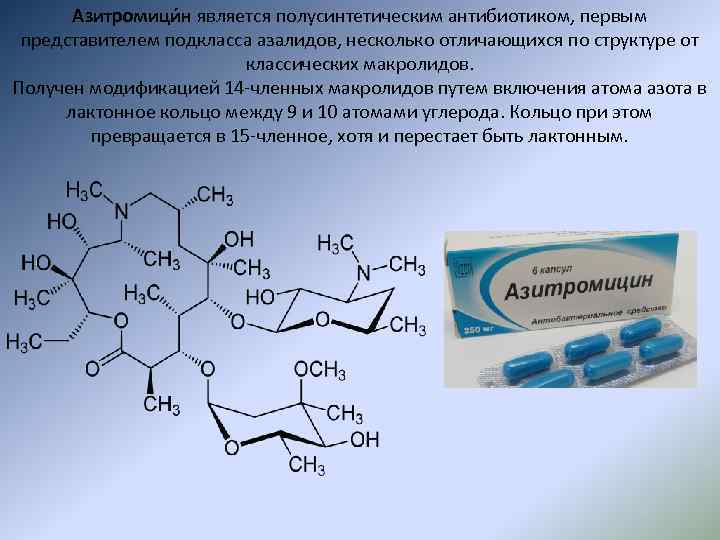
Азитромици н является полусинтетическим антибиотиком, первым представителем подкласса азалидов, несколько отличающихся по структуре от классических макролидов. Получен модификацией 14 -членных макролидов путем включения атома азота в лактонное кольцо между 9 и 10 атомами углерода. Кольцо при этом превращается в 15 -членное, хотя и перестает быть лактонным.

В 1981 г. исследовательская группа фармацевтичеcкой компании «PLIVA» (Хорватия) путем включения атома азота в 14 -членное лактонное кольцо эритромицина между 9 -м и 10 -м атомами углерода синтезировала новый антибиотик, отнесенный к группе полусинтетических 15 -членных макролидных антибиотиков — азалидов, — в которой азитромицин до настоящего времени остается единственным представителем. В 1988 г. по завершении многочисленных доклинических испытаний азитромицин был выведен на мировой фармацевтический рынок; в этом же году он под торговым названием «Сумамед» ® был зарегистрирован в нашей стране.
Получение азитромицина
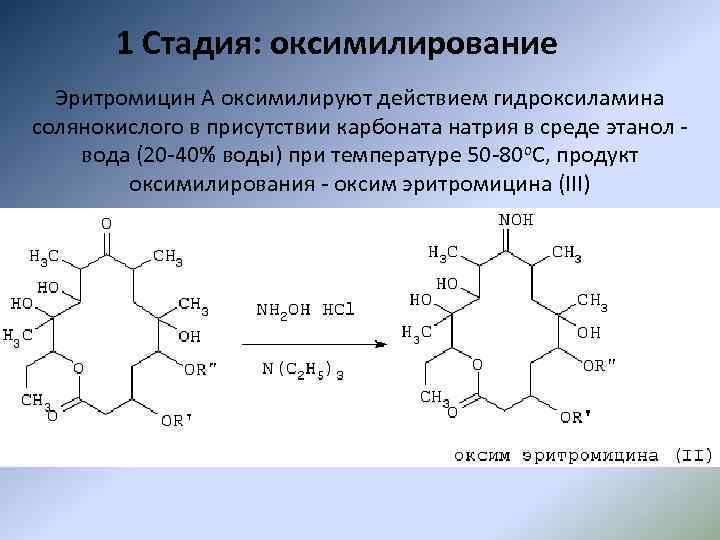
1 Стадия: оксимилирование Эритромицин А оксимилируют действием гидроксиламина солянокислого в присутствии карбоната натрия в среде этанол - вода (20 -40% воды) при температуре 50 -80 o. С, продукт оксимилирования - оксим эритромицина (III)
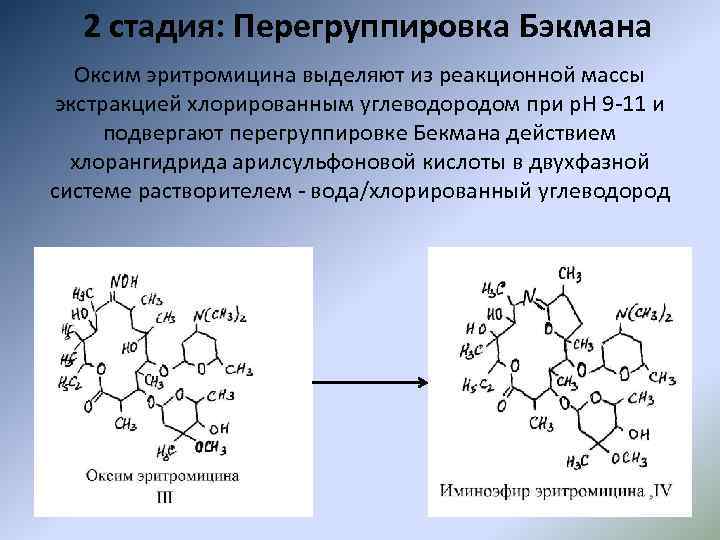
2 стадия: Перегруппировка Бэкмана Оксим эритромицина выделяют из реакционной массы экстракцией хлорированным углеводородом при р. Н 9 -11 и подвергают перегруппировке Бекмана действием хлорангидрида арилсульфоновой кислоты в двухфазной системе растворителем - вода/хлорированный углеводород
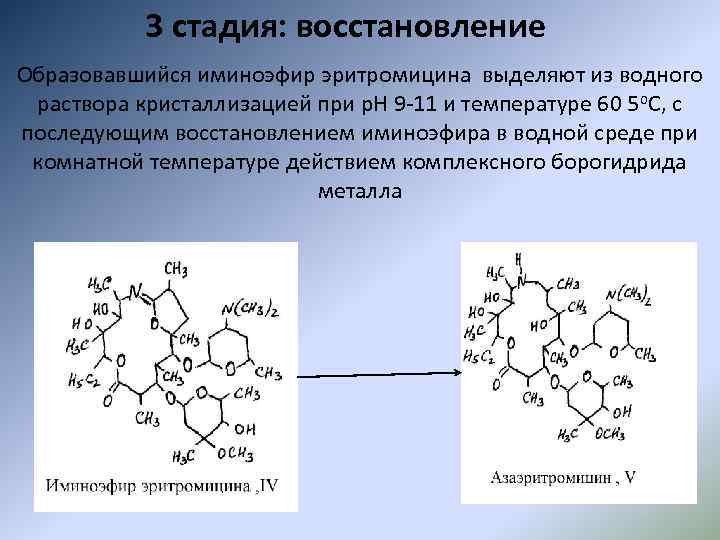
3 стадия: восстановление Образовавшийся иминоэфир эритромицина выделяют из водного раствора кристаллизацией при р. Н 9 -11 и температуре 60 5 o. C, с последующим восстановлением иминоэфира в водной среде при комнатной температуре действием комплексного борогидрида металла

4 стадия: метилирование Продукт восстановления 9 -аза-9 а-гомоэритромицин метилируют при кипячении в среде хлорированного углеводорода в присутствии муравьиной кислоты HCHO HCOOH 9 -деоксо-9 а-аза-9 а-гомоэритромицин А Азитромицин
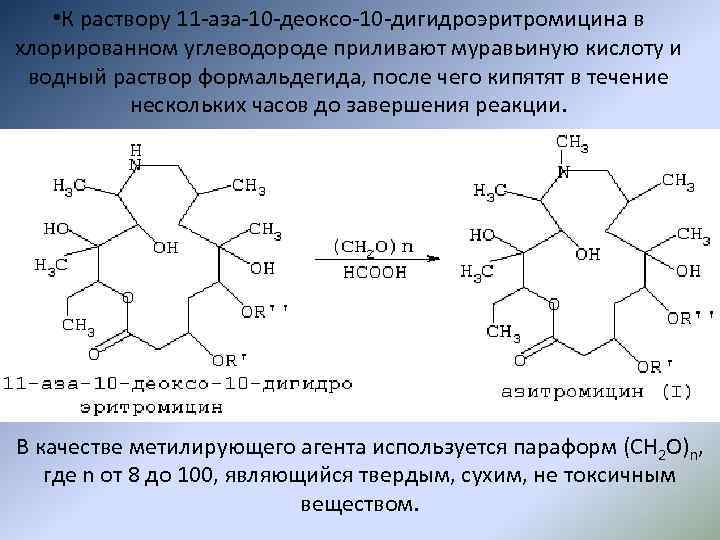
• К раствору 11 -аза-10 -деоксо-10 -дигидроэритромицина в хлорированном углеводороде приливают муравьиную кислоту и водный раствор формальдегида, после чего кипятят в течение нескольких часов до завершения реакции. В качестве метилирующего агента используется параформ (СН 2 O)n, где n от 8 до 100, являющийся твердым, сухим, не токсичным веществом.
Курсовая работа на тему.pptx