БИОФИЗИКА_1.ppt
- Количество слайдов: 164

Санкт-Петербургский Государственный Электротехнический Университет «ЛЭТИ» Кафедра БМЭ и ОС БИОФИЗИКА Анна Юрьевна Виллевальде 2012

Биофизика • • Цели и задачи Объект исследования (ОИ) • Методы 2

Биофизика (от др. -греч. βiοs — жизнь, др. -греч. φύσις — природа) • Раздел физики и современной биологии, изучающий физические аспекты существования живой природы на всех её уровнях, начиная от молекул и клеток и заканчивая биосферой в целом. • Наука о физических процессах, протекающих в биологических системах разного уровня организации и о влиянии на биологические объекты различных физических факторов. • Физика явлений жизни, изучаемых на всех уровнях, начиная с молекул и клеток и кончая биосферой в целом. • Наука о наиболее простых и фундаментальных взаимодействиях, лежащих в основе биологических явлений. 3
![Цели и задачи: познание явлений жизни [физическая закономерность vs физиологическая классификация] Физическая постановка задачи, Цели и задачи: познание явлений жизни [физическая закономерность vs физиологическая классификация] Физическая постановка задачи,](https://present5.com/presentation/-30032156_68401611/image-4.jpg)
Цели и задачи: познание явлений жизни [физическая закономерность vs физиологическая классификация] Физическая постановка задачи, относящейся к живой природе, т. е. задача формулируется, исходя из общих законов физики и атомномолекулярного строения вещества => • изучение особенностей функционирования физических законов на биологическом уровне организации вещества; • выявление связи между физическими механизмами, лежащими в основе организации живых объектов, и биологическими особенностями их жизнедеятельности; • нахождение общих принципов биологически значимых взаимодействий на молекулярном уровне, раскрытие их природы в соответствии с законами современной физики, химии с использованием новейших достижений математики и разработка на основе этого исходных обобщённых понятий, адекватных описываемым биологическим явлениям. 4

Физические методы исследования в биофизике: • не должны оказывать существенного влияния на исследуемые процессы; • по возможности не должны нарушать целостность исследуемой системы (vs биохимия); • достаточно чувствительные; • высокоточные; Методы физики часто не могут быть использованы для исследований БО (в своей первоначальной форме). => + к задачам: приспособление методов и методик физики для решения биологических задач. Применяют различные оптические методы, рентгеноструктурный анализ с использованием синхротронного излучения, ЯМРспектроскопию, различные электрометрические методы, микроэлектродную технику, методы хемилюминесценции, метод меченых атомов и др. 5

Моделирование – один из главных этапов биофизического исследования. БО, как правило, очень сложны и на протекающие в них процессы влияют многие факторы, которые часто зависят друг от друга => БО – сложная система, не всегда доступная для точного физического эксперимента. Модель – это такой материальный или мысленно представляемый объект, который в процессе исследования замещает объект-оригинал так, что его непосредственное изучение дает новые знания об объекте-оригинале. • Физическая; • Вербальная; • Математическая; • Информационная. Адекватность модели и оценка степени ее приближенности к оригиналу? Физика позволяет создать упрощенные модели объекта, которые описываются законами термодинамики, электродинамики, квантовой и классической механики. С помощью корреляции физических данных с биологическими можно получить более глубокое понимание процессов в исследуемом биологическом объекте. 6

Личности и даты связь с идеями и методами физики, химии, физической химии и математики; использование в исследовании БО точных экспериментальных методов => экспериментальные доказательства приложимости основных законов физики к БО От изучения физических свойств организмов и физических воздействий на них (свет, звук, электричество) к фундаментальным проблемам (наследственность и изменчивость, метаболизм, биоэнергетика) Луиджи Гальвани открыл биоэлектричество; Герман Гельмгольц замерил скорость нервных импульсов; Джеймс Максвелл разработал теорию цветного зрения; Ирвинг Ленгмюр разработал концепцию одномолекулярного органического покрытия (НП по химии 1932 г. ); Морис Уилкинс (+ Д. Уотсон и Ф. Крик) открыл трёхмерную молекулярную структуру ДНК (НП по физиологии и медицине 1962 г. ); Эрвин Шрёдингер, «Что такое жизнь с точки зрения физики» (1945) рассматривал важнейшие проблемы, такие как термодинамические основы жизни, общие структурные особенности живых организмов, соответствие биологических явлений законам квантовой механики и др. Дьёрдь фон Бекеши исследовал человеческое ухо (НП 1961 г. ); Макс Перуц и Джон Кендрю исследовали строение белков с помощью рентгеноструктурного анализа (НП по химии 1962 г. ); Эрнст Руска создал электронный микроскоп (НП по физике 1986 г. ); Герд Бинниг разработал сканирующий туннельный и сканирующий атомно-7 силовой микроскопы (НП по физике 1986 г. )

ОИ – живой организм Термодинамическое представление о жизни З начала термодинамики 1. Никакая энергия не возникает и не исчезает, а только переходит из одного вида в другой. 2. При переходе энергии из одного вида в другой часть ее превращается в тепловую и рассеивается. 3. Любой неживой открытой системе присущ переход энергии от более высокого уровня к более низкому (внутри неживой системы энтропия увеличивается). Закрытая система (изолированная система) – в которую извне не поступает энергия. Открытая система – частично или полностью восстанавливает свое состояние за счет энергии извне. 8

Энтропия (от греч. ἐντροπία — поворот, превращение) понятие, впервые введённое в термодинамике для определения меры необратимого рассеивания энергии, меры отклонения реального процесса от идеального. Определённая как сумма приведённых теплот, она является функцией состояния и остаётся постоянной при обратимых процессах, тогда как в необратимых — её изменение всегда положительно. Термин широко применяется и в других областях знания: в статистической физике — как мера вероятности осуществления какого-либо макроскопического состояния; в теории информации как мера неопределённости какого-либо опыта (испытания), который может иметь разные исходы. d. S=∂Q/T для обратимых процессов, где ∂Q - количество теплоты, T - абсолютная температура (273 К). Для всех необратимых процессов d. S> ∂Q/T. Энтропия системы в этих случаях всегда возрастает. Живая система стремится к упорядоченности (минимуму энтропии), снижает энтропию внутри себя, рассеивает снаружи. 9

Эрвин Бауэр: Жизнь – это открытая неравновесная (энтропически) система, которая поддерживает свое неравновесие путем обмена веществ (энергии и информации) оптимальным образом (с минимальными энергозатратами внутри системы). Гомеостазис – постоянство внутренней среды. ОИ – живой организм • открытая, саморегулирующаяся, самовоспроизводящаяся и развивающаяся гетерогенная система; • важнейшими функциональными веществами являются биополимеры – белки и нуклеиновые кислоты; • историческая система: является результатом филогенетического, эволюционного развития и сама проходит путь онтогенетического развития – от зиготы до старости и смерти. 10

Внешние функции жизни 1. Обмен веществ 2. Рост 3. Размножение 4. Раздражимость 5. Сократимость 1– 3 все живые существа, 4– 5 только животный мир 11

Особенности БО 1. 2. 3. 4. 5. 6. 7. 8. Непрерывный обмен с окружающей средой массой и энергией (открытая термодинамическая система) Наличие непрерывно изменяющегося комплекса множества факторов, воздействующих на живой организм, причем полный и точный учет самих факторов и результатов их воздействия невозможен, особую роль играют психофизические факторы Состояние БО описывается набором физиологических процессов, при этом сами процессы неоднозначно влияют на состояние организма, например, равновесие или норма может обеспечиваться при разных значениях определяющих параметров этих биологических процессов Сложность внутреннего функционирования и строения БО, а именно внутри каждой системы органов совместно и слажено работают разнородные системы с разными постоянными времени и качественно различными управляющими сигналами (электрическими, химическими, информационными и др. ) Существенная нелинейность биологических систем, например, реакция на сумму воздействий почти никогда не равна сумме реакций на каждое отдельное воздействие Различные патологические процессы, возникающие или проявляющиеся в различных подсистемах организма могут рефлекторно, особенно через высшие уровни управления, влиять на функцию и жизнедеятельность других систем Наличие большого уровня внутренних шумов требует статистической обработки информации или других способов выявления полезной информации Необходимость учета пространственных соотношений при протекании биохимических реакций и того, что часто в этих реакциях участвуют всего несколько молекул 12

Морфофункциональные уровни организма 0. Элементный уровень: биоэлементы или мономеры, для белков – аминокислоты, для сахаров – моносахара, для жиров – жирные кислоты и многоатомные спирты, для нуклеиновых кислот – нуклеотиды 1. Биополимеры (макромолекулы): белки, жиры, углеводы, нуклеиновые кислоты 2. Ансамбль макромолекул (субклеточный уровень): ядра и ядрышки, шероховатая эндоплазматическая сеть, митохондрии, лизосомы, гладкая эндоплазматическая сеть, клеточные включения 3. Клеточный уровень: клетки и питательная среда 4. Ткани 5. Органы 6. Системы органов 7. Организм 13

Основные разделы биофизики 1. Молекулярная биофизика 1. 1. Строение и физические свойства биологических макромолекул, главным образом белков и нуклеиновых кислот. 1. 2. Кинетика и термодинамика биологических процессов 2. Биофизика клетки 2. 1. Ультраструктура клетки, ее физические и физико-химические особенности, например, вязкость протоплазмы, поверхностное натяжение, давление внутри клетки и др. 2. 2. Физико-химические проявления функциональной активности клеток, а именно проницаемость мембран, биоэлектрические потенциалы, электрическое сопротивление клеток, транспорт веществ и др. характеристики 3. Биофизика органов чувств 3. 1. Молекулярные физико-химические механизмы рецепции (слуховой, зрительный и т. д. ) 3. 2. Трансформация энергии в рецепторных системах 3. 3. Кодирование информации в органах чувств 4. Биофизика сложных систем 4. 1. Регулирование и саморегулирование сложноустроенных многоклеточных систем 4. 2. Термодинамика и кинетические особенности этих систем (системы кровообращения и поддержания температуры) 4. 3. Экосистемы 5. Действие внешних факторов на клеточные структуры и организм в целом (ионизирующие излучения, электромагнитное поле и др. ) 14

Основы молекулярной биофизики Молекулярная биофизика изучает на основе методов и положений физики свойства и процессы в биологических молекулах и системах, которые ими образованы. 15

Особенности биологических молекул 1. 2. 3. 4. 5. Живая природа характеризуется единством химического строения. Основные вещества и основные химические механизмы едины во всей живой природе: все белки строятся из 20 аминокислот, все нуклеиновые кислоты – из 4 нуклеотидов, одни и те же атомные структуры фигурируют во всех организмах; однотипны и фундаментальные биохимические процессы. Разнообразие организмов определяется разнообразием сочетаний одних и тех же атомных групп и их взаимодействий. Биохимические процессы и биологические молекулы являются результатом эволюционного развития. Биологической эволюции предшествовала химическая, далее они были связаны неразрывно. Виды и организмы характеризуются биохимической, молекулярной адаптацией к условиям среды. Жизнь характеризуется точной и тонкой индивидуализацией: например, этиловый спирт вызывает опьянение, метиловый спирт – слепоту (различия между метильной и этильной группами). Биологические молекулы и макромолекулы имеют строго определенные состав и строение. Химические реакции в организмах строго регулируются как прямыми и обратными связями в многостадийных процессах метаболизма, так и пространственным разделением реакций вследствие компартментации, реализуемой клеточными и внутриклеточными мембранами. Поддерживаются тонкие концентрационные градиенты. Биологические молекулы построены из атомов легких элементов: С, Н, О, N, P, S. Кроме того, в организмах универсальна функциональность ионов щелочных и щёлочноземельных металлов Na, К, Са, Mg. Важнейшую роль играют малые количества других металлов – Fe, Zn и т. д. , вплоть до Мо. 16

Живые организмы неоднородны (гетерогенны). Органические соединения составляют 20– 30% массы клетки живого организма. К ним относятся: биологические полимеры – белки, нуклеиновые кислоты и углеводы, а также жиры и ряд небольших молекул – гормоны, пигменты, аминокислоты, простые сахара, нуклеотиды и т. д. Приблизительный элементный состав организма человека (в процентах к сухому весу) 17

Основные сложные органические биомолекулы, присутствующие в клетках и тканях Нуклеиновые кислоты, белки и полисахариды являются полимерами, которые построены из блоков. Липиды, вообще говоря, не являются биополимерами, и не во всех случаях в качестве их строительных блоков используются жирные кислоты. 18

Нормальный химический состав организма человека 19

Аминокислоты • строительный материал белков Белки могут содержать и другие компоненты, однако их трехмерная структура и, следовательно, их биологические свойства определяются в основном аминокислым составом, порядком чередования аминокислот в полипептидной цепи и их взаимным пространственным расположением. + функции: • некоторые аминокислоты участвуют в передаче нервных импульсов (глицин, глутаминовая кислота) • аминокислоты необходимо употреблять в пищу для поддержания роста в детстве и здоровья во взрослом состоянии, т. к. в результате метаболизма аминокислот образуются соединения, имеющие биомедицинское значение (например, амины – гистамин, аминомасляная кислота) 20
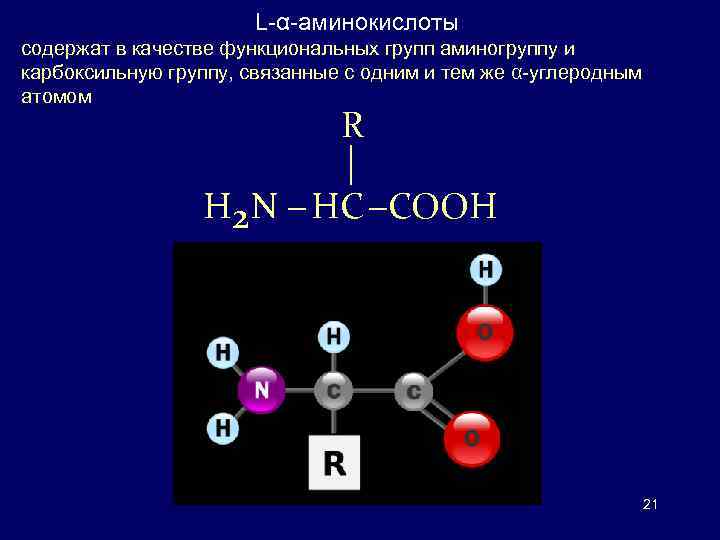
L-α-аминокислоты содержат в качестве функциональных групп аминогруппу и карбоксильную группу, связанные с одним и тем же α-углеродным атомом R H 2 N HC COOH 21

Некоторые физические и химические свойства аминокислот В природе: ок. 300 аминокислот, в белках – 20 из них. Одни и те же 20 аминокислот в белковых молекулах всех форм жизни: растений, животных и микроорганизмов. • Тетраэдрическая форма расположения атомов => оптическая активность: способность поворачивать плоскость поляризации плоскополяризованного света; правовращающие и левовращающие аминокислоты. • У всех аминокислот 4 группы, связанные с α-углеродным атомом, различны. Искл. глицин: R – атом водорода. • Аминокислоты несут по крайней мере 2 слабоионизируемые кислые группы. В растворе находятся в двух формах, заряженной и незаряженной, между которыми поддерживается протонное равновесие: R – COOH↔R – COOH- + H+ R – NH 3+↔R – NH 2 - + H+ Полный (суммарный) заряд аминокислоты зависит от p. H, т. е. от концентрации протонов в окружающем растворе. Значение p. H, при котором суммарный заряд аминокислоты равен нулю и поэтому она не перемещается в постоянном электрическом поле, – изоэлектрическая точка. 22

Некоторые физические и химические свойства аминокислот • 2 группы аминокислот, входящих в состав белков: с полярной или неполярной R-группой. • В аминокислотах – несколько заряженных групп => хорошо растворяются в полярных растворителях (вода, этанол) и не растворяются в неполярных (бензол, эфир). • Температура плавления высокая, > 200 о. С. Для разрыва ионных связей, стабилизирующих структуру кристалла, нужно сравнительно большое количество энергии. 23
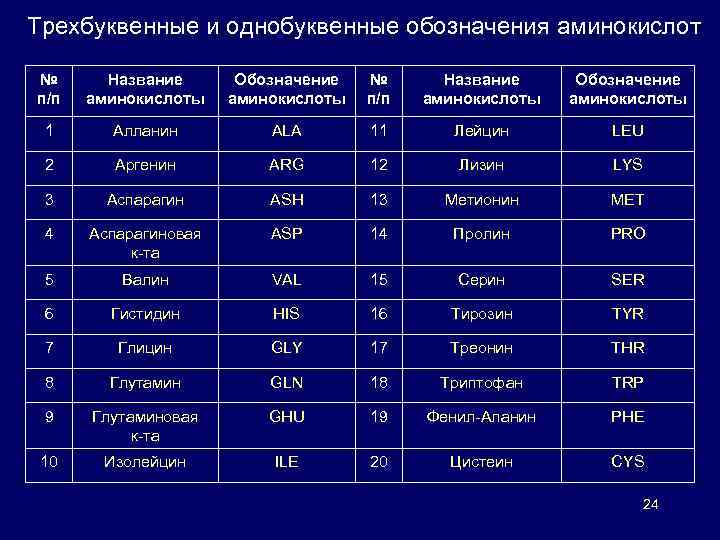
Трехбуквенные и однобуквенные обозначения аминокислот № п/п Название аминокислоты Обозначение аминокислоты 1 Алланин ALA 11 Лейцин LEU 2 Аргенин ARG 12 Лизин LYS 3 Аспарагин ASH 13 Метионин MET 4 Аспарагиновая к-та ASP 14 Пролин PRO 5 Валин VAL 15 Серин SER 6 Гистидин HIS 16 Тирозин TYR 7 Глицин GLY 17 Треонин THR 8 Глутамин GLN 18 Триптофан TRP 9 Глутаминовая к-та GHU 19 Фенил-Аланин PHE 10 Изолейцин ILE 20 Цистеин CYS 24
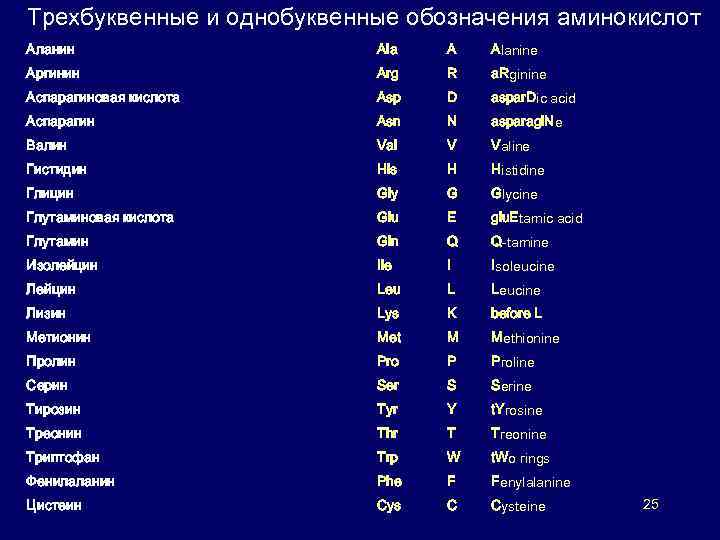
Трехбуквенные и однобуквенные обозначения аминокислот Аланин Ala A Alanine Аргинин Arg R a. Rginine Аспарагиновая кислота Asp D aspar. Dic acid Аспарагин Asn N asparagi. Ne Валин Val V Valine Гистидин His H Histidine Глицин Gly G Glycine Глутаминовая кислота Glu E glu. Etamic acid Глутамин Gln Q Q-tamine Изолейцин Ile I Isoleucine Лейцин Leu L Leucine Лизин Lys K before L Метионин Met M Methionine Пролин Pro P Proline Серин Ser S Serine Тирозин Tyr Y t. Yrosine Треонин Thr T Treonine Триптофан Trp W t. Wo rings Фенилаланин Phe F Fenylalanine Цистеин Cys C Cysteine 25
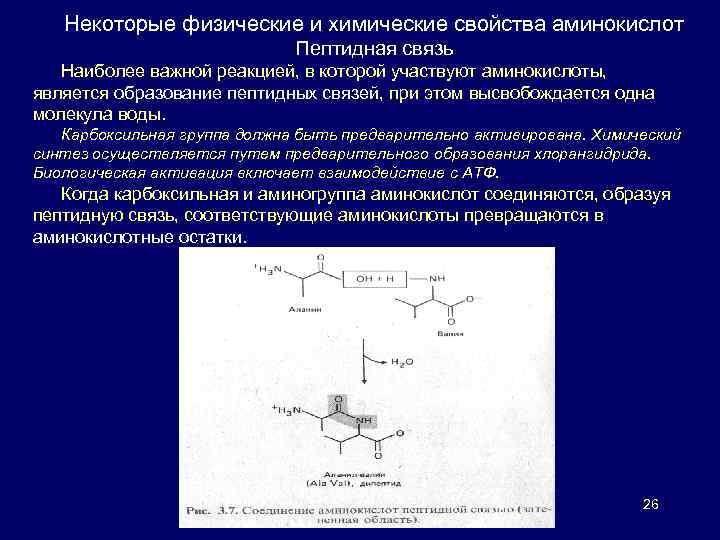
Некоторые физические и химические свойства аминокислот Пептидная связь Наиболее важной реакцией, в которой участвуют аминокислоты, является образование пептидных связей, при этом высвобождается одна молекула воды. Карбоксильная группа должна быть предварительно активирована. Химический синтез осуществляется путем предварительного образования хлорангидрида. Биологическая активация включает взаимодействие с АТФ. Когда карбоксильная и аминогруппа аминокислот соединяются, образуя пептидную связь, соответствующие аминокислоты превращаются в аминокислотные остатки. 26
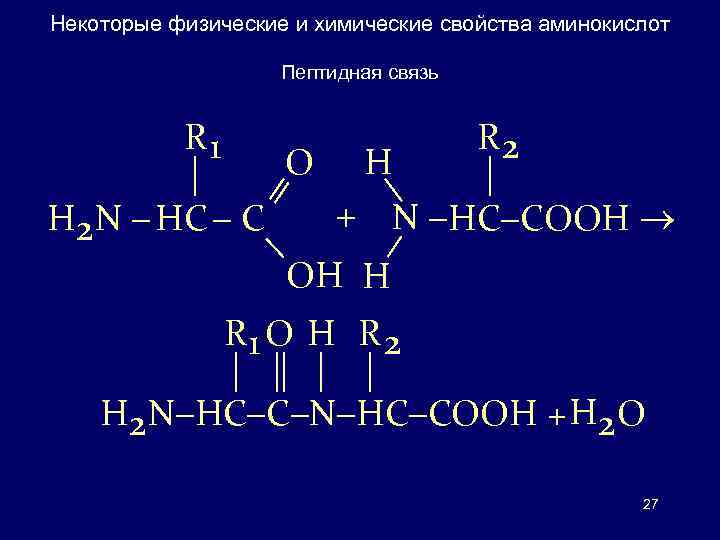
Некоторые физические и химические свойства аминокислот Пептидная связь R 2 R 1 O H + N HC COOH H 2 N HC C OH H R 1 O H R 2 H 2 N HC COOH + H 2 O 27

Пептиды Пептид состоит из двух или более аминокислотных остатков, связанных пептидными связями. Пептиды из более чем 10 аминокислот называются полипептидами. Трипептид содержит 3 остатка, но не 3 пептидные связи. Изображение: N-концевой остаток (со свободной α-аминогруппой) слева, C-концевой остаток (со свободной α -карбоксильной группой) Линейная последовательность аминокислотных остатков в полипептидной цепи – первичная структура пептида: число, химическая структура и порядок расположения аминокислотных остатков (обозначения аминокислот) Роль: многие важнейшие гормоны, например, инсулин; антибиотики. Замена всего одной аминокислоты на другую в линейной последовательности из 100 и более аминокислот может привести к снижению или полной потере биологической активности пептида, наследуемые 28 нарушения метаболизма (серповидноклеточная анемия).

Белки Все белки являются высокомолекулярными полипептидами. Условная граница между крупными полипептидами и белками – молекулярная масса 8000– 10 000. Простые белки содержат только аминокислоты, сложные – еще и неаминокислотные компоненты: производные витаминов, липидные или углеводные. Простые белки = белки Значение: Играют центральную роль в процессах жизнедеятельности клетки (например, ферменты) и в формировании клеточных структур. Анализ содержания в крови (заболевания печени – относительное содержание альбуминов и глобулинов; иммуноглобулины) и моче (в норме не содержит белка). 29

Классификация белков, основанная на их растворимости 30

Функции белков • Строительная функция: белки участвуют в образовании всех клеточных мембран в органоидах клетки и внеклеточных структур. • Каталитическая функция (от греч. katalysis – разрушение): все биологические катализаторы – ферменты – вещества белковой природы. Они ускоряют химические реакции, протекающие в клетке. Фермент катализирует только одну реакцию, т. е. он специфичен. Высокая специфичность ферментативных реакций обусловлена тем, что пространственная конфигурация активного центра фермента, т. е. участка белка, который связывает какую-либо молекулу, точно соответствует конфигурации этой молекулы. • Двигательная функция организма обеспечивается сократительными белками. Эти белки участвуют во всех видах движения, к которым способны клетки и организмы: мерцание ресничек и биение жгутиков у простейших, сокращение мышц у животных. • Транспортная функция белков заключается в присоединении химических элементов (например, кислорода) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела. • При поступлении в организм чужеродных белков или микроорганизмов в белых кровяных тельцах – лейкоцитах – образуются особые белки – антитела. Они связывают и обезвреживают несвойственные организму вещества. В этом выражается защитная функция белков. • Белки служат и одним из источников энергии в клетке, т. е. выполняют энергетическую функцию. При полном расщеплении 1 г белка выделяется 31 17, 6 к. Дж энергии.

Классификация белков в соответствии с их функцией 32

Взаимодействия атомов в биологических молекулах Сильные: ковалентные связи, образуются внешними оболочками атомов, например, С-С 348, 6 к. Дж/моль; С-N 336 к. Дж/моль. Слабые: ок. 10 к Дж/моль • ионные (Кулоновские силы, заряд иона) • ион-дипольные (Кулоновские силы, заряд иона, дипольный момент) • дипольные (ориентационные, Кулоновские силы, дипольный момент) • индукционные (индуцированный дипольный момент) • дисперсионные (квантовомеханические, взаимодействие электронных оболочек, мгновенные диполи, молекулы H 2 O, CO 2) 4– 9 к. Дж/моль • водородные (донорно-акцепторные, создаются атомами водорода O-H, N-H) • гидрофобные (отталкивание между неполярной атомной группой и водой) 33
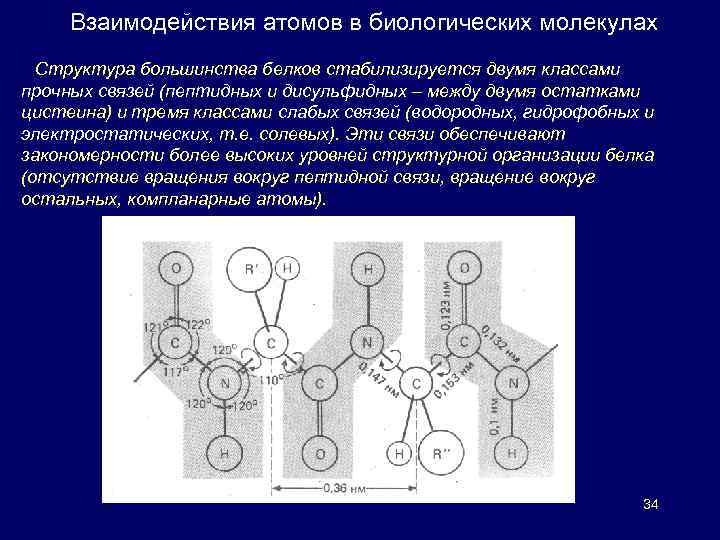
Взаимодействия атомов в биологических молекулах Структура большинства белков стабилизируется двумя классами прочных связей (пептидных и дисульфидных – между двумя остатками цистеина) и тремя классами слабых связей (водородных, гидрофобных и электростатических, т. е. солевых). Эти связи обеспечивают закономерности более высоких уровней структурной организации белка (отсутствие вращения вокруг пептидной связи, вращение вокруг остальных, компланарные атомы). 34

Конформации полипептидов Упорядоченные: α-Спираль: Высокоупорядоченная конформация, стабилизируемая водородными связями между пептидными группами; образуется самопроизвольно, является наиболее устойчивой, отвечает минимуму свободной энергии. Складчатый β-слой: образование водородных связей между NH- и COгруппами соседних цепей (но более удаленных вдоль цепи). Неупорядоченная конформация (клубок): не относятся ни к спиральным, ни к складчатым структурам, но столь же важные с точки зрения биологической функции. 35
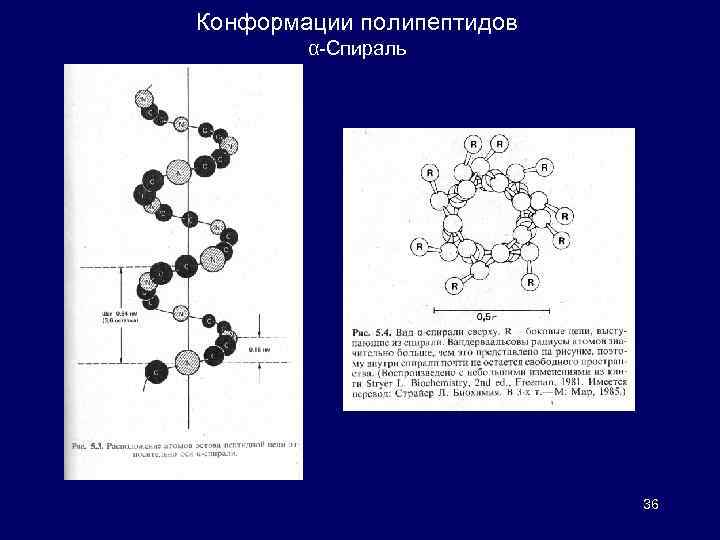
Конформации полипептидов α-Спираль 36

Конформации полипептидов Складчатый β-слой 37

Уровни структурной организации белка Первичная структура – последовательность аминокислот полипептидной цепи (цепей) и положение дисульфидных связей, если они имеются; Вторичная структура – стерические взаимосвязи между расположенными близко к другу вдоль цепи аминокислотами: -спираль, -слой, неупорядоченная конформация; Третичная структура – общее расположение, взаимная укладка различных областей, нет четкой границы с вторичной, но под третичной понимают стерические взаимосвязи между аминокислотными остатками, далеко отстоящими друг от друга по цепи; Четвертичная структура – если белки состоят из двух и более полипептидных цепей, связанных между собой нековалентными (не пептидными и не дисульфидными) связями, то они обладают четвертичной структурой; стабилизируются водородными связями и электростаическими взаимодействиями между остатками – олигомеры (составялющие – протомеры, мономеры, субъединицы) Вторичная и третичная структуры белка формируются самопроизвольно и определяются первичной структурой полипептидной цепи, т. е. первичная структура специфически определяет конформацию белка. Формируется 38 термодинамически наиболее устойчивая структура в данных условиях.

Денатурация белка Денатурация – разупорядочивание конформации полипептидной цепи без разрушения ее первичной структуры; утрата белковой молекулой структурной организации. Сравнительно слабые связи, ответственные за формирование вторичной, третичной и четвертичной структуры белка, легко разрушаются, что приводит к потере его биологической активности. • • Факторы: Изменение температуры; Обезвоживание; Резкое изменение p. H среды; Рентгеновское излучение; и др. 39

Нуклеотиды присутствуют во всех без исключения живых клетках, выполняя ряд ключевых функций. Пуриновые и пиримидиновые нуклеотиды – мономеры-предшественники (рибозо- и дезоксирибозонуклеозидмонофосфатные звенья) при биосинтезе нуклеиновых кислот РНК и ДНК. + перенос энергии (АТФ), образование коферментов, участие в роли акцепторов в окислительном фосфорилировании и др. ; синтетические аналоги природных нуклеотидов, способные замещать их в структуре нуклеиновых кислот и оказывать ингибирующее действие на синтез РНК и ДНК, находят применение в химиотерапии рака. Исходные структурные элементы молекул нуклеозидов и нуклеотидов – гетероциклические основания: производные пурина и пиримидина. Главные пиримидиновые основания: цитозин, тимин и урацил; из пуриновых оснований чаще всего встречаются аденин и гуанин. 40
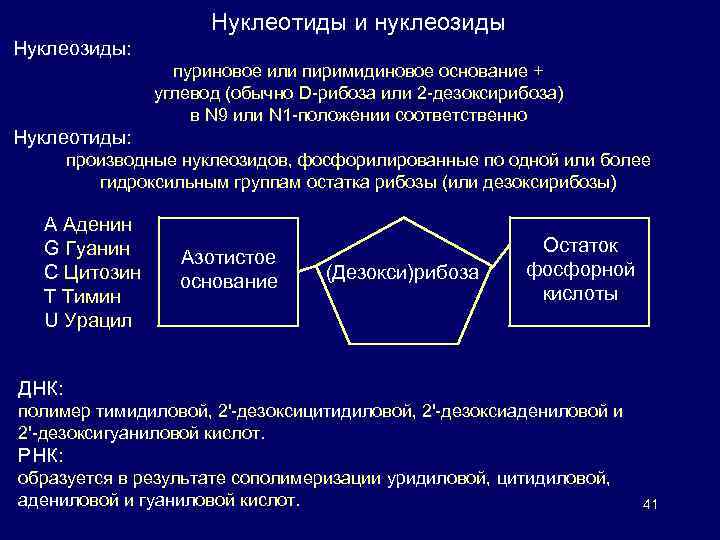
Нуклеотиды и нуклеозиды Нуклеозиды: пуриновое или пиримидиновое основание + углевод (обычно D-рибоза или 2 -дезоксирибоза) в N 9 или N 1 -положении соответственно Нуклеотиды: производные нуклеозидов, фосфорилированные по одной или более гидроксильным группам остатка рибозы (или дезоксирибозы) A Аденин G Гуанин С Цитозин Т Тимин U Урацил Азотистое основание (Дезокси)рибоза Остаток фосфорной кислоты ДНК: полимер тимидиловой, 2'-дезоксицитидиловой, 2'-дезоксиадениловой и 2'-дезоксигуаниловой кислот. РНК: образуется в результате сополимеризации уридиловой, цитидиловой, адениловой и гуаниловой кислот. 41
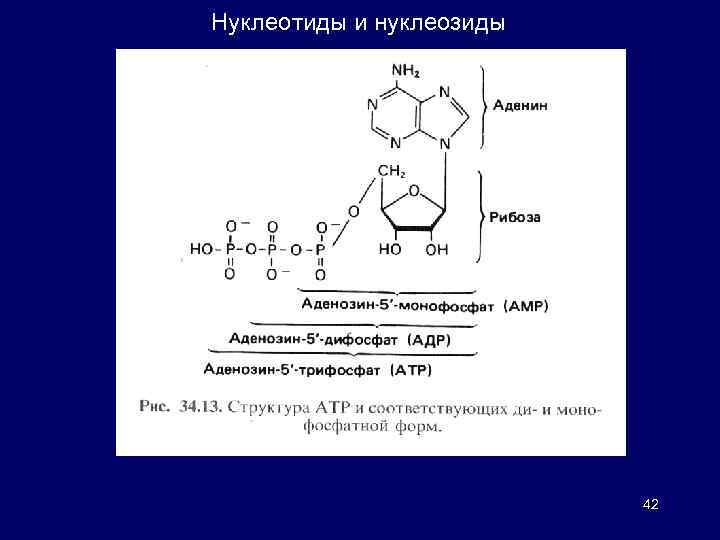
Нуклеотиды и нуклеозиды 42

ДНК биополимер сложной структуры, организованный в двойную спираль. Основные элементы: пуриновые (аденин и гуанин) и пиримидиновые (тимин и цитозин) основания присоединены к атому углевода (дезоксирибозы); углеводные остатки соединены между собой фосфодиэфирными связями Чередующиеся остатки дезоксирибозы и фосфатные группы образуют остов двойной спирали. Направление связей (3' --> 5‘) определяет ориентацию данной цепи, и, поскольку ориентации двух комплементарных цепей противоположны, их называют антипараллельными. В основе построения и функционирования молекул ДНК -- принцип комплементарных взаимодействий пар оснований (принцип спаривания оснований). Комплементарные основания: аденин всегда образует пару с тимином, а гуанин с цитозином. Содержание остатков гуанина в любом фрагменте ДНК всегда в точности соответствует содержанию цитозина. Так же равны другу количества аденина и тимина. Две цепи ДНК удерживаются друг возле друга за счет комплементарных взаимодействий пар оснований и гидрофобных «стэкинг» взаимодействий. Двойная спираль упакована в компактную структуру, образованную за счет взаимодействий с целым рядом белков, называемых гистонами. ДНК ядра клетки при полном расплетании достигает длины 1 м. Хромосомные белки упаковывают 43 гигантскую молекулу в ядро объемом всего лишь в несколько кубических микрон.
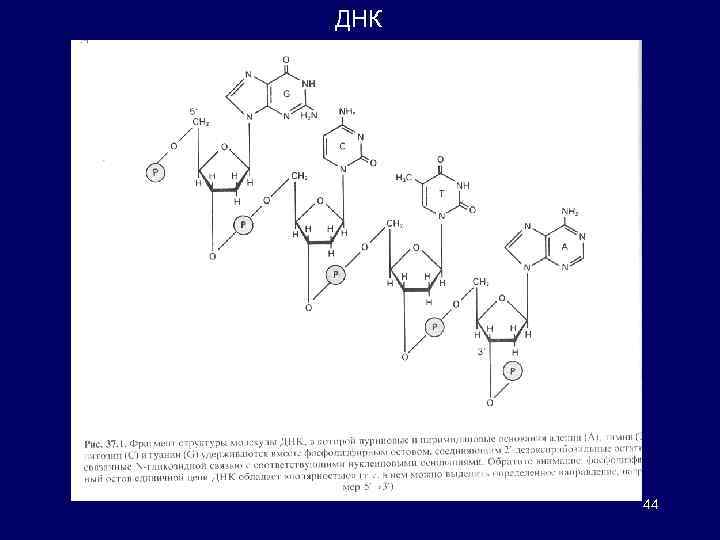
ДНК 44
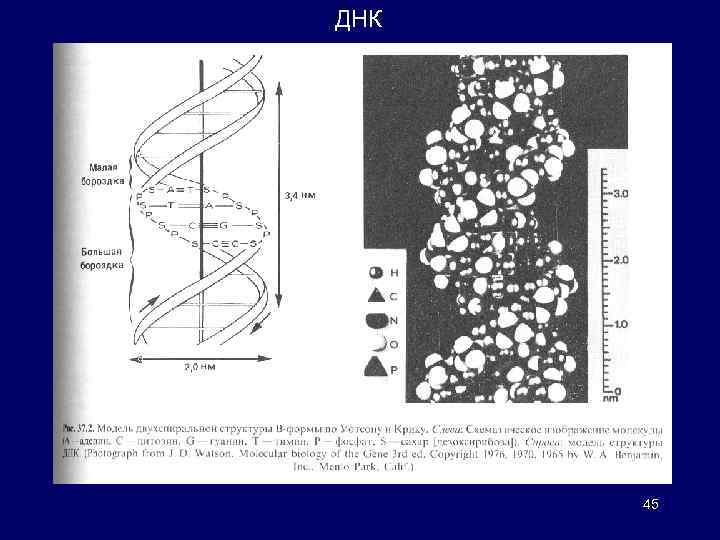
ДНК 45

Функция ДНК кодирует генетическую информацию. Генетическая информация, закодированная в последовательности нуклеотидов ДНК, служит двум целям: 1. необходима для синтеза белковых молекул; 2. обеспечивает передачу самой себя в ряду клеточных поколений и поколений организмов; т. е. молекула ДНК служит матрицей: 1. для транскрипции – перекодирования информации в структуру молекул РНК; 2. для репликации – копирования информации в дочерних молекулах ДНК. 46

Функция ДНК Комплементарность цепей двойной спирали => полуконсервативный способ репликации ДНК: Цепи расходятся и каждая служит матрицей для синтеза новой комплементарной последовательности. Две образовавшиеся двухспиральные молекулы ДНК, каждая из которых состоит из одной родительской и одной вновь синтезированной комплементарной цепи, распределяются между двумя дочерними клетками. Таким образом, каждая из дочерних клеток получает информацию, идентичную той, которой обладала родительская клетка. В каждой из двух дочерних клеток сохраняется одна цепь от исходной родительской ДНК. 47

РНК Рибонуклеиновая кислота представляет собой сополимер пуриновых и пиримидиновых рибонуклеотидов, соединенных друг с другом, как и в ДНК, фосфодиэфирными мостиками. Основные отличия от ДНК: 1. углеводный остаток – рибоза; 2. пиримидиновые компоненты: не содержит тимина, содержит урацил; 3. одноцепочечная молекула. Информация, содержащаяся в одноцепочечной РНК, реализуется в виде определенной последовательности пуриновых и пиримидиновых оснований, т. е. в первичной структуре полимерной цепи. Эта последовательность комплементарна кодирующей цепи гена, с которой «считывается» РНК. Вследствие комплементарнсти молекула РНК способна специфически связываться (гибридизоваться) с кодирующей цепью, но не гибридизуется с некодирующей цепью ДНК. Последовательность РНК (за исключением замены Т на U) идентична последовательности некодирующей цепи гена. Виды РНК: матричная РНК (м. РНК) – молекула цитоплазматической РНК, выполняющая функции матрицы белкового синтеза; транспортная РНК (т. РНК) – участвует в трансляции (переводе) информации м. РНК в последовательность аминокислот в белках; рибосомная РНК (р. РНК) – цитоплазматическая РНК, структурный компонент рибосом (клеточных органелл, играющих важную роль в 48 синтезе белка).

Генетический код Гаплоидный набор (23 пары хромосом) человека состоит примерно из 3∙ 109 пар нуклеотидов. В настоящее время считается, что в геноме человека 20000– 25000 различных генов; известна функция около 1, 5 % геномной ДНК (кодирование белка и РНК). Генетический код основан на использовании «алфавита» , состоящего всего из четырех букв! A, G, Т, С (соответствуют нуклеотидам, найденным в ДНК) => кодоны (трехбуквенные кодовые слова) Общий набор таких кодонов составляет генетический код. Последовательность серии кодонов, расположенных в цепи ДНК, образует определенный ген, по которому как по матрице синтезируется молекула РНК. Большинство молекул РНК участвует в том или ином этапе синтеза белков. Биомедицинское значение: До расшифровки генетического кода было невозможно понять механизм синтеза белка и объяснить происхождение мутаций. Открытие генетического кода позволило ответить на вопрос о том, как связаны между собой дефекты определенных белков человека и наследственные заболевания. Кроме того, благодаря расшифровке генетического кода были созданы необходимые предпосылки для диагностики и лечения таких заболеваний. 49

Синтез белка Генетическая информация, закодированная в последовательности нуклеотидов ДНК, транскрибируется в ядре в специфические нуклеотидные последовательности молекул м. РНК. Последовательность нуклеотидов в РНКтранскрипте комплементарна кодирующей цепи гена в соответствии с правилами образования комплементарных пар оснований. Трансляция: клетки должны обладать специальными механизмами для точного, аккуратного и эффективного перевода последовательности м. РНК в соответствующую последовательность аминокислот кодируемого белка. Молекулы м. РНК сами по себе не обладают каким-либо сродством к аминокислотам => адапторная молекула, т. РНК. Эта молекула должна узнавать, с одной стороны, специфическую последовательность м. РНК и, с другой – определенную аминокислоту. С помощью такой молекулы клетка может направлять определенную аминокислоту в соответствующее, диктуемое нуклеотидной последовательностью м. РНК, положение в молекуле синтезируемого белка. Рибосома – внутриклеточный компонент, в котором сходятся и взаимодействуют все элементы механизма трансляции белка. Полирибосомы (полисомы): множество рибосом одновременно транслируют одну и ту же цепь м. РНК. Шероховатый плазматический ретикулум – компартмент клетки, в котором мембраносвязанные полисомы продуцируют как мембранные белки, так и белки, подлежащие экскреции и транспорту. Полирибосомные структуры присутствуют и в свободной форме в цитоплазме, 50 где они синтезируют внутриклеточные белки.
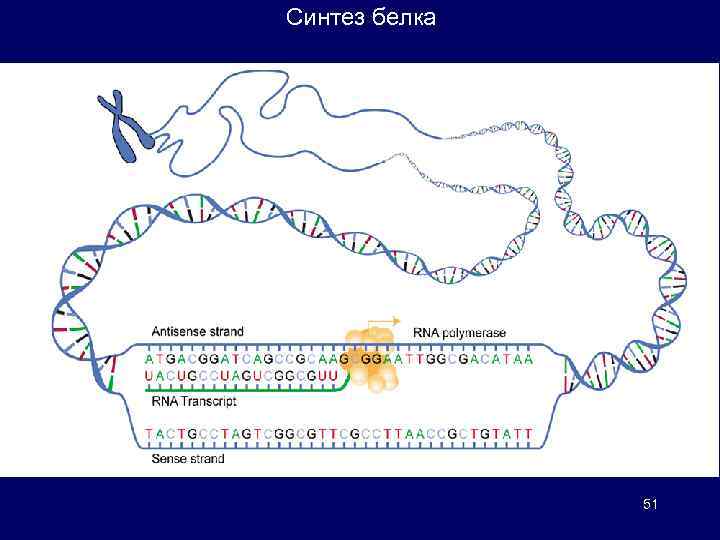
Синтез белка 51
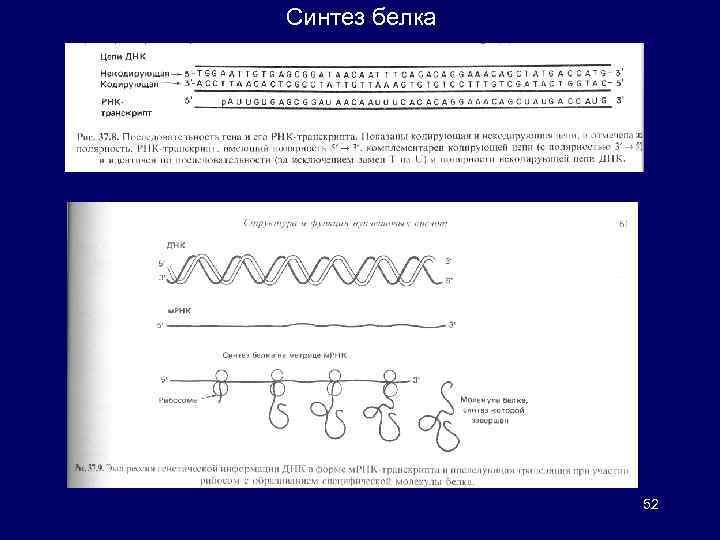
Синтез белка 52

Синтез белка Для синтеза клеточных белков необходимо 20 аминокислот => д. б. 20 различных кодонов, составляющих генетический код! м. РНК = нуклеотиды 4 х типов => каждый кодон должен состоять >1 нуклеотида: 2 нуклеотида в кодоне => 16 (42) различных кодонных вариантов; 3 нуклеотида в кодоне => 64 (43) варианта. Генетический код является триплетным (Маттэи и Ниренберг): • 3 нонсенс (nonsense)-кодона не кодируют каких-либо аминокислот, сигналы терминации, определяют, где должен остановиться синтез полипептидной цепи; • остальные триплеты – кодирование 20 аминокислот. Важнейшее свойство генетического кода – его «вырожденность» , несколько кодонов кодируют одну и ту же аминокислоту. 53
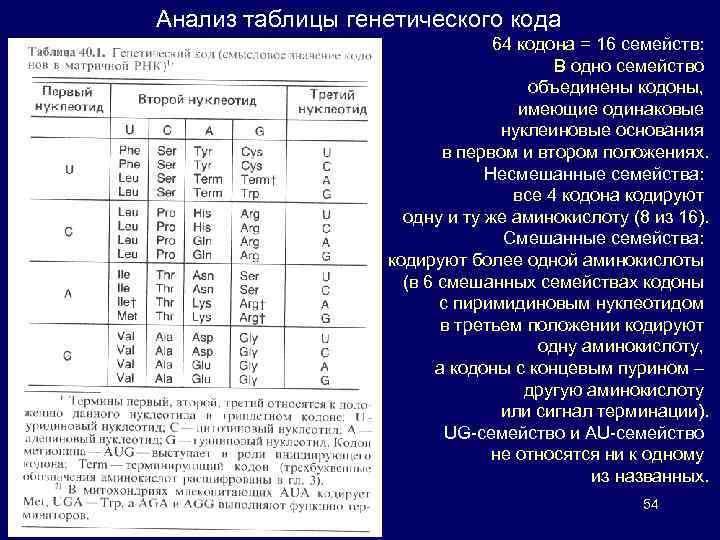
Анализ таблицы генетического кода 64 кодона = 16 семейств: В одно семейство объединены кодоны, имеющие одинаковые нуклеиновые основания в первом и втором положениях. Несмешанные семейства: все 4 кодона кодируют одну и ту же аминокислоту (8 из 16). Смешанные семейства: кодируют более одной аминокислоты (в 6 смешанных семействах кодоны с пиримидиновым нуклеотидом в третьем положении кодируют одну аминокислоту, а кодоны с концевым пурином – другую аминокислоту или сигнал терминации). UG-семейство и AU-семейство не относятся ни к одному из названных. 54

Свойства генетического кода • Вырожденность кода: Таким образом (см. таблицу), с точки зрения специфичности включения определенной аминокислоты третий нуклеотид в кодонах оказывается, как правило, менее важен, чем первые два. • Однозначность кода: Каждому данному кодону соответствует одна и только одна определенная аминокислота. По сигналу данного кодона происходит встраивание в белковую цепь только одной определенной аминокислоты, хотя каждая аминокислота может кодироваться и более чем одним определенным кодоном. • Генетический код – неперекрывающийся: Процесс считывания генетического кода при синтезе белка не допускает возможности перекрывания кодонов. • Генетический код не содержит знаков пунктуации: Начавшись на определенном кодоне, считывание следующих непосредственно друг за другом нуклеотидных триплетов идет далее без каких-либо пропусков вплоть до достижения нонсенскодона. • Генетический код – универсален, при этом частота использования каждого кодона варьирует от вида к виду и даже от ткани к ткани для одного и того же вида. Таблицы частот использования кодонов постоянно подвергаются уточнению по мере определения нуклеотидной последовательности все большего числа генов. 55

Мутации изменения в нуклеотидной последовательности гена Даже если первоначально мутация произошла в некодирующей цепи гена, одна из образующихся в ходе репликации дочерних молекул будет обязательно содержать мутацию в соответствующем месте кодирующей цепи и даст начало популяции мутантных клеток. Мутации замены оснований 1. транзиции: замена пуриновых оснований на пуриновые, а пиримидиновых — на пиримидиновые; 2. трансверсии: замена пуриновых оснований на пиримидиновые или пиримидиновых оснований на пуриновые. 56

Мутации замены оснований Если нуклеотидная последовательность гена, содержащего замену, транскрибируется, то образовавшаяся молекула м. РНК будет иметь комплементарную замену в соответствующем локусе. Последствия точковой замены: 1. если замена приходится на 3 ий нуклеотид кодона, то существует вероятность того, что аминокислотная последовательность останется неизменной и мутация никак не проявится (вырожденность генетического кода); 2. может иметь место миссенс-эффект, когда одна аминокислота вследствие замены нуклеотида замещается другой аминокислотой. Замена (в зависимости от ее локализации в аминокислотной последовательности белка) в отношении функции данного белка: • Приемлемая: молекула белка функционально неотличима о нормальной; • Частично приемлемая: нарушается нормальное функционирование белка; • Неприемлемая: приводит к полной потере функции белка. 3. может возникнуть нонсенс-кодон, присутствие которого приводит к преждевременной терминации синтеза белка. Как правило, фрагмент белка, образующийся в результате преждевременной терминации, не способен выполнять свои функции. + мутации сдвига рамки считывания; супрессорные молекулы т. РНК 57

Клетка – элементарная единица строения и жизнедеятельности всех живых организмов (кроме вирусов, о которых нередко говорят как о неклеточных формах жизни), обладающая собственным обменом веществ, способная к самостоятельному существованию, самовоспроизведению и развитию. Клетка – структурная и функциональная единица живого организма, которой присущи все основные жизненные функции. Клетка – элементарная биологическая единица способная самостоятельно существовать в отсутствие других живых организмов. Раздел биологии, занимающийся изучением строения и жизнедеятельности клеток, получил название цитологии. Все живые организмы либо, как многоклеточные животные, растения и грибы, состоят из множества клеток, либо, как многие простейшие и бактерии, являются одноклеточными организмами. 58

Прокариотическая и эукариотическая клетка Прокариоты (от лат. pro – перед, до и греч. κάρῠον – ядро, орех) – организмы, не обладающие, в отличие от эукариот, оформленным клеточным ядром и другими внутренними мембранными органоидами. Единственная крупная кольцевая (у некоторых видов – линейная) молекула ДНК, в которой содержится основная часть генетического материала клетки не образует комплекса с белками-гистонами (хроматина). К прокариотам относятся бактерии, в том числе сине-зелёные водоросли. Потомками прокариотических клеток являются органеллы эукариотических клеток – митохондрии и пластиды. Эукариоты (эвкариоты) (от греч. ευ – хорошо, полностью и κάρῠον – ядро, орех) – организмы, обладающие оформленным клеточным ядром, отграниченным от цитоплазмы ядерной оболочкой. Генетический материал заключён в нескольких линейных молекулах ДНК (в зависимости от вида организмов их число на ядро может колебаться от двух до нескольких сотен), прикреплённых изнутри к мембране клеточного ядра и образующих у подавляющего большинства комплекс с белками-гистонами, называемый хроматином. В клетках эукариот имеется система внутренних мембран, образующих, помимо ядра, ряд других органоидов (эндоплазматическая сеть, аппарат Гольджи и др. ). Кроме того, у подавляющего большинства имеются постоянные внутриклеточные симбионтыпрокариоты – митохондрии, а у водорослей и растений – также и пластиды. 59
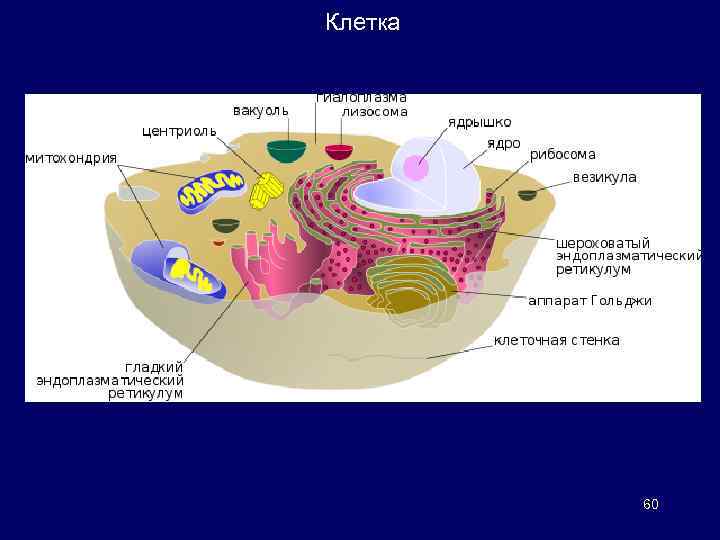
Клетка 60

Клетка В основе структурной организации клетки лежит мембранный принцип. Наружная цитоплазматическая мембрана Имеется у всех клеток и отграничивает содержимое цитоплазмы от внешней среды, образуя поверхность клетки. Обеспечивает транспорт веществ. Цитоплазма Находится под поверхностным слоем клетки. Включает ряд структур – органелл (органоидов), и различные вещества – включения: гранулы (плотные) и вакуоли (жидкие). Органоиды – постоянные, жизненно важные составные части клеток. Включения – непостоянные структуры цитоплазмы (а иногда и ядра), которые то возникают, то исчезают в процессе жизнедеятельности клетки. 61

Клетка Эндоплазматическая сеть (эндоплазматический ретикулум) Система переходящих друг в друга мембранных отсеков (трубок и цистерн). Общая внутриклеточная циркуляционная система, по каналам которой осуществляется транспорт веществ, а в мембраны этих каналов встроены многочисленные ферменты, обеспечивающие жизнедеятельность клетки. ЭПР особенно развит в клетках с интенсивным обменом веществ: в среднем составляет от 30 до 50 % всего объема клетки. Гранулярный (шероховатый) ЭПР: к его мембранам прикреплены рибосомы, на них происходит синтез белков. Гладкий (агранулярный) ЭПР: на стенках которого нет рибосом, принимает участие в синтезе липидов и углеводов. Внутренние пространства гладкого и гранулярного ЭПР не изолированы, а переходят друг в друга и сообщаются с просветом ядерной оболочки. Рибосомы Сферические частицы диаметром 15– 35 нм, состоящие из двух субъединиц (примерно равных по массе): белок и РНК. Рибосомная РНК (р. РНК) синтезируется в ядре на молекуле ДНК одной из хромосом в зоне ядрышка. Там же формируются рибосомы, которые затем покидают ядро. В цитоплазме рибосомы могут располагаться свободно или быть прикрепленными к наружной поверхности мембран эндоплазматической сети. В зависимости от типа синтезируемого белка рибосомы могут работать по одиночке или объединяться в комплексы – полирибосомы (полисомы). 62

Клетка Аппарат (комплекс) Гольджи Стопка плоских мембранных цистерн, несколько расширенных ближе к краям. Цистерны комплекса Гольджи соединены с каналами ЭПР. Синтезированные на мембранах ЭПР вещества (в том числе белки) транспортируются к комплексу Гольджи, конденсируются внутри его структур и «упаковываются» в виде секрета, готового либо к выделению, либо к использованию в самой клетке в процессе ее жизнедеятельности (например, для образования лизосом). Аппарат Гольджи асимметричен: Цистерны располагающиеся ближе к ядру клетки (цис-Гольджи) содержат наименее зрелые белки, к этим цистернам непрерывно присоединяются мембранные пузырьки – везикулы, отпочковывающиеся от ЭПР. По-видимому, при помощи таких же пузырьков происходит дальнейшее перемещение созревающих белков от одной цистерны к другой. В конце концов от противоположного конца органеллы (транс-Гольджи) отпочковываются пузырьки, содержащие полностью зрелые белки. 63
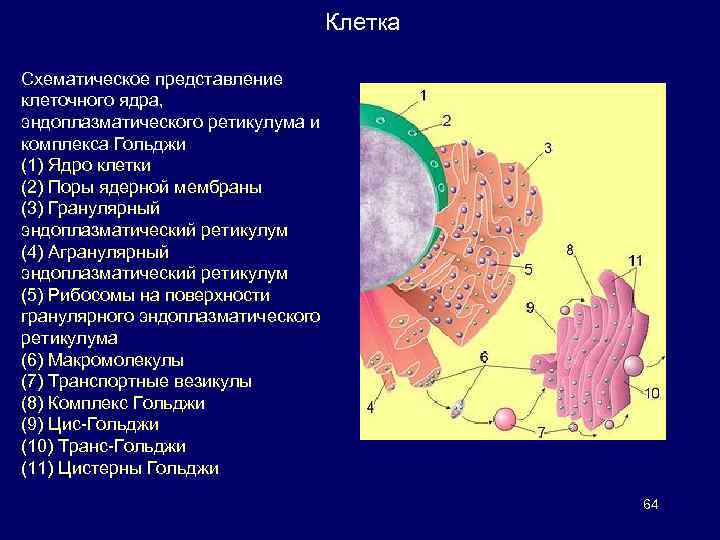
Клетка Схематическое представление клеточного ядра, эндоплазматического ретикулума и комплекса Гольджи (1) Ядро клетки (2) Поры ядерной мембраны (3) Гранулярный эндоплазматический ретикулум (4) Агранулярный эндоплазматический ретикулум (5) Рибосомы на поверхности гранулярного эндоплазматического ретикулума (6) Макромолекулы (7) Транспортные везикулы (8) Комплекс Гольджи (9) Цис-Гольджи (10) Транс-Гольджи (11) Цистерны Гольджи 64

Клетка Ядро Важнейшая составная часть клетки. Содержит молекулы ДНК, на которых записана генетическая информация организма. Большинство клеток имеет одно ядро, но можно наблюдать 2– 3 ядра в одной клетке (например, в клетках печени); известны и многоядерные клетки, причем число ядер может достигать нескольких десятков. Функции: 1. хранение и воспроизведение генетической информации; в ядре происходит репликация (удвоение) молекул ДНК, а также транскрипция (синтез) молекул РНК. 2. регуляция процессов обмена веществ, протекающих в клетке. 65

Клетка Ядерная оболочка Часть мембранной системы клетки. Отграничивает ядерное содержимое от цитоплазмы, создавая возможность существования особой внутриядерной среды, отличной от окружающей цитоплазмы. Выросты внешней ядерной мембраны соединяются с каналами эндоплазматической сети, образуя единую систему сообщающихся каналов. Состоит из двух мембран: наружная ядерная мембрана с поверхности, обращенной в цитоплазму, покрыта рибосомами, внутренняя мембрана гладкая. Обмен веществ между ядром и цитоплазмой: 1. ядерная оболочка пронизана многочисленными порами, через которые идет обмен молекулами между ядром и цитоплазмой; 2. вещества из ядра в цитоплазму и обратно могут попадать вследствие отшнуровывания впячиваний и выростов ядерной оболочки; кроме того, мелкие молекулы могут диффундировать через ядерную оболочку. Ядрышко Характерная структура ядра. Плотное округлое тельце, погруженное в ядерный сок. Число ядрышек (в ядрах разных клеток, а также в ядре одной и той же клетки в зависимости от ее функционального состояния) от 1 до 5– 7 (и более). Ядрышки есть только в неделящихся ядрах (во время митоза они исчезают, а после завершения деления вновь появляются). Ядрышко не представляет собой самостоятельную структуру ядра. Оно образуется вокруг участка хромосомы, в котором закодирована структура р. РНК (ядрышкового организатора). Ядрышко - это скопление р. РНК и субъединиц рибосом на разных этапах формирования. 66

Клетка Цитоскелет, клеточный центр (центриоли) Включает белковые структуры, расположенные в цитоплазме клетки. Центр организации цитоскелета – клеточный центр (центриоли). Цилиндрические белковые структуры, расположенные вблизи ядра клеток. Боковая поверхность образована наборами микротрубочек. Играют большую роль в делении клетки. Клетка перед делением содержит две центриоли, расположенные под прямым углом друг к другу. В ходе митоза они расходятся к разным концам клетки, формируя полюса веретена деления. Каждая дочерняя клетка получает по одной центриоли, которая удваивается к следующему делению. Удвоение центриолей происходит не делением, а путём синтеза новой структуры, перпендикулярной существующей. 67

Клетка Митохондрии Основные функции: 1. синтез АТФ, универсального носителя энергии 2. дыхание (поглощение кислорода и выделение углекислого газа). В состав входит молекула ДНК, однако в ней закодированы не все митохондриальные белки (большая часть генов митохондриальных белков находится в ядерном геноме, а соответствующие им продукты синтезируются в цитоплазме, а затем транспортируются в митохондрии). Стенка митохондрий состоит из двух мембран – наружной, гладкой, и внутренней, от которой вглубь отходят перегородки (кристы). На мембранах крист располагаются ферменты, участвующие в энергетическом обмене. Внутренний просвет митохондрий (матрикс) содержит ферменты, принимающие участие в дыхании и синтезе АТФ. Митохондрии тесно связаны с мембранами ЭПР, каналы которого могут открываться прямо в митохондрии. Лизосомы Очень мелкие овальные тельца, окруженные мембраной, образуются из структур комплекса Гольджи или из ЭПР. Содержат более 30 типов ферментов, способных расщеплять белки, нуклеиновые кислоты, полисахариды, липиды и другие вещества (осуществлять их лизис). Основная функция: участие во внутриклеточном переваривании пищевых веществ, а также разрушение структур самой клетки, например, при ее отмирании. 68

Субклеточное фракционирование Для изучения клеточных органелл необходимо получить их в относительно чистом виде Этапы: 1. Экстракция (растворение) Большинство органелл и многие биомолекулы (в частности, белки) весьма лабильны (неустойчивы) и легко утрачивают биологическую активность. Экстрагирование проводят в мягких условиях: в водных растворах, избегая экстремальных значений p. H, высоких температур (обычно проводят при 0– 4 о. С), с помощью специализированных растворов (например, раствор сахарозы СТКМ). 2. Гомогенизация Измельченные фрагменты тканей помещают в раствор для гомогенизации (может быть тот же, что и в 1), и приводят смесь во вращение. При контролируемой скорости вращения возникают силы вязкого трения => клетки разрушаются, содержимое попадает в раствор => гомогенат – смесь неповрежденных органелл с раствором. 3. Центрифугирование Субфракционирование гомогената путем дифференциального центрифугирования. 3 стадии при возрастающих скоростях: образуются осадок и надосадочная жидкость (супернатант), которая подвергается центрифугированию на следующей стадии => ядерная, митохондриальная и микросомная (смесь фрагментов гладкого ЭПР и свободных рибосом) фракции. Супернатант на конечной стадии ~ клеточный сок. Для определения содержания выделенной фракции применяют электронный микроскоп и «маркерные» химические соединения (ферменты, ДНК и др. ). Модификации подхода: различные среды для гомогенизации, условия или методы центрифугирования. 69

Области исследования клетки 1. Изучение вязкости протоплазмы (изучение основ коллоидной химии протоплазмы) 2. Изучение биологических мембран 3. Изучение электрических свойств клетки 4. Изучение клеточной проницаемости для различных веществ 5. Изучение оптических свойств клетки 70

Биологические мембраны чрезвычайно вязкие, но тем не менее пластичные структуры; формируют клетки (плазматическая мембрана), а также специализированные компартменты внутри клетки, клеточные органеллы (внутриклеточные мембраны). Основные функции • барьерная – обеспечивает селективный (избирательный), регулируемый, пассивный и активный обмен веществом с окружающей средой (мембрана является барьером, с помощью которого поддерживается различный состав вне- и внутриклеточной среды); Селективная проницаемость обеспечивается работой каналов и насосов, транспортирующих различные ионы и субстраты, и специфическими рецепторами, например рецепторами гормонов. С помощью плазматических мембран осуществляется обмен веществами между клеточным содержимым и окружающей средой путем экзо- и эндоцитоза; существуют также особые мембранные структуры – щелевые контакты, через которые соседние клетки обмениваются веществами. • матричная – обеспечивает определенное взаимное расположение и ориентацию мембранных белков, обеспечивает их оптимальное взаимодействие (например, оптимальное взаимодействие мембранных ферментов); • механическая – обеспечивает прочность и автономность клетки, внутриклеточных структур (обеспечивает изоляцию одной клетки от другой и обусловливает их индивидуальность). 71

Функции биологических мембран • энергетическая – синтез АТФ на внутренних мембранах митохондрий и фотосинтез в мембранах хлоропластов; • генераторная – генерация и проведение биопотенциалов; • рецепторная – механическая, акустическая, обонятельная, зрительная, химическая, терморецепция – мембранные процессы (в мембранах локализованы ферменты, функционирующие как интегральные элементы процесса возбуждения и ответа на него). Общая площадь всех биологических мембран в организме человека достигает десятков тысяч квадратных метров. Относительно большая совокупная площадь связана с огромной ролью мембран в жизненных процессах. Биомедицинское значение: Изменения в мембранных структурах могут сказываться на водном балансе и ионных потоках, а следовательно, на любых процессах, протекающих внутри клетки. Отсутствие какого-то мембранного компонента или его модификация приводят к различным заболеваниям. Очевидно, что нормальное функционирование клеток начинается с формирования нормальных мембран. 72

Барьерная функция мембраны Поддержание нормального состава среды внутри клетки и вокруг нее – основа жизнедеятельности. Вода составляет около 56 % мышечной массы тела человека; распределена между двумя большими компартментами: Внутриклеточная жидкость: содержит 2/3 всей массы воды и создает условия, необходимые для 1) преобразования, хранения и использования энергии; 2) осуществления гомеостаза; 3) репликации; 4) выполнения специфических функций. Состав: богата ионами К+ и Mg 2+, а основным анионом является фосфат; концентрация глюкозы ниже, а концентрация белков выше, чем во внеклеточной жидкости. Внеклеточная жидкость: содержит примерно 1/3 всей воды, которая распределена между плазмой и интерстициальным пространством; 1) обеспечивает систему доставки к клеткам питательных веществ (например, глюкозы, жирных кислот, аминокислот), кислорода, различных ионов и микроэлементов, а также многочисленных молекул регуляторов (гормонов), координирующих работу пространственно разобщенных клеток; 2) удаляет CО 2, отходы метаболизма и токсичные или обезвреженные вещества из непосредственного окружения клетки. Состав: содержит в большом количестве ионы Na+ и Са 2+, а основным анионом является Сl-1. Ионный состав внутриклеточной жидкости сильно отличается от состава внеклеточной среды. Барьер – мембрана с встроенными в нее насосами, обеспечивающая постоянство внутренней микросреды. 73

Мембраны – сложные структуры, состоят из липидов, белков и углеводов. Различные мембраны внутри клеток и между ними имеют неодинаковый состав, характеризуемый отношением белки : липиды (состав обусловлен функцией). Мембраны являются асимметричными плоскими замкнутыми структурами, обладающими внешней и внутренней поверхностями. Мембраны термодинамически стабильны и метаболически активны. В мембранах «заякорены» особые белковые молекулы, которые осуществляют функции, специфические для определенных органелл, клеток или организмов. Липидный состав (мембраны млекопитающих): фосфолипиды (фосфоглицериды и сфинго-миелины), гликосфинголпиды (липиды, содержащие остатки сахаров) и стеролы (холестерол). Амфифильная природа мембран: все основные липиды мембран содержат как гидрофобные, так и гидрофильные области. 74

Организация мембранных липидов Гипотезы: 1902 г. : замечено, что через мембраны лучше всего проникают вещества, хорошо растворимые в липидах => мембраны состоят из тонкого слоя фосфолипидов; монослой (одномолекулярный слой) липидов: полярные "головы" погружены в полярную среду (вода), а неполярные "хвосты" ориентированы в сторону неполярной среды (воздух). 1925 г. , Гортер и Грендел: площадь монослоя липидов, экстрагированных из мембран эритроцитов = 2 суммарная площадь поверхности эритроцитов; амфифильные молекулы образуют в водной среде термодинамически стабильный бимолекулярный слой, бислой, – это плоская структура, в которой гидрофобные области фосфолипидов недоступны для воды, а гидрофильные в нее погружены. Замкнутый бислой обеспечивает одно из основных свойств мембраны: он непроницаем для большинства водорастворимых молекул, поскольку они не растворяются в его гидрофобной сердцевине. 75

Организация мембранных липидов 1935 г. , Коул и Кертис: исследования электрических параметров биологических мембран: • высокое электрическое сопротивление 107 Ом м 2; • большая емкость 0, 5 102 Ф/м 2; Мембрану можно рассматривать как конденсатор: пластины – электролиты наружного и внутриклеточного растворов; диэлектрик – двойной слой неполярных хвостов липидных молекул (ε ~= 2). Ёмкость: C = εε 0 S/d (ε 0 = 8, 85 10 -12 Ф/м – электрическая постоянная) …=> d ~= 3, 5 нм (соответствует толщине неполярной части бислоя липидов) 76

Мембранные белки 1935 г. , Даниелли и Девсон (+ 40 лет): экспериментальные данные => мембрана состоит и из белковых молекул (измерения поверхностного натяжения клеточных мембран: коэффициент поверхностного натяжения значительно ближе к коэффициенту поверхностного натяжения на границе раздела белок-вода, около 10 -4 Н/м, нежели на границе раздела липид-вода, около 10 -2 Н/м); бутербродная модель, мембрана – трехслойная: два слоя белковых молекул по краям липидного бислоя. 77

Мембранные белки 1972 г. , Сингер и Николсон: Функционирующие мембраны представляют собой раствор глобулярных белков, диспергированных в жидком фосфолипидном матриксе. Жидкостно-мозаичная модель мембран: мембранные фосфолипиды играют роль растворителя для мембранных белков, создавая микроокружение, в котором последние могут функционировать. Белки могут образовывать единое целое с мембраной: их гидрофильные участки выступают из мембраны внутрь клетки и наружу, а гидрофобные пронизывают гидрофобную сердцевину бислоя (гидрофобные и гидрофильные аминокислоты). Различают поверхностные (или периферические) и интегральные белки. Число разных белков в мембране: от нескольких до более чем 100 (в плазматической мембране) – ферменты, транспортные белки, структурные белки, антигены и рецепторы для разных молекул. Каждая мембрана характеризуется своим набором белков (говорить о существовании некой типичной структуры мембран нельзя). 78

Мембранные белки Жидкостно-мозаичная модель мембран 79

Искусственные мембраны обычно состоят из одного фосфолипида (природного или синтетического) или их смеси; получают с помощью специально разработанных методик; Липосомы (фосфолипидные везикулы, пузырьки): образуются при соединении раствора фосфолипидов (в спирте, хлороформе или других растворителях) с водой в соответствующих условиях (например, при мягкой обработке ультразвуком), d = var 25– 400 нм. Плоские бислойные липидные мембраны: получают на маленьких отверстиях диаметром около 1 мм в пластинке из пластика (например, фторопласта), погруженной в водную среду, на отверстие наносят каплю раствора фосфолипидов; растворитель диффундирует из раствора в воду, и на отверстии остается пленка липида, которая спонтанно утончается (лишний липид собирается в виде ободка у краев отверстия), h = около 6 нм. 80

Искусственные мембраны Преимущества, примеры использования липосом: • Содержание разных липидов в искусственных мембранах можно варьировать: позволяет проводить систематическое исследование влияния липидного состава мембран на ту или иную функцию или свойство: электрические свойства, проницаемость, транспорт, барьерную функцию и т. д. • В везикулы можно встраивать очищенные мембранные белки или ферменты: позволяет выявить, какие молекулы необходимы для реконструкции функции очищенных белков и реконструировать, например, ионный насос (достаточно одного белка и одного липида). • Микроокружение искусственных систем можно жестко контролировать и целенаправленно варьировать (например, изменять концентрацию ионов). Их можно подвергать действию лигандов, специфичных к определенным белковым рецепторам, содержащимся в липосоме. • При формировании липосом ими могут захватываться те или иные компоненты, например лекарственные вещества или изолированные гены: использование липосом для доставки лекарств к конкретным тканям (для этого в мембраны липосом необходимо включить компоненты, позволяющие адресовать их конкретным тканям или опухолям, например, антитела к определенным молекулам клеточной поверхности). 81

Мембранный транспорт веществ Транспорт веществ через мембраны – необходимое условие жизни Способы адаптации клеток к постоянно меняющимся условиям внешней среды? Средства коммуникации между соседними и отдаленными друг от друга клетками: координирование комплекса биологических процессов? Если плазматическая мембрана относительно непроницаема, то как попадают в клетку большинство молекул? Чем обусловлена селективность их переноса? Химический потенциал данного вещества – величина, численно равная энергии Гиббса, приходящейся на 1 моль этого вещества; определяется как частная производная от энергии Гиббса по количеству вещества, при постоянстве условий среды (T, P и количеств всех других веществ): μx = (δG/ δmk)T, P, m(l≠k) Свободная энергия Гиббса – это термодинамический потенциал вида: G = E + PV – TS Энергию Гиббса можно понимать как полную химическую энергию системы (E – внутренняя энергия, P – давление, V – объем, T – температура, S – энтропия). Для разбавленного раствора концентрации C: μx = μ 0 + RTln. C μ 0 – стандартный химический потенциал, численно равный μx при концентрации вещества в растворе 1 моль/л (R = 8, 31 Дж/(моль К) – универсальная газовая постоянная) Электрохимический потенциал – величина, численно равная энергии Гиббса на 1 моль вещества, помещенного в электрическое поле, для разбавленных растворов: μ~ = μ 0 + RTln. C + ZFφ 82 F = 96500 Кл/моль – число Фарадея, Z – заряд иона электролита (в элементарных единицах заряда), φ – потенциал электрического поля.
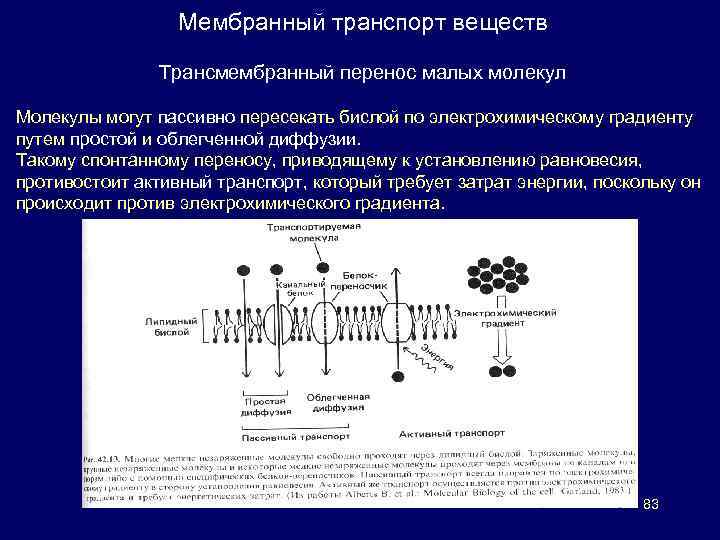
Мембранный транспорт веществ Трансмембранный перенос малых молекул Молекулы могут пассивно пересекать бислой по электрохимическому градиенту путем простой и облегченной диффузии. Такому спонтанному переносу, приводящему к установлению равновесия, противостоит активный транспорт, который требует затрат энергии, поскольку он происходит против электрохимического градиента. 83

Мембранный транспорт веществ Пассивный транспорт Некоторые вещества, например, газы, могут проникать в клетку за счет трансмембранной диффузии по электрохимическому градиенту; при этом никаких энергетических затрат не требуется. Пассивный транспорт – перенос вещества из мест с большим значением электрохимического потенциала к местам с его меньшим значением. Идет с уменьшением энергии Гиббса => не требует энергозатрат. Плотность потока вещества при пассивном транспорте, уравнение Теорелла: U – подвижность частиц, C – концентрация (перенос происходит в сторону убывания μ~) величина, численно равная количеству вещества, перенесенного за единицу времени через единицу площади поверхности, перпендикулярной направлению переноса (моль/м 2 с): Уравнение Нернста-Планка (для разбавленных растворов при μ 0 = const): 84

Пассивный транспорт Определяется следующими факторами: • Трансмембранным концентрационным градиентом веществ Растворенные вещества перемещаются в сторону понижения концентрации. Свободная (простая) диффузия – молекулярное движение вещества из области с большей концентрацией в область, где ее концентрация ниже. При отсутствии электрического поля или в случае неэлектролитов: => Закон Фика – уравнение, описывающее диффузию (D = URT – коэффициент диффузии) Градиент концентрации – разность концентраций вещества в мембране около одной и другой ее поверхностей (трудно определить, поэтому пользуются концентрациями в растворах около поверхностей мембраны) , моль/м 3, на толщину мембраны. 85

Пассивный транспорт Свободная (простая) диффузия P – коэффициент проницаемости мембраны, м/с, зависит от свойств мембраны и переносимых веществ если считать концентрации вещества у поверхности в мембране прямо пропорциональными концентрациям у поверхности вне мембраны, K – коэффициент распределения, тогда Коэффициент проницаемости тем больше, чем больше коэффициент диффузии (чем меньше вязкость мембраны), чем тоньше мембрана (меньше l), чем лучше вещество растворяется в мембране (больше K). Пассивный транспорт определяется следующими факторами: • Температурой Чем выше температура, тем больше скорость частиц (выше коэффициент диффузии) и, следовательно, частота столкновений между частицами и мембраной. 86 • Коэффициентом проницаемости мембраны для данного вещества.

Пассивный транспорт Определяется следующими факторами: • Трансмембранной разностью электрических потенциалов Градиент потенциала вызывает перенос положительных зарядов от мест с большим к местам с меньшим потенциалом или движение растворенных веществ в сторону раствора с противоположным зарядом. Электроосмос – перемещение растворителя с полярными молекулами под действием электрохимического градиента. Следует учитывать: м. б. перенос вещества от мест с меньшей концентрацией к местам с большей концентрацией; аналогично с потенциалом. 87

Пассивный транспорт Определяется следующими факторами: • Градиентом гидростатического давления на мембране При повышении давления будет увеличиваться скорость столкновений молекул и мембраны. Фильтрация – проникновение растворителя через полупроницаемую мембрану под действием гидростатического давления. Закон Пуазейля, скорость переноса при фильтрации: объемная скорость переноса раствора, гидравлическое сопротивление (l – длина поры, r – радиус поры, η – коэффициент вязкости раствора): • Градиентом осмотического давления на мембране Осмос – прохождение растворителя (воды) через полупроницаемую мембрану (непроницаемую для растворенного вещества и проницаемую для растворителя) из области с меньшей концентрацией растворенного вещества в область с большей концентрацией за счет осмотического давления; процесс диффузии растворителя из менее концентрированного раствора в более концентрированный раствор. 88

Пассивный транспорт Некоторые вещества диффундируют через мембраны по электрохимическому градиенту быстрее, чем можно ожидать исходя из их размеров, заряда или коэффициента распределения. Облегченная диффузия – транспорт веществ через клеточные мембраны, который происходит в том же направлении, что и свободная диффузия, но гораздо быстрее (перенос осуществляется без энергетических затрат). Предполагается, что в основе облегченной диффузии лежит трансмембранное перемещение белков-переносчиков с помощью механизма «пинг-понг» . Скорость, с которой растворенное вещество поступает в клетку, зависит от: 1) трансмембранного концентрационного градиента; 2) количества переносчика (ключ к регуляции); 3) быстроты связывания вещества с переносчиком; 4) быстроты конформационных изменений нагруженного и ненагруженного переносчика. Гормоны регулируют облегченную диффузию, изменяя число доступных переносчиков. Инсулин повышает интенсивность транспорта глюкозы в жировых и мышечных тканях, индуцируя поступление новых переносчиков из некого внутриклеточного пула. 89
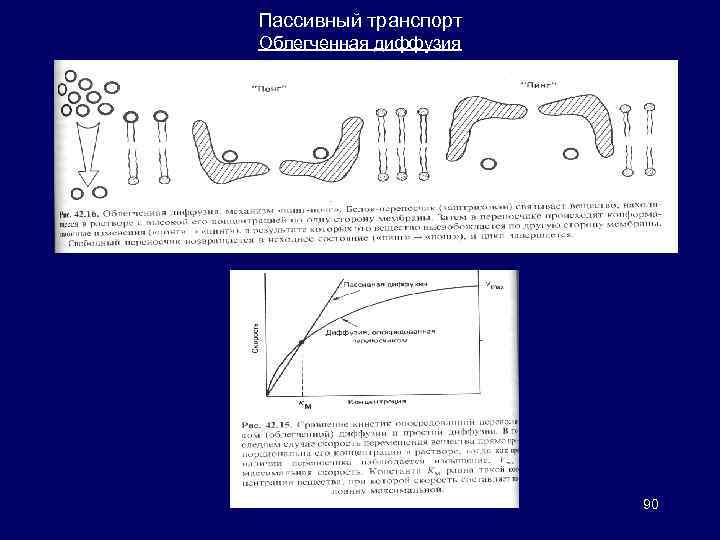
Пассивный транспорт Облегченная диффузия 90

Активный транспорт перенос вещества в направлении, противоположном тому, которое предопределено термодинамическим сопряжением концентрационного, электрического, осмотического и фильтрационного (гидростатического) градиентов. сопровождается смещением состояния системы от термодинамического равновесия (ростом энергии Гиббса) => требует энергетических затрат Источники энергии: гидролиз АТФ, процесс переноса электронов или свет. Поддержание электрохимических градиентов играет столь большую роль в биологических системах, что на него затрачивается около 30– 40% всей потребляемой клеткой энергии. С точки зрения термодинамики активный транспорт удерживает организм в неравновесном состоянии, поддерживает жизнь. 91
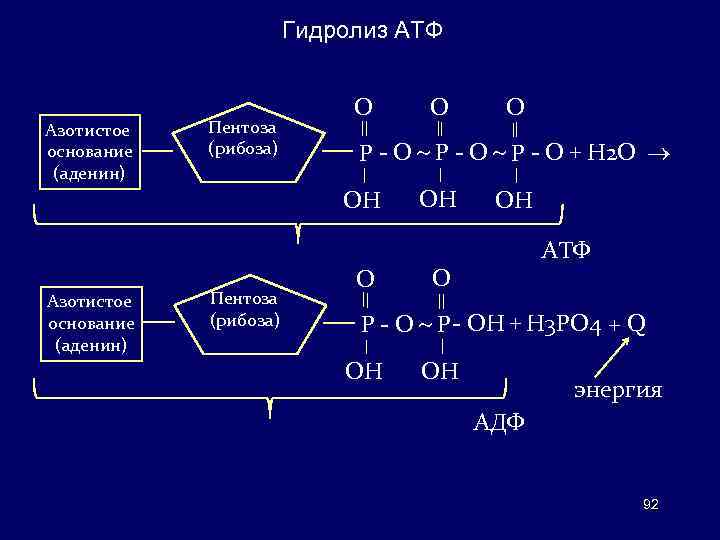
Гидролиз АТФ Азотистое основание (аденин) Пентоза (рибоза) O P - O + H 2 O OH Азотистое основание (аденин) O O OH OH АТФ O P - OH + H 3 PO 4 + Q OH OH энергия АДФ 92

Активный транспорт Ионные насосы в клетках Калий-натриевый насос (К+-Na+-АТФаза): за счет энергии, освобождающейся при гидролизе АТФ, в клетку переносится 2 иона калия и одновременно выкачиваются 3 иона натрия (внутри клетки поддерживается низкая концентрация Na+ и высокая К+). Этапы работы фермента К+-Na+-АТФазы: 1. 2. 3. 4. 5. 6. 7. образование комплекса фермента с АТФ на внутренней поверхности мембраны (реакция активируется ионами магния); связывание комплексом трех ионов натрия; фосфорилирование фермента с образованием АТФ; переворот ( «флип-флоп» ) фермента внутри мембраны; реакция ионного обмена натрия на калий, происходящая на внешней поверхности мембраны; обратный переворот ферментного комплекса с переносом ионов калия внутрь клетки; возвращение фермента в исходное состояние с освобождением ионов калия и фосфата. т. е. за полный цикл происходят: выброс из клетки 3 х ионов натрия, обогащение цитоплазмы 2 мя ионами калия и гидролиз 1 ой АТФ. Кальциевый насос (Ca 2+-АТФаза): переносятся 2 иона кальция. Протонная помпа (H+-АТФаза, H+-насос): переносятся 2 протона. 93
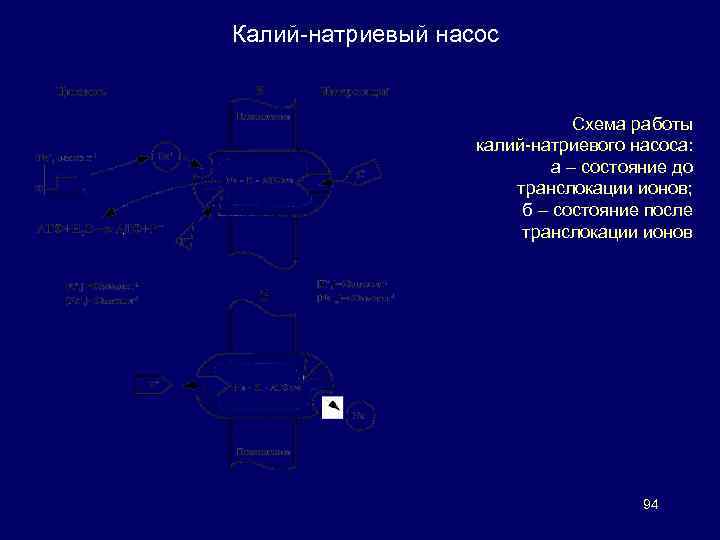
Калий-натриевый насос Схема работы калий-натриевого насоса: а – состояние до транслокации ионов; б – состояние после транслокации ионов 94

Активный транспорт Свойства систем активного транспорта: • Перенос веществ осуществляется вопреки действию физико-химических градиентов. • Необходимость энергетического обеспечения. • Специфичность: обеспечивается перенос через биологические мембраны только данного вещества (или группы веществ), и другие не переносятся. Компоненты активного транспорта: • Источник свободной энергии (АТФ); • Переносчик данного вещества; • Сопрягающий (регуляторный) фактор (перенос фосфатной группы с АТФ на переносчик). 95

Трансмембранное перемещение макромолекул Цитоз Эндоцитоз – процесс, с помощью которого клетки захватывают крупные молекулы: источники питательных веществ (например, полисахариды, белки и полинуклеотиды), рецепторы гормонов и др. Фагоцитоз – проникновение в клетку твёрдых частиц. Пиноцитоз – прохождение сквозь клеточную мембрану пузырьков с жидким содержимым. Из клетки макромолекулы выходят путем экзоцитоза. Как при эндоцитозе, так и при экзоцитозе образуются везикулы, сливающиеся с плазматической мембраной или отшнуровывающиеся от нее. 96

Трансмембранное перемещение макромолекул Эндоцитоз У всех эукариотических клеток часть плазматической мембраны постоянно оказывается внутри цитоплазмы. Это происходит в результате инвагинации фрагмента плазматической мембраны, образования эндоцитозной везикулы, замыкания шейки везикулы и отшнуровывания ее в цитоплазму вместе с содержимым. Впоследствии везикулы могут сливаться с другими мембранными структурами и, таким образом, переносить свое содержимое в другие клеточные компартменты или даже обратно, во внеклеточное пространство. Большинство эндоцитозных везикул сливаются с первичными лизосомами и образуют вторичные лизосомы, которые содержат гидролитические ферменты и являются специализированными органеллами. Макромолекулы перевариваются в них до аминокислот, простых сахаров и нуклеотидов, которые диффундируют из везикул и утилизуются в цитоплазме. Для эндоцитоза необходимы: 1) энергия, источником которой обычно служит АТР; 2) внеклеточный Са 2+; 3) сократительные элементы в клетке (вероятно, 97 системы микрофиламентов).

Трансмембранное перемещение макромолекул Эндоцитоз Фагоцитоз осуществляется только с участием специализированных клеток, макрофагов и гранулоцитов. Происходит поглощение крупных частиц – вирусов, бактерий, клеток или их обломков. Макрофаги исключительно активны в этом отношении и могут включать в себя объем, составляющий 25% собственного объема, за 1 ч. Пиноцитоз присущ всем клеткам. Клетка поглощает жидкости и растворенные в ней компоненты. 2 типа: Жидкофазный пиноцитоз – это неизбирательный процесс, при котором количество растворенного вещества, поглощаемого в составе везикул, пропорционально его концентрации во внеклеточной жидкости. Адсорбционный пиноцитоз – селективный процесс, опосредуемый медиатором. Поглощение макромолекул, для которых на плазматической мембране существует ограниченное число связывающих участков. Эти рецепторы, обладающие высоким сродством, выборочно концентрируют лиганды из среды при минимуме поглощаемой жидкости и растворенных в ней несвязывающихся молекул и заметно увеличивают эффективность поступления специфических молекул в клетку. Везикулы, образующиеся при адсорбционном пиноцитозе, образуются в месте инвагинаций (ямок), покрытых с цитоплазматической стороны волокнистым материалом (обычно клатрин, периферический мембранный белок). Окаймленные ямки могут занимать до 2% поверхности 98 некоторых клеток.
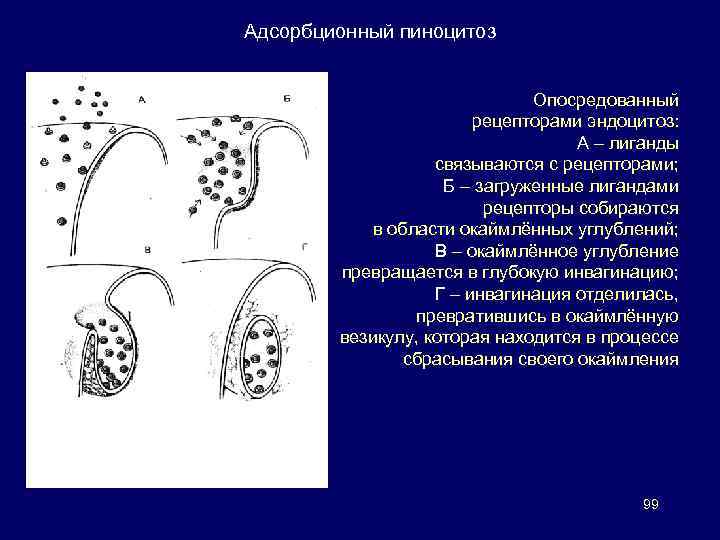
Адсорбционный пиноцитоз Опосредованный рецепторами эндоцитоз: А – лиганды связываются с рецепторами; Б – загруженные лигандами рецепторы собираются в области окаймлённых углублений; В – окаймлённое углубление превращается в глубокую инвагинацию; Г – инвагинация отделилась, превратившись в окаймлённую везикулу, которая находится в процессе сбрасывания своего окаймления 99

Трансмембранное перемещение макромолекул Экзоцитоз Большинство клеток высвобождают макромолекулы во внешнюю среду путем экзоцитоза. Играет роль в обновлении мембраны, когда ее компоненты, синтезированные в аппарате Гольджи, доставляются в составе везикул к плазматической мембране. Сигнал к началу эндоцитоза часто подается с помощью гормона, который, связываясь с рецептором на клеточной поверхности, инициирует локальные и обратимые изменения концентрации Са 2+, которые инициируют эндоцитоз. Вещества, высвобождаемые путем экзоцитоза можно разделить на три категории: 1) вещества, связывающиеся с клеточной поверхностью и становящиеся периферическими белками, например антигены; 2) вещества, включающиеся во внеклеточный матрикс, например коллаген и гликозаминогликаны; 3) вещества, выходящие во внеклеточную среду и служащие сигнальными молекулами для других клеток. Так, инсулин и катехоламины упаковываются в гранулы и созревают внутри клетки, а затем при соответствующей стимуляции высвобождаются наружу. 100

Мембранный транспорт веществ С подвижными переносчиками Биологических веществ Фагоцитоз Экзоцитоз Пиноцитоз Ионов Активный транспорт Цитоз Эндоцитоз Облегченная диффузия Электроосмос Фильтрация Осмос Свободная диффузия Пассивный транспорт С фиксированными переносчиками 101

Биоэлектрические потенциалы Генерация и передача биопотенциалов – одна из важнейших функций биологической мембраны => возбудимость клеток, регуляция внутриклеточных процессов, работа нервной системы, регуляция мышечного сокращения, рецепция. Биопотенциалы органов и тканей => диагностические методы: электрокардиография, электроэнцефалография, электромиография; лечебные воздействия, электростимуляция. Мембранный потенциал возникает вследствие градиента концентрации ионов и переноса ионов через мембрану; определяется как разность потенциалов между внутренней (цитоплазматической) и наружной поверхностями мембраны: 102
Биоэлектрические потенциалы Прогресс в исследовании биопотенциалов обусловлен: 1) разработкой микроэлектродного метода внутриклеточного измерения потенциалов; 2) созданием специальных усилителей биопотенциалов, обладающих высоким входным сопротивлением (до 1010 Ом), малой постоянной времени (от 10 мс) и высокой чувствительностью (токи от 10– 12 А) ; 3) выбором удачных объектов исследования: крупных клеток и среди них гигантского аксона кальмара, d до 0, 5 мм, что примерно в 100 -1000 больше, чем диаметр аксонов позвоночных животных, в том числе человека. 103

Биоэлектрические потенциалы Электрические явления на клеточных мембранах могут измеряться с помощью острых стеклянных микроэлектродов, которые вводятся в клетку: стеклянная микропипетка + металлический неполяризующийся электрод (пластичен, не может проколоть клеточную мембрану), например, серебряная проволока, покрытая солью Ag. Cl + раствор электролита, КСl или Na. Cl Электрод сравнения -- в растворе у наружной поверхности клетки. Регистрирующее устройство Р, содержащее усилитель постоянного тока, измеряет мембранный потенциал. 104

Биоэлектрические потенциалы Мембранные потенциалы: потенциалы покоя и потенциалы действия. Потенциал покоя -- стационарная разность электрических потенциалов, регистрируемая между внутренней и наружной поверхностями мембраны в невозбужденном состоянии. Потенциал покоя определяется разной концентрацией ионов по разные стороны мембраны и диффузией ионов через мембрану. Если концентрация какого-либо иона внутри клетки отлична от концентрации этого иона снаружи, и мембрана проницаема для этого иона, возникает поток заряженных частиц через мембрану, вследствие чего нарушается электрическая нейтральность системы, образуется разность потенциалов внутри и снаружи клетки, которая будет препятствовать дальнейшему перемещению ионов через мембрану. P+ P+ Q- Q- I II Система из двух отсеков разделена избирательно проницаемой мембраной. Предположим, что концентрация некоторого иона Р+ в отсеке I превышает его концентрацию в отсеке II. Мембрана непроницаема для другого иона Q-. Р+ будет диффундировать из I в II. Диффузия ведет к накоплению положительного заряда в отсеке II. Заряд, благодаря электростатическим силам, собирается на мембране справа и оставляет в отсеке I избыток отрицательного заряда (на мембране слева). Это приводит к образованию электрического поля, направленного от II к I и возрастающего по величине по мере диффузии ионов Р+ из I в II. Возрастающее электрическое поле препятствует диффузии до тех пор, пока не наступит равновесие. При равновесии сила электрического поля (направленная влево) в точности компенсирует диффузионную силу (направленную вправо). 105

Потенциал покоя При установлении равновесия выравниваются значения электрохимических потенциалов по разные стороны мембраны: => формула Нернста для равновесного мембранного потенциала: Для К+ [К+]вн(in) > [К+]нар(out) и Z = +1 Для Na+ [Na+]вн < [Na+]нар, Z = +1 Для С 1[Сl-]вн < [Сl-]нар, Z = -1 106
![Потенциал покоя в клетках Объект Концентрация, ммоль/л [К] вн. [Nа] нар. вн. φm, м. Потенциал покоя в клетках Объект Концентрация, ммоль/л [К] вн. [Nа] нар. вн. φm, м.](https://present5.com/presentation/-30032156_68401611/image-107.jpg)
Потенциал покоя в клетках Объект Концентрация, ммоль/л [К] вн. [Nа] нар. вн. φm, м. В По формуле Нернста φm, м. В exp [Сl] нар. вн. нар. К+ Na+ С 1 - Гигантский аксон кальмара 360 10 70 420 160 500 -90 50 -30 -60 Мышца лягушки 125 2, 5 15 125 11 120 -98 60 -87 -94 Из сравнения рассчитанных и экспериментальных значений мембранного потенциала видно, что потенциал покоя на самом деле ближе к потенциалу, рассчитанному по формуле Нернста для К+. Расхождение экспериментальных и теоретических значений <= не учтена проницаемость мембраны для других ионов! 107

Потенциал покоя в клетках Трудность применения уравнения Нернста к биологической мембране (даже в случае одномерного ее описания) состоит в том, что изменения величин С или φ внутри мембраны неизвестны и зависят от существующих пространственных электрических зарядов. мембрана тонка => линейный закон изменения φ внутри мембраны (приближение) В общем случае биологическая мембрана не может быть в равновесии для всех ионов. Если вычислить потенциалы Нернста для К, Na, Cl при их обычных концентрациях, то полученные величины окажутся различными. Таким образом, никакой трансмембранный потенциал не может одновременно уравновесить все ионы. Условие покоя может быть охарактеризовано только как стационарное состояние. Одновременная диффузия через мембрану ионов К+, Na+ и Сl- учитывается уравнением Гольдмана(-Ходжкина-Катца) (можно вывести из уравнения Нернста-Планка): где l -- толщина мембраны. В состоянии покоя проницаемость мембраны для ионов К+ значительно больше, чем для Na+, и больше, чем для Сl-: PK >> PNa, PK > PCl. Для аксона кальмара: PK : PNa : PCl = 1: 0, 04 : 0, 45. Если учесть, что проницаемость мембраны для ионов K выше, чем для остальных, из уравнения Гольдмана можно получить Нернста. 108

Потенциал покоя в клетках Мембранный потенциал, рассчитанный по уравнению Гольдмана, оказался по абсолютной величине < мембранного потенциала, рассчитанного по формуле Нернста, и ближе к экспериментальным его значениям в крупных клетках. И формула Нернста, и уравнение Гольдмана не учитывают активного транспорта ионов через мембрану, наличия в мембранах электрогенных (вызывающих разделение зарядов, а следовательно и возникновение разности потенциалов) ионных насосов (К+-Nа+-АТФазы, перекачивающие K внутрь клетки, а Na из клетки). С учетом работы электрогенных ионных насосов для мембранного потенциала было получено уравнение Томаса (Томас, 1972 г. ): где m -- отношение количества ионов натрия к количеству ионов калия, перекачиваемых ионными насосами через мембрану. Чаще всего К+-Ка+-АТФаза работает в режиме, когда m = 3/2, m всегда > 1. (нет ионных насосов, перекачивающих Сl, поэтому в уравнении Томаса отсутствуют члены c [Сl-]) Коэффициент m > 1 усиливает вклад градиента концентрации калия в создание мембранного потенциала, поэтому мембранный потенциал, рассчитанный по Томасу, больше по абсолютной величине, чем мембранный потенциал, рассчитанный по Гольдману, и дает совпадение с экспериментальными значениями для мелких клеток. 109

Потенциал покоя в клетках • Нарушение биоэнергетических процессов в клетке и работы К+-Nа+-АТФазы приводит к уменьшению абсолютного значения мембранного потенциала, в этом случае он лучше описывается уравнением Гольдмана. • Повреждение клеточной мембраны приводит к повышению проницаемости клеточных мембран для всех ионов: к повышению и РK, и PNa, и РСl. Вследствие уменьшения различия проницаемостей абсолютное значение мембранного потенциала снижается. • Для сильно поврежденных клеток абсолютное значение мембранного потенциала еще меньше, но сохраняется отрицательный мембранный потенциал за счет содержащихся в клетке полианионов -- отрицательно заряженных белков, нуклеиновых кислот и других крупных молекул, не могущих проникнуть через мембрану. 110

Потенциал действия Посредством электрических нервных импульсов (потенциалов действия) в живом организме передается информация от рецепторов к нейронам мозга и от нейронов мозга к мышцам. Живой организм является полностью электрифицированной системой. Без электричества нет жизни. При возбуждении нервных и мышечных клеток между внутриклеточной средой и межклеточной жидкостью возникает изменение мембранного потенциала, называемое потенциалом действия. Потенциалом действия называется электрический импульс, обусловленный изменением ионной проницаемости мембраны и связанный с распространением по нервам и мышцам волны возбуждения. Потенциал действия был открыт раньше потенциала покоя. Животное электричество: разряды электрического угря (до 600 В, ок. миллисекунды) Луиджи Гальвани, 1791 г. : электрический нервный импульс; мышечные сокращения конечностей препарированной лягушки могут вызваться электрическим импульсом, сама живая система является источником электрического импульса. XIX в. : представление о распространении электрических токов по нервам, как по проводам. Гельмгольц, вт. пол. XIX в. : скорость распространения нервного импульса составляет лишь 1 -100 м/с << скорости распространения электрического импульса по проводам (до 3∙ 108 м/с) => к. XIX в. : гипотеза электрической природы нервного импульса была отвергнута большинством физиологов (vs химическая реакция). На самом деле, как было показано позже, медленное распространение электрического нервного импульса связано с медленной перезарядкой конденсаторов, которые представляют собой клеточные мембраны, через большие сопротивления. Постоянная времени перезарядки мембраны τ = RC велика, так как велики емкость мембраны С и сопротивление R нервного волокна. сер. 20 -го в. : нервный импульс представляет собой импульс электрического тока, английский физиолог А. Ходжкин и его сотрудники. (1963 г. : Ходжкин, Хаксли и Иклс, Нобелевская премия по медицине за 111 оперирование нервных клеток).

Потенциал действия Опыты по исследованию потенциала действия проведены на гигантских аксона кальмара методом микроэлектродов с использованием высокоомных измерителей напряжения. В опытах по исследованию потенциала действия использовали 2 микроэлектрода, введенных в аксон На первый микроэлектрод подается импульс с амплитудой V от генератора Г прямоугольных импульсов, меняющий мембранный потенциал. Мембранный потенциал измеряется при помощи второго микроэлектрода высокоомным регистратором напряжения Р. Возбуждающий импульс вызывает лишь на короткое время смещение мембранного потенциала, которое быстро пропадает, и восстанавливается потенциал покоя. В том случае, когда возбуждающий импульс смещается дальше в отрицательную сторону, он сопровождается гиперполяризацией мембраны. Также не формируется потенциал действия, когда возбуждающий импульс положительный (деполяризующий), но его амплитуда < порогового значения Vпор. Если амплитуда положительного деполяризующего импульса > Vпор, мембранный потенциал становится > φпор, и в мембране развивается процесс, в результате которого происходит резкое повышение мембранного потенциала и мембранный потенциал даже меняет свой знак -- становится положительным (φвн > φнар). Достигнув некоторого положительного значения φм, рев(rev), потенциала реверсии, мембранный 112 потенциал возвращается к значению потенциала покоя φм, п(p), совершив «затухающее колебание» .

Потенциал действия В нервных волокнах и скелетных мышцах длительность потенциала действия около 1 мс, а в сердечной мышце около 300 мс. После снятия возбуждения еще в течение 1 -3 мс в мембране наблюдаются некоторые остаточные явления, во время которых мембрана рефрактерна (невозбудима). Новый деполяризующий потенциал V > Vпор может вызвать образование нового потенциала действия только после полного возвращения мембраны в состояние покоя. Амплитуда потенциала действия не зависит от амплитуды деполяризующего потенциала (при V > Vпор): Если в покое мембрана поляризована (потенциал цитоплазмы отрицателен по отношению к внеклеточной среде), то при возбуждении происходит деполяризация мембраны (потенциал внутри клетки положителен) и после снятия возбуждения происходит реполяризация мембраны. 113

Потенциал действия Характерные свойства: 1) наличие порогового значения деполяризующего потенциала; 2) закон «все или ничего» , то есть, если деполяризующий потенциал больше порогового, развивается потенциал действия, амплитуда которого не зависит от амплитуды возбуждающего импульса, и нет потенциала действия, если амплитуда деполяризующего потенциала меньше пороговой; 3) есть период рефрактерности, невозбудимости мембраны во время развития потенциала действия и остаточных явлений после снятия возбуждения; 4) в момент возбуждения резко уменьшается сопротивление мембраны (у аксона кальмара от 0, 1 Ом∙м 2 в покое до 0, 0025 Ом∙м 2 при возбуждении). 114

Потенциал действия Диффузия натрия создает положительную разность потенциалов между внутренней и наружной поверхностями мембраны (см. таблицу) => положительный потенциал реверсии имеет натриевую природу => можно менять амплитуду импульса потенциала действия, изменяя концентрацию натрия в наружной среде: при уменьшении наружной концентрации натрия амплитуда потенциала действия уменьшается, так как меняется потенциал реверсии; если из окружающей клетку среды полностью удалить натрий, потенциал действия вообще не возникает. Опыты => при возбуждении проницаемость для натрия резко возрастает (в 500 раз для аксона кальмара). Расчеты мембранного потенциала реверсии по уравнению Гольдмана, если в него подставить значения проницаемостей мембраны для возбужденного состояния, совпадают с экспериментальными данными. 115

Потенциал действия Возбуждение мембраны описывается уравнениями Ходжкина-Хаксли: где Im -- ток через мембрану, Сm -- емкость мембраны, ΣIi -- сумма ионных токов через мембрану. Электрический ток через мембрану складывается из ионных токов: ионов калия, натрия и других ионов, в том числе хлора, называемого током утечки, а также ёмкостного тока. Ёмкостной ток обусловлен перезарядкой конденсатора, который представляет собой мембрана, перетеканием зарядов с одной ее поверхности на другую. Его величина определяется количеством заряда, перетекающего с одной обкладки на другую за единицу времени dq/dt, заряд конденсатора q = Сmφm. Полный мембранный ток: 116

Потенциал действия Эквивалентная электрическая схема элемента возбудимой мембраны Каждый ионный ток определяется разностью мембранного потенциала φm и равновесного нернстовского потенциала, создаваемого диффузией ионов данного типа, φeq : где gi – проводимость, величина, обратная сопротивлению Ri элемента мембраны для ионов данного типа. На эквивалентной электрической схеме элемента мембраны равновесные потенциалы Нернста моделируются источниками напряжений с электродвижущими силами φ; проводимости для разных ионов моделируются резисторами. Согласно теории Ходжкина-Хаксли, возбуждение элемента мембраны связано с изменениями проводимости мембраны для ионов Na и К. 117 Проводимости мембраны сложным образом зависят от мембранного потенциала и времени.

Потенциал действия Опыты с фиксацией мембранного потенциала (напряжения) φм (для доказательства решающей роли ионных токов в генерации нервного импульса) Поддержание постоянного φm при исследовании токов через возбужденную мембрану позволяет: 1) избавиться от емкостных токов Сmdφm/dt; 2) исключить изменение ионных проводимостей g. Na и g. K при изменении φm и изучить их изменение в различные фазы развития возбуждения: gi = f(t). Постоянная разность потенциалов между внутренней и наружной поверхностями мембраны => специальная электронная схема, ключевой элемент: операционный усилитель (ОУ -- усилитель постоянного тока, охваченный отрицательной обратной связью по напряжению). 118

Потенциал действия Опыты с фиксацией напряжения Между входами ОУ -- разность потенциалов микроэлектрода, помещенного внутрь аксона кальмара (1), и электрода сравнения (2), т. е. мембранный потенциал φм = φвн–φнар. На выходе ОУ -- напряжение, компенсирующее изменение трансмембранного потенциала => подается на серебряный проводник (3), расположенный вдоль аксона => одна и та же мембранная разность потенциалов по всему волокну. Электронная схема удерживает на выходе (внутри аксона) тот же потенциал, что и на входе ОУ, таким образом: φм = const. Генератор постоянного напряжения (4) => можно изменить входное напряжение ОУ, например, поднять его выше порогового. Амперметр (5) измеряет протекающий через мембрану ток (между электродом сравнения (2) и выходящим электродом ОУ (3)). В опытах с фиксацией напряжения можно исследовать изменение мембранного тока во времени, при 119 развитии возбуждения, задавая разные постоянные значения мембранного потенциала φм.

Опыты с фиксацией напряжения Пусть: ток, направленный из клетки наружу в окружающий раствор, – положительный, внутрь клетки из окружающего раствора – отрицательный. Опыты => если поднять мембранный потенциал φм выше порогового, сначала ток течет внутрь клетки, а затем из клетки наружу. Фаза 1 мембранного тока связана с потоком ионов натрия из окружающей среды (где концентрация натрия больше) в клетку (где она меньше); Фаза 2 объясняется вытеканием ионов калия из клетки наружу. 120

Опыты с фиксацией напряжения Ионный состав окружающего раствора = var: Если снаружи убрать натрий, фаза 1 мембранного тока (ток внутрь клетки) пропадает => фаза 1 развития потенциала действия связана с увеличением проницаемости мембраны для ионов натрия. Поток положительных частиц в клетку приводит к деполяризации мембраны -- внутренняя ее поверхность заряжается положительно по отношению к наружной. В фазе 2 резко увеличивается проницаемость мембраны для калия, и из клетки наружу выходят положительно заряженные ионы калия, в то время как натриевый ток уменьшается. Аксоплазма препарированного аксона <=> наружный раствор; Ионный состав наружного раствора = нормальная аксоплазма => изменила знак разность потенциалов на мембране. Гипотеза: селективное (избирательное) изменение ионной проницаемости возбужденной мембраны, сначала для Na, а потом для К, объясняется тем, что в мембране имеются специальные ионные каналы (предположительно, это поры, образованные белковыми молекулами). Открывание и закрывание ионных каналов вызывается изменением мембранного потенциала. Одно из доказательств наличия в мембране ионных каналов -- существование веществ, блокирующих ионные потоки через мембрану: содержащийся в рыбе фугу тетродотоксин блокирует поступление внутрь клетки натрия (калиевых каналов – тетраэтиламмоний). 121

Ионные каналы клеточных мембран Модель возбудимой мембраны по теории Ходжкина-Хаксли предполагает регулируемый перенос ионов через мембрану. Однако непосредственный переход иона через липидный бислой весьма затруднен. Предполагается, что в мембране должны быть некоторые специальные структуры – проводящие ионы; они были найдены и названы ионными каналами. Подобные каналы выделены из различных объектов: плазматической мембраны клеток, постсинаптической мембраны мышечных клеток и других объектов. Известны также ионные каналы, образованные антибиотиками. Основные свойства ионных каналов: 1) селективность; 2) независимость работы отдельных каналов; 3) дискретный характер проводимости; 4) зависимость параметров каналов от мембранного потенциала. 122

Ионные каналы клеточных мембран Селективность – способность ионных каналов избирательно пропускать ионы какого-либо одного типа. Опыты на аксоне кальмара => ионы Na и К по-разному влияют на мембранный потенциал: ионы К меняют потенциал покоя, а ионы Na -- потенциал действия. Модель Ходжкина-Хаксли => независимые калиевые и натриевые ионные каналы: первые пропускают только ионы К+, а вторые - только ионы Na+. Измерения => ионные каналы обладают абсолютной селективностью по отношению к катионам (катион-селективные каналы), либо к анионам (анион-селективные каналы). Через катион-селективные каналы способны проходить катионы различных химических элементов, но проводимость мембраны для неосновного иона (и ток через нее) будет существенно ниже: например, для Na+-кaнала калиевый ток через него будет в 20 раз меньше. Способность ионного канала пропускать различные ионы – относительная селективность, характеризуется рядом селективности -- соотношением проводимостей канала для разных ионов, взятых при одной концентрации, при этом для основного иона селективность принимают за 1. Для Na+-канала этот ряд имеет вид: Na+ : К+ = 1: 0, 05 123

Ионные каналы клеточных мембран Независимость работы отдельных каналов: Прохождение тока через отдельный ионный канал не зависит от того, идет ли ток через другие каналы. Например, К+-каналы могут быть включены или выключены, но ток через Nа+-каналы не меняется. Влияние каналов друг на друга происходит опосредованно: изменение проницаемостей каких-либо каналов (например, натриевых) меняет мембранный потенциал, а уже он влияет на проводимости прочих ионных каналов. 124

Ионные каналы клеточных мембран Дискретный характер проводимости ионных каналов Ионные каналы представляют собой комплекс белков, пронизывающий мембрану, в центре – трубка, сквозь которую могут проходить ионы. Количество натриевых каналов на 1 мкм 2 поверхности мембраны аксона кальмара – около 500. Те трансмембранные токи, которые измеряют в обычных экспериментах, например, на аксоне кальмара, обусловлены суммарным ответом (изменением проводимости) ионных каналов (плавное изменение проводимости во времени). Ответ одиночного ионного канала меняется во времени принципиально иным образом: дискретно. Метод экспериментального исследования – метод локальной фиксации потенциала мембраны "Patch Clamp": микроэлектрод тонким концом, имеющим диаметр 0, 5 -1 мкм, присасывается к мембране таким образом, чтобы в его внутренний диаметр попал ионный канал; тогда, используя схему фиксации потенциала, можно измерять токи, которые проходят только через одиночный канал мембраны, а не через все каналы одновременно, как это происходит при использовании стандартного метода фиксации потенциала. Результаты экспериментов, выполненных на различных ионных каналах, показали, что проводимость ионного канала дискретна и он может находиться в двух состояниях: открытом или закрытом. Переходы между состояниями происходят в случайные моменты времени и подчиняются статистическим закономерностям: нельзя сказать, что данный ионный канал откроется именно в этот момент времени, можно лишь сделать утверждение о вероятности открытия канала в определенном интервале времени. 125

Ионные каналы клеточных мембран Зависимость параметров канала от мембранного потенциала: Ионные каналы нервных волокон чувствительны к мембранному потенциалу; после начала деполяризации мембраны соответствующие токи начинают изменяться с той или иной кинетикой. Ион-селективный канал имеет сенсор -- элемент, чувствительный к действию электрического поля. При изменении мембранного потенциала меняется величина действующей на него силы, в результате сенсор перемещается и меняет вероятность открывания или закрывания ворот -- «заслонок» , действующих по закону «все или ничего» . Эксперимент => под действием деполяризации мембраны увеличивается вероятность перехода натриевого канала в проводящее состояние. Скачок напряжения на мембране, создаваемый при измерениях методом фиксации потенциала, приводит к тому, что большое число каналов открывается => через них проходит больше зарядов, протекает больший ток. Существенно, что процесс роста проводимости канала определяется увеличением вероятности перехода канала в открытое состояние, а не увеличением диаметра открытого канала. Плавные кинетические кривые токов, регистрируемых при электрических измерениях на больших мембранах, получаются вследствие суммации многих скачкообразных токов, протекающих через отдельные каналы. Ионные каналы могут быть чувствительны и к другим физическим воздействиям: механическим деформациям, связыванию химических веществ и т. д. , -- являются структурной основой, соответственно, механорецепторов, хемо-рецепторов и т. д. 126

Ионные каналы клеточных мембран Структура Ион-селективный канал состоит из: • погруженной в бислой белковой части; • селективного фильтра, образованного отрицательно заряженными атомами кислорода, которые жестко расположены на определенном расстоянии друг от друга и пропускают ионы только определенного диаметра; • воротной части. Ворота ионного канала управляются мембранным потенциалом и могут находиться как в закрытом (нормальном), так и в открытом (вероятность увеличивается под действием электрического поля) состояниях. Когда ворота открываются, поток гидратированных ионов получает возможность проходить сквозь селективный фильтр. Если ион подходит по диаметру, то он сбрасывает гидратную оболочку и проскакивает на другую сторону ионного канала. Если же ион слишком велик по диаметру, как, например, тетраэтиламмоний, он не в состоянии пролезть сквозь фильтр и не может пересечь мембрану. Если же, напротив, ион слишком мал, то у него возникают сложности в селективном фильтре, на сей раз связанные с трудностью сброса гидратной оболочки иона. Блокаторы ионных каналов либо не могут пройти сквозь него, застревая в фильтре, либо они стерически соответствуют какому-либо входу в канал. Так как блокаторы несут положительный заряд, их заряженная часть втягивается в канал к селективному фильтру как обычный катион, а макромолекула закупоривает его. Таким образом, изменения электрических свойств возбудимых биомембран осуществляется с помощью ионных каналов, -- белковых макромолекул, пронизывающих липидный бислой, которые могут находиться в нескольких дискретных состояниях. Свойства каналов, селективных для ионов К, Na и Са, могут по-разному зависеть от мембранного потенциала, что и определяет динамику потенциала 127 действия в мембране, а также отличия таких потенциалов в мембранах разных клеток.

Распространение нервного импульса вдоль возбудимого волокна Если в каком-нибудь участке возбудимой мембраны сформировался потенциал действия, мембрана деполяризована, возбуждение распространяется на другие участки мембраны. Передача нервного импульса по аксону И в аксоплазме, и в окружающем растворе возникают локальные токи: между участками поверхности мембраны с большим потенциалом (положительно заряженными) и участками с меньшим потенциалом (отрицательно заряженными). Локальные электрические токи приводят к повышению потенциала внутренней поверхности невозбужденного участка мембраны φвн и к понижению φнар наружного потенциала невозбужденного участка мембраны, оказавшегося по соседству с возбужденной зоной. Таким образом, отрицательный потенциал покоя φм, п уменьшается по абсолютной величине, то есть повышается. В областях, близких к возбужденному участку, φм повышается выше порогового значения. Под действием изменения мембранного потенциала открываются натриевые каналы и дальнейшее повышение происходит уже за счет потока ионов натрия через мембрану. Происходит деполяризация мембраны, развивается потенциал действия. Затем возбуждение передается дальше на покоящиеся участки мембраны. Почему возбуждение распространяется по аксону не в обе стороны от зоны, до которой дошло возбуждение, ведь локальные токи текут в обе стороны от возбужденного участка? Возбуждение может распространяться только в область мембраны, находящуюся в состоянии покоя, то есть в одну сторону от возбужденного участка аксона. В другую сторону нервный импульс не может распространяться, так как области, через которые прошло возбуждение, некоторое время остаются 128 невозбудимыми -- рефрактерными.

Распространение нервного импульса вдоль возбудимого волокна Повышение мембранного потенциала – величина деполяризующего потенциала V, передаваемого от возбужденных участков вдоль мембраны, зависит от расстояния х: ΔφV 0 – повышение мембранного потенциала в зоне возбуждения, х – расстояние от возбужденного участка; λ – константа длины нервного волокна, равная расстоянию, на котором деполяризующий потенциал уменьшается в е раз. Константа длины нервного волокна где rm -- удельное электрическое сопротивление оболочки волокна, δ -- толщина оболочки, а -- радиус нервного волокна, ri -- удельное электрическое сопротивление цитоплазмы. Чем больше константа длины мембраны, тем больше скорость распространения нервного импульса. λ тем больше, чем больше радиус аксона и удельное сопротивление мембраны и чем меньше удельное сопротивление цитоплазмы. 129

Распространение нервного импульса вдоль возбудимого волокна Большую скорость распространения нервного импульса по аксону кальмара обеспечивает их гигантский по сравнению с аксонами позвоночных диаметр. У позвоночных большая скорость передачи возбуждения в нервных волокнах достигает другими способами: аксоны позвоночных снабжены миелиновой оболочкой, которая увеличивает сопротивление мембраны и ее толщину. Возбуждение по миелинизированному волокну распространяется сальтаторно (скачкообразно) от одного перехвата Ранвье (участка, свободного от миелиновой оболочки) до другого. Нервные импульсы проводятся по аксонам в какой-то степени аналогично тому, как передаются электрические сигналы по кабельно-релейной линии: электрический импульс передается без затухания за счет его усиления на промежуточных релейных станциях, роль которых в аксонах выполняют участки возбудимой мембраны, в которых генерируются потенциалы действия. 130

Биофизика мышечного сокращения Мышечная активность – одно из общих свойств высокоорганизованных живых организмов. Вся жизнедеятельность человека связана с мышечной активностью. Независимо от назначения, особенностей строения и способов регуляции принцип работы различных мышц организма одинаков. Отличие мышечной клетки от других видов возбудимых клеток: Сократимость – способность генерировать механическое напряжение и укорачиваться. Кроме того, мышцы являются генератором тепла, при чем не только при мышечной работе, холодовой дрожи, но и в режиме нетонического термогенеза. Мышечная активность в процессе жизнедеятельности обеспечивает работы отдельных органов и целых систем: работу двигательного аппарата, легких, сосудистую активность, активность желудочнокишечного тракта, сократительную способность сердца. Нарушение работы мышц (например, определяющих функционирование легких, сердца) может привести к патологиям, а ее прекращение – к смерти. В теле человека 640 мышц (в зависимости от метода подсчёта дифференцированных групп мышц их общее число определяют от 639 до 850). Самые маленькие прикреплены к мельчайшим косточкам, расположенным в ухе. Самые крупные – большие ягодичные мышцы, они приводят в движение ноги. Самые сильные мышцы – икроножные, жевательные. 131

Структура мышцы Мышечная ткань мышечные клетки (волокна) + внеклеточное вещество (коллаген, эластин и др. ) + густая сеть нервных волокон и кровеносных сосудов Мышцы (по строению): Независимо от строения имеют близкие механические свойства, одинаковый механизм активации и близкий химический состав. гладкие – мышцы кишечника, стенки сосудов; поперечно-полосатые – скелетные, мышцы сердца: d мышечного волокна = 20– 80 мкм h плазматической мембраны = 10 нм Каждое отдельное волокно – это сильно вытянутая клетка, l волокна (клетки) = от сотен микрон до нескольких сантиметров (в зависимости от вида мышцы) Внутри волокна (кроме известных органелл -- ядро, митохондрии, аппарат Гольджи и др. ): • сократительный аппарат клетки: 1000– 2000 параллельно расположенных миофибрилл, d = 1– 2 мкм • клеточные органеллы: саркоплазматический ретикулум и Т-система – система поперечных трубочек 132
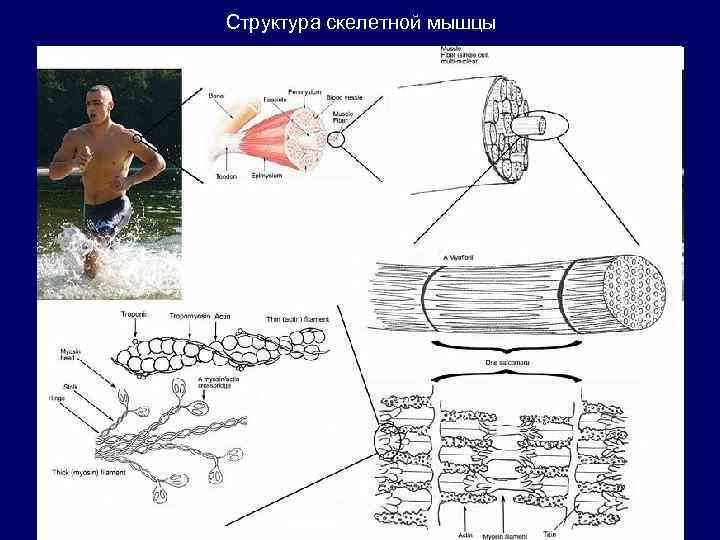
Структура скелетной мышцы 133

Структура мышцы Миофибрилла: А-зона – темные полосы, которые в поляризованном свете дают двойное лучепреломление, т. е. обладают свойством анизотропии I-зона – светлые полосы, не дающие двойного лучепреломления, т. е. изотропные Z-диск (от нем. zwischenscheibe – промежуточный диск) – темная узкая полоса в области I-зоны Промежуток между двумя Z-дисками называется саркомером и является элементарной сократительной единицей мышечной клетки. Саркомер – это упорядоченная система толстых и тонких нитей, расположенных гексагонально в поперечном сечении. Толстая нить: h =12 нм, L =1, 5 мкм, состоит из белка миозина. Тонкая нить: d = 8 нм, L = 1 мкм, состоит из белка актина, прикрепленного одним концом к Z-диску. 134

Структура мышцы Тонкая нить, актиновая: два закрученных один вокруг другого мономеров актина толщиной по 5 нм; ~ две нитки бус, скрученные по 14 бусин в витке. В цепях актина регулярно примерно через 40 нм встроены молекулы тропонина, а сама цепь охватывает нить тропомиозина. При сокращении мышцы тонкие нити вдвигаются между толстыми (миозин). Происходит относительное скольжение нитей без изменения их длины: взаимодействие особых выступов миозина – поперечных мостиков с активными центрами, расположенными на актине. Мостики отходят от толстой нити периодично на расстоянии 14, 5 нм друг от друга. 135

Модель скользящих нитей подтверждена экспериментально и является опытным фактом, на котором основаны все современные теории мышечного сокращения Х. Хаксли, В. И. Дещеревский а) В расслабленном состоянии миофибрилл молекулы тропомиозина блокируют прикрепление поперечных мостиков к актиновым цепям. б) Ионы Са 2+ активируют мостики и открывают участки их прикрепления к актину. в) В результате мостики миозина прикрепляются к актиновым нитям, расщепляются молекулы АТФ и изменяется конформация мостиков: их головки поворачиваются внутрь саркомера. Это приводит к генерации силы, скольжению актина относительно толстой нити миозина к центру саркомера, что вызывает укорочение мышцы. После окончания активации мостик размыкается и саркомер возвращается в исходное состояние. При укорочении объем саркомера практически не меняется, а следовательно, он становится толще, что и подтверждается на снимках поперечного сечения мышц с помощью электронной микроскопии. Каждый цикл замыкание-размыкание сопровождается расщеплением одной молекулы АТФ. Таким образом, актин-миозиновый комплекс является механохимическим преобразователем энергии АТФ. 136

Модель скользящих нитей Основные положения: 1. Длины нитей актина и миозина в ходе сокращения не меняются. 2. Изменение длины саркомера при сокращении – результат относительного продольного смещения нитей актина и миозина. 3. Поперечные мостики, отходящие от миозина, могут присоединяться к комплементарным центрам актина. 4. Мостики прикрепляются к актину не одновременно. 5. Замкнувшиеся мостики подвергаются структурному переходу, при котором они развивают усилие, после чего происходит их размыкание. 6. Сокращение и расслабление мышцы состоит в нарастании и последующем уменьшении числа мостиков, совершающих цикл замыкание-размыкание. 7. Каждый цикл связан с гидролизом одной молекулы АТФ. 8. Акты замыкания-размыкания мостиков происходят не зависимо друг от друга. 137
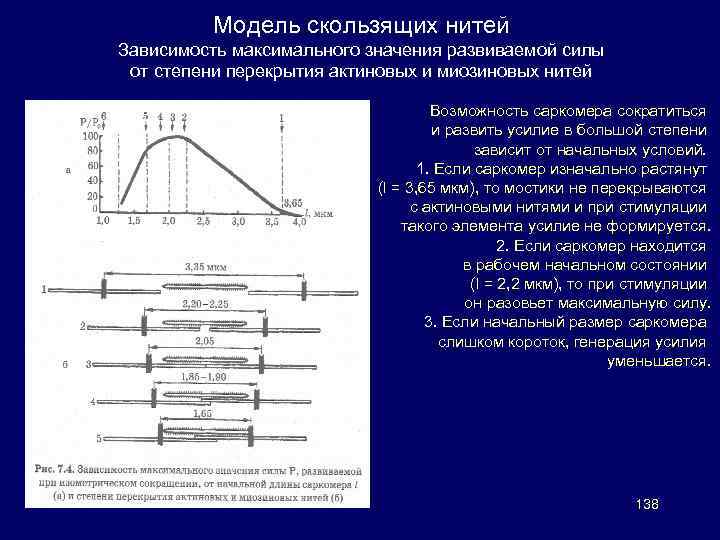
Модель скользящих нитей Зависимость максимального значения развиваемой силы от степени перекрытия актиновых и миозиновых нитей Возможность саркомера сократиться и развить усилие в большой степени зависит от начальных условий. 1. Если саркомер изначально растянут (l = 3, 65 мкм), то мостики не перекрываются с актиновыми нитями и при стимуляции такого элемента усилие не формируется. 2. Если саркомер находится в рабочем начальном состоянии (l = 2, 2 мкм), то при стимуляции он разовьет максимальную силу. 3. Если начальный размер саркомера слишком короток, генерация усилия уменьшается. 138

Биомеханика мышцы Мышцы можно представить как сплошную среду, т. е. среду, состоящую из большого числа элементов, взаимодействующих между собой без соударений и находящихся в поле внешних сил. Мышца одновременно обладает свойствами упругости и вязкости, то есть является вязко-упругой средой. Для такой среды предполагаются справедливыми законы классической механики. Фундаментальные понятия механики сплошных сред: Упругость – свойство тел менять размеры и форму под действием сил и самопроизвольно восстанавливать их при прекращении внешних воздействий. Упругость тел обусловлена силами взаимодействия его атомов и молекул. При снятии внешнего воздействия тело самопроизвольно возвращается в исходное состояние. Вязкость – внутреннее трение среды; свойство текучих тел оказывать сопротивление перемещению одной их части относительно другой. Деформация – относительное изменение длины: L – начальная длина, ΔL – значение удлинения, может менять знак. Напряжение механическое – мера внутренних сил, возникающих при деформации материала. Для однородного стержня: S – площадь сечения, F – сила, приложенная к стержню. 139

Биомеханика мышцы Упругая деформация возникает и исчезает одновременно с нагрузкой и не сопровождается рассеянием энергии. Для упругой деформации справедлив закон Гука: Е – модуль Юнга, определяемый природой вещества. При растяжении различных материалов, в общем случае, Е = f(ε). При малых растяжениях считают Е = const. В случае вязкой среды напряжение определяется скоростью деформации: η – коэффициент вязкости среды. Для вязкоупругой деформации характерна явная зависимость ε от процесса нагружения во времени, причем при снятии нагрузки деформация с течением некоторого времени самопроизвольно стремится к нулю. Пассивные механические свойства вязкоупругой среды можно моделировать сочетанием упругих и вязких элементов. Вязкость моделируется демпфером η, а упругость пружиной Е. 140

Биомеханика мышцы Пассивное растяжение Трехкомпонентная модель Хилла В терминах механической модели и модели скользящих нитей: Параллельный упругий элемент Е 1 определяет механические свойства внешних мембран клеток (сарколеммы) и внутренних структур – Т-системы и саркоплазматического ретикулума. Последовательный элемент Е 2 определяет упругость актин-миозинового комплекса, обусловленную, прежде всего, местами прикрепления актина к Z-дискам и местами соединения мостиков с активными центрами тонких нитей. Вязкий элемент η обусловлен скольжением нитей актина относительно миозина. Эта компонента резко возрастает при пассивном режиме мышцы, так как в этом случае мостики разомкнуты. Это проявляется в возможности сильного растяжения пассивной мышцы даже при незначительных нагрузках. 141

Биомеханика мышцы Пассивное растяжение Для установления характерной зависимости деформации мышцы во времени приложении к ней мгновенного воздействия упростим модель. Допустим, что элемент Е 2 отсутствует (σ2 = 0). Тогда для вязкоупругой среды напряжение в системе будет определяться упругой и вязкой составляющими: Найдем зависимость ε(t), решая дифференциальное уравнение и считая, что в начальный момент времени t = 0 деформация ε = 0: где называется временем запаздывания. Скорость нарастания деформации максимальна при t = 0: Отсюда следует, что чем больше величина вязкой компоненты η, тем меньше угол наклона кривой ε(t). Деформация ε(t) растет с убывающей скоростью и асимптотически приближается к стационарному значению: 142

Биомеханика мышцы Активное сокращение Для исследования характеристик сокращающихся мышц используют два искусственных режима: 1. Изометрический режим, при котором длина мышцы L = const, а регистрируется развиваемая сила F(t). 2. Изотонический режим, при котором мышца поднимает постоянный груз Р = const, а регистрируется изменение ее длины во времени Δl(t). 143
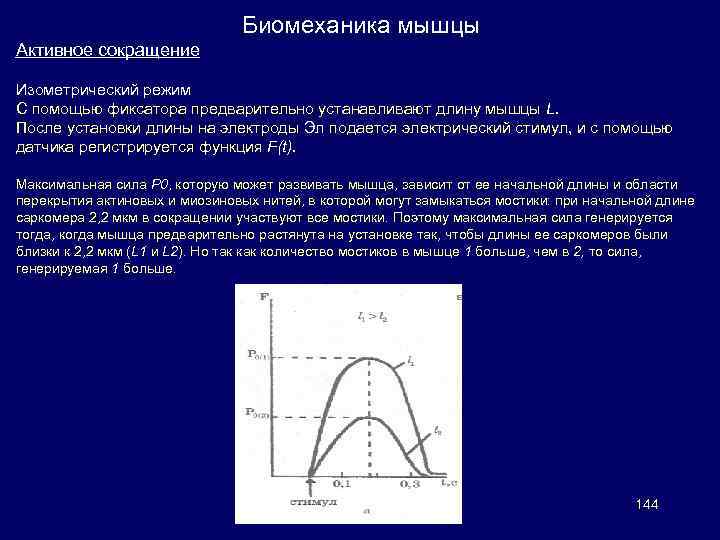
Биомеханика мышцы Активное сокращение Изометрический режим С помощью фиксатора предварительно устанавливают длину мышцы L. После установки длины на электроды Эл подается электрический стимул, и с помощью датчика регистрируется функция F(t). Максимальная сила Р 0, которую может развивать мышца, зависит от ее начальной длины и области перекрытия актиновых и миозиновых нитей, в которой могут замыкаться мостики: при начальной длине саркомера 2, 2 мкм в сокращении участвуют все мостики. Поэтому максимальная сила генерируется тогда, когда мышца предварительно растянута на установке так, чтобы длины ее саркомеров были близки к 2, 2 мкм (L 1 и L 2). Но так количество мостиков в мышце 1 больше, чем в 2, то сила, генерируемая 1 больше. 144
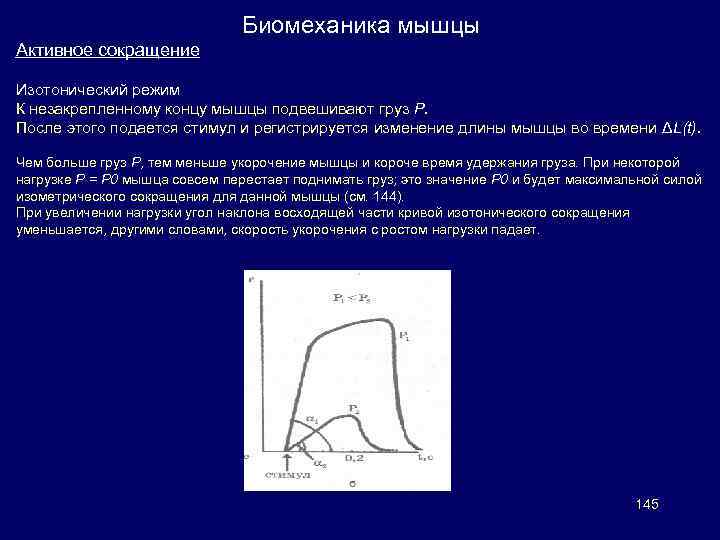
Биомеханика мышцы Активное сокращение Изотонический режим К незакрепленному концу мышцы подвешивают груз Р. После этого подается стимул и регистрируется изменение длины мышцы во времени ΔL(t). Чем больше груз Р, тем меньше укорочение мышцы и короче время удержания груза. При некоторой нагрузке Р = Р 0 мышца совсем перестает поднимать груз; это значение Р 0 и будет максимальной силой изометрического сокращения для данной мышцы (см. 144). При увеличении нагрузки угол наклона восходящей части кривой изотонического сокращения уменьшается, другими словами, скорость укорочения с ростом нагрузки падает. 145
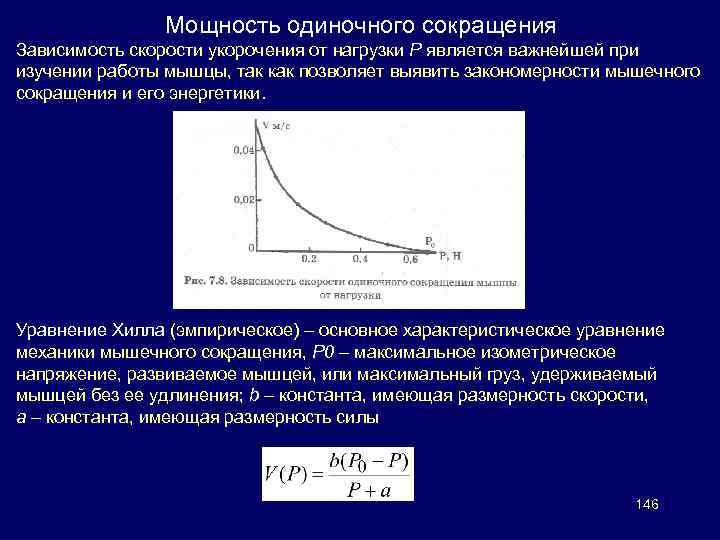
Мощность одиночного сокращения Зависимость скорости укорочения от нагрузки Р является важнейшей при изучении работы мышцы, так как позволяет выявить закономерности мышечного сокращения и его энергетики. Уравнение Хилла (эмпирическое) – основное характеристическое уравнение механики мышечного сокращения, Р 0 – максимальное изометрическое напряжение, развиваемое мышцей, или максимальный груз, удерживаемый мышцей без ее удлинения; b – константа, имеющая размерность скорости, а – константа, имеющая размерность силы 146

Мощность одиночного сокращения => максимальная скорость развивается при Р = 0: При Р = P 0 получаем V = 0, то есть укорочение не происходит. Работа А, производимая мышцей при одиночном укорочении на величину Δl: Эта зависимость, очевидно, нелинейная, так как V = f(P). Но на ранней фазе сокращения можно пренебречь этой нелинейностью и считать V = const: Тогда развиваемая мышцей мощность: Зависимость мощности мышцы от нагрузки Р: 147
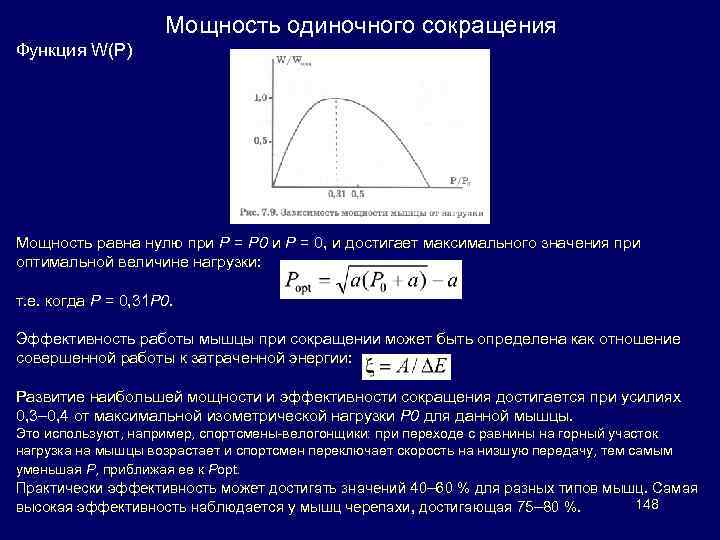
Мощность одиночного сокращения Функция W(P) Мощность равна нулю при Р = Р 0 и Р = 0, и достигает максимального значения при оптимальной величине нагрузки: т. е. когда Р = 0, 31 Р 0. Эффективность работы мышцы при сокращении может быть определена как отношение совершенной работы к затраченной энергии: Развитие наибольшей мощности и эффективности сокращения достигается при усилиях 0, 3– 0, 4 от максимальной изометрической нагрузки Р 0 для данной мышцы. Это используют, например, спортсмены-велогонщики: при переходе с равнины на горный участок нагрузка на мышцы возрастает и спортсмен переключает скорость на низшую передачу, тем самым уменьшая Р, приближая ее к Рopt. Практически эффективность может достигать значений 40– 60 % для разных типов мышц. Самая 148 высокая эффективность наблюдается у мышц черепахи, достигающая 75– 80 %.

Моделирование мышечного сокращения Вид уравнения Хилла указывает на существование в мышце внутреннего вязкого (зависящего от скорости) трения, препятствующего ее укорочению. Однако природа этого, как и физический смысл констант а и b, оставались не ясными. => математическая модель сокращения мышцы, предложенная В. Дещеревским, на модели скользящих нитей Предполагается, что сила сокращения волокна равна сумме сил, генерируемых мостиками в слое, равном половине саркомера. Скорость изменения длины волокна: N – число саркомеров в волокне, V* – относительная скорость скольжения нитей. При скольжении нитей мостик может находиться в одном из трех возможных состояний: разомкнутое, замкнутое тянущее – когда головка генерирует силу +f, направленную к центру саркомера, и замкнутое тормозящее – когда актиновая нить прошла координату центра прикрепления головки и прикрепленный мостик создает отрицательную по направлению силу -f, после чего он размыкается. Переходы из одного состояния в другое определяются соответствующими константами скоростей. Полный цикл мостика сопровождается распадом молекул АТФ. 149

Моделирование мышечного сокращения Для общего числа тянущих х и тормозящих z мостиков развиваемая саркомером сила F: первое слагаемое – это сила, генерируемая замкнутыми, а второе – тормозящими мостиками. Тогда система кинетических дифференциальных уравнений для состояний мостиков может быть записана в виде: где а(L) — число мостиков, способных замыкаться при длине 0, 5 саркомера в слое волокна толщиной I, M – масса нагрузки, Р – сила, развиваемая волокном. Смысл кинетических уравнений: например, в первом уравнении левая часть – скорость изменения количества тянущих мостиков. В правой части первое слагаемое а(L) – общее число мостиков минус количество тянущих х и тормозящих z мостиков, т. е. в квадратных скобках – количество оставшихся разомкнутых мостиков. Умножая это количество на константу скорости замыкания свободного мостика k 1, получаем скорость увеличения количества тянущих мостиков; второе слагаемое – скорость уменьшения количества тянущих мостиков за счет их перехода в тормозящее состояние. Разность между скоростями роста и убывания количества тянущих мостиков дает искомую 150 скорость изменения их количества.

Моделирование мышечного сокращения При изотоническом сокращении с постоянной скоростью в области с постоянным числом мостиков а(L) = а 0 – максимальное число мостиков, которые могут участвовать в сокращении, значения х, z и U не меняются во времени, т. е. система находится в стационарном состоянии: Тогда: Выражение для стационарной скорости укорочения (скольжения нитей) совпадает с уравнением Хилла. При этом: Таким образом, кинетическая модель Дещеревского позволила объяснить феноменологическое уравнение Хилла, смысл констант а и b, входящих в него, смысл величины максимальной силы Р 0 изометрического сокращения. Кроме того, показано, что внутренняя вязкая компонента мышцы определяется силой, развиваемой тормозящими мостиками, число которых растет с увеличением скорости сокращения мышцы. 151

Моделирование мышечного сокращения Электронная микроскопия, рентгеноструктурный анализ + рассмотренная модель => на одну нить актина приходится усилие 3∙ 10 -10 Н при максимальной изометрической нагрузке Р 0 = 30 Н/см 2; считая, что в каждой структурной единице находится 1 молекула миозина, и за каждый цикл замыкания-размыкания расщепляется 1 молекула АТФ, энергия которой используется на 50 %, получены следующие характеристики единичного элемента: f = 3∙ 10 -12 Н; δ = 10 -8 м; энергия сокращения 6∙ 10 -20 Дж; время замыкания 1 мс. Целая мышца может развивать силу до 104 Н (до 1 тонны)! 152

Электромеханическое сопряжение в мышцах Потенциал действия кардиомиоцита Длительность возбуждения (деполяризации) кардиомиоцита (мышечной клетки сердца ) составляет 250 --300 мс >> длительности возбуждения потенциала действия нервного волокна (1 мс), клетки скелетной мышцы (2– 3 мс) Распределение ионов К+ и Na+ в кардиомиоцитах близко к распределению этих ионов в скелетной мышце. Однако в кардиомиоците при формировании ПД и в процессе сокращения существенную роль играют и ионы Са 2+. Их концентрация снаружи клетки составляет около 2 ммоль/л, но внутри клетки концентрация свободных ионов Са 2+ очень мала: 10 -4 ммоль/л. При сокращении концентрация свободных ионов Са 2+ внутри клетки может возрастать -3 ммоль/л, но в фазе реполяризации до 10 избыток этих ионов удаляется из клетки. Сохранение ионного баланса в кардиомиоцитах обеспечивает К+- Na+- и Са 2+-насосы, активно перекачивающие ионы Na+ и Са 2+ наружу, а ионы К+ – внутрь клетки. Работу этих насосов обеспечивают ферменты К+- Na+- АТФаза и Са 2+-АТФаза, находящиеся в сарколемме миокардиальных клеток. В покое проницаемость мембраны для ионов Na+ и Са 2+ весьма мала: PNa/РK = 0, 05; отношение РСа/РK также мало, мала и концентрация ионов Са 2+ вне клетки. Поэтому потенциал покоя, как и в 153 нервных волокнах, определяется в основном разностью концентраций ионов К+ по обе стороны клеточной мембраны.

Потенциал действия кардиомиоцита Потенциал действия клетки миокарда имеет 3 характерные фазы: деполяризация (I), плато (II) и реполяризация (III) I фаза, деполяризация: определяется резким ростом проницаемости мембраны для ионов натрия (как и в аксоне), РK : PNa = 1 : 20 в момент превышения φм порогового значения при возбуждении. II фаза, плато: медленный спад φм от пикового значения (+30 м. В) до нуля. В этой фазе одновременно работают два типа каналов – медленные кальциевые каналы и калиевые каналы. Проводимость мембраны для Ca уменьшается, a для K увеличивается, происходит постепенное выравнивание текущих навстречу другу токов, а потенциал мембраны φм понижается почти до нуля, суммарный ток мембраны также стремится к нулю. III фаза, реполяризация: закрытие кальциевых каналов, рост проводимость мембраны для K и усиление выходящего тока К+. 154 T – время жизни соответствующих каналов, φпор – порог активации.

Электромеханическое сопряжение в мышцах Электромеханическое сопряжение – это цикл последовательных процессов, начинающийся с возникновения потенциала действия на сарколемме (клеточной мембране) и заканчивающийся сократительным ответом мышцы. Процесс сокращения кардиомиоцита: 1. при подаче на клетку стимулирующего импульса открываются быстрые (время активации 2 мс) натриевые каналы, ионы Na+ входят в клетку, вызывая деполяризацию мембраны; 2. в результате деполяризации плазматической мембраны в ней открываются потенциал-зависимые медленные кальциевые каналы (время жизни 200 мс), и ионы Са 2+ поступают из внеклеточной среды внутрь клетки; 3. кальций, поступающий в клетку, активирует мембрану саркоплазматического ретикулума (СР), являющегося внутриклеточным депо ионов Са 2+, и высвобождает кальций из его пузырьков, в результате чего возникает "кальциевый залп". Ионы Са 2+ поступают на актин-миозиновый комплекс миофибриллы, открывают активные центры актиновых цепей, вызывая замыкание мостиков и дальнейшее развитие силы и укорочения саркомера; 4. по окончании процесса сокращения миофибрилл ионы Са 2+ с помощью кальциевых насосов, находящихся в мембране СР, активно закачиваются внутрь СР; 155 5. К+ пассивно выходит из клетки, вызывая реполяризацию мембраны; 2+ активно выводятся во внеклеточную среду с помощью кальциевых насосов сарколеммы. 6. ионы Са
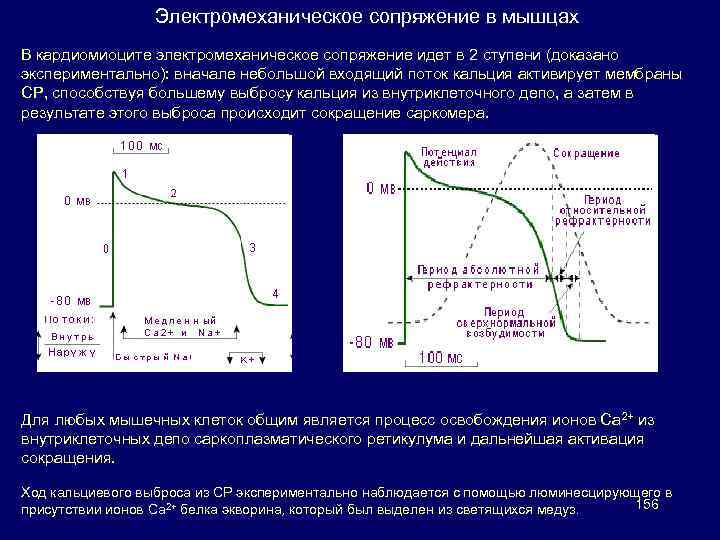
Электромеханическое сопряжение в мышцах В кардиомиоците электромеханическое сопряжение идет в 2 ступени (доказано экспериментально): вначале небольшой входящий поток кальция активирует мембраны СР, способствуя большему выбросу кальция из внутриклеточного депо, а затем в результате этого выброса происходит сокращение саркомера. Для любых мышечных клеток общим является процесс освобождения ионов Са 2+ из внутриклеточных депо саркоплазматического ретикулума и дальнейшая активация сокращения. Ход кальциевого выброса из СР экспериментально наблюдается с помощью люминесцирующего в 156 присутствии ионов Са 2+ белка экворина, который был выделен из светящихся медуз.

Электрическая активность органов от клеточного уровня на органный => задача описания распределения электрических потенциалов на поверхности этого органа в результате последовательного возбуждения отдельных его клеток. Клетки, образуя целостный орган, формируют сложную картину его электрической активности. Она определяется как электрической активностью отдельных клеток, так и взаимодействием между ними, устройством самого органа, неоднородностью структуры этого органа, процессами регуляции в нем и целым рядом других причин. Электрическая активность в большой степени отражает функциональное состояние клеток, тканей и органов. Регистрация и анализ электрической активности позволяют проводить биофизические и медико-биологические исследования с целью изучения работы органов и проведения клинической диагностики. В процессе жизнедеятельности состояние органа, а следовательно, и его электрическая активность меняются с течением времени. Это вызвано прежде всего распространением волн возбуждения по нервным и мышечным волокнам. В исследовательских целях можно измерять разность потенциалов непосредственно на поверхности или на внутренних структурах изучаемого органа (сердца, мозга и др. ). Однако в клинической практике такое прямое измерение разности потенциалов на органе трудно осуществимо. Но даже в случаях, когда удается измерить разности потенциалов непосредственно на внутренних органах, то их картирование и описание изменений во времени представляет собой трудноразрешимую задачу. 157

Внешние электрические поля органов Принцип эквивалентного генератора состоит в том, что изучаемый орган, состоящий из множества клеток, возбуждающихся в различные моменты времени, представляется моделью единого эквивалентного генератора. Считается, что этот эквивалентный генератор находится внутри организма и создает на поверхности тела электрическое поле, которое изменяется в соответствии с изменением электрической активности изучаемого органа. Термин "эквивалентный“: распределение потенциалов на поверхности тела и их изменение во времени, порождаемое органом, должны быть близки таковым, порождаемым гипотетическим (воображаемым) генератором. Теория Эйнтховена: сердце, клетки которого возбуждаются в сложной последовательности, представляется токовым диполем, причем изменение потенциалов электрического поля на поверхности грудной клетки, вызываемое изменением электрического момента диполя, такое же, как и от работающего сердца. 158

Электрография – метод исследования работы органов или тканей, основанный на регистрации во времени потенциалов электрического поля на поверхности тела. Два электрода, приложенные к разным точкам на поверхности тела, регистрируют меняющуюся во времени разность потенциалов. Временная зависимость изменения этой разности потенциалов – электрограмма. Название электрограммы указывает на органы (или ткани), функционирование которых приводит к появлению регистрируемых изменений разности потенциалов: сердца – ЭКГ (электрокардиограмма), сетчатки глаза – ЭРГ (электроретинограмма), головного мозга – ЭЭГ (электроэнцефалограмма), мышц – ЭМГ (электромиограмма) и др. В электрографии существуют две фундаментальные задачи: 1) прямая задача – расчет распределения электрического потенциала на заданной поверхности тела по заданным характеристикам эквивалентного генератора; 2) обратная задача – определение характеристик эквивалентного генератора (изучаемого органа) по измеренным потенциалам на поверхности тела. Обратная задача – это задача клинической диагностики: измеряя и регистрируя, например, ЭКГ, определять функционально состояние сердца. 159

Электрокардиография – изучение электрической активности сердца Экспериментальные данные показывают, что процесс распространения возбуждения по различным частям сердца сложен. Скорости распространения возбуждения варьируются в сердце по направлению и величине. Основные постулаты модели Эйнтховена (НП 1924 г. ): 1. Электрические поле сердца представляется как электрическое поле точечного токового диполя с дипольным моментом, называемым интегральным электрическим вектором сердца, ИЭВС) (складывается из диполей разных частей сердца: 2. ИЭВС находится в однородной изотропной проводящей среде, которой являются ткани организма. 3. Интегральный электрический вектор сердца меняется по величине и направлению. Его начало неподвижно и находится в атриовентрикулярном узле, а конец описывает сложную пространственную кривую, проекция которой на фронтальную плоскость образует за цикл сердечной деятельности (в норме) три петли: Р, QRS и Т. Очевидно, в этом случае в разных точках поверхности грудной клетки человека в некоторый момент времени будут возникать различные по величине и знаку электрические потенциалы. В следующий момент времени распределение этих потенциалов на поверхности тела изменится. 160
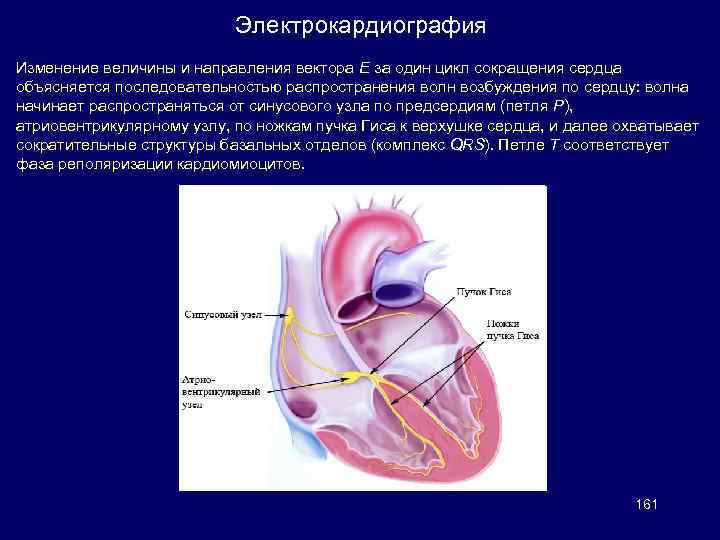
Электрокардиография Изменение величины и направления вектора Е за один цикл сокращения сердца объясняется последовательностью распространения волн возбуждения по сердцу: волна начинает распространяться от синусового узла по предсердиям (петля Р), атриовентрикулярному узлу, по ножкам пучка Гиса к верхушке сердца, и далее охватывает сократительные структуры базальных отделов (комплекс QRS). Петле Т соответствует фаза реполяризации кардиомиоцитов. 161
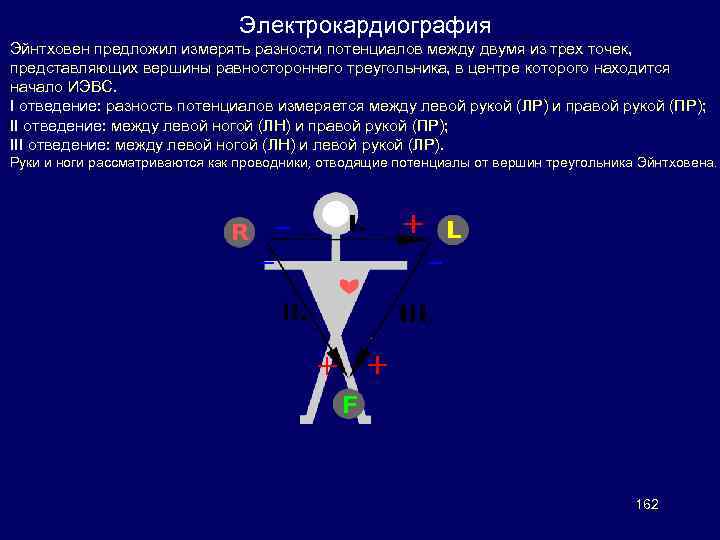
Электрокардиография Эйнтховен предложил измерять разности потенциалов между двумя из трех точек, представляющих вершины равностороннего треугольника, в центре которого находится начало ИЭВС. I отведение: разность потенциалов измеряется между левой рукой (ЛР) и правой рукой (ПР); II отведение: между левой ногой (ЛН) и правой рукой (ПР); III отведение: между левой ногой (ЛН) и левой рукой (ЛР). Руки и ноги рассматриваются как проводники, отводящие потенциалы от вершин треугольника Эйнтховена. 162
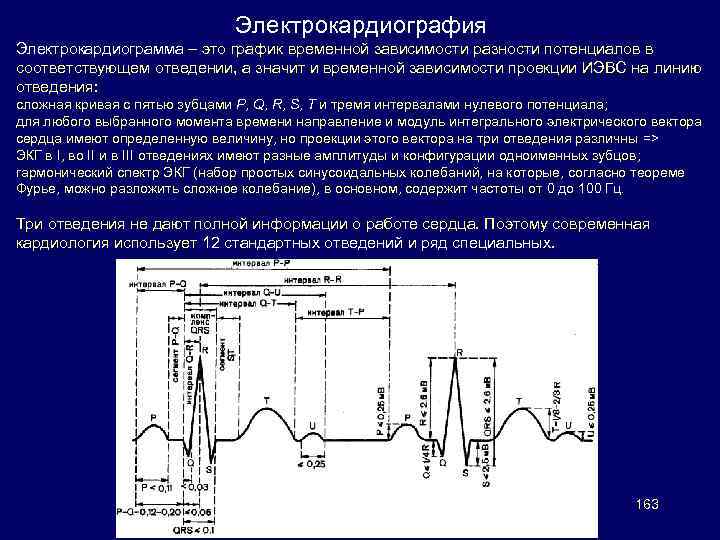
Электрокардиография Электрокардиограмма – это график временной зависимости разности потенциалов в соответствующем отведении, а значит и временной зависимости проекции ИЭВС на линию отведения: сложная кривая с пятью зубцами Р, Q, R, S, Т и тремя интервалами нулевого потенциала; для любого выбранного момента времени направление и модуль интегрального электрического вектора сердца имеют определенную величину, но проекции этого вектора на три отведения различны => ЭКГ в I, во II и в III отведениях имеют разные амплитуды и конфигурации одноименных зубцов; гармонический спектр ЭКГ (набор простых синусоидальных колебаний, на которые, согласно теореме Фурье, можно разложить сложное колебание), в основном, содержит частоты от 0 до 100 Гц. Три отведения не дают полной информации о работе сердца. Поэтому современная кардиология использует 12 стандартных отведений и ряд специальных. 163

Электрокардиография Допущения модели Эйнтховена: 1. Организм не является однородной электропроводной средой: кровь, лимфа, сосуды, мышцы и другие ткани имеют различные удельные проводимости. Кроме того, проводимость меняется со временем, например, при вдохе и выдохе. 2. Вектор Е, вращаясь, создает сложную объемную фигуру, а не проекцию лишь на одну плоскость, и начало его может смещаться. 3. Не представляется возможным точно описать изменения Е сердца только изменением момента одного точечного диполя. Однако медицинская практика показывает, что эти недостатки не столь существенны. Модель Эйнтховена успешно используется в электрокардиографии. В научных исследованиях разработана более точная мультипольная модель сердца, учитывающая то, что сердце имеет конечные размеры. В этой модели сердце представляется не одним, а многими диполями. 164
БИОФИЗИКА_1.ppt