Гемоглобин.pptx
- Количество слайдов: 15

Сабақтың тақырыбы: Гемоглобин мен коллагеннің құрылымы мен қызметі. Сабақтың мақсаты: Гемоглобин мен коллаген құрылымын сипаттау және олардың қызметтері арасындағы өзара байланысты түсіндіру. 2. Әр түрлі жағдайлардың ақуыздар құрылымына әсерін зерттеу. Тақырыпты ашатын сұрақтар тізбегі. 1. 2. 3. 4. 5. 6. 7. 8. 9. Эритроцит құрамында қызыл түсті беретін нәруыз? Гемоглобин құрамына не кіреді? Оның негізгі қызметі? Қандай аминқышқылдарынан тұрады? Гемоглобиннің қызметі: Гемоглобиннің 4 -інші реттік құрылымында қандай байланыстар болады: Коллагеннің/құрылысы ? Коллагеннің кездесетін орындары: Коллагеннің қызметі:

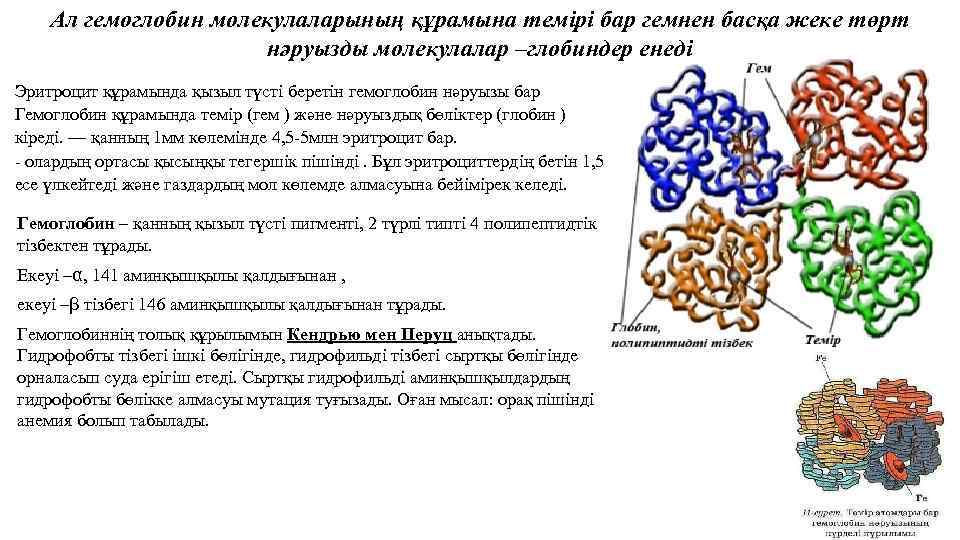
Ал гемоглобин молекулаларының құрамына темірі бар гемнен басқа жеке төрт нәруызды молекулалар –глобиндер енеді Эритроцит құрамында қызыл түсті беретін гемоглобин нәруызы бар Гемоглобин құрамында темір (гем ) және нәруыздық бөліктер (глобин ) кіреді. — қанның 1 мм көлемінде 4, 5 -5 млн эритроцит бар. - олардың ортасы қысыңқы тегершік пішінді. Бұл эритроциттердің бетін 1, 5 есе үлкейтеді және газдардың мол көлемде алмасуына бейімірек келеді. Гемоглобин – қанның қызыл түсті пигменті, 2 түрлі типті 4 полипептидтік тізбектен тұрады. Екеуі –α, 141 аминқышқылы қалдығынан , екеуі –β тізбегі 146 аминқышқылы қалдығынан тұрады. Гемоглобиннің толық құрылымын Кендрью мен Перуц анықтады. Гидрофобты тізбегі ішкі бөлігінде, гидрофильді тізбегі сыртқы бөлігінде орналасып суда ерігіш етеді. Сыртқы гидрофильді аминқышқылдардың гидрофобты бөлікке алмасуы мутация туғызады. Оған мысал: орақ пішінді анемия болып табылады.
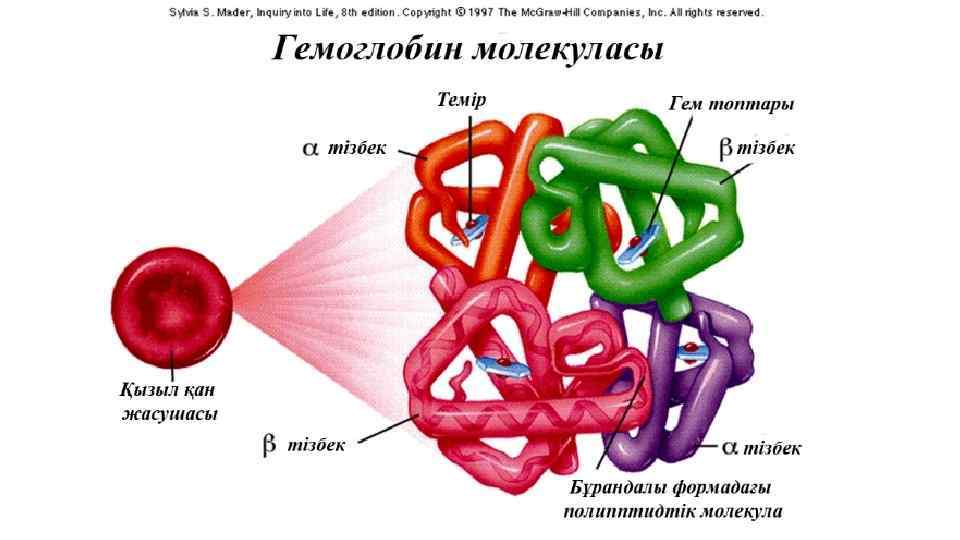
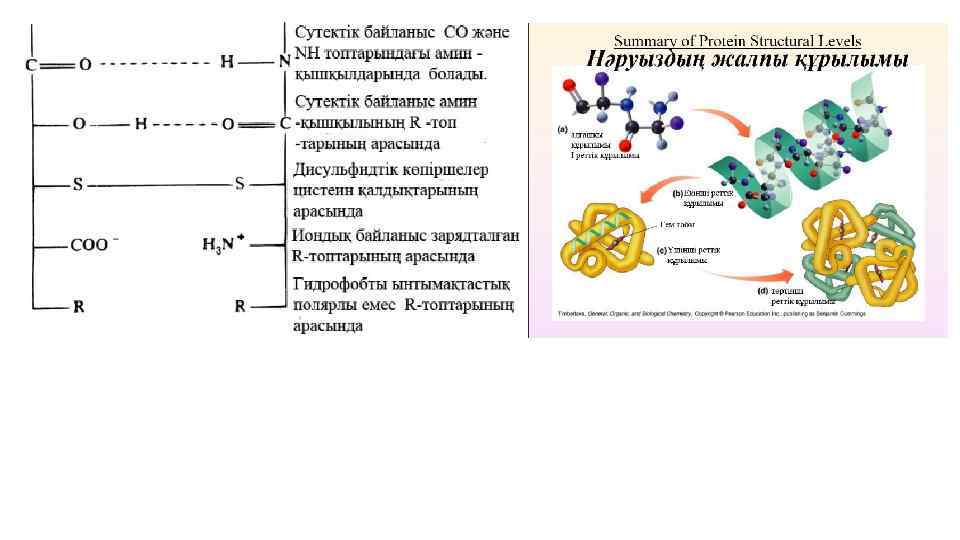
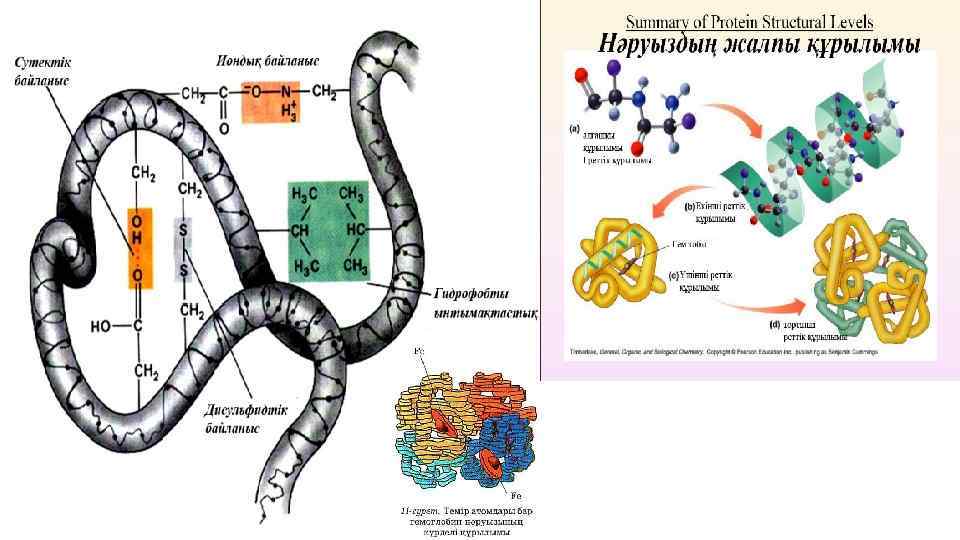
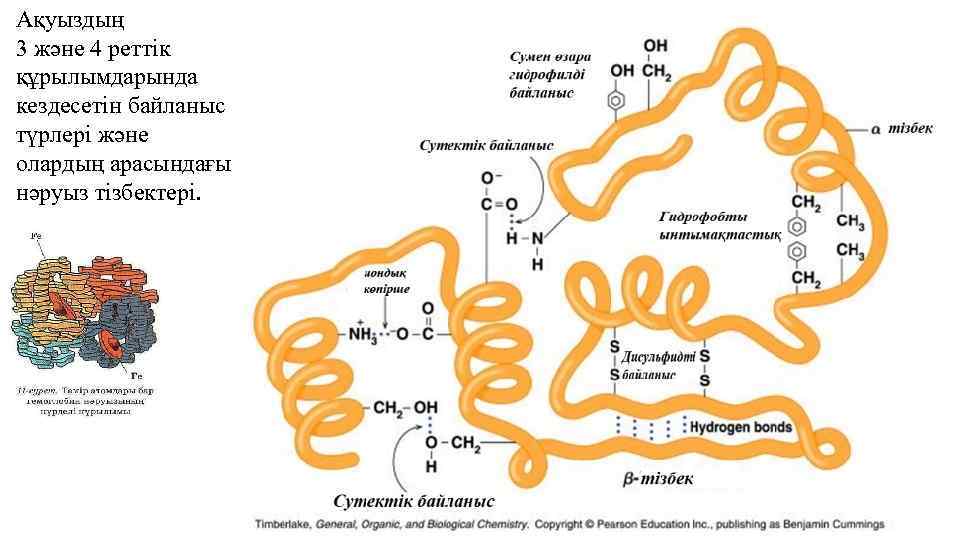
Ақуыздың 3 және 4 реттік құрылымдарында кездесетін байланыс түрлері және олардың арасындағы нәруыз тізбектері.

Денатурация – (табиғатын жоғалту немесе бұрыңғы қалпынан айырылу) бұзылу. Ренатурация- егер нәруыз бірінші реттік құрылымы бұзылмаса (пептидтік байланыс) аминқышқылдарының барлығының арасындағы пептидтік байланыс сақталса, онда қалпына келу үдерісі –ренатурация болуы да мүмкін. Нәруызға әр түрлі факторлардың Нәруыздың өзгеріске ұшырауы. әсері. Қыздыру немесе сәулелену Инфрақызыл, ультракүлгін сәулелер әсерінен әлсіз сутектік , иондық байланыстар ажырап нәруыз ұйып (коагулияция) Күшті қышқылдар, сілтілер, тұздар иондық байланыстар ажырап нәруыз ұйып (коагулияция)қалады, ұзаққа созылса құрылымы бұзылып, пептидтік байланыстар үзіледі. Ауыр металдар Ерігіштігін төмендетеді, нәтижесінде нәруыз тұнбаға түседі. Гидрофобтық қасиетін жояды, сутектік байланыстар үзіледі, спирттің әсерінен кез келген бактерия әсерінен белок денатурацияға ұшырайды. Органикалық еріткіштер немесе детергенттер.
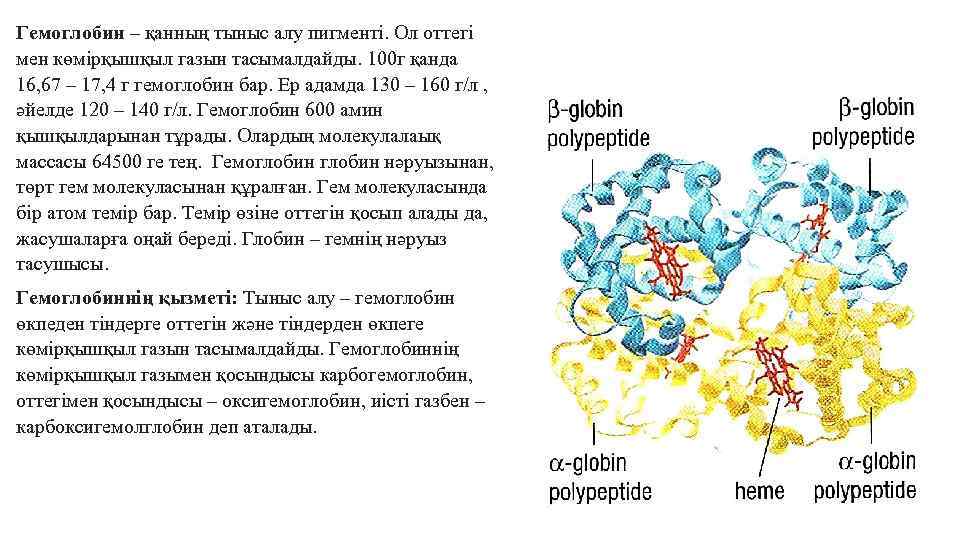
Гемоглобин – қанның тыныс алу пигменті. Ол оттегі мен көмірқышқыл газын тасымалдайды. 100 г қанда 16, 67 – 17, 4 г гемоглобин бар. Ер адамда 130 – 160 г/л , әйелде 120 – 140 г/л. Гемоглобин 600 амин қышқылдарынан тұрады. Олардың молекулалаық массасы 64500 ге тең. Гемоглобин нәруызынан, төрт гем молекуласынан құралған. Гем молекуласында бір атом темір бар. Темір өзіне оттегін қосып алады да, жасушаларға оңай береді. Глобин – гемнің нәруыз тасушысы. Гемоглобиннің қызметі: Тыныс алу – гемоглобин өкпеден тіндерге оттегін және тіндерден өкпеге көмірқышқыл газын тасымалдайды. Гемоглобиннің көмірқышқыл газымен қосындысы карбогемоглобин, оттегімен қосындысы – оксигемоглобин, иісті газбен – карбоксигемолглобин деп аталады.
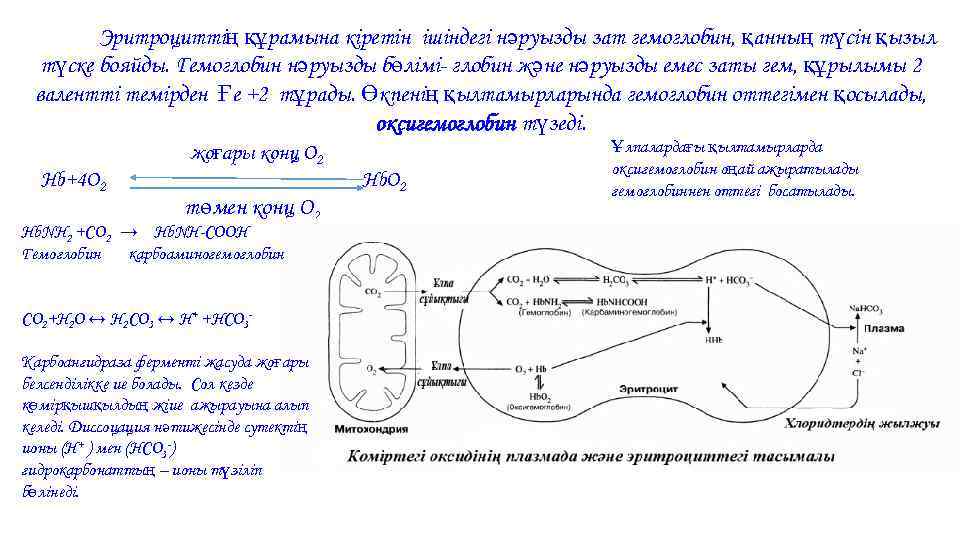
Эритроциттің құрамына кіретін ішіндегі нәруызды зат гемоглобин, қанның түсін қызыл түске бояйды. Гемоглобин нәруызды бөлімі- глобин және нәруызды емес заты гем, құрылымы 2 валентті темірден Ғе +2 тұрады. Өкпенің қылтамырларында гемоглобин оттегімен қосылады, оксигемоглобин түзеді. Hb+4 O 2 жоғары конц О 2 төмен конц О 2 Hb. NH 2 +CO 2 → Hb. NH-COOH Гемоглобин карбоаминогемоглобин СО 2+Н 2 О ↔ Н 2 СО 3 ↔ Н+ +НСО 3 - Карбоангидраза ферменті жасуда жоғары белсенділікке ие болады. Сол кезде көмірқышқылдың жіие ажырауына алып келеді. Диссоцация нәтижесінде сутектің ионы (Н+ ) мен (НСО 3 -) гидрокарбонаттың – ионы түзіліп бөлінеді. Hb. О 2 Ұлпалардағы қылтамырларда оксигемоглобин оңай ажыратылады гемоглобиннен оттегі босатылады.
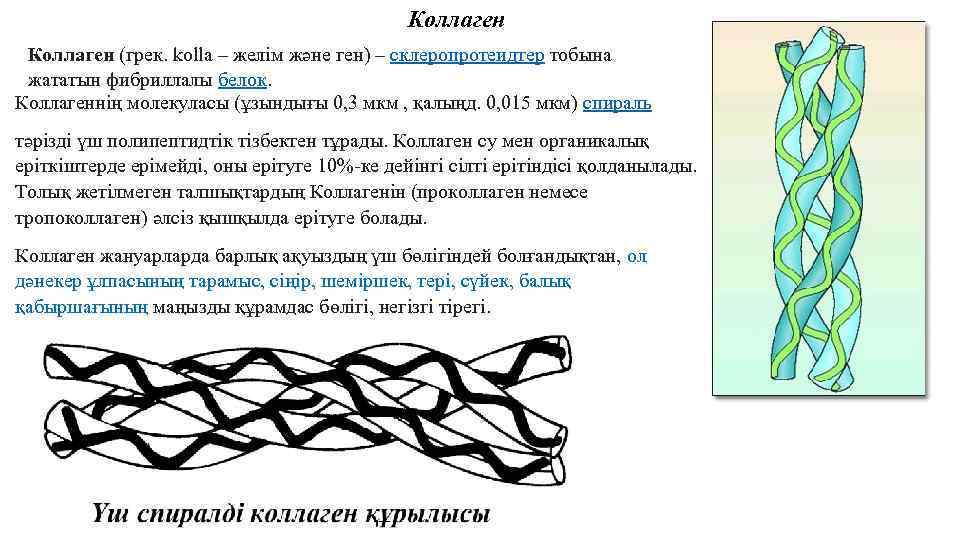
Коллаген (грек. kolla – желім және ген) – склеропротеидтер тобына жататын фибриллалы белок. Коллагеннің молекуласы (ұзындығы 0, 3 мкм , қалыңд. 0, 015 мкм) спираль тәрізді үш полипептидтік тізбектен тұрады. Коллаген су мен органикалық еріткіштерде ерімейді, оны ерітуге 10%-ке дейінгі сілті ерітіндісі қолданылады. Толық жетілмеген талшықтардың Коллагенін (проколлаген немесе тропоколлаген) әлсіз қышқылда ерітуге болады. Коллаген жануарларда барлық ақуыздың үш бөлігіндей болғандықтан, ол дәнекер ұлпасының тарамыс, сіңір, шеміршек, тері, сүйек, балық қабыршағының маңызды құрамдас бөлігі, негізгі тірегі.

Адам мен жануарлардың дәнекер тінінің (ұлпасының) талшығын коллаген талшықтары деп атайды. Оның негізі коллаген ақуызынан тұрады. Коллаген талшығының жуандығы. 1 – 12 мкм, ал диам. 0, 3 – 0, 5 мкм, тармақталған фибрилла жіпшелерінен тұрады. Ал фибриллалар жуанд. 0, 04 мкм микрофибриллалардан құралады. Коллаген талшығында проколлаген не тропоколлаген молекуласы микрофибриллалардың ұзына бойына қара, ашық түсті болып кезектесіп орналасады. Коллаген талшықтарының серпімділігі нашар, олар шеміршекте болса – хондриондық, сүйектен табылса – оссейндік талшықтар деп аталады. Коллаген типті ақуыздар сүтқоректілердің терісінен (ретикулин), көздің шыны тәрізді денесінен (витрозин), сүйекті және шеміршекті балықтардың, маржандардың, губкалардың тінінен (спонгин, горгонин, антипатин) алынған. Өсімдіктерде Коллаген кездеспейді. Илік заттар Коллагеннің химиялық және физикалық, сондай-ақ, бактериялық әсерлерге беріктігін арттырады, тері илеу осы қасиетке негізделген. Көптеген бактерия уларының қауіпті әрекеті, организмдегі тіршілік үшін маңызы зор қосылыстардың бүлінуі коллагеноза ферментінің әрекетіне байланысты. Дәнекер ұлпаның (Коллаген талшықтарының) морфолгиялық белгілерінің өзгеруіне байланысты пайда болатын сырқаттарды коллагеноздар деп атайды
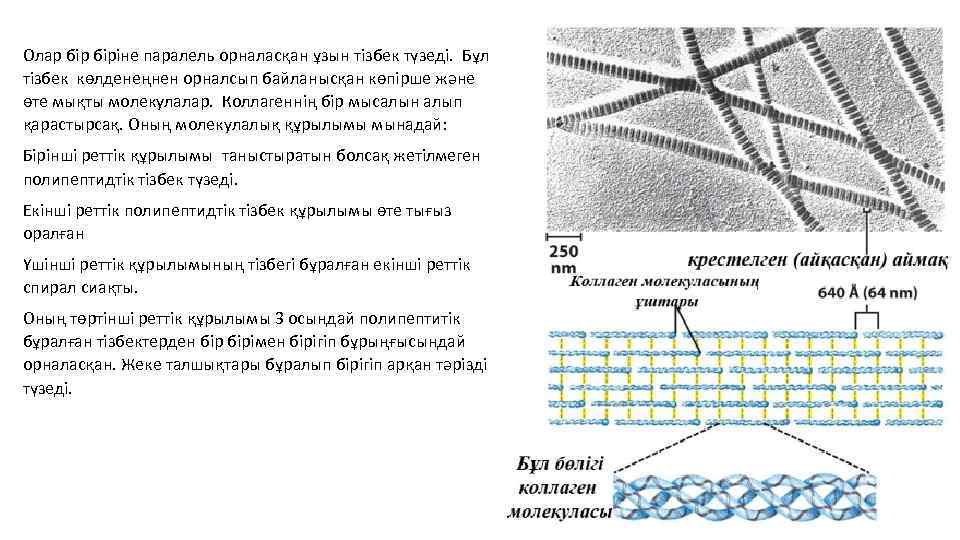
Олар біріне паралель орналасқан ұзын тізбек түзеді. Бұл тізбек көлденеңнен орналсып байланысқан көпірше және өте мықты молекулалар. Коллагеннің бір мысалын алып қарастырсақ. Оның молекулалық құрылымы мынадай: Бірінші реттік құрылымы таныстыратын болсақ жетілмеген полипептидтік тізбек түзеді. Екінші реттік полипептидтік тізбек құрылымы өте тығыз оралған Үшінші реттік құрылымының тізбегі бұралған екінші реттік спирал сиақты. Оның төртінші реттік құрылымы 3 осындай полипептитік бұралған тізбектерден бірімен бірігіп бұрыңғысындай орналасқан. Жеке талшықтары бұралып бірігіп арқан тәрізді түзеді.

Коллагеннің маңызы Ол үлкен молекулалылы нәруызды бұранда, олар біріктіруші ұлпаларды жақсы деңгейде сақтайды және адамның нәруызының жалпы массасының 1/3 құрайды. Олар өте жоғары беріктікке ие болады және олар созылмайды. Әр түрлі ұлпаларға әртүрлі әсер етеді коллаген түрлері. Оның қызметі. Қорғаныштық- Ұлпалардың мықтылығын және механикалық соғылудан қорғайды. Тірек —Мүшелердің формасын біріктіреді және бекітеді скрепление и формирование формы органов; Қалпына келтіреді (Жасушалық регенерация) ұлпаның созылғыштығын сонымен қатар талшықтардың созылғыштығын қамтамассыз етеді. Меланомның (қатерлі ісікті) дамуын тоқтатады. (опухолевидные образования кожи); Жасуша қабықшасының түзылуын ынталандырады.
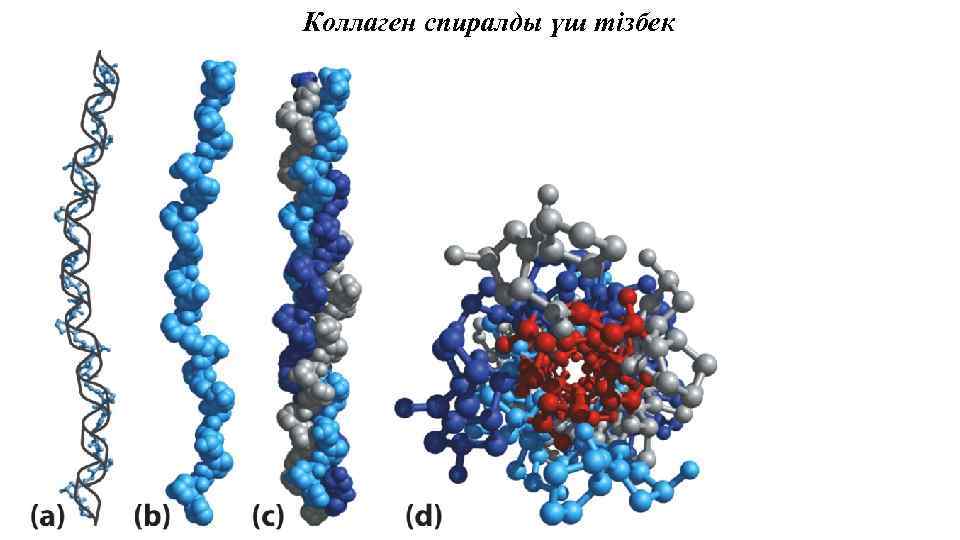
Коллаген спиралды үш тізбек
Гемоглобин.pptx