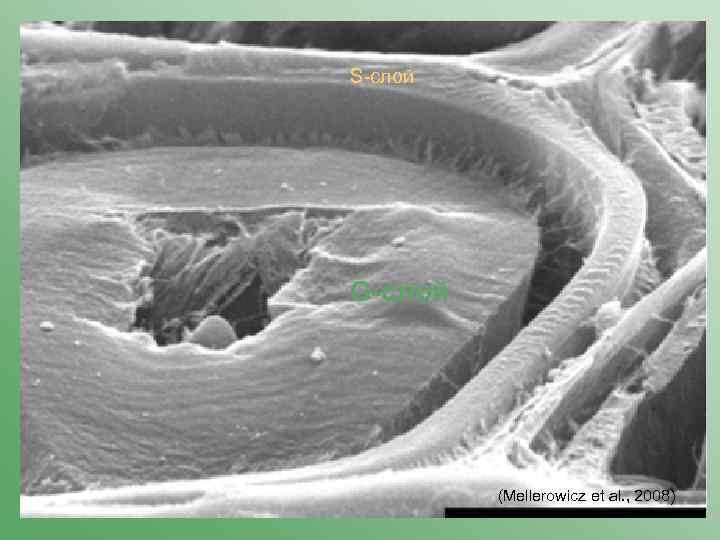
 S-слой G-слой (Mellerowicz et al. , 2008)
S-слой G-слой (Mellerowicz et al. , 2008)
 Растение способно осуществлять работу по перемещению отдельных частей в пространстве и/или формировать натяжение. В растениях существуют структуры, обладающие контрактильными свойствами.
Растение способно осуществлять работу по перемещению отдельных частей в пространстве и/или формировать натяжение. В растениях существуют структуры, обладающие контрактильными свойствами.
 Наиболее известный пример – реакционная древесина. Древесина натяжения (tension wood) формируется в ходе механического стресса и способствует возвращению ствола в вертикальное положение Эвкалипт (Eucalyptus sp. ) Paux et al. , 2005)
Наиболее известный пример – реакционная древесина. Древесина натяжения (tension wood) формируется в ходе механического стресса и способствует возвращению ствола в вертикальное положение Эвкалипт (Eucalyptus sp. ) Paux et al. , 2005)

 Beilschmiedia taraire
Beilschmiedia taraire
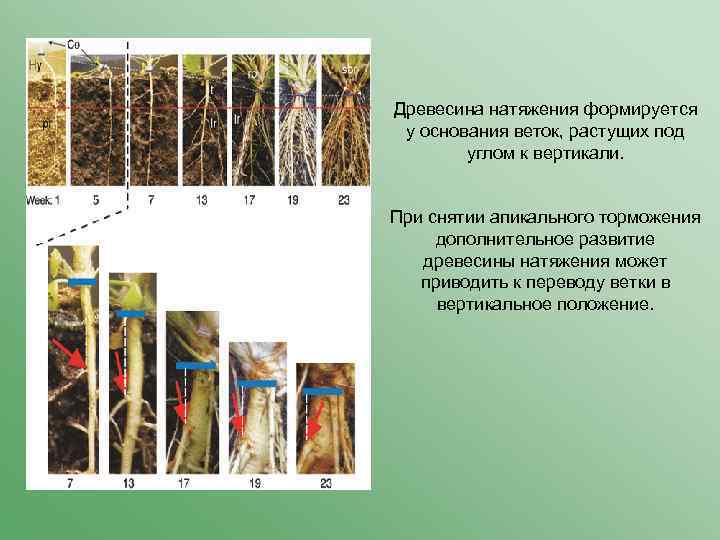 Древесина натяжения формируется у основания веток, растущих под углом к вертикали. При снятии апикального торможения дополнительное развитие древесины натяжения может приводить к переводу ветки в вертикальное положение.
Древесина натяжения формируется у основания веток, растущих под углом к вертикали. При снятии апикального торможения дополнительное развитие древесины натяжения может приводить к переводу ветки в вертикальное положение.
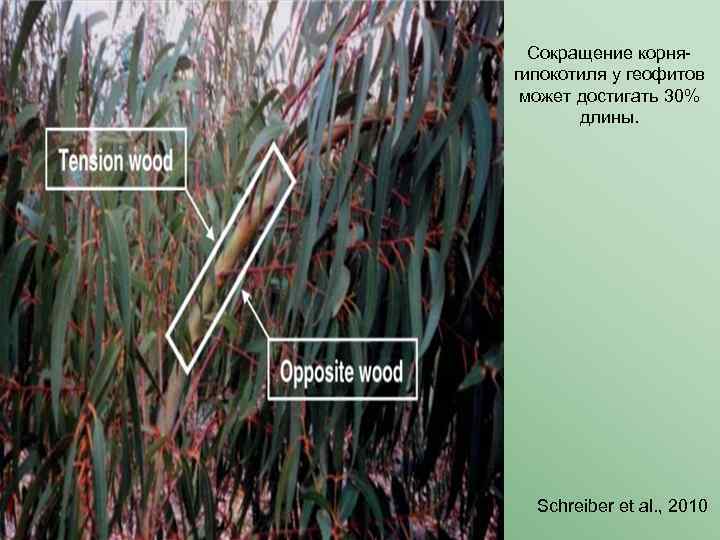 Сокращение корнягипокотиля у геофитов может достигать 30% длины. Schreiber et al. , 2010
Сокращение корнягипокотиля у геофитов может достигать 30% длины. Schreiber et al. , 2010
 У тонкостебельных высоких растений стебель приобретает свойства пружины, что позволяет противостоять, например, ветру.
У тонкостебельных высоких растений стебель приобретает свойства пружины, что позволяет противостоять, например, ветру.
 У льна хорошо выражена способность возвращать стебель в вертикальное положение Гравитропические ответы растений льна хорошо выражены в любом месте стебля благодаря желатинозным волокнам
У льна хорошо выражена способность возвращать стебель в вертикальное положение Гравитропические ответы растений льна хорошо выражены в любом месте стебля благодаря желатинозным волокнам

 Баньян (дерево-роща) – растение, ветви и ствол которого образуют множественные воздушные корни, которые достигают земли, укореняются (натягиваясь) и становятся дополнительным стволом. Одно дерево может иметь несколько сотен стволов и занимать значительную площадь.
Баньян (дерево-роща) – растение, ветви и ствол которого образуют множественные воздушные корни, которые достигают земли, укореняются (натягиваясь) и становятся дополнительным стволом. Одно дерево может иметь несколько сотен стволов и занимать значительную площадь.
 Какие структуры обеспечивают формирование контрактильных свойств?
Какие структуры обеспечивают формирование контрактильных свойств?
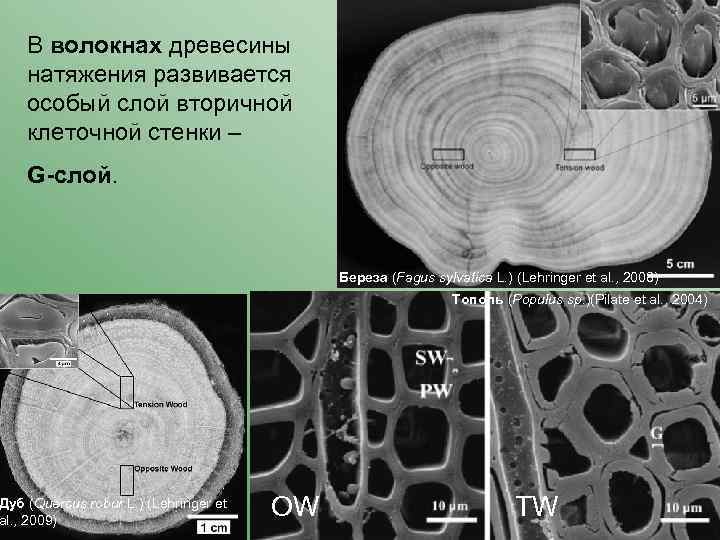 В волокнах древесины натяжения развивается особый слой вторичной клеточной стенки – G-слой. Дуб (Quercus robur L. ) (Lehringer et al. , 2009) Береза (Fagus sylvatica L. ) (Lehringer et al. , 2008) Тополь (Populus sp. )(Pilate et al. , 2004) OW TW
В волокнах древесины натяжения развивается особый слой вторичной клеточной стенки – G-слой. Дуб (Quercus robur L. ) (Lehringer et al. , 2009) Береза (Fagus sylvatica L. ) (Lehringer et al. , 2008) Тополь (Populus sp. )(Pilate et al. , 2004) OW TW
 Способность к натяжению пропорциональна степени развития волокон, содержащих в клеточной стенке G-слои «Мускулы» Фикус Бенджамина (Ficus benjamina L. ) (Zimmermann et al. , 1968)
Способность к натяжению пропорциональна степени развития волокон, содержащих в клеточной стенке G-слои «Мускулы» Фикус Бенджамина (Ficus benjamina L. ) (Zimmermann et al. , 1968)
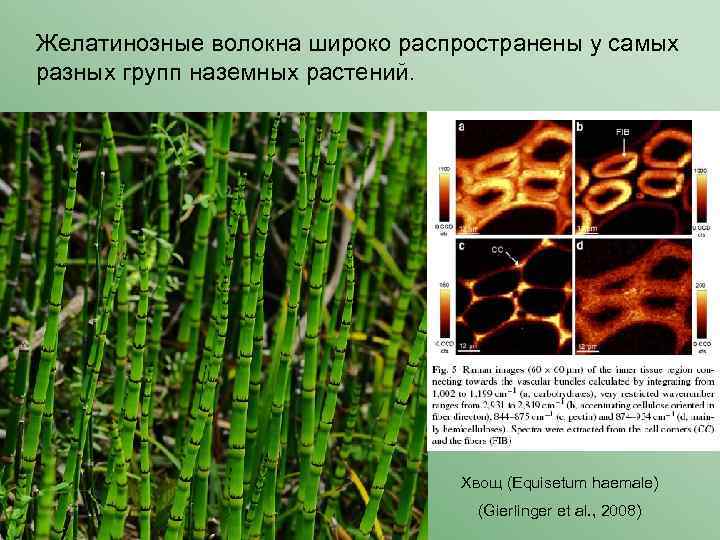 Желатинозные волокна широко распространены у самых разных групп наземных растений. Хвощ (Equisetum haemale) (Gierlinger et al. , 2008)
Желатинозные волокна широко распространены у самых разных групп наземных растений. Хвощ (Equisetum haemale) (Gierlinger et al. , 2008)
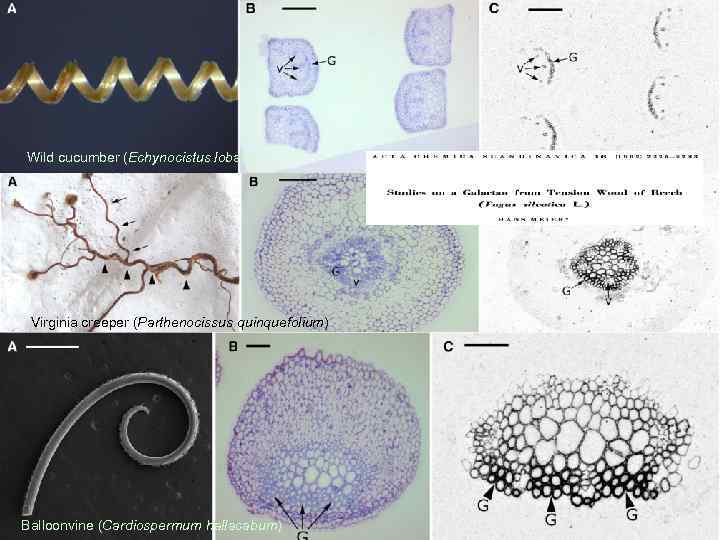 Wild cucumber (Echynocistus lobata) Virginia creeper (Parthenocissus quinquefolium) Balloonvine (Cardiospermum hallacabum)
Wild cucumber (Echynocistus lobata) Virginia creeper (Parthenocissus quinquefolium) Balloonvine (Cardiospermum hallacabum)
 Конопля (Cannabis sativa) Лен (Linum usitatissimum) Желатинозные волокна
Конопля (Cannabis sativa) Лен (Linum usitatissimum) Желатинозные волокна

 Способность формировать желатинозные волокна присуща многим, если не всем, наземным растениям. G-слои встречаются в различных органах. Но всегда – только в волокнах – т. е. специализированных клетках склеренхимы.
Способность формировать желатинозные волокна присуща многим, если не всем, наземным растениям. G-слои встречаются в различных органах. Но всегда – только в волокнах – т. е. специализированных клетках склеренхимы.
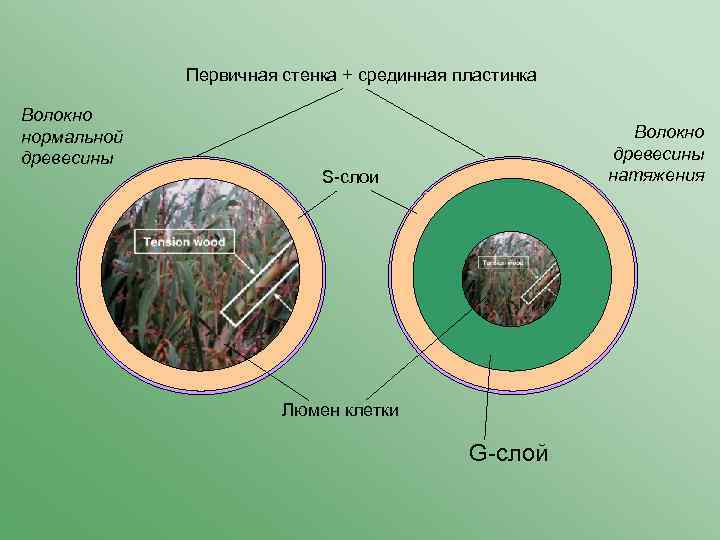 Первичная стенка + срединная пластинка Волокно нормальной древесины Волокно древесины натяжения S-слои Люмен клетки G-слой
Первичная стенка + срединная пластинка Волокно нормальной древесины Волокно древесины натяжения S-слои Люмен клетки G-слой
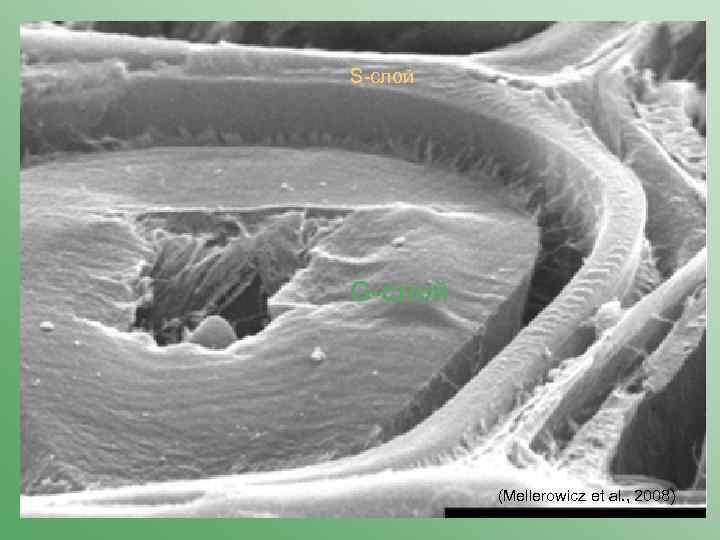 S-слой G-слой (Mellerowicz et al. , 2008)
S-слой G-слой (Mellerowicz et al. , 2008)
 Для G-слоев характерно наличие контрактильных свойств
Для G-слоев характерно наличие контрактильных свойств

 За счет чего в клеточной стенке желатинозного типа возникает натяжение?
За счет чего в клеточной стенке желатинозного типа возникает натяжение?
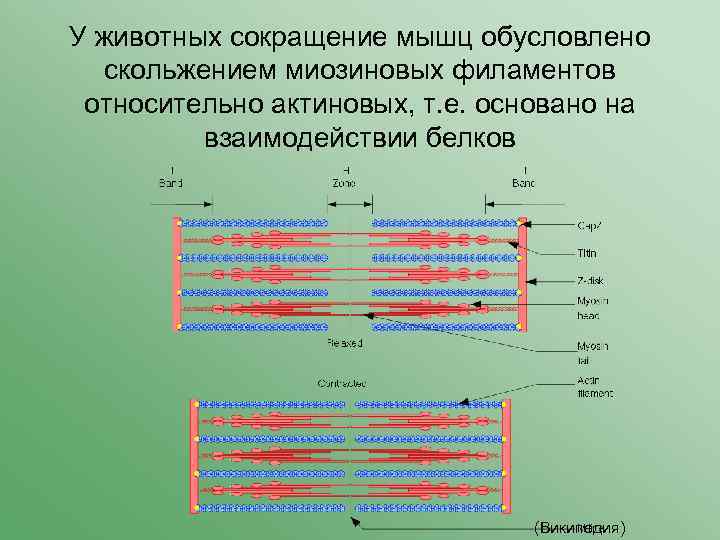 У животных сокращение мышц обусловлено скольжением миозиновых филаментов относительно актиновых, т. е. основано на взаимодействии белков (Википедия)
У животных сокращение мышц обусловлено скольжением миозиновых филаментов относительно актиновых, т. е. основано на взаимодействии белков (Википедия)
 У растений способность проявлять контрактильные свойства пропорциональна степени развития волокон, содержащих в клеточной стенке G-слои. «Мускулы» формируются на основе взаимодействия полисахаридов Похожие слова: Миофибриллы -микрофибриллы Мышечные волокна - растительные волокна
У растений способность проявлять контрактильные свойства пропорциональна степени развития волокон, содержащих в клеточной стенке G-слои. «Мускулы» формируются на основе взаимодействия полисахаридов Похожие слова: Миофибриллы -микрофибриллы Мышечные волокна - растительные волокна
 Что отличает G-слои от «обычной» вторичной клеточной стенки? 1) Состав (нет лигнина, нет ксилана, ~90% - целлюлоза); 2) Расположение микрофибрилл целлюлозы (вдоль клетки, а не по спирали); 3) Повышенная степень кристалличности целлюлозы и увеличенный размер кристаллита; 4) Толщина клеточной стенки (до 10 -15 мкм вместо 1 -2 мкм) 5) Высокое содержание воды. Свойства геля.
Что отличает G-слои от «обычной» вторичной клеточной стенки? 1) Состав (нет лигнина, нет ксилана, ~90% - целлюлоза); 2) Расположение микрофибрилл целлюлозы (вдоль клетки, а не по спирали); 3) Повышенная степень кристалличности целлюлозы и увеличенный размер кристаллита; 4) Толщина клеточной стенки (до 10 -15 мкм вместо 1 -2 мкм) 5) Высокое содержание воды. Свойства геля.
 Демонстрация состава слоев клеточной стенки с помощью Рамановской спектроскопии
Демонстрация состава слоев клеточной стенки с помощью Рамановской спектроскопии
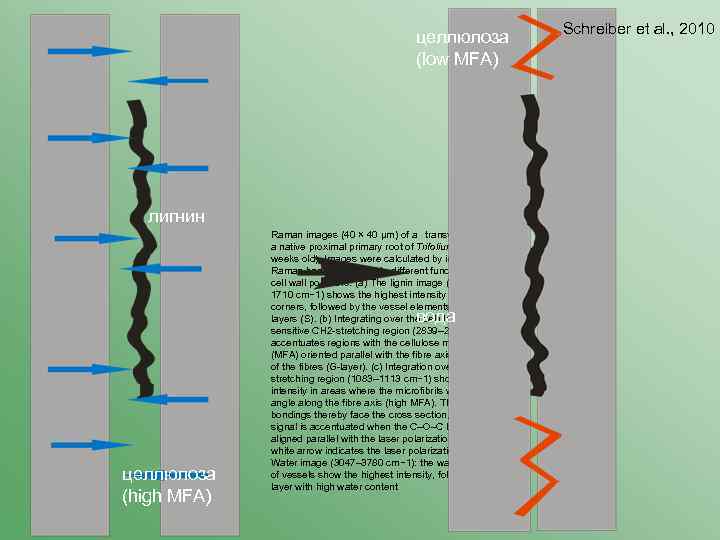 целлюлоза (low MFA) лигнин Raman images (40 × 40 μm) of a transverse section of a native proximal primary root of Trifolium pratense (7 weeks old). Images were calculated by integrating over Raman bands attributed to different functional groups of cell wall polymers. (a) The lignin image (1560– 1710 cm− 1) shows the highest intensity in the cell corners, followed by the vessel elements (ve) and Slayers (S). (b) Integrating over the cellulose orientationsensitive CH 2 -stretching region (2839– 2937 cm− 1) accentuates regions with the cellulose microfibril angle (MFA) oriented parallel with the fibre axis: the inner part of the fibres (G-layer). (c) Integration over the C–O–C stretching region (1083– 1113 cm− 1) shows high intensity in areas where the microfibrils wind with an angle along the fibre axis (high MFA). The C–O–C bondings thereby face the cross section, and the Raman signal is accentuated when the C–O–C bonding is aligned parallel with the laser polarization direction (the white arrow indicates the laser polarization direction). (d) Water image (3047– 3780 cm− 1): the water-filled lumen of vessels show the highest intensity, followed by a Glayer with high water content вода целлюлоза (high MFA) Schreiber et al. , 2010
целлюлоза (low MFA) лигнин Raman images (40 × 40 μm) of a transverse section of a native proximal primary root of Trifolium pratense (7 weeks old). Images were calculated by integrating over Raman bands attributed to different functional groups of cell wall polymers. (a) The lignin image (1560– 1710 cm− 1) shows the highest intensity in the cell corners, followed by the vessel elements (ve) and Slayers (S). (b) Integrating over the cellulose orientationsensitive CH 2 -stretching region (2839– 2937 cm− 1) accentuates regions with the cellulose microfibril angle (MFA) oriented parallel with the fibre axis: the inner part of the fibres (G-layer). (c) Integration over the C–O–C stretching region (1083– 1113 cm− 1) shows high intensity in areas where the microfibrils wind with an angle along the fibre axis (high MFA). The C–O–C bondings thereby face the cross section, and the Raman signal is accentuated when the C–O–C bonding is aligned parallel with the laser polarization direction (the white arrow indicates the laser polarization direction). (d) Water image (3047– 3780 cm− 1): the water-filled lumen of vessels show the highest intensity, followed by a Glayer with high water content вода целлюлоза (high MFA) Schreiber et al. , 2010
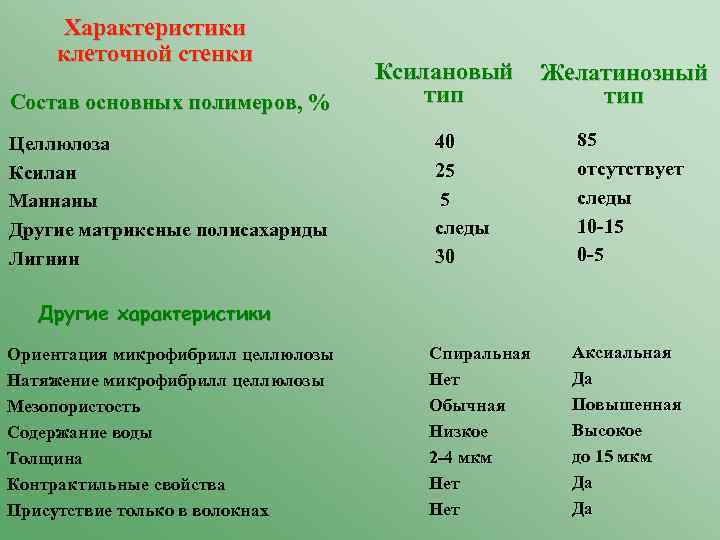 Характеристики клеточной стенки Состав основных полимеров, % Целлюлоза Ксилан Маннаны Другие матриксные полисахариды Лигнин Ксилановый тип 40 25 5 следы 30 Желатинозный тип 85 отсутствует следы 10 -15 0 -5 Другие характеристики Ориентация микрофибрилл целлюлозы Натяжение микрофибрилл целлюлозы Мезопористость Содержание воды Толщина Контрактильные свойства Присутствие только в волокнах Спиральная Нет Обычная Низкое 2 -4 мкм Нет Аксиальная Да Повышенная Высокое до 15 мкм Да Да
Характеристики клеточной стенки Состав основных полимеров, % Целлюлоза Ксилан Маннаны Другие матриксные полисахариды Лигнин Ксилановый тип 40 25 5 следы 30 Желатинозный тип 85 отсутствует следы 10 -15 0 -5 Другие характеристики Ориентация микрофибрилл целлюлозы Натяжение микрофибрилл целлюлозы Мезопористость Содержание воды Толщина Контрактильные свойства Присутствие только в волокнах Спиральная Нет Обычная Низкое 2 -4 мкм Нет Аксиальная Да Повышенная Высокое до 15 мкм Да Да
 Идея 1 Натяжение создается за счет различий в набухании G и S-слоев, которые определяются различиями в ориентации микрофибрилл целлюлозы
Идея 1 Натяжение создается за счет различий в набухании G и S-слоев, которые определяются различиями в ориентации микрофибрилл целлюлозы
 Продольная ориентация микрофибрилл целлюлозы установлена с помощью: 1) Рентгеноструктурного анализа с использованием синхротрона (Muller et al. , 2006); 2) Рентгеноструктурного анализа – широкоугольное рассеивание (WAXS) (Goswami et al. 2008); 3) Рамановской спектроскопии (Gierlinger and Schwanninger, 2006; Schreiber et al. , 2010); 4) 4) Электронной микроскопии (Prodhan et al. , 1995; Lehringer et al. , 1995).
Продольная ориентация микрофибрилл целлюлозы установлена с помощью: 1) Рентгеноструктурного анализа с использованием синхротрона (Muller et al. , 2006); 2) Рентгеноструктурного анализа – широкоугольное рассеивание (WAXS) (Goswami et al. 2008); 3) Рамановской спектроскопии (Gierlinger and Schwanninger, 2006; Schreiber et al. , 2010); 4) 4) Электронной микроскопии (Prodhan et al. , 1995; Lehringer et al. , 1995).
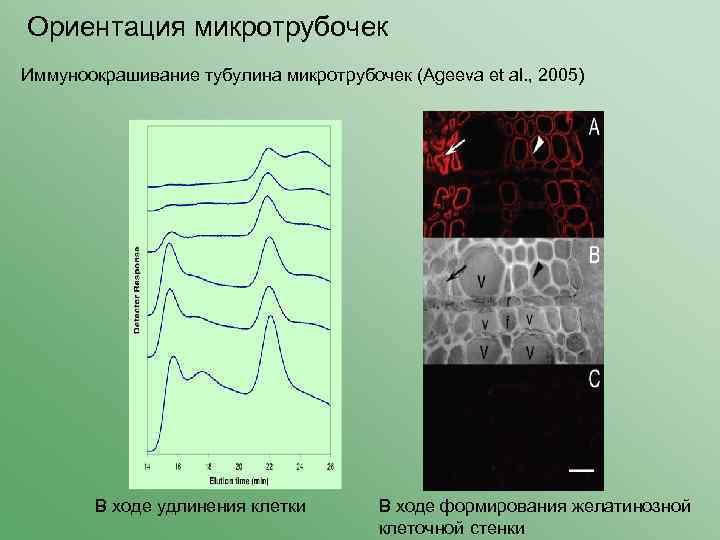 Ориентация микротрубочек Иммуноокрашивание тубулина микротрубочек (Ageeva et al. , 2005) В ходе удлинения клетки В ходе формирования желатинозной клеточной стенки
Ориентация микротрубочек Иммуноокрашивание тубулина микротрубочек (Ageeva et al. , 2005) В ходе удлинения клетки В ходе формирования желатинозной клеточной стенки
 Ориентация микрофибрилл целлюлозы существенно влияет на свойства клеточных стенок Tensile deformation of an hypothetic composite of extremely stiff (essentially undeformable) fibrils (gray) in a soft matrix (white). (A) Isostrain case: both fibrils and matrix are strained equally, which means that no extension is possible, (B) Isostress case: fibrils and matrix are stressed equally and the extension is due to the stretching of the soft matrix, (C) Intermediate case: deformation occurs by matrix shear; the stiffness of the composite depends on the angle of the fibrils with respect to the direction of stretching. The box that deforms into a more complex shape visualizes the deformation pattern. (Burgert, Fratzl 2009) Сопротивляемость клеточной стенки растяжению зависит от ориентации микрофибрилл целлюлозы. Микрофибриллы целлюлозы сами по себе практически не растягиваются. Schematic stress–strain-curves of cell walls, which show the influence of the orientation of the cellulose microfibril on the deformation behavior of plant tissues. The respective microfibril angles in the S 2 layers are indicated by the black lines in the cylindrical cells. Кривая зависимости деформаций от напряжений при разной ориентации микрофибрилл и сходном количестве полимеров матрикса.
Ориентация микрофибрилл целлюлозы существенно влияет на свойства клеточных стенок Tensile deformation of an hypothetic composite of extremely stiff (essentially undeformable) fibrils (gray) in a soft matrix (white). (A) Isostrain case: both fibrils and matrix are strained equally, which means that no extension is possible, (B) Isostress case: fibrils and matrix are stressed equally and the extension is due to the stretching of the soft matrix, (C) Intermediate case: deformation occurs by matrix shear; the stiffness of the composite depends on the angle of the fibrils with respect to the direction of stretching. The box that deforms into a more complex shape visualizes the deformation pattern. (Burgert, Fratzl 2009) Сопротивляемость клеточной стенки растяжению зависит от ориентации микрофибрилл целлюлозы. Микрофибриллы целлюлозы сами по себе практически не растягиваются. Schematic stress–strain-curves of cell walls, which show the influence of the orientation of the cellulose microfibril on the deformation behavior of plant tissues. The respective microfibril angles in the S 2 layers are indicated by the black lines in the cylindrical cells. Кривая зависимости деформаций от напряжений при разной ориентации микрофибрилл и сходном количестве полимеров матрикса.
 Клеточные стенки с различной ориентацией микрофибрилл целлюлозы по-разному набухают (A)Клеточные стенки с продольным расположением микрофибрилл укорачиваются. (B) Клеточные стенки со спиральным расположением микрофибрилл удлиняются. (Burgert et al. 2007)
Клеточные стенки с различной ориентацией микрофибрилл целлюлозы по-разному набухают (A)Клеточные стенки с продольным расположением микрофибрилл укорачиваются. (B) Клеточные стенки со спиральным расположением микрофибрилл удлиняются. (Burgert et al. 2007)
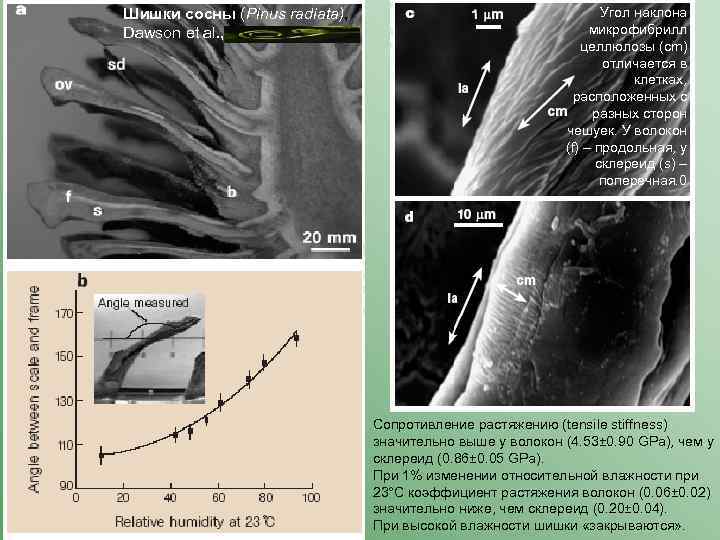 Шишки сосны (Pinus radiata), Dawson et al. , Угол наклона микрофибрилл целлюлозы (cm) отличается в клетках, расположенных с разных сторон чешуек. У волокон (f) – продольная, у склереид (s) – поперечная. 0 Сопротивление растяжению (tensile stiffness) значительно выше у волокон (4. 53± 0. 90 GPa), чем у склереид (0. 86± 0. 05 GPa). При 1% изменении относительной влажности при 23°C коэффициент растяжения волокон (0. 06± 0. 02) значительно ниже, чем склереид (0. 20± 0. 04). При высокой влажности шишки «закрываются» .
Шишки сосны (Pinus radiata), Dawson et al. , Угол наклона микрофибрилл целлюлозы (cm) отличается в клетках, расположенных с разных сторон чешуек. У волокон (f) – продольная, у склереид (s) – поперечная. 0 Сопротивление растяжению (tensile stiffness) значительно выше у волокон (4. 53± 0. 90 GPa), чем у склереид (0. 86± 0. 05 GPa). При 1% изменении относительной влажности при 23°C коэффициент растяжения волокон (0. 06± 0. 02) значительно ниже, чем склереид (0. 20± 0. 04). При высокой влажности шишки «закрываются» .
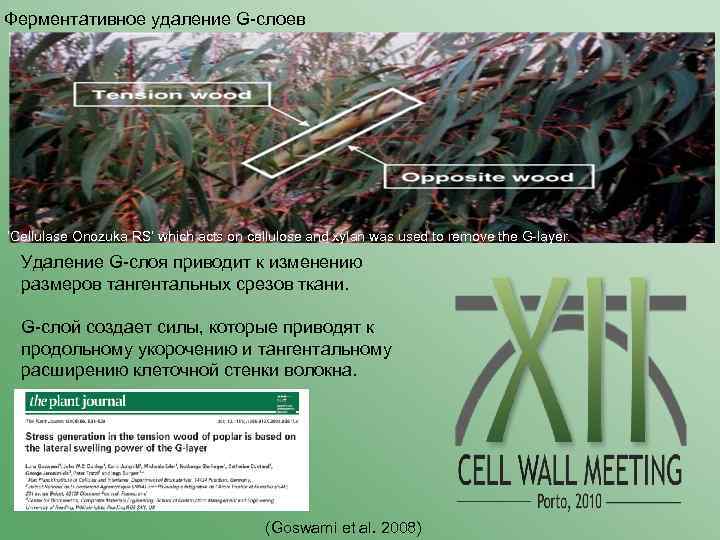 Ферментативное удаление G-слоев The orientation of cellulose microfibrils in the tension wood fibres was measured by wide-angle X -ray scattering (WAXS). In the presence of the G-layer, the wide-angle scattering signal of untreated tension wood mainly originates from the axially orientated, highly cystalline cellulose fibrils of the G-layer (Figure 1 c, left) which overshadows the much weaker signal from the other cell wall layers. Removal of the G-layer facilitated the measurement of the orientation of the cellulose in the surrounding secondary cell wall. An angle of the cellulose fibrils with respect to the cell axis (the MFA) of l 36 was calculated from the WAXS patterns of the treated samples (Figure 1 c, right). ‘Cellulase Onozuka RS’ which acts on cellulose and xylan was used to remove the G-layer. Удаление G-слоя приводит к изменению размеров тангентальных срезов ткани. G-слой создает силы, которые приводят к продольному укорочению и тангентальному расширению клеточной стенки волокна. (Goswami et al. 2008)
Ферментативное удаление G-слоев The orientation of cellulose microfibrils in the tension wood fibres was measured by wide-angle X -ray scattering (WAXS). In the presence of the G-layer, the wide-angle scattering signal of untreated tension wood mainly originates from the axially orientated, highly cystalline cellulose fibrils of the G-layer (Figure 1 c, left) which overshadows the much weaker signal from the other cell wall layers. Removal of the G-layer facilitated the measurement of the orientation of the cellulose in the surrounding secondary cell wall. An angle of the cellulose fibrils with respect to the cell axis (the MFA) of l 36 was calculated from the WAXS patterns of the treated samples (Figure 1 c, right). ‘Cellulase Onozuka RS’ which acts on cellulose and xylan was used to remove the G-layer. Удаление G-слоя приводит к изменению размеров тангентальных срезов ткани. G-слой создает силы, которые приводят к продольному укорочению и тангентальному расширению клеточной стенки волокна. (Goswami et al. 2008)
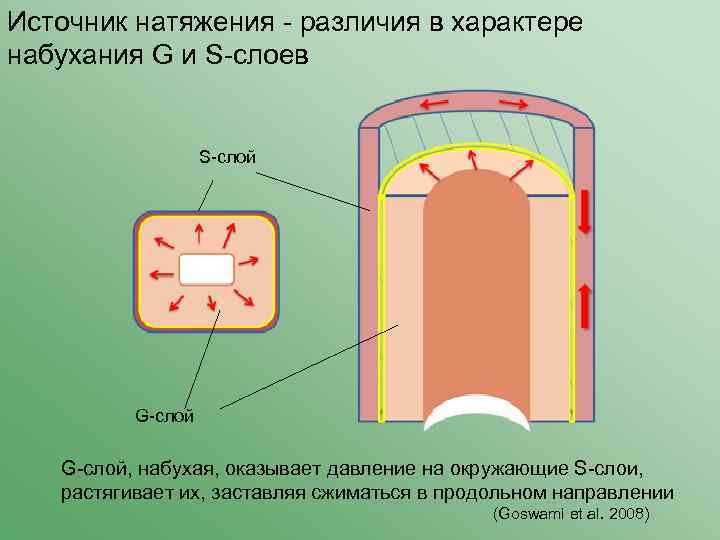 Источник натяжения - различия в характере набухания G и S-слоев S-слой G-слой, набухая, оказывает давление на окружающие S-слои, растягивает их, заставляя сжиматься в продольном направлении (Goswami et al. 2008)
Источник натяжения - различия в характере набухания G и S-слоев S-слой G-слой, набухая, оказывает давление на окружающие S-слои, растягивает их, заставляя сжиматься в продольном направлении (Goswami et al. 2008)
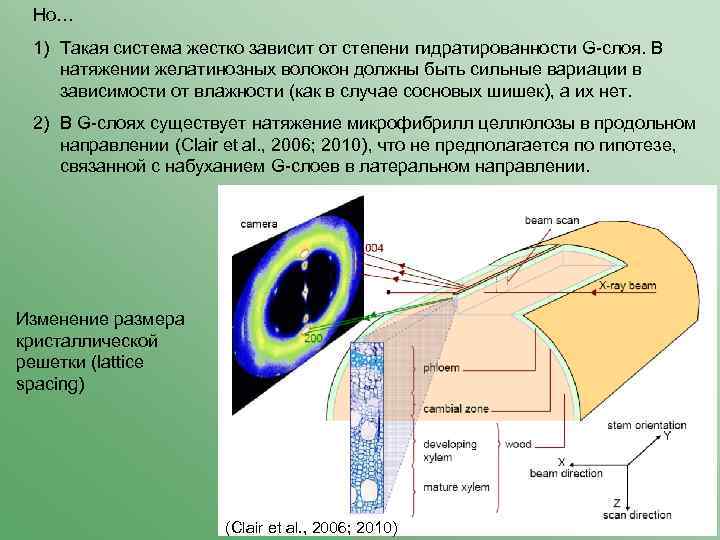 Но… 1) Такая система жестко зависит от степени гидратированности G-слоя. В натяжении желатинозных волокон должны быть сильные вариации в зависимости от влажности (как в случае сосновых шишек), а их нет. 2) В G-слоях существует натяжение микрофибрилл целлюлозы в продольном направлении (Сlair et al. , 2006; 2010), что не предполагается по гипотезе, связанной с набуханием G-слоев в латеральном направлении. Изменение размера кристаллической решетки (lattice spacing) (Сlair et al. , 2006; 2010)
Но… 1) Такая система жестко зависит от степени гидратированности G-слоя. В натяжении желатинозных волокон должны быть сильные вариации в зависимости от влажности (как в случае сосновых шишек), а их нет. 2) В G-слоях существует натяжение микрофибрилл целлюлозы в продольном направлении (Сlair et al. , 2006; 2010), что не предполагается по гипотезе, связанной с набуханием G-слоев в латеральном направлении. Изменение размера кристаллической решетки (lattice spacing) (Сlair et al. , 2006; 2010)
 Но… 1) Такая система жестко зависит от степени гидратированности G-слоя. В натяжении желатинозных волокон должны быть сильные вариации в зависимости от влажности (как в случае сосновых шишек), а их нет. 2) В G-слоях существует натяжение микрофибрилл целлюлозы в продольном направлении (Сlair et al. , 2006; 2010), что не предполагается по гипотезе, связанной с набуханием G-слоев в латеральном направлении 3) Для желатинозных слоев характерна мезопористость: наличие пор диаметром от 2 до 50 нм, площадь поверхности которых в единице объема в десятки раз выше, чем в S-слоях (Clair et al. , 2008; Chang et al. , 2009). 4) При инициации G-слоя происходит активация экспрессии ферментов метаболизма полисахаридов матрикса. 5) Иммуноцитохимический анализ выявляет в G-слоях присутствие полисахаридов матрикса
Но… 1) Такая система жестко зависит от степени гидратированности G-слоя. В натяжении желатинозных волокон должны быть сильные вариации в зависимости от влажности (как в случае сосновых шишек), а их нет. 2) В G-слоях существует натяжение микрофибрилл целлюлозы в продольном направлении (Сlair et al. , 2006; 2010), что не предполагается по гипотезе, связанной с набуханием G-слоев в латеральном направлении 3) Для желатинозных слоев характерна мезопористость: наличие пор диаметром от 2 до 50 нм, площадь поверхности которых в единице объема в десятки раз выше, чем в S-слоях (Clair et al. , 2008; Chang et al. , 2009). 4) При инициации G-слоя происходит активация экспрессии ферментов метаболизма полисахаридов матрикса. 5) Иммуноцитохимический анализ выявляет в G-слоях присутствие полисахаридов матрикса
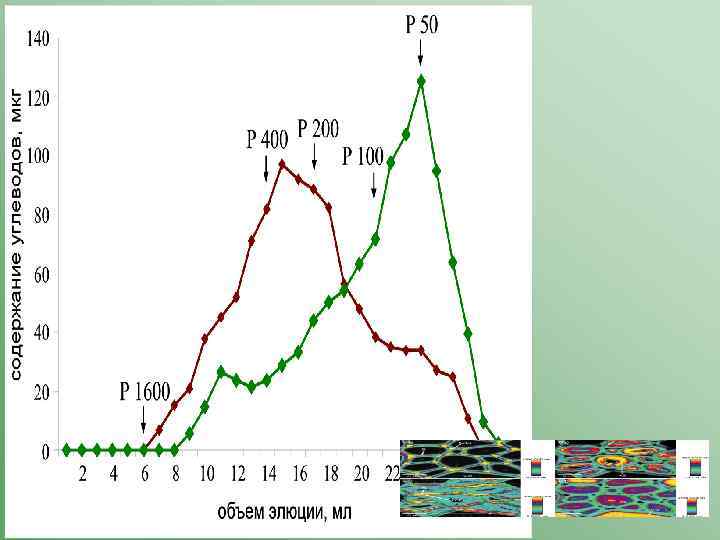
 Идея 2 В создании натяжения участвуют полисахариды матрикса клеточной стенки
Идея 2 В создании натяжения участвуют полисахариды матрикса клеточной стенки
 Аргументы в пользу присутствия тех или иных полисахаридов в G-слоях 1. Иммуноцитохимическая локализация (не всегда все выявляет из-за высокой кристалличности целлюлозы) 2. Биохимическое выделение (нужно изолировать G-слои не только от клеточной стенки других тканей, но и от других слов клеточной стенки волокон) 3. Анализ динамики отложения (если гликопротеид – микрочипы, если полисахарид – pulse-chase подходы).
Аргументы в пользу присутствия тех или иных полисахаридов в G-слоях 1. Иммуноцитохимическая локализация (не всегда все выявляет из-за высокой кристалличности целлюлозы) 2. Биохимическое выделение (нужно изолировать G-слои не только от клеточной стенки других тканей, но и от других слов клеточной стенки волокон) 3. Анализ динамики отложения (если гликопротеид – микрочипы, если полисахарид – pulse-chase подходы).
 Полисахариды матрикса, присутствие которых в G-слоях можно предполагать по данным, полученным с использованием разных подходов: Арабиногалактановые белки Ксилоглюкан Рамногалактуронан I
Полисахариды матрикса, присутствие которых в G-слоях можно предполагать по данным, полученным с использованием разных подходов: Арабиногалактановые белки Ксилоглюкан Рамногалактуронан I
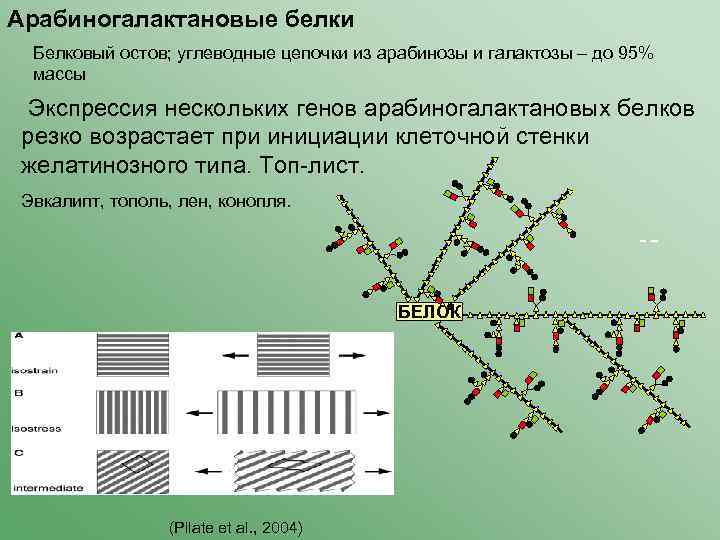 Арабиногалактановые белки Белковый остов; углеводные цепочки из арабинозы и галактозы – до 95% массы Экспрессия нескольких генов арабиногалактановых белков резко возрастает при инициации клеточной стенки желатинозного типа. Топ-лист. Эвкалипт, тополь, лен, конопля. БЕЛОК (Pilate et al. , 2004)
Арабиногалактановые белки Белковый остов; углеводные цепочки из арабинозы и галактозы – до 95% массы Экспрессия нескольких генов арабиногалактановых белков резко возрастает при инициации клеточной стенки желатинозного типа. Топ-лист. Эвкалипт, тополь, лен, конопля. БЕЛОК (Pilate et al. , 2004)
 Структура арабиногалактана в древесине натяжения и в нормальной древесине отличается
Структура арабиногалактана в древесине натяжения и в нормальной древесине отличается
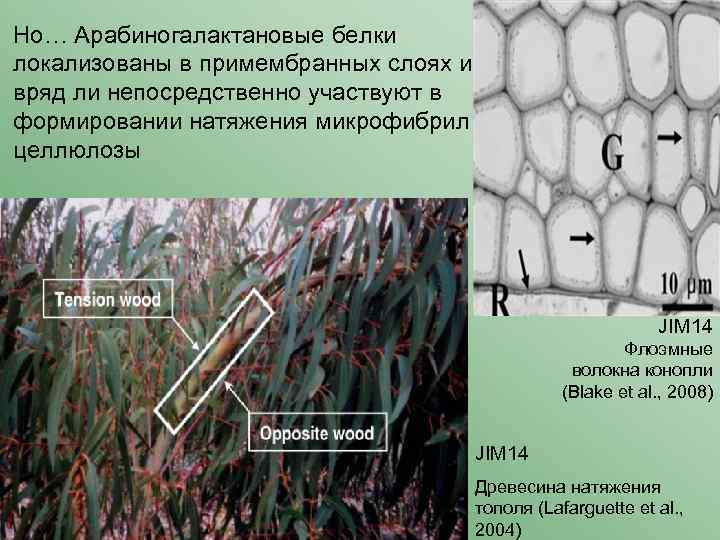 Но… Арабиногалактановые белки локализованы в примембранных слоях и вряд ли непосредственно участвуют в формировании натяжения микрофибрил целлюлозы JIM 14 Флоэмные волокна конопли (Blake et al. , 2008) JIM 14 Древесина натяжения тополя (Lafarguette et al. , 2004)
Но… Арабиногалактановые белки локализованы в примембранных слоях и вряд ли непосредственно участвуют в формировании натяжения микрофибрил целлюлозы JIM 14 Флоэмные волокна конопли (Blake et al. , 2008) JIM 14 Древесина натяжения тополя (Lafarguette et al. , 2004)
 Ксилоглюкан Нейтральный полисахарид регулярного строения. Остов из глюкана, боковые цепочки из одиночных остатков ксилозы, иногда соединенний с галактозой и, далее, с фукозой. α-(1→ 6)-D-Xylp β-(1→ 2)-D-Galp β-(1→ 4)-D-Glcp α-(1→ 2)-L-Fucp Наиболее распространенный связующий гликан первичной клеточной стенки. Наличие в G-слоях древесины натяжения доказано биохимически.
Ксилоглюкан Нейтральный полисахарид регулярного строения. Остов из глюкана, боковые цепочки из одиночных остатков ксилозы, иногда соединенний с галактозой и, далее, с фукозой. α-(1→ 6)-D-Xylp β-(1→ 2)-D-Galp β-(1→ 4)-D-Glcp α-(1→ 2)-L-Fucp Наиболее распространенный связующий гликан первичной клеточной стенки. Наличие в G-слоях древесины натяжения доказано биохимически.
 В древесине натяжения всегда хорошо выражены S-слои. G-слой можно отделить с помощью ультразвука (Nishikubo et al. , 2007)
В древесине натяжения всегда хорошо выражены S-слои. G-слой можно отделить с помощью ультразвука (Nishikubo et al. , 2007)
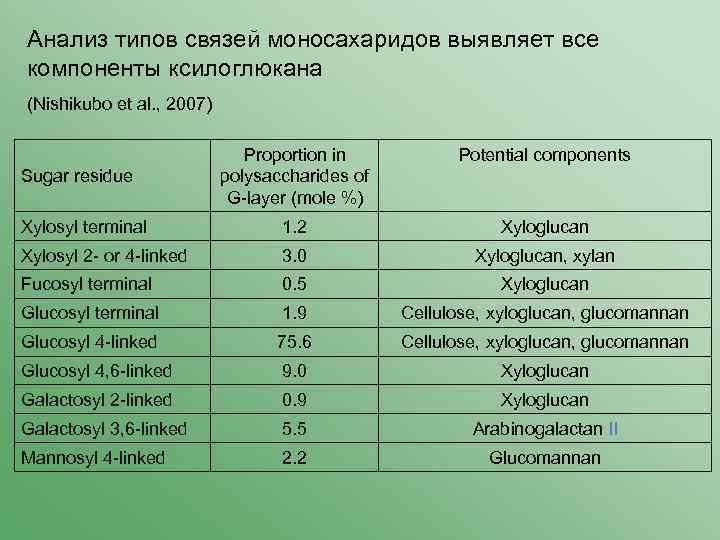 Анализ типов связей моносахаридов выявляет все компоненты ксилоглюкана (Nishikubo et al. , 2007) Proportion in polysaccharides of G-layer (mole %) Potential components Xylosyl terminal 1. 2 Xyloglucan Xylosyl 2 - or 4 -linked 3. 0 Xyloglucan, xylan Fucosyl terminal 0. 5 Xyloglucan Glucosyl terminal 1. 9 Cellulose, xyloglucan, glucomannan Glucosyl 4 -linked 75. 6 Cellulose, xyloglucan, glucomannan Glucosyl 4, 6 -linked 9. 0 Xyloglucan Galactosyl 2 -linked 0. 9 Xyloglucan Galactosyl 3, 6 -linked 5. 5 Arabinogalactan II Mannosyl 4 -linked 2. 2 Glucomannan Sugar residue
Анализ типов связей моносахаридов выявляет все компоненты ксилоглюкана (Nishikubo et al. , 2007) Proportion in polysaccharides of G-layer (mole %) Potential components Xylosyl terminal 1. 2 Xyloglucan Xylosyl 2 - or 4 -linked 3. 0 Xyloglucan, xylan Fucosyl terminal 0. 5 Xyloglucan Glucosyl terminal 1. 9 Cellulose, xyloglucan, glucomannan Glucosyl 4 -linked 75. 6 Cellulose, xyloglucan, glucomannan Glucosyl 4, 6 -linked 9. 0 Xyloglucan Galactosyl 2 -linked 0. 9 Xyloglucan Galactosyl 3, 6 -linked 5. 5 Arabinogalactan II Mannosyl 4 -linked 2. 2 Glucomannan Sugar residue
 Локализация активности ХЕТ с помощью флюорогенного субстрата в развивающейся древесине натяжения. Окрашиваются только волокна с формирующимся G-слоем; клетки паренхимы и сосуды не окрашиваются. Внизу – после кипячения ткани окрашивание не проявляется
Локализация активности ХЕТ с помощью флюорогенного субстрата в развивающейся древесине натяжения. Окрашиваются только волокна с формирующимся G-слоем; клетки паренхимы и сосуды не окрашиваются. Внизу – после кипячения ткани окрашивание не проявляется
 В трансгенных растениях, содержащих ген фермента, расщепляющего ксилоглюкан, снижены контрактильные свойства G-слоев (Hayashi et al. , 2010)
В трансгенных растениях, содержащих ген фермента, расщепляющего ксилоглюкан, снижены контрактильные свойства G-слоев (Hayashi et al. , 2010)
 Но… 1) В G-слоях флоэмных волокон ксилоглюкан не выявляется; 2) Во флоэмных волокнах S-слой может быть выражен крайне слабо, как у льна и рами. 3) В развивающихся волокнах древесины натяжения активность ХЕТ выявляется, в основном в G-слое, а в более зрелых – только в S-слоях. (Mellerowicz et al. , 2008) Ксилоглюкан необходим для соединения G- и S-слоев в древесине натяжения
Но… 1) В G-слоях флоэмных волокон ксилоглюкан не выявляется; 2) Во флоэмных волокнах S-слой может быть выражен крайне слабо, как у льна и рами. 3) В развивающихся волокнах древесины натяжения активность ХЕТ выявляется, в основном в G-слое, а в более зрелых – только в S-слоях. (Mellerowicz et al. , 2008) Ксилоглюкан необходим для соединения G- и S-слоев в древесине натяжения
 Идея 2 а Натяжение возникает в G-слое в результате латерального взаимодействия микрофибрилл целлюлозы и захвата полисахаридов матрикса
Идея 2 а Натяжение возникает в G-слое в результате латерального взаимодействия микрофибрилл целлюлозы и захвата полисахаридов матрикса
 Аргументы: 1) В G-слоях отмечается увеличенный размер кристаллитов целлюлозы (Muller et al. , 2006). На «поперечном срезе» кристаллита примерно четыре «обычные» микрофибриллы. 2) В G-слоях отсутствует лигнин, а содержание полисахаридов матрикса очень низко – ничто не препятствует латеральному взаимодействию микрофибрилл целлюлозы. 3) В G-слоях увеличено содержание полисахаридов, прочно удерживаемых микрофибриллами целлюлозы.
Аргументы: 1) В G-слоях отмечается увеличенный размер кристаллитов целлюлозы (Muller et al. , 2006). На «поперечном срезе» кристаллита примерно четыре «обычные» микрофибриллы. 2) В G-слоях отсутствует лигнин, а содержание полисахаридов матрикса очень низко – ничто не препятствует латеральному взаимодействию микрофибрилл целлюлозы. 3) В G-слоях увеличено содержание полисахаридов, прочно удерживаемых микрофибриллами целлюлозы.
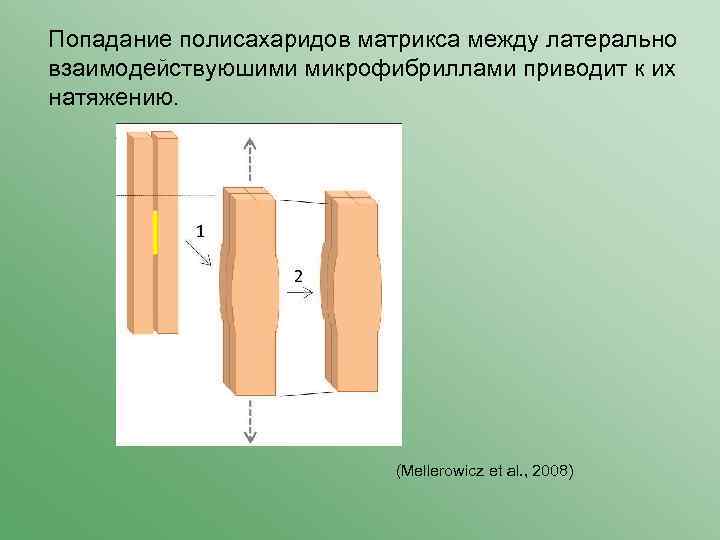 Попадание полисахаридов матрикса между латерально взаимодействуюшими микрофибриллами приводит к их натяжению. (Mellerowicz et al. , 2008)
Попадание полисахаридов матрикса между латерально взаимодействуюшими микрофибриллами приводит к их натяжению. (Mellerowicz et al. , 2008)
 «Запечатываемым» полисахаридом служит ксилоглюкан (Mellerowicz et al. , 2008). Но… 1) В древесине натяжения ксилоглюкан не обнаруживается во фракции полимеров, прочно удерживаемых микрофибриллами целлюлозы; 2) Во флоэмных волокнах ксилоглюкан вообще не обнаруживается; 3) При инициации G-слоя происходит резкая активация экспрессии ферментов метаболизма пектиновых веществ; 4) Простые цитохимические окрашивания выявляют в волокнах древесины натяжения кислые полисахариды.
«Запечатываемым» полисахаридом служит ксилоглюкан (Mellerowicz et al. , 2008). Но… 1) В древесине натяжения ксилоглюкан не обнаруживается во фракции полимеров, прочно удерживаемых микрофибриллами целлюлозы; 2) Во флоэмных волокнах ксилоглюкан вообще не обнаруживается; 3) При инициации G-слоя происходит резкая активация экспрессии ферментов метаболизма пектиновых веществ; 4) Простые цитохимические окрашивания выявляют в волокнах древесины натяжения кислые полисахариды.
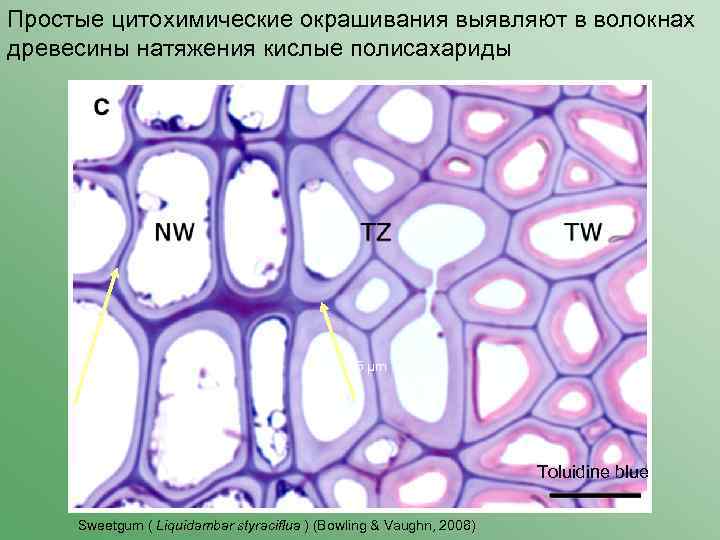 Простые цитохимические окрашивания выявляют в волокнах древесины натяжения кислые полисахариды 25 μm Toluidine blue Sweetgum ( Liquidambar styraciflua ) (Bowling & Vaughn, 2008)
Простые цитохимические окрашивания выявляют в волокнах древесины натяжения кислые полисахариды 25 μm Toluidine blue Sweetgum ( Liquidambar styraciflua ) (Bowling & Vaughn, 2008)
 «Запечатываемым» полисахаридом служит ксилоглюкан (Mellerowicz et al. , 2008). Но… 1) В древесине натяжения ксилоглюкан не обнаруживается во фракции полимеров, прочно удерживаемых микрофибриллами целлюлозы; 2) Во флоэмных волокнах ксилоглюкан вообще не обнаруживается; 3) При инициации G-слоя происходит резкая активация экспрессии ферментов метаболизма пектиновых веществ; 4) Простые цитохимические окрашивания выявляют в волокнах древесины натяжения кислые полисахариды. 5) Ксилоглюкан «не очень подходит» для создания натяжения.
«Запечатываемым» полисахаридом служит ксилоглюкан (Mellerowicz et al. , 2008). Но… 1) В древесине натяжения ксилоглюкан не обнаруживается во фракции полимеров, прочно удерживаемых микрофибриллами целлюлозы; 2) Во флоэмных волокнах ксилоглюкан вообще не обнаруживается; 3) При инициации G-слоя происходит резкая активация экспрессии ферментов метаболизма пектиновых веществ; 4) Простые цитохимические окрашивания выявляют в волокнах древесины натяжения кислые полисахариды. 5) Ксилоглюкан «не очень подходит» для создания натяжения.
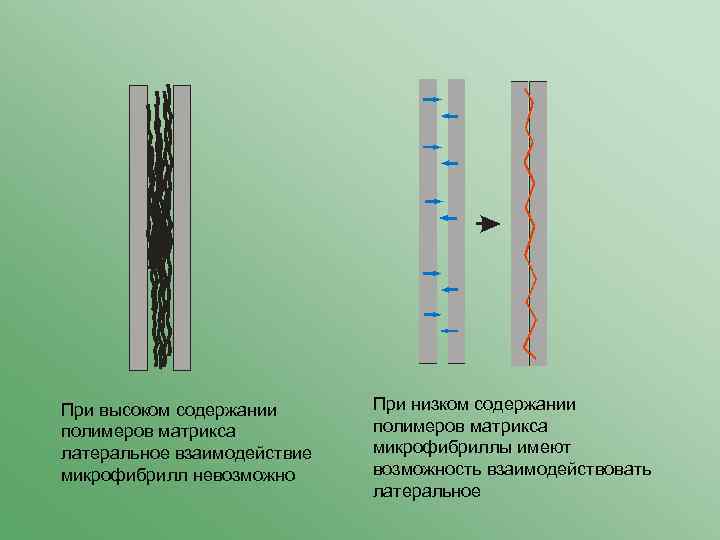 При высоком содержании полимеров матрикса латеральное взаимодействие микрофибрилл невозможно При низком содержании полимеров матрикса микрофибриллы имеют возможность взаимодействовать латеральное
При высоком содержании полимеров матрикса латеральное взаимодействие микрофибрилл невозможно При низком содержании полимеров матрикса микрофибриллы имеют возможность взаимодействовать латеральное
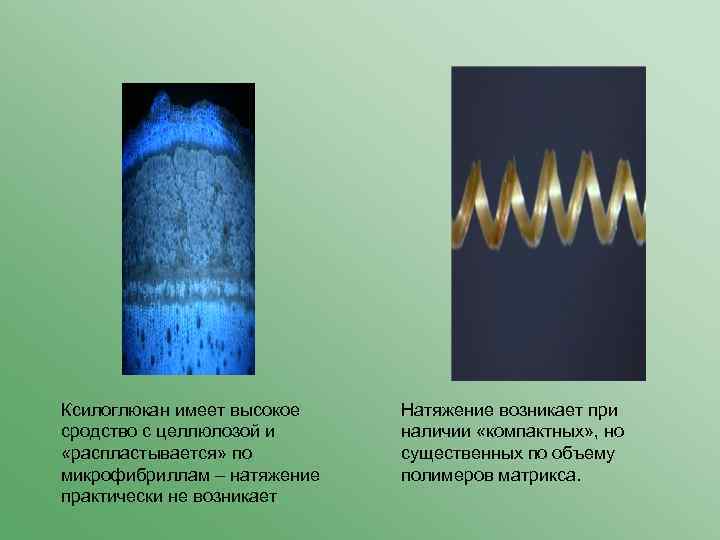 Ксилоглюкан имеет высокое сродство с целлюлозой и «распластывается» по микрофибриллам – натяжение практически не возникает Натяжение возникает при наличии «компактных» , но существенных по объему полимеров матрикса.
Ксилоглюкан имеет высокое сродство с целлюлозой и «распластывается» по микрофибриллам – натяжение практически не возникает Натяжение возникает при наличии «компактных» , но существенных по объему полимеров матрикса.
 Такой полисахарид – рамногалактуронан I сложного строения, способный формировать ассоциаты, слабо взаимодействующие с целлюлозой.
Такой полисахарид – рамногалактуронан I сложного строения, способный формировать ассоциаты, слабо взаимодействующие с целлюлозой.
 Two types of secondary cell wall within flax stem (UV, staining with Cellufluor) Xylem Phloem fibers
Two types of secondary cell wall within flax stem (UV, staining with Cellufluor) Xylem Phloem fibers
 У льна хорошо выражена способность возвращать стебель в вертикальное положение
У льна хорошо выражена способность возвращать стебель в вертикальное положение
 При инициации формирования клеточной стенки желатинозного типа появляется новый полисахарид – высокомолекулярный галактан Galactans SP 1 2 3 4 5 AG(P)s 1 2 3 4 5 6 6 1 cm sections
При инициации формирования клеточной стенки желатинозного типа появляется новый полисахарид – высокомолекулярный галактан Galactans SP 1 2 3 4 5 AG(P)s 1 2 3 4 5 6 6 1 cm sections
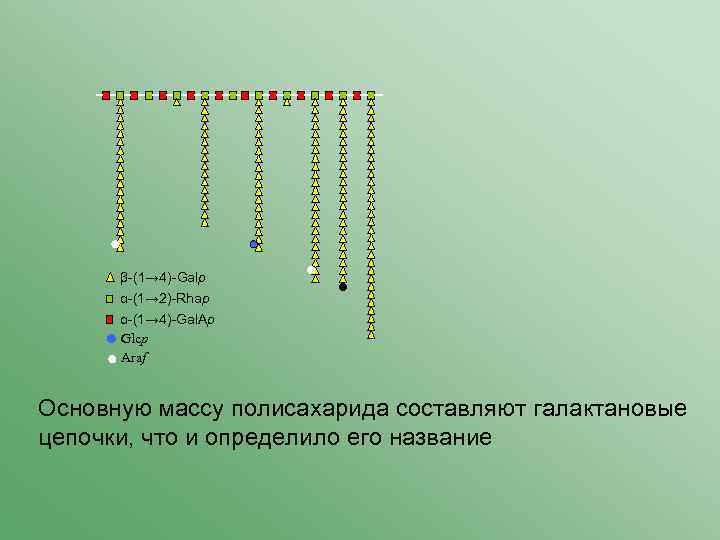 β-(1→ 4)-Galp α-(1→ 2)-Rhap α-(1→ 4)-Gal. Ap Glcp Araf Основную массу полисахарида составляют галактановые цепочки, что и определило его название
β-(1→ 4)-Galp α-(1→ 2)-Rhap α-(1→ 4)-Gal. Ap Glcp Araf Основную массу полисахарида составляют галактановые цепочки, что и определило его название
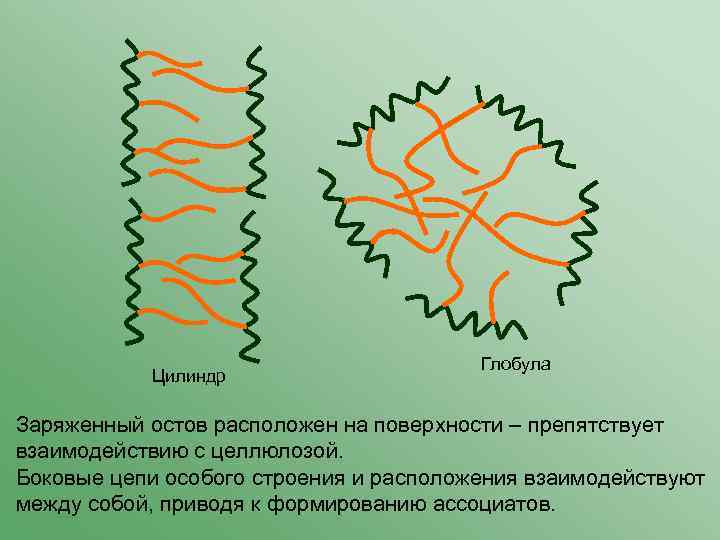 Цилиндр Глобула Заряженный остов расположен на поверхности – препятствует взаимодействию с целлюлозой. Боковые цепи особого строения и расположения взаимодействуют между собой, приводя к формированию ассоциатов.
Цилиндр Глобула Заряженный остов расположен на поверхности – препятствует взаимодействию с целлюлозой. Боковые цепи особого строения и расположения взаимодействуют между собой, приводя к формированию ассоциатов.
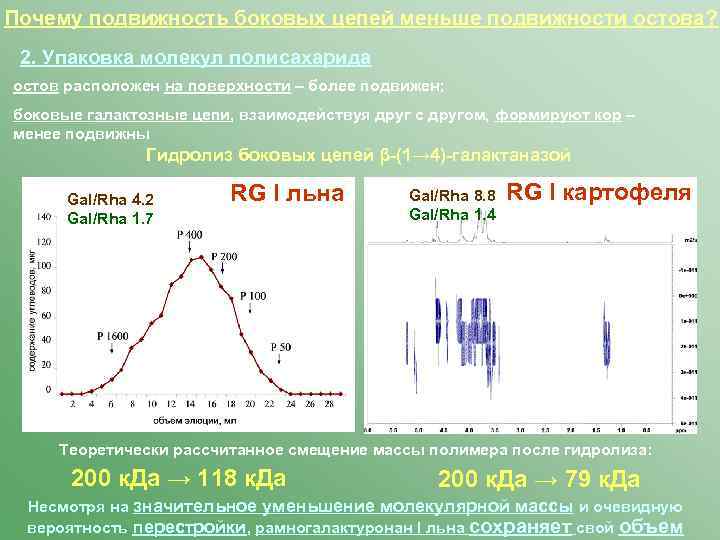 Почему подвижность боковых цепей меньше подвижности остова? 2. Упаковка молекул полисахарида остов расположен на поверхности – более подвижен; боковые галактозные цепи, взаимодействуя друг с другом, формируют кор – менее подвижны Гидролиз боковых цепей β-(1→ 4)-галактаназой Gal/Rha 4. 2 Gal/Rha 1. 7 RG I льна Gal/Rha 8. 8 Gal/Rha 1. 4 RG I картофеля Теоретически рассчитанное смещение массы полимера после гидролиза: 200 к. Да → 118 к. Да 200 к. Да → 79 к. Да Несмотря на значительное уменьшение молекулярной массы и очевидную вероятность перестройки, рамногалактуронан I льна сохраняет свой объем
Почему подвижность боковых цепей меньше подвижности остова? 2. Упаковка молекул полисахарида остов расположен на поверхности – более подвижен; боковые галактозные цепи, взаимодействуя друг с другом, формируют кор – менее подвижны Гидролиз боковых цепей β-(1→ 4)-галактаназой Gal/Rha 4. 2 Gal/Rha 1. 7 RG I льна Gal/Rha 8. 8 Gal/Rha 1. 4 RG I картофеля Теоретически рассчитанное смещение массы полимера после гидролиза: 200 к. Да → 118 к. Да 200 к. Да → 79 к. Да Несмотря на значительное уменьшение молекулярной массы и очевидную вероятность перестройки, рамногалактуронан I льна сохраняет свой объем
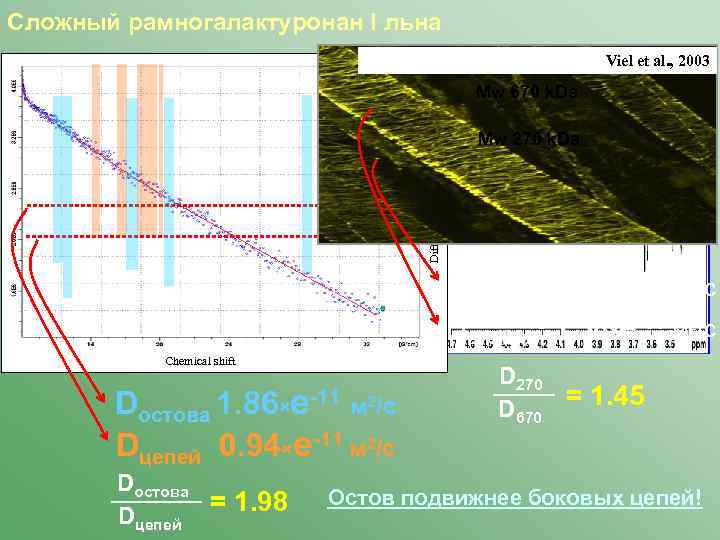 Сложный рамногалактуронан I льна Viel et al. , 2003 Mw 670 k. Da Sepharose CL-4 B Mw 270 k. Da Diffusion coefficient Gal/Rha 4. 2 D 270 k. Da~ 2. 00×e-11 м 2/с D 670 k. Da~ 1. 38×e-11 м 2/с β-(1→ 4)-Galp α-(1→ 2)-Rhap α-(1→ 4)-Gal. Ap Glcp Araf Chemical shift Dостова 1. 86×e-11 м 2/с Dцепей 0. 94×e-11 м 2/с Dостова = 1. 98 Dцепей D 270 = 1. 45 D 670 Остов подвижнее боковых цепей!
Сложный рамногалактуронан I льна Viel et al. , 2003 Mw 670 k. Da Sepharose CL-4 B Mw 270 k. Da Diffusion coefficient Gal/Rha 4. 2 D 270 k. Da~ 2. 00×e-11 м 2/с D 670 k. Da~ 1. 38×e-11 м 2/с β-(1→ 4)-Galp α-(1→ 2)-Rhap α-(1→ 4)-Gal. Ap Glcp Araf Chemical shift Dостова 1. 86×e-11 м 2/с Dцепей 0. 94×e-11 м 2/с Dостова = 1. 98 Dцепей D 270 = 1. 45 D 670 Остов подвижнее боковых цепей!
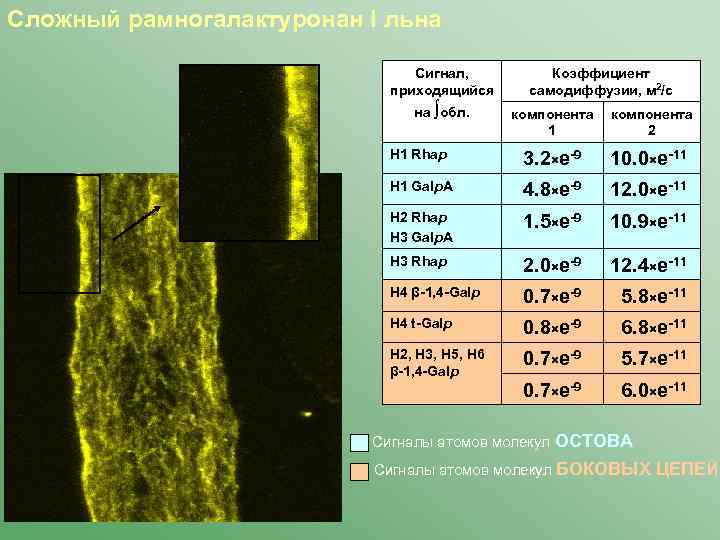 Сложный рамногалактуронан I льна Сигнал, приходящийся на ∫обл. Коэффициент самодиффузии, м 2/с компонента 1 компонента 2 H 1 Rhap 3. 2×e-9 10. 0×e-11 H 1 Galp. A 4. 8×e-9 12. 0×e-11 H 2 Rhap H 3 Galp. A 1. 5×e-9 10. 9×e-11 H 3 Rhap 2. 0×e-9 12. 4×e-11 H 4 β-1, 4 -Galp 0. 7×e-9 5. 8×e-11 H 4 t-Galp 0. 8×e-9 6. 8×e-11 H 2, H 3, H 5, H 6 β-1, 4 -Galp 0. 7×e-9 5. 7×e-11 0. 7×e-9 6. 0×e-11 Сигналы атомов молекул ОСТОВА Сигналы атомов молекул БОКОВЫХ ЦЕПЕЙ
Сложный рамногалактуронан I льна Сигнал, приходящийся на ∫обл. Коэффициент самодиффузии, м 2/с компонента 1 компонента 2 H 1 Rhap 3. 2×e-9 10. 0×e-11 H 1 Galp. A 4. 8×e-9 12. 0×e-11 H 2 Rhap H 3 Galp. A 1. 5×e-9 10. 9×e-11 H 3 Rhap 2. 0×e-9 12. 4×e-11 H 4 β-1, 4 -Galp 0. 7×e-9 5. 8×e-11 H 4 t-Galp 0. 8×e-9 6. 8×e-11 H 2, H 3, H 5, H 6 β-1, 4 -Galp 0. 7×e-9 5. 7×e-11 0. 7×e-9 6. 0×e-11 Сигналы атомов молекул ОСТОВА Сигналы атомов молекул БОКОВЫХ ЦЕПЕЙ
 FLAX NASCENT GALACTAN Sepharose CL-4 B Content of sugar, g 400 1600 Rhamnogalacturonan hydrolase Mw ~ 120 k. D 53 Rha Gal/Rha 92 Mw ~ 35 k. D 2 Rha Mw ~ 20 k. D 6 Rha 400 200 100 50 Vi # fraction Molecular mass of the original polymer is around 265 k. D, the backbone contains 85 dimers of Rha and Gal. Long chains of galactose do not make such structures by themselves. It is necessary to have backbone of certain length.
FLAX NASCENT GALACTAN Sepharose CL-4 B Content of sugar, g 400 1600 Rhamnogalacturonan hydrolase Mw ~ 120 k. D 53 Rha Gal/Rha 92 Mw ~ 35 k. D 2 Rha Mw ~ 20 k. D 6 Rha 400 200 100 50 Vi # fraction Molecular mass of the original polymer is around 265 k. D, the backbone contains 85 dimers of Rha and Gal. Long chains of galactose do not make such structures by themselves. It is necessary to have backbone of certain length.
 Галактаны сложного строения обнаруживали и в древесине натяжения Но в 1966 году Р. Н. Norberg и Н. Meier опубликовали статью, утверждавшую что изолированные G-слои на 98. 5% состоят из целлюлозы (бумажная хроматография). Точка зрения, что G-слои состоят только из целлюлозы, была в течение 40 лет настолько доминирующей, что полисахариды матрикса клеточной стенки вообще не рассматривались при обсуждении механизмов создания натяжения.
Галактаны сложного строения обнаруживали и в древесине натяжения Но в 1966 году Р. Н. Norberg и Н. Meier опубликовали статью, утверждавшую что изолированные G-слои на 98. 5% состоят из целлюлозы (бумажная хроматография). Точка зрения, что G-слои состоят только из целлюлозы, была в течение 40 лет настолько доминирующей, что полисахариды матрикса клеточной стенки вообще не рассматривались при обсуждении механизмов создания натяжения.
 В изолированных их волокон древесины натяжения тополя G -слоях среди нейтральных моносахаридов обнаруживают рамнозу (Nishikubo et al. , 2007)
В изолированных их волокон древесины натяжения тополя G -слоях среди нейтральных моносахаридов обнаруживают рамнозу (Nishikubo et al. , 2007)
 Положения нашей гипотезы: • Натяжение возникает в G-слое в результате латерального взаимодействия микрофибрилл целлюлозы и захвата полисахаридов матрикса. • Латеральное взаимодействие микрофибрилл становится возможным, благодаря исключительно высокому содержанию целлюлозы и отсутствию прослоек из ксилана и лигнина. • Благодаря одинаковой продольной ориентации всех микрофибрилл в толстом G-слое их натяжение суммируется. Исключительная длина волокон усиливает эффект. • Захватываемый полисахарид – сложный рамногалактуронан I, содержащий длинные боковые цепочки особой структуры и расположения, который способен формировать крупные водорастворимые ассоциаты. • Захват крупных образований приводит к формированию микропористости и увеличивает натяжение микрофибрилл. • Высокая гигроскопичность рамногалактуронана способствует удержанию воды в G-слое • Условия для латерального взаимодействия могут создаваться in murо после модификации захватываемого полимера с помощью специальной галактозидазы.
Положения нашей гипотезы: • Натяжение возникает в G-слое в результате латерального взаимодействия микрофибрилл целлюлозы и захвата полисахаридов матрикса. • Латеральное взаимодействие микрофибрилл становится возможным, благодаря исключительно высокому содержанию целлюлозы и отсутствию прослоек из ксилана и лигнина. • Благодаря одинаковой продольной ориентации всех микрофибрилл в толстом G-слое их натяжение суммируется. Исключительная длина волокон усиливает эффект. • Захватываемый полисахарид – сложный рамногалактуронан I, содержащий длинные боковые цепочки особой структуры и расположения, который способен формировать крупные водорастворимые ассоциаты. • Захват крупных образований приводит к формированию микропористости и увеличивает натяжение микрофибрилл. • Высокая гигроскопичность рамногалактуронана способствует удержанию воды в G-слое • Условия для латерального взаимодействия могут создаваться in murо после модификации захватываемого полимера с помощью специальной галактозидазы.
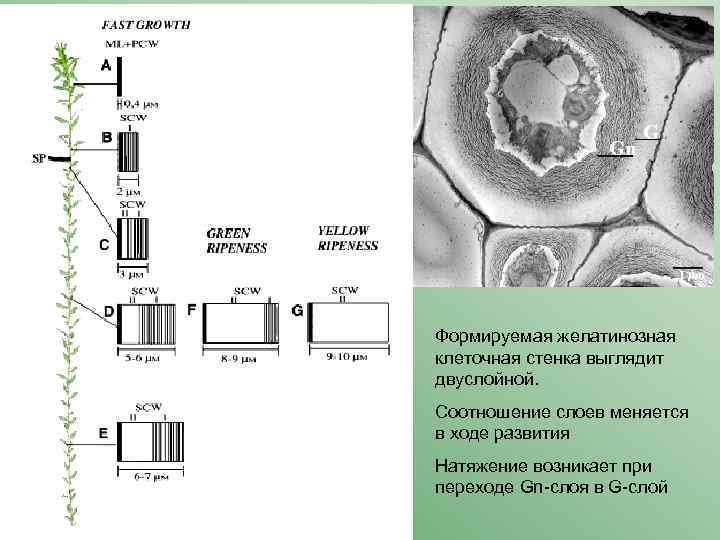 Gn G 1 mm Формируемая желатинозная клеточная стенка выглядит двуслойной. Соотношение слоев меняется в ходе развития Натяжение возникает при переходе Gn-слоя в G-слой
Gn G 1 mm Формируемая желатинозная клеточная стенка выглядит двуслойной. Соотношение слоев меняется в ходе развития Натяжение возникает при переходе Gn-слоя в G-слой
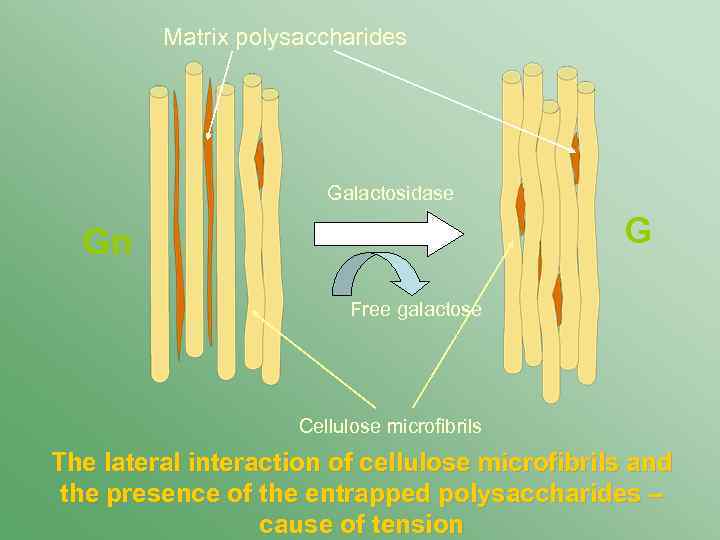 Matrix polysaccharides Galactosidase G Gn Free galactose Cellulose microfibrils The lateral interaction of cellulose microfibrils and the presence of the entrapped polysaccharides – cause of tension
Matrix polysaccharides Galactosidase G Gn Free galactose Cellulose microfibrils The lateral interaction of cellulose microfibrils and the presence of the entrapped polysaccharides – cause of tension
 Трансгенные растения льна со сниженным уровнем экспрессии специфичной -галактозидазы Lu. BGAL-RNAi • Не нарушена общая морфология растения и анатомия стебля. • Снижена экспрессия гена (ОТ-ПЦР) • Снижена активность фермента (хромогенный субстрат). • Снижено содержание свободной галактозы (ВЭЖХ). • Больше галактана легко извлекается из клеточной стенки Контрольные (WT) и трансгенные линии растений льна (4 -2, 6 -1, 6 -2) Трансформация проведена M. Roach, M. Deyholos (Университет Альберты, Канада)
Трансгенные растения льна со сниженным уровнем экспрессии специфичной -галактозидазы Lu. BGAL-RNAi • Не нарушена общая морфология растения и анатомия стебля. • Снижена экспрессия гена (ОТ-ПЦР) • Снижена активность фермента (хромогенный субстрат). • Снижено содержание свободной галактозы (ВЭЖХ). • Больше галактана легко извлекается из клеточной стенки Контрольные (WT) и трансгенные линии растений льна (4 -2, 6 -1, 6 -2) Трансформация проведена M. Roach, M. Deyholos (Университет Альберты, Канада)
 20 m
20 m
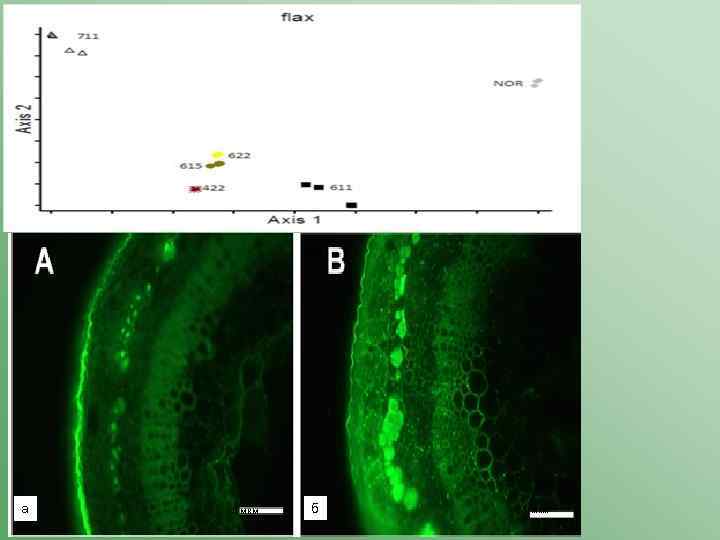 20 мкм а 5 мкм б 5 мкм
20 мкм а 5 мкм б 5 мкм
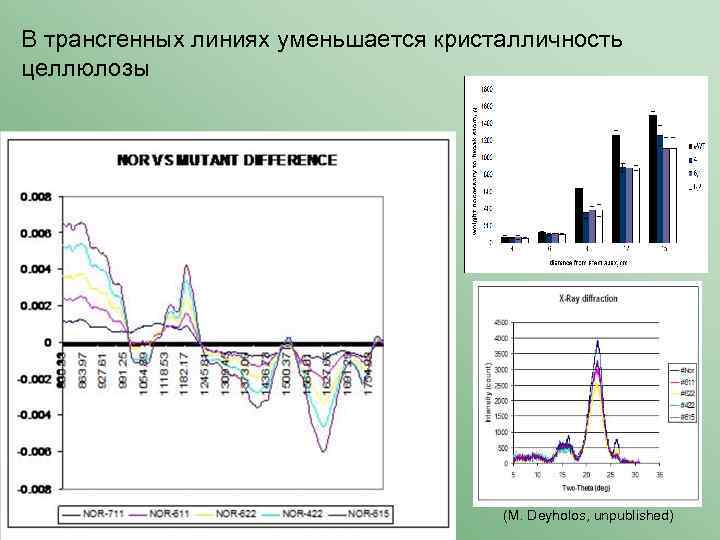 В трансгенных линиях уменьшается кристалличность целлюлозы (M. Deyholos, unpublished)
В трансгенных линиях уменьшается кристалличность целлюлозы (M. Deyholos, unpublished)
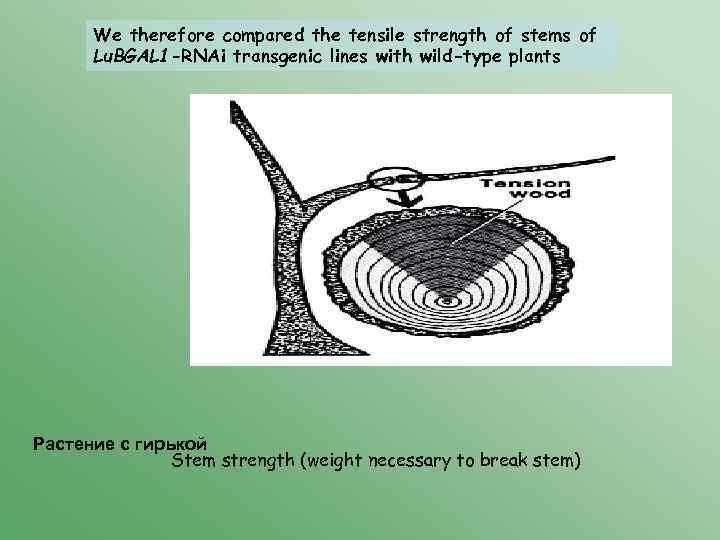 We therefore compared the tensile strength of stems of Lu. BGAL 1 -RNAi transgenic lines with wild-type plants Растение с гирькой Stem strength (weight necessary to break stem)
We therefore compared the tensile strength of stems of Lu. BGAL 1 -RNAi transgenic lines with wild-type plants Растение с гирькой Stem strength (weight necessary to break stem)
 Формирование особых механических свойств желатинозных волокон связано с образованием тканеспецифичных пектиновых веществ сложного строения и их активной модификацией in muro.
Формирование особых механических свойств желатинозных волокон связано с образованием тканеспецифичных пектиновых веществ сложного строения и их активной модификацией in muro.


